Hauptsätze der Wärmelehre
Werbung

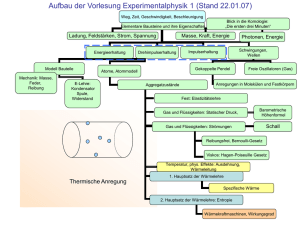
Hauptsätze der Wärmelehre Innere Energie U — die Energie der chaotischen Bewegung (Wärmebewegung) der Mikroteilchen des Systems (Moleküle, Atome, Elektronen, Atomkerne usw.) und die Wechselwirkungsenergie dieser Teilchen. Die innere Energie ist: •eine eindeutige Funktion des thermodynamischen Zustandes des Systems •unabhängig davon, wie das System in diesen Zustand gelangte •ist vergleichbar zur potentiellen Energie der Mechanik, d.h. ist gespeicherte Energie •innere Energie dient der Beschreibung eines Prozesses bei konstantem Volumen (isochorer Prozess) 1 Der 1. Hauptsatz der Wärmelehre Arbeit dW Alles, was Medium zugefuhrt wird, wird positiv gerehnet, Abgabe negativ. Medium dU Warme dQ 3 U = n ⋅ N A ⋅ Wkin = nRT 2 Innere Energie Dann gilt: dU = dQ + dW Energieerhaltung Für ideales Gas dU = dQ + pdV 2 Der 1. Hauptsatz der Wärmelehre Die Der 1 HS ist nichts anderes als Energieerhaltungssatz unter Einbeziehung von Warme als Energieform 3 Reversible und irreversible Prozesse 4 Der 2 Hauptsatz der Wärmelehre •(Erfahrungs-) Tatsache mann kann die Wärme nicht ohne weiteres in mechanischne Arbeit umwandeln Wärme ist eine ungeordnete Bewegung, die man allenfalls teilweise in geordnete mechaniscne Arbeit mechanischne Arbeit (Etwa als kinetische Energie eines Fahrzeugs) umwandeln kann. •Man kann die Unordnung der Welt nie verringern, aber man vergrossert sie durch (fast) alles, was man tut. •Die Erzeugung von mechanischne Arbeit aus Warme verringert nicht die Unordnung in der Welt. Sie verlagert sie nur. Die Physiker haben fur die Unordnung eigenen Begrieff, mit den man rechnen kann: Die Entropie 5 Entropie 6 Entropie •Weitere Möglichkeit der Einführung der Entropie: als ein Maß für die Wahrscheinlichkeit, dass sich ein bestimmter Zustand realisieren lässt •Diese Wahrscheinlichkeit umso höher, je geringer die Ordnung im System Entropie Maß für den Ordnungsgrad des System ∆S = k lnW Die Entropie eines Zustandes ist proportional dem Logarithmus seiner thermodynamischen Wahrscheinlichkeit Boltzmann (1872) Für zwei Systeme, die nicht in Kontakt stehen, ist W der gleich dem Produkt der Einzelwahrscheinlichkeiten W = W1.W2 Dann S = S1 + S2 7 Der 2. Hauptsatz ∆S > 0 Dieser Satz ist ein Erfahrungssatz, d.h. es ist physikalisch nicht unmöglich dass etwas passiert das den 2. Hauptsatz widerlegt, es ist nur extrem unwahrscheinlich. 8 Der 2. Hauptsatz der Wärmelehre Maxwellscher Dämon ein Gedankenexperiment Verstoß gegen den zweiten Hauptsatz: Perpetuum Mobile zweiter Art! physikalisch nicht realisierbar kleines Loch mit Klappe 9 Der 2. Hauptsatz der Wärmelehre Der zweite Hauptsatz der Thermodynamik hat tiefe philosophische Diskussionen hervorgebracht, weil er die in allen mikroskopischen Systemen bestehende Zeitsymmetrie (die Vergangenheit verhält sich wie die Zukunft) bricht und eine Zeitachse auszeichnet. Teilweise wird versucht, das Wesen der Zeit mit dem Zweiten Hauptsatz zu verstehen. Energiebilanz beim lebenden Organismus 10 Der 3. Hauptsatz der Thermodynamik Die ersten beiden Hauptsätze der Thermodynamik geben nur ungenügend Auskunft über das Verhalten thermodynamischer Systeme bei Null Kelvin. Der dritte Hauptsatz der Thermodynamik (oder das Theorem von Nernst und Planck): Die Entropie aller Körper strebt im Gleichgewichtszustand bei Annäherung der Temperatur gegen Null Kelvin gegen Null. lim S =0 T →0 11 Nullter Hauptsatz Wenn A und B sowie B und C die gleiche Temperatur haben, so hat A die gleiche Temperatur wie C. Dieses Gesetz wurde erst nach den anderen drei formuliert, obwohl es eine wichtige Basis bildet. Deswegen die seltsame Nummerierung. 12 Richtungsabhängigkeit Entropie und Energie Da die Entropie in einem abgeschlossenen System sich immer in eine Richtung entwickelt, wollen wir Entropie eine Richtungsgröße nennen, zum Unterschied von der Energie, die für dasselbe System eine Erhaltungsgröße ist. 13 Schlussfolgerungen Es sind viele Schlussfolgerungen möglich. Einige davon: • Alle natürlichen Prozesse sind irreversibel. • Alle Prozesse mit Reibung sind irreversibel. • Wärme kann nie von selbst von einem Körper niedriger Temperatur auf einen Körper höherer Temperatur übergehen. Es ist dazu Energie von außen notwendig (z. B. Kühlschrank, Wärmepumpe). • Wärme lässt sich nicht komplett in andere Energieformen umwandeln. • Das Gleichgewicht isolierter thermodynamischer Systeme ist durch ein Maximalprinzip der Entropie ausgezeichnet. • Die Entropie im Universum strebt einem Maximum zu. 14 Einstein zur Thermodynamik "A theory is the more impressive the greater the simplicity of its premises, the more different kinds of things it relates, and the more extended its area of applicability. Hence the deep impression that classical thermodynamics made upon me. It is the only physical theory of universal content concerning which I am convinced that within the framework of applicability of its basic concepts, will never be overthrown.“ 15