Kettenquiz – Atombau / Radioaktivität
Werbung

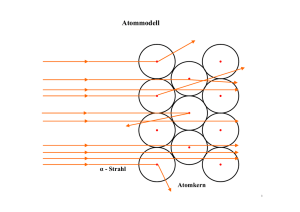
Kettenquiz – Atombau / Radioaktivität Was bezeichnet man als Protonen? Reinelemente (z.B. Aluminium, Gold) An welcher Stelle des Atoms befindet sich dessen größte Masse? Positiv geladene Kernteilchen Welche Teilchen bezeichnet man als Nukleonen? Im Atomkern Woraus folgerte man, dass der Atomkern positiv geladen sein muss? Protonen und Neutronen Wer zog diesen folgenschweren Schluss und entwickelte ein neues Atommodell? Alphateilchen wurden sehr stark abgelenkt ohne den Kern zu treffen. Wie bezeichnet man sein Atommodell? Ernest Rutherford Warum trägt es diese Bezeichnung? Kern-Hülle-Modell Was ist hierbei der Unterschied zum Atommodell nach Dalton? Das Atom gliedert sich in eine fast masselose Hülle und einen dichten Kern. Warum sind Atome nicht unveränderlich und ewig? Dalton sah in Atomen feste, kugelförmige Teilchen, die unveränderlich sind. Welche Möglichkeit der Umwandlung gibt es? Atome eines Elements können zu Atomen eines anderen Elements werden. Welche hauptsächlichen Arten radioaktiver Strahlung gibt es? Elemente können sich durch radioaktive Strahlung umwandeln. Wie kann man Alphastrahlen charakterisieren? Alpha-, Beta- und Gammastrahlen Und wie kann man Betastrahlen charakterisieren? Sie bestehen aus He2+-Teilchen und haben eine geringe Reichweite. Wer entdeckte die Radioaktivität? Diese bestehen aus Elektronen (e-) und haben eine größere Reichweite. Wer untersuchte das Phänomen eingehend und gab ihm den Namen Radioaktivität? Henri Bequerel Wie konnte Ernest Rutherford die Strahlungsarten unterscheiden? Marie und Pierre Curie Warum treten Alpha- und Betastrahlung zumeist in Kombination auf? Durch ihr Verhalten im elektrischen Feld. Welche Bedingung gilt für elektrisch neutrale Atome? Bei radioaktiver Strahlung entstehen elektrisch neutrale Elemente. Wo befinden sich die Elektronen innerhalb des Atoms? Das Atom besitzt die gleiche Anzahl an Protonen und Elektronen. Welche Ladung trägt ein Elektron? In der Hülle, die somit negativ geladen ist. Wie bezeichnet man diese Ladung eines Elektrons? -1,6 · 10-19 C (Coulomb) Wodurch unterscheidet sich diese Elementarladung von der eines Protons? Elementarladung Welche relative Masse besitzt ein Proton? Durch das mathematische Vorzeichen. Welche relative Masse besitzt ein Neutron? Etwa 1,007 u. Welche relative Masse besitzt ein Elektron? Etwa 1,009 u. Wie ermittelt man die Anzahl der Protonen eines Atoms? Etwa 0,00055 u. Wie ermittelt man die Anzahl der Neutronen eines Atoms? Man kann sie an der Kernladungszahl im Periodensystem der Elemente ablesen. Was ist Isotopie? Sie ergibt sich aus Nukleonenzahl abzüglich der Kernladungszahl. Was bezeichnet man als Isotope? Das Auftreten von Isotopen eines Elements. Worin unterscheiden sich Isotope im Atombau voneinander? Elemente mit gleichen Eigenschaften aber unterschiedlichen Massen. Wie bezeichnet man Elemente, die aus Isotopen bestehen? Sie unterscheiden sich durch die Anzahl der Neutronen im Kern. Wie bezeichnet man Elemente, die nur aus einer einzigen Atomart bestehen? Mischelemente (z.B. Wasserstoff, Kohlenstoff, …)