Chemie Tabelle - Gymnasium Kirchseeon
Werbung
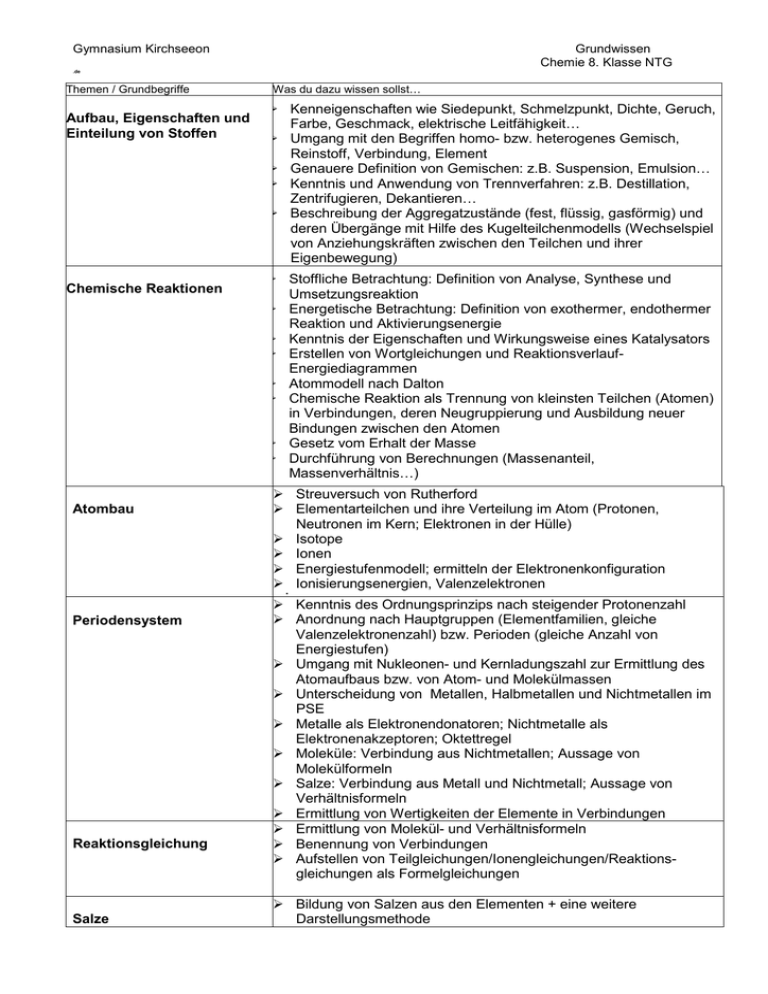
Gymnasium Kirchseeon Grundwissen Chemie 8. Klasse NTG .de Themen / Grundbegriffe Aufbau, Eigenschaften und Einteilung von Stoffen Chemische Reaktionen Atombau Was du dazu wissen sollst… Kenneigenschaften wie Siedepunkt, Schmelzpunkt, Dichte, Geruch, Farbe, Geschmack, elektrische Leitfähigkeit… Umgang mit den Begriffen homo- bzw. heterogenes Gemisch, Reinstoff, Verbindung, Element Genauere Definition von Gemischen: z.B. Suspension, Emulsion… Kenntnis und Anwendung von Trennverfahren: z.B. Destillation, Zentrifugieren, Dekantieren… Beschreibung der Aggregatzustände (fest, flüssig, gasförmig) und deren Übergänge mit Hilfe des Kugelteilchenmodells (Wechselspiel von Anziehungskräften zwischen den Teilchen und ihrer Eigenbewegung) Stoffliche Betrachtung: Definition von Analyse, Synthese und Umsetzungsreaktion Energetische Betrachtung: Definition von exothermer, endothermer Reaktion und Aktivierungsenergie Kenntnis der Eigenschaften und Wirkungsweise eines Katalysators Erstellen von Wortgleichungen und ReaktionsverlaufEnergiediagrammen Atommodell nach Dalton Chemische Reaktion als Trennung von kleinsten Teilchen (Atomen) in Verbindungen, deren Neugruppierung und Ausbildung neuer Bindungen zwischen den Atomen Gesetz vom Erhalt der Masse Durchführung von Berechnungen (Massenanteil, Massenverhältnis…) Streuversuch von Rutherford Elementarteilchen und ihre Verteilung im Atom (Protonen, Neutronen im Kern; Elektronen in der Hülle) Isotope Ionen Energiestufenmodell; ermitteln der Elektronenkonfiguration Ionisierungsenergien, Valenzelektronen Periodensystem Reaktionsgleichung Salze Kenntnis des Ordnungsprinzips nach steigender Protonenzahl Anordnung nach Hauptgruppen (Elementfamilien, gleiche Valenzelektronenzahl) bzw. Perioden (gleiche Anzahl von Energiestufen) Umgang mit Nukleonen- und Kernladungszahl zur Ermittlung des Atomaufbaus bzw. von Atom- und Molekülmassen Unterscheidung von Metallen, Halbmetallen und Nichtmetallen im PSE Metalle als Elektronendonatoren; Nichtmetalle als Elektronenakzeptoren; Oktettregel Moleküle: Verbindung aus Nichtmetallen; Aussage von Molekülformeln Salze: Verbindung aus Metall und Nichtmetall; Aussage von Verhältnisformeln Ermittlung von Wertigkeiten der Elemente in Verbindungen Ermittlung von Molekül- und Verhältnisformeln Benennung von Verbindungen Aufstellen von Teilgleichungen/Ionengleichungen/Reaktionsgleichungen als Formelgleichungen Bildung von Salzen aus den Elementen + eine weitere Darstellungsmethode Gymnasium Kirchseeon Grundwissen Chemie 8. Klasse NTG Gewinnung von Kochsalz (Salinebecken…) Teilvorgänge bei der Bildung eines Salzes aus den Elementen sowie Verrechnung der Einzelenergien Vorstellung von der Ausbildung eines Salzkristalls, Anordnung der Ionen und Ursache des Zusammenhalts (elektrostatische Anziehung, Ionengitter, Koordinationszahl, dichteste Kugelpackung, Ionenbindung) Kenntnis und Erklärung der Salzeigenschaften ((Un-)Löslichkeit, Sprödigkeit, elektrische Leitfähigkeit…) Metalle Moleküle Formulierung einer Darstellungsmöglichkeit: Elektrolyse, Umsetzungsreaktion Vorstellung vom Aufbau eines Metalls und der Ursache des Zusammenhalts der Atome (Metallgitter, delokalisierte Elektronen, Elektronengas, positiv geladene Atomerümpfe) Erklärung der Metaleigenschaften (Verformbarkeit, Wärmeleitfähigkeit, elektrische Leitfähigkeit, Verformbarkeit… Unterscheidung von unedlen und edlen Metallen aufgrund ihres Bestrebens zur Elektronenabgabe Aufbau von Legierungen Vorstellung vom Aufbau von Molekülen und Ursache des Zusammenhalts der Atome durch gemeinsame Elektronenpaare ( = Atombindung, Elektronenpaarbindung, kovalente Bindung) Ermitteln von Valenzstrichformeln ( = Lewisformeln); Einfach- und Mehrfachbindungen, Formalladungen Verbindungen/Elemente Molekülanionen („Gruppen“) und Ableitung der entsprechenden Säure bzw. Base bzw. eines Salzes Nachweisreaktionen Praktische Kenntnisse Wasser Wasserstoffsulfid (Kenneigenschaft: Geruch) Wasserstoffchlorid (in Wasser gelöst: Salzsäure) Wasserstoffperoxid Ammoniak (Kenneigenschaft: Geruch) Kohlenstoffdioxid Zweiatomige Elemente nach der „HOFBrINCl-Regel“ Chlorid, Salzsäure, z.B. Natriumchlorid Nitrat, Salpetersäure, z.B. Kaliumnitrat ( = Kaliumsalpeter) Nitrit, salpetrige Säure, z.B. Natriumnitrit (Konservierungsmittel) Sulfid, Wasserstoffsulfid, z.B. Zinksulfid Sulfat, Schwefelsäure, z.B. Calciumsulfat ( = Gips) Sulfit, schweflige Säure, z.B. Natriumsulfit (Konservierungsmittel) Carbonat, Kohlensäure, z.B. Calciumcarbonat ( = Kalk) Phosphat, Phosphorsäure, z.B. Calciumphosphat Hydroxid, Natriumhydroxid ( = in Wasser gelöst: Natronlauge) Knallgasprobe Glimmspanprobe Kohlenstoffdioxidnachweis mit Calcium- oder Bariumhydroxidlösung Kenntnis der Sicherheitsregeln im Labor und beim Umgang mit Chemikalien Kenntnis der wichtigsten Laborgeräte Erstellen eines Versuchsprotokolls Befolgung von Versuchsanleitungen Selbstständige Durchführung von Experimenten Sorgfalt im Umgang mit Laborgeräten, Chemikalien; sorgfältige Reinigung der Laborgeräte und des Arbeitsplatzes; sachgemäße Entsorgung von Chemikalien