Schalenbau der Atome am Beispiel Schwefel
Werbung

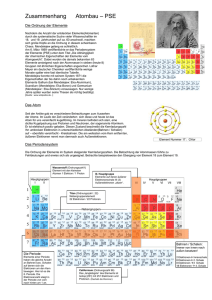
Schalenbau der Atome am Beispiel Schwefel (S): 1) Sieh nach in welcher Periode (waagrechte Zeile) Schwefel steht. Schwefel steht in der dritten Periode, d.H. Schwefel besteht aus einem Kern und drei Schalen. 2) In der ersten Periode stehen 2 Elemente (H und He), deshalb befinden sich dort 2 Elektronen. Zeichne also in die erste Schale 2 Elektronen. 3) In der zweiten Periode stehen 8 Elemente (Li, Be, B, C, N, O, F, Ne), deshalb befinden sich dort 8 Elektronen. Zeichne auf die zweite Schale 8 Elektronen. 4) Schwefel (S) steht in der dritten Periode und in der 6. Spalte. Das heißt dass auf der dritten Schale nur noch 6 Elektronen sind. Aufgabe: Zeichne folgende Elemente auf: Cs, Al, Se, Ne, Xe Wichtige Zahlen im PSE Jedes Element hat eine Ordnungszahl. Diese geht nach der Reihe. H=1 He = 2 Li = 3 Heft: Die Ordnungszahl, auch Kernladungszahl, Atomnummer oder Protonenzahl, gibt die Stellung eines chemischen Elements im Periodensystem der Elemente an. Sie ist gleich der Anzahl der PROTONEN, die sich im Atomkern jedes Atoms dieses Elements befinden. Wenn ein Element in einem neutralen Zustand ist, muss es dieselbe Anzahl Protonen wie ELEKTRONEN aufweisen. Welche Ordnungszahl haben Schwefel, Argon, Kalium, Zinn, Iod, Blei und Radon? Die Anzahl der NEUTRONEN errechnet sich aus der Atommasse. 11-5 = 6 Bor hat also 6 Neutronen Wie viel Protonen, Neutronen und Elektronen haben: Protonen Aluminium Kohlenstoff Magnesium Natrium P O H Elektronen Neutronen