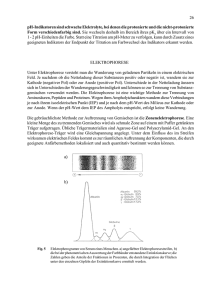
Langfassung
Werbung

Behandlung gentechnischer Verfahren im Rahmen der Elektrostatik ein Unterrichtsvorschlag fŸr 7 Ð 9 Unterrichtsstunden Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Stra§e Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -1- 1 2 †BERSICHT UNTERRICHTSABLAUF 3 4 2.1 EinfŸhrung in die Thematik 4 2.2 EinfŸhrung in die Elektrostatik 4 2.3 Ionenwanderung in FlŸssigkeiten 5 2.4 Aufbau und Funktionsweise der Elektrophoreseapparatur 6 3 ERWEITERUNGSM…GLICHKEITEN †BER DIE FACHGRENZEN HINAUS 8 4 FACHSPEZIFISCHE UND FACH†BERGREIFENDE INHALTE 9 5 MATERIALIEN 10 5.1 Ionenleitung in FlŸssigkeiten 5.1.1 Experiment 1 5.1.2 Experiment 2 10 12 15 5.2 ErgŠnzende Literatur 5.2.1 Ionenwanderung 5.2.2 Elektrophorese 5.2.3 DNA-Fingerprint 5.2.4 Materialien des Modellversuchs BINGO 5.2.5 Weitere Literaturhinweise 15 15 15 15 16 16 GemŠ§ dem Fachrahmenplan Physik 1998 sind die physikalischen Inhalte Themenbereichen zuzuordnen. Diese Unterrichtssequenz fŸgt sich in den Themenbereich III ÒStatische FelderÓ ein. Au§erdem sind die Inhalte der Abschnitte eines Kurses jeweils nach Leitgesichtspunkten zu strukturieren. Je nach Einbindung in den Unterricht des gesamten Halbjahres ist in dieser Sequenz der Leitgesichtspunkt ÒPhysik in NachbardisziplinenÓ oder ÒPhysik im AnwendungszusammenhangÓ enthalten. Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -2- 1 †bersicht Die aktuelle Diskussion um die kŸnstliche VerŠnderbarkeit von Lebewesen (gentechnische Eingriffe im Rahmen der Medizin, der Nahrungsmittelproduktion und der ZŸchtung von Lebewesen Ñ im weitesten Sinne Ñ nach Ma§) einerseits und der kŸnstlichen Erhaltung von Erbinformationen (Klonierung bei Tieren und Menschen) andererseits darf auch im Unterricht in Physik der gymnasialen Oberstufe nicht unbeachtet bleiben. Zweifelsfrei handelt es sich um einen gesellschaftspolitischen, škonomischen und historischen Bereich von au§erordentlicher Relevanz fŸr die Zukunft. Ausgehend von den historischen Erfahrungen im Zusammenhang mit Eugenik und Euthanasie wŠhrend des Faschismus, Ÿber die EntschlŸsselung der DNA, der Entdeckung des natŸrlichen Gentransfers bei Bakterien bis zur škonomisch verwertbaren, kŸnstlichen Handhabung von Genen steht unsere Gesellschaft heute in der ethisch-moralischen, škologischen und škonomischen Auseinandersetzung um die Grenzen der Forschung und ihrer Anwendung. SchŸler mŸssen auf die persšnliche Auseinandersetzung mit dieser vollstŠndig nur fachŸbergreifend erfa§baren Problematik vorbereitet werden. Eine naturwissenschaftlich fundierte Behandlung mu§ einerseits fŠcherŸbergreifend ausgerichtet sein, andererseits in bestimmten Bereichen auch fachspezifisch orientiert sein. Die SchŸlerInnen sollten mšglichst selbstŠndig, fachŸbergreifend und teamorientiert arbeiten, damit in den Lernproze§ die kritische Auseinandersetzung mit den erworbenen Kenntnissen einbezogen wird. Dennoch kann Basiswissen auch im fachbezogenen Rahmen eines Physikkurses (Grund- oder Leistungskurs) vermittelt werden. †berwiegend biologische und/oder chemische Fragestellungen kšnnen dann nur in begrenztem Umfang bearbeitet werden. Der fachspezifische Einstieg in das Halbjahr kann Ÿber Probleme der gentechnischen Forschung und Anwendung am Beispiel von mšglicherweise gentechnisch manipulierten Lebensmitteln, von aktuellen Zeitungsartikeln oder anhand von Texten mit Stellungnahmen zur Gentechnik erfolgen. Eine eher fachspezifisch ausgerichtete Phase des Unterrichts schlie§t sich an. Die SchŸlerInnen sollen so Basisqualifikationen erwerben, die unbedingte Voraussetzung fŸr das VerstŠndnis der gentechnischen Verfahren sind. Zeitlicher Rahmen: 1. Unterrichtswoche: Einstimmung der SchŸlerinnen und SchŸler auf die Thematik 2. - 9. Unterrichtswoche: Vermittlung von Basisqualifikationen 10. - 12. Unterrichtswoche: Gentechnische Verfahren aus der Sicht der Physik Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -3- zz. Unterrichtswoche: Abschlu§ der Arbeit zum Thema Gentechnologie z.B. durch eine Diskussion mit Experten aus Forschung und Wirtschaft 2 Unterrichtsablauf 2.1 EinfŸhrung in die Thematik An Hand einer Vorbemerkung aus dem Buch ÒAm Faden des LebensÓ (Winnacker 1993, 11 ff) und aktuellen Zeitungsartikeln kann der Begriff ÒGentechnikÓ erklŠrt und die AktualitŠt dieses Kursthemas an Hand der Diskussion Ÿber Anwendungsgebiete (Manipulation von Lebensmitteln, Verbesserung von Impfstoffen, prŠnatale Diagnostik, TŠterŸberfŸhrung durch den gentechnischen Fingerprint u.a.) verdeutlicht werden. Aktuelle BezŸge sind herzustellen und durch Anschauungsmaterial Tomaten, SŸ§waren wie ÒButterfingerÓ, Sojaprodukte zu ergŠnzen. Die SchŸlerInnen werden so auf die Relevanz dieses Themas aufmerksam gemacht und bei geeigneter Wahl der Texte auf physikalisch begrŸndete Verfahren der Genmanipulationen hingewiesen. Der Schwerpunkt des physikalischen Aspektes in der Gentechnologie liegt in den Trennverfahren, die zur Analyse der DNA-MolekŸle eingesetzt werden. Die Elektrophorese ist ein zentrales elektrostatisches Trennverfahren bei Stoffuntersuchungen. Um einen Einblick in die Funktionsweise der Elektrophorese und die damit verbundenen physikalischen ZusammenhŠnge zu erhalten, mŸssen sich die SchŸlerInnen zunŠchst mit elektrischen Feldern und den sich in ihm bewegenden Ladungen auseinandersetzen. Neben dem Verfahren der Elektrophorese wird in der Gentechnologie das Verfahren der isoelektrischen Fokussierung angewendet. Auch hier sind unter Einbeziehung chemischen Basiswissens Kenntnisse zu erarbeiten. 2.2 EinfŸhrung in die Elektrostatik Aus der in kleinen Versuchen beobachteten wechselseitigen Kraftwirkung zweier gleichnamig oder ungleichnamig geladener Kšrper aufeinander wird das elektrische Feld als Kraftwirkungseigenschaft des Raumes auf geladene Teilchen eingefŸhrt und an Hand von Feldlinienbildern visualisiert. Die Auswertung eines SchŸlerexperimentes mit zwei gleichnamig geladenen Styroporkugeln als Zentralkšrper bzw. Probekšrper fŸhrt zum Coulombschen Kraftgesetz im Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -4- Radialfeld. Im Zusammenhang mit diesem Radialfeld wird die elektrische FeldstŠrke als probeladungsunabhŠngige Kraftgrš§e eingefŸhrt. Die anschlie§end zu behandelnden Begriffe elektrische Arbeit, Potential und Spannung werden am Beispiel des homogenen elektrischen Feldes eingefŸhrt. FŸr das VerstŠndnis elektrophoretischer VorgŠnge reicht diese Betrachtung aus. Je nach Wunsch kann hier eine Vertiefung der Begriffe vorgenommen werden. Der proportionale Zusammenhang zwischen der FlŠchenladungsdichte und der elektrischen FeldstŠrke kšnnen relativ leicht am Plattenkondensator nachgewiesen werden (Grundgleichung der Elektrostatik). Die KapazitŠt eines Kondensators wird definiert und die Wirkung von Nichtleitern (Dielektrika) am Plattenkondensator gezeigt und Ÿber die Polarisation erklŠrt. Abschlie§end kann die Formel fŸr die im elektrischen Feld gespeicherte Energie hergeleitet werden. †bungsaufgaben kšnnen zur Reflexion Ÿber die eingefŸhrten physikalischen Grš§en und zur EinŸbung des Umgangs mit ihnen gelšst werden. 2.3 Ionenwanderung in FlŸssigkeiten Die Elektrophorese ist die zentrale Apparatur der gentechnischen Analyse. Mit Hilfe dieses Verfahrens werden geladene Teilchen in einem elektrischen Feld getrennt. Die Wanderungsgeschwindigkeit der Elemente ist von ihrer Ladungsgrš§e, ihrer MolekŸlgrš§e und den Dimensionen des elektrischen Feldes abhŠngig. Alle drei Relationen kšnnen experimentell untersucht werden. Zur Veranschaulichung der Ionenbewegung kann ein einfacher Versuchsaufbau verwendet werden. In eine flache, mit destilliertem Wasser gefŸllte, durchsichtige Schale wird ein Kšrnchen Kaliumpermanganat gegeben, welches sofort dissoziiert, die Kaliumionen sind unsichtbar, die Permanganat-Ionen bilden einen roten Fleck aus. Ohne elektrisches Feld kann zunŠchst die Ausbreitung dieses roten Flecks beobachtet und gemessen werden. Es ergibt sich eine Ausbreitungsgeschwindigkeit, die zur weiteren Beurteilung der Versuchsergebnisse benštigt wird. Wiederholt man dies Experiment mit angelegtem elektrischen Feld, so tritt sichtbar zusŠtzlich Ionenwanderung auf Grund der Ladung der Permanganat-Ionen ein. Die Wanderungsgeschwindigkeit kann mit Hilfe einer Stoppuhr und einer Skala (unter die Schale gelegtes Millimeterpapier oder Folie mit Millimeterraster bei einer Projektion mittels OHP) ermittelt werden. Eine genaue Beschreibung ist im Anhang zu finden. Exaktere Ergebnisse liefert ein weiteres Experiment, bei dem ebenfalls Permanganat-Ionen in einem elektrischen Feld wandern. Dazu wird eine Kaliumpermanganatlšsung unter eine Kaliumnitratlšsung geschichtet und die Wanderung der Ionen im elektrischen Feld beobachtet. Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -5- Dieses Experiment liefert so gute Ergebnisse, dass daraus auf den Durchmesser der Ionen geschlossen werden kann. Weitere Angaben sind im Anhang und in der angegebenen Literatur zu finden. 2.4 Aufbau und Funktionsweise der Elektrophoreseapparatur Die Elektrophorese ist heute in Biologie und Medizin eine Standardmethode zur Trennung und Identifizierung von MolekŸlen, wie z.B. Peptide, Glycopeptide, AminosŠuren, Proteinen und NukleinsŠuren, die in leitenden Lšsungen (Pufferlšsungen) ionisiert werden. Die Driftgeschwindigkeiten der verschiedenen MolekŸlarten unterscheiden sich untereinander aufgrund ihrer unterschiedlichen MolekŸlgrš§e und ihrer unterschiedlichen elektrischen Ladungsmenge in einer Pufferlšsung bei konstantem elektrischen Feld. Zwar sind diese organischen MolekŸle viel grš§er als die zuvor im Unterricht behandelten Ionen, doch kšnnen sie auch eine viel grš§ere elektrische Ladung tragen, so dass die Geschwindigkeiten im elektrischen Feld und damit die Beweglichkeiten dieser in Pufferlšsung ionisierten MolekŸle ungefŠhr mit denen der Ionen vergleichbar sind. Die Elektrophoreseapparatur besteht im Wesentlichen aus einer flachen Kammer (Elektrophoresekammer) mit je einer Elektrode (Kathode und Anode) an zwei gegenŸberliegenden Kammerenden. †ber ein entsprechende Quelle wird eine Gleichspannung zwischen Kathode und Anode angelegt. Die Ionen in der in die Kammer eingegebenen Pufferlšsung leiten dann den elektrischen Strom. Da es bei der QualitŠt der Auftrennung der in die Pufferlšsung eingegebenen, und damit ionisierten MolekŸle besonders auf ein hinsichtlich der Temperatur und der LeitfŠhigkeit stabiles Medium zwischen der Kathode und der Anode ankommt, verwendet man als TrŠgermedium Papier, Cellulose, DŸnnschichtplatten aus Siliziumoxid oder Gele aus Agar Agar oder Polyacrylamid. Insbesondere hat sich bei der Auftrennung eines Stoffes nach seiner MolekŸlgrš§e oder nach den isoelektrischen Punkten der ionisierten MolekŸlarten die Gelelektrophorese, d.h. die Elektrophorese mit Gelen als TrŠgermedium, sehr bewŠhrt. Die Ursache hierfŸr ist die homogene, siebŠhnliche Struktur dieses halbstarren TrŠgermediums, dessen Porengrš§e durch die Konzentration der jeweiligen Substanz im Gel, besonders bei Polyacrylamid, gut regulierbar ist. Bei der Auftrennung von Protein-MolekŸlen nach ihrer Grš§e durch Gelelektrophorese wird der Pufferlšsung Natriumdodecysulfat beigemischt. Dies hat zur Folge, dass die in Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -6- Lšsung befindliche Protein-MolekŸle die gleichen Ladungsdichten erhalten und sie zusŠtzlich bis auf ihre PrimŠrstruktur die unterschiedlichen rŠumlichen Strukturen verlieren. Die so denaturalisierten Eiwei§-MolekŸle erfahren dann, bei entsprechender, konstanter Porengrš§e des Gels und konstantem elektrischen Feld, eine Auftrennung nach ihrer MolekŸlgrš§e, da ihre Beweglichkeit nun nur noch von der LŠnge der PrimŠrstruktur der MolekŸle abhŠngt (Experiment hierzu: ÒAuftrennung der Proteine im Eiklar des HŸhnereis und bestimmung ihrer molaren Masse Ÿber GelelektrophoreseÓ in PHYWE-Schriftenreihe, Handbuch Gelelektrophorese). Ein vom Prinzip her analoges Verfahren der Gelelektrophorese wird bei der DNA-Fingerprinting-Methode angewendet. Die doppelstrŠngigen, helixfšrmigen DNA-MolekŸle (DesoxiribonukleinsŠure-MolekŸle) werden durch spezifische Restriktionsenzyme an bestimmten BasenplŠtzen zerschnitten. Hierbei ist die Anzahl und die LŠnge der entstehenden DNA-BruchstŸcke aufgrund des Sequenzpolymorphismus fŸr jedes Individuum unterschiedlich (Restriktions-FragmentlŠngen-Polymorphismus (RFLP)). Durch die Phosphatgruppen der DNA ist in der Pufferlšsung eine gleichmŠ§ige negative Ladungs- und Massendichte der einzelnen DNAFragmente erreicht. In einem Gel mit charakteristischer Maschenweite kšnnen die DNAMolekŸle entsprechend ihrer nur noch von der MolekŸlgrš§e abhŠngigen Beweglichkeit in Banden fraktioniert werden (Gel-Elektrophorese nach der DNA-MolekŸlgrš§e; Experiment hierzu: ÒDer Lambda KitÓ, Versuchkit des NCBE (National Centre for Biotechnology Education) und des IPN (Institut fŸr die PŠdagogik der Naturwissenschaften, 1994). Ein weiteres, auf der Gelelektrophorese beruhendes Trennverfahren ist die Isoelektrische Fokussierung bei ProteinmolekŸlen. Sie beruht darauf, dass ein Protein-MolekŸl sich in einer + Pufferlšsung mit einem spezifischen pH-Wert (negativer Logarithmus der H -Ionenkonzentration) zu einem insgesamt neutralen Zwitterion ausbildet. Diesen neutralen Ladungszustand, bei dem keine translatorische Bewegung des MolekŸls im elektrischen Feld mehr mšglich ist, bezeichnet man als isoelektrischen Punkt (IEP). Die Grš§e der Ladung ist bei AminosŠuren, die sowohl basische als auch anionische Gruppen enthalten, vom pH-Wert des Lšsungsmittels abhŠngig. In einer sauren Lšsung entsteht so ein Kation, in alkalischen Lšsungen ein Anion. Zum Beispiel wird aus der AminosŠure Glycin im sauren Bereich das Kation H3+NCH2OOH und im alkalischen Bereich das Anion H2NCH2COO- , da OH - aufgenommen bzw. abgegeben wird. In Lšsungen mit pH < IEP ist das ProteinmolekŸl insgesamt positiv ionisiert ist, wŠhrend es in Lšsungen mit pH > IEP insgesamt negativ ionisiert ist. TrŠgt man nun das Gel in gleich dicken Schichten mit unterschiedlichen pH-Werten in der in den Gelschichten verwendeten Pufferlšsung auf, wobei man z.B. bei der Anode mit pH 3 beginnt und an der Kathode mit z.B. pH 8 endet, so lŠsst sich mit diesem Verfahren eine Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -7- Trennung der unterschiedlichen ProteinmolekŸle nach ihren IEPÕs durchfŸhren. Dazu gie§t man das zu untersuchende Proteingemisch (es reichen schon 10 ng aus) in eine parallel zu den Streifenbahnen in das Gel eingekerbte Mulde, die nahe der Anode angebracht ist. Die hier alle positiv geladenen ProteinmolekŸle bewegen sich in der elektrischen Feldlinienrichtung zu der Gelschicht hin, die ihrem isoelektrischen Punkt entspricht. WŠhrend der Trennung sind die ProteinmolekŸle also stŠndig im Zustand eines Kations, dessen positiver LadungsŸberschuss sich aber von pH-Schicht zu pH-Schicht verringert. Ist der IEP erreicht, so erhŠlt es eine neutrale Gesamtladung und kommt zur Ruhe. Nach einer vom Verfahren abhŠngigen Laufzeit der Elektrophorese, wird die Gelschicht aus der Kammer gelšst und mit vom jeweiligen Verfahren abhŠngigen, speziellen Farbstoffen eingefŠrbt, um die einzelnen Banden des aufgetrennten MolekŸlgemisches sichtbar zu machen. Alternativ bieten sich radioaktive Markierungsverfahren der Banden an, die dann Ÿber einen durch radioaktive Strahlung belichteten Ršntgenfilm sichtbar gemacht werden. 3 Erweiterungsmšglichkeiten Ÿber die Fachgrenzen hinaus Das Thema an sich trŠgt den Ansatz zur Kooperation mit Biologie und Chemie in sich. Die in der Gentechnik verwendeten Verfahren kšnnen nur fŠcherŸbergreifend vollstŠndig erfa§t und verstanden werden. Die Physik ist in der Lage einen wesentlichen Beitrag zum VerstŠndnis der AblŠufe zu liefern, jedoch ist eine ganzheitliche Betrachtung allein aus der Sicht dieses Faches nicht mšglich. Desgleichen gilt fŸr die beiden anderen Naturwissenschaften Biologie und Chemie. Erst in der eingehenden Kooperation der drei FŠcher besteht die Mšglichkeit, bei den SchŸlerInnen ein umfassendes VerstŠndnis fŸr die AblŠufe zu erlangen. Der Informationsaustausch zwischen den FŠchern kann direkt Ÿber die SchŸlerInnen geschehen, indem sie gemeinsam ihre in den einzelnen FŠchern gewonnenen Kompetenzen zur Lšsung einer umfangreichen Aufgabe in einer Projektarbeitsphase einbringen. Diese Aufgabenstellung mu§ so konzipiert sein, dass sie nur unter Einbeziehung aller in der fachspezifischen Arbeitsphase erworbenen Kenntnisse in dem gewŠhlten Fach lšsbar ist. Beispiele dazu sind im Modellversuch BINGO erarbeitet worden. Eine ausfŸhrliche Beschreibung der Vorgehensweise, umfangreiche Materialien sowie drei Aufgabenbeispiele stehen auf der Homepage des Modellversuchs zur VerfŸgung (Adresse im Anhang). Die Erstellung eines DNA-Fingerprints im Unterricht gelingt mit Hilfe einer vom IPN Kiel vertriebenen Versuchseinheit mit einem vertretbaren Zeitaufwand zuverlŠssig. Der Lambda-Kit enthŠlt alle fŸr die DurchfŸhrung erforderlichen Chemikalien, die Versuchseinrichtung und eine Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -8- ausfŸhrliche Anleitung. Das Experiment wird mit dem Bakteriopharge Lambda, einem relativ einfachen Organismus, durchgefŸhrt. Die einzelnen Schritte sind ausfŸhrlich erklŠrt. Nach einer Vorbereitungszeit von etwa 2 Stunden kann in max. 12 Stunden die elektrophoretische Auftrennung der Fragmente erfolgen. Nach dem anschlie§enden AnfŠrben der BruchstŸcke ist der DNA-Fingerprint sichtbar. Die Bezugsquelle ist dem Anhang zu entnehmen [7]. 4 Fachspezifische und fachŸbergreifende Inhalte Neben den fachspezifischen Inhalten der Elektrostatik kšnnen fachŸberschreitende Inhalte mit dem Thema verknŸpft und in den Unterricht des Physik-Kurses eingefŸgt werden. Die folgende Tabelle gibt eine †bersicht Ÿber die mšglichen Stichpunkte: FachŸberschreitend Fachspezifisch ¥ EinfŸhrung des Themas Ÿber Zeitungsartikel zu gentechnisch manipulierten Lebensmitteln; EinfŸhrung in die Elektrostatik ¥ Genmanipulationen mittels elektrostatischer Felder (Artikel aus SZ-Magazin: ÒDa entstehen kleine SaurierÓ); ¥ Hinweis auf die Elektrophorese als ein zentrales Trennverfahren bei Stoffuntersuchungen. ¥ Kraftwirkung auf Ladung im elektrischen Feld; ¥ Coulombsches Gesetz; ¥ Arbeit, Potential und Spannung im homogenen elektrischen Feld; FŠcherverbindende Projektphase mit folgenden fachŸber- ¥ Grundgleichung der Elektrostagreifenden Inhalten: tik; ¥ Aufbau von AminosŠuren zu MakromolekŸlen ¥ Dielektrika; (Eiwei§e); ¥ KapazitŠt des Plattenkondensa¥ Aufbau der DNA; tors; ¥ Der Proze§ der Eiwei§synthese; ¥ Beweglichkeit eines geladenen ¥ der isoelektrische Punkt; ¥ Trennung der Eiwei§e mittels des elektrophoretischen Verfahrens der isoelektrischen Fokussierung; Teilchens in einem Medium; ¥ Ionenleitung in FlŸssigkeiten. ¥ PCR-Verfahren; ¥ DNA-Fingerprintverfahren. Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse -9- 5 Materialien 5.1 Ionenleitung in FlŸssigkeiten + — Q Im homogenen Feld zwischen den Platten eines Kondensators wirkt auf eine Ladung Q eine konstante elektrische Kraft. F = má a Þ má a = Qá E F = Qá E Mit dieser Kraft wird das geladenen Teilchen von der gleichnamig geladenen Platte zur entgegengesetzt geladenen Platte gleichmŠ§ig beschleunigt, solange der Raum zwischen den Platten im Vakuum liegt. Ist der Raum zwischen den beiden Platten mit einem Gas oder einer FlŸssigkeit angefŸllt, so erfŠhrt das geladene Teilchen einen Reibungswiderstand, der die gleichmŠ§ig beschleunigte Bewegung hemmt und sie schon nach sehr kurzer Zeit in eine gleichfšrmige Bewegung mit der Endgeschwindigkeit v Ÿbergehen lŠsst. r des geladenen Die hierbei wirkende Reibungskraft FR steigt proportional zur Geschwindigkeit r FR gerade die elektrische Teilchens r an. Ist die Endgeschwindigkeit v erreicht, so kompensiert Kraft Fel . r FŸr den Betrag der Reibungskraft FR gilt: FR = C ?v , wobei die ProportionalitŠtskonstante C von der Form des geladenen Teilchens und von der ZŠhigkeit des Mediums abhŠngig ist. Im Fall der KrŠftekompensation und der hiermit verbundenen gleichfšrmigen Bewegung gilt: r r FR = Fel Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse - - 10 Cá v = Qá E Q v = áá E C Q wird als Beweglichkeit des geladenen Teilchens in einem Medium bezeichnet. C Die Beweglichkeit ist von der Ladung und der Form des Teilchens sowie von der ZŠhigkeit des Mediums abhŠngig. r Da die Endgeschwindigkeit v eines geladenen Teilchens und die elektrische FeldstŠrke E leichter messbar sind, definiert man die Beweglichkeit als Der Quotient v c= E m2 [c ]= V ás . AbschŠtzung der Beweglichkeit eines einfachen Iones FŸr die nachfolgende Betrachtung sei idealisierend vorausgesetzt, dass die Gestalt des Ions einer Kugel mit dem durchschnittlichen Atomradius von r = 10-10 m entspricht. Die Reibungskraft einer in einem gasfšrmigen oder flŸssigen Raum bewegten Kugel mit dem Radius r lŠsst sich durch FR = 6áá p áh á r á v (Stokessches Gesetz) beschreiben, wobei h die ZŠhigkeit des umgebenden Mediums angibt. Die erwŠhnte ProportionalitŠtskonstante C kann also im Fall einer Kugel durch C = 6á p á h á r ausgedrŸckt werden. FŸr die Beweglichkeit eines einfach geladenen Ions ergibt sich mit Q = 1áe : e C= . 6á p á h á r -3 Ns Da das Wasser bei 20¡C die ZŠhigkeit h = 1,0á 10 m2 besitzt, gilt: 2 -8 m C = 8,5á 10 . V ás Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse - - 11 5.1.1 Experiment 1 Wanderung von MnO4 --Ionen in einem elektrischen Feld Bei der Analyse von Proteinen wird oft ein Verfahren benutzt, bei dem diese zu untersuchenden Substanzen in einem elektrischen Feld getrennt werden. Um diesen Vorgang genauer beurteilen zu kšnnen, soll die folgende Versuchsreihe als Modell durchgefŸhrt werden. Statt die Wanderung von Proteinen im elektrischen Feld zu beobachten, wird Kaliumpermanganat verwendet. Kaliumpermanganat dissoziert in Wasser zu K +- und MnO 4- - Ionen. Diese Ionen werden sich unter dem Einflu§ eines elektrischen Feldes bewegen. Dabei sind die MnO 4- Ionen auf Grund der Farbe gut zu beobachten. Ihre Wanderungsgeschwindigkeit v in destilliertem Wasser ist von verschiedenen Grš§en abhŠngig. Diese ZusammenhŠnge sollen in einer Reihe von Experimenten untersucht werden. 1. Welche AbhŠngigkeiten vermutest Du? Notiere die von Dir und Deinen MitschŸlerinnen und MitschŸlern geŠu§erten Vermutungen. Folgender Versuchsaufbau eignet sich zur Untersuchung einiger AbhŠngigkeiten. Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse - - 12 Seitenansicht + _ K+- und MnO4- - Ionen aqua dest. Ansicht von oben + _ 2. Verdeutliche Dir den Versuchsaufbau und Ÿberlege, in welche Richtung sich die jeweiligen Ionen bewegen werden. Um die Beobachtung der Ionenwanderung zu erleichtern, wird der Versuchsaufbau auf den Tageslichtschreiber gestellt und projeziert. Die Ionenbewegung ist entlang eines Ma§stabs zu beobachten. Im ersten Versuch soll lediglich die Wanderungsgeschwindigkeit der MnO4- - Ionen ermittelt werden. Anschlie§end wird der Versuchsaufbau entsprechend den unter 1. genannten AbhŠngigkeiten modifiziert. FŸr diesen ersten Versuch gelten folgende Daten: angelegte Spannung: 140 V Elektrodenabstand: 13 cm; Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse - - 13 Diese Me§tabelle soll nach Abschlu§ des Experimentes auch alle Me§daten Deiner MitschŸlerinnen und MitschŸler enthalten: Strecke s in mm Zeit t in s MittelStandardwert fŸr t abweichung 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 18 20 22 24 26 28 30 32 Ein Vergleich mit Tabellenwerten zeigt, dass dieser theoretisch bestimmte Beweglichkeitswert grš§er ist als der Literaturwert. Die Hauptursache dieser Abweichung liegt in den unterschiedlichen Ionenradien der Stoffe untereinander und insbesondere in der Tatsache, dass sich jedes Ion mit einer Wolke aus WassermolekŸlen (Dipoleigenschaft!) umgibt, die dann mitbewegt werden muss. Diese so genannte Hydration vergrš§ert also den anzunehmenden Teilchenradius erheblich. Die Grš§enunterschiede zwischen den verschiedenen Ionen werden au§erdem verwischt. Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse - - 14 5.1.2 Experiment 2 FŸr genauere Betrachtungen eignen sich die in [1], [3] und [4] dargestellten Experimente. In ein U-Rohr mit angeschmolzenem Steigrohr wird eine Kaliumnitrat-Lšsung eingefŸllt. Durch das Steigrohr wird sehr langsam eine Kaliumpermanganat-Lšsung mit deutlicher Schichtgrenzenbildung untergeschichtet. Um die Dichte der Permanganat-Lšsung zu erhšhen, kann Harnstoff zugesetzt werden. In die beiden …ffnungen des U-Rohres werden Elektroden eingefŸhrt und die FlŸssigkeit bei 30 Ð 50 V in 20 Ð 30 Minuten elektrolysiert. Es zeigt sich eine deutliche Verschiebung der Grenzschicht, diese Wanderungsgeschwindigkeit ist me§bar. Das Experiment kann abgewandelt werden, indem statt der Lšsung Agar Agar als zu durchwanderndes Medium verwendet wird. Eine genaue Anleitung findet man in [1]. Dieses Experiment zeigt deutliche Parallelen zur Gelelektrophorese auf. 5.2 ErgŠnzende Literatur 5.2.1 Ionenwanderung [1]www.phys.chemie.uni-muenchen.de/lp/exp/elektrochemie/ionenw.htm [2] www.tu-bs.de/institute/pci/aggericke/PC1/Kap_VI/Elektrolyte.htm [3] www.uni-ulm.de/uni/fak/natwis/sroel/exp/edm0299.html [4] www.chemieonline.de/index1.html 5.2.2 Elektrophorese [5] www.chemieonline.de/index1.html 5.2.3 DNA-Fingerprint [7] Lambda-Kit zu beziehen Ÿber: Institut fŸr die PŠdagogik der Naturwissenschaften an der UniversitŠt Kiel (IPN), Olshausenstra§e 62, 24098 Kiel Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse - - 15 5.2.4 Materialien des Modellversuchs BINGO [6] www.physik.uni-bremen.de/physics.education/niedderer/bingo/index.html 5.2.5 Weitere Literaturhinweise Brian H.Kaye: Mit der Wissenschaft auf Verbrecherjagd, Wiley-VCH, Weinheim, 1997 www.quarks.de/taeter/03.htm Leybold-Heraeus, Physikalsiche HandblŠtter, DK 537.311.3;a Ionenwanderung in einer flachen Kammer Erstellt von Carl-Otto Spichal und Barbara Winter, SZ Alwin-Lonke-Strasse - - 16