26 pH-Indikatoren sind schwache Elektrolyte, bei denen die
Werbung

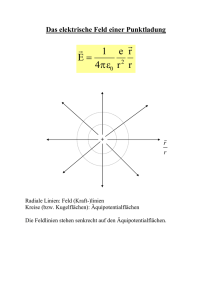
26 pH-Indikatoren sind schwache Elektrolyte, bei denen die protonierte und die nicht-protonierte Form verschiedenfarbig sind. Sie wechseln deshalb im Bereich ihres pKa über ein Intervall von 1 - 2 pH-Einheiten die Farbe. Statt eine Titration am pH-Meter zu verfolgen, kann durch Zusatz eines geeigneten Indikators der Endpunkt der Titration am Farbwechsel des Indikators erkannt werden. ELEKTROPHORESE Unter Elektrophorese versteht man die Wanderung von geladenen Partikeln in einem elektrischen Feld. Je nachdem ob die Nettoladung dieser Substanzen positiv oder negativ ist, wandern sie zur Kathode (negativer Pol) oder zur Anode (positiver Pol). Unterschiede in der Nettoladung äussern sich in Unterschieden der Wanderungsgeschwindigkeit und können so zur Trennung von Substanzgemischen verwendet werden. Die Elektrophorese ist eine wichtige Methode zur Trennung von Aminosäuren, Peptiden und Proteinen. Wegen ihres Ampholytcharakters wandern diese Verbindungen je nach ihrem isoelektrischen Punkt (IEP) und je nach dem pH-Wert des Milieus zur Kathode oder zur Anode. Wenn der pH-Wert dem IEP des Ampholyts entspricht, erfolgt keine Wanderung. Die gebräuchlichste Methode zur Auftrennung von Gemischen ist die Zonenelektrophorese. Eine kleine Menge des zu trennenden Gemisches wird als schmale Zone auf einem mit Puffer getränkten Träger aufgetragen. Übliche Trägermaterialien sind Agarose-Gel und Polyacrylamid-Gel. An den Elektrophorese-Träger wird eine Gleichspannung angelegt. Unter dem Einfluss des im Streifen wirksamen elektrischen Feldes kommt es zur räumlichen Auftrennung der Komponenten, die durch geeignete Anfärbemethoden lokalisiert und auch quantitativ bestimmt werden können. Fig. 5 Elektropherogramm von Serum eines Menschen. a) angefärbter Elektrophoresestreifen, b) die bei der photometrischen Auswertung der Farbbänder entstandene Extinktionskurve; die Zahlen geben die Anteile der Fraktionen in Prozenten, die durch Integration der Flächen unter den einzelnen Gipfeln der Extinktionskurve ermittelt werden. 27 Das Auflösungsvermögen der Polyacrylamid-Gelelektrophorese ist besonders hoch, weil im Gel Moleküle aufgrund ihrer Ladung und ihrer Grösse aufgetrennt werden. Während auf Agarose die Serumproteine nur in die grösseren Gruppen Albumin, α1- und α2-, β1- und β2-, und γ-Globuline aufgetrennt werden, vermag die Polyacrylamid-Gelelektrophorese Dutzende verschiedener Serumproteine zu unterscheiden. Ausschliesslich nach der Grösse aufgetrennt werden Proteine in der SDSGelelektrophorese (vgl. S. 14). Vereinfachte quantitative Behandlung der Wanderungsgeschwindigkeit qeladener Teilchen im elektrischen Feld. Auf ein Teilchen mit der Ladung Q wirkt im elektrischen Feld E (V/cm) die Kraft Q@E, so dass die Wanderungsgeschwindigkeit des Teilchens v = Q@E/f (1) beträgt. Für den Idealfall einer Kugel ist der Reibungskoeffizient f = 6 πηr (r = Stokes'scher Radius, η = Viskosität des Mediums). Gleichung (1) zeigt, dass die Wanderungsgeschwindigkeit proportional zum Spannungsabfall (= Feldstärke = Spannung pro Längeneinheit des Elektrophoresestreifens, Volt/cm) und proportional zur Ladung des wandernden Teilchens ist. Die Ladung ist bei Aminosäuren und Proteinen vom pH-Wert abhängig. Der Reibungskoeffizient f ist abhängig von Form und Grösse der Teilchen und von der Viskosität des Mediums. Bei der Elektrophorese entsteht Wärme. Die pro Zeiteinheit gebildete Wärme H beträgt R@I2 (R = elektrischer Widerstand, I = Stromstärke). Bei der Hochspannungselektrophorese (Feldstärken bis einige 100 V/cm und Stromstärken von gegen 1 Ampère) wird die entstehende Wärme mit einem Kühlsystem abgeführt. CHROMATOGRAPHIE Chromatographische Trennmethoden beruhen im wesentlichen darauf, dass sich die zu trennenden Substanzen je nach ihren physikalisch-chemischen Eigenschaften zwischen einer stationären und einer mobilen Phase ungleich verteilen. Die verschiedenen Verfahren können grob klassifiziert werden in Verteilungschromatographie (Papier-, Dünnschicht-, Gaschromatographie), Adsorptionschromatographie (Ionenaustauscher-, Affinitätschromatographie) und Gelchromatographie (Gelfiltration). Die Verteilungschromatographie beruht auf der verschiedenen Löslichkeit der zu trennenden Substanzen in den Phasen. Bei der Adsorptionschromatographie wirken verschieden starke nichtkovalente Bindungskräfte zwischen den zu trennenden Substanzen und den Molekülen der einzelnen Phasen. In der Gelchromatographie beruht die Trennung auf der räumlich begrenzten Zugänglichkeit der verschiedenen Phasen für unterschiedlich grosse Moleküle. Während der chromatographischen Trennung werden die stationäre und die mobile Phase gegeneinander verschoben. Verschiedene Kombinationen von festen, flüssigen und gasförmigen Phasen sind je nach Chromatographietyp möglich. Eine Übersicht gibt die folgende Tabelle.