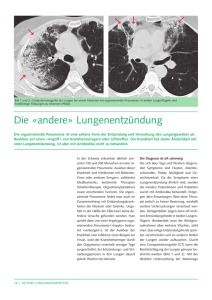
Stellenwert des konventionellen Röntgen-Thorax in der
Werbung

Stellenwert des konventionellen Röntgen-Thorax in der Diagnostik von Infektionen bei ambulanten Patienten nach Chemotherapie und Niedrigrisiko-Neutropenie (Retrospektive Analyse) Der Medizinischen Fakultät der Friedrich-Alexander-Universität Erlangen-Nürnberg zur Erlangung des Doktorgrades Dr. med. dent. vorgelegt von Martina Thaller aus Weiden in der Oberpfalz Als Dissertation genehmigt von der Medizinischen Fakultät der Friedrich-Alexander-Universität Erlangen-Nürnberg Vorsitzender des Promotionsorgans: Prof. Dr. Dr. h.c. J. Schüttler Gutachter: Prof. Dr. Stefan Krause Gutachter: Prof. Dr. Andreas Mackensen Tag der mündlichen Prüfung: 22. Januar 2015 MEINEN ELTERN GEWIDMET I Inhaltsverzeichnis 1. Einleitung ............................................................................................. 1 1.1 Neutropenie (Granulozytopenie): ....................................................................... 1 1.2 Fieber..................................................................................................................... 2 1.3 Infektionen bei Neutropenie ................................................................................ 3 1.4 Die Röntgen-Thorax-Aufnahme ......................................................................... 5 1.5 Therapie ................................................................................................................ 6 2. Ziel der Studie / Fragestellung ........................................................... 8 3. Patienten und Methoden .................................................................... 9 3.1 Patienten ............................................................................................................... 9 3.1.1 Patientenkollektiv................................................................................................ 9 3.1.2 Definitionen......................................................................................................... 9 3.1.3 Einschlusskriterien ............................................................................................ 10 3.1.4 Ausschlusskriterien ........................................................................................... 10 3.1.5 Stratifizierung der zu analysierenden Kollektive .............................................. 11 3.2 Methoden ............................................................................................................ 12 3.2.1 Dokumentation / Datenerhebung ...................................................................... 12 3.2.3 Datenanalyse ..................................................................................................... 19 4. Ergebnisse .......................................................................................... 22 4.1 Screening und Studieneinschluss ...................................................................... 22 4.2 Darstellung der Studienpatienten ..................................................................... 22 4.3 Verteilung der Einschlusspatienten auf vier verschiedene Kollektive .......... 23 4.4 Grunderkrankungen .......................................................................................... 23 4.5 Chemotherapien und Therapielinien ............................................................... 24 4.6 Auswertungsparameter der vier Studienkollektive ........................................ 25 4.6.1 Pulmonale Vorerkrankungen ............................................................................ 25 4.6.2 Fieber ................................................................................................................ 25 4.6.3 Infektsymptome................................................................................................. 26 4.6.3.1 Respiratorische Symptome ................................................................... 26 4.6.3.2 Nicht-respiratorische Symptome ........................................................... 26 4.6.3.3 Nicht Pneumonie-spezifische, respiratorische Symptome .................... 27 4.6.3.4 Technische Befunde für die weitere Abklärung einer Pneumonie........ 28 4.7 Auswertung der Röntgen-Thorax-Untersuchungen ....................................... 29 II 4.8 Auswertung der CT-Thorax-Untersuchungen ................................................ 33 4.9 Therapieumstellung aufgrund positiver Befunde in der Röntgen-ThoraxUntersuchung ........................................................................................................... 35 4.10 Behandlungsdauer ........................................................................................... 37 4.11 Abschließende Beurteilungen für das Indexereignis .................................... 38 4.12 Korrelation der abschließenden Diagnosen mit den Röntgen-ThoraxErgebnissen ............................................................................................................... 40 4.13 Überlebenswahrscheinlichkeit und Mortalitätsrate ..................................... 41 4.13.1 Überlebenswahrscheinlichkeit ........................................................................ 41 4.13.2 Mortalitätsrate ................................................................................................. 41 5. Diskussion .......................................................................................... 42 5.1 Infektionen nach Chemotherapie und Niedrigrisiko-Neutropenie ............... 42 5.2 Radiologischer Nachweis einer Infektion mit der Röntgen-ThoraxAufnahme .................................................................................................................. 44 5.2.1 Stellenwert der konventionellen Röntgen-Thorax-Aufnahme .......................... 44 5.2.2 CT-Thorax-Untersuchungen zur weiteren diagnostischen Abklärung des Röntgen-Thorax ......................................................................................................... 46 5.3 Therapie und Therapieumstellung ................................................................... 49 5.4 Behandlungsdauer und Sterblichkeit mit und ohne Pneumonie ................... 51 6. Zusammenfassung ............................................................................. 53 6.1 Hintergrund und Ziele ....................................................................................... 53 6.2 Methoden (Patienten und Untersuchungsmethoden) ..................................... 53 6.3 Ergebnisse und Beobachtungen ........................................................................ 53 6.4 Praktische Schlussfolgerungen ......................................................................... 54 7. Literaturverzeichnis.......................................................................... 55 8. Abbildungsverzeichnis ...................................................................... 61 9. Tabellenverzeichnis ........................................................................... 62 10. Abkürzungsverzeichnis .................................................................. 64 11. Anhang ............................................................................................. 65 12. Danksagung ..................................................................................... 73 -1- 1. Einleitung Für onkologische Patienten stellen Infektionen eines der größten Risiken dar (7, 12, 22, 56). Laut Buchheidt et al. (11) werden ca. 70 % der tödlichen Komplikationen durch Infektionen verursacht. Neben der Grunderkrankung selbst ist die zytotoxische und immunsuppressive Therapie eine der essentiellen Ursachen für die Schwächung der körpereigenen Abwehr. Das wesentliche Defizit der Zytostatika besteht darin, dass diese nicht nur auf die Tumorzellen wirken, sondern auch gesunde Zellen des Körpers, wie z. B. Zellen des Knochenmarks, angreifen. Da neutrophile Granulozyten im Knochenmark gebildet werden, wird auch deren Neubildung durch Zytostatikagabe unterdrückt, weshalb es zur Neutropenie kommt und somit die Infektanfälligkeit enorm ansteigt (33). Der Zusammenhang zwischen dem Ausmaß und der Dauer einer chemotherapiebedingten Neutropenie und der Morbidität und Letalität durch Infektionen ist bereits seit den 60er Jahren bekannt (7). Die Arbeitsgemeinschaft Infektionen in der Hämatologie und Onkologie (AGIHO) der Deutschen Gesellschaft für Hämatologie und Onkologie (DGHO) (15) formulierte erstmals 1999 offizielle Leitlinien zur Behandlung neutropener Patienten, die seitdem stets aktualisiert werden und in der vorliegenden Arbeit als richtungweisend gelten. 1.1 Neutropenie (Granulozytopenie): Die deutsche Gesellschaft für Hämatologie und Onkologie (15) definiert Neutropenie folgendermaßen: „Neutrophile Granulozyten (Segment- und Stabkernige) < 500/mm3 oder < 1000/mm3 mit erwartetem Abfall < 500/mm3 innerhalb der nächsten zwei Tage (15).“ Risikozuordnung der Patienten nach erwarteter Neutropeniedauer und Risikofaktoren (15) Niedrigrisiko Neutropeniedauer ≤ 5 Tage Mittleres Risiko Neutropeniedauer 6 - 9 Tage Hochrisiko Neutropeniedauer ≥ 10 Tage Tab. 1: Risikozuordnung der Patienten nach erwarteter Neutropeniedauer und Risikofaktoren (15) -2Laut Bodey et al. (6, 7) sind bei Infektionen die Dauer und Schwere der Granulozytopenie für die Überlebenschancen der Patienten entscheidend. Auch Hughes et al. (27) geben an, dass bei Granulozytenzahlen unter 1000/µl das Infektionsrisiko rapide ansteigt und bei weiterem Abfall unter 500/µl für über zehn Tage die Zahl lebensbedrohlicher Infektionen hochsignifikant ansteigt. Außerdem beschreiben sowohl Bodey et al. (7) als auch Hughes et al. (27), dass fast alle letalen Infektionen bei Granulozytenzahlen < 100/µl auftreten und nach Unterschreitung dieser Grenze bereits bei jedem zweiten Patienten eine Bakteriämie vorliegt. Steigen die Granulozyten, z. B. bei gramnegativer Sepsis, nicht wieder über diese Grenze, liegt die Letalität der Infektion laut EORTC (18) bei über 80 %. Die durchgeführte retrospektive Analyse setzt sich mit neutropenen NiedrigrisikoPatienten auseinander, weshalb im Folgenden speziell darauf Bezug genommen wird. 1.2 Fieber Die AGIHO der DGHO (15) definiert Fieber als einmalige Temperaturerhöhung ≥ 38,3° C oder als Temperaturanstieg ≥ 38,0° C, der für mindestens eine Stunde andauert bzw. zweimal innerhalb von 12 Stunden auftritt. Ist dem diagnostizierten Fieber kein eindeutiger klinischer oder mikrobiologischer Infektionsbefund zuzuordnen, spricht man von Fieber unklarer Genese bzw. von „fever of unknown origin“ (FUO). Laut Pizzo (48) bleibt die Ätiologie des Fiebers bei etwa zwei Drittel der Fieberepisoden onkologischer Patienten ungeklärt (FUO) und bei 5 % - 10 % der Fieberepisoden werden schwere Komplikationen als Folge von bakteriellen Infektionen beschrieben (22, 56). Auch wenn bei neutropenen Patienten Fieber oft das einzige Zeichen einer Infektion ist, wird laut Link (37) nur bei 50 % aller Patienten eine Infektion diagnostiziert, während bei den anderen 50 % kein Infekt gefunden wird. Als nennenswert erscheint Link (37) dabei die Letalität einer zu spät behandelten Infektion, da diese bei 70 % - 100 % liegt. -3- 1.3 Infektionen bei Neutropenie Die Häufigkeit und Bedrohlichkeit verschiedener Infektionserreger sind in erster Linie vom Status des Patienten (Grunderkrankung, Toxizität der Chemotherapie, Begleiterkrankungen, Alter) und in zweiter Linie von der Praxis der Infektionsprophylaxe (Chemoprophylaxe, Expositionsprophylaxe, Klinikhygiene) abhängig (43). Aufgrund der Vielzahl möglicher Infektionserreger werden bei ersten klinischen Anzeichen einer Infektion, z. B. Fieber, empirische Therapieregime mit einem breiten Wirkspektrum eingesetzt (15). Durch dieses Vorgehen konnte die durch Infektionen bedingte Letalität in den letzten Jahrzehnten erheblich gesenkt werden (53). In einer Studie der Paul-Ehrlich-Gesellschaft (PEG-1) (44) (Tab.2) wurden die am häufigsten klinisch oder mikrobiologisch gesicherten Infektionen dokumentiert. Infektionsort Anzahl Anteil der Infektionen Pneumonie 269 35 % Haut / ZVK 139 18 % Peritoneal / perineal 72 9% Harnwegsinfekt 18 2% Andere 53 7% Bakteriämie / Fungämie 222 29 % Tab. 2: Häufigkeit der Infektionsherde in der multizentrischen PEG-Studie mit 1.573 Patienten, bei denen 773 (49 %) Infektionen klinisch oder mikrobiologisch dokumentiert wurden (44). Wie in Tabelle 2 ersichtlich ist, stellen Pneumonien (35 %) und Bakteriämien / Fungämien (29 %) die häufigsten Infektionen dar. Husten, Schmerzen beim Atmen, Pleurareiben und Rasselgeräusche über der Lunge stehen dabei in einem engen Zusammenhang mit einer Pneumonie (Lungenentzündung) (2, 49). -4Die im Folgenden genannten Erreger sind speziell für Pneumonien verantwortlich (4): Bakterien Streptococcus pneumoniae, Staphylokokken, Haemophilus influenzae, Klebsiellen Proteus, Mykoplasmen, Chlamydien. Legionella pneumoniae, Pseudomonas aeruginosa Viren RS-, Paramyxo-, Picorna-, Adeno-, Herpes-, Zytomegalie-Viren Pilze Candida, Aspergillus, Mucor, Cryptococcus, Pneumocysti jiroveci Protozoen Toxoplasma Tab. 3: Erreger einer Pneumonie (4) Obwohl die Übertragungswege unterschiedlich sind, erfolgen Ansteckungen hauptsächlich über Tröpfcheninfektion, wie z. B. die Pneumokokkenpneumonie (Streptococcus pneumoniae, welche die häufigste Pneumonieform darstellt) oder die Viruspneumonie (50 % bei Influenza) und über Aerosole (Klimaanlage, Wasserleitung) wie die Legionellenpneumonie (Legionella pneumonia) (4). Hierbei gilt der Grundsatz, dass Pneumonien unverzüglich behandelt werden müssen, damit es nicht zu Komplikationen wie septischem Schock mit respiratorischer Insuffizienz, Lungenabszess, Pleuraemphysem, Pleuraerguss oder Lungenfibrose kommt. Da bakterielle Infektionen und Pneumonien eine ungünstigere Prognose als sonstige Infektionen oder neutropenisches Fieber unklarer Ursache (FUO) haben, ist gerade bei Patienten mit Immunschwäche nach einer Chemotherapie höchste Aufmerksamkeit geboten, zumal diese innerhalb von Stunden zu gravierenden Verschlechterungen bis hin zum Tod führen können (43). Eine frühe Diagnostik (klinisch, mikrobiologisch und klinisch-chemisch) (15) ist daher stets angezeigt. -5- 1.4 Die Röntgen-Thorax-Aufnahme Bei Patienten, die wegen Fiebers oder eines Verdachts auf einen Infekt nach einer stattgefundenen Chemotherapie eine Klinik aufsuchen, gehört zur Standarddiagnostik eine Röntgen-Thorax-Aufnahme in zwei Ebenen. Bei der Thoraxaufnahme handelt es sich um eine Routineuntersuchung, bei der Lunge, Herzgröße, Mediastinum, Pleura, Zwerchfell und der knöcherne Brustkorb mit Rippen, Sternum und Brustwirbelsäule beurteilt werden können. Pulmonale Infekte zeigen anfangs nur selten eine klassische Symptomatik. Treten Husten, Thoraxschmerz, Tachypnoe oder Ähnliches auf, liegt häufig schon eine ausgedehnte Infektion vor (23). Da bei etwa einem Drittel aller neutropenen Patienten eine auf der Thoraxübersicht erkennbare Pneumonie nachweisbar ist (40, 45), sollte die Lunge allein bei Vorliegen eines neutropenischen Fiebers radiologisch untersucht werden. Aus diesem Grund wurde diese bei den Patienten, deren Daten in der vorliegenden Arbeit ausgewertet wurden, zur Abklärung von Pneumonien, eines Pneumothoraxes oder eines etwaigen Pleuraergusses verwendet, um die Lokalisation des möglichen Infektionsherdes zu finden und anschließend mit der Identifikation des die Infektion verursachenden Erregers fortfahren zu können. Jedoch ist die diagnostische Wertigkeit bei Thoraxübersichtsaufnahmen begrenzt. Bei der Pneumoniesuche sind beispielsweise 40 % - 50 % der Übersichtsaufnahmen falsch negativ. Deshalb kann eine Pneumonie selbst bei normalem Übersichtsbild nicht ausgeschlossen werden (3, 24, 25). Die DGHO (16) empfiehlt in ihren Leitlinien: „Bei Patienten mit Fieber unklarer Genese (FUO) oder dokumentierter Infektion jenseits von Lungeninfiltraten, die nicht innerhalb der ersten 72 - 96 Stunden nach Therapiebeginn auf eine antibakterielle Behandlung ansprechen, sollte innerhalb von 24 Stunden eine Computertomographie der Thoraxorgane durchgeführt werden. Hierbei ist eine "High Resolution"-Technik oder eine Dünnschicht-Technik im Rahmen einer Mehrzeilen-CT zu bevorzugen. Bei Patienten mit pathologischen Befunden auf einer konventionellen Thorax-Röntgenaufnahme wird die Durchführung einer CT-Aufnahme der Thoraxorgane zur besseren Differenzierung der Infiltrate empfohlen (16).“ In Anlehnung an diese Empfehlungen sollte stets die zusätzliche Untersuchung mittels einer Computertomographie erfolgen, da hierbei eine überlagerungsfreie Darstellung des Lungenparenchyms gewährleistet wird, Pneumonien früher erkannt werden und die Sensitivität sowie die Spezifität gegenüber der Thoraxübersicht signifikant höher sind (3, 13, 21, 32, 55). -6- 1.5 Therapie Um lebensbedrohliche Infektionsverläufe zu vermeiden, gilt es, febrile Patienten innerhalb von zwei Stunden nach Auftreten des Fiebers mit Antibiotika zu behandeln (37, 54). Die DGHO (15) empfiehlt zur empirischen Therapie für Niedrigrisiko-Patienten folgendes Vorgehen: Abb. 1: Niedrigrisiko-Patienten, empirische Therapie und Management (15) -7Kontrolle des therapeutischen Ansprechens Laut DGHO (15) muss das Behandlungsergebnis jeweils innerhalb von 72 - 96 Stunden nach Beginn oder Modifikation der antimikrobiellen Therapie (initiales Ansprechen), zum Zeitpunkt der Beendigung der antimikrobiellen Therapie (definitives Ansprechen) und nach Ablauf einer adäquaten Nachbeobachtungszeit (in der Regel sieben Tage) beurteilt werden. Eine Kontrolle des Behandlungserfolges wird nach 72 Stunden antimikrobieller Therapie getroffen. Von einem Erfolg kann dann gesprochen werden, wenn zum Zeitpunkt der Beurteilung die Körpertemperatur weniger als 38° C beträgt, ohne dass Anzeichen für eine Infektion bestehen. Sind die Kriterien für eine erfolgreiche Behandlung erfüllt, empfiehlt die DGHO (15), das Therapieregime bis zur Fieberfreiheit an insgesamt sieben konsekutiven Tagen fortzuführen, sofern die Zahl der neutrophilen Granulozyten weiterhin < 1000/mm3 bleibt. Bei einem Wiederanstieg der neutrophilen Granulozyten > 1000/mm3 genügen zwei weitere fieberfreie Tage nach Eintritt der Entfieberung. Nach Beendigung der antimikrobiellen Therapie ist gemäß den DGHO-Richtlinien (15) eine (ambulante) Nachbeobachtung von sieben Tagen erforderlich, um ein Infektionsrezidiv oder eine Sekundärinfektion erfassen zu können. Die Therapie kann schließlich beendet werden, wenn die Patienten fieberfrei sind und der Wert der Leukozyten > 1000/mm3 ist (15). -8- 2. Ziel der Studie / Fragestellung Da Infektionen bei onkologischen Patienten nach wie vor ein großes Problem darstellen und die Diagnostik dieser Infektionen weiterhin schwierig ist, fand in der vorliegenden retrospektiven Analyse eine Untersuchung des Stellenwertes der konventionellen Röntgen-Thorax-Aufnahme in der Diagnostik von Infektionen bei ambulanten Patienten nach Chemotherapie und Niedrigrisiko-Neutropenie statt. Folgende Fragen wurden geprüft und ausgewertet: 1. Wie hoch war der prozentuale Anteil der Röntgen-Thorax-Aufnahmen? 2. Wie hoch war die Anzahl der positiven Befunde im Röntgen-Thorax? - Pneumonien und Pneumonieverdachtsfälle - Andere Diagnosen, die vorher nicht bekannt waren (vorbekannte Veränderungen führten zum Ausschluss des Patienten aus der Studie) Dabei wurde ggf. die Absicherung der Diagnose aus dem Röntgen-Thorax durch weitere Diagnostikverfahren berücksichtigt. 3. Gab es Therapieänderungen oder eine ergänzende Diagnostik aufgrund von positiven Befunden? 4. Welche Unterschiede gab es hinsichtlich der Behandlungsdauer bei Patienten mit Pneumonie im Gegensatz zu solchen, die keine Pneumonie hatten? Zusammenfassend sollte die Frage geklärt werden, ob die konventionellen RöntgenThorax-Aufnahmen in ihrem Stellenwert unzureichend und deshalb verzichtbar sind. -9- 3. Patienten und Methoden 3.1 Patienten 3.1.1 Patientenkollektiv Im Rahmen dieser retrospektiven Studie wurde im Zeitraum von Januar 2005 bis einschließlich Februar 2007 an der Klinik für Hämatologie / Onkologie des Universitätsklinikums Regensburg bei ambulanten Patienten der Stellenwert des konventionellen Röntgen-Thorax in der Diagnostik von Infektionen nach Chemotherapie und Niedrigrisiko-Neutropenie untersucht. Die Auswahl der Patienten erfolgte mit Hilfe der Arztbriefdatenbank. Als Suchbegriffe dienten: Neutropenie, Fieber und Infekt. Alle auf diese Weise erfassten Patienten wurden auf vorher klar definierte Einschluss- und Ausschlusskriterien (3.1.3 und 3.1.4) überprüft. 3.1.2 Definitionen Die genauen Definitionen erfolgten in Anlehnung an die Leitlinien und Empfehlungen der Arbeitsgemeinschaft Infektionen in der Hämatologie und Onkologie (AGIHO) der Deutschen Gesellschaft für Hämatologie und Onkologie (DGHO) (15) sowie festgelegte Normwerte für das Blutbild aus dem Institut für Klinische Chemie und Laboratoriumsmedizin der Universitätsklinik Regensburg. Normwerte für Leukozyten, neutrophile Granulozyten, Thrombozyten, Hämoglobin-Wert und CRP-Wert: Leukozyten (/nl): 4,8 - 10,8 Neutrophile Granulozyten (%): 41,2 - 70,1 Thrombozyten (/nl): 130 - 140 Hämoglobin (g/dl): 13,3 - 17,7 CRP (mg/l): < 5,0 - 10 - Fieber in der Neutropenie (15): Fieber: ≥ 38,3° C oder ≥ 38,0° C für mindestens eine Stunde oder zweimal innerhalb von zwölf Stunden Neutropenie: Neutrophile Granulozyten < 500/µl oder < 1000/µl mit zu erwartendem Abfall unter 500/µl innerhalb der nächsten zwei Tage Niedrigrisiko-Neutropenie: Neutropeniedauer ≤ 5 Tage 3.1.3 Einschlusskriterien Die Patienten dieser Studie mussten folgende Kriterien erfüllen, um in der Auswertung erfasst werden zu können: Es musste eine maligne Erkrankung vorliegen. Eine Chemotherapie fand mindestens einen Tag vorher statt und wurde vor weniger als 28 Tagen abgeschlossen. Der Patient kam von zu Hause während oder nach der Neutropenie. Der Patient kam wegen Fiebers oder eines Verdachts auf einen Infekt, z. B. Husten, Pleurareiben, Rasselgeräusche über der Lunge, Schmerzen beim Atmen etc., in die Notaufnahme, Ambulanz oder direkt auf Station. Insgesamt erfüllten letzten Endes 119 Patienten diese Kriterien und konnten in die Studie aufgenommen werden. 3.1.4 Ausschlusskriterien Zum Ausschluss kam es, wenn folgende Diagnosen zutrafen: Ein Infektverdacht ließ sich bereits nach der Anamnese nicht aufrechterhalten. Es lagen bekannte Lungenveränderungen vor, die eine Diagnose der Pneumonie erschwerten, z. B.: - eine bekannte Pneumonie mit bekannten Residuen oder der Zustand nach einer Pneumonie in den letzten acht Wochen - ein bekannter Pleuraerguss - eine bekannte Lungenfibrose, Strahlenpneumonitis etc. - Lungenmetastasen Ausnahme: Es bestand bei einzelnen, gut abgrenzbaren Lungenmetastasen kein Ausschlussgrund. - 11 - 3.1.5 Stratifizierung der zu analysierenden Kollektive Die Patienten wurden entsprechend den klinischen Diagnosen in vier verschiedene Kollektive eingeteilt, die folgendermaßen zustande kamen: Bestand zum Indexdatum (= Fieberbeginn) noch eine Neutropenie: ja oder nein Atemwegserkrankungen mit klinischem Verdacht auf Pneumonie: ja oder nein Daraus ergaben sich schließlich folgende vier Kollektive: Kollektiv 1: Fieber in / während der Neutropenie ohne konkreten Hinweis auf eine Atemwegserkrankung Kollektiv 2: Fieber in / während der Neutropenie mit Hinweis auf eine Atemwegserkrankung bzw. Pneumonie: - Husten - Schmerzen beim Atmen - Pleurareiben - Rasselgeräusche über der Lunge Anmerkung: Symptome des oberen Respirationstraktes (nur Schnupfen, Halsschmerzen etc.) wurden nicht als Hinweis auf mögliche Pneumonie gewertet. Kollektiv 3: Fieber nach der Neutropenie ohne konkreten Hinweis auf eine Atemwegserkrankung Kollektiv 4: Fieber nach der Neutropenie mit Hinweis auf eine Atemwegserkrankung bzw. Pneumonie: - Husten - Schmerzen beim Atmen - Pleurareiben - Rasselgeräusche über der Lunge - 12 - 3.2 Methoden 3.2.1 Dokumentation / Datenerhebung Für eine systematische Dokumentation der Patientenkollektive wurde für jeden Einschlusspatienten zunächst ein Auswertungsbogen (Anhang 1, S. 65/66) bearbeitet. In diesem wurden allgemeine Patientendaten mit Vor- und Nachnamen sowie Geburtsdaten vermerkt. Außerdem erfolgte die Dokumentation der Tumordiagnose, der Chemotherapie und deren Therapielinie (first-line, second-line, third-line oder mehr) sowie pulmonale Vor- und Begleiterkrankungen, wie z. B. einzelne, gut abgrenzbare Lungenmetastasen, eine frühere Pneumonie und COPD (= chronic obstructive pulmonary disease). Um respiratorische und / oder nicht-eindeutig-respiratorische Beschwerden / Befunde bei Infektverdacht zu dokumentieren, musste zunächst das Datum der Untersuchung aufgrund des Fiebers bzw. des Infektverdachtes (= Indexdatum) notiert werden, auf welches sich alle Diagnosen und Befunde, die innerhalb der drei darauf folgenden Tage stattfanden, bezogen. Im Einzelnen wurden folgende respiratorischen und nicht-eindeutig-respiratorischen Beschwerden / Befunde untersucht: Respiratorische Beschwerden / Symptome: Husten Schmerzen beim Atmen Pulmonale Rasselgeräusche Pleurareiben Nicht-eindeutig-respiratorische Beschwerden / Symptome: Fieber Atemnot Verschlechterung des Allgemeinzustandes Halsschmerzen und Schnupfen Schluckbeschwerden Bauchschmerzen und / oder Diarrhoe Halsrötung Giemen und / oder Obstruktion Verdacht auf Thrombose - 13 Beim Blutbild interessierten die Werte der Leukozyten, der neutrophilen Granulozyten, der Thrombozyten, der Hämoglobin- und der CRP-Wert. Diese wurden jeweils mit den Normwerten des Institutes für Klinische Chemie und Laboratoriumsmedizin des Universitätsklinikums Regensburg verglichen und die Patienten schließlich den jeweiligen Kollektiven zugeordnet (3.1.5). Bei den Röntgen-Thorax-Aufnahmen war für die Studie entscheidend: Durchführung einer Röntgenuntersuchung: ja oder nein Datum der Untersuchung: Einschluss nur, wenn die Röntgenuntersuchung innerhalb der drei folgenden Tage nach Indexdatum stattfand. Befund der Untersuchung: - Keine Pneumonie - Keine Pneumonie, jedoch anderer spezifischer Befund - Keine Pneumonie und unauffälliger Befund - Fragliche Pneumonie - Gesicherte Pneumonie Die gesammelten Auswertungen wurden mit den weiterführenden klinischen Diagnostiken, d. h. Blut-, Urin- und Stuhlkultur, Sputum-Untersuchung, Rachenabstrich und radiologischen Diagnostiken, wie z. B. das Röntgen des Abdomens, die Sonographie etc. untersucht, sofern diese innerhalb von drei Tagen nach Indexdatum durchgeführt wurden. Für den weiteren Behandlungsverlauf der für die Studie aufgenommenen Patienten beinhaltete der Auswertungsbogen außerdem die Dokumentationen über: Einleitung, Umsetzung und Fortführung einer bestimmten Antibiose, wie z. B. Clarithromycin, Erythromycin o. ä. Verabreichung anderer Medikationen, z. B. Antimykotika, Virustatika o. ä. Ambulanter oder stationärer Aufenthalt der Patienten mit jeweiliger Dauer Überlebenszeit der Patienten: mehr oder weniger als vier Wochen Die gesamte Datenerhebung erfolgte mit Hilfe von SAP und den jeweiligen stationären bzw. archivierten Krankenakten mit allen zur Auswertung erforderlichen Daten (Vorbefunde, Arztbriefe, Röntgenbefunde, Laborbefunde und histopathologische Befunde). - 14 - 3.2.2 Datenverarbeitung Nach Erfassung der Auswertungsbögen hinsichtlich der bereits genannten Kriterien wurden die gewonnenen Daten in eine Excel-Tabelle des Microsoft-Office-ExcelProgramms 2003 übertragen und anhand statistischer Funktionen desselbigen ausgewertet. Maximal- und Minimalwerte der Daten wurden in Säulendiagrammen zur Veranschaulichung dargestellt. Folgende Daten fanden in der Excel-Datei Berücksichtigung: Patient ein- oder ausgeschlossen Patientennummer Patienten-Identifikationsnummer Nachname Vorname Geschlecht Geburtsdatum Alter Tumor-Diagnose Indextermin: Datum der Untersuchung wegen Fiebers bzw. Infektes Ausschlussgründe: keine Tumorerkrankung, bekannter Pleuraerguss, Pneumonie vor weniger als acht Wochen, Dauerchemotherapie, letzte Chemotherapie fand vor mehr als 28 Tagen statt, kein Zustand nach Chemotherapie, Lungenmetastasen, keine eindeutigen Infektzeichen, Radiochemotherapie Zeitspanne des Fiebers (Angabe der Fiebertage) Patient kommt über die Notaufnahme in die Klinik: ja oder nein Chemotherapie-Schema Beginn der Chemotherapie Ende der Chemotherapie Therapielinie Pulmonale Vorerkrankungen, wie z. B. Pneumonie, Lungenmetastasen, Lungenfibrose, COPD (= chronic obstructive pulmonary disease) etc. Leukozyten-Wert Anzahl der neutrophilen Granulozyten CRP-Wert - 15 Allgemeine Infektzeichen, wie z. B. Fieber, CRP-Erhöhung ohne Fieber, Verschlechterung des Allgemeinzustandes Infektsymptome, wie z. B. Husten, Pleurareiben oder -schmerz, Rasselgeräusche, Halsschmerzen, Mukositis, Diarrhoe, Venenthrombose, Harnblasenreizung etc. Respiratorische Symptome wie Husten, Schmerzen beim Atmen, Pleurareiben, Rasselgeräusche (z. B. Giemen) über der Lunge Nicht-eindeutig-respiratorische Symptome wie Mukositis, Diarrhoe, Blasenentzündung etc. Nicht Pneumonie-spezifische, respiratorische Symptome wie Halsschmerzen, Halsrötung, Schluckbeschwerden, Dyspnoe Stratum / Kollektive 1-4 (3.1.5) Röntgen-Auswertung: 1. Keine Röntgen-Thorax-Aufnahme 2. Röntgen-Untersuchung: nur Röntgen-Thorax oder CT-Thorax erst später 3. Zeitlicher Abstand der Röntgen-CT-Untersuchung: Röntgen-ThoraxAufnahme, dann CT-Untersuchung innerhalb von drei Tagen 4. Sonstige Röntgenuntersuchungen, z. B. Röntgen-Abdomen 5. CT-Untersuchung: direkte CT-Untersuchung ohne weitere Röntgenaufnahmen 6. Sonstiges: weitere Bildgebung, z. B. Sonographie Zeitlicher Abstand zwischen Röntgen-Thorax- und CT-Thorax-Aufnahme Röntgen-Thorax-Ergebnis: 1. Keine Pneumonie 2. Keine Pneumonie, jedoch anderer spezifischer Befund 3. Keine Pneumonie und unauffälliger Befund 4. Fragliche Pneumonie 5. Gesicherte Pneumonie CT-Thorax-Ergebnis: 1. Unauffälliger Befund 2. Fragliche Pneumonie 3. Gesicherte Pneumonie 4. Metastasen 5. Lungenembolie - 16 6. Erguss 7. Sonstiges (Pleuraerguss, Flüssigkeitsansammlung etc.) Weitere technische Befunde: 1. Blutkultur negativ 2. Blutkulturen fraglich positiv 3. Blutkulturen sicher positiv 4. Anderer bakterieller Infekt (nachgewiesen im Urin oder Stuhl) 5. Urin- / Stuhl-Probe negativ 6. Urin- / Stuhl-Probe fraglich 7. Positiver Befund aus der bronchoalveolären Lavage (BAL) 8. Aspergillus-Antigen positiv im Serum 9. Aspergillus-Antigen positiv im Serum fraglich 10. Aspergillus-Antigen negativ im Serum 11. Virusinfekt nachgewiesen (PCR) 12. Sonstiges (Sputum-Untersuchung, Rachenabstrich etc.) Beurteilungsindex: 1. Gesicherte Pneumonie Pneumonische Infiltrate in der Röntgen-Thorax-Aufnahme sichtbar, CT-Befund und andere Befunde widerlegen Pneumonie nicht oder Gesicherte Pneumonie im CT-Thorax 2. Fragliche Pneumonie Verdacht auf pneumonische Infiltrate in der Röntgen-Thorax-Aufnahme und Keine eindeutigen Hinweise auf gesicherte Pneumonie im CT-Thorax oder anderen Befunden und Keine eindeutigen Hinweise auf anderen Infekt in klinischen und / oder technischen Befunden, so dass fragliche Pneumonie am wahrscheinlichsten bleibt. - 17 - 3. Nicht-pulmonaler Infekt Initial keine Hinweise auf gesicherte Pneumonie oder Verdacht auf Pneumonie in der Röntgen-Thorax-Aufnahme oder im CT-Thorax und Nachweis eines nicht-pulmonalen Infektes mit gesichertem Infektionsort in klinischen und / oder technischen Befunden (z. B. Harnwegsinfekt, Katheterinfekt) oder Symptome, die einen HNO-Infekt nahe legen, aber ohne Hinweis für Pneumonie sind: Halsschmerzen, Bronchitis, Tonsillitis, Schluckbeschwerden etc. 4. Fieber, Verdacht auf Infekt ohne einen Organfokus Keine Hinweise auf gesicherte Pneumonie oder Verdacht auf Pneumonie in der Röntgen-Thorax-Aufnahme oder im CT-Thorax und Verdacht auf Infekt mit oder ohne Nachweis einer Septikämie, Bakteriämie, jedoch ohne konkreten Hinweis auf einen Infektionsort 5. Sonstiges Keine Hinweise auf gesicherte Pneumonie oder Verdacht auf Pneumonie in der Röntgen-Thorax-Aufnahme und Respiratorische, nicht-pulmonale Symptome ohne konkreten Nachweis auf einen Infekt: Halsschmerzen, Bronchitis, Tonsillitis, Schluckbeschwerden, Hinweise auf eine nicht-infektiöse Ursache: Dyspnoe, Lungenembolie, Mukositis, Tumorfieber etc. Antibiose: 1. Orale Antibiose begonnen 2. i.v. Antibiose begonnen 3. Orale Antibiose umgesetzt oder orale Antibiose zugesetzt 4. Systemische Pilztherapie begonnen (Diflucan zählt nicht) 5. Diflucan begonnen 6. Laufende Antibiose beibehalten 7. Keine Antibiose begonnen - 18 Medikation: 1. Antimykotika (nicht Fluconazol, d. h., nicht Diflucan, aber z. B. Voriconazol / V-Fend) 2. Erweiterung der antibiotischen Therapie (z. B. Erythromycin, Clarythromycin etc.) 3. Bronchoalveoläre Lavage (BAL) Dauer des stationären Aufenthaltes Überlebensdauer der Patienten (Richtwert: vier Wochen) Weitere Diagnosen (z. B. Tumorfieber, Lungenembolie etc.) - 19 - 3.2.3 Datenanalyse Die Analyse der Daten erfolgte mit dem Statistikprogramm SPSS für Windows. Die Signifikanz der Ergebnisse wurde mit dem CHI-QUADRAT-TEST nach PEARSON ermittelt. Das minimale Signifikanzniveau wurde bei allen statistischen Tests mit p ≤ 0,05 festgesetzt. Anmerkung: Liegt der p-Wert im Bereich zwischen 0,05 und 0,01 spricht man von „signifikant“, liegt er unter 0,01, ist das Ergebnis „sehr signifikant“. Folgende Fragestellungen wurden auf Signifikanz geprüft: 1. Gibt es bei klinischem Verdacht signifikant häufiger einen Röntgen-Thorax mit Pneumonie oder Verdacht auf Pneumonie? Ergebnis: Ja, p = 0,0006 60 50 Fälle 40 Keine Pneumonie 30 Fragliche Pneumonie Pneumonie 20 10 0 Klinischer Verdacht Kein Verdacht Abb. 2: Klinischer Verdacht auf Pneumonie vs. kein Verdacht: Einfluss auf das Ergebnis des Röntgen-Thorax Klinischer Verdacht Kein Verdacht (Kollektive 2+4) (Kollektive 1+3) Keine Pneumonie 18 59 Fragliche Pneumonie 14 7 Pneumonie 5 5 Tab. 4: Klinischer Verdacht auf Pneumonie vs. kein Verdacht: Einfluss auf das Ergebnis des Röntgen-Thorax - 20 2. Ist die Mortalität der Gruppen (Enddiagnose) Pneumonie, fragliche Pneumonie und keine Pneumonie signifikant unterschiedlich? Ergebnis: Nein, p = 0,41 80 Anzahl Patienten 70 60 50 lebt 40 tot 30 20 10 0 Pneumonie Fragliche Pneumonie Andere Abb. 3: Mortalität in Abhängigkeit von der abschließenden Diagnose Pneumonie Fragliche Pneumonie Andere lebt 12 9 78 tot 4 3 13 Tab. 5: Mortalität in Abhängigkeit von der abschließenden Diagnose - 21 3. Wurde die Antibiose beim Röntgen-Thorax-Befund Pneumonie häufiger geändert als bei einer nicht-diagnostizierten Pneumonie? Ergebnis: Ja, p = 0,0003 70 Anzahl Patienten 60 50 40 Änderung Keine Änderung 30 20 10 0 Pneumonie Fragliche Pneumonie Andere Abb. 4: Geänderte Antibiose aufgrund des Röntgen-Thorax-Ergebnisses Pneumonie Fragliche Pneumonie Andere Änderung 5 8 7 Keine Änderung 5 13 70 Tab. 6: Änderung der Antibiose aufgrund des Röntgen-Thorax-Ergebnisses - 22 - 4. Ergebnisse 4.1 Screening und Studieneinschluss Von 590 gescreenten Patienten (d. h. nach Stichwortsuche in der Arztbriefdatenbank als mögliche Studienpatienten gefunden) wurden insgesamt 471 aus der Analyse ausgeschlossen. Die Ausschlusskriterien mit der jeweiligen Patientenanzahl dieser Studie stellt folgende Tabelle dar: Ausschlusskriterium Anzahl (n = 471) Keine Tumorerkrankung 3 Pleuraerguss 38 Pneumonie vor weniger als acht Wochen 25 Dauerchemotherapie 18 letzte Chemotherapie vor mehr als 28 Tagen 64 kein Zustand nach Chemotherapie 292 Lungenmetastasen 3 keine eindeutigen Hinweise auf Infekt 25 Radiochemotherapie 3 Tab. 7: Anzahl der jeweiligen Ausschlusskriterien 4.2 Darstellung der Studienpatienten Der Stellenwert, den die konventionelle Röntgen-Thorax-Aufnahme bei Infektionen nach einer Chemotherapie während oder nach der Neutropenie hat, konnte bei 119 Einschlusspatienten untersucht werden. Von diesen waren 80 Patienten männlich (Anteil: 67,2 %) und 39 Patienten weiblich (Anteil: 32,8 %). 98 % dieser Patienten kamen in die Notaufnahme, 2 % wurden ambulant behandelt oder kamen direkt auf Station des Universitätsklinikums Regensburg. Altersstruktur: Das Durchschnittsalter der in der Studie ausgewerteten Patienten lag im Jahr 2005 bei 54 Jahren, in den Jahren 2006 und 2007 bei 56 Jahren. Daraus ergab sich für den ausgewählten Zeitraum von zwei Jahren und zwei Monaten ein Durchschnittsalter der behandelten Patienten von 55 Jahren. Die Altersspanne reichte dabei von 17 bis 87 Jahren. - 23 - 4.3 Verteilung der Einschlusspatienten auf vier verschiedene Kollektive Folgende Tabelle zeigt die Verteilung der 119 Studienpatienten in einer Übersicht: Kollektiv 1 Kollektiv 2 Kollektiv 3 Kollektiv 4 Anzahl (n) 51 30 30 8 Anteil (%) 42,9 25,2 25,2 6,7 Tab. 8: Verteilung der Einschlusspatienten; Anzahl und Anteil der Kollektive 1-4 4.4 Grunderkrankungen Die Einschlusspatienten, die nach Chemotherapie wegen Fiebers oder V.a. einen Infekt im Universitätsklinikum Regensburg behandelt wurden, zeigten folgende maligne Erkrankungen auf: Maligne Erkrankung Anzahl (n = 119) Anteil (%) ALL 4 3,4 AML 4 3,4 CLL 5 4,2 NHL 41 34,4 (*) M. Hodgkin 3 2,5 Plasmozytom 16 13,4 Sarkom 10 8,4 andere 36 30,3 Tab. 9: Verteilung der Grunderkrankungen bei Patienten mit Infektionen nach Chemotherapie und Niedrigrisiko-Neutropenie (*) Modifiziert im Rahmen der Rundungsgenauigkeit zu gesamt 100 % - 24 - 4.5 Chemotherapien und Therapielinien Die folgenden Chemotherapie-Schemata kamen bei den Studienpatienten am häufigsten zum Einsatz: Diverse Chemotherapieschemata, wie z. B. BEACOPP (Cyclophosphamid, Etopsid, Adriamycin, Procarbazin, Vincristin, Bleomycin, Prednisolon), FOLFIRI (Folinsäure, Fluorouracil, Irinotecan), R-GEMOX (Gemcitabine, Oxaliplatin) etc. machten mit 64,7 % den größten Anteil aus. Das R-CHOP-Schema (Rituximab, Cyclophosphamid, Doxorubicin, Vincristin, Prednisolon) fand zu 17,7 % Verwendung und das R-DHAPSchema (Rituximab, Dexamethason, Cytarabin, Cisplatin) zu 6,7 %. Eine IEVMobilisierungschemotherapie erhielten 10,9 % der gescreenten Einschlusspatienten. Chemotherapie Anzahl (n) Anteil (%) R- CHOP 21 17,7 (*) R- DHAP 8 6,7 IEV- Mobilisierungschemotherapie 13 10,9 andere 77 64,7 Tab. 10: Bezeichnung und Anzahl der Chemotherapien (*) Modifiziert im Rahmen der Rundungsgenauigkeit zu gesamt 100 % Definition der Therapielinien: Die Einleitung einer Chemotherapie beginnt als ‚first line'-Erstlinientherapie. Sie kann mehrere Zyklen und Pausen umfassen. Spricht die Erstlinientherapie nicht an oder taucht nach erfolgreicher Therapie später ein Rezidiv auf, kommt ein Umstieg auf ein alternatives Schema, die ‚second line'-Therapie mit geänderter Wirkstoffzusammensetzung zum Tragen. In der Fortsetzung sind weitere Therapielinien möglich, mit denen der Tumor wieder und wieder zurückgeworfen werden soll. Folgende Tabelle macht die Verteilung der jeweiligen Therapielinien deutlich: Therapielinie Anzahl (n) Anteil (%) first line 76 64,0 (*) second line 21 17,6 third line 21 17,6 unbekannt 1 0,8 Tab. 11: Verteilung der Therapielinien (*) Modifiziert im Rahmen der Rundungsgenauigkeit zu gesamt 100 % - 25 - 4.6 Auswertungsparameter der vier Studienkollektive 4.6.1 Pulmonale Vorerkrankungen Für die genauere Beurteilung und Auswertung der Patientendaten dienten unter Anderem pulmonale Vorerkrankungen, wie z. B. Zustand nach Pneumonie vor mehr als acht Wochen, COPD (chronic obstructive pulmonary disease) und gut abgrenzbare Lungenmetastasen (einzelne oder viele). Folgende Tabelle zeigt die Gesamtanzahl pulmonaler Vorerkrankungen der vier Einschlusskollektive: Pulmonale Vorerkrankungen Anzahl (n) Kein Befund 87 Bekannte Pneumonie > 8 Wochen 13 COPD 0 Einzelne Lungenmetastasen 6 Viele Lungenmetastasen 1 Sonstiges 12 Tab. 12: Pulmonale Vorerkrankungen 4.6.2 Fieber Fieber, das als mögliches Symptom für einen Infekt gewertet werden muss, zeigte sich bei den Kollektiven 1-4 anhand der Fiebertage folgendermaßen: Fiebertage Anzahl (i) Anteil (p) 0 Tage 24 20,2 1 Tag 67 56,3 2 Tage 17 14,3 3 Tage 6 5,0 > 3 Tage 5 4,2 Tab. 13: Anzahl und Anteil der Fiebertage der Kollektive 1-4 Anmerkung: n = 119 (Gesamtanzahl der Einschlusspatienten); p = i*100/n; Angaben in % - 26 - 4.6.3 Infektsymptome 4.6.3.1 Respiratorische Symptome Während bei den Kollektiven 1+3 definitionsgemäß keine pneumonietypischen Hinweise auf Atemwegserkrankungen vorlagen (3.1.5), zeigten diese Patienten demzufolge keine respiratorischen Symptome. Dagegen traten bei den Kollektiven 2+4, den Patienten mit Atemwegserkrankungen bzw. Pneumonie (3.1.5), folgende respiratorischen Symptome auf: Husten Schmerzen beim Atmen Pleurareiben Rasselgeräusche über der Lunge Kollektiv 2 Kollektiv 4 Kollektive 2+4 (n = 30) (n = 8) (n = 38) 23 3 26 3 5 8 0 0 0 16 6 22 Tab. 14: Aufschlüsselung und Anzahl respiratorischer Symptome Anmerkung: Einzelne Patienten zeigten teilweise mehrere Symptome 4.6.3.2 Nicht-respiratorische Symptome Nicht-respiratorische Symptome wie Mukositis, Diarrhoe, gastrointestinaler Infektverdacht stellten sich innerhalb der Kollektive folgendermaßen dar: Kollektive 1+3 Kollektive 2+4 (n = 81) (n = 38) Auftreten nicht-respiratorischer 35 5 Symptome 43,2 % 13,2 % Tab. 15: Anzahl und Anteil nicht-respiratorischer Symptome Kollektiv 1 Kollektiv 2 Kollektiv 3 Kollektiv 4 (n = 51) (n = 30) (n = 30) (n = 8) Mukositis 7 0 2 0 Diarrhoe 13 3 12 1 Bauchschmerzen 7 2 6 0 Tab. 16: Aufschlüsselung und Anzahl nicht-respiratorischer Symptome Anmerkung: Einzelne Patienten zeigten teilweise mehrere Symptome - 27 - 4.6.3.3 Nicht Pneumonie-spezifische, respiratorische Symptome Solche Symptome waren Halsschmerzen, Halsrötung, Schluckbeschwerden und Dyspnoe. Die jeweilige Anzahl und Verteilung auf die Gesamtpatientenzahl der jeweiligen Kollektive veranschaulichen die Tabellen 17 und 18. Auftreten fraglich-respiratorischer Symptome Kollektive 1+3 Kollektive 2+4 (n = 81) (n = 38) 30 20 37,0 % 52,6 % Tab. 17: Anzahl fraglich-respiratorischer Symptome Kollektiv 1 Kollektiv 2 Kollektiv 3 Kollektiv 4 (n = 51) (n = 30) (n = 30) (n = 8) Halsschmerzen, -rötung 13 8 2 0 Schluckbeschwerden 9 2 1 0 Dyspnoe 6 7 5 5 Tab. 18: Aufschlüsselung und Anzahl fraglich-respiratorischer Symptome Anmerkung: Einzelne Patienten zeigten teilweise mehrere Symptome - 28 - 4.6.3.4 Technische Befunde für die weitere Abklärung einer Pneumonie Zur weiterführenden Abklärung einer Pneumonie dienten (neben dem Röntgen, s.u.) zusätzlich positive Befunde aus Blutkultur, bronchoalveolärer Lavage und die Diagnose einer infektiösen Aspergillose mit Hilfe von Serumuntersuchungen. Folgende Tabellen (Tab. 19, 20) zeigen die jeweilige Anzahl bzw. den Anteil der Befunde: Kollektive 1+3 Kollektive 2+4 (n = 81) (n = 38) Positive Blutkultur 12 3 Positiver Befund aus BAL (bronchoalveoläre Lavage) 0 1 Positives Aspergillus-Antigen im Serum 0 2 Kollektive 1-4 Kollektive 1-4 Anzahl (i) Anteil (p) Positive Blutkultur 15 12,6 Positiver Befund aus BAL (bronchoalveoläre Lavage) 1 0,8 Positives Aspergillus-Antigen im Serum 2 1,7 Untersuchung Tab. 19: Anzahl pneumonietypischer, technischer Befunde Untersuchung Tab. 20: Anzahl (i) und Anteil (p) pneumonietypischer, technischer Befunde der Kollektive 1-4 Anmerkung: n= 119 (Gesamtanzahl der Einschlusspatienten); p = i*100/n; Angaben in % Des Weiteren wurden Urin-, Stuhl- und PCR-Untersuchungen durchgeführt, die bei positivem Befund auf einen anderen möglichen Infekt (z. B. Harnwegsinfekt, Virusinfekt) hinweisen. Kollektive 1+3 Kollektive 2+4 (n = 81) (n = 38) 5 5 Positives Clostridium Toxin A im Stuhl 5 1 Positive Noro-Virus-RNA (PCR) im Stuhl 1 1 Untersuchung Positiver Uricult 1 Tab. 21: Anzahl weiterer technischer Befunde 1 Nachgewiesene Bakterienspezies: Pseudomonas aeroginosa Citrobacter freundii E-coli Klebsiellen - 29 - 4.7 Auswertung der Röntgen-Thorax-Untersuchungen Um die Bedeutung des Stellenwertes, den die konventionelle Röntgen-ThoraxAufnahme in der Diagnostik von Infektionen bzw. Pneumonien nach einer Chemotherapie und Niedrigrisiko-Neutropenie hat, feststellen zu können, standen für die Auswertung der 119 Studienpatienten insgesamt 108 bzw. 90,8 % Röntgen-Thorax-Aufnahmen zur Verfügung. Die jeweilige Anzahl bzw. den prozentualen Anteil an Röntgenaufnahmen bei den vier Kollektiven zeigen Tabellen 22 und 23: Kollektive 1+3: Kollektiv 1 Kollektiv 3 Kollektive 1+3 n = 51 n = 30 n = 81 Anzahl (i) 46 25 71 Anteil (p) 90,2 83, 3 87,7 Tab. 22: Anzahl (i) und Anteil (p) der Röntgen-Thorax-Aufnahmen bei den Kollektiven 1+3 Anmerkung: n = Patientenanzahl; p = i*100/n; Angaben in % Kollektive 2+4: Kollektiv 2 Kollektiv 4 Kollektive 2+4 n = 30 n=8 n = 38 Anzahl (i) 29 8 37 Anteil (p) 96,7 100 97,4 Tab. 23: Anzahl und Anteil der Röntgen-Thorax-Aufnahmen bei den Kollektiven 2+4 Anmerkung: n = Patientenanzahl; p = i*100/n; Angaben in % - 30 Die jeweiligen Röntgenaufnahmen wurden anschließend auf eine mögliche Pneumonie hin untersucht und die folgenden Befunde ausgewertet: Röntgen-Thorax-Untersuchungen Kollektiv 1: Kollektiv 3: Kollektive 1+3: n = 46 n = 25 n = 71 Anzahl (i) 39 20 59 Anteil (p) 84,8 80,0 83,1 Anzahl (i) 3 5 8 Anteil (p) 6,5 20,0 11,3 Anzahl (i) 36 15 51 Anteil (p) 78,3 60,0 71,8 Anzahl (i) 4 3 7 Anteil (p) 8,7 12,0 9,9 Anzahl (i) 3 2 5 Anteil (p) 6,5 8,0 7,0 ohne Pneumonie jedoch mit anderem spezifischen Befund2 mit unauffälligem Befund Röntgen-Thorax-Untersuchungen mit fraglicher Pneumonie Röntgen-Thorax-Untersuchungen mit Befund Pneumonie Tab. 24: Anzahl (i) und Anteil (p) der Befunde aus den Röntgen-Thorax-Untersuchungen der Kollektive 1+3 Anmerkung: n = Anzahl Röntgen-Thorax-Untersuchungen, p = i*100/n; Angaben in % 2 Spezifische Befunde: Dislokation Portkatheter Diskrete Pleuraergüsse Pneumothorax Stauung, Emphysem - 31 - Röntgen-Thorax-Untersuchungen Kollektiv 2: Kollektiv 4: Kollektive 2+4: n = 29 n=8 n = 37 Anzahl (i) 15 3 18 Anteil (p) 51,7 37,5 48,7 (*) Anzahl (i) 5 1 6 Anteil (p) 17,2 12,5 16,2 Anzahl (i) 10 2 12 Anteil (p) 34,5 25,0 32,4 Anzahl (i) 10 4 14 Anteil (p) 34,5 50,0 37,8 Anzahl (i) 4 1 5 Anteil (p) 13,8 12,5 13,5 ohne Pneumonie jedoch mit anderem spezifischen Befund3 mit unauffälligem Befund Röntgen-Thorax-Untersuchungen mit fraglicher Pneumonie Röntgen-Thorax-Untersuchungen mit Befund Pneumonie Tab. 25: Anzahl (i) und Anteil (p) der Befunde aus den Röntgen-Thorax-Untersuchungen der Kollektive 2+4 Anmerkung: n = Anzahl Röntgen-Thorax-Untersuchungen; p = i*100/n; Angaben in % (*) Modifiziert im Rahmen der Rundungsgenauigkeit zu gesamt 100 % 3 Spezifische Befunde: Narbig-fibrotische Veränderungen, betontes Pulmonalissegment Multiples kleinfleckiges Infiltrat in beiden Lungen, am ehesten disseminierte Metastasen Rundherd mit Pleurafinger im Lungenapex Interstitielle Zeichnungsvermehrung, Rückbildung der diffusen fleckigen Infiltrate mit residuellen Befunden V.a. TBC, Pilzpneumonie, Abszess - 32 - Vergleich der Röntgen-Thorax-Befunde zwischen den Kollektiven 1+3 und den Kollektiven 2+4 In Zusammenschau der beiden Tabellen (Tab. 24, 25) wird deutlich, dass sich bei Patienten mit klinischem Hinweis auf Atemwegserkrankungen (Kollektive 2+4) ein Verdacht auf Pneumonie (37,8 % ↔ 9,9 %) bzw. eine gesicherte Pneumonie (13,5 % ↔ 7,0 %) bereits im Röntgen-Thorax deutlich häufiger diagnostizieren ließ als bei Patienten ohne Atemwegserkrankungen (Kollektive 1+3). Außerdem erbrachte die statistische Prüfung im CHI-QUADRAT-TEST mit p = 0,0006 einen sehr signifikanten Einfluss auf das Röntgen-Ergebnis bei klinischem Verdacht auf Pneumonie (3.2.3). - 33 - 4.8 Auswertung der CT-Thorax-Untersuchungen Zur weiteren diagnostischen Abklärung des Röntgen-Thorax dienten CT-Thorax-Untersuchungen, die innerhalb von drei Tagen durchgeführt wurden. Kollektive 1+3: Kollektiv 1 Kollektiv 3 Kollektive 1+3 n = 51 n = 30 n = 81 Anzahl (i) 6 4 10 Anteil (p) 11,8 13, 3 12,3 Tab. 26: Anzahl (i) und Anteil (p) der CT-Thorax-Untersuchungen bei den Kollektiven 1+3 Anmerkung: n = Patientenanzahl; p = i*100/n; Angaben in % Kollektive 2+4: Kollektiv 2 Kollektiv 4 Kollektive 2+4 n = 30 n=8 n = 38 Anzahl (i) 3 2 5 Anteil (p) 10,0 25,0 13,2 Tab. 27: Anzahl und Anteil der CT-Thorax-Untersuchungen bei den Kollektiven 2+4 Anmerkung: n = Patientenanzahl; p = i*100/n; Angaben in % Vergleich der Anzahl der CT-Thorax-Untersuchungen bei verschiedenen RöntgenThorax-Befunden zwischen den Kollektiven 1+3 und den Kollektiven 2+4 CT-Thorax-Untersuchungen Kollektive 1+3 Kollektive 2+4 Röntgen-Thorax ohne Pneumonie 9 2 1 2 0 1 n = 77 Röntgen-Thorax mit fraglicher Pneumonie n = 21 Röntgen-Thorax mit Pneumonie n = 10 Tab. 28: Anzahl der CT-Thorax-Untersuchungen bei verschiedenen Röntgen-Thorax-Befunden der Kollektive 1+3 und der Kollektive 2+4 - 34 - Auswertungen der CT-Thorax-Untersuchungen in Übersicht: Röntgen-Thorax ohne Röntgen-Thorax mit Röntgen-Thorax mit Pneumonie: fraglicher Pneumonie: gesicherter Pneumonie: 77 21 10 30mal CT-Thorax- CT-Thorax- CT-Thorax- Untersuchungen: 11 Untersuchungen: 3 Untersuchungen: 1 Pneumonie: Pneumonie: Pneumonie: 1 2 1 Tab. 29: Gesamtergebnisse der CT-Thorax-Untersuchungen zur weiteren diagnostischen Abklärung des Röntgen- Thorax Insgesamt wurden bei 119 Einschlusspatienten 15 CT-Thorax-Untersuchungen durchgeführt. Dies entspricht einem prozentualen Anteil von 12,6%. Im Detail wurde bei Kollektiv 1 von sechs CT-Thorax-Untersuchungen zweimal eine Pneumonie nachgewiesen und der zeitliche Abstand zur Röntgen-Thorax-Untersuchung betrug einen Tag. Bei Kollektiv 2 kam von drei Untersuchungen zweimal eine Pneumonie zum Vorschein und der zeitliche Abstand zur Röntgen-Thoraxaufnahme betrug im Durchschnitt einen Tag. Sowohl bei Kollektiv 3 mit vier CT-Thorax-Untersuchungen als auch bei Kollektiv 4 mit zwei CT-Thorax-Untersuchungen konnte bei keiner CTThorax-Aufnahme eine Pneumonie nachgewiesen werden. Eine Pneumonie war schließlich bei insgesamt 15 CT-Thorax-Untersuchungen viermal nachweisbar (26,7%). - 35 - 4.9 Therapieumstellung aufgrund positiver Befunde in der RöntgenThorax-Untersuchung Ergänzend wurde untersucht, ob positive oder verdächtige Befunde im Röntgen zu einer Änderung der Therapiestrategie führten. Hierzu zählten insbesondere die Gabe Aspergillus-Pneumonie-wirksamer Antibiotika oder Antimykotika, die typischerweise zur Abdeckung atypischer Erreger bei Pneumonie verwendet werden (Erythromycin, Clarithromycin, Voriconazol) oder ob aufgrund eines Pneumonieverdachts weitere Maßnahmen (z. B. Bronchiallavage) durchgeführt wurden. RöntgenRöntgen- Thorax- Thorax- Röntgen- Befund ohne Befund mit Thorax-Befund Pneumonie fraglicher mit Pneumonie (anderer Pneumonie spezieller Befund) Patientenanzahl (n) Medikation (i) RöntgenThoraxBefund ohne Pneumonie (unauffälliger Befund) Kollektive Kollektive Kollektive Kollektive 1+3: 1+3: 1+3: 1+3: n=7 n=5 n=8 n = 51 2 (V-Fend) 0 0 5 (V-Fend) 0 0 Antimykotika (nicht Fluconazol, aber z. B. Voriconazol (V-Fend) Erweiterung der antibiotischen Therapie (z. B. Erythromycin, 1 (Klacid) 1 (Erythromycin) 2 (Klacid) Clarithromycin (Klacid) etc.) Bronchoalveoläre Lavage (BAL) Gesamtanteil der Therapieänderungen (p) 0 0 0 0 42,9 60 0 9,8 Tab. 30: Anzahl (n) und Gesamtanteil (%) der Therapieänderungen, mit jeweiliger Medikation, aufgrund positiver Befunde im Röntgen-Thorax bei den Kollektiven 1+3 Anmerkung: n = Patientenanzahl; i = Anzahl der jeweiligen Medikation bei Therapieänderung; p = i*100/n, wobei (i) = gesamte Anzahl der Medikationen bei verschiedenen Röntgenbefunden - 36 - RöntgenRöntgenThorax-Befund mit fraglicher Pneumonie Thorax-Befund Röntgen- ohne Thorax-Befund Pneumonie mit Pneumonie (anderer spezieller Befund) Patientenanzahl (n) Medikation (i) RöntgenThorax-Befund ohne Pneumonie (unauffälliger Befund) Kollektive 2+4: Kollektive 2+4: Kollektive 2+4: Kollektive 2+4: n = 14 n=5 n=6 n = 12 4 (V-Fend) 1 0 1 (V-Fend) 1 (Klacid) 1 (Klacid) 0 1 (Klacid) 0 0 0 0 35,7 40 0 16,7 Antimykotika (nicht Fluconazol, aber z. B. Voriconazol (V-Fend) Erweiterung der antibiotischen Therapie (z. B. Erythromycin, Clarithromycin (Klacid) etc.) Bronchoalveoläre Lavage (BAL) Gesamtanteil der Therapieänderungen (p) Tab. 31: Anzahl (n) und Gesamtanteil (%) der Therapieänderungen, mit jeweiliger Medikation, aufgrund positiver Befunde im Röntgen-Thorax bei den Kollektiven 2+4 Anmerkung: n = Patientenanzahl; i = Anzahl der jeweiligen Medikation bei Therapieänderung; p = i*100/n, wobei (i) = gesamte Anzahl der Medikationen bei verschiedenen Röntgenbefunden Vergleicht man beide Tabellen (Tab. 30, 31), ist bei einem Verdacht auf Pneumonie bzw. einer gesicherten Pneumonie im Röntgen-Thorax mit insgesamt 41,9 % ein beachtlicher Anteil an Therapieänderungen (13 von 31 Patienten) festzustellen. Auch die statistische Prüfung im CHI-QUADRAT-TEST erbrachte mit p = 0,0003 eine sehr signifikante Änderung der Antibiose, wenn im Röntgen-Thorax eine Pneumonie diagnostiziert wurde (3.2.3). - 37 - 4.10 Behandlungsdauer Die folgende Tabelle zeigt in Übersicht den jeweiligen stationären Aufenthalt bei unterschiedlichen Röntgen-Thorax-Befunden. Stationärer Aufenthalt Röntgen-Thorax-Befund mit Pneumonie Röntgen-Thorax-Befund mit fraglicher Pneumonie Röntgen-Thorax-Befund ohne Pneumonie Kollektive 1+3 Kollektive 2+4 alle 14,4 Tage 7,2 Tage 10,8 Tage 14,1 Tage 15,7 Tage 14,9 Tage 11,4 Tage 10,6 Tage 11,0 Tage Tab. 32: Behandlungsdauer Pneumonie vs. keine Pneumonie - 38 - 4.11 Abschließende Beurteilungen für das Indexereignis Folgende Enddiagnosen wurden unter Einbezug aller durchgeführten Untersuchungen letztendlich für die vier stratifizierten Kollektive ersichtlich (Anhang 2, S. 67 ff): Fragliche Pneumonie Nichtpulmonaler Infekt Fieber, V.a. Infekt ohne Organfokus Sonstiges4 Anteil (%) Pneumonie gesichert Kollektiv 1 5 2 19 24 1 (n = 51) (9,8 %) (3,9 %) (37,3 %) (47,1 %) (1,9 %) (*) Kollektiv 2 6 7 7 9 1 (n = 30) (20,0 %) (23, 3 %) (23, 3 %) (30,0 %) (3, 3 %) Kollektiv 3 2 1 13 13 1 (n = 30) (6,7 %) (3, 3 %) (43, 3 %) (43, 3 %) (3, 3 %) Kollektiv 4 3 2 1 1 1 (n = 8) (37,5 %) (25,0 %) (12,5 %) (12,5 %) (12,5 %) Kollektive 1-4 16 12 40 47 4 (n = 119) (13,4 %) (10,1 %) (33,6 %) (39,5 %) (3,4 %) Anzahl (n) Tab. 33: Anzahl (n) und Anteil (%) der abschließenden Diagnosen (*) Modifiziert im Rahmen der Rundungsgenauigkeit zu gesamt 100 % 4 Sonstiges: 274: Chemoinduzierte Enteritis 300: Progredientes Lymphom 385: Transfusionspflichtige Anämie bei Fieber in der Neutropenie ohne V.a. Infekt 478: Progrediente pulmonale Metastasierung - 39 - Zusammenfassung der Enddiagnosen in Gegenüberstellung der Kollektive 1+3 und Kollektive 2+4: 50 45 40 35 30 25 Koll. 1+3 20 Koll. 2+4 15 10 5 0 Pneum onie gesichert Fragliche NichtFieber, V.a. Pneum onie pulm onaler Infekt ohne Infekt Organfokus Sonstiges Abb. 5: Prozentualer Anteil der Enddiagnosen der Kollektive 1+3 sowie der Kollektive 2+4; %-Angaben bezogen auf die Gesamtanzahl der Patienten der jeweiligen Kollektive Bei der Analyse des Säulendiagramms (Abb. 5) ist ein deutlicher Unterschied zwischen den Kollektiven erkennbar. Während sich bei Patienten mit Atemwegserkrankungen (Kollektive 2+4) eine fragliche Pneumonie bzw. eine gesicherte Pneumonie deutlich häufiger diagnostizieren ließ als bei Patienten ohne Atemwegserkrankungen (Kollektive 1+3), verhielt es sich bei den Diagnosen eines nicht-pulmonalen Infektes bzw. bei Fieber, V.a. Infekt ohne Organfokus bei den beiden Kollektivgruppen mehr oder minder umgekehrt. - 40 - 4.12 Korrelation der abschließenden Diagnosen mit den RöntgenThorax-Ergebnissen Von den 119 Studienpatienten wurden 108 Patienten mit Hilfe einer Röntgen-ThoraxAufnahme untersucht. Dies entspricht einem Anteil an Röntgen-Thorax-Aufnahmen von 90,8 %. Tabelle 34 zeigt die Korrelation der abschließenden Diagnosen mit den dazugehörigen Röntgen-Ergebnissen. Beurteilungs- Pneumonie Fragliche Nicht- Fieber, V.a. Pneumonie pulmonaler Infekt ohne Infekt Organfokus n = 40 n = 47 Ergebnis n = 34 (Rönt- n = 42 (Rönt- Anzahl (i) gen-Thorax- gen-Thorax- Anteil (p) Aufnahmen) Aufnahmen) index Anzahl Rö- (n) RöntgenThoraxBefund ohne Pneumonie n = 16 n = 12 Sonstiges5 n=4 2 0 26 34 1 12,5 0 76,5 80,9 (*) 25,0 0 0 5 6 3 0 0 14,7 14,3 75,0 4 12 3 2 0 25,0 100 8,8 4,8 0 10 0 0 0 0 62,5 0 0 0 0 RöntgenThoraxBefund ohne Pneumonie (anderer spezieller Befund) RöntgenThoraxBefund mit fraglicher Pneumonie RöntgenThoraxBefund mit Pneumonie Tab. 34: Anzahl (i) und Anteil (p) der Röntgen-Thorax-Ergebnisse in Korrelation zum Indexereignis Anmerkung: n = Patientenanzahl; p = i*100/n; Angaben in %. (*) Modifiziert zu gesamt 100 % 5 Sonstiges: Progrediente pulmonale Metastasierung Chemoinduzierte Enteritis - 41 - 4.13 Überlebenswahrscheinlichkeit und Mortalitätsrate 4.13.1 Überlebenswahrscheinlichkeit Überle- Kollektiv 1 Kollektiv 2 Kollektiv 3 Kollektiv 4 Kollektive benszeit 4 n = 51 n = 30 n = 30 n=8 1-4 Wochen n = 119 Anzahl (i) 48 25 22 4 99 Anteil (p) 94,1 83, 3 73, 3 50 83,2 Anzahl (i) 3 5 8 4 20 Anteil (p) 5,9 16,7 26,7 50 16,8 ja nein Tab. 35: Überlebenszeit von vier Wochen der Kollektive 1-4 Anmerkung: p = i*100/n; Angaben in % 4.13.2 Mortalitätsrate Für die Enddiagnosen, die sich letztlich für das Indexdatum ergaben, zeigten sich im Zeitraum von vier Wochen folgende Mortalitätsraten: Diagnosen Mortalitätsrate Mortalitätsrate (Anzahl n) (Anzahl i) (Anteil p) Gesicherte Pneumonie 16 4 25,0 Fragliche Pneumonie 12 3 25,0 40 4 10,0 47 7 14,9 Sonstiges 4 2 50,0 Gesamtanteil 119 20 16,8 Diagnosen Nicht-pulmonaler Infekt Fieber, V.a. Infekt ohne Organfokus Tab. 36: Sterblichkeit bei verschiedenen Diagnosen Anmerkung: p = i*100/n; Angaben in % Die statistische Prüfung im CHI-QUADRAT-TEST erbrachte mit p = 0,41 keinen signifikanten Unterschied in der Mortalität der Gruppen mit den Enddiagnosen: Pneumonie, fragliche Pneumonie und keine Pneumonie (3.2.3). - 42 - 5. Diskussion 5.1 Infektionen nach Chemotherapie und Niedrigrisiko-Neutropenie Eines der größten Probleme bei onkologischen Patienten stellt die durch Chemotherapie bedingte Morbidität und die damit verbundene Letalität durch Infektionen dar. Von entscheidender Bedeutung hierbei ist es, den Zusammenhang zwischen dem Risiko infektionsbedingter Morbidität und Letalität im Verhältnis zu der Gesamtdauer der Neutropenie zu beurteilen. Dabei wird ein Patient mit einer erwarteten NeutropenieDauer (< 500 Granulozyten/µl) von ≤ 5 Tagen in der Regel als Niedrigrisikopatient, ein Patient mit einer Neutropenie-Dauer von 6 - 9 Tagen als Standardrisikopatient und ein Patient mit einer Neutropenie-Dauer ≥ 10 Tagen als Hochrisikopatient eingestuft (28, 39, 42). In der vorliegenden Studie wurden von Januar 2005 bis Februar 2007 119 NiedrigrisikoPatienten mit einem Durchschnittsalter von 55 Jahren eingeschlossen, die aufgrund einer malignen Erkrankung und dem Zustand nach einer Chemotherapie (mit Fieber in / nach der Neutropenie, mit / ohne Hinweise auf Atemwegserkrankungen) das Universitätsklinikum Regensburg aufsuchten. Diese Patienten haben, wie bereits eine Reihe von Untersuchungen zeigte, ein hohes Infektionsrisiko (13, 26, 38). In der Infektionsdiagnostik kommt der Beurteilung von Fieber ein hoher Stellenwert zu. Da bei neutropenen Patienten Fieber oft das einzige Zeichen einer Infektion ist, muss bedacht werden, dass Fieber keineswegs ausschließlich infektionsbedingt ist, sondern auch andere klinische Hinweise einen Infektionsverdacht begründen können. Wie die genaue Analyse der Auswertungen zeigt, war Fieber, neben den genannten klinischen Infektzeichen, eines der möglichen Hinweise für einen Infekt, jedoch hatten die Patienten dieses meist nicht länger als einen Tag, bevor sie die Klinik aufsuchten. Im Detail hatten von den 119 Studienpatienten 24 Patienten kein Fieber, bei 67 Patienten bestand Fieber seit einem Tag, bei 17 Patienten seit zwei Tagen, bei sechs Patienten seit drei Tagen und bei fünf Patienten seit mehr als drei Tagen. Somit kann Fieber als alleiniges Infektzeichen nicht als aussagekräftig bewertet werden, da es auch nachgewiesenermaßen einen beachtlichen Anteil an Patienten gab, die sich ohne Fieber (n = 24; 20,2 %), jedoch mit anderen klinischen Infektzeichen (Husten, Schmerzen beim Atmen, Pleurareiben, Rasselgeräusche über der Lunge), in der Klinik vorstellten. Rieger et al. (51) untersuchten Fieber unklarer Genese und kamen zu folgendem Schluss: Auch wenn Fieber bei Tumorpatienten ein häufiges Infektsymptom ist, ist dessen genaue Zuordnung oft nicht möglich (= FUO). So bestehen febrile Temperaturen - 43 nicht nur bei sogenanntem „Tumorfieber“, sondern auch nach zytoreduktiver Chemotherapie, bei der dem Fieber teils schwere Infektionen durch chemoinduzierte Neutropenie zugrunde liegen. Um das Mortalitätsrisiko zu senken, sind eine umgehende Diagnostik und antibiotische Therapie daher stets angezeigt. Ziel dieser Arbeit war es, den Stellenwert, den die konventionelle Röntgen-ThoraxAufnahme in der Diagnostik von Infektionen bei ambulanten Patienten nach einer Chemotherapie und einer Niedrigrisiko-Neutropenie hat, zu untersuchen. Hierbei interessierten die Fragen, wie hoch der prozentuale Anteil an Röntgen-Thorax-Aufnahmen insgesamt war, wie häufig durch diese Untersuchungsmethode eine Infektion (Pneumonie oder deren Verdacht) aufgezeigt bzw. bestätigt werden konnte, welche Therapieänderungen bei positiven Röntgenbefunden vorgenommen wurden und welche Unterschiede es bezüglich der Behandlungsdauer bei Pneumonie-Patienten im Gegensatz zu Patienten ohne Pneumonie gab. - 44 - 5.2 Radiologischer Nachweis einer Infektion mit der Röntgen-ThoraxAufnahme 5.2.1 Stellenwert der konventionellen Röntgen-Thorax-Aufnahme Da bakterielle Infektionen und Pneumonien eine äußerst ungünstige Prognose haben, gilt es, diese so früh wie möglich aufzudecken, damit eine zeitnahe, effektive Behandlung und Therapie eingeleitet werden können. Im Rahmen des konventionellen Procedere bei Infektionen neutropener Patienten gehört die Röntgen-Thorax-Aufnahme meist zu den Standarduntersuchungen. Auch in der vorliegenden Studie erhielten die Patienten zu 90,8 % eine Röntgenuntersuchung des Thorax. Jedoch erscheint es fraglich, ob eine Infektion frühzeitig im RöntgenThorax erkennbar ist, da dieser bei Fieber, Neutropenie und fehlenden weiteren Symptomen häufiger unauffällig ist (Tab. 24, 25). Demzufolge war es geboten, sich mit dem Problem genauer und fundierter auseinanderzusetzen. Neben Fieber haben Atemwegserkrankungen mit respiratorischen (Husten, Schmerzen beim Atmen, Pleurareiben, Rasselgeräusche über der Lunge), nicht-respiratorischen (Mukositis, Diarrhoe, gastrointestinaler Infektverdacht) und nicht Pneumonie-spezifischen, respiratorischen Symptomen (Halsschmerzen, Halsrötung, Schluckbeschwerden und Dyspnoe) in der Infektionsdiagnostik einen hohen Stellenwert. Diesbezüglich wurden alle Studienpatienten nach folgenden Kriterien unterschieden: Fieber in (während) / nach der Neutropenie mit / ohne Atemwegserkrankungen (Kollektive 1+3, Kollektive 2+4). In der Röntgen-Thorax-Untersuchung zeigte sich schließlich, dass positive PneumonieBefunde deutlich häufiger bei Patienten mit Atemwegserkrankungen diagnostiziert werden konnten: Fragliche Pneumonie: Kollektive 1+3: 9,9 %, Kollektive 2+4: 37,8 %; Pneumonie: Kollektive 1+3: 7,0 %, Kollektive 2+4: 13,5 %. Der CHI-QUADRATTEST lieferte hierzu mit p = 0,0006 außerdem ein sehr signifikantes Ergebnis. Auch das Studium der wissenschaftlichen Literatur bestätigt diese Ergebnisse: Feusner et al. (20) zeigten in einer retrospektiven Studie über den Stellenwert des Röntgen-Thorax bei 134 Röntgenaufnahmen onkologischer Kinder mit Fieber und Neutropenie Folgendes: Acht (6 %) Röntgenaufnahmen waren positiv, vier davon (2,9 %) indizierten eine pulmonale Infektion als mögliche Fieberursache. Alle diese vier Patienten hatten bereits vorher respiratorische Symptome. Somit kamen Feusner et al. (20) zu dem Schluss, dass ein Kind mit auffälligen Atembefunden wahrscheinlich auch ein auffälliges Röntgen-Thorax-Ergebnis hat; ein Kind mit unauffälligen Untersuchungsergebnissen demzufolge auch ein unauffälliges Röntgen-Thorax-Ergebnis aufweist. - 45 Katz et al. (31) führten eine ähnliche Studie durch. Sie untersuchten bei insgesamt 131 Kindern, die wegen Fiebers und Neutropenie aufgenommen wurden, 128 Röntgenaufnahmen. Das Röntgen-Ergebnis wurde auf An- und Abwesenheit von bestehenden respiratorischen Symptomen für Pneumonie untersucht. 20 % der Röntgenaufnahmen zeigten einen auffälligen Befund, darunter 6 % gesicherte Pneumonie. D. h., bei 3 von 128 (2,3 %) der Kinder wurde eine Pneumonie im Röntgen diagnostiziert, die bei klinischer Untersuchung nicht vorhersehbar war. Mit diesem Ergebnis kamen Katz et al. (31) zu der Schlussfolgerung, dass bei Fehlen von klinischen Anzeichen für eine Pneumonie ein routinemäßiges Röntgen überflüssig ist, da die Inzidenz einer Pneumonie im Röntgen bei Kindern mit Fieber und Neutropenie gering ist. Jochelson et al. (29) überprüften in einer prospektiven Studie den Röntgen-Thorax-Befund bei 75 Patienten mit Fieber und Neutropenie, jedoch ohne Anzeichen für eine Pneumonie und kamen zu folgendem Ergebnis: Bei insgesamt 95 durchgeführten Röntgen-Thorax-Aufnahmen war die Diagnose der Pneumonie nur sechsmal (8 %) positiv (bei 4 % der Patienten oder 3 % der Röntgenbilder bestand eine Infektion). Auch in einer prospektiven Studie von Navigante et al. (47) mit 113 fiebrigen und neutropenen Patienten konnte lediglich bei 16 % der Patienten ohne respiratorische Symptome eine Pneumonie im Röntgen-Thorax diagnostiziert werden. Die zitierten Studien (20, 29, 31, 47) stimmen mit den Ergebnissen der vorliegenden Arbeit zum Großteil überein. Unterschiede bestehen allerdings zum einen in den untersuchten Kollektiven von Feusner et al. (20) und Katz et al. (31), da diese ihre Studien bei Kindern durchführten. Zum anderen handelte es sich bei Jochelson et al. (31) und Navigante et al. (47) um einen prospektiven Studientyp im Gegensatz zu der vorliegenden retrospektiven Studie. In der Zusammenschau dieser Studien und unserer Ergebnisse wird deutlich, dass die Röntgen-Thorax-Aufnahme nicht zwingend zur Beurteilung fiebriger, neutropener Patienten ohne Atemauffälligkeiten notwendig ist, da die Früherkennungsrate einer Pneumonie relativ gering ist (Kollektive 1+3: Fragliche Pneumonie im Röntgen: 9,9 %, gesicherte Pneumonie im Röntgen: 7,0 %). Der Röntgen-Thorax hat jedoch einen bedeutenderen Stellenwert bei Patienten mit Atemauffälligkeiten, da hierbei ein größerer Anteil an Pneumonien und Pneumonieverdachtsfällen aufgedeckt werden konnte (Kollektive 2+4: Fragliche Pneumonie im Röntgen: 37,8 %, gesicherte Pneumonie im Röntgen: 13,5 %). Insgesamt konnten in dieser Arbeit die Ergebnisse der oben genannten Studien bestätigt werden. Patienten mit Atemwegserkrankungen zeigten signifikant häufiger - 46 (p = 0,0006 im CHI-QUADRAT-TEST) positive Befunde im Röntgen-Thorax als Patienten ohne Atemwegserkrankungen. Somit ist die Thoraxaufnahme bei Patienten mit Atemwegserkrankungen ein wichtiger Bestandteil in der Diagnostik von Infektionen, könnte jedoch den Patienten ohne Atemwegserkrankungen aufgrund der geringen positiven Befunderhebung erspart bleiben. Im Allgemeinen weist die Röntgen-Thorax-Untersuchung deutliche Grenzen in der frühen Aufdeckung von Pneumonien auf. Da jedoch eine schnelle und genaue Diagnostik bei Infektverdacht angezeigt ist, sollten andere, sensiblere Diagnoseverfahren, wie z. B. die CT-Thorax-Untersuchung, zum Einsatz kommen. 5.2.2 CT-Thorax-Untersuchungen zur weiteren diagnostischen Abklärung des Röntgen-Thorax Die Beurteilbarkeit der Thoraxübersicht in zwei Ebenen ist durch Überlagerungen begrenzt (Heussel et al.) (23). Bei empirischem Therapieversagen oder klinischer Symptomatik einer Pneumonie befürwortet die AGIHO (15, 17, 19) daher, eine ergänzende Computertomographie als Methode der Wahl zur überlagerungsfreien Darstellung des Lungenparenchyms anzuschließen. Die DGHO (16) empfiehlt in den Leitlinien zur Behandlung febriler Neutropenie mit Lungeninfiltraten außerdem: „Bei Patienten mit Fieber unklarer Genese (FUO) oder einer dokumentierten Infektion jenseits von Lungeninfiltraten, die nicht innerhalb der ersten 72 - 96 Stunden nach Therapiebeginn auf eine antibakterielle Behandlung ansprechen, sollte innerhalb von 24 Stunden eine Computertomographie der Thoraxorgane durchgeführt werden. Bei Patienten mit pathologischen Befunden auf einer konventionellen Röntgen-Thorax-Aufnahme wird die Durchführung einer CT-Untersuchung der Thoraxorgane zur besseren Differenzierung der Infiltrate empfohlen.“ Auch Heussel et al. (23) vertreten die Auffassung, dass Pneumonien in der CT-Aufnahme früher erkannt werden und die Sensitivität sowie die Spezifität gegenüber der Thoraxübersicht signifikant höher sind. In der vorliegenden Arbeit kamen bei den Patienten mit respiratorischen Symptomen (Kollektive 2+4) CT-Thorax-Untersuchungen mit 13,2 % etwas häufiger zum Einsatz als bei Patienten ohne respiratorische Symptome (Kollektive 1+3) mit 12,3 %. Die Fokussuche lieferte hierbei folgende Ergebnisse: Bei Patienten ohne respiratorische Symptome (Kollektive 1+3) wurde beim Thoraxbefund „fragliche Pneumonie“ in einer daraufhin durchgeführten CT-Aufnahme einmal eine Pneumonie gesichert, bei den Patienten mit respiratorischen Symptomen (Kollektive 2+4) bei zwei CT-Aufnahmen einmal. Die Diagnose „gesicherte Pneumonie“ im - 47 Röntgen-Thorax zeigte sich im CT-Thorax folgendermaßen: Bei den Kollektiven 1+3 gab es nie eine zusätzliche CT-Aufnahme, während bei den Kollektiven 2+4 eine zusätzliche CT-Aufnahme zur Diagnosesicherung angefertigt wurde, in der schließlich auch die Pneumonie bestätigt werden konnte. Heussel et al. (24) beschrieben in einer prospektiven Studie mit 146 Fällen eine frühere Erkennung der Pneumonie im CT-Thorax als im Röntgen-Thorax. In 48 % (70 von 146) der Fälle war die Röntgen-Thorax-Aufnahme ohne Befund, während im CT-Thorax eine Pneumonie diagnostiziert werden konnte. Bei nur 5 % wurde bei einem unauffälligen CT-Befund sieben Tage später eine Pneumonie erkannt (p < 0,005). Außerdem stellten sie, wie auch Karthaus et al. (30), fest, dass im CT-Thorax fünf Tage früher als im Röntgen-Thorax positive Befunde dargestellt werden können. Des Weiteren zeigten sie in ihrer Studie die Aufdeckung pneumonietypischer Mikroorganismen im CT (in 30 von 70 Fällen) und kamen zu dem Ergebnis, dass 19 von diesen 30 Patienten bis zu diesem Zeitpunkt nicht optimal therapiert worden waren. Somit folgerten sie, dass bei allen Patienten mit FUO und unauffälligem Röntgen-Thorax eine CT-Aufnahme das adäquate Mittel zur Aufdeckung von Pneumonie sein sollte, um den Patienten eine rechtzeitige und effektive Therapie zu ermöglichen. Demirkazik et al. (14) bewiesen in einer retrospektiven Studie bei Patienten mit Pneumonie bei 57 CT-Untersuchungen dessen hohe Sensitivität. Sowohl Pilzinfektionen (95 %) als auch Pneumocystis carinii pneumonia (PCP) (87,5 %) wurden mit sehr hoher Wahrscheinlichkeit erkannt, bakterielle Infektionen mit 73,7 % und virale Infektionen mit 75 % dagegen etwas seltener. Selbst wenn es in dieser Arbeit nur einen sehr geringen Anteil an CT-Aufnahmen 12,6 %, im Vergleich zu 90,8 % Röntgen-Thorax-Aufnahmen gab, was sicher auch in dem geringen Stichprobenumfang von 119 Einschlusspatienten begründet liegt, sollte aufgrund der Wahrscheinlichkeit, mit einer CT-Aufnahme früher eine Pneumonie feststellen zu können als mit der konventionellen Röntgen-Thorax-Aufnahme, diese das probate Mittel in der Diagnostik fiebriger, neutropener Patienten mit Infektverdacht sein. Heussel et al. (23) vertreten zudem die Meinung, dass neben der Identifikation eines Fokus auch der Ausschluss eines Organbefalls wichtig ist. Zudem sind sie der Auffassung, dass neben der rechtzeitigen Diagnose einer Pneumonie eine Zuordnung der häufig zugrunde liegenden Erreger für Pneumonie nützlich ist, da eine mikrobiologische Identifikation unter Umständen einige Tage beansprucht. Bei sofortiger Identifikation des Fokus bestehe die Möglichkeit zur gezielten antiinfektiven Therapie. Im Rahmen der dargestellten Behandlungsmethoden müssen Verfügbarkeit, Erfahrung und Therapiekosten stets berücksichtigt werden. - 48 Schlussfolgerung: Lange Zeit gehörte die Röntgenuntersuchung des Thorax in der radiologischen Diagnostik von Infektionen zum Goldstandard bei der Aufdeckung einer Pneumonie. Aufgrund der geringen Sensitivität wurde sie vom CT-Thorax abgelöst. Da Patienten jedoch sowohl bei Röntgen-Thorax-Untersuchungen als auch bei CT-Thorax-Untersuchungen hoher Strahlenbelastung ausgesetzt sind, ist die Untersuchung mittels MRT hierbei ein neuer Ansatz. In einer Studie von Rieger et al. (50) konnte dessen Effektivität nachgewiesen werden. Pulmonale Infiltrate wurden bei neutropenen Patienten in 91,0 % der Fälle diagnostiziert. Dies kommt der Sensitivität einer CT-Untersuchung in etwa gleich. Daher bleibt zu hoffen, dass sich die MRT-Untersuchung, trotz der derzeit hohen Kosten, bei neutropenen Patienten mit Infektverdacht in den nächsten Jahren als neuer Goldstandard durchsetzen wird. - 49 - 5.3 Therapie und Therapieumstellung Grundlage dieser Arbeit sind die Leitlinien der Arbeitsgemeinschaft Infektionen der Deutschen Gesellschaft für Hämatologie und Onkologie (AGIHO) zur Diagnostik und Therapie infektiöser Komplikationen bei neutropenen Patienten (15). Da bei neutropenen Patienten Fieber oft das einzige Zeichen einer Infektion ist und nur bei 50 % aller Patienten der Keimnachweis gelingt, vertritt Link (37) die Auffassung, dass febrile Patienten innerhalb von zwei Stunden nach Auftreten des Fiebers mit Antibiotika behandelt werden müssen. In den Leitlinien der AGIHO (5, 10, 11, 15, 17, 19, 39, 41, 52) zur Diagnostik und Therapie infektiöser Komplikationen bei neutropenen Patienten wird der Beginn einer antimikrobiellen Therapie unverzüglich nach Fiebereintritt empfohlen, da durch eine Verzögerung das Risiko lebensbedrohlicher Komplikationen enorm ansteigt. Bei zu spät behandelten Infektionen, die sich zur Sepsis entwickeln, beschreibt Link (37) sogar eine Letalität von 70 - 100 %. Link und Maschmeyer (38) werten Therapieverzögerungen von mehr als zwei Stunden nach Beginn der ersten Infektsymptomatik bereits als „zu spät“. Bei Fieberzuständen muss man differenzieren, ob sie durch einen Tumor oder durch Infektionen ausgelöst werden. Da die Unterscheidung trotz intensiver Diagnostik häufig nicht gelingt, wird in der initialen Diagnostik die Verabreichung einer empirischen, antiinfektiven Therapie mit Breitspektrumantibiotika zur Abdeckung grampositiver und gramnegativer Keime empfohlen (5, 39). Diese grampositiven Erreger können ebenso wie gramnegative Auslöser für gravierende Infektionen sein, die, wenn nicht rechtzeitig therapiert wird, zu ernsthaften Komplikationen bis zum Tod des Patienten führen. Infektionen besonders ungünstiger Prognose stellen dabei systemische Pilzinfektionen (Aspergillosen) dar (8, 9). Daher empfiehlt die AGIHO (9) eine gezielte Diagnostik, da aus der Charakterisierung des Erregers entscheidende Konsequenzen für den Patienten im Hinblick auf die Wahl des Antibiotikums, die Therapiedauer, chirurgische Intervention, Kontrolluntersuchungen oder eine spätere antimykotische Prophylaxe gezogen werden können. In der vorliegenden Arbeit dienten zu deren Diagnose, neben der konventionellen Röntgenaufnahme des Thorax, zusätzlich positive Befunde aus Blutkultur (12,6 %), BAL (0,8 %) und die Diagnose einer infektiösen Aspergillose (1,7 %). Der Ausschluss anderer Infektionen (Harnwegsinfekt, Virusinfekt) fand mit Hilfe von Urin-, Stuhl- und PCRUntersuchungen statt. Nachgewiesene Bakterienspezies wurden für die weiteren Auswertungen in dieser Studie nicht berücksichtigt. - 50 Einzig und allein die Diagnose einer pneumonietypischen Infektion war das entscheidende Kriterium für die weitere Therapie. Therapieumstellung: Die Initialtherapie sollte, wie bereits erwähnt, aus einem Breitspektrumantibiotikum bestehen, wobei laut AGIHO (15) Kombinationen oder Monosubstanzen empfohlen werden. In unserer Studie wurde zudem untersucht, ob positive oder verdächtige Befunde im Röntgen-Thorax zu einer Therapieänderung führten. Bei Verdacht auf eine AspergillusPneumonie wurde die empirische Antibiose modifiziert und den Patienten Clarithromycin (Klacid) und Voriconazol (V-Fend) zur antiinfektiven Therapie verabreicht. Bei einer gesicherten Pneumonie im Röntgen erhielten diese Patienten ebenfalls eine antibiotische Therapie mit Clarithromycin und Erythromycin mit der zusätzlichen Verabreichung des Antimykotikums Voriconazol. Bei positivem oder fraglich positivem Röntgenbefund erbrachte die Auswertung der Ergebnisse eine Änderung der Therapie zu 41,9 % (13 Therapieänderungen bei 31 Patienten). Auch die statistische Prüfung im CHI-QUADRAT-TEST zeigte mit p = 0,0003 eine sehr signifikante Änderung der Antibiose. - 51 - 5.4 Behandlungsdauer und Sterblichkeit mit und ohne Pneumonie Die Beherrschung infektiöser Komplikationen ist ein essentieller Bestandteil der Behandlung maligner Erkrankungen. Durch optimale Prophylaxe, Diagnostik und antimikrobielle Therapie kann heute, so Maschmeyer et al. (42), die Rate infektionsbedingter Letalität bis auf ≤ 10 % gesenkt werden. Dabei ist es jedoch von enormer Bedeutung, dass Infektionen bzw. die Risikofaktoren für Fieber und Neutropenie rechtzeitig erkannt werden, um eine gezielte Therapie einleiten oder ändern zu können. Behandlungsdauer: Die Behandlungsdauer der Patienten wurde im Zusammenhang mit den RöntgenThorax-Befunden untersucht. Im Fall einer Pneumonie im Röntgen lag der Krankenhausaufenthalt bei 10,8 Tagen, im Fall einer fraglichen Pneumonie im Röntgen bei 14,9 Tagen und, wenn keine Pneumonie diagnostiziert wurde, bei 11,0 Tagen. Somit gab es keinen bedeutenden Unterschied hinsichtlich der Behandlungsdauer, ob der Patient eine Pneumonie im Röntgen hatte oder nicht. Mortalität: Betrachtet man nun die tatsächliche Mortalitätsrate der Patienten, so zählen zu den größten Risikofaktoren für Mortalität laut Kuderer et al. (34) neben der Tumorerkrankung selbst invasive Pilzinfektionen, gramnegative Sepsis und die Pneumonie. Lal et al. (35) zeigten in einer Studie mit 80 febrilen, neutropenen Patienten eine Mortalitätsrate von 11 % auf. Dabei waren Pneumonie oder septischer Schock die Haupttodesursachen. In einer Studie von Lima et al. (36) mit 116 febrilen, neutropenen Patienten lag die durchschnittliche Mortalitätsrate bei 21,6 %. Dabei hatten Niedrigrisikopatienten eine Sterblichkeit von 16,2 % und Hochrisikopatienten von 39,1 %. Die Haupttodesursache hierfür war Sepsis. In der vorliegenden Arbeit erbrachte die statistische Prüfung im CHI-QUADRAT-TEST bei den Enddiagnosen: Pneumonie, fragliche Pneumonie und keine Pneumonie mit p = 0,41 keinen signifikanten Unterschied in der Mortalitätsrate. Diese lag sowohl bei gesicherter als auch bei fraglicher Pneumonie bei jeweils 25,0 % und war die Haupttodesursache. Bei nicht-pulmonalen Infekten lag die Sterblichkeit bei 10,0 %, bei Fieber und Verdacht auf Infekt ohne Organfokus bei 14,9 %. Insgesamt war die Mortalitätsrate mit 16,8 % relativ gering, was dem Ergebnis von Lal et al. (35) mit einer Mortalitätsrate von 11 % nahe kommt und unsere Auswertungen stützt. Die Überlebenswahrscheinlich- - 52 keit der Studienpatienten lag somit bei 83,2 %. Im Detail waren bei den jeweiligen Studienkollektiven die Überlebenschancen mit 94,1 % (Kollektiv 1), 83, 3 % (Kollektiv 2), 73, 3 % (Kollektiv 3) und 50,0 % (Kollektiv 4) sehr hoch. Aliberti et al. (1) haben in einer Studie mit 3.106 Patienten mit Pneumonie herausgefunden, dass es keinen signifikanten Unterschied zwischen Patienten mit / ohne Neutropenie bei Betrachtung des durchschnittlichen Krankenhausaufenthaltes (9,2 ± 7,7 / 9,9 ± 9,6 Tage) und der Mortalität (18 % / 15 %) gab. Die Phase der Neutropenie stand in keinem Zusammenhang mit der Mortalität. Aus diesem Grund empfehlen die neuesten Richtlinien von National Comprehensive Cancer Network (46), dass sowohl immunsupprimierten Patienten ohne Neutropenie als auch denen mit Neutropenie die gleiche Aufmerksamkeit zuteilwerden muss. Dieses Prinzip wurde in der vorliegenden Arbeit konsequent verfolgt. In unserer Studie war das Mortalitätsrisiko mit insgesamt 16,8 % relativ gering. Dieses Ergebnis deckt sich im Großen und Ganzen mit dem Ergebnis von Lima et al. (36), die eine Sterblichkeit von 16,2 % für Niedrigrisikopatienten angeben. Abschließend muss bei der vorliegenden Arbeit berücksichtigt werden, dass durch die anfangs vorgenommen Ausschlusskriterien der Stichprobenumfang mit 119 Einschlusspatienten relativ gering ausfällt und dass aufgrund dieser verhältnismäßig kleinen Stichprobe die Ergebnisse nur als bedingt aussagekräftig angesehen werden können. Ein größerer Stichprobenumfang könnte die Fehlerwahrscheinlichkeit noch weiter minimieren und dabei signifikantere Resultate liefern. - 53 - 6. Zusammenfassung 6.1 Hintergrund und Ziele Infektionen sind bei hämatologisch-onkologischen Patienten bekanntlich äußerst problematisch. Um eine zeitnahe und effektive Behandlung derselben zu ermöglichen, gilt es, die Lokalisation des Infektionsgeschehens und die anschließende Identifikation des verursachenden Erregers schnellstmöglich aufzudecken. Die Lunge ist dabei das am häufigsten von Infektionen betroffene Organ. Die Röntgen-Thorax-Aufnahme gehört hierbei zu der diagnostischen Basis in der Erkennung von Pneumonien. Im Laufe der Zeit nahm die Anzahl der immunsupprimierten Patienten mit entsprechenden infektiösen Komplikationen zu und deshalb steigen die Anforderungen an die radiologische Diagnostik. Da der Stellenwert des konventionellen Röntgen-Thorax in der Diagnostik von Infektionen bei ambulanten Patienten nach Chemotherapie und NiedrigrisikoNeutropenie nicht ausreichend durch klinische Studien gesichert ist, wurde das Problem in der vorliegenden Arbeit genauer eruiert. 6.2 Methoden (Patienten und Untersuchungsmethoden) In einer retrospektiven Analyse von Behandlungsfällen aus dem Universitätsklinikum Regensburg untersuchten wir, wie hoch der prozentuale Anteil an Röntgen-ThoraxAufnahmen insgesamt war und welche Anzahl an positiven Befunden (Pneumonien oder Pneumonieverdachtsfälle) schließlich im Röntgen-Thorax gefunden wurden. Außerdem wurde untersucht, ob es Therapieänderungen oder eine ergänzende Diagnostik aufgrund von positiven Befunden gab. Zuletzt wurde geprüft, ob bzw. welche Unterschiede bei der Behandlungsdauer im Verhältnis der Patienten mit Pneumonie und der Patienten ohne Pneumonie festzustellen waren. Zusammenfassend sollte schließlich die Frage geklärt werden, ob konventionelle Röntgen-Thorax-Aufnahmen in ihrem Stellenwert unzureichend sind und man darauf verzichten könnte. 6.3 Ergebnisse und Beobachtungen Unter den hämatologisch-onkologischen Patienten, die von Januar 2005 bis Februar 2007 in der Abteilung für Hämatologie / Onkologie des Universitätsklinikums Regensburg behandelt wurden, konnten schließlich 119 Patienten für diese Studie erfasst werden. Im weiteren Verlauf der Arbeit wurde die Fokussuche auf Pneumonie, Pneumonieverdachtsfälle oder Befunde ohne Pneumonie bei insgesamt 108 Röntgen-ThoraxAufnahmen durchgeführt. - 54 Positive Röntgenergebnisse (gesicherte, fragliche Pneumonie) wurden mit dem klinischen Verlauf verglichen. Zusätzlich hatten die Patienten insgesamt 15 CT-ThoraxUntersuchungen erhalten. In der Röntgenuntersuchung des Thorax konnte bei 5 von 71 (7,0 %) der Patienten ohne respiratorische Symptome und bei 5 von 37 (13,5 %) der Patienten mit respiratorischen Symptomen eine Pneumonie sowie bei 7 von 71 (9,9 %) bzw. 14 von 37 (37,8 %) der Patienten eine fragliche Pneumonie diagnostiziert werden. In den Leitlinien der Arbeitsgemeinschaft Infektionen in der Hämatologie und Onkologie (AGIHO) (15) wird der Beginn einer empirischen, antiinfektiven Therapie mit Breitspektrumantibiotika unverzüglich nach Fiebereintritt (Infektionsverdacht) empfohlen. In der vorliegenden Arbeit wurde zudem untersucht, ob positive oder verdächtige Befunde im Röntgen-Thorax zu einer Änderung der Therapiestrategie führten. Eine Therapiemodifikation fand bei positivem oder fraglich positivem Röntgenbefund zu 41,9 % (13 Therapieänderungen bei 31 Patienten) statt. Die Behandlungsdauer der Patienten mit Pneumonie (10,8 Tage) oder ohne Pneumonie (11 Tage) im Röntgen-Thorax war annähernd gleich. Auch die Untersuchung der Mortalitätsraten erbrachte in der statistischen Prüfung im Chi-Quadrat-Test mit p = 0,41 keinen signifikanten Unterschied. 6.4 Praktische Schlussfolgerungen Zusammenfassend gelangt man bei den Auswertungen dieser Arbeit zu der Erkenntnis, dass durch die Röntgen-Thorax-Aufnahme bei Patienten mit respiratorischen Symptomen einige pulmonale Infektionen aufgedeckt werden konnten, häufig jedoch mit diagnostischer Unsicherheit (Verdachtsfälle). Der Stellenwert einer Röntgen-ThoraxAufnahme bei Patienten ohne Atemwegserkrankungen erscheint wegen der geringen Anzahl an positiven Befunden sehr fraglich. Falls aus klinischer Sicht eine schnelle und genaue Diagnostik bei Infektverdacht angezeigt ist, sollten andere, sensiblere Diagnoseverfahren, wie z. B. die CT-Untersuchung, zum Einsatz kommen. - 55 - 7. Literaturverzeichnis 1. Aliberti S, Myers JA, Peyrani P, Blasi F, Menendez R, Rossi P, Cosentini R, Lopardo G, de Vedia L, Ramirez JA: The role of neutropenia on outcomes of cancer patients with community-acquired pneumonia. Eur Respir J. 2009 Jan; 33 (1): 6 – 8. 2. Azoulay E, Darmon M: Acute respiratory distress syndrome during neutropenia recovery. Crit Care. 2010; 14(1): 114. doi: 10.1186/cc8198. Epub 2010 Feb 10. 3. Barloon TJ, Galvin JR, Mori M, Standford W, Gingrich RD: High-resolution ultrafast chest CT in the management of febrile bone marrow transplant patients with normal or nonspecific chest roentgenograms. Chest. 1991 Apr; 99(4): 928 – 933. 4. Barreiro Coton S, Schaps KP: Pneumologie. Innere Medizin, Springer-Lehrbuch, 2007: 81 – 112. 5. Bertz H, Auner HW, Weissinger F, Salwender HJ, Einsele H, Egerer G, Sandherr M, Schüttrumpf S, Südhoff T, Maschmeyer G; Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO): Antimicrobial therapy of febrile complications after high-dose chemo- / radiotherapy and autologous hematopoietic stem cell transplantation. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol. 2003 Okt; 82(suppl. 2): 167 – 174. 6. Bodey GP: Infections in cancer patients- a continuing association. Am J Med. 1986; 81: 11 – 26. 7. Bodey GP, Buckley M, Sathe YS, Freireich EJ: Quantitative relationships between circulating leukocytes and infections in patients with acute Leukemia. Ann Intern Med. 1966 Feb; 64(2): 328 – 340. 8. Böhme A: Prophylaxe, Therapie und Diagnostik von Infektionskomplikationen. Der Onkologe. 1998; 4: 820 – 826. 9. Böhme A, Buchheidt D, Donhuijsen K, Einsele H, Enzensberger R, Glasmacher A, Gümbel H, Heussel CP, Karthaus M, Lambrecht E, Ruhnke M, Südhoff T: Diagnostik systemischer Pilzinfektionen in der Hämatologie und Onkologie Leitlinien der Arbeitsgemeinschaft Infektionen in der Hämatologie und Onkologie (AGIHO) der Deutschen Gesellschaft für Hämatologie und Onkologie (DGHO) AGHIO. 2001. - 56 - 10. Böhme A, Ruhnke M, Buchheidt D, Karthaus M, Einsele H, Guth S, Heussel G, Heussel CP, Junghanss C, Kern WK, Kubin T, Maschmeyer G, Sezer O, Silling G, Südhoff T, Szelényi Dagger H, Ullmann AJ; Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO): Treatment of fungal infections in hematology and oncology. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol. 2003 Okt; 82 (suppl. 2): 133 – 140. 11. Buchheidt D, Böhme A, Cornely OA, Fätkenheuer G, Fuhr HG, Heussel G, Junghanss C, Karthaus M, Kellner O, Kern WV, Schiel X, Sezer O, Südhoff T, Szelényi H; Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO): Diagnosis and treatment of documented infections in neutropenic patients. Recommendations of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol. 2003 Okt; 82 (suppl. 2): 127 – 132. 12. Celkan T, Ozkan A, Apak H, Diren S, Can G, Yuksel L, Yildiz I: Bacteremia in childhood cancer. J Trop Pediatr. 2002 Dez; 48(6): 373 – 377. 13. Chanock S: Evolving risk factors for infectious complications of cancer. Hematol Oncol Clin North Am. 1993 Aug; 7(4): 771 – 793. 14. Demirkazik FB, Akin A, Uzun O, Akpinar MG, Ariyürek MO: CT findings in immunocompromised patients with pulmonary infections.Diagn Interv Radiol. 2008 Jun; 14(2): 75 – 82. 15. Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie e. V. (DGHO): Infektionen in der Hämatologie und Onkologie, 27.08.09 http://www.dgho-infektionen.de 16. Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie e. V. (DGHO): Febrile Neutropenie mit Lungeninfiltraten nach intensiver Chemotherapie (Fieber in Neutropenie), 15.03.11 http://www.dgho-onkopedia.de/onkopedia 17. Einsele H, Bertz H, Beyer J, Kiehl MG, Runde V, Kolb HJ, Holler E, Beck R, Schwerdfeger R, Schumacher U, Hebart H, Martin H, Kienast J, Ullmann AJ, Maschmeyer G, Krüger W, Niederwieser D, Link H, Schmidt CA, Oettle H, Klingebiel T; Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO): Infectious complications after allogenic stem cell transplantation: epidemiology and interventional therapy strategies. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol. 2003 Okt; 82 (suppl. 2): 175 – 185. 18. EORTC International Antimicrobial Therapy Cooperative Group: Ceftazidime combined with a short or long course of amikacin for empirical therapy of gram-negative bacteremia in cancer patients with granulocytopenia. N Engl J Med. 1987; 317: 1692 – 1698. - 57 - 19. Fätkenheuer G, Buchheidt D, Cornely OA, Fuhr HG, Karthaus M, Kisro J, Leithäuser M, Salwender H, Südhoff T, Szelényi H, Weissinger F; Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO): Central venous catheter (CVC)-related infections in neutropenic patients. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol. 2003 Okt; 82 (suppl. 2): 149 – 157. 20. Feusner J, Cohen R, O'Leary M, Beach B: Use of Routine Chest Radiography in the Evaluation of Fever in Neutropenic Pediatric Oncology Patients. J Clin Oncol. 1988 Nov; 6(11): 1699 – 1702. 21. Gartenschläger M, Braunschweig R, Ehninger G, Strayle M, Claussen CD: CT und HR-CT in der Diagnostik pulmonaler Komplikationen bei Knochenmarktransplantationen. Rofo. 1994 Apr; 160(4): 303 – 311. 22. Hann I, Viscoli C, Paesmans M, Gaya H, Glauser M: A comparison of outcome from febrile neutropenic episodes in children compared with adults: results from four EORTC studies. International Antimicrobial Therapy Cooperative Group (IATCG) of the European Organization for Research and Treatment of Cancer (EORTC). Br J Hematol. 1997 Dez; 99(3): 580 – 588. 23. Heussel CP, Kauczor HU, Heussel G, Derings HG, Thelen M: Fokussuche bei neutropenischem Fieber. Der Onkologe, Springer-Verlag 1999; 5: 153 – 167. 24. Heussel CP, Kauczor HU, Heussel G, Fischer B, Mildenberger P, Thelen M: Early Detection of Pneumonia in Febrile Neutropenic Patients: Use of Thin- Section CT. AJR Am J Roentgenol. 1997 Nov; 169(5): 1347 – 1353. 25. Heussel CP, Kauczor HU, Matzke G, Fischer B, Mildenberger P: Hochauflösende Computertomographie der Lunge bei neutropenischen Patienten mit Fieber. Rofo. 1996 Mai; 164(5): 368 – 375. 26. Hiddemann W, Maschmeyer G, Runde V, Einsele H: Prophylaxe, Diagnostik und Therapie von Infektionen bei Patienten mit malignen Erkrankungen. Internist. 1996 Dez; 37(12): 1212 – 1224. 27. Hughes WT, Armstrong D, Bodey GP, Feld R, Mandell GL, Meyers JD, Pizzo PA, Schimpff SC, Shenep JL, Wade JC: From the Infectious Diseases Society of America. Guidelines for the use of antimicrobial agents in neutropenic patients with unexplained fever. J Infect Dis. 1990; 161(3): 381 – 396. 28. Hughes WT, Armstrong D, Bodey GP, Bow EJ, Brown AE, Calandra T, Feld R, Pizzo PA, Rolston KV, Shenep JL, Young LS: 2002 guidelines for the use of antimicrobial agents in neutropenic patients with cancer. Clin Infect Dis. 2002 Mär; 34(6): 730 – 751. 29. Jochelson MS, Altschuler J, Stomper PC: The Yield of Chest Radiography in Febrile and Neutropenic Patients. Ann Intern Med. 1986 Nov; 105(5): 708 – 709. - 58 - 30. Karthaus M, Meier PN, Manns MP, Ganser A, Hertenstein B: Hepatische Komplikationen bei Stammzelltransplantationen. Dtsch Med Wschr. 1997 Sep 19; 122(38): 1154 – 1160. 31. Katz JA, Bash R, Rollins N, Cash J, Buchanan GR: The Yield of Routine Chest Radiography in Children with Cancer Hospitalized for Fever and Neutropenia. Cancer. 1991 Sep 1; 68(5): 940 – 943. 32. Kauczor HU, Schnütgen M, Fischer B, Schwickert HC, Härtel S, SchadmandFischer S, Gerken G, Schweden F: Pulmonary manifestations in HIV patients: role of chest films, CT and HRCT. Rofo. 1995 Apr; 162(4): 282 – 287. 33. Klastersky J, Zinner SH: Synergistic combinations of antibiotics in gram-negative bacillary infections. Rev Infect Dis. 1982 Mär-Apr; 4(2): 294 – 301. 34. Kuderer NM, Dale DC, Crawford J, Cosler LE, Lyman GH: Mortality, morbidity, and cost associated with febrile neutropenia in adult cancer patients. Cancer. 2006 Mai 15; 106(10): 2258 – 2266. 35. Lal A, Bhurgri Y, Rizvi N, Virwani M, Memon RU, Saeed W, Sardar MR, Kumar P, Shaikh AJ, Adil S, Masood N, Khurshed M: Factors influencing in-hospital length of stay and mortality in cancer patients suffering from febrile neutropenia. Asian Pac J Cancer Prev. 2008 Apr-Jun; 9(2): 303 – 308. 36. Lima SS, Franca MS, Godoi CC, Martinho GH, de Jesus LA, Romanelli RM, Clemente WT: Neutropenic patients and their infectious complications at a University Hospital. Rev Bras Hematol Hemoter. 2013; 35 (1): 18 – 22. 37. Link H: Infektionen in der Neutropenie. Der Onkologe. 2004; 10(4): 358 – 375. 38. Link H, Maschmeyer G: Therapie und Prophylaxe von Infektionen bei Neutropenie. Kompendium Internistische Onkologie. 2006; 32: 2088 – 2131. 39. Link H, Böhme A, Cornely OA, Höffken K, Kellner O, Kern WV, Mahlberg R, Maschmeyer G, Nowrousian MR, Ostermann H, Ruhnke M, Sezer O, Schiel X, Wilhelm M, Auner HW; Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO); Group Interventional Therapy of Unexplained Fever, Arbeitsgemeinschaft Supportivmassnahmen in der Onkologie (ASO) of the Deutsche Krebsgesellschaft (DKG-German Cancer Society): Antimicrobial therapy of unexplained fever in neutropenic patients. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO), Study Group Interventional Therapy of Unexplained Fever, Arbeitsgemeinschaft Supportivmaßnahmen in der Onkologie (ASO) of the Deutsche Krebsgesellschaft (DKG-German Cancer Society). Ann Hematol. 2003 Okt; 82 (suppl. 2): 105 – 117. - 59 - 40. Marina NM, Flynn PM, Rivera GK, Hughes WT: Candida tropicalis and Candida albicans fungemia in children with leukemia. Cancer. 1991; 68: 594 – 599. 41. Maschmeyer G, Beinert T, Buchheidt D, Einsele H, Heussel CP, Kiehl M, Lorenz J; Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO): Diagnosis and antimicrobial therapy of pulmonary infiltrates in febrile neutropenic patients. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol. 2003 Okt; 82 (suppl. 2): 118 – 126. 42. Maschmeyer G, Böhme A, Buchheidt D, Cornely OA, Fricke HJ, Karthaus M, Lehrnbecher T, Link H, Shah PM, Wilhelm M: Diagnostik und Therapie von Infektionen bei Patienten in der Hämatologie und Onkologie. Chemother J. 2004; 13: 134 – 141. 43. Maschmeyer G, Kern WV: Infektionen bei hämatologischen und onkologischen Erkrankungen. www.dgho.de/informationen/dokumente-der-arbeitskreise/infektionen-in-derhaematologie-und-onkologie 44. Maschmeyer G, Link H, Hiddemann W, Meyer P, Helmerking M, Eisenmann E, Schmitt J, Adam D: Empirische antimikrobielle Therapie bei neutropenischen Patienten. Ergebnisse einer multizentrischen Studie der Paul-Ehrlich-Gesellschaft. Med Klin. 1994 Mär 15; 89(3): 114 – 123. 45. Maschmeyer G, Link H, Hiddemann W, Meyer P, Helmerking M, Eisenmann E, Schmitt J, Adam D: Pulmonary infiltrations in febrile neutropenic patients. Risk factors and outcome under empirical antimicrobial therapy in a randomized multicenter trial. Cancer. 1994 Mai 1; 73(9): 2296 – 2304. 46. National Comprehensive Cancer Network: Prevention and treatment of cancer-related infections 2007. www.nccn.org/about/news/newsinfo.asp?newsID=107 47. Navigante AH, Cerchietti CA, Costantini P, Salgado H, Castro MA, Lutteral MA, Cabalar ME: Conventional Chest Radiography in the initial assessment of adult cancer patients with fever and neutropenia. Cancer Control. 2002 Jul / Aug; 9 (4): 346 – 351. 48. Pizzo PA: Infectious Complications in the child with cancer. Pathophysiology of the compromised host and the initial evaluation and management of the febrile cancer patient. J Pediatr. 1981 Mär; 98(3) 341 – 354. 49. Rhee CK, Kang JY, Kim YH, Kim JW, Yoon HK, Kim SC, Kwon SS, Kim YK, Kim KH, Moon HS, Park SH, Kim HJ, Lee S, Song JS: Risk factors for acute respiratory distress syndrome during neutropenia recovery in patients with hematologic malignancies. Crit Care. 2009; 13(6): R173. Epub 2009 Nov 3. - 60 - 50. Rieger C, Herzog P, Eibel R, Fiegl M, Ostermann H: Pulmonary MRI- a new approach for the evaluation of febrile neutropenic patients with malignancies. Support Care Cancer. 2008; 16: 599 – 606. 51. Rieger CT, Peterson L, Ostermann H: Fieber unklarer Genese bei malignen Erkrankungen. Internist. 2009 Jun; 50(6): 685 – 690. 52. Ruhnke M, Böhme A, Buchheidt D, Donhuijsen K, Einsele H, Enzensberger R, Glasmacher A, Gümbel H, Heussel CP, Karthaus M, Lambrecht E, Südhoff T, Szelényi H; Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO): Diagnosis of invasive fungal infections in hematology and oncology. Guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol. 2003 Okt; 82 (suppl. 2): 141 – 148. 53. Schimpff SC: Empiric antibiotic therapy for granulocytopenic cancer patients. Am J Med. 1986 Mai 30; 80 (suppl. 5c): 13 – 20. 54. Springer Berlin Heidelberg: Therapie und Prophylaxe von Infektionen bei Neutropenie. Medikamentöse Tumortherapie in der Urologie. 2009: 57 – 62. 55. Uhrmeister P, Astinet F, Langer M, Zwicker C, Schönfeld N, Felix R: HR-CT in intestinal lung disease. Rofo. 1992 Jan; 156(1): 53 – 60. 56. Viscoli C, Bruzzi P, Castagnola E, Boni L, Calandra T, Gaya H, Meunier F, Feld R, Zinner S, Klastersky J: Factors associated with bacteraemia in febrile, granulocytopenic cancer patients. The International Antimicrobial Therapy Cooperative Group (IATCG) of the European Organization for Research and Treatment of Cancer (EORTC). Eur J Cancer. 1994; 30A(4): 430 - 437. - 61 - 8. Abbildungsverzeichnis Abbildung 1: Niedrigrisiko-Patienten, empirische Therapie und Management Abbildung 2: Klinischer Verdacht auf Pneumonie vs. kein Verdacht: Einfluss auf das Ergebnis des Röntgen-Thorax Abbildung 3: Mortalität in Abhängigkeit von der abschließenden Diagnose Abbildung 4: Geänderte Antibiose aufgrund des Röntgen-Thorax-Ergebnisses Abbildung 5: Prozentualer Anteil der Enddiagnosen der Kollektive 1+3 sowie der Kollektive 2+4 - 62 - 9. Tabellenverzeichnis Tabelle 1: Risikozuordnung der Patienten nach erwarteter Neutropeniedauer und Risikofaktoren Tabelle 2: Häufigkeit der Infektionsherde in der multizentrischen PEG-Studie mit 1.573 Patienten, bei denen 773 (49 %) Infektionen klinisch oder mikrobiologisch dokumentiert wurden Tabelle 3: Erreger einer Pneumonie Tabelle 4: Klinischer Verdacht auf Pneumonie vs. kein Verdacht: Einfluss auf das Ergebnis des Röntgen-Thorax Tabelle 5: Mortalität in Abhängigkeit von der abschließenden Diagnose Tabelle 6: Änderung der Antibiose aufgrund des Röntgen-Thorax-Ergebnisses Tabelle 7: Anzahl der jeweiligen Ausschlusskriterien Tabelle 8: Verteilung der Einschlusspatienten; Anzahl und Anteil der Kollektive 1-4 Tabelle 9: Verteilung der Grunderkrankungen bei Patienten mit Infektionen nach Chemotherapie und Niedrigrisiko-Neutropenie Tabelle 10: Bezeichnung und Anzahl der Chemotherapien Tabelle 11: Verteilung der Therapielinien Tabelle 12: Pulmonale Vorerkrankungen Tabelle 13: Anzahl und Anteil der Fiebertage der Kollektive 1-4 Tabelle 14: Aufschlüsselung und Anzahl respiratorischer Symptome Tabelle 15: Anzahl und Anteil nicht-respiratorischer Symptome Tabelle 16: Aufschlüsselung und Anzahl nicht-respiratorischer Symptome Tabelle 17: Anzahl fraglich-respiratorischer Symptome Tabelle 18: Aufschlüsselung und Anzahl fraglich-respiratorischer Symptome Tabelle 19: Anzahl pneumonietypischer, technischer Befunde Tabelle 20: Anzahl (i) und Anteil (p) pneumonietypischer, technischer Befunde der Kollektive 1-4 Tabelle 21: Anzahl weiterer technischer Befunde Tabelle 22: Anzahl (i) und Anteil (p) der Röntgen-Thorax-Aufnahmen bei den Kollektiven 1+3 Tabelle 23: Anzahl und Anteil der Röntgen-Thorax-Aufnahmen bei den Kollektiven 2+4 Tabelle 24: Anzahl (i) und Anteil (p) der Befunde aus den Röntgen-ThoraxUntersuchungen der Kollektive 1+3 - 63 Tabelle 25: Anzahl (i) und Anteil (p) der Befunde aus den Röntgen-ThoraxUntersuchungen der Kollektive 2+4 Tabelle 26: Anzahl (i) und Anteil (p) der CT-Thorax-Untersuchungen bei den Kollektiven 1+3 Tabelle 27: Anzahl (i) und Anteil (p) der CT-Thorax-Untersuchungen bei den Kollektiven 2+4 Tabelle 28: Anzahl der CT-Thorax-Untersuchungen bei verschiedenen RöntgenThorax-Befunden der Kollektive 1+3 und der Kollektive 2+4 Tabelle 29: Gesamtergebnisse der CT-Thorax-Untersuchungen zur weiteren diagnostischen Abklärung des Röntgen-Thorax Tabelle 30: Anzahl (n) und Gesamtanteil (%) der Therapieänderungen, mit jeweiliger Medikation, aufgrund positiver Befunde im Röntgen-Thorax bei den Kollektiven 1+3 Tabelle 31: Anzahl (n) und Gesamtanteil (%) der Therapieänderungen, mit jeweiliger Medikation, aufgrund positiver Befunde im Röntgen-Thorax bei den Kollektiven 2+4 Tabelle 32: Behandlungsdauer Pneumonie vs. keine Pneumonie Tabelle 33: Anzahl (n) und Anteil (%) der abschließenden Diagnosen Tabelle 34: Anzahl (i) und Anteil (p) der Röntgen-Thorax-Ergebnisse in Korrelation zum Indexereignis Tabelle 35: Überlebenszeit von vier Wochen der Kollektive 1-4 Tabelle 36: Sterblichkeit bei verschiedenen Diagnosen - 64 - 10. Abkürzungsverzeichnis AGIHO: Arbeitsgemeinschaft Infektionen in der Hämatologie und Onkologie ALL: Akute lymphatische Leukämie AML: Akute myeloische Leukämie AZ: Allgemeinzustand BAL: Bronchoalveoläre Lavage CLL: Chronische lymphatische Leukämie COPD: Chronic Obstructive Pulmonary Disease CRP: C-reaktives Protein CT: Computertomographie DD: Differentialdiagnose DGHO: Deutsche Gesellschaft für Hämatologie und Onkologie EBV: Epstein-Barr-Virus E-coli: Escherichia coli EORTC: European Organisation for Research and Treatment of Cancer FUO: Fever of Unknown Origin HNO: Hals-Nasen-Ohren M. Hodgkin: Morbus Hodgkin MRT: Magnetresonanztomographie NHL: Non-Hodgkin-Lymphom PEG: Paul-Ehrlich-Gesellschaft PCP: Pneumocystis Carinii Pneumonie (heute: Pneumocystis Jirovecii) PCR: Polymerase Chain Reaction SIRS: Systemisches inflammatorisches Response-Syndrom Mengenangaben: dl: Deziliter g: Gramm l: Liter mg: Milligramm mm3: Kubikmillimeter nl: Nanoliter µl: Mikroliter - 65 - 11. Anhang Anhang 1: Röntgen-Thorax bei Fieber in der Neutropenie bei ambulanten Niedrig-Risiko Patienten Patient ....................................................................... geb............................. Doku-Blatt Nr………… Tumordiagnose: ………………………………………………….…………………………………………………………………. Chemotherapie: ……………………………….…. O von . …………bis……………………………….. (Schema) Tage mit Steroid allein zählen nicht mit zu den Chemo-Tagen Therapielinie: O 1st line O 2nd line O 3rd line oder höher Pulmonale Vor-, Begleiterkrankungen: ........................................................................................................................ Beschwerden/Befunde bei Infektverdacht: Datum der Untersuchung wegen Fieber/Infekt (Indexdatum): …………………………………………………………… O Fieber O AZ-Verschlechterung O …………………………….. O Husten O Halsschmerzen, Schnupfen O Schmerzen beim Atmen O Atemnot O Schluckbeschwerden O Bauchschmerzen, Diarrhoe O ………………………………………………………………………………………………………………….. respiratorische und/oder nicht-respiratorische Beschwerden O Rasselgeräusche pulmonal O Giemen, Obstruktion O Halsrötung O V.a. / Thrombose O Pleurareiben O ………………………………………………………………………………………………………………….. respiratorische und/oder nicht-respiratorische Befunde Leuko: ……….. /nl Neutrophile ...................% Neutrophile: ................/nl Hb................. g/dl Thrombo: ................... /nl CRP: ………………..mg/dl O Stratum 1 (Kein Va. a. Atemwegserkr.) O Stratum 2 (V.a. Atemwegserkr.) - 66 - Röntgen-Thorax: O n.d. O am: ……………… O o. p. B. O path Befund: ……………………………………………………….……………………………………………………………. CT Thorax (nur wenn innerhalb 3 Tagen): O n.d. O am: ……………………….O o.B. weitere Diagnostik (nur wenn innerhalb 3 Tagen):……………………………………………… O path Befund: ……………………………………………………….…………………………………………………………….. Sonstige Befunde/ Anmerkungen: .................................................................................................................................................................... .................................................................................................................................................................... Diagnose: ……………………………………………………………………………………………………………………… bei Verlegung/Entlassung aus der NA und gegebenenfalls revidiert nach weiteren Befunden Verlauf: O keine Antibiose O Antibiose fortgeführt O Antibiose eingeleitet/umgesetzt O Medikament(e): …………………………………………………………………………………..………………………………. O Pat. bleibt ambulant O Pat. wird stationär aufgenommen, Dauer Aufenthalt ……Tage O Pat. hat 4 Wochen überlebt O ist gestorben, Todesursache………………………………… - 67 - Anhang 2: 1. Detaillierte Darstellung der Enddiagnosen für das Indexereignis (Kollektiv 1-4) 1.1 Pneumonie gesichert: Kollektiv 1: Pat.nr.: 40 Befund im Röntgen-Thorax: diskrete Zeichnungsvermehrung rechts basal entsprechend einer beginnenden Pneumonie Enddiagnose: Beginnende Pneumonie rechts basal Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 266 Befund im Röntgen-Thorax: Pneumonie gesichert, Infiltrate links Enddiagnose: Pneumonie links bei beginnender Sepsis Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Blutkultur: gramneg. Stäbchen: positiv, Staphylokokkus aureus Pat.nr.: 355 Befund im Röntgen-Thorax: Infiltrat rechts basal, V.a. beginnende Pneumonie, DD: Pilzinfektion Enddiagnose: Pneumonie rechts basal Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Giemen Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) CT-Thorax: V.a. pulmonale Aspergillose Pat.nr.: 476 Befund im Röntgen-Thorax: Pneumonie gesichert, Infiltrat im rechten Mittelfeld Enddiagnose: Mittellappenpneumonie Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 570 Befund im Röntgen-Thorax: nicht beurteilbar, vgl. CT-Thorax Enddiagnose: Pseudomonas-Pneumonie links basal Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg Technische Befunde: Abdomen-CT: Pneumonie im Unterlappen Blutkultur: pos.: Pseudomonas aeruginosa - 68 - Kollektiv 2: Pat.nr.: 30 Befund im Röntgen-Thorax: diskrete Zeichnungsvermehrung im Bereich des linken Unterfeldes, vereinbar mit beginnendem Infiltrat Enddiagnose: Linksseitige Pneumonie Nachgewiesen durch: „unter Einbezug der Klinik und des erhöhten CRP...“ Klinische Befunde: Fieber, CRP-Anstieg, Husten, Rasselgeräusche, Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 107 Befund im Röntgen-Thorax: links basale Zeichnungsvermehrung einem Infiltrat entsprechend, gesicherte Pneumonie Enddiagnose: Pneumonie Nachgewiesen durch: Klinische Befunde: Fieber, Husten, Rasselgeräusche, Belastungsdyspnoe Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 199 Befund im Röntgen-Thorax: V.a. Infiltrat rechts apikal und rechts basal mit ausgedehntem positivem Bronchoaerogramm, V.a. Pneumonie Enddiagnose: Pneumonie in der Neutropenie Nachgewiesen durch: „unter Einbezug der Klinik und des erhöhten CRP...“ Klinische Befunde: Fieber, CRP-Anstieg, Rasselgeräusche Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Serum: Aspergillus-Antigen positiv Pat.nr.: 210 Befund im Röntgen-Thorax: V.a. pneumonische Infiltrate Enddiagnose: Pneumonie beidseits Nachgewiesen durch: Klinische Befunde: CRP-Anstieg, Rasselgeräusche, Halsrötung Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) CT-Thorax: pneumonische Infiltrate Pat.nr.: 343 Befund im Röntgen-Thorax: V.a. Pneumonie, linker Unterlappen im Vgl. zur VA: leicht zunehmende Zeichnungsvermehrung Enddiagnose: Pneumonie in beiden Unterlappen, diskreter Pleuraerguss beidseits Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Husten, Diarrhoe Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) CT-Thorax: diskreter Pleuraerguss beidseits mit Dystelektasen beidseits, zusätzlich pneumonische Infiltrate im Unterlappen links > rechts Pat.nr.: 560 Befund im Röntgen-Thorax: Infarktpneumonie, keilförmiges Infiltrat links, diskrete Infiltrate rechts Enddiagnose: Pneumonie Nachgewiesen durch: Klinische Befunde: CRP-Anstieg, Atemnot, Rasselgeräusche, Giemen Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) CT-Thorax: Pneumonie linker Oberlappen - 69 - Kollektiv 3: Pat.nr.: 68 Befund im Röntgen-Thorax: diskrete retikuläre Zeichnungsvermehrung in beiden Unterlappen Enddiagnose: Atypische Pneumonie in beiden Unterlappen Nachgewiesen durch: „unter Einbezug der Klinik und des erhöhten CRP...“ Klinische Befunde: Fieber, CRP-Anstieg Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 402 Befund im Röntgen-Thorax: Infiltrat rechter Unterlappen entsprechend einer Pneumonie Enddiagnose: Pneumonie rechter Unterlappen Nachgewiesen durch: Klinische Befunde: CRP-Anstieg, Giemen Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Kollektiv 4: Pat.nr.: 253 Befund im Röntgen-Thorax: pneumonisches Infiltrat rechts Enddiagnose: Pneumonie rechts Nachgewiesen durch: Klinische Befunde: CRP-Anstieg, Husten, Atemnot, thorakale Schmerzen, Rasselgeräusche, Orthopnoe, Dyspnoe Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 428 Befund im Röntgen-Thorax: keine Pneumonie Enddiagnose: Pneumonie Nachgewiesen durch: Klinische Befunde: Fieber, Giemen, Atemnot Technische Befunde: CT-Thorax: Ausgedehnte Infiltrate in beiden Lungen BAL-Untersuchung: Pneumocystis carinii positiv Pat.nr.: 509 Befund im Röntgen-Thorax: Transparenzminderung im linken Unterlappen, DD: pneumonisches Infiltrat, Lymphombefall Enddiagnose: Pneumonie bei Infiltraten im Unterlappen Nachgewiesen durch: Klinische Befunde: CRP-Anstieg, Husten, rechts-thorakale Schmerzen beim Husten, Rasselgeräusche Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) CT-Thorax: V.a. pneumonische Infiltrate im linken Unterlappen, DD: Pilzpneumonie - 70 - 1.2 Fragliche Pneumonie, keine plausiblere Diagnose gefunden, evtl. kombinierte Infekte: Kollektiv 1: Pat.nr.: 118 Befund im Röntgen-Thorax: V.a. Pneumonie, fragl. Infiltrat rechts basal Enddiagnose: Fieber, V.a. Infekt ohne Organfokus und Mukositis Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Halsschmerzen, Schluckbeschwerden Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Kollektiv 2: Pat.nr.: 62 Befund im Röntgen-Thorax: Infiltrat links nicht genau abgrenzbar, V.a. Pneumonie Enddiagnose: V.a. Pneumonie Nachgewiesen durch: Klinische Befunde: Husten, Dyspnoe, CRP-Anstieg Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 71 Befund im Röntgen-Thorax: V.a. Pneumonie, pneumonische Infiltrate möglich Enddiagnose: V.a. Pneumonie Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Husten, Dyspnoe, Schmerzen beim Atmen Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) CT-Thorax: pneumonische Infiltrate möglich Pat.nr.: 178 Befund im Röntgen-Thorax: V.a. interstitielle Pneumonie, (Lungeninfiltrat) Enddiagnose: Fieberhafter unklarer Infekt bei V.a. Pneumonie Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Husten, Rasselgeräusche Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 304: Befund im Röntgen-Thorax: V.a. Pneumonie, neu aufgetretenes pneumonisches Infiltrat im rechten Unterlappen Enddiagnose: Fieber, V.a. Infekt: AZ-Verschlechterung mit Fieber bei Leukozytopenie Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Husten Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 341: Befund im Röntgen-Thorax: V.a. Pneumonie, Verschattungen: V.a. pneumonisches Infiltrat Enddiagnose: Fieber, V.a. Infekt: Fieber in der Neutropenie, Stomatitis Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Husten, Halsschmerzen Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Abstrich (Mund): EBV-DNA positiv EBV - 71 - Pat.nr.: 467 Befund im Röntgen-Thorax: V.a. Pneumonie, perhiläre Infiltrate beidseits, V.a. pneumonische Infiltrate Enddiagnose: Fieber, V.a. Infekt: Fieber in der Leukopenie Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Husten, Atemnot, Rasselgeräusche Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 541 Befund im Röntgen-Thorax: V.a. Pneumonie, basale Zeichnungsvermehrung links, evtl. einem Infiltrat entsprechend Enddiagnose: V.a. Pneumonie Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg,-Verlauf Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 572 Befund im Röntgen-Thorax: V.a. frisches pneumonisches Infiltrat Enddiagnose: V.a. Pneumonie linker Unterlappen Nachgewiesen durch: „unter Einbezug der Klinik und des erhöhten CRP...“ Klinische Befunde: Fieber, CRP-Anstieg, Husten, Halsschmerzen Technischen Befund: Röntgen-Thorax-Untersuchung: (siehe oben) Kollektiv 3: Pat.nr.: 189 Befund im Röntgen-Thorax: V.a. Pneumonie, in rechter Lunge mehrere flaue fleckige Verdichtungen bei entsprechender Klinik vereinbar mit einem beginnenden pneumonischen Infiltrat Enddiagnose: Fieber, V.a. Infekt ohne Organfokus: Fieber in der Neutropenie nach Chemotherapie Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Diarrhoe Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Laborbefund: ausgeprägte Leukopenie Kollektiv 4: Pat.nr.: 193 Befund im Röntgen-Thorax: V.a. Pneumonie, rechts parakardiale Zeichnungsvermehrung im Sinne infiltrativer Veränderung Enddiagnose: Fieber, V.a. Infekt: Fieber in der Neutropenie, Aspergillus-Antigen Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Rasselgeräusche, thorakale Schmerzen Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Aspergillus-Antigen: positiv Pat.nr.: 281 Befund im Röntgen-Thorax: Verdichtung im Bereich des linken Unterfeldes, DD: Infiltration, Metastasierung Enddiagnose: V.a. Pneumonie Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Atemnot, Rasselgeräusche, thorakale Schmerzen Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) CT-Thorax: V.a. neu aufgetretene pneumonische Infiltrationen, z.T. pilztypisch Untersuchung - 72 - 2. Patienten mit fraglicher Pneumonie im Röntgen-Thorax, aber andere Enddiagnose ist für das Indexereignis plausibler Kollektiv 1: Pat.nr.: 88 Befund im Röntgen-Thorax: V.a. Pneumonie, flächige fleckige Zeichnungsvermehrung rechts parahilär. Beide Hili verbreitert. Vereinbar mit einem Infiltrat Enddiagnose: Nicht-pulmonaler Infekt: Clostridium difficile Colitis Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Diarrhoe Technische Befunde: Stuhl-Untersuchung: Clostridium difficile Toxin A positiv Kollektiv 2: Pat.nr.: 462 Befund im Röntgen-Thorax: neue Infiltrate im Bereich der Lingula, im linken Oberlappen und Unterlappen: V.a. atypische Pneumonie Enddiagnosen: Exitus letalis bei Sepsis in der Neutropenie, SIRS, akutes Nierenversagen, Harnwegsinfekte Nachgewiesen durch: Klinische Befunde: CRP-Anstieg, Brennen beim Wasserlassen, Rasselgeräusche, Giemen, Thoraxschmerz, akuter Harnverhalt Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) U-Stix: Leukos 10-25, Eiweiß 30, Blut 250 Urikult: Leukozyten +++, Nitrat pos. Kollektiv 3: Pat.nr.: 289 Befund im Röntgen-Thorax: V.a. Pneumonie Enddiagnose: Fieber, V.a. Infekt ohne Organfokus Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Pat.nr.: 309 Befund im Röntgen-Thorax: V.a. Pneumonie, beidseits retikuläre Zeichnungsvermehrung, DD: beginnendes Infiltrat Enddiagnose: Fieber, V.a. freie Luft intraabdominell, Gastroenteritis durch Noro-Virus Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, Bauchschmerzen Technische Befunde: Röntgen-Abdomen: freie Luft intraabdominell PCR (Stuhl): Noro-Virus: positiv Kollektiv 4: Pat.nr.: 31 Befund im Röntgen-Thorax: Verdichtung dorsobasal beidseits rechts betont, abgerundete Rec. im Sinne von Pleuraergüssen und angrenzenden dorsobasalen Dystelektasen, zusätzliche pneumonische Infiltrate können maskiert sein Enddiagnose: Fieber, Tumorprogress Nachgewiesen durch: Klinische Befunde: Fieber, CRP-Anstieg, massiv progrediente Leberfiliae Technische Befunde: Röntgen-Thorax-Untersuchung: (siehe oben) Sono-Abdomen: Aszites, diffuse Lebermetastasierung - 73 - 12. Danksagung Zunächst möchte ich natürlich vor allem Herrn Prof. Dr. Stefan Krause, meinem Doktorvater, herzlich danken, dass er mir dieses klinisch relevante Thema zur Dissertation überlassen hat. Vom ersten Tag an fühlte ich mich sehr gut betreut und seine Tür stand stets für mich offen. Selbst als er seine neue Lehrtätigkeit an der Universitätsklinik Erlangen aufnahm, war alles so organisiert, dass ich ohne zeitlichen Verzug jederzeit Antwort auf meine drängenden Fragen erhielt. Sogar an Wochenenden war Herr Prof. Dr. Krause für mich erreichbar. Mein besonderer Dank gilt ebenfalls Herrn OA Dr. Joachim Hahn von der Universitätsklinik Regensburg, der mir während der Umzugszeit von Herrn Prof. Dr. Krause nach Erlangen als hilfsbereiter und geduldiger Betreuer zur Seite stand. Zu großem Dank bin ich auch Frau Heike Kassubek für die Bereitstellung eines Arbeitsplatzes in ihrem Büro und ihrer Hilfe und Geduld bei meiner Aktenrecherche verpflichtet. Nicht zuletzt danke ich von ganzem Herzen meinen Eltern, die mir besonders dann, wenn ich an mir zweifelte, seelischen Beistand gaben und mich zum Durchhalten bei der Erstellung der Dissertation ermutigten.