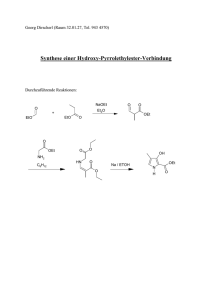
Jede im Protokoll angegebene Struktur erhält eine Nummer. Diese
Werbung

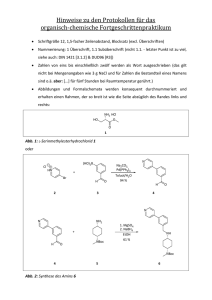
Leitfaden zu Protokollen für das IGSP 1. Formales 1.1. Erfolg eines Präparates Eine Synthese gilt als erfolgreich abgeschlossen, wenn eine angemessene Ausbeute erreicht wurde und die Reinheit ≥ 95% (NMR/HPLC od. GC) beträgt. Was angemessen ist, entscheidet der Assistent bzw. der Praktikumsleiter. Je höher die Ausbeuten eines reinen Produktes sind, desto besser. Reinigungen sollten also nicht nach Erreichen einer bestimmten Menge Produkt abgebrochen werden! Der Assistent und Praktikumsleiter entscheidet, ob eine Synthesestufe bei zu geringer Ausbeute oder Reinheit des Produkts wiederholt werden muss. 1.2. Struktur Im Protokoll müssen folgende Punkte enthalten sein: Deckblatt, Einleitung, Experimenteller Teil (mit Versuchsansatz, Durchführung, vollständige Auswertung/Charakterisierung), Diskussion, Referenzen und Anhang (mit analytischen Daten). 1.3. Deckblatt Bitte verwenden Sie das vorgeschlagene Deckblatt. Dies erleichtert die Zuordnung und Bearbeitung der Protokolle. 1.4. Generelles Im Fortgeschrittenen-Praktikum sind alle Protokolle in englischer Sprache abzugeben. Experimentalteile sind den ACS-Vorgaben entsprechend zu verfassen (siehe hierzu: http://pubs.acs.org/paragonplus/submission/orlef7/orlef7_authguide.pdf) Arial, Schriftgröße 12, 1.5-facher Zeilenabstand (erleichtert das Korrigieren), Blocksatz (exkl. Überschriften) Zahlen von eins bis einschließlich zwölf werden als Wort ausgeschrieben. Das gilt nicht bei Mengenangaben (3 g NaCl) und für Zahlen die Bestandteil eines Namens sind o.ä. Bsp: The mixture was stirred for five hours at room temperature. Abbildungen und Formelschemata werden konsequent durchnummeriert. (Figure 1: Description. Scheme 1: Synthesis of Compound 1.) Strukturen in Abbildungen müssen gleich groß sein, d.h. ein Benzolring in Abbildung 1 muss die gleiche Größe haben wie einer in Abbildung 5. Am besten direkt durch CopyPaste von ChemDraw in Word einfügen. Jede im Protokoll angegebene Struktur erhält eine Nummer. Diese wird unterhalb der Struktur angegeben (Zahl wird fett gesetzt); bezieht man sich später im Text auf diese Struktur, wird die Zahl verwendet und wieder fett gesetzt. z.B.: Compound 3 was isolated as white solid in 36% yield. WICHTIG: Die Zahlen müssen so vergeben werden, dass die Strukturen nach Reihenfolge ihres Erscheinens im Protokoll nummeriert sind, d.h. die Struktur, die als erste im Protokoll auftaucht, bekommt die Nummer 1, die zweite die 2 usw. Hinweis: Basen, Säuren, Katalysatoren und Lösungsmittel werden, damit sie nicht in die Nummerierung eingeschlossen werden müssen, über den Reaktionspfeil platziert. Wiederholt auftretende Strukturen erhalten immer wieder dieselbe Nummer. (vgl. Compound 4 in Scheme 2) 2. Einleitung Jede Synthese verfolgt einen Zweck. Warum möchte ich dieses Molekül herstellen? Wozu wird es benötigt? (Beispiele: Chloro-Inosine - wichtige Vorstufe für 6-modifizierte AdenosinDerivate, THPTA – wichtiger Ligand für Kupfer(I) katalysierte Klick-Reaktionen) Beschreibe den Zweck deines Präparates in zwei bis drei Sätzen. Beschreibung der Syntheseroute Welches sind die Edukte? Wie viele Stufen hat die Syntheseroute? Welche Reaktionen werden verwendet? (z.B. nukleophile Substitution, Sonogashira-Reaktion, Veresterung) Entstehen Nebenprodukte? Sinn ist das schlüssige, fachgerechte Formulieren einer Syntheseroute ohne experimentelle Details Beispiel: Scheme 6: Synthesis of Si-TMR (3). The convergent, seven-step synthesis of Si-TMR (3) was first described by G. Lukinavičius et al.[1] and is depicted in Scheme 6. Synthesis starts from commercial 3-bromo-N,N-dimethylaniline (7) which undergoes a condensation reaction with formaldehyde to form methylene-bridged compound 8. Then, lithium-halogen exchange and consecutive ring closure is used for the formation of intermediate 9, which is directly oxidised to silicon-containing compound 10. Prior to coupling of the two aromatic precursors, commercial 2-bromo-terephthalic acid (11) is bisprotected with 4,4-dimethyl-2-oxazoline. Therefore, 2-bromo-terephthalic acid (11) is reacted with 2amino-2-methylpropan-1-ol to obtain the respective bis(amide) 12. Induced by treatment with SOCl2, bis(oxazoline) 13 is obtained in a ring closure according to SNi mechanism. Then, protected 2-bromo-terephthalic acid undergoes a lithium-halogen exchange and a nucleophilic addition onto the keto-group of 10 results in the formation of compound 14. Finally, target molecule 3 synthesised by acid catalysed deprotection of compound 14. 3. Experimenteller Teil 3.1. Formelles - die Experimente wurden vor einiger Zeit abgeschlossen, folgerichtig ist die für die Durchführung zu verwendende Zeitform das Präteritum - Laborsprache ist zu vermeiden, verwende eher Schriftsprache z.B.: to extract; to stir under reflux conditions (or 80 °C); the solvent was removed under reduced pressure… nicht to cook, to shake… - Beschreibung der genauen, eigenen Versuchsdurchführung. Auch Farbumschläge, Ausfallen von Feststoffen… erwähnen. (keine Abschrift der Versuchsvorschrift – eventuelle Abweichungen werden im Diskussionsteil diskutiert) - Sätze wie „I spilled the compound and extracted the bench“ gehören nicht in den experimentellen Teil. Solche Informationen kommen in den Diskussionsteil. - „I“ ist im experimentellen Teil nicht zu verwenden. Stattdessen nutzt man Passivformulierungen: Bsp.: Compound 7 was isolated in 87% yield (5.78 g, 3.67 mmol). - Grundsätzlich erfolgt die Angabe der Menge für alle verwendeten Reagenzien immer dreigeteilt: Angabe der Masse in Gramm, der Stoffmenge in mol bzw. mmol oder μmol und die Angabe der Äquivalente z.B.: A mixture of 3-(pyridin-4-yl)benz-aldehyd (150 mg, 819 μmol, 1.0 eq.), tert-butyl(trans-4-aminocyclohexyl)methyl-carbamate (187 mg, 819 μmol, 1.0 eq.) and anhydrous magnesium sulfate (119 mg, 989 μmol, 1.2 eq.) in absolute ethanol (7.0 mL) was stirred for eight hours at 80°C. Bei Flüssigkeiten wird zusätzlich das Volumen angegeben: Triethylamine (3.25 mL, 2.37 g, 23.4 mmol, 1.5 eq.) - WICHTIG: Auf signifikante Ziffern achten! Angaben wie (3.4 g, 12.345 mmol) sind inkorrekt. Die Stoffmenge wird hier mit fünf signifikanten Ziffern angegeben, obwohl die gemessene Größe (Masse) nur mit zwei signifikanten Ziffern bestimmt wurde. Es muss also korrekt heißen: (3.4 g, 12 mmol). Da im Praktikum hauptsächlich auf 1-10 mg genau gemessen wurde, ergibt sich in der Regel also solch eine Angabe: (1.23 g, 17.5 mmol, X.X eq.) - Zwischen Zahl und Einheit kommt ein Leerzeichen, sie bilden eine Einheit und sollen nicht durch Zeilenumbrüche o.ä. getrennt werden. Hilfreich für die Formatierung ist das Verwenden geschützter Leerzeichen (Strg+Shift+Leer). 3.2. Angabe und Interpretation analytischer Daten DC: Der Rf-Wert wird auf zwei Nachkommastellen angegeben, in Klammern steht das Lösungsmittelgemisch, getrennt durch Schrägstrich und das Verhältnis, getrennt durch Doppelpunkt, sowie der Zusatz v/v, z.B.: Rf = 0.49 (n-Hexan/Essigester 3:1 v/v) Schmelzpunkte: Zur vollständigen Angabe des Schmelzpunktes gehört die Nennung des Lösungsmittels, aus welchem das Produkt umkristallisiert wurde m.p.: 134 °C (CH3OH). NMR: 1H-NMR: Angegeben werden zunächst Resonanzfrequenz und Lösungsmittel (CDCl , 3 CD3OD, DMSO-d6, D2O und andere). Dann folgen die Signale mit ihren chemischen Verschiebungen (zwei Nachkommastellen), beginnend bei niedrigen ppm-Werten. Bei Signalen mit definierten Multiplizitäten (s, d, t, q, p, dd, ddd, dt, td, tt, u.a.) wird der Signalschwerpunkt angegeben. Bei Multipletts wird der Signalbereich angegeben. - Hinter der chemischen Verschiebung folgen in Klammern: Multiplizität abgekürzt als s (Singulett), d (Duplett), t (Triplett), q (Quartett oder Quadruplett), p (Quintett oder Pentuplett), m (Multiplett), dd (Duplett vom Duplett) etc. - Relatives Integral des Signals (Anzahl der H-Atome dieses Signals) bei Dupletts, Tripletts, etc. werden als nächstes die Kopplungskonstante(n) angegeben. - Kopplungskonstanten werden in Hertz mit einer Nachkommastelle angegeben. Das J wird kursiv gesetzt. Ganz korrekt wäre eine Angabe wie folgt: xJHH = 7.8 Hz (Wobei das x durch eine Zahl ersetzt werden muss, die angibt, über wie viele Bindungen diese Kopplung zustande kommt. Der Index bezeichnet die koppelnden Kernspezies. Bei Angabe von mehr als einer Kopplungskonstante bei einem Signal (z.B. bei einem Doppelduplett) werden diese nach ihrem Betrag absteigend sortiert angegeben. Die Zuordnung zu einem Proton: Es gibt zur Kennzeichnung zwei Möglichkeiten: a) Man verwendet sinnvolle Abkürzungen für Formelausschnitte wie OCH3, CO2CH3 oder CH2CH3, wobei das/die betreffende/n Wasserstoffatome fett oder kursiv hervorgehoben wird/werden. Oder b) man bezeichnet ein H z. B. mit H-1, wobei dann allerdings die Nummerierung aus dem Substanznamen hervorgehen muss (IUPAC-Nummerierung der Atome). Die Einheit der chemischen Verschiebung ppm kann am Anfang oder am Ende stehen. Das Ganze sieht dann z. B. folgendermaßen aus: (300 MHz, CDCl3) δ [ppm] = 1.04 (s, 9H, C(CH3)3), 1.34-1.42 (m, 1H, H-7), 2.01 (dd, 1H, HH=6.9 Hz, 2JHH=4.3 Hz, H-2), 7.35-7.46 (m, 3H, Harom). 1H-NMR 3J oder (300 MHz, CDCl3) δ = 1.04 (s, 9H, C(CH3)3), 1.34-1.42 (m, 1H, H-7), 2.01 (dd, 1H, 2 HH=6.9 Hz, JHH=4.3 Hz, H-2), 7.35-7.46 (m, 3H, Harom) ppm. 1H-NMR 3J 13C-NMR: Analog zum 1H-NMR, aber nur eine Nachkommastelle angeben, bei der Zuordnung die gleiche Nummerierung wie beim 1H-NMR verwenden bzw. das/die betreffende/n C-Atom/e im Formelausschnitt fett oder kursiv setzen Das Ganze sieht dann z. B. folgendermaßen aus: (100 MHz, CDCl3): δ [ppm] = 27.7 (C-3, C-3’), 28.5 (-N-CH3), 28.5 (C(CH3)3), 32.0 (C-2, C-2’), 38.9 (-SO2-CH3), 52.5 (br, C-4), 79.7 (-C(CH3)3), 80.1 (C-1), 155.6 (C=O) 13C-NMR 4. Diskussion der Ergebnisse Hier erfolgt die kritische Reflexion mit den vorgelegten Ergebnissen und ist essentiell für jedwedes wissenschaftliche Arbeiten. - War die Synthese erfolgreich? Wenn nicht, warum? - Stimmen die erhaltenen physikalischen Daten mit der Literatur überein? (Achtung Quellen angeben!) - Sind die Ausbeuten in Übereinstimmung mit der Literatur? Wenn nicht, warum? (Literaturwert ± 10% normal) - Gab es Probleme bei der Durchführung? Mussten Vorschriften abgeändert werden? Konnte die benutzte Vorschrift reproduzierbar umgesetzt werden? - Gibt es Verbesserungsvorschläge oder andere zielführende Synthesewege? 5. Referenzen Alle Quellen müssen ordnungsgemäß, richtig und nachvollziehbar aufgeführt werden; das gilt insbesondere für Vergleichsspektren und Literaturangaben von Messwerten. Im fließenden Text werden Literaturverweise hochgestellt angegeben. Am Ende des Protokolls werden alle Literaturstellen in der Reihenfolge ihrer Erwähnung im Text aufgeführt. Bei Zeitschriften müssen alle Autoren genannt, Zeitschriftenbezeichnungen wie international üblich abgekürzt (siehe im Internet unter: http://cassi.cas.org/) sowie das Erscheinungsjahr, der Jahrgang und die Seitenzahlen „von – bis“ angegeben werden. Hinter die Literaturangaben wird immer ein Punkt gesetzt. Alle Angaben haben einheitlich zu erfolgen. z. B.: [1] Ian B. Seiple, Shun Su, Ian S. Young, Chad A. Lewis, Junichiro Yamaguchi, Phil S. Baran, Angew. Chem. 2010, 122, 1113-1116. Bei Büchern wird angegeben: Autor(en), Titel (in Klammern der Herausgeber falls abweichend), Auflage, Verlag, Sitz des Verlages, das Erscheinungsjahr und die Seitenzahlen. z.B.: [2] Y. S. Cho, H. J. Kwon in Protein Targeting with Small Molecules: Chemical Biology Techniques and Applications (Hrsg.: H. Osada), Vol. 1, John Wiley & Sons, Hoboken, 2009, S. 81-90. Bei Internetquellen muss die gesamte URL angegeben werden und das Datum des Besuches, z.B.: [3] http://de.wikipedia.org/wiki/Zitieren_von_Internetquellen (Stand: 17.06.2014). 6. Analytische Daten Hier sollen analytische Daten aufbereitet und nachvollziehbar angehängt werden. DC Zeichnung der während des Praktikums angefertigten Reaktionskontrollen, muss für jede Stufe enthalten: Edukt, Reaktionsmischung, aufgereinigtes Produkt, Färbereagenz, LM-Gemisch NMR-Spektren mit z.B. MestReNova ausgewertet und zugehöriger chemischer Struktur auf dem Spektrum (darf von Hand gezeichnet sein). Spektrum muss beschriftet (z.B. 1H-NMR von Verbindung 1 (400 MHz) in CDCl3), referenziert, integriert, interpretiert und zugeordnet sein (z.B. Wasser und Aceton-Reste hier kennzeichnen) Andere Daten z.B. MS oder IR beschriftet und nachvollziehbar Musterdeckblatt: Name / Laborplatz; WS 15/16 Assistant: date Sythesis of XXX (Endprodukt) Syntheseschema komplett (alle Stufen eines Präparats) mit Reagenzien und Reaktionszeit auf Reaktionspfeil Beispiel: Scheme 1: Synthesis of Rhodamine 110 chloride (3) in one step. Auf den folgenden Seiten folgen analog „Leitfaden zu Protokollen für das IGSP“ 1. Introduction 2. Results 2.1 Step 1: Synthesis of XXX 2.1.1 Batch 2.1.2 Experimental procedure 2.1.3 Characterization 2.2 Step 2: Synthesis of YYY 3. 2.2.1 Batch … Discussion 4. References 5. Attachment (Analytical Data, NMR…)