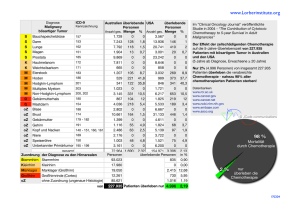
„Therapie bei onkologischen Erkrankungen“
Werbung

Bachelorarbeit Studium der Gesundheits- und Pflegewissenschaften „Therapie bei onkologischen Erkrankungen“ Lehrveranstaltung: Physiologie Betreuerin: Ao.Univ.-Prof. Dr.phil. Anna Gries Institut für Physiologie E-Mail: [email protected] Vorgelegt von: Kristina Glettler im: August 2016 Eidesstattliche Erklärung: Ich erkläre ehrenwörtlich, dass ich die vorliegende Bachelorarbeit selbstständig und ohne fremde Hilfe verfasst habe, andere als die angegebenen Quellen nicht verwendet und die den benutzten Quellen wörtlich oder inhaltlich entnommenen Stellen als solche kenntlich gemacht habe. Graz, August 2016 Kristina Glettler, eh. Zusammenfassung In Österreich erkranken laut Angaben des Bundesministeriums für Gesundheit jährlich etwa 38.000 Menschen an Krebs. Auch wenn die Medizin in ihren Möglichkeiten immer weiter fortschreitet und es laut ExpertInnen in den nächsten Jahren zu einem Rückgang der Krebsneuerkrankungen kommen wird, könnte die immer höhere Lebenserwartung und die dadurch bedingte Alterung der Gesellschaft dies wieder „ausgleichen“. Zu Beginn der Arbeit werden Begriffserklärungen rund um die Tumortherapie gegeben, es wird die Entstehung maligner Tumore erläutert und beeinflussbare bzw. nicht beeinflussbare Risikofaktoren genannt. Im mittleren Teil geht es komplementären/alternativen um die Arten der Chemotherapie Behandlungsmöglichkeiten und deren und die Vor- und Nachteile. Weiters wird genauer auf das Mammakarzinom, als häufigstes Karzinom der Frau, eingegangen. Am Ende der Arbeit werden die Stomapflege und Präventionsmaßnahmen behandelt. Die Forschungsfrage zu dieser Arbeit lautet: „Kann einer Krebsentstehung vorgebeugt werden und sind Krebsvorsorgeuntersuchungen in der Regel sinnvoll?“. Inhaltsverzeichnis 1 Einleitung .............................................................................................................................................. 5 2 Begriffserklärungen .............................................................................................................................. 6 2.1 Chemotherapie .............................................................................................................................. 6 2.2 Strahlentherapie............................................................................................................................ 7 2.3 Antikörpertherapie ........................................................................................................................ 8 3 Entstehung maligner Tumoren ............................................................................................................. 8 3.1 Einteilung ....................................................................................................................................... 8 3.2 Kriterien für Malignität .................................................................................................................. 9 3.3 Ursachen für die Entstehung maligner Tumoren .......................................................................... 9 4 Risikofaktoren..................................................................................................................................... 11 4.1 Nicht beeinflussbare Risikofaktoren ........................................................................................... 11 4.2 Beeinflussbare Risikofaktoren ..................................................................................................... 11 5 Arten der Chemotherapie .................................................................................................................. 18 5.1 Systemische Chemotherapie ....................................................................................................... 18 5.2 Regionale Chemotherapie ........................................................................................................... 18 5.3 Chemoembolisation .................................................................................................................... 18 5.4 Intrakavitäre Chemotherapie ...................................................................................................... 18 5.5 Transdermale Chemotherapie .................................................................................................... 19 6 Komplementäre und alternative Therapien in der Onkologie ........................................................... 20 6.1 Begriffsdefinitionen ..................................................................................................................... 20 6.2 Kategorien von Komplementär- und Alternativmedizin nach dem National Center for Complementary and Alternative Medicine........................................................................................ 20 6.3 Risiken von Komplementär- und Alternativmedizin ................................................................... 21 7 Mammakarzinom bei Frauen ............................................................................................................. 23 7.1 Brusterhaltende Operation ......................................................................................................... 23 7.2 Mastektomie und Brustrekonstruktion ....................................................................................... 23 7.3 Lymphknotenentfernung............................................................................................................. 23 7.4 Nachsorge .................................................................................................................................... 24 7.5 Breast Care Nurse ........................................................................................................................ 24 8 Stomapflege........................................................................................................................................ 24 8.1 Stoma des Darms......................................................................................................................... 24 8.1.1 Definition und Indikationen ................................................................................................. 24 8.1.2 Stomalokalisation und Stomaformen ................................................................................... 25 8.1.3 Stomaplatzierung ................................................................................................................. 26 8.2 Harnableitendes Stoma ............................................................................................................... 26 8.3 Information von PatientInnen und Angehörigen ....................................................................... 27 9 Präventionsmaßnahmen .................................................................................................................... 28 9.1 Nationales Krebsvorsorgeprogramm des BMG ........................................................................... 28 9.2 Krebsvorsorgeuntersuchungen ................................................................................................... 29 10 Diskussion ......................................................................................................................................... 31 11 Literaturverzeichnis .......................................................................................................................... 33 12 Internetquellen................................................................................................................................. 34 13 Abbildungsverzeichnis ...................................................................................................................... 35 14 Tabellenverzeichnis .......................................................................................................................... 36 1 Einleitung Bösartige Krebserkrankungen stellen nach Herz-Kreislauf-Erkrankungen die zweithäufigste Todesursache in Österreich dar. Heutzutage gibt es bereits eine Vielzahl an diversen Therapiemöglichkeiten, angefangen von operativen Maßnahmen, über Chemo-, Hormon- und Bestrahlungstherapie. Die folgende Arbeit soll einen groben Überblick über genau diese Möglichkeiten geben, die Entstehung und Ursache von Krebs erläutern und über aktuelle Präventionsmaßnahmen informieren. Da sich die Betroffenen oft an jede noch so kleine Hoffnung klammern, wird auch ein Einblick in die Komplementärtherapien in der Onkologie gegeben. In der Gesundheitspolitik wird verhaltenspräventiven Maßnahmen eine immer größere Bedeutung Verantwortung für zugeschrieben die Erhaltung zurückgegeben. Aus diesem Grund und und den Menschen Wiederherstellung so wieder ihrer mehr Gesundheit werden auch beeinflussbare und nicht beeinflussbare Risikofaktoren erläutert und die Forschungsfrage behandelt „Kann einer Krebsentstehung vorgebeugt werden und sind Krebsvorsorgeuntersuchungen in der Regel sinnvoll?“. 5 2 Begriffserklärungen Neben der operativen Tumortherapie stehen den ÄrztInnen und PatientInnen auch noch Therapien wie die Chemotherapie und die Bestrahlung als alleinige oder supportive Behandlungsmöglichkeiten im Kampf gegen bösartige Erkrankungen zur Verfügung. 2.1 Chemotherapie Die Chemotherapie ist eine Form der medikamentösen Therapie von malignen Tumoren. Der Begriff „Chemotherapie“ entstand bereits 1908 und war ursprünglich ein Überbegriff für die Behandlung von Infektionskrankheiten mit chemischen Substanzen. Heutzutage verwendet der Großteil der ExpertInnen diesen Begriff im Zusammenhang mit der Behandlung von Malignomen mit Zytostatika (Margulies, Kroner et al. 2011, S. 137-138). „Zytostatika sind Substanzen, die das Zellwachstum beeinflussen. Insbesondere können sie die Zellteilung verhindern, verzögern, und/oder Zellen in Apoptose (programmierter Zelltod) führen. Zytostatika wirken nur auf aktive, sich teilende Zellen. Die Rationale für den Einsatz von zytostatischen Substanzen in der onkologischen Therapie beruht darauf, dass Tumorzellen eine höhere Zellteilungsrate haben als normale Zellen.“ (Zeimet, Frank et al. 2007, S.1) Allgemein lassen sich folgende Anwendungsbereiche der Chemotherapie unterscheiden: kurative Chemotherapie: um eine Heilung zu erzielen adjuvante Chemotherapie: Nach einer Operation, um die Bildung von Metastasen oder einen Rückfall der Tumorerkrankung zu verhindern. neoadjuvante Chemotherapie: Vor einer Operation, um das Ausmaß derselben zu verringern und das Resultat zu verbessern. palliative Chemotherapie: um im fortgeschrittenen Stadium Schmerzen und Beschwerden zu lindern (Petru, Petru et al. 2010, S. 13) 6 2.2 Strahlentherapie Aufgabe der Strahlentherapie – oder Radioonkologie ist es, maligne Tumoren mithilfe ionisierender Strahlen zu bekämpfen. Dies kann allein durch eine Radiotherapie oder in Kombination mit anderen Therapien durchgeführt werden. Die ersten Erfolge mit dieser Art von Behandlung konnten in Schweden bereits 1899 bei zwei HautkrebspatientInnen erzielt werden. Doch erst der Einsatz von Hochvoltgeräten und die Entwicklung der exakten Dosismessung machten eine exakte Strahlenbehandlung mit geringeren Nebenwirkungen möglich (Margulies, Kroner et al. 2011, S. 114). Eine Strahlentherapie kann mit folgenden Methoden erfolgen: Teletherapie: Dabei handelt es sich um die häufigste und wichtigste Form und bedeutet, dass die Tumorregion von außen (perkutan) bestrahlt wird und die Strahlungsquelle üblicherweise 80-120 cm von der Körperoberfläche entfernt ist. Brachytherapie: Dabei werden Radionuklide direkt an Organen oder Geweben appliziert. Diese Art der Strahlentherapie wird daher auch als Kurzdistanztherapie bezeichnet (Margulies, Kroner et al. 2011, S. 115). Wie bei der Chemotherapie gibt es auch bei der Radiotherapie unterschiedliche Anwendungsbereiche: Kurative Radiotherapie nicht-operierter Tumoren: „Eine Reihe von Tumorerkrankungen ist auch ohne Operation durch eine Strahlentherapie zu einem hohen Prozentsatz heilbar. Es handelt sich um Tumoren mit lokaler Wachstumstendenz und einer geringen Neigung zur Fernmetastasierung. Im Einzelfall ist jedoch die Vorhersage einer Heilung unsicher. Es gelten vielmehr statistische Wahrscheinlichkeiten […].“ (Margulies, Kroner et al. 2011, S. 126) Adjuvante Radiotherapie: Dabei wird im Anschluss an eine radikale Operation eine zusätzliche Bestrahlung eines Tumorgebietes durchgeführt um mikroskopische Tumorreste zu vernichten. Dadurch kann die Häufigkeit von Lokalrezidiven gesenkt und die Heilungsrate gegenüber einer alleinigen Operation um das Vielfache erhöht werden (Margulies, Kroner et al. 2011, S. 126). 7 Palliative Radiotherapie: Palliative Bestrahlung kann zur wesentlichen Verbesserung der Lebensqualität beitragen. Im Vergleich zur kurativen Strahlentherapie ist die Dauer der Behandlung kürzer und die Gesamtstrahlendosis geringer und somit kaum mit Nebenwirkungen verbunden (Margulies, Kroner et al. 2011, S. 126). Kombinierte Radio-Chemotherapie: Je nach Indikation und nach sorgfältigem Abwiegen der Vor- und Nachteile für den Patienten/die Patientin kann die Kombination sequentiell oder gleichzeitig zur Anwendung kommen (Margulies, Kroner et al. 2011, S. 127). 2.3 Antikörpertherapie „Monoklonale Antikörper sind in Zellkulturen biotechnisch hergestellte Immunglobuline, die nur mit einem einzigen, definierten Antigen reagieren. Viele Krebszellen zeigen auf ihrer Oberfläche charakteristische Proteine, die als Antigene zu betrachten sind. Diese Antigene sind allerdings meist nicht tumorspezifisch […]. Eine Antikörpertherapie kommt vor allem dann in Frage, wenn die Tumorzellen das Antigen in viel höherer Konzentration als die normalen Zellen aufweisen.“ (Margulies, Kroner et al. 2011, S. 147). „Antikörper können mit radioaktiven Substanzen oder mit Toxinen gekoppelt werden.“ (Margulies, Kroner et al. 2011, S. 148) 3 Entstehung maligner Tumoren 3.1 Einteilung Tumor: Unter einem Tumor versteht sich jegliche Schwellung eines Gewebes ohne die Beschreibung einer Ursache. Neoplasie: Darunter versteht man eine Gewebeneubildung, sprich ein vermehrtes Zellwachstum durch gestörte Wachstumskontrolle und -regulation. Dignität: Dies beschreibt das biologische Verhalten eines Tumors – sprich, ob eine Gutartigkeit oder eine Bösartigkeit des Tumors vorliegt. Gutartige (benigne) Tumoren sind meist lokal begrenzt, wachsen nicht invasiv und metastasieren nicht. Allerdings können sie durch stetige Größenzunahme benachbarte Strukturen verdrängen und dadurch schädigen. Im Einzelfall kann ein benigner Tumor in einen malignen Tumor übergehen (Margulies, Kroner et al. 2011, S. 4). 8 3.2 Kriterien für Malignität unkontrollierte Zellproliferation invasives und infiltratives Wachstum Fähigkeit, in andere Organe zu metastasieren gestörte Zelldifferenzierung (Margulies, Kroner et al. 2011, S. 4) 3.3 Ursachen für die Entstehung maligner Tumoren „Die Entstehung maligner Tumoren geschieht in einem Mehrschrittprozess, wobei jeder Schritt hin zur malignen Zelle einer weiteren Veränderung des Erbgutes (Mutation) entspricht. Dabei durchlaufen Zellen verschiedene prämaligne Stadien und erwerben dabei weitere Mutationen, bis schließlich eine Zelle mit allen malignen Eigenschaften entsteht. […] Die Schritte der Karzinomentstehung sind durch mehrere, charakteristische Mutationen von wachstumsregulierenden Genen definiert. Typischerweise überwiegt dabei die Zahl der inaktivierten Tumorsuppressorgene deutlich die Zahl der aktivierten Onkogene […].“ (Margulies, Kroner et al. 2011, S. 18) In der Regel dauert es Jahre bis Jahrzehnte von der ersten Mutation in einer Zelle bis zur Entstehung eines malignen Tumors. Bei sehr aggressiven Karzinomen kann sich dieser Prozess in wenigen Monaten abspielen (Margulies, Kroner et al. 2011, S. 18). 9 Abbildung 1: Mutation und die Entstehung maligner Tumoren (Margulies, Kroner et al. 2011, S. 20) Die Ursachen für diese Zellmutationen können vielfältig sein: sie können angeboren, im Laufe des Lebens erworben oder ein spontaner Fehler in der Zellteilung sein. Weiters können innere und äußere Einflüsse den auslösenden Faktor für eine Mutation darstellen (Margulies, Kroner et al. 2011, S. 19). 10 4 Risikofaktoren Es gibt eine Reihe von exogenen und endogenen Risikofaktoren, welche krebsauslösende Erbgutveränderungen begünstigen. Viele von ihnen sind heutzutage bekannt und wissenschaftlich belegt. 4.1 Nicht beeinflussbare Risikofaktoren Alter: Obwohl der Krebs in jedem Alter auftreten kann, ist das Alter einer der wichtigsten Risikofaktoren, da in der Regel viele Jahre zwischen der Exposition mit dem Karzinogen und dem Ausbruch der Erkrankung liegen. Eine Ausnahme bilden hier die ersten fünf Lebensjahre, in welchen das Krebsrisiko relativ hoch ist. Geschlecht: Wie beim Alter, besteht auch beim Geschlecht eine unterschiedlich hohe Inzidenzrate bezüglich Krebserkrankungen. Genetik: Der genetisch bedingte Anteil unter den Risikofaktoren für eine Krebsentstehung wird auf ca. 5-10% geschätzt. Diese vererbten Gendefekte betreffen meist zellwachstumssteuernde Gene bzw. Tumorsuppressorgene oder jene, die als DNA-Reparaturgene funktionieren (Margulies, Kroner et al. 2011, S. 4547). 4.2 Beeinflussbare Risikofaktoren Etwa 40 % aller krebsbedingten Todesfälle sind auf vermeidbare Risikofaktoren zurückzuführen. Rauchen: Das Inhalieren von Tabakrauch verursacht neben tödlichen Herz-KreislaufErkrankungen auch Krebskrankheiten unterschiedlichster Lokalisationen, wie zum Beispiel der Mundhöhle, des Rachens, der Speiseröhre, der Niere, der Lunge oder der Bauchspeicheldrüse. Laut einer Schätzung der WHO ist der Konsum von Tabakrauch für etwa 17% aller Todesfälle verantwortlich (Margulies, Kroner et al. 2011, S. 48). Entgegen weit verbreiteter Annahmen sind auch E-Zigaretten und Light-Zigaretten keineswegs harmlos. In elektronischen Zigaretten ist zwar kein Teer, aber durchaus krebserregende Stoffe und Nikotin enthalten und der Dampf kann die Atemwege reizen, weshalb ExpertInnen von deren Konsum abraten. Light-Zigaretten haben einen reduzierten Nikotingehalt, aber dieselbe Menge krebserregender Stoffe im 11 Vergleich zu „normalen“ Zigaretten. Außerdem kann der reduzierte Nikotingehalt dazu führen, dass Raucher ihren Zigarettenkonsum erhöhen, um die Nikotinsucht zu stillen (Majorczyk 2014, S. 21). Ernährung: Die Ernährungsgewohnheiten haben einen wesentlichen Einfluss auf das Risiko bzw. die Prävention für die Entstehung von Krebserkrankungen in bestimmten Körperregionen/-organen. Laut der Untersuchung des World Cancer Research Fund und dem daraus resultierenden Expertenbericht von 2007 gilt als erwiesen, dass es einen Zusammenhang gibt zwischen einem geringen Obst- und Gemüseverzehr und einem deutlich erhöhten Krebserkrankungsrisiko. Weiters wurden Wahrscheinlichkeiten für die krebsfördernde Wirkung von rotem Fleisch und die krebsrisikosenkende Wirkung von Ballaststoffen, vor allem bezüglich Darmkrebs, beschrieben (Margulies, Kroner et al. 2011, S. 48-49). Tabelle 1: Beispiele für risikoerhöhende Effekte von Ernährung auf einzelne Krebsarten (Margulies, Kroner et al. 2011, S. 49) Tabelle 2: Beispiele für risikosenkende Effekte von Ernährung auf einzelne Krebsarten (Margulies, Kroner et al. 2011, S. 49) 12 Alkohol: Nicht nur der Alkoholkonsum an sich erhöht das Krebserkrankungsrisiko, er verstärkt auch die krebserregende Wirkung von Nikotin. Die Todesfälle durch alkoholinduzierte Krebserkrankungen werden mit 3% angegeben. Besonders betroffen sind die Leber, der Darm, die Brust, die Mundhöhle (und Rachen), die Speiseröhre und der Kehlkopf (Margulies, Kroner et al. 2011, S. 50). Übergewicht und mangelnde körperliche Bewegung: „Übergewicht erhöht das Krebsrisiko für eine ganze Reihe von Tumoren wie Brustkrebs in der Menopause, Dickdarm-, Pankreas-, Gallenblasen-, Endometrium- und Nierenzellkarzinom. Einen schützenden Effekt hat dagegen körperliche Aktivität - besonders ausgeprägt im Hinblick auf Dickdarmkrebs, aber auch auf postmenopausalen Brustkrebs und Endometriumkarzinom.“ (Margulies, Kroner et al. 2011, S. 50) Strahlen: „[…] Von 2 Strahlenarten - den ionisierenden und den ultravioletten Strahlen - ist eine krebsauslösende Wirkung mit Sicherheit nachgewiesen. Von anderen elektromagnetischen Strahlen (Radiowellen, Mikrowellen, elektrische und magnetische Felder in der Umgebung von Radiostationen und Funktelefonen) ist eine krebsauslösende Wirkung nicht belegt.“ (Margulies, Kroner et al. 2011, S. 50) Belastungen durch Umweltschadstoffe: Wie groß der kausale Zusammenhang zwischen Umweltschadstoffen in Wasser, Erde und Luft ist, kann man äußerst schwer nachweisen da diese nur in geringen Mengen in den Elementen enthalten sind und so eine karzinogene Wirkung nicht bewiesen werden kann (Margulies, Kroner et al. 2011, S. 52). 13 Infektionen: Auch wenn schon seit langer Zeit bekannt ist, dass Viren, Parasiten und Bakterien Krebs verursachen können, ist der krebsauslösende Mechanismus noch weitgehend ungeklärt. Weltweit werden Schätzungen zufolge 18% aller Krebskrankheiten durch Viren, Bakterien oder Parasiten verursacht (Margulies, Kroner et al. 2011, S. 52). Tabelle 3: Infektionskrankheiten als Risikofaktoren für maligne Tumoren (Margulies, Kroner et al. 2011, S. 52) 14 Sexualität, hormonelle Faktoren und Fortpflanzung: Betroffen sind vor allem hormonabhängige Gewebe, wie die Brustdrüse oder die Gebärmutter. Verschiedene Faktoren können risikoerhöhend oder –senkend auf eine Krebsentstehung wirken, wie in Tabelle 4 beschrieben. Zum Beispiel kann eine frühe erste Schwangerschaft einen schützenden Effekt gegen Brustkrebs haben. Da aber in den Industrieländern das Geburtenalter steigt bzw. die Geburtenrate sinkt, nehmen Forscher an, dass in diesen Gebieten die Brustkrebsrate in den nächsten Jahren weiter steigen wird (Margulies, Kroner et al. 2011, S. 53). Tabelle 4: Sexuelle Risikofaktoren für die Entwicklung weiblicher Tumoren (Margulies, Kroner et al. 2011, S. 53) 15 Belastungen bei der Arbeit: „Schadstoffexpositionen am Arbeitsplatz gehörten mit zu den ersten identifizierten Krebsursachen. […] 5% der Krebstodesfälle werden durch die berufsbedingte Einwirkung von Karzinogenen verursacht. Das am häufigsten betroffene Zielorgan ist die Lunge. 7-12% aller Lungenkrebserkrankungen sind durch Expositionen am Arbeitsplatz verursacht.“ (Margulies, Kroner et al. 2011, S. 51) Tabelle 5: Krebserzeugende Substanzen und Krebserkrankungen (Margulies, Kroner et al. 2011, S. 51) 16 Medikamente: Einige Medikamente haben nicht nur eine heilenden Wirkung, sondern können auch krebserregend sein. Dazu gehören in erster Linie Zytostatika und Hormonersatzpräparate, aber auch die Langzeiteinnahme von bestimmten Analgetika und Immunsuppressiva kann eine Krebsentstehung fördern, wie in Tabelle 6 gezeigt. Wissenschafter vermuten, dass die Zahl der karzinogen wirkenden Medikamente in Zukunft noch weiter ansteigen wird (Margulies, Kroner et al. 2011, S. 53). Tabelle 6: Beispiele an Medikamenten mit erhöhtem Krebsrisiko (Margulies, Kroner et al. 2011, S. 53) 17 5 Arten der Chemotherapie 5.1 Systemische Chemotherapie „Ob ein Medikament sowohl intravenös als auch oral verabreicht werden kann, hängt in erster Linie von seiner chemischen Struktur ab: Kleine Moleküle […] werden in der Regel im Darm gut resorbiert und können deshalb oral verabreicht werden. Große Moleküle dagegen werden zum Teil im Darm verdaut und dadurch unwirksam […] oder nicht resorbiert. […] Bei einigen klassischen Zytostatika […] sind sowohl die orale als auch die intravenöse Applikation möglich.“ (Margulies, Kroner et al. 2011, S. 171). Die orale Gabe hat Vorteile, wie das Ersparen einer Venenpunktion und die Unabhängigkeit von einer medizinischen Einrichtung. Doch auch die Nachteile dieser Verabreichungsform sind nicht zu unterschätzen, wie zum Beispiel die Abhängigkeit der Resorption von der Funktion des Magen-Darm-Traktes und die Compliance der PatientInnen. Daher muss die Darreichungsart für jede/n Patienten/in individuell ausgewählt werden (Margulies, Kroner et al. 2011, S. 171). 5.2 Regionale Chemotherapie Bei einer regionalen Chemotherapie wird der Wirkstoff direkt in das Blutgefäß verabreicht, welches die befallene Region versorgt Wirkstoffkonzentration zu erreichen. Indikationen um dafür lokal sind eine zum hohe Beispiel Primärtumoren, lokalisierte Metastasen oder Tumoren, welche schlecht auf eine systemische Therapie ansprechen (Margulies, Kroner et al. 2011, S. 171). 5.3 Chemoembolisation „Bei der Chemoembolisation wird gleichzeitig mit der lokalen Infusion eines Zytostatikums das den Tumor versorgende Gefäß embolisiert und der Tumor so seiner Gefäßversorgung beraubt.“ (Margulies, Kroner et al. 2011, S. 172) 5.4 Intrakavitäre Chemotherapie Bestimmte Indikationsstellungen verlangen eine Zytostatikaverabreichung direkt in eine Körperhöhle. Intrathekale Chemotherapie: Dabei werden Zytostatika direkt in den Liquorraum appliziert um so die Blut-Liquor-Schranke zu umgehen (Margulies, Kroner et al. 2011, S. 172). 18 Intraperitoneale Chemotherapie: Die Instillation von Zytostatika direkt in die Bauchhöhle eignet sich nur bei sehr kleinen Tumorknötchen, da das Medikament nur wenige Millimeter tief in das Tumorgewebe eindringt (Margulies, Kroner et al. 2011, S. 173). Intravesikale Chemotherapie: Dabei handelt es sich um das Einbringen des Zytostatikums mittels Blasenkatheter in die Harnblase. Dies wird neben einer Operation bei Frühformen des Blasenkarzinoms durchgeführt (Margulies, Kroner et al. 2011, S. 173). Intrapleurale/intraperikardiale Chemotherapie: „Die Instillation von Zytostatika in den Pleura- oder Perikardraum wird praktisch nur zur symptomatischen Behandlung von rezidivierenden malignen Ergüssen durchgeführt. Ziel ist nicht die Behandlung des Tumors, sondern die Unterdrückung der Ergussbildung. Zytostatika werden deshalb bei dieser Indikation im Allgemeinen nicht zur Zerstörung von Tumorzellen eingesetzt, sondern zur Auslösung einer unspezifischen Entzündung, die ihrerseits zur Verklebung der Perikard- bzw. Pleurablätter führt. Es werden deshalb neben Zytostatika zahlreiche andere entzündungsauslösende Substanzen angewendet.“ (Margulies, Kroner et al. 2011, S. 173) 5.5 Transdermale Chemotherapie Diese Art der Chemotherapie ist limitiert bei oberflächlichen malignen Hautveränderungen angezeigt. Durch den lokalen Einsatz fallen systemische Nebenwirkungen weg (Margulies, Kroner et al. 2011, S. 173). 19 6 Komplementäre und alternative Therapien in der Onkologie 6.1 Begriffsdefinitionen Konventionelle Medizin: „Auch Schulmedizin genannt. Sie bemüht sich, ihre Konzepte durch eine naturwissenschaftlich-statistische Methodologie zu begründen. Aus ihr ist die sog. >>evidence based medicine<< entstanden.“ (Margulies, Kroner et al. 2011, S. 187) Komplementärmedizin: „Therapien und Methoden, die die konventionelle Medizin ergänzen sollen. In der Onkologie typischerweise mit supportiven Zielsetzungen wie Besserung der Symptomkontrolle und Lebensqualität.“ (Margulies, Kroner et al. 2011, S. 187) Alternativmedizin: „Therapien und Methoden, die anstelle der konventionellen Medizin propagiert werden. Betrachtet sich als Alternative zur konventionellen Medizin. Ob eine Therapie nun als alternativ oder komplementär eingestuft wird, hängt auch vom Verhalten von TherapeutIn und PatientIn ab.“ (Margulies, Kroner et al. 2011, S. 187) Integrative Medizin: „Integration von Komplementärmedizin und konventioneller Medizin im Rahmen eines Gesamtkonzeptes. Integrative Medizin wird an den meisten amerikanischen Krebszentren (>>comprehensive cancer centers<<) angeboten und wird zunehmend in Europa bekannt.“ (Margulies, Kroner et al. 2011, S. 187) 6.2 Kategorien von Komplementär- und Alternativmedizin nach dem National Center for Complementary and Alternative Medicine „Das amerikanische NCCAM (National Center for Complementary and Alternative Medicine) hat die Komplementär- und Alternativmedizin zur Vereinfachung in fünf Kategorien eingeteilt: ganzheitliche medizinische Systeme, Psyche-Körper- Therapien, biologische Therapien, Körpertherapien und energetische Therapien.“ (Margulies, Kroner et al. 2011, S. 189) 20 Tabelle 7: Einteilung von Komplementär- und Alternativmedizin gemäß dem NCCAM (Margulies, Kroner et al. 2011, S. 189) Tabelle 8: Meist angewandte Komplementärmedizin (KM), nach Land/Kontinent (Margulies, Kroner et al. 2011, S. 189) 6.3 Risiken von Komplementär- und Alternativmedizin Bei KAM steht in den meisten Fällen keine wissenschaftliche Evidenz im Hintergrund. Ein Risiko für PatientInnen besteht dann, wenn der Anbieter, wie so oft, die konventionelle medizinische Therapie als falsch und gefährlich bezeichnet und somit bei Nichtwirksamkeit der KAM der Zeitpunkt für eine kurative oder palliative Behandlung verabsäumt wird. 21 Weiters kann es bei Kombination aus einer konventionellen Therapie und einer komplementären Therapie zu Wechselwirkungen kommen, was eine Rücksprache mit dem/r behandelnden Arzt/Ärztin unumgänglich macht (Margulies, Kroner et al. 2011, S. 193). Tabelle 9: Mögliche Wechselwirkungen und Nebenwirkungen von komplementären Substanzen (Margulies, Kroner et al. 2011, S. 194) „Charakteristisch v.a. für die Alternativmedizin ist die oft erhebliche Diskrepanz zwischen dem Erfolgsanspruch und den Erfolgsbelegen. Paradoxerweise ist es gerade die maßlos übertriebene Erfolgsmeldung, die in aussichtslosen Fällen bei Betroffenen Hoffnung aufkeimen lässt. Dies empfinden viele PatientInnen als vorübergehende Hilfe, auch wenn später die Verzweiflung umso größer sein kann.“ (Margulies, Kroner et al. 2011, S. 195) 22 7 Mammakarzinom bei Frauen 7.1 Brusterhaltende Operation „Heutzutage gilt die brusterhaltende Therapie (BET) mit anschließender Bestrahlung als Standard.“ (Majorczyk 2014, S. 171) Voraussetzung für die Durchführung der BET sind örtliche Begrenzung des Tumors, ein im Verhältnis zum verbleibenden Brustgewebe kleiner Tumor, die Begrenzung des Tumors auf einen Quadranten, mehrere kleine Tumoren im selben Quadranten oder dass eine abgegrenzte Brustkrebsvorstufe vorliegt (Friedrichs, Oellerich et al. 2014, S. 75). „Häufig wird vor der BET eine Chemotherapie verabreicht, um den Tumor zu verkleinern. […] Die Lymphknoten werden bei der Operation je nach Befall entnommen.“ (Majorczyk 2014, S. 171) 7.2 Mastektomie und Brustrekonstruktion „Die vollständige Entfernung der Brust (Mastektomie) ist notwendig, wenn sich Krebsherde in verschiedenen Bereichen der Brust befinden oder der Tumor sehr groß ist. Je nach weiterer Therapie kann auf Wunsch der Patientin ein Wiederaufbau gleichzeitig oder zu einem späteren Zeitpunkt durchgeführt werden. Sind die Achsellymphknoten unauffällig, so wird die Wächterlymphknotenentfernung gewähltdas heißt, nur der nächstgelegene Lymphknoten wird entnommen und auf Tumorzellen hin untersucht. Ansonsten erfolgt die Entfernung aller Achsellymphknoten.“ (Majorczyk 2014, S. 171) 7.3 Lymphknotenentfernung Der/die Wächter- oder Sentinel-Lymphknoten wird/werden vor der Operation mithilfe einer radioaktiven Flüssigkeit markiert, wodurch der/die Operateur/In diesen während der Operation leichter lokalisieren kann. Anschließend wird der Lymphknoten vom Pathologen untersucht. Befinden sich darin Krebszellen, wird eine ausgedehnte axilläre Lymphadenektomie durchgeführt. 23 7.4 Nachsorge Eine ärztliche Untersuchung findet in den ersten drei Jahren alle drei Monate, im vierten und fünften Jahr alle sechs Monate und ab dem sechsten Jahr einmal jährlich statt. Einmal jährlich werden eine Mammographie und eine gynäkologische Untersuchung empfohlen (https://www.gesundheit.gv.at/Portal.Node/ghp/public/ content/Rehabilitation_Brustkrebs_LN1.html#headline21, 15.7.2016). 7.5 Breast Care Nurse „Zunehmend etabliert sich im Therapieprozess von Frauen mit Brustkrebs die Einbeziehung einer Breast Care Nurse (auf die Information, Beratung und Anleitung von Frauen mit Brustkrebs spezialisierte Pflegende) mit dem Ziel, Betroffene bei der Entscheidungsfindung sowie bei der Bewältigung der Krankheit und der Nebenwirkungen der Therapien zu unterstützen. Breast Care Nurses und/oder Pflegende haben in der postoperativen Phase die Aufgabe, Patientinnen in der Anpassung an das veränderte Körperbild und in der Bewältigung von Krankheit und Therapie zu unterstützen.“ (Margulies, Kroner et al. 2011, S. 574) 8 Stomapflege Stoma oder Ostomie bezeichnet eine künstlich geschaffene Verbindung zwischen einem Hohlorgan und der Körperoberfläche (Margulies, Kroner et al. 2011, S. 588). 8.1 Stoma des Darms 8.1.1 Definition und Indikationen „Ziel der Stomaanlage ist die Ausleitung des Darminhalts. […] Die Anlage eines Stomas ist bei Tumorpatienten […] in den folgenden Situationen zwingend und unvermeidbar: Entlastung des Darms bei akutem Verschluss, Ausleitung des Darms bei intraabdominellen septischen Komplikationen, Inkontinenz […] (z.B. nach Strahlentherapie bei Rektum- oder Analkarzinom), Verlust des natürlichen Ausgangs nach resezierender Operation (Rektumamputation). 24 Die Stomaanlage kann bei bestimmten Erkrankungen und operativen Eingriffen im Sinne einer vorübergehenden Ausschaltung erkrankter oder operativ behandelter Darmabschnitte hilfreich sein […].“(Margulies, Kroner et al. 2011, S. 588) 8.1.2 Stomalokalisation und Stomaformen „Da mitunter beachtliche Abstände zwischen Bauchraum und Hautniveau bei der Anlage von Stomata überwunden werden müssen, eignen sich alle gut beweglichen Darmabschnitte zur Stomaanlage: Ileum, Colon transversum, Colon descendens und Sigma. Davon abhängig ist die Benennung: Ileostomie (im terminalen Ileum platziertes Stoma), Kolostomie (im Dickdarm lokalisiertes Stoma). Die Zusatzbezeichnung zur Form - endständig oder doppelläufig - beschreibt die Anzahl der Öffnungen eines einzelnen Stomas. Sie ist abhängig vom Behandlungskonzept: Endständige Stomata (eine Öffnung = ein Lumen) werden in der Regel angelegt, wenn es sich um ein definitives Stoma handelt und eine Rückverlagerung nicht mehr geplant oder möglich ist […]. Doppelläufige Stomata (zwei Lumen) werden in der Regel in Situationen angelegt, in denen ein operativer Wiederanschluss vorübergehend ausgeschalteter Darmanteile geplant ist oder in denen eine Entlastung ausgeschalteter Darmanteile nach 2 Richtungen (Stoma und Via naturalis) erforderlich ist.“ (Margulies, Kroner et al. 2011, S. 588-589) Die Form des sichtbaren Anteils des Stomas wird nach der Stuhlfestigkeit gewählt. Wie in Abbildung 2 dargestellt, erfolgt die Anlage eines Kolostomas knapp über Hautniveau (a), da der geförderte Stuhl weniger aggressiv und dickflüssiger ist. Ein Ileostoma hingegen wird prominent angelegt (b), da Dünndarmstuhl dünnflüssig und durch seine Reichhaltigkeit an Verdauungsenzymen aggressiv ist. Diese hervorstehende Anlage erleichtert die Versorgung und kann Hautreizungen vorbeugen (Margulies, Kroner et al. 2011, S. 589). 25 Abbildung 2: Anlage eines planen endständigen Kolostomas (a) und eines prominenten endständigen Ileostomas (b) durch sämtliche Schichten der Bauchdecke (Margulies, Kroner et al. 2011, S. 590) 8.1.3 Stomaplatzierung „Für eine optimale Selbstversorgung ist die künftige Lage des Stomas von entscheidender Bedeutung. Da intraoperativ am liegenden, überstreckten Patienten die Hautfalten und Fettpolster nicht zuverlässig beurteilbar sind, muss die richtige Stomaplatzierung vorher am stehenden, sitzenden und sich bewegenden Patienten festgelegt werden. Damit sich der Patient später selbst versorgen kann, muss er bestätigen, dass er die vom Chirurgen und Stomatherapeuten vorgeschlagene Stomaplatzierung an seinem Bauch sehen kann.“ (Margulies, Kroner et al. 2011, S. 589-590) 8.2 Harnableitendes Stoma „Durch Änderung und Verbesserung der medizinischen Behandlungsmöglichkeiten sinkt die Notwendigkeit zur Anlage von Urostomata seit Jahren. Indikationen bestehen bei Verlust (z.B. Zystektomie wegen eines Blasenkarzinoms) oder irreversibler Schädigungen (z.B. nach Strahlentherapie der Blase) der unteren harnableitenden Wege (Blase, Harnröhre).“ (Margulies, Kroner et al. 2011, S. 591) 26 8.3 Information von PatientInnen und Angehörigen Es ist wichtig, PatientInnen und bei Bedarf pflegende Angehörige so schnell wie möglich in die Stomaversorgung mit einzubeziehen. Neben der Handhabung des Stomasystems ist es außerdem von Bedeutung, Informationen über Ernährung und Medikamenteneinnahme bei einem liegenden Stoma zu geben. Weiters ist es für das Funktionieren einer optimalen Versorgung zuhause unabdingbar, dass die Betroffenen über mögliche Komplikationen, deren Anzeichen und mögliche prophylaktische Interventionen (Tabelle 10) Bescheid wissen. Tabelle 10: Die 4 häufigsten Stomakomplikationen (Margulies, Kroner et al. 2011, S. 600) 27 9 Präventionsmaßnahmen 9.1 Nationales Krebsvorsorgeprogramm des BMG Das nationale Krebsrahmenprogramm 2014 wurde vom Bundesministerium für Gesundheit beauftragt und die Erstellung erfolgte durch den Onkologie-Beirat einem multiprofessionellen und interdisziplinären Expertengremium, welches den/die Bundesminister/in für Gesundheit zum Thema Krebsprävention und -versorgung berät. Die Expertengruppe definierte - basierend auf einer IST-Stand-Analyse zur aktuellen Situation der Onkologie in Österreich - Ziele, Maßnahmen und Messgrößen. Neben den Themen Prävention, Diagnostik, Behandlung und Forschung wurden auch Bereiche mit eingeschlossen, welche sonst eher weniger im Mittelpunkt stehen, wie die Psychoonkologie, die Palliativ- und Hospizversorgung, die onkologische Rehabilitation und die Epidemiologie, welche auf den Daten der Statistik Austria aufbaute. Für die Zielgruppen „Kinder und Jugendliche“ und „Ältere Menschen“ wurden eigene Ziele definiert, da deren Versorgung eine besondere Herausforderung darstellt. Für die einzelnen zu behandelnden Bereiche wurden nicht nur operative Ziele definiert, welche der Verhaltensprävention zuzuschreiben sind, sondern es wurde auch auf verhältnispräventionsassoziierte Ziele großer Wert gelegt. Dies verdeutlicht die Notwendigkeit, nach dem „Health in all Policies“-Ansatz zu operieren und alle dem Thema Gesundheit und Prävention verschriebenen Bereiche in deren Umsetzung mit einzubeziehen. Ausschlaggebend für die Argumentation gegenüber Gesundheitspolitik und Entscheidungsträgern ist der Bereich der Epidemiologie, welcher nicht nur ISTStand-Analysen zulässt, sondern wichtige Aussagen über zukünftige Entwicklungen tätigen und somit Bereiche beleuchten kann, welche künftig mehr Bedeutung bekommen werden, wie zum Beispiel die Palliativ- und Hospizversorgung. Deswegen sind die Genauigkeit und der Ausbau der Datensammlung auch ein besonders wichtiger Aspekt des nationalen Krebsrahmenprogramms, da dadurch die Aufmerksamkeit konkret auf Bereiche gelenkt werden kann, welche ansonsten vielleicht eher stiefmütterlich behandelt werden (http://www.bmgf.gv.at/cms/home/ attachments/2/7/0/CH1480/CMS1412233312313/krebsrahmenprogramm.pdf, 28.7.2016). 28 9.2 Krebsvorsorgeuntersuchungen Die Vorsorgeuntersuchung hat zum einen das Ziel, gesundheitliche Risikofaktoren zu vermeiden und zum anderen, Krankheiten frühzeitig zu erkennen, wobei der Schwerpunkt auf der Prävention, Früherkennung und Senkung der Mortalität von Herz-Kreislauf- und Krebserkrankungen liegt. Krebsvorsorge für Frauen: Krebsabstrich: Einmal jährlich sollte ab dem 18. Lebensjahr ein Krebsabstrich bei einem/einer Gynäkologen/in durchgeführt werden. Tastuntersuchung der Brust durch den Arzt Selbstuntersuchung der Brust Mammografie: Hierdurch können nicht tastbare kleine Tumore festgestellt werden. Seit 2014 erhalten Frauen zwischen 45 und 69 Jahren im Rahmen des nationalen Brustkrebs-Früherkennungsprogramms alle zwei Jahre eine Einladung. Frauen zwischen 40 und 44 Jahren und ab dem 71. Lebensjahr können sich für eine Einladung registrieren und erhalten diese folglich auch alle zwei Jahre automatisch zugesandt. Okkulttest: der Test auf nicht sichtbare Blutbeimengungen im Stuhl sollte ab dem 41. Lebensjahr einmal jährlich durchgeführt werden. Koloskopie: Eine Darmspiegelung sollte ab dem 51. Lebensjahr alle 7-10 Jahre durchgeführt werden, um etwaige Veränderungen der Darmschleimhaut zu erkennen und zu untersuchen. Hautselbstuntersuchung: Diese sollte zwei Mal im Jahr, jeweils vor und nach dem Sommer, durchgeführt werden. Ergänzend dazu sollte einmal jährlich ein/e Dermatologe/in aufgesucht werden (https://www.krebshilfe.net/ information/ krebs-vorsorge/frauen/, 26.7.2016). Krebsvorsorge für Männer: Selbstuntersuchung der Hoden: Dies ist ab dem 21. Lebensjahr einmal im Monat empfohlen. Prostatauntersuchung durch den Arzt: Ab dem 46. Lebensjahr sollte die Prostatakrebsfrüherkennungsuntersuchung regelmäßig durchgeführt werden. 29 Harnuntersuchung: Die Untersuchung auf Blut im Harn sollte zur Blasenkrebsprävention regelmäßig ab dem 41. Lebensjahr gemacht werden. Okkulttest: Der Test auf nicht sichtbare Blutbeimengungen im Stuhl sollte ab dem 41. Lebensjahr einmal jährlich durchgeführt werden. Koloskopie: Eine Darmspiegelung sollte ab dem 51. Lebensjahr alle 7-10 Jahre durchgeführt werden, um etwaige Veränderungen der Darmschleimhaut zu erkennen und zu untersuchen. Hautselbstuntersuchung: Diese sollte zwei Mal im Jahr, jeweils vor und nach dem Sommer, durchgeführt werden. Ergänzend dazu sollte einmal jährlich ein Dermatologe aufgesucht werden (https://www.krebshilfe.net/information/ krebs-vorsorge/maenner/, 26.7.2016). Impfung gegen HPV: Seit Herbst 2014 können Eltern ihre Kinder kostenlos im Rahmen des Schulimpfprogramms oder vergünstigt bei öffentlichen Impfstellen impfen lassen. Die kostenlose HPV-Impfung erhalten Mädchen und Buben ab dem 10. bis zum 13. Lebensjahr. Für Kinder ab dem 13. bis zum 16. Lebensjahr bieten die Bundesländer „Nachholimpfungen“ (Catch-up-HPV-Impfungen) stark vergünstigt an (http:// www.bmgf.gv.at/cms/home/attachments/4/9/5/CH1100/CMS1409912120595/ hpv_broschuere.pdf, 26.7.2016). 30 10 Diskussion Mithilfe der Literaturrecherche konnte die Forschungsfrage beantwortet werden, diese lautete „Kann einer Krebsentstehung vorgebeugt werden und sind Krebsvorsorgeuntersuchungen in der Regel sinnvoll?“. Wie im Punkt 4 beschrieben, können wir selbst sehr wohl dazu beitragen, ob sich unser persönliches Risiko für eine Krebsentstehung erhöht oder senkt. Auch wenn eine Neuentstehung von Krebs ein meist multifaktoriell bedingtes Geschehen ist und Ursachen, wie eine Zellmutation, nicht verhindert werden können, gibt es dennoch einige Faktoren, welche unserer eigenen Verantwortung und der der Gesundheitspolitik unterliegen, wie zum Beispiel das Rauchen, die körperliche Betätigung, die Ernährung oder Umweltbelastungen. Denn auch, wenn präventive Vorsorgeuntersuchungen durchaus Sinn machen, darf man die Verantwortlichkeit nicht nur in deren Hände legen. Die Vorsorgeuntersuchungen sorgen von Zeit zu Zeit für unterschiedliche Meinungen und Verunsicherung in der Bevölkerung, meist dann, wenn eine jahrelang als wichtige Prävention beworbene Untersuchung, wie die Vaginalsonographie, bei der jährlichen gynäkologischen Kontrolle plötzlich nicht mehr von der Krankenkassa bezahlt wird. Dann fragt man sich natürlich als Laie, woher nun plötzlich diese Erkenntnis kommt oder ob es sich nicht doch vielleicht um einen ausschließlich finanziellen Aspekt handelt. Doch haben sich Vorsorgeuntersuchungen allgemein und Krebsvorsorgeuntersuchungen im Speziellen seit deren Einführung in Österreich im Jahre 1974 durchaus bewährt. Denn lag davor die durchschnittliche Lebenserwartung der Frauen bei zirka 75 Jahren und die der Männer bei etwa 67 Jahren, leben Frauen heute um durchschnittlich sieben und Männer um acht Jahre länger. Auch in Bezug auf einzelne Erkrankungen konnten seither deutliche Erfolge erzielt werden. Zum Beispiel konnte seit der Einführung der PAP- Abstrichuntersuchung die Sterblichkeitsrate bei Gebärmutterhalskrebs um die Hälfte gesenkt werden. Abschließend ist zu sagen, auch wenn in den Jahren Vorsorgeuntersuchungen dazugekommen oder wieder aus dem Standardvorsorgeprogramm genommen worden sind, liegt das nicht immer nur an engeren Budgetierungen, sondern auch an 31 den Weiterentwicklungen in den medizinischen und wissenschaftlichen Erkenntnissen. 32 11 Literaturverzeichnis Friedrichs K., Oellerich H., Wessels M. (2014) Brustkrebs – Der Leitfaden durch das große Therapieangebot. 2. Auflage, Gräfe und Unzer Verlag GmbH, München. Majorczyk S. (2014) Das Handbuch gegen Krebs – Neues Wissen. Neue Hoffnung. Neue Therapien. Zabert Sandmann GmbH Verlag, München. Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Petru E., Petru C., Klocker-Kaiser U, Klocker J. (2010) Chemotherapie - Eine praxisorientierte Hilfe für PatientInnen, Angehörige und Betreuer. 3. Auflage, UniPress Verlag, Graz. Zeimet A., Frank A., Wiesbauer P., Schwarzl S. (2007) Systemische Malignomtherapie in der gynäkologischen Onkologie – Leitfaden für Ärzte und Pflegepersonen. Springer Verlag Wien New York, Wien. 33 12 Internetquellen https://www.gesundheit.gv.at/Portal.Node/ghp/public/content/ Rehabilitation_Brustkrebs_LN1.html#headline21 (15.7.2016) http://www.bmgf.gv.at/cms/home/attachments/4/9/5/CH1100/CMS1409912120595/ hpv_broschuere.pdf (26.7.2016) https://www.krebshilfe.net/information/krebs-vorsorge/maenner/ (26.7.2016) https://www.krebshilfe.net/information/krebs-vorsorge/frauen/ (26.7.2016) http://www.bmgf.gv.at/cms/home/attachments/2/7/0/CH1480/CMS1412233312313/ krebsrahmenprogramm.pdf (28.7.2016) 34 13 Abbildungsverzeichnis Abbildung 1: Mutation und die Entstehung maligner Tumoren Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Abbildung 2: Anlage eines planen endständigen Kolostomas (a) und eines prominenten endständigen Ileostomas (b) durch sämtliche Schichten der Bauchdecke Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. 35 14 Tabellenverzeichnis Tabelle 1: Beispiele für risikoerhöhende Effekte von Ernährung auf einzelne Krebsarten Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Tabelle 2: Beispiele für risikosenkende Effekte von Ernährung auf einzelne Krebsarten Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Tabelle 3: Infektionskrankheiten als Risikofaktoren für maligne Tumoren Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Tabelle 4: Sexuelle Risikofaktoren für die Entwicklung weiblicher Tumoren Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Tabelle 5: Krebserzeugende Substanzen und Krebserkrankungen Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Tabelle 6: Beispiele an Medikamenten mit erhöhtem Krebsrisiko Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. 36 Tabelle 7: Einteilung von Komplementär- und Alternativmedizin gemäß dem NCCAM Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Tabelle 8: Meist angewandte Komplementärmedizin (KM), nach Land/Kontinent Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Tabelle 9: Mögliche Wechselwirkungen und Nebenwirkungen von komplementären Substanzen Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. Tabelle 10: Die 4 häufigsten Stomakomplikationen Margulies A., Kroner Th., Gaisser A., Bachmann-Mettler I. (2011) Onkologische Krankenpflege. 5. Auflage, Springer Verlag, Berlin Heidelberg. 37