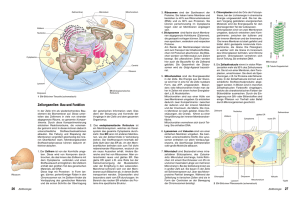
Untersuchungen zu Struktur und Funktion eines Porenproteins der
Werbung

Deckblatt Untersuchungen zu Struktur und Funktion eines Porenproteins der äußeren Chloroplastenmembran von Diplom-Biochemiker Dirk Linke aus Leonberg von der Fakultät II - Mathematik und Naturwissenschaften der Technischen Universität Berlin zur Erlangung des akademischen Grades Doktor der Naturwissenschaften -Dr. rer.nat.genehmigte Dissertation Promotionsausschuß: Vorsitzender: Prof. Dr. R. Schomäcker, TU Berlin Berichter: Priv. Doz. Dr. Petra Fromme, TU Berlin Berichter: Prof. Dr. G. H. Findenegg, TU Berlin Tag der wissenschaftlichen Aussprache: 10. Juli 2002 Berlin 2002 D 83 INHALT DECKBLATT .............................................................................................................. 0 INHALT....................................................................................................................... 1 ZUSAMMENFASSUNG.............................................................................................. 4 ABKÜRZUNGSVERZEICHNIS .................................................................................. 5 EINLEITUNG .............................................................................................................. 6 Die Erbse (Pisum Sativum)......................................................................................................6 Die Pflanzenzelle .......................................................................................................................7 Der Chloroplast.........................................................................................................................8 Aufbau.....................................................................................................................................8 Funktion des Chloroplasten in der pflanzlichen Zelle ............................................................9 Endosymbiontentheorie...........................................................................................................9 Die äußere Chloroplastenmembran......................................................................................10 Lipide der äußeren Chloroplastenmembran ..........................................................................10 Proteine der äußeren Chloroplastenmembran und ihre Funktion..........................................12 Proteinimport über die äußere und innere Chloroplastenmembran ......................................13 Proteinimport in die äußere Chloroplastenmembran ............................................................14 OEP16 ......................................................................................................................................14 Sequenzen..............................................................................................................................15 Aufbau...................................................................................................................................16 Funktion und Regulation.......................................................................................................16 Faltung von Membranproteinen ...........................................................................................19 Allgemeine strukturelle Eigenschaften von Membranproteinen...........................................19 Mechanismen der Insertion in die Membran in vivo.............................................................19 Thermodynamische Stabilität von Membranproteinen .........................................................20 Der Faltungsprozeß ...............................................................................................................21 Zielsetzung...............................................................................................................................23 MATERIAL UND METHODEN ................................................................................. 25 Überexpression von OEP16 in E.coli ....................................................................................25 Reinigung von OEP16 ............................................................................................................25 SDS-Gelelektrophorese ..........................................................................................................26 1 Faltung von OEP16 ................................................................................................................27 Liposomen .............................................................................................................................27 Detergenz-basierte Methoden für die Rekonstitution ...........................................................28 Spektroskopische Methoden..................................................................................................29 Proteinbestimmung nach Bradford........................................................................................29 Fluoreszenz-Spektroskopie ...................................................................................................30 CD-Spektroskopie .................................................................................................................30 IR-Spektroskopie...................................................................................................................31 Zeitaufgelöste Spektroskopie ................................................................................................31 Physikalisch-chemische Methoden........................................................................................32 DSC .......................................................................................................................................32 Elektronenmikroskopie..........................................................................................................33 Kristallisation..........................................................................................................................33 Probenvorbereitung ...............................................................................................................33 Kristallisationsansätze...........................................................................................................34 Messung der Röntgenbeugung ..............................................................................................35 Theoretische Strukturvorhersage .........................................................................................35 "Multiple Sequence Alignment" ...........................................................................................35 Vorhersage transmembraner Bereiche ..................................................................................36 Hydrophobe Cluster-Analyse................................................................................................37 ERGEBNISSE .......................................................................................................... 38 Von der Proteinreinigung zum gefalteten Protein (eine Einleitung) .................................38 Proteinreinigung .....................................................................................................................40 Faltungsmethoden ..................................................................................................................42 Dialyse...................................................................................................................................42 Gelfiltration ...........................................................................................................................44 Verdünnung...........................................................................................................................44 Fluoreszenzspektroskopie .....................................................................................................45 CD-Spektroskopie .................................................................................................................55 IR-Spektroskopie...................................................................................................................59 Biophysikalische Daten des gefalteten Proteins...................................................................62 DSC .......................................................................................................................................62 Zeitaufgelöste Spektroskopie ................................................................................................65 Zeitaufgelöste Fluoreszenzspektroskopie .............................................................................65 Zeitaufgelöste CD-Spektroskopie .........................................................................................67 Zeitkonstanten und Aktivierungsenergien ............................................................................68 Das Protein wird sichtbar ......................................................................................................73 Elektronenmikroskopie .........................................................................................................73 Kristallisation ........................................................................................................................75 2 Theoretische Ansätze zur Strukturaufklärung....................................................................81 Multiple Sequence Alignment...............................................................................................82 Hydropathie und Vorhersage transmembraner Segmente.....................................................83 Hydrophobe Cluster-Analyse................................................................................................85 Topologie ..............................................................................................................................87 ZUSAMMENFASSUNG DER ERGEBNISSE........................................................... 90 LITERATUR ............................................................................................................. 92 DANKSAGUNG...................................................................................................... 100 3 Zusammenfassung In der vorliegenden Arbeit wurde die biophysikalischen Eigenschaften eines kleinen Kanalproteins aus der äußeren Chloroplastenmembran der Erbse, genannt OEP16 („outer envelope Protein 16 kDa“), untersucht und ein neues Strukturmodell entwickelt, auf dessen Basis die Funktion des Proteins mit molekularbiologischen Methoden nun genauer erforscht werden kann. OEP16 ist ein Membranprotein mit ungewöhnlichen Eigenschaften. Als Protein der äußeren Chloroplastenmembran insertiert es selbständig in geeignete Lipiddoppellschichten und in Detergenzmizellen. Bei vielen eukaryontischen Membranproteinen kommt eine bakterielle Überexpression zur Gewinnung großer Proteinmengen nicht in Frage, da zumeist ein korrekter Einbau in eine Membran mangels der komplexen eukaryontischen Faltungsmaschinerie in diesen Systemen nicht gegeben ist. OEP16 hingegen erlaubt es, aufgrund seiner selbsttätigen Renaturierung das Protein ohne Rücksicht auf die native Struktur in E.coli überzuexprimieren und erst anschließend rückzufalten. Es konnte gezeigt werden, daß man große Mengen korrekt gefalteten Proteins erhalten kann, indem man in chaotropen Puffersystemen aufgereinigtes Protein durch einen Verdünnungsschritt in einen detergenzhaltigen Puffer überführt. Der Nachweis, daß sich OEP16 in Detergenzmizellen in eine native Form faltet, ist schwierig, da die Funktion des Proteins, seine Kanalaktivität, nur in einem Membransystem meßbar ist. Durch den Vergleich von Fluoreszenz- und CD-Spektren von detergenzhaltigen Proteinlösungen und dem in Liposomen eingebautem Protein (mit nachgewiesener Funktionalität) konnte gezeigt werden, daß die Struktur von OEP16 in den auf unterschiedliche Weise rekonstituierten Proben übereinstimmte. Zeitaufgelöste Messungen mit denselben spektroskopischen Methoden lieferten Daten über den Verlauf und die Geschwindigkeit der Proteinfaltung bei dieser Renaturierungsmethode, einschließlich der Aktivierungsenergien für den Prozeß. Kalorimetrische Messungen (DSC) erlaubten eine Abschätzung der Faltungsenthalpie. Durch hochauflösende CDMessungen und Infrarotspektroskopie wurde schließlich am in vitro gefalteten Protein gezeigt, daß es sich bei OPE16 entgegen bisheriger Voraussagen um ein rein α-helikales Membranprotein handelt. Dieser Befund konnte durch theoretische Methoden der Strukturbestimmung bestätigt werden. Ein neues Strukturmodell wurde erstellt. Erste vielversprechende Ansätze der Proteinkristallisation und der Elektronenmikroskopie zeigen, daß eine detaillierte Struktur von OEP16 in absehbarer Zeit erhältlich sein könnte. Dies wäre weltweit die erste hochaufgelöste Struktur eines im Reagenzglas gefalteten Membranproteins. In einer Zeit, in der Proteomics, also das Überexprimieren und Analysieren von Proteinen, die Arbeit der größtenteils abgeschlossenen Sequenzierungprojekte fortführen sollen, konnte mit OEP16 ein Modellsystem für die detaillierte Struktur- und Funktionsanalyse von Membranproteinen etabliert werden. 4 Abkürzungsverzeichnis ATP C8E4 C10E6 C12E6 C12E8 Capso CD CMC DGDG β-DM DNA DTT EDTA E.coli ER FTIR HCA Hepes in vitro in vivo IPTG kDa MDGD MPD mRNA NMR OEP β-OG PC PCR PE PEG PG PI PS R RNA SB12 SDS SQDG Adenosintriphosphat Tetraethylenglykol-Monooctylether Hexaethylenglykol-Monodecylether Hexaethylenglykol-Monododecylether Octaethylenglykol-Monododecylether 3-Cyclohexylamino-2-hydroxy-1-propansulfonsäure Zirkulardichroismus (Circular Dichroism) Kritische Mizellare Konzentration (critical micellaer concentration) Digalaktosyldiacylglycerin β-D-Dodecylmaltosid Desoxyribonukleinsäure Dithiothreitol Ethylendiamintetraessigsäure Escherichia coli Endoplasmatisches Retikulum Fourier-Transform-Infrarotspektroskopie Hydrophobe Cluster-Analyse N-2-Hydroxyethylpiperazin-N'-2-Ethansulfonsäure „im Reagenzglas“ „im lebenden Organismus“ Isopropyl–β–D–thiogalactopyranoside Kilodalton Monogalaktosyldiacylglyzerin 2-Methyl-2,4-Pentandiol Boten-Ribonukleinsäure (m für engl. „messenger“) Kernspinresonanz (nuclear magnetic resonance) „Outer Envelope Protein“ β-D-Octylglukosid Phosphatidylcholin Polymerasekettenreaktion (polymerase chain reaction) Phosphatidylethanolamin Polyethylenglykol Phosphatidylserin Phospahtidyinositol Phosphatidylserin Reynolds-Konstante, R = 8,314 J/mol*K Ribonukleinsäure n-Dodecyl-N,N-Dimethyl-3-ammoniopropansulfonat Natriumdodecylsulfat Sulfoquinovosyldiacylglyzerin 5 Einleitung Die Erbse (Pisum Sativum) Die Erbse ist schon seit den berühmten Experimenten zur Vererbungslehre von Mendel ein wichtiger Modellorganismus der biologischen Forschung. Für die Untersuchung von Chloroplasten ist die Erbse besonders geeignet, weil sich diese Plastiden aus den schnell wachsenden Erbsenkeimlingen vergleichsweise einfach und vor allem intakt isolieren lassen. Es ist daher nur konsequent, für Experimente zum Stofftransport über die Chloroplastenmembranen, aber auch für weiterführende molekularbiologische und biochemische Forschung gerade die Erbsenpflanze als Modell zu wählen. Abbildung 1: Foto eines Erbsenkeimlings, wenige Tage alt. 6 Die Pflanzenzelle Abbildung 2: Schematische Darstellung einer Pflanzenzelle. Eukaryontische Zellen unterscheiden sich von den einfacher aufgebauten bakteriellen Zellen durch die Existenz eines Zellkerns, der das Erbgut vom Cytosol der Zelle abtrennt. Die Pflanzenzelle stellt eine besondere Form der eukaryontischen Zelle dar. Zusätzlich zur Zellmembran, einem Zellkern, den Mitochondrien und Lysosomen, dem endoplasmatischen Reitculum (ER) und dem Golgiapparat, die praktisch allen eukaryontischen Zellen gemeinsam sind, besitzt eine pflanzliche Zelle eine Zellwand, Plastiden und eine oder mehrere Vakuolen. Die Zellmembran umhüllt die gesamte Zelle und grenzt sie gegenüber der Außenwelt ab. Stofftransport durch diese Membran ist nur durch Transportproteine möglich. Die Zellwand der Pflanzen ist eine harte, poröse Struktur aus komplexen Kohlenhydraten, die die Zelle mechanisch schützt. Die Flüssigkeit innerhalb der Zelle wird als Cytosol bezeichnet. Es umgibt alle Organellen der Zelle und ist Ort der Biosynthese vieler für die Zelle lebensnotwendiger Substanzen. Im Cytosol befindet sich auch der Apparat zur Zellteilung. Der Zellkern enthält die Chromosomen der Pflanzenzelle. Er ist von einer Doppelmembran, der Kernmembran, umgeben, die Verbindung zum endoplasmatischen Retikulum hat. Am rauhen ER bzw. den daran angelagerten Ribosomen findet die Proteinbiosynthese statt. Die Proteine werden dann durch ein Erkennungs- und Transportsystem, den Golgi-Apparat, mit letzten Modifikationen versehen und mit Hilfe von Vesikeln an ihren Bestimmungsort geschleust. Am glatten ER werden hauptsächlich chemische Signale von der Zellmembran verarbeitet und weitergegeben (z.B. in den Zellkern zur Veränderung der Genexpression). In den Lysosomen werden überflüssige Zellbestandteile zerlegt und giftige Substanzen abgebaut. Die Vakuole dient als Speicher für Wasser und Nährstoffe und kann Giftstoffe wie z.B. Schwermetalle einlagern und sie so für die Zelle unschädlich machen. Die Mitochondrien sind die Kraftwerke der Zelle. Hier wird der Großteil der Energie gewonnen, der zum Aufrechterhalten der Zellfunktionen notwendig ist. Bei der „Atmung“ werden Kohlenhydrate 7 zu Wasser und CO2 oxidiert und die frei werdende Energie in Form von ATP und anderen biochemischen Energieträgern gespeichert. Die Mitochondrien verfügen über ein Doppelmembransystem und ein eigenes Genom, das für einen kleinen Teil der in der Organelle vorhandenen Proteine codiert. Auch die Plastiden, deren prominenteste Vertreter die Chloroplasten sind, verfügen über eigenes Erbgut. Ihr Aufbau und ihre Funktion werden im folgenden detaillierter erläutert. Der Chloroplast Plastiden sind die Zellorganellen, durch die sich Pflanzenzellen von den Zellen aller anderen Eukaryonten unterscheiden. Die grünen Chloroplasten sind die wichtigsten und bekanntesten Plastiden. Erwähnenswert sind aber auch die Chromoplasten, die Pflanzenblüten und Früchten vor allem durch ihren hohen Carotinoid-Gehalt ihre Farbe verleihen und die Amyloplasten, die den Stärkespeicher in Pflanzensamen, Wurzeln und Knollen bilden. Auch andere Plastidentypen in hoch spezialisierten Pflanzengeweben sind bekannt, so sind zum Beispiel die Plastiden in Wurzeln hauptsächlich mit der Assimilierung von anorganischem Stickstoff befaßt (Joyard, 1998) (Lam, 1996). Aufbau Chloroplasten bestehen aus mehreren Membranschichten von sehr unterschiedlichem Aufbau und Funktion. Vom Cytosol ist der Chloroplast durch die äußere (1) und die innere Chloroplastenmembran (2) getrennt. Der Kern eines Chloroplasten wird von gestapelten Ausstülpungen der Thylakoidmembran, den Grana (3,4) gebildet. Diese Membran umschließt das Lumen und trennt es vom Stroma (5), dem Raum zwischen den Thylakoiden und der inneren Chloroplastenmembran, ab. Das Lumen ist ein durchgehender Raum, die Grana sind durch Membrankanäle, die sogenannten Stromathylakoide, verbunden. Der Chloroplast besitzt ein eigenes, im Stroma lokalisiertes Genom, das jedoch nur für einen Teil der Chloroplastenproteine codiert, ebenso eigene Ribosomen für die Translation von RNA in Proteine. Chloroplasten sind in der Lage, sich unabhängig von der Pflanzenzelle zu teilen und besitzen den gesamten hierfür notwendigen biochemischen Apparat (Pyke, 1999). 8 Abbildung 3: Schematischer Aufbau eines Chloroplasten. 1: Äußere Chloroplastenmembran 2: Innere Chloroplastenmembran 3: Thylakoide (Querschnitt, darin das Lumen) 4: Thylakoide (Außenansicht) 5: Stroma Funktion des Chloroplasten in der pflanzlichen Zelle Die Hauptaufgabe der Chloroplasten ist die Erzeugung von chemischer Energie aus Licht, Kohlendioxid und Wasser, die Photosynthese. Dieser Prozeß läuft an den Thylakoidmembranen („Lichtreaktion“, das Aufbauen eines elektrochemischen Gradienten) und im Stroma („Dunkelreaktion“, die CO2-Fixierung) ab. Als Produkte entstehen Kohlenhydrate, die die Grundlage des Stoffwechsels einer Pflanzenzelle darstellen. Gewissermaßen als Nebenprodukt entsteht Sauerstoff, der in die Atmosphäre abgegeben wird. Darüber hinaus enthalten Chloroplasten Enzyme für eine ganze Reihe grundlegender Stoffwechselwege, insbesondere für die Lipidbiosynthese und den Aminosäuremetabolismus (Lam, 1996). Auch eine Reihe von Pflanzenhormonen wird in den Chloroplasten aus Lipidvorstufen synthetisiert (Joyard, 1998). Ein Austausch von Stoffwechselprodukten und deren Vorstufen, aber auch anorganischen Ionen über die innere und äußere Chloroplastenmembran wird durch eine Vielzahl hoch spezialisierter Transportsysteme ermöglicht (Flügge, 1998). Endosymbiontentheorie Chloroplasten sind nicht in der Lage, außerhalb der pflanzlichen Zelle zu leben. Dennoch geht man davon aus, daß Chloroplasten von Vorläufern der Cyanobakterien abstammen, die eine symbiotische Verbindung mit frühen eukaryontischen Zellen eingegangen sind (CavalierSmith, 2000; Margulis, 1996). Dafür spricht zum Beispiel, daß diese Organellen ihr eigenes 9 Genom besitzen, das allerdings im Lauf der Evolution stark reduziert wurde und inzwischen von Genen ergänzt wird, die im Zellkern der Pflanze liegen (Leon, 1998). Die Ribosomen im Stroma der Chloroplasten unterscheiden sich signifikant von den Ribosomen im Cytosol der Zelle. Sie sind bakteriellen, nicht eukaryontischen Typs(Harris, 1994). Die Untereinheiten des Proteinimportkomplexes, der im Cytosol translatierte Proteine ins Innere der Chloroplasten transportiert, haben große Sequenzähnlichkeiten zu cyanobakteriellen Membranproteinen (McFadden, 1999; Reumann, 1999). Auch die große Ähnlichkeit des in den Thylakoiden lokalisierten Photosyntheseapparates zu dem der Cyanobakterien zeigt das enge verwandtschaftliche Verhältnis der Plastiden zu ihren Vorfahren(Blankenship, 1998). Die Lipidzusammensetzung der Chloroplastenmembranen ist sehr ähnlich zu der photosynthetischer Bakterien und unterscheidet sich grundlegend von allen anderen Membranen der pflanzlichen Zelle. So kommt das anionische Lipid Sulfoquinovosyldoacylglcerin fast ausschließlich in photosynthetischen Bakterien und Chloroplasten vor(Benning, 1998). Die äußere Chloroplastenmembran Gemeinsam bilden die innere und äußere Chloroplastenmembran 5-10% der gesamten Membranfläche der Chloroplasten. Dennoch enthalten sie nur 1-2% des Gesamtproteins der Organelle. Die äußere Membran besteht aus 2,5 bis 3 mg Lipid pro mg Protein, dem höchsten Lipidanteil aller pflanzlichen Membransysteme, und hat damit auch eine sehr geringe Dichte von 1,08 g/cm3. Dies kann man sich für die Abtrennung von der inneren Plastidenmembran zu Nutze machen(Joyard, 1991). Wegen ihrer scheinbaren Durchlässigkeit für Substanzen mit einem Molekulargewicht von unter 10000 g/mol wurde bisher angenommen, daß die äußere Chloroplastenmembran wie die entsprechende mitochondriale Membran in vivo keinerlei Membranpotential besitzt. Sollte der Transport durch dieses Membransystem jedoch einer Regulation unterliegen, wofür es Hinweise gibt(Flügge, 2000; Soll, 2000), ist unter bestimmten physiologischen Bedingungen ein durch unterschiedliche Metabolitenkonzentrationen dies- und jenseits der Membran gebildetes Potential vorstellbar(Lemeshko, 2000). Lipide der äußeren Chloroplastenmembran Biologische Membranen bestehen aus einer Lipid-Doppelschicht. Ihre Hauptbestandteile bei Pflanzen sind anionische Phospholipide (hauptsächlich Phosphatidylcholin (PC), 10 Phosphatidylethanolamin (PE) und Phosphatidylglycerin(PG)) und nichtionische Glykolipide (Mono- und Digalaktosyldiacylglycerin(MGDG und DGDG)) sowie das anionische Glykolipid Sulfoquinovosyldiacylglycerin (SQDG). Abbildung 4: Strukturen der häufigsten pflanzlichen Membranlipide. Alle Fettsäuren sind als Palmitinsäure dargestellt. 11 In kleineren Mengen kommen auch pflanzliche Sterole und Phosphatidylinositol (PI), Phosphatidyserin (PS) und Cardiolipin (Diphosphatidydiacylglycerin) vor. Interessant ist, daß sich diese Lipide sehr ungleichmäßig auf die verschiedenen pflanzlichen Membransysteme verteilen. Insbesondere die Chloroplastenmembranen weichen deutlich von der Zusammensetzung anderer eukaryontischer Membranen ab. So kommen die beiden Galaktolipide und das Sulfolipid ausschließlich in Chloroplasten vor. Im Gegensatz dazu findet man in den Chloroplastenmembranen kein Phosphatidylethanolamin(Block, 1983). Auch unter den verschiedenen Membranen innerhalb der Plastiden gibt es gravierende Unterschiede. Phosphatidylcholin findet sich zum Beispiel kaum in den Thylakoiden, in großen Mengen jedoch in den beiden umhüllenden Membranen der Organelle. Die äußere Chloroplastenmembran besteht bei den gut untersuchten Spinatchloroplasten aus etwa 20% MGDG, 30% DGDG, 5% SQDG, 30% PC, 10% PG und 5% PI (Block, 1983). Auch kleine Mengen Sterole wurden gefunden(Poincelot, 1973). Proteine der äußeren Chloroplastenmembran und ihre Funktion In vielen Textbüchern zur Physiologie und Biochemie der Pflanzen werden die äußere Chloroplastenmembran und ihre Bestandteile nur am Rande erwähnt. Dies liegt hauptsächlich daran, daß bis vor wenigen Jahren nur eine Handvoll Proteinkomponenten dieser Membran identifiziert worden waren. Bekannt war der Proteinimportapparat der Chloroplasten, der sich über die äußere und innere Membran der Organelle erstreckt, und bekannt war auch, daß es Porenproteine geben mußte, die dafür sorgten, daß Stoffwechselprodukte die Lipiddoppelschicht passieren können. Man ging davon aus, daß es sich hierbei um Proteine des Porin-Typs handeln mußte, und tatsächlich konnten in Wurzelplastiden der Erbse solche Porine identifiziert werden. Allerdings wurden diese den mitochondrialen Porinen ähnlichen Proteine in vitro nur in nicht-grüne Plastiden importiert. In grünen Chloroplasten scheinen sie nicht vorzukommen (Fischer, 1994; Popp, 1997). Hinweise auf unterschiedliche spezifische Kanalpoteine lieferten elektrophysiologische Messungen an intakten äußeren Chloroplastenmembranen(Heiber, 1995). Später wurden die entsprechenden Gene mit molekularbiologischen Methoden identifiziert(Bölter, 1999; Pohlmeyer, 1997a; Pohlmeyer, 1998) und die Proteine genauer charakterisiert(Linke, 2000; Röhl, 1999; Steinkamp, 2000). Auch viele für den Stoffwechsel der Pflanze wichtige Enzyme sind an oder in der äußeren Membran der Plastiden lokalisiert. Dies konnte unter anderem für das Enzym DGDGSynthase gezeigt werden, welches das Membranlipid Monogalaktosyldiacylglycerin in 12 Digalaktosyldiacylglycerin umwandelt(Froehlich, 2001) und für die Acyl-Coenzym-ASynthase, ein zentrales Enzym des Fettsäurestoffwechsels(Block, 1983). Auch die pflanzliche Hexokinase, die Glucose und auch Fructose unter ATP-Verbrauch in energiereiche Zuckerphosphate umwandelt, ist in der Hüllmembran verankert und verhindert dort durch die Umsetzung möglicherweise einen Rücktransport von Glucose ins Innere der Organelle durch spezifische Glucose-Translokatoren in der inneren Chloroplastenmembran(Wiese, 1999). Proteinimport über die äußere und innere Chloroplastenmembran Ein großer Teil der Proteine in den Chloroplasten wird von Genen im Zellkern codiert. Diese Proteine, die von den Ribosomen im Cytosol der Pflanzenzelle synthetisiert werden, müssen mittels spezifischer Transportprozesse in die Chloroplasten gelangen. Dazu ist nicht nur ein Importsignal innerhalb der Aminosäuresequenz des Proteins nötig, sondern auch ein spezieller Import-Apparat, der das Peptid über die äußere und innere Chloroplastenmembran transportiert. Im allgemeinen enthalten für den Chloroplasten bestimmte Proteine ein sogenanntes Signalpeptid an ihrem N-Terminus, das während des Importvorgangs in die Organelle abgespalten wird. Signalpeptide für den Transport ins Stroma und in die innere Membran der Chloroplasten enthalten oft viele basische und hydroxylierte Aminosäuren und werden von einer cytosolischen Proteinkinase an einem Serin- oder Threoninrest phosphoryliert. Die Dephosphorylierung erfolgt vor dem eigentlichen Importprozess vermutlich an der äußeren Chloroplastenmembran(Heins, 1998). Das Signalpeptid wird dann von einer im Stroma befindlichen spezifischen Protease beim Durchtritt durch den Importapparat entfernt(Bruce, 2000). Im Gegensatz zu mitochondrialen Signalsequenzen bilden die Signalpeptide der Chloroplasten selbst keinerlei Sekundärstruktur aus(von Heijne, 1991). Eine solche Struktur entsteht erst durch Wechselwirkungen mit den Lipiden der äußeren Chloroplastenmembran und ermöglicht damit den Import des Proteins(Pinnaduwage, 1996; Van't Hof, 1993). Dieser Vorgang ist vermutlich deshalb selektiv für die äußere Chloroplastenmembran, weil sie als einzige zum Cytosol exponierte Membran die Glykolipide Mono- und Digalaktosyldiacylglycerin enthält und die Signalpeptide nachweislich mit diesen Lipiden wechselwirken können(Pinnaduwage, 1996). Auch hat dieses Membransystem ein hohes Lipid/Protein-Verhältnis von 3.0(Keegstra, 1989), was eine starke Exponierung von LipidKopfgruppen zum Cytosol zur Folge hat. Veränderungen in der Lipidzusammensetzung dieser Membran haben eine Veränderung des Import-Verhaltens zur Folge(Kerber, 1992). 13 Die Signalsequenzen für die innere Chloroplastenmembran unterscheiden sich nicht von den für das Stroma codierenden Signalen. Es wird vermutet, daß die Information für das Inserieren in die Membran während des Importvorganges in hydrophoben Bereichen des Proteins außerhalb der abspaltbaren Signalsequenz liegt(Heins, 1998). Für den Import in das Lumen der Thylakoide oder in die Thylakoidmembran muß das Signalpeptid hingegen aus zwei Teilen bestehen, einem abspaltbaren Peptid für den Transport ins Stroma und einer weiteren Sequenz, die nach dem Durchtritt durch die Thylakoidmembran von einer im Lumen befindlichen spezifischen Protease abgeschnitten wird(Keegstra, 1999). Die Importmechanismen in die Thylakoide haben Ähnlichkeit mit Transportvorgängen in Bakterien und im endoplasmatischen Reticulum der Eukaryonten(Cline, 1996; Settles, 1998). Proteinimport in die äußere Chloroplastenmembran Der Importweg von Proteinen der äußeren Chloroplastenmembran ist nur in Einzelfällen komplett aufgeklärt. OEP75 („outer envelope protein 75 kDa“), selbst Bestandteil der Proteinimport-Maschinerie der äußeren Chloroplastenmembran, enthält ein Signalpeptid für den Transport ins Stroma. Eine weitere, ebenfalls abspaltbare Signalsequenz sorgt jedoch dafür, daß OEP75 nicht komplett ins Stroma überführt wird, sondern im Importkanal stecken bleibt und in der äußeren Membran verbleibt(Tranel, 1996). Andere, kleinere Proteine wie OEP34 werden jedoch direkt und ohne Signalpeptid in die äußere Chloroplastenmembran insertiert(Keegstra, 1999). Hierbei spielt besonders eine hydrophobe Sequenz am C-Terminus des Proteins eine entscheidende Rolle(Li, 1991). Für OEP14 konnte eine nicht abspaltbare Signalsequenz im NTerminus des Proteins identifiziert werden, die für den spezifischen Import verantwortlich ist(Li, 1996). Die kleinen Kanalproteine der Hüllmembran der Chloroplasten integrieren spontan durch hydrophobe Wechselwirkungen in die Lipid-Doppelschicht(Cline, 1996; Heins, 1998). Man kann davon ausgehen, daß die besondere Lipidzusammensetzung auch hier eine entscheidende Rolle für die Selektivität des Imports in die Chloroplastenmembran spielt(Joyard, 1991; Keegstra, 1989). OEP16 OEP16 („Outer Envelope Protein 16 kDa“) ist ein in der äußeren Chloroplastenmembran lokalisiertes Kanalprotein. Entdeckt wurde es, als man versuchte, durch systematische Analyse von Proteinbestandteilen der äußeren Chloroplastenmembran neue Untereinheiten 14 des Proteinimportkomplexes der Chloroplasten und andere Transportproteine zu finden. Das Protein wurde ansequenziert und seine Gensequenz mittels PCR mit degenerierten Primern aus einer Genbank ermittelt(Pohlmeyer, 1997a). Schnell stellte sich heraus, daß es sich um einen eigenständigen Kanal handelte, ohne direkten Bezug zur Import-Maschinerie. Neben OEP16 wurden weitere Kanalproteine in der äußeren Chloroplastenmembran entdeckt, namentlich OEP21(Bölter, 1999) und OEP24(Pohlmeyer, 1998). OEP16 konnte in Chloroplasten aus Blättern und Stengeln, aber auch in dunkel adaptierten Chloroplasten und in Wurzelplastiden nachgewiesen werden(Pohlmeyer, 1997a). OEP16 inseriert ebenso wie OEP24 in die äußere Chloroplastenmembran, ohne daß ein Signalpeptid abgespalten wird. Der Import ist unabhängig vom Proteinimportkomplex der Chloroplasten und von ATP, und auch Deletionsmutanten, denen der N-Terminus (20 Aminosäuren) oder der C-Terminus (53 Aminosäuren) fehlt, werden korrekt in die äußere Membran integriert(Pohlmeyer, 1997b). Sequenzen 1 MPRSSFSGSL SSPKLDVVID MGNPFLNLTV DGFLKIGAVA ATRSVAEDTF HIIRKGSISS 61 NDFEKSLKKM CKEGAYWGAI AGVYVGMEYG VERIRGTRDW KNAMFGGAVT GALVSAASNN 121 KKDKIAVDAI TGAAIATAAE FINYLT Abbildung 5: Aminosäuresequenz von OEP16 aus Erbse (Pisum sativum) Inzwischen kennt man die Gensequenz von OEP16 nicht nur aus der Erbse(Pohlmeyer, 1997a), sondern auch aus Gerste (Baldi, 1999) und der Ackerschmalwand (Arabidopsis thaliana), deren komplettes Genom inzwischen sequenziert wurde(Arabidopsis Genome Initiative, 2000; Lin, 1999; Mayer, 1999; Salanoubat, 2000; Tabata, 2000; Theologis, 2000). OEP16 aus Erbse wurde auch auf Ähnlichkeiten zu anderen, bekannten Proteinen untersucht. Das Kanalprotein hat in Teilbereichen starke Homologien zu Tim17, Tim22 und Tim23, Untereinheiten verschiedener Präproteinimportkanäle in der inneren Mitochondrienmembran, und zu LivH, einem Aminosäuretransporter aus E.coli(Rassow, 1999). Ein auffälliger Sequenzbereich (Aminosäuren 72-92) mit fünf Glycylresten in einem Abstand von je drei Aminosäuren hat erstaunlich hohe Homologie zu einem Abschnitt aus den Sequenzen von Na+-Glucose-Kotransportern aus Mensch, Huhn, Schaf und Ratte. Dasselbe gilt für Teile eines Na+-Nukleosid-Kotransporters aus Kaninchen, für Permeasen für verzweigte Aminosäuren aus Salmonella und Pseudomonas, und für einen Na+-Kotransporter für neutrale Aminosäuren aus dem Schwein(Pohlmeyer, 1997b). 15 Aufbau Der N-Terminus von OEP16 kann in Chloroplasten und Vesikeln der äußeren Chloroplastenmembran, die mit der Außenseite außen ("right side out") präpariert wurden(Waegemann, 1992), von der Protease Thermolysin abgespalten werden und ist somit in vivo zu Cytosol hin exponiert(Pohlmeyer, 1997b). Der Sequenzbereich, der für die Bildung der eigentlichen Pore zuständig ist, konnte auf die Aminosäuren 21-93 eingeengt werden(Steinkamp, 2000). Erste Untersuchungen an nativen Membranen ergaben, daß OEP16 ein Homodimer sein könnte. Dafür sprechen Crosslink-Experimente(Pohlmeyer, 1997a) und die Tatsache, daß sich OEP16 durch Zugabe von Kupfer(II)-Chlorid oxidativ dimerisieren läßt(Seedorf, 1995), und zwar über das in der Sequenz nur ein einziges Mal vorkommende Cystein in Position Cys71(Pohlmeyer, 1997a). Dieser Vorgang ist reversibel. Funktion und Regulation Elektrophysiologische Eigenschaften Die Existenz von OEP16 als Kanalprotein konnte indirekt durch Messung seiner elektrophysiologischen Eigenschaften in nativen äußeren Chloroplastenmembranen nachgewiesen werden(Heiber, 1995), zusammen mit anderen spezifischen Kanalproteinen dieses Membransystems. Genaue Kenntnis über Leitfähigkeit und Permeabilität für verschiedene Substrate brachten jedoch Untersuchungen an rekombinantem Protein, das in Liposomen rekonstituiert und zur Messung in planare Lipid-Doppelschichten eingebaut wurde(Pohlmeyer, 1997a). Die Lipiddoppelschicht überspannt hierbei ein Loch in einer Teflon-Membran, welche zwei Elektrodenkammern voneinander trennt. Durch Zugabe verschiedener Puffer oder Substrate in die beiden Kammern können damit die spezifischen physiologischen Eigenschaften von OEP16 bestimmt werden. Gemessen in 250 mM KCl auf beiden Seiten der Membran hat OEP16 die höchste Offen-Wahrscheinlichkeit (etwa 80% offene Kanäle) bei einer äußeren Spannung von 0 mV. Dies dürfte dem physiologischen Zustand in vivo nahekommen, auch wenn geringe Membranpotentiale für ähnliche Membransysteme postuliert wurden(Lemeshko, 2000). Bei einer angelegten Spannung von ± 150 mV waren praktisch alle Kanäle geschlossen. 16 Substrate Es zeigte sich, daß der Kanal über eine gewisse Selektivität für Kationen verfügt, auch wenn kleine Anionen wie Cl- praktisch ungehindert passieren können. Etwas größere, organische Moleküle können aber nur noch dann durch die Pore diffundieren, wenn sie Aminogruppen und/oder positive Ladungen tragen. Selektivität des rekonstituierten OEP16-Kanals Substrat Permeabilität Glycin Ja* Valin Ja Arginin Ja* Lysin Ja Glutamat Ja Glutamin Ja* Kadaverin Ja Sucrose Nein* Glucose Nein Fructose Nein* 1-Phosphoglycerat Nein* Dihydroxyaceton Nein* Tetraethylamin Nein* Tris-(hydroxymethyl)-aminomethan Ja* Sorbitol Nein Mannitol Nein Abbildung 6: Die in der Tabelle gezeigten Substrate wurden mittels Leitfähigkeitsmessungen auf ihre Fähigkeit, durch die OEP16-Pore zu diffundieren, getestet. Mit * markierte Ergebnisse wurden durch osmotisch induzierte Fusion von OEP16-Liposomen mit planaren Lipiddoppelschichten bestätigt. (Pohlmeyer, 1997a) Eine ganze Reihe Stoffwechselprodukte müssen die äußere Chloroplastenmembran passieren, um die Funktion der Pflanzenzelle aufrecht erhalten zu können. OEP16 ist jedoch lediglich für einen kleinen Ausschnitt dieser organischen Moleküle selektiv. OEP16 ist für alle Aminosäuren durchlässig, ebenso wie für biologisch relevante Amine wie Cadaverin. Auch das unphysiologische Tris-Kation konnte die Pore passieren. Praktisch undurchlässig ist 17 OEP16 hingegen für Kohlenhydratprodukte der Glycolyse und Zuckerphosphate, tertiäre Amine und von Kohlenhydraten abgeleitete Substanzen wie Sorbitol und Mannitol(Pohlmeyer, 1997a). Oxidative Zerstörung der Kanalfunktion Kupfer(II)-Chlorid ist ein effektiver Katalysator zur Bildung von Disulfidbrücken(Seedorf, 1995). Diese kovalente Verknüpfung zweier benachbarter Cysteinreste kann auch zwischen Cysteinen verschiedener Peptidketten entstehen und spielt in vielen Proteinen und Proteinkomplexen eine wichtige strukturelle Rolle. OEP16 wird durch Zugabe von CuCl2 dimerisiert(Pohlmeyer, 1997a). Dabei geht die Kanalleitfähigkeit durch die Membran verloren, der Vorgang ist jedoch umkehrbar. Ob dieser Vorgang auch in vivo reversibel ist, durch welche biologisch relevanten Oxidationsmittel er ausgelöst werden kann und ob er der Regulation der Kanalaktivität dient, ist bisher ungeklärt. Phosphorylierung Natives OEP16 in der äußeren Chloroplastenmembran ist vermutlich phosphoryliert. Bei in vitro Phosphorylierungsexperimenten wurde OEP16 durch eine in der äußeren Chloroplastenmembran befindliche Kinase mit radioaktivem Phosphat verestert. An Deletionsmutanten konnte gezeigt werden, daß die Phosphorylierungsstelle im Bereich des NTerminus, genauer innerhalb der ersten 20 Aminosäuren in der Sequenz, liegen muß(Pohlmeyer, 1997b). In diesem Bereich befinden sich sechs Serinreste, die als Phosphatakzeptoren in Frage kommen. Genexpression In Gerste ist bekannt, daß die Expression von OEP16 bei Kälte stark zunimmt(Baldi, 1999). Dies konnte sowohl auf RNA- als auch auf Proteinebene gezeigt werden. Welche Funktion OEP16 bei der Kälteregulation zukommt, ist bisher ungeklärt. In Spinat macht OEP16 einen beträchtlichen Teil der Gesamtproteinmenge in der äußeren Chloroplastenmembran aus(Koike, 1998). 18 Faltung von Membranproteinen Allgemeine strukturelle Eigenschaften von Membranproteinen Anders als lösliche, globuläre Proteine müssen Membranproteine bestimmten strukturellen Vorgaben gehorchen, die aus dem Kontakt mit dem hydrophoben Inneren der biologischen Membranen resultieren. Entsprechend zeigen die bekannten Strukturen von Membranproteinen weit weniger verschiedene Strukturmotive, als ihre vielfältigen Funktionen vermuten lassen(Cowan, 1994). Typische Strukturelemente von Membranproteinen sind amphiphile Helices, die parallel zur Lipiddoppelschicht angeordnet sind und mit ihrem hydrophoben Teil in sie hineinragen, und membranspannende Strukturen, die entweder aus sogenannten „β-Barrels“, antiparallelen β-Faltblattstrukturen, oder Bündeln von α-Helices bestehen(White, 1999). Große Domänen von Membranproteinen, die nicht in direktem Kontakt mit den Lipiden stehen, verhalten sich hingegen wie lösliche Proteine(von Heijne, 1996). Während die genannten amphiphilen Helices häufig bei Proteinen vorkommen, die lediglich teilweise in die Membran hineinragen, bilden transmembrane Proteine entweder eine β-Barrel-Struktur oder Helixbündel aus. Gemischte Strukturen sind nicht bekannt. Typische Vertreter der β-Barrel-Struktur sind die bakteriellen Porine, Diffusionskanäle mit einem großen Innendurchmesser(Buchanan, 1999; Hirsch, 1997; Klebba, 1998; Kreusch, 1994). Die am besten untersuchten Vertreter der Helixbündel-Proteine sind die bakteriellen Reaktionszentren(Allen, 1987; Deisenhofer, 1985) und das Bakteriorhodopsin(Griegorieff, 1996). Auch bakterielle(McDermott, 1995) und eukaryontische(Kühlbrandt, 1994) Lichtsammelkomplexe, die Photosysteme I und II(Jordan, 2001; Zouni, 2001), die ATPSynthase(Stock, 1999), die Calcium-ATPase(Toyoshima, 2000) und die Cytochrom C Oxidase(Iwata, 1995; Tsuhikara, 1996) bestehen in ihrem transmembranen Bereich ausschließlich aus Helixstrukturen. Mechanismen der Insertion in die Membran in vivo In eukaryontischen Zellen werden die meisten Membranproteine direkt bei der Translation durch Ribosomen in die Membran eingebaut. Die Ribosomen können mRNA-Moleküle, die für Membranproteine codieren, von denen für lösliche Proteine unterscheiden. Sie haften sich dann an das sogenannte Translocon, einen großen Proteinkomplex in der Membran des endoplasmatischen Reticulums an. Das entstehende Polypeptid wird vom Translocon in die 19 Membran eingefädelt. Hier geschehen auch die ersten posttranslationalen Modifikationen. Später werden die neuen Membranproteine je nach ihren Signalsequenzen über endoplasmatisches Reticulum und Golgi-Apparat an ihren Bestimmungsort in der Zelle transportiert. Eine ganze Reihe von Membranproteinen können aber auch spontan in Membranen eingebaut werden, ohne Mithilfe von anderen Proteinen. Die bestuntersuchten Vertreter dieser Proteine sind bakterielle Toxine, zum Beispiel das Diphterie-Toxin(White, 1999). Generell werden ungefaltete Proteine in Zellen meist von Chaperonen in Lösung gehalten. Diese Faltungshelfer verhindern die Aggregation von Peptiden und helfen ihnen, ihren Bestimmungsort zu erreichen. Auch in Organellen wie den Mitochondrien und Plastiden gibt es eigene Chaperone(Miernyk, 1999). Für lösliche Proteine ist aufgrund einer Vielzahl von thermodynamischen, strukturellen und funktionellen Daten bekannt, daß sich ihre Strukturen unter normalen physiologischen Bedingungen in einem lokalen Minimum der freien Enthalpie der Proteinfaltung befinden. Es gibt viele Belege dafür, daß dies auch für Membranproteine gilt(White, 1999). So konnte gezeigt werden, daß sich auch in Stücke geschnittene Membranproteine in der Lipiddoppelschicht zu funktionellen Komplexen zusammenlagern können. Dies gilt sowohl für α-helikale Proteine(Ridge, 1995) als auch für β-Barrel-Proteine(Koebnick, 1996). Auch Proteine, die wie das Diphterie-Toxin eine stabile lösliche Struktur haben, können in der Lipidumgebung thermodynamisch stabile Strukturen annehmen(Zhan, 1995). Thermodynamische Stabilität von Membranproteinen Drei unterschiedliche Typen von Wechselwirkungen bestimmen Struktur und Stabilität von Membranproteinen: die Wechselwirkungen von Proteinketten untereinander, die Wechselwirkungen mit dem wäßrigen Medium und mit der Lipidmembran. Meßbar werden diese Kräfte durch Untersuchungen des Faltungsprozesses oder des umgekehrten Vorganges, der Denaturierung, mittels Temperaturänderungen oder durch Zugabe chaotroper Reagenzien, welche die Proteinstruktur destabilisieren(White, 1999). Das Hauptproblem hierbei ist, daß Membranproteine häufig nicht komplett denaturieren, weil die in die Lipidumgebung eingebetteten Bereiche besonders stabil sind. Erfaßt werden dann nur die Dissoziation von Untereinheiten und die Entfaltung von Domänen außerhalb der Membran. Zudem sind diese Prozesse oft irreversibel(Haltia, 1995). 20 Die freie Enthalpie ∆G für das Eindringen von hydrophoben Peptiden in eine Lipiddoppelschicht läßt sich in zwei Faktoren unterteilen. Hydrophobe AminosäureSeitenketten partitionieren freiwillig in die Lipid-Doppelschicht. Die Peptidbindungen des Protein-Rückrads hingegen können aufgrund ihrer polaren Struktur in der Wasserphase energetisch günstigere Wasserstoffbrückenbindungen ausbilden. Nur bei der Ausbildung von Sekundärstrukturelementen, in denen sämtliche beteiligten Peptidbindungen untereinander HBrücken bilden, also bei α-Helices und β-Faltblattstrukturen, ist ein Verbleiben in der Membran bei direktem Kontakt mit den Lipiden energetisch möglich. In diesem Fall kompensieren die neu gebildeten hydrophoben Wechselwirkungen der Seitenketten mit der Membran den Verlust an freier Enthalpie, der durch den Übergang des hydrophilen Peptidrückrads in das lipophile Medium entsteht(White, 1999). Alternativ dazu können hydrophile Bereiche in der Membran durch benachbarte Proteinstrukturen bedeckt werden, so daß sie praktisch nicht mit den Lipiden in Berührung kommen. Der Faltungsprozeß Es gibt eine Reihe von Hypothesen und Modellrechnungen über den genauen Ablauf des Faltungsprozesses, deren komplette Darstellung den Rahmen dieser Arbeit sprengen würde. Im Folgenden wird die gängigste Hypothese zur Membranproteinfaltung kurz erläutert. Danach läßt sich der Prozeß der Membranproteinfaltung in vier separate Teilschritte zerlegen. Zunächst partitioniert ein hydrophobes Peptid aus der Wasserphase in die Grenzfläche zwischen Wasserphase und Lipidmembran. Im nächsten Schritt bilden sich dort Sekundärstrukturelemente aus, die das Passieren der Grenzfläche erlauben, im allgemeinen sind das α-Helices(White, 1999). Diese Sekundärstrukturelemente dringen im dritten Schritt in die Membran ein und lagern sich zuletzt zu einem funktionell intakten Membranprotein zusammen(Bechinger, 2000). Die Anlagerung an die Grenzfläche der Membran ist in erster Linie auf den hydrophoben Effekt zurückführbar, der lipophile Aminosäureseitenketten aus der Wasserphase verdrängt. Bei der Assoziation von Membranproteinen mit der Lipiddoppelschicht spielen aber auch elektrostatische Wechselwirkungen positiv geladener Seitenketten mit den anionischen Phospholipiden eine entscheidende Rolle. In nativen Membranproteinen liegt oft ein Großteil der positiv geladenen Seitenketten in dem wäßrigen Medium zugänglichen Bereichen auf 21 einer Seite der Membran. Vermutlich spielen sie eine entscheidende Rolle bei der Frage, in welcher Orientierung ein Membranprotein in die Membran eingebaut wird. Das Ausbilden von Sekundärstrukturelementen ist notwendig, um Peptiden das Eindringen in die Membran zu ermöglichen. Sind alle Peptidbindungen zum Beispiel zu einer α-Helices verbrückt, können diese im dritten Schritt der Faltung als helikale Haarnadelstrukturen in die Membran eindringen. Für den letzten Schritt, die Anordnung der Sekundärstrukturelemente zum aktiven Membranprotein, ist eine Vielzahl unterschiedlicher Faktoren verantwortlich. Transmembrane Strukturelemente werden oft durch aromatische Aminosäurereste in der Grenzfläche der Membran verankert. Untereinander können sie durch Wasserstoffbrückenbindungen, Disulfidbrücken, hydrophobe Wechselwirkungen und ionische Wechselwirkungen zusammengelagert sein. Auch die Bindung von Kofaktoren und das Zusammenwirken von Domänen außerhalb der Membran kann für die korrekte Anlagerung von transmembranen Elementen aneinander eine Rolle spielen(Booth, 1999). 22 Zielsetzung Proteine sind wichtigster Bestandteil aller Lebensvorgänge. Neben vielfältigen strukturellen Aufgaben in der Zelle katalysieren sie vor allem die Stoffwechselreaktionen und sorgen für den gezielten Transport lebenswichtiger Substanzen an ihren Bestimmungsort. Die funktionelle Vielseitigkeit der Proteine liegt in der Vielzahl der möglichen Sequenzen begründet, die aus den 20 Grundbausteinen, den Aminosäuren, gebildet werden können, und in den komplexen Strukturen, zu denen sich solch ein Proteinstrang zusammenlagern kann. Um detaillierte Informationen über Struktur und Funktion eines Proteins zu gewinnen, bedarf es großer Mengen des hochreinen Proteins. In vielen Fällen kann dieser Bedarf nicht durch Aufreinigung des Zielproteins aus dem ursprünglichen Organismus gedeckt werden. Dies gilt besonders für Membranproteine, die schwierig zu isolieren sind und oft nur in geringsten Mengen in der Zelle vorkommen. So gibt es zum Beispiel Rezeptoren in medizinisch relevanten Signaltransduktionsprozessen, die nur in wenigen oder gar einer Kopie pro Zelle vorliegen. Diese geringe Verfügbarkeit ist zusammen mit den Schwierigkeiten bei der Kristallisation der Grund dafür, daß bisher weniger als 30 verschiedene Membranproteinstrukturen aufgeklärt wurden, gegenüber mehr als 5000 Strukturen löslicher Proteine. Die Überexpression – das Produzieren eines Proteins in einem Wirtsorganismus mit gentechnischen Methoden – ist ein häufig genutztes Mittel zur Herstellung großer Proteinmengen. Als Wirtsorganismen eignen sich besonders Bakterien, nicht nur weil sie einfach und kostengünstig zu handhaben sind, sondern auch weil die Proteinausbeuten weit über denen eukaryontischer Expressionssysteme liegen. Bei der Überexpression von eukaryontischen Proteinen in Bakterien (meist E.coli) können jedoch verschiedene Probleme auftreten. Insbesondere Membranproteine werden von Bakterien zumeist nicht in ihrer korrekten Konformation hergestellt. Dies trifft auch auf das in dieser Arbeit untersuchte Protein OEP16 zu. OEP16 ist ein Protein aus der Erbse, das den spezifischen Transport von Aminosäuren und Aminen durch die äußere Chloroplastenmembran ermöglicht. Es wird von E.coli in Form von „Inclusion bodies“, großen Proteinaggregaten, produziert. Da OEP16 in der Erbsenpflanze nur in relativ kleinen Mengen vorkommt und bisher keine Reinigungsprozedur für das native Protein besteht, sollten in der vorliegenden Arbeit Wege gefunden werden, das fehlgefaltete 23 Protein aus E.coli für strukturelle und funktionelle Untersuchungen zugänglich zu machen. Im Erfolgsfall würde dies OEP16 darüber hinaus zu einem Modell für die Strukturbildung von Membranproteinen in vitro machen – ein Vorgang, über dessen Mechanismen bisher nur sehr wenig bekannt ist. Der erste Teil dieser Arbeit beschäftigt sich daher mit der Faltung des Membranproteins in vitro. Bisher existierende Strukturmodelle von OEP16, die sich hauptsächlich auf CrosslinkExperimente, CD-Spektren und Primärsequenzanalysen stützten, sprachen für ein Homodimer mit einer gemischten Struktur aus transmembranen α-Helices und transmembranen βFaltblattstrukturen. Bisher kennt man Membranproteine dieser Größe nur als rein α-helikal (z.B. Bakteriorhodopsin) oder als reine β-Faltblattstrukturen (z.B. Porine). Bekannte Transportproteine der äußeren Membranen von Chloroplasten, Mitochondrien und auch gramnegativen Bakterien sind ausschließlich aus β-Faltblättern aufgebaut. OEP16 ist nach den bisherigen Untersuchungen demnach ein Vertreter einer neuen Familie von Membranproteinen. Dies macht weitergehende Untersuchungen zur Struktur des Proteins besonders interessant. Im zweiten Teil der Arbeit sollten physikochemische und spektroskopische Daten erfaßt werden, die Schlüsse auf die Struktur von OEP16 zulassen. Die gewonnenen Daten und theoretischen Betrachtungen zur Aminosäuresequenz von OEP16 sollten genutzt werden, um ein neues, detailliertes Modell für die Struktur dieses ungewöhnlichen Transportproteins zu erstellen. Darüber hinaus sollten mit Methoden der Proteinkristallographie und Elektronenmikroskopie Vorarbeiten geleistet werden, auf denen aufbauend in Zukunft ein Strukturmodell mit nahezu atomarer Auflösung geschaffen werden kann. 24 Material und Methoden Überexpression von OEP16 in E.coli Die Überexpression von OEP16 erfolgte in der Arbeitsgruppe von Prof. Soll im Botanischen Institut der Universität Kiel. Verwendet wurde ein pET-Vektor der Firma Novagen. Der E.coli-Expressionsstamm BL21(DE3) wuchs in 2YT-Medium (1,6% Caseinhydrolysat, 1% Hefeextrakt und 0,5% NaCl) mit dem Selektionsantibiotikum Ampicillin (135 mg/l) in 500 ml-Schüttelkulturen. OEP16 lag nach Induktion der Überexpression mit IPTG aggregiert in Form von so genannten Inclusionbodies vor. Diese Proteinpartikel wurden nach Lyse der E.coli-Zellen bei 1200 psi in einer „French Press“ in einem Lysepuffer (20 mM Tris/HCl pH 8, 1 mM EDTA, 25% Saccharose) und anschließender Ultraschallbehandlung zur Zerstörung von DNA mehrfach durch Zentrifugieren (10 min bei 10000 g in einer Sorvall Zentrifuge mit GSA-Rotor) und Resuspendieren in detergenzhaltigem Puffer gewaschen. Der erste Waschschritt erfolgte in einem Detergenzpuffer (20 mM Tris/HCl pH 7,5, 200 mM NaCl, 1% Desoxycholat, 1% Nonidet P40, 1 mM EDTA, 10 mM β-Mercaptoethanol). Anschließend wurde zweimal mit einem ähnlichen Puffer (mit 0,5% MEGA9 als Detergenz und ohne Kochsalz) resuspendiert und erneut abzentrifugiert und anschließend in Puffer (Tris/HCl pH 7,5, 1 mM EDTA, 10 mM DTT) bei –80°C gelagert bzw. auf Trockeneis versandt. Reinigung von OEP16 Die OEP16-Inclusionbodies (bis zu 500 µl Pelletvolumen) wurden in 10 ml harnstoffhaltigem Solubilisierungspuffer (Puffer C) gelöst. Dies geschah entweder durch Schütteln im Kühlraum über Nacht oder durch Beschallen mit der Mikrospitze eines Branson Sonifiers (30% Puls, maximale Energie) für etwa 5 Minuten auf Eis. Die Lösung wurde anschließend 10 min bei 5000 g zentrifugiert und anschließend durch einen 0,2 µm Spritzenfilter filtriert. Abzentrifugieren und Filtrieren der Probe wurde notwendig, um feine Verunreinigungen zu entfernen, die regelmäßig die Pumpenköpfe der verwendeten Chromatographieanlage verstopften. Die chromatographische Reinigung erfolgte bei Raumtemperatur in einem Abzug. Verwendet wurde eine Knauer-HPLC-Anlage mit zwei Pumpen und einer Programm-Einheit, die das Mischen des Salzgradienten und die Flußraten steuert. Die Detektion des Proteins erfolgte mit 25 einem Filter-UV-Detektor bei 280 nm Wellenlänge. Chromatogramme (UV-Signal) und Gradient (Leitfähigkeit) wurden mit einem Zweikanalschreiber aufgezeichnet. Die Präpaprationspuffer (Puffer A und B) für die Säulenchromatographie entsprechen dem Puffer zum Lösen der Inclusionbodies, enthielten aber eine geringere Harnstoffkonzentration (6M). Der Hochsalzpuffer B enthielt zusätzlich 1 M NaCl. Der erste Schritt zur chromatographischen Reinigung des Proteins erfolgte mit einer Source30Q Anionenaustauschsäule (Pharmacia) mit einem Säulenvolumen von 30 ml und einem Querschnitt von 25 mm. Die Flußrate betrug 3 ml/min. Das Protein befindet sich aufgrund seines hohen isoelektrischen Punktes von 9 im Druchbruch der Säule, während ein Großteil der Verunreinigungen, vor allem Proteine mit negativer Nettoladung und Nukleinsäuren, zurückgehalten werden. Details zum Gradienten und das Elutionsprofil werden im Ergebnisteil dieser Arbeit gezeigt und diskutiert. Der aufgefangene Druchbruch hat ein Volumen von 15-25 ml und eine geringe Ionenstärke (50-70 µS). In einem zweiten Schritt wird das so vorgereinigte OEP16 direkt auf eine MonoS Kationenaustauschsäule mit 1 ml Säulenvolumen (Pharmacia) aufgetragen. Bei einer Fließgeschwindigkeit von 1 ml/min bindet das Protein an die Kationenaustauschmatrix und eluiert nach starten des Salzgradienten bei einer Salzkonzentration von 120 mM NaCl. Typischerweise erhält man so aus 300 µl Inclusionbodies 3-4 ml einer OEP16-Lösung mit einer Konzentration von 1 mg/ml. Die für die Präparation verwendeten Puffer sind: Puffer A (Präpapration) Puffer B (Präparation) Puffer C (Solubilisierung) 6 M Harnstoff 6 M Harnstoff 8 M Harnstoff 20 mM Hepes/KOH pH 7,5 20 mM Hepes/KOH pH 7,5 20 mM Hepes/KOH pH 7,5 10 mM ß-Mercaptoethanol 10 mM ß-Mercaptoethanol 10 mM ß-Mercaptoethanol 1 mM EDTA 1 mM EDTA 1 mM EDTA 1 M NaCl SDS-Gelelektrophorese 10 µl des gereinigten Proteins in Harnstoff wurden unverdünnt mit 10 µl Probenpuffer (20 mM Tris/HCl pH 7,5, 2 mM EDTA, 0,2% SDS und 0,2% DTT) versetzt und 5 min auf 95°C 26 erhitzt, um Cysteinreste zu reduzieren und das Protein vollständig zu denaturieren. jeweis 1 µl der entstandenen Proteinlösung wurden dann mit einem Probenkamm (Pharmacia) auf ein SDS-HD-Gel (ebenfalls Pharmacia) aufgetragen. Die elektrophoretische Trennung erfolgte mit einem PhastSystem (Pharmacia) mit einem Standardprogramm (500 V, 10 mA, 158 Vh bei 15°C). Die Gele wurden einer Silberfärbung nach Vorschrift des Herstellers unterzogen. Faltung von OEP16 Liposomen In vivo insertiert OEP16 vermutlich spontan in die äußere Chloroplastenmembran(Cline, 1996; Heins, 1998). Dieser Vorgang läßt sich durch Rekonstitution in Liposomen imitieren. Für elektrophysiologische Messungen an OEP16 werden Liposomen aus Phosphatidylcholin verwendet (siehe unten), die mit dem Detergenz MEGA-9 aufgelöst und mit OEP16 in Harnstoff versetzt wurden. Nach anschließender Dialyse zur Entfernung von Harnstoff und Detergenz erhält man Liposomen mit eingebautem OEP16, das dieselbe Kanalleitfähigkeit wie das native Protein zeigt(Pohlmeyer, 1997a). Diese Liposomen lassen sich auch für spektroskopische Untersuchungen von OEP16 in seiner Lipidumgebung verwenden. Als Lipid wurde entweder eine Mischung aus hochreinem Phosphatidylcholin mit Phosphatidsäure (Firma Lipoid) im Verhältnis 20:1 verwendet, oder selbst nachgereinigtes Phosphatidylcholin (Typ S-IV, Sigma). Zum Reinigen des S-IV-Lipids wurde die Lipidsuspension (100 mg/ml in 10 mM Tricin/KOH pH 8,2) mit sechs Volumenteilen Methanol/Chloroform versetzt (Methanol/Chloroform 2:1) und nach Zusatz von zwei Volumenteilen 1M KCl, 0.2M H3PO4 im Scheidetrichter ausgeschüttelt. Danach wird die Lösung stehengelassen und gewartet, bis sich die Phasen getrennt haben. Die (untere) Lipidphase wird abgelassen und der pH der Wasserphase mit KOH auf ca. 8 eingestellt. Dann wird die Wasserphase erneut mit Lösungsmittel ausgeschüttelt. Anschließend werden die organischen Phasen vereinigt und das Lipid im Rotationsverdampfer getrocknet. Dieses Lipid enthält neben Phosphatidylcholin Spuren vieler anderer pflanzlicher Membranlipide. 27 Die Liposomen werden wie folgt hergestellt: 500 µl OEP16-Lösung (1 mg/ml) im Präparationspuffer (Puffer A mit ca. 150 mM NaCl) werden mit 500 µl einer Lipidlösung (50 mg/ml gelöst in Puffer D mit 160 mM MEGA-9) versetzt und durch Schütteln und Beschallen im Ultraschallbad bei Raumtemperatur gemischt, bis das Lipid vollständig gelöst ist. Die klare Lösung wird in einen Dialyseschlauch mit 3500 Da maximaler Porengröße (Spectrum) gefüllt. Die Dialyse zur Bildung der Liposomen erfolgt gegen 5 l Puffer D zunächst bei Raumtemperatur, da das Detergenz MEGA-9 bei diesen hohen Konzentrationen in der Kälte ausfällt. Nach etwa zwei Stunden wird die Dialyse über Nacht im Kühlraum fortgesetzt. Detergenz-basierte Methoden für die Rekonstitution Detergenzien können Proteine aus Lipidmembranen herauslösen, indem sie die Bestandteile dieser Membranen imitieren und ersetzen. Ähnlich wie Membranlipide besitzen Detergenzien langkettige, hydrophobe Bereiche, die an einem hydrophilen Kopf sitzen. Sie bilden in wäßrigen Medien Mizellen mit einem hydrophoben Kernbereich. Da OEP16 spontan in Lipidmembranen eingebaut und korrekt gefaltet werden kann, sollte dieser Vorgang auch in Detergenzmizellen zu imitieren sein, wenn man das geeignete Detergenz wählt. Gelfiltration Getestet wurden verschiedene Sephadex-Materialien (G10, G25 und G50) sowie analytische Gelfiltrationssäulen mit Superdex-Matrix (Superdex75 und Superdex200). Sephadex-Säulen mit einem Durchmesser von 0,9 cm und einer Bettlänge von 8 cm wurden selbst nach Vorschriften des Herstellers (Pharmacia) gegossen. Als Laufpuffer diente der für die Dialysemethode verwendete Puffer (siehe dort) unter Zusatz einer Detergenzkonzentration von 0,03% C12E8. Es wurde dieselbe Knauer HPLC-Anlage wie für die Proteinreinigung verwendet. Die Flußraten lagen bei 0,5 ml/min für selbst gegossene Säulen und bei 1 ml/min für die fertigen Superdex-Säulen. Von der Matrix gebundenes Protein wurde mit 0,5 M NaOH eluiert und die Säule anschließend mit 30% Isopropanol gewaschen. Wiederfindungsraten wurden aus dem UVSignal des HPLC-Detektors abgeschätzt. 28 Dialyse Zur Rekonstitution des Proteins mittels Dialyse wurden der Proteinlösung in Harnstoffpuffer die notwendige Menge hochkonzentrierter Detergenz-Stammlösung zugesetzt, um die für weitergehende Untersuchungen notwendige Endkonzentration an Detergenz zu erhalten ohne das Protein dabei unnötig zu verdünnen. Die Lösung wurde anschließend in Dialyseschläuche oder in Dialysebuttons (Hampton Research) gefüllt und diese in ein großes Reservoir Dialysepuffer versenkt. Das Endvolumen der Dialyseansätze betrug (je nach Bedarf des anschließenden Experiments) 0,2 bi 2 ml. Die Dialyse erfolgte im allgemeinen über Nacht. Verwendet wurden ausschließlich Dialysemembranen der Forma Spectrum mit einer Porenweite von 2500 Da. Der Dialysepuffer enthielt 20 mM Hepes/KOH pH 7,5 und 1 mM EDTA. Verdünnung OEP16-Proben, die im weiteren Verlauf dieses Kapitels erwähnt werden, wurden (wenn nicht anders angegeben) durch Verdünnen hergestellt. Hierzu werden 100 µl der aus der chromatographischen Reinigung erhaltenen OEP16-Lösung in Puffer A ohne weitere Behandlung mit 900 µl detergenzhaltigem Puffer in einem Reaktionsgefäß (1,5 ml, Plastibrand) durch vortexen gemischt. Der Verdünnungspuffer enthielt neben der gewünschten Detergenzkonzentration 20 mM Hepes/KOH (pH 7,6) und 1 mM EDTA. Die Arbeitskonzentrationen der Detergenzien lagen üblicherweise oberhalb ihrer CMC, im Bereich 1 x CMC bis 10 x CMC. Die Faltungsreaktion erfolgt bei Raumtemperatur. Spektroskopische Methoden Proteinbestimmung nach Bradford Da die meisten Proteinbestimmungmethoden auf das Reduktionsmittel β-Mecaptoethanol emfindlich reagieren, das in allen OEP16-Proben enthalten ist, konnte die Konzentration des Proteins nur mittels der Bradford-Methode bestimmt werden. Da diese Methode durch die Gegenwart von Detergenzien erheblich gestört wird, beziehen sich alle Proteinkonzentrationen auf die Messung der Ausgangskonzentration von OEP16 in der 29 Harnstofflösung (Präparationspuffer A mit 150 mM NaCl). Ist von Endkonzentrationen die Rede, sind diese durch Berücksichtigung des Verdünnungsfaktors aus der Ausgangskonzentration berechnet. Fluoreszenz-Spektroskopie Die in dieser Arbeit gezeigten Spektren wurden mit einem FluoroMax-2 Spektrometer der Firma ISA in 1 ml Halbmikro-Quartzküvetten mit einer Schichtdicke von 0,5 cm in der Anregungsrichtung und 1 cm in der Meßrichtung aufgenommen. Die Bandbreiten für die Anregungs- und Meßwellenlängen betrugen üblicherweise 1 bis 2 nm. Zur Aufnahme der Spektren wurden in den meisten Fällen 100 µl einer OEP16-Lösung in Puffer A mit 900 µl einer geeigneten Detergenzlösung (Detergenzkonzentration wie beim jeweiligen Experiment angegeben, in 20 mM Hepes/KOH pH 7,6, 1 mM EDTA) in einem 1,5 ml Reaktionsgefäß gemischt und anschließend in die Küvette gefüllt. Das Mischen in der Küvette ist aufgrund der unterschiedlichen Viskositäten ond Dichten der Lösungen schwierig. Die Endkonzentration von OEP16 in diesen Ansätzen betrug je nach Experiment 0,03 bis 0,1 mg/ml. Die Messungen erfolgten bei Raumtemperatur. Zum Messen von Differenzspektren (OEP16-Liposomen/leere Liposomen) wurden die wie im Abschnitt „Liposomen“ beschrieben hergestellten Liposomen mit den oben genannten Parametern ohne weitere Verdünnung gemessen. Die Spektren wurden ohne weitere Bearbeitung voneinander abgezogen, um das störende Fluoreszenzsignal der Liposomenlösung zu eliminieren. CD-Spektroskopie Alle CD-Spektren wurden mit einem Jasco J500 CD-Spektropolarimeter bei Raumtemperatur aufgenommen. Die verwendeten Küvetten hatten eine Schichtdicke von 0,2 mm, die Probenkammer wurde ständig mit Stickstoff gespült, um Absorptionseffekte durch Sauerstoff sowie oxidative Beschädigung der empfindlichen Spiegelsysteme des Geräts zu vermeiden. Die Spektren wurden mit einer Auflösung von 0,1 nm und einer Aufnahmezeit von 10s/nm aufgenommen. Es wurden jeweils fünf Spektren gemittelt. Die Proteinkonzentrationen lagen je nach Messung zwischen 0,1 und 0,5 mg/ml. Die Proben wurden wie im Abschnitt „Detergenz-basierte Methoden für die Rekonstitution“ erläutert hergestellt. 30 Für hochauflösende Spektren im gesamten Wellenlängenbereich wurden Proben mit 0,5 mg/ml OEP16, dialysiert gegen 10 mM Natrimcacodylatpuffer (pH 7,0, mit 50 mM Natriumsulfat), in Tonnenküvetten mit einer Schichtdicke von 0,05 mm gemessen. Es wurden wiederum fünf Spektren gemittelt. Alle CD-Messungen erfolgten bei Raumtemperatur. IR-Spektroskopie FT-IR-Spektren (Fuorier-Transform-Infrarotspektren) wurden mit einem IFS28/B Spektrometer der Firma Bruker Optik GmbH, Ettlingen aufgenommen. Die Probenkammer wurde mit getrockneter Luft gespült. Die Signale wurden mit einem DTGS-Detektor erfaßt und mittels Fourier-Transformation („Happ-Genzel apodization“) in Infrarotspektren umgewandelt. Die Geräteauflösung betrug 4 Wellenzahlen. Es wurden jeweils 32 Messungen gemittelt, um das Rauschen zu reduzieren. Die Spektren sind in ihrer zweiten Ableitung dargestellt. Da Protein-FTIR-Spektren wegen der störenden anregbaren Schwingungen des Wassers (insbesondere der symmetrischen Deformationsschwingung δ bei 1595 cm-1) im interessierenden Wellenlängenbereich (Wellenzahlen zwischen 2000 und 1400 cm-1) nur in D2O meßbar sind, mußten die Proben vorher in D2O überführt werden. Den Liposomen wurden hierzu über nacht in einer Gefriertrocknungsanlage das Wasser entzogen; sie wurden erst kurz vor der Messung in reinem D2O wieder aufgenommen. Gleichzeitig mit dem Wechsel des Lösungsmittels kann so auch eine höhere Probenkonzentration erreicht werden. Liposomensuspensionen mit einem ursprünglichen Volumen von 1 ml wurden in 100 µl aufgenommen. Die OEP16-Endkonzentration in diesen Proben betrug für die Messung etwa 5 mg/ml. Die Suspension wird in eine IR-Küvette mit CaCl2-Fenstern gefüllt, die mit Dichtungsringen zu einer Schichtdicke von 50 µm zusammengepreßt werden. Gemessen wurde bei Raumtemperatur; Die Probenkammer wurde vor der Messung ausreichend (mindestens 20 Minuten) mit getrockneter Luft gespült, um den störenden Einfluß von Wasserdampf auf die Spektren zu minimieren. Zeitaufgelöste Spektroskopie Zeitaufgelöste Intensitätsunterschiede der Tryptophanfluoreszenz von OEP16 während des Faltungsprozesses wurden im Zeitfenster von 1 bis 100 ms mit einem SX-18MV stopped flow 31 Apparat der Firma Applied Photophysics (Leatherhead, Großbrittanien) gemessen. UVAnregung erfolgte durch eine Xenondrucklampe bei einer Wellenlänge von 280 ± 20 nm. Die Detektion wurde mit einem Interferenzfilter auf 334 ± 5 nm Wellenlänge eingeschränkt. Das Mischungsverhältnis von Proteinprobe zu Verdünnungspuffer betrug 1:10, was einer Enkonzentration von 0,07 mg/ml OEP16 in 600 mM Harnstoff, 20 mM Hepes/KOH (pH 7,6), 1 mM EDTA und 1 mM ß-Mercaptoethanol mit unterschiedlicher Detergenzkonzentration (je nach Experiment) entsprach. Die erhaltenen Signale wurden mittels nichtlinearer Regression in einem Bereich von 3-100 ms mit der Methode der kleinten Quadrate als doppelt exponentielle Kurven angenähert. Einzelne Meßkurven wurden mit einem π∗-180 stopped flow Apparat desselben Herstellers aufgenommen, der ein besseres Signal-Rausch-Verhältnis hat, was den relativen Fehler für die mathematische Bestimmung der Zeitkonstanten von <10% auf <1% reduziert. Bei niedrigen Detergenzkonzentrationen konnten hier 3-fach exponentielle Kurven angenähert werden. Die Standardmessungen erfolgten bei Raumteperatur (25°C). Die temperaturabhängigen Messungen wurden im Temperaturbereich von 10°C bis 35°C durchgeführt. Messungen mit CD-Detektion erfolgten ebenfalls mit einem π∗-180 stopped flow Apparat unter denselben Bedingungen (25°C). Die Änderung der Elliptizität wurde bei einer Wellenlänge von 228 nm im Bereich von 2-200 ms aufgenommen. Physikalisch-chemische Methoden DSC Denaturierungskurven wurden in einem Microcal MC-2 Scanning-Kalorimeter aufgenommen. Die Proteinkonzentration für die Messungen betrug 0,55 mg/ml in einem Meßvolumen von 1,225 ml. Der Puffer enthielt 20 mM Hepes/KOH (pH 7,6), 1 mM EDTA und variable Mengen Detergenz. Die Proben wurden wie im Abschnitt „Detergenz-basierte Methoden für die Rekonstitution“ erläutert hergestellt. Die Referenzprobe bestand aus demselben Puffer ohne Protein. Die Heizrate betrug 30°C/h, gemessen wurde im Bereich zwischen 20° und 95°C. Meßgröße war die Wärmekapazität als eine Funktion der Temperatur, die unter Berücksichtigung von Volumen und Konzentration der Probe auf die molare Wärmekapazität umgerechnet wurde. Denaturierungstemperatur (Kurvenmaximum) und –enthalpie (Fläche unter der Kurve) wurden aus der gemessenen Kurve nach Abziehen des Untergrundsignals bestimmt. 32 Elektronenmikroskopie Für die Transmissions-Elektronenmikroskopie an OEP16 wurden 5 µl der durch Verdünnung hergestellten Proteinlösung mit einer Endkonzentration von 0,01 mg/ml auf einem hydrophilisierten kohlenstoffbeschichteten Gitter (hergestellt durch 60 s Plasmabehandlung bei 8 W Leistung mit einem Baltec MED 020) aufgetragen, überschüssige Flüssigkeit abgesaugt und die Probe luftgetrocknet. Ein Tropfen Phospho-Wolframsäure (2% w/v, pH 7,0) wurde für 45 s zugegeben und anschließend wieder abgesaugt. Diese Vorgänge erfolgten bei Raumtemperatur. Die erneut getrocknete Probe wurde dann in einem Philips CM12 Transmissions-Elektronenmikroskop bei einer 58300-fachen primären Vergrößerung betrachtet. Hierzu wurde ein „Nieder-Dosis-Protokoll“ des Herstellers verwendet, um unnötige Strahlungsschäden an der Probe zu vermeiden. Die Bildaufzeichnung erfolgte fotografisch. Kristallisation Probenvorbereitung Erste Kristallisationsexperimente wurden mit OEP16, rekonstituiert in C12E8, durchgeführt. Die Proben wurden wie im Abschnitt „Detergenz-basierte Methoden für die Rekonstitution“ erläutert hergestellt. Die Detergenzkonzentration betrug 0,03%. Um eine möglichst hohe Proteinkonzentration zu erreichen, wurde das gefaltete Protein in Puffer mit gesättigter Ammoniumsulfatlösung im Verhältnis 1:1 versetzt und dabei präzipitiert. Das Protein wurde in Wasser wiederaufgenommen, so daß das Endvolumen einem zehntel des Ausgangsvolumens entsprach, was einer Proteinkonzentration von etwa 10 mg/ml entspricht. Da auch das verwendete Detergenz mit Ammoniumsulfat aus der Lösung ausfällt, erhöht sich auch die Detergenzkonzentration entsprechend. Die erhaltene Lösung wurde mit maximaler Geschwindigkeit (13.000 upm in einer Heraeus Mikrizentrifuge) abzentrifugiert, um reichlich vorhandene Aggregate abzutrennen und mit den Pufferlösungen der Kristallisationsansätze versetzt. 33 Kristallisationsansätze Grundsätzlich wurde wegen der einfachen Handhabbarkeit die Methode der hängenden Tropfen genutzt. Hierbei wird ein kleiner Tropfen der Proteinlösung mit Puffer hängend an einem Deckglas angebracht, der mittels Dampfdiffusion mit einem Pufferreservoir in Kontakt steht. Die Salzkonzentration im Reservoir ist höher als im Tropfen, so daß Salz- und Proteinkonzentration während des Diffusionsprozesses im Tropfen zunehmen. Hierbei wird idealerweise die Phasengrenze für die Löslichkeit des Proteins überschritten – eine notwendige Bedingung für die Kristallisation. Das Verhältnis von Proteinlösung zu Präzipitationslösung betrug 4:1. Auf diese Weise wurde eine weitere Aufkonzentrierung der Proteinlösung durch den Diffusionsvorgang erreicht. Das Startvolumen der hängenden Tropfen zu Beginn des Diffusionsvorganges betrug 5 µl, die Tropfen wurden dann auf unbehandelte Deckgläser aufgebracht. Deckgläser und Pufferreservoire wurden durch Silikonpaste gasdicht miteinander verbunden und derart abgedichtet, um ein Austrocknen der Ansätze zu vermeiden. Die Löslichkeit von OEP16 wurde durch Variation der Parameter Fällungsmittel, pH, Kristallisationsansätze und Temperatur verringert. Fällungsmittel, pH-Werte und Zusätze wurden zunächst durch die fertigen Lösungen zur Proteinkristallisation der Firma Hampton Research bestimmt. Die Zusammensetzung dieser Lösungen beruht auf empirischen Erfahrungen bei der Kristallisation von Membranproteinen. Die Ansätze wurden bei 18°C in einem Temperierschrank und bei 4°C im Kühlraum inkubiert und täglich mit einem Mikroskop überprüft, ob sich Präzipitat oder Kristalle in den Tropfen gebildet hatten. In einigen Ansätzen trat auch eine Phasentrennung in zwei nicht mischbare, wäßrige Phasen auf. Die besten Kristalle wurden mit Natriumzitrat als Fällungsmittel erhalten. Die auftretende Phasentrennung entsteht wohl in erster Linie durch die geringe Löslichkeit von Polyethylenglykolen (und damit auch von PEG-haltigen Detergenzien) in ZitratLösungen(Marcos, 1999). Die Proteinkristalle bilden sich in der entstandenen detergenzreichen Phase erst nach der Phasentrennung aus. Unter dem Mikroskop läßt sich die Veränderung von runden, öligen Tropfen (detergenzreiche Phase) zu kantigeren, doppelbrechenden Kristallen im Lauf von 1-3 Tagen gut beobachten. 34 Messung der Röntgenbeugung Die einzelnen OEP16-Kristalle wurden vorsichtig mit einer kleinen Kunststofföse (0,5 mm Durchmesser) zusammen mit einem Tropfen Kristallsiationslösung aus den Ansätzen „gefischt“. Die Öse („Loop“) wurde in eine dünne Quarzkapillare mit 2 mm Durchmesser gesteckt und mit dieser so mit Wachs verbunden, daß der Kristall die Quarzoberfläche nicht berühren konnte (bei Berührung lösten sich die Kristalle auf) und das Röhrchen gasdicht verschlossen war. Die Kapillare wurde dann auf einen Gonometerkopf aufgebracht und in den Röntgenstrahl gebracht. Die Röntgenbeugung der OEP16-Kristalle wurde mit einer rotierenden Kupferanode bei einer Wellenlänge von 15,4 nm gemessen. Der Generator wurde mit 40 kV und 65 mA betrieben, die Blenden für die Strahlbegranzung waren auf 0,3 mm eingestellt. Reflexe wurden mit einer Imageplate (MAR Research) mit 18 cm Durchmesser erfaßt. Die Messung und die anschließende Auswertung der Beugungsbilder mit dem Programm DENSO in Verbindung mit dem Grafikprgramm XDISPLAYF erfolgte bei der AG Sänger, FU Berlin. Theoretische Strukturvorhersage Sämtliche im Folgenden beschriebenen Methoden sind im Internet abrufbar. Besonders hilfreich für das Finden solcher Analysewerkzeuge sind die Server des Europäischen Molekularbiologie-Netzwerks (http://www.embnet.org), des Proteinanalyse-Systems Expasy (http://www.expasy.ch) oder des Institut Pasteur (http://bioweb.pasteur.fr). Im Folgenden werden die für diese Arbeit verwendeten Methoden kurz beschrieben und genaue Internetadressen angegeben. "Multiple Sequence Alignment" Um Sequenzen eines Proteins aus verschiedenen verwandten Organismen überhaupt miteinander vergleichen zu können, muß man sie in geeigneter Weise nebeneinander darstellen. Was sich zunächst wie ein triviales Problem anhört, wird um so schwieriger, je geringer der Verwandtschaftsgrad der untersuchten Proteine ist. Das so genannte "Multiple 35 Sequence Alignment" berücksichtigt auch Sequenzbereiche, die nicht in allen Proteinen einer untersuchten Gruppe vorkommen und markiert diese entsprechend. Hier wurde der Algorithmus Dialign (Version 2.1) verwendet(Morgenstern, 1999), der unter der Adresse http://bibiserv.techfak.uni-bielefeld.de/dialign/ genutzt werden kann. Dialign gibt nicht nur die entsprechend ihrer Homologie angeordneten Sequenzen aus, sondern berechnet für jede Position in der Sequenz einen Homologie-Index mit einem Wert zwischen 0 und 5, wobei 0 komplette Abweichung und 5 eine komplette Übereinstimmung im untersuchten Sequenzbereich bedeutet. Vorhersage transmembraner Bereiche Die Vorhersage von transmembranen Bereichen wird im allgemeinen über sogenannte Hydrophobizitäts-Plots(Kyte, 1982) vorgenommen. Diese Methode errechnet die durchschnittliche Hydrophobizität eines kurzen Sequenzbereichs. Anhand solcher Hydrophobizitätswerte aus Proteinen, deren Struktur bekannt ist, kann man einen Grenzwert der Hydrophobizität bestimmen, über dem ein Sequenzbereich mit hoher Wahrscheinlichkeit innerhalb einer Membran liegen muß. Leider versagt diese Methode bei transmembranen βFaltblattstrukturen ebenso wie bei amphiphilen α-Helices, da diese relativ viele hydrophile Aminosäuren enthalten können, wenn sie zum Beispiel einen Kanal durch die Membran bilden. Hilfreich ist hier die Verwendung von "Multiple Sequence Alignments". Das Programm „Pepwindowall“ (http://bioweb.pasteur.fr/seqanal/interfaces/pepwindowall.html) erlaubt das Erstellen von gemittelten Hydrophobizitätsplots aus mehreren verwandten Sequenzen. Im Fall von OEP16 treten hierdurch die transmembranen Segmente deutlicher zu Tage. Auf ganz andere Weise funktioniert derAlgorithmus TMPred zur Vorhersage transmembraner Helices(Hofmann, 1993), verfügbar unter der Adresse http://www.ch.embnet.org/software/TMPRED_form.html. Hier werden Sequenzbereiche mit einer Sequenzdatenbank bekannter transmembraner Helices direkt verglichen und so ein Topologiemodell erstellt. 36 Hydrophobe Cluster-Analyse Die hydrophobe Cluster-Analyse HCA(Callebaut, 1997) erlaubt ebenfalls Vorhersagen über transmembrane Bereiche und erkennt auch amphiphile Bereiche in vielen Fällen. Die zweidimensionale Darstellung einer Sequenz zeigt jede Aminosäure umgeben von den sechs Aminosäuren in ihrer näheren Umgebung (Position -3 bis -1 und 1 bis drei in der Sequenz um die untersuchte Aminosäure). So lassen sich Sequenzbereiche mit hoher Hydrophobizität einfach bildlich darstellen. Amphiphile Bereiche und transmembrane β-Faltblattstrukturen ergeben auffällige Muster. HCA-Plots können unter der Adresse http://smi.snv.jussieu.fr/hca/hca-form.html erstellt werden. 37 Ergebnisse Von der Proteinreinigung zum gefalteten Protein (eine Einleitung) OEP16 ist ein kleines Membranprotein aus der äußeren Chloroplastenmembran der Erbse. Bis heute gibt es kein Reinigungsprotokoll, das die Isolierung großer Mengen des nativen Proteins aus Erbsenpflanzen erlaubt. Zum einen ist der Anteil von OEP16 am Gesamtprotein einer Pflanzenzelle sehr gering, zum anderen ist selbst bei einer Isolierung äußerer Chloroplastenmembranen und der damit verbundenen Anreicherung von OEP16 das Abtrennen anderer Membrankomponenten, vor allem der anderen OEPs mit vergleichbaren isoelektrischen Punkten, schwierig. Bei Überexpression des Gens in E.coli hingegen kann man große Mengen des Proteins gewinnen. Dieses Protein ist jedoch fehlgefaltet und läßt sich nur in Form sogenannter „Inclusion bodies“ isolieren, großen stabilen Proteinaggregaten mit eingeschlossenen Verunreinigungen. Diese bestehen meist aus RNA und anderen, bakteriellen Proteinen(Brill, 2000). Als Voraussetzung für alle Experimente zur Struktur- und Funktionsaufklärung müssen diese Proteinaggregate gelöst und das darin enthaltene OEP16 gereinigt werden. Anschließend gilt es, Methoden zu finden, die eine Faltung in die native Struktur in vitro erlauben. Abbildung 7 zeigt die möglichen Strategien, um zu korrekt gefaltetem, für Funktionsuntersuchungen und die Kristallisation geeignetem Protein zu gelangen. 38 Abbildung 7: Strategien zur Kristallisation von Membranproteinen Abbildung 7 zeigt schematisch die Schritte, die bis zur Proteinkristallisation notwendig sind. Nach erfolgreicher Überexpression des Proteins muß das Protein zunächst effizient solubilisiert werden, um es in einem nächsten Schritt von Verunreinigungen befreien zu können. Die verschiedenen in Abbildung 7 aufgezeigten Wege zur Rekonstitution von OEP16 39 unterscheiden sich in ihrer Handhabbarkeit und ihrer Effizienz. Der Einbau in eine künstliche Lipid-Doppelschicht ermöglicht es, bei Wahl einer geeigneten Lipidzusammensetzung die natürliche Membranumgebung des Proteins möglichst genau nachzuahmen. Dies sollte zu hohen Rekonstitutionsraten führen, hat aber den Nachteil, daß das Protein in einer Membran für viele biophysikalische Methoden und vor allem für die Proteinkristallisation nicht verwendbar ist und erst wieder solubilisiert, d.h. mit Detergenzien aus der Membran herausgelöst werden muß. Ein System, das es ermöglicht, das Protein direkt in Detergenz-Mizellen einzubringen und dabei in seine native Form zu falten, könnte ohne Umwege große Mengen Protein liefern. OEP16 ist aber ein Porenprotein, dessen Aktivität sich nur in Membranen messen läßt. Die Schwierigkeit eines reinen Detergenzsystems ist weniger seine Handhabung, als die Frage, wie man die korrekte Strukturbildung eines Kanalproteins in Lösung bzw. in Mizellen zeigen kann. Im Folgenden soll gezeigt werden, daß mit spektroskopischen Methoden in Detergenz solubilisiertes Protein mit in Membranen eingebautem Protein verglichen werden kann. Der Beweis der Faltung in Detergenzmizellen ist hierbei indirekter Natur. Die Aktivität als wichtigster Beleg für eine korrekte Struktur kann nur in Liposomen gezeigt werden. Hier läßt sich ein Membranpotential aufbauen und die Diffusion von Substraten durch den Kanal wird meßbar. Die in Verlauf dieser Arbeit erläuterten Methoden der Fluoreszenz-, CD- und Infrarotspektroskopie ermöglichen dann vergleichende Untersuchungen der unterschiedlich präparierten Proben. Nur wenn alle verwendeten vergleichenden Methoden eine Übereinstimmung der Proben in Liposomen und Mizellen zeigen, kann man von einer korrekten Faltung von OEP16 in Detergenzmizellen ausgehen und Strukturdaten gewinnen. Zunächst wird der erste Arbeitsschritt, die Reinigung des Proteins im ungefalteten Zustand, genauer betrachtet. Proteinreinigung Die im Kapitel „Material und Methoden“ beschriebene Proteinreinigung basiert auf der in der Literatur(Pohlmeyer, 1997a; Pohlmeyer, 1997b) beschriebenen Reinigungsmethode für denaturiertes OEP16 und wurde weiter optimiert. Zur Solubilisierung wurde ein Beschallungsschritt eingeführt, um das langwierige Lösen des Proteins im Solubilisierungspuffer zu beschleunigen (siehe Material und Methoden). Durch Abzentrifugieren und Filtrieren der Probe konnten feine Verunreinigungen entfernt werden, 40 die regelmäßig die Pumpenköpfe der verwendeten Chromatographieanlage verstopften. Flußgeschwindigkeiten und die Gradienten wurden der Chromatographieanlage angepaßt. Die Reinigung erfolgte bei Raumtemperatur in einem Abzug. Die OEP16-Lösung wurde mittels einer 30 ml Anionenaustauschsäule (SOURCE Q, Pharmacia) von anionischen Verunreinigungen befreit (Flußrate 3 ml/min). Schematisch wird dieser Reinigungsschritt in Abbildung 8 dargestellt. Abbildung 8: Schematische Darstellung der AnionenaustauschChromatographie Abbildung 8 zeigt den Salzgradienten (schwarz) und das Elutionsprofil der UV-aktiven Substanzen in der Lösung (grau) bei der Vorreinigung von OEP16 mit einer SourceQAnionenaustauschsäule. Während der Durchbruch der Säule vorwiegend OEP16 enthält, eluieren bei höheren Salzkonzentrationen zwei sehr markante Peaks, die zu einem großen Teil aus Nukleinsäuren bestehen(Brill, 2000). Der abschließende Reinigungsschritt bestand aus einer Kationenaustauschsäule (MONO S, Pharmacia) mit 1 ml Säulenvolumen (Fließgeschwindigkeit 1 ml/min), schematisch dargestellt in Abbildung 9. Abbildung 9: Schematische Darstellung der KationenaustauschChromatographie 41 Abbildung 9 zeigt schematisch den zweiten Reinigungsschritt von OEP16 (schwarz dargestellt ist der Salzgradient, grau das Elutionsprofil). OEP16 eluiert von der Kationenaustauschsäule mit 120 mM NaCl. Im Durchbruch der Säule befindet sich eine Substanz, die zwar UV-Licht absorbiert, jedoch laut SDS-Gelelektrophorese keine nennenswerten Mengen Nukleinsäuren oder Protein enthält. Möglicherweise handelt es sich hier um kleine Bruchstücke von Proteinen und RNA/DNA. Das Eluat enthält gereinigtes OEP16 in einer Konzentration von 0,5-1 mg/ml. Es dient als Ausgangslösung für die im Folgenden beschriebenen Experimente zur Faltung des Proteins in seine native Struktur. Faltungsmethoden Zunächst soll die Wechselwirkung von OEP16 mit verschiedenen Detergenzien betrachtet werden. Das Protein wird in präparativem Maßstab in einem Puffersystem mit 6 M Harnstoff gereinigt. Der Harnstoff, ein sogenanntes chaotropes Reagenz, verhindert die Sekundärstrukturbildung. Dies geschieht sowohl durch das Aufbrechen von Wasserstoffbrückenbindungen des Proteinrückrates, die für α-Helix- und β-FaltblattStrukturen hauptsächlich verantwortlich sind, als auch durch das Stören von Wechselwirkungen zwischen benachbarten Aminosäureseitenketten. Um diese Wirkung aufzuheben und gleichzeitig einen Einbau des Proteins in Detergenzmizellen zu erreichen, wurden verschiedene Methoden getestet. Dialyse Ähnlich zu den Verfahren zur Liposomenherstellung kann man die Protein-Harnstofflösung mit Detergenz versetzen und den Harnstoff anschließend durch Dialyse entfernen. Dabei gilt es zu beachten, daß Detergenzmizellen im Gleichgewicht mit Detergenzmonomeren in der Lösung stehen. Detergenzien mit kurzem hydrophobem Alkylrest haben im allgemeinen eine hohe CMC (kritische mizellare Konzentration), solche mit einem langen hydrophoben Rest eine niedrige. Oberhalb dieser Konzentration bilden sich Mizellen, eine konstante Konzentration an monomerem Detergenz in der Lösung bleibt aber erhalten. Benutzt man Dialysemembranen mit einem Ausschlußvolumen kleiner als die Mizellengröße, können nur 42 Detergenzmonomere bei der Dialyse entfernt werden. In der Probe lösen sich Mizellen auf, um eine konstante Monomerkonzentration entsprechend der CMC aufrechtzuerhalten. Die Dialysegeschwindigkeit hängt generell vom Konzentrationsgefälle über die Dialysemembran ab. Im Falle von Detergenzien ist das Gefälle und damit die Geschwindigkeit der Detergenzentfernung um so höher, je höher die CMC und damit die Konzentration an monomerem Detergenz in der Probe ist. Membranproteine können durch Detergenzmizellen solubilisiert und in Lösung gehalten werden. Eine Membranproteinlösung muß also unbedingt eine Detergenzkonzentration oberhalb der CMC enthalten. Unterhalb dieser Konzentration neigen die hydrophoben Proteine dazu, zu denaturieren und zu aggregieren. In der Dialyse muß also dem Dialysepuffer Detergenz zugesetzt werden, um die Konzentration konstant zu halten. Da hochreine Detergenzien sehr teuer sind, kann das Zusetzen von Detergenz zum Dialysepuffer ein Nachteil der Dialysemethode sein, insbesondere bei Detergenzien mit hoher CMC. Andere Detergenzien (solche mit langem hydrophobem Rest) sind aufgrund der geringen Monomerkonzentration und der kinetischen Stabilität der Mizellen durch Dialyse nur sehr langsam entfernbar und somit für diese Methode besser geeignet. Generell ist die Dialyse ein langsamer Prozeß, bei dem die Harnstoffkonzentration in einem Zeitraum von Stunden auf ein Minimum herabgesetzt wird. Alle Experimente zur Rekonstitution durch Dialyse wurden mit Membranen durchgeführt, die 3500 Da Porenweite besitzen. Die enge Porenweite ist notwendig, um sicherzustellen, daß denaturierte Proteinstränge nicht durch die Membran dringen können. Für das korrekt gefaltete Protein sollten Membranen mit 10 bis 12 kDa Ausschlußgrenze ausreichend sein. Der Proteinlösung in Harnstoffpuffer wurde die notwendige Menge hochkonzentrierter Detergenz-Stammlösung zugesetzt, um die für das Folgeexperiment benötigte Endkonzentration an Detergenz zu erhalten ohne das Protein unnötig zu verdünnen. Die Lösung wurde anschließend in Dialyseschläuche oder in Dialysebuttons (Hampton Research) gefüllt und diese gegen 5 l Dialysepuffer dialysiert. Die Dialysemethode führte generell zu denselben Ergebnissen wie das Verdünnen des Proteins (siehe dort). Besonders für die Probenvorbereitung zur CD-Spektroskopie erwies sie sich als hilfreich, weil störende Pufferkomponenten wie z.B. Harnstoff komplett entfernt werden können. Wegen des verhältnismäßig hohen Zeitaufwandes wurde jedoch bei einem Großteil der Experimente die Verdünnungsmethode bevorzugt. 43 Gelfiltration Gelfiltrationsmaterialien sind grobkörnige Matrizes, die von Poren definierten Durchmessers durchzogen werden. Partikeln, die in diese Poren eindringen können, steht ein größeres Aufenthaltsvolumen zur Verfügung, kleine Partikel wandern also langsamer durch eine Gelfiltrationssäule als große. Um Protein aus einer Harnstofflösung mittels Gelfiltration in eine Detergenzlösung zu überführen, muß die Säule mit dem detergenzhaltigen Puffer äquilibriert werden. Das Protein wandert schneller als der Harnstoff durch das Säulenbett und wird dadurch in das Laufpuffersystem überführt. Ein Nachteil dieser Methode ist, daß die oft recht hydrophoben Matrizes der Gelfiltrationsmaterialien stark mit Detergenzien wechselwirken. Detergenz im Laufpuffer bindet an die Säulenmatrix, der eluierende Puffer hat eine unbekannte Detergenzkonzentration. Auch wechselwirken hydrophobe Proteine häufig mit dem Gelfiltrationsmaterial. Die Methode ist schneller als die Dialysemethode, aber in vielen Fällen konnte die Adsorption von Protein an das Säulenmaterial beobachtet werden, mit Substanzverlusten bis zu 100% je nach Gelfiltrationsmaterial und verwendetem Detergenz. Für OEP16 konnte kein Gelfiltrationsmaterial gefunden werden, das akzeptable Wiederfindungsraten des Proteins erbrachte. Getestet wurden verschiedene Sephadex-Materialien (G10, G25 und G50) sowie analytische Gelfiltrationssäulen mit Superdex-Matrix (Superdex75 und Superdex200). Von den Superdexsäulen konnte das Protein erst mit 0,5M NaOH wieder entfernt werden. Bei den Sephadexmaterialien fand sich nach dem Lauf nur etwa 10-20% des eingesetzten Proteins wieder, der Rest eluierte erst mit 0,5 M NaOH oder 30% Isopropanol. Verdünnung Die einfachste und schnellste Methode zur Verringerung hoher Harnstoffkonzentrationen ist das Verdünnen mit detergenzhaltigem Puffer. Dem Protein wird schlagartig ein Großteil des denaturierenden Harnstoffs entzogen (siehe auch Abbildung 11 weiter unten), gleichzeitig kommt es mit Detergenzmizellen in Kontakt. Nachteil ist, daß auch das Protein entsprechend verdünnt wird und oft für spektroskopische Messungen anschließend wieder ankonzentriert werden muß. Große Vorteile bieten die Geschwindigkeit und einfache Handhabbarkeit der Methode. 44 Während den Versuchen zeigte sich, daß – abgesehen von Substanzverlusten bei der Gelfiltration – die angesprochenen Methoden alle bei der Wahl eines geeigneten Detergenz zu erfolgreicher Rekonstitution von OEP16 führen können. Leider ist es nur mittels IRSpektroskopie möglich, genaue Aussagen über die Rekonstitutionseffizienz, also das Verhältnis von ungefaltetem zu gefaltetem Protein in einer Probe zu machen. Da die IRSpektroskopie (siehe dort) aber hohe Probenkonzentrationen benötigt, ist eine Festlegung auf die effizienteste Methode der Rekonstitution nicht möglich. Im Folgenden wurde daher meist die einfachste und schnellste Methode, die Verdünnung, verwendet, um mittels verschiedener spektroskopischer Methoden die korrekte Faltung des Membranproteins OEP16 nachzuweisen. Fluoreszenzspektroskopie Kann eine Substanz Lichtquanten bestimmter Wellenlänge absorbieren, so ist der resultierende angeregte Zustand nur von kurzer Lebensdauer. Die Rückführung der elektronischen Struktur in den energetisch günstigeren Grundzustand kann unter Aussendung von Licht erfolgen. Der Grundzustand ist im allgemeinen durch ein Elektronenpaar gekennzeichnet, das nach dem Pauli-Prinzip antiparallele Spins trägt. Kommt es bei der Anregung durch Lichtabsorption zur Spinumkehr bei einem der Elektronen, bildet sich durch diesen quantenmechanisch eigentlich verbotenen Übergang ein Triplett-Zustand. Der Übergang dieses Triplett-Zustandes in den Grundzustand unter Emission von Licht wird als Phosphoreszenz bezeichnet. Verläuft die Anregung ohne Spinumkehr, entsteht ein SingulettZustand, dessen Rückführung in den Grundzustand Fluoreszenz genannt wird. Wegen der erforderlichen erneuten, „verbotenen“ Spinumkehr ist die Lebensdauer der Phosphoreszenz deutlich größer als die der Fluoreszenz. Fluoreszenz wird zumeist bei aromatischen und heterozyklischen Molekülen mit zwei oder mehr kondensierten Ringen beobachtet. Da die angeregten Singulett-Zustände solcher Moleküle eine höhere Polarität als ihr Grundzustand besitzen, zeigen sie eine stärkere DipolWechselwirkung mit polaren Lösungsmitteln. Die Folge davon ist, daß die FluoreszenzEmission gegenüber dem Absorptionsspektrum des Grundzustandes zu größeren Wellenlängen verschoben wird als in unpolaren Lösungsmitteln. Die DipolWechselwirkungen stabilisieren den angeregten Zustand, die Energie des emittierten Lichts ist 45 geringer. Somit kann man aus dem Fluoreszenz-Emissionsspektrum eines Moleküls auf die Polarität seiner Umgebung schließen. In Proteinen ist Tryptophan die Aminosäure, die aufgrund hoher Fluoreszenzausbeute, einem Absorptionsmaximum von 280 nm (ε280 = 5600 cm-1M-1) und ihrer relativen Seltenheit innerhalb einer Proteinsequenz als intrinsische Fluoreszenzprobe am häufigsten untersucht wird(Chen, 1998). Potentiell fluoreszieren auch die aromatischen Aminosäuren Phenylalanin (ε280 < 100 cm-1M-1) und Tyrosin (ε280 < 1000 cm-1M-1) , wegen ihrer geringeren Extinktionskoeffizienten im Wellenlängenbereich um 280 nm können sie aber für die im folgenden gezeigten Fluoreszenzspektren vernachlässigt werden. Da Tryptophan im Protein in eine lange Kette von Aminosäuren eingebaut ist, bestimmt sich die Hydrophobizität seiner Umgebung selten durch das Lösungsmittel, sondern im allgemeinen aus der Aminosäurezusammensetzung seiner Umgebung im gefalteten Protein. Bei Membranproteinen ist zusätzlich zu beachten, daß Tryptophanreste, die aus der Proteinstruktur herausragen und so Kontakt mit dem Lösungsmittel haben, potentiell auch im transmembranen Bereich des Proteins angesiedelt sein können und somit mit der Lipiddoppelschicht einer Membran oder – nach Solubilisierung – mit der hydrophoben Detergenzmizelle wechselwirken können. Auch die Fluoreszenzintensität der einzelnen Tryptophanreste in einem Protein kann sich deutlich unterscheiden. So ist bekannt, daß die Aminosäuren Lysin und Tyrosin sowie Cystein und, schwächer, Glutamin, Asparagin, Glutaminsäure, Asparaginsäure und (protoniertes) Histidin die Fluoreszenz von Tryptophan quenchen können(Chen, 1998). Auch die Halbwertsbreite des Fluoreszenzpeaks von Tryptophanresten kann Informationen über deren Umgebung liefern. Grundsätzlich ist der Emissionspeak um so schmaler, je kleiner die Wellenlänge des Emissionsmaximums ist. Diese Abhängigkeit ist linear und kann genutzt werden, um vergleichsweise breite Fluoreszenzspektren aus mehreren Tryptophan-Resten eines Proteins in ihre Bestandteile zu zerlegen und somit auf die Umgebung des einzelnen Tryptophans zurückzuschließen(Burstein, 1973). Abbildung 10 zeigt diesen Effekt in einem sehr einfachen Experiment. 46 346 344 Wellenlänge [nm] 342 340 338 336 334 332 330 328 326 0 2 4 6 8 10 12 Kettenlänge des primären Alkohols Abbildung 10: Die Abbildung zeigt die Fluoreszenz von reinem L-Tryptophan in verschiedenen primären Alkoholen. Je hydrophober das Lösungsmittel ist, desto stärker blauverschoben ist die Fluoreszenz bei konstanter Anregungswellenlänge von 280 nm. Die Aminosäuresequenz von OEP16 aus Erbse enthält zwei Tryptophanreste(Pohlmeyer, 1997a). Beide liegen laut den verschiedenen Strukturvorhersagen im Bereich transmembraner Proteinsegmente und sollten bei korrekter Proteinfaltung mit dem hydrophoben Medium (entweder der Lipiddoppelschicht oder der Detergenzmizelle) in Kontakt treten. Man erwartet also eine Blauverschiebung der Fluoreszenz gegenüber dem ungefalteten Protein in 6M Harnstoff. Bekannt ist, daß Harnstoff seine denaturierende Wirkung oft erst bei Konzentrationen über 1 M entfalten kann. Korrekte Faltung eines tryptophanhaltigen Membranproteins sollte eine maximale Blauverschiebung der Fluoreszenz als Zeichen maximaler Exposition der Tryptophanreste zum hydrophoben Medium zur Folge haben. Abbildung 11 zeigt die Abhängigkeit der Tryptophanfluoreszenz von OEP16 von der Harnstoffkonzentration (bei konstanter Detergenzkonzentration). 47 355 Wellenlänge [nm] 350 345 340 335 0 1 2 3 4 5 6 Harnstoffkonzentration [M] Abbildung 11: Tryptophanfluoreszenz von OEP16 in Abhängigkeit von der Harstoffkonzentration. Aufgetragen wurden die Maxima der Flureszenzspektren. Es zeigt sich hier am Beispiel des Detergenz C12E8, daß die Blauverschiebung von OEP16 bereits bei Harnstoffkonzentrationen unter 2M maximal ist. Eine Verdünnung auf ein zehntel der Harnstoffkonzentration von 6 M auf 600 mM ist also in jedem Falle ausreichend, um eine hohe Faltungseffizienz zu erreichen – vorausgesetzt, daß die Blauverschiebung ein geeignetes Maß für die korrekte Faltung ist. Bevor dies abschließend geklärt wird, sollen zunächst die Unterschiede zwischen verscheidenen Detergenzien und Detergenzklassen untersucht werden. 48 Abbildung 12: Fluoreszenzspektren von OEP16 in Harnstoff (Spektrum A1), in den Detergenzien β-D-Octylglykosid (1% w/v, Spektrum A2) und C12E8 (0,03% w/v, Spektrum A3), und in Liposomen (Spektrum B4). Bei letztgenanntem Spektrum handelt es sich um ein Differenzspektrum, gemessen gegen Liposomen ohne Protein. Abbildung 12 zeigt die Fluoreszenzspektren von OEP16 in Harnstoff (Spektrum A1), in den Detergenzien β-D-Octylglykosid (1% w/v, Spektrum A2) und C12E8 (0,03% w/v, Spektrum A3), und in Liposomen (Spektrum B4). Das Spektrum in Harnstoff zeigt ein Fluoreszenzmaximum bei 355 nm, die Spektren in Detergenz zeigen ein Maximum bei 335 nm. Bei dem Spektrum in Liposomen handelt es sich um ein Differenzspektrum. Leere Liposomen, hergestellt aus S-IV-Lipid (siehe Material und Methoden), haben eine beträchtliche Eigenfluoreszenz. Für die Aufnahme des Differenzspektrums wurde eine gleich behandelte Probe leerer Liposomen gemessen, und das resultierende Spektrum von einem OEP16-Spektrum in Liposomen abgezogen. Auch das Differenzspektrum hat ein Emissionsmaximum bei 335 nm Wellenlänge. Das Spektrum in β-D-Oktylglycosid zeigt eine deutliche Schulter. Man kann sich vorstellen, daß diese Schulter durch Überlagerung eines blauverschobenen Spektrums (des gefalteten Proteins) und eines rotverschobenen Spektrums (des ungefalteten Proteins) entsteht. Daraus kann geschlossen werden, daß die Probe in 1% Octylglycosid vermutlich noch beträchtliche Anteile denaturierten Proteins enthält. Das Spektrum in 0,03% C12E8 hingegen entspricht recht gut dem Spektrum in Liposomen, auch wenn der Fluoreszenzpeak etwas schmaler zu sein scheint. Möglicherweise enthält auch die Liposomenpräparation noch aggregiertes, 49 denaturiertes Protein. Dies zeigt sich deutlicher in den FTIR-Spektren an vergleichbaren Proben (siehe dort). Offensichtlich kann die Fluoreszenz allein nur Hinweise auf geeignete Faltungprotokolle geben. Zwar kann qualitativ gezeigt werden, ob sich Protein zu seiner nativen Struktur faltet, ein Maß für die Effizienz der Faltungsmethode oder eine Quantifizierung des Anteils ungefalteten Proteins ist nicht gegeben. Dennoch ist die Tryptophanfluoreszenz hilfreich, um schnell viele verschiedene Detergenzien in unterschiedlichen Konzentrationen auf ihre Eignung, OEP16 in eine native Struktur zu überführen, zu testen. 120000 ß-DM C12E8 C12E6 C8E4 ß-OG SB12 C10E6 Harnstoff Fluoreszenz [a.u.] 100000 80000 60000 40000 20000 0 250 300 350 400 450 500 Wellenlänge [nm] Abbildung 13: Fluoreszenzspektren von OEP16 in verschiedenen Puffersystemen. Alle Detergenzkonzentrationen betragen 1% (w/v), Die Proteinkonzentration lag bei 0,05 mg/ml. In Abbildung 13 sind die Fluoreszenzspektren von OEP16 in verschiedenen Detergenzien gleicher Konzentration (1% w/v) abgebildet. Deutlich zu sehen ist, daß die Detergenzien Octylglycosid, SB12 und C12E8 ein Fluoreszenzmaximum von 335 nm erzeugen, dem Wert, der auch in Liposomen gemessen wurde (siehe auch Abbildung 12). Die Schulter im Oktylglycosid-Spektrum ist in dieser Darstellung nicht deutlich zu erkennen. Um so stärker 50 kann man einen Doppelpeak im Spektrum mit β-D-Dodecylmaltosid sehen. Offensichtlich überwiegt hier sogar der Anteil an fehlgefaltetem bzw. ungefaltetem Protein. Die Detergenzien C8E4 und C10E6 zeigen eine noch ausgeprägtere Blauverschiebung der Spektren. Eine Verschiebung über den Wert in Liposomen hinaus kann aber nicht wünschenswert sein. Auch zeigten die Proben in diesen Detergenzien eine schwache Trübung, die auf Aggregation des Proteins hindeutet. Es scheint, als hätten Detergenzien mit glycosidischen Kopfgruppen vergleichbare Effekte (Spektren mit zwei Peaks), während Detergenzien mit Polyetherkopfgruppe alle einen einzigen, vergleichsweise schmalen Peak mit maximaler Blauverschiebung liefern. Das zwitterionische Detergenz SB12 scheint denselben Einfluß auf das Fluoreszenzspektrum von OEP16 zu haben wie C12E8. Dies hat sich besonders für kalorimetrische Messungen als hilfreich erwiesen (siehe unten). Im nächsten Schritt soll aufgeziegt werden, welchen Einfluß die Konzentration der Detergenzien auf die Faltung von OEP16 hat. 120 ß-DM (0,03%) ß-DM (0,3%) ß-DM (1%) ß-OG (0,1%) ß-OG (0,3%) ß-OG (1%) Harnstoff 6M Fluoreszenz [a.u.] 100 80 60 40 20 0 250 300 350 400 450 500 Wellenlänge [nm] Abbildung 14: Fluoreszenzspektren von OEP16 in verschiedenen glykosidischen Detergenzien. ß-DM: ßDodecylmaltosid, ß-OG: ß-Octylglukosid 51 C10E6 (0,3%) C12E8 (0,3%) C12E6 (0,3%) C8E4 (0,3%) Harnstoff 6M Fluoreszenz [a.u.] 60 40 20 0 250 300 350 400 450 500 Wellenlänge [nm] Abbildung 15: Fluoreszenzspektren von OEP16 in verschiedenen Detergenzien mit Ether-Kopfgruppen. Beispielhaft gezeigt sind die Spektren für eine Detergenzkonzentration von 0,3%. Eine Variation der Detergenzkonzentration veränderte die Spektren nicht. Die glykosidischen Detergenzien zeigen eine Konzentrationsabhängigkeit der Fluoreszenzverschiebung. β-OG verschiebt die Fluoreszenz von OEP16 unterhalb seiner CMC von 0,7% w/v weniger stark als oberhalb seiner CMC (Abbildung 14). In vivo baut sich ungefaltetes OEP16 selbsttätig in die äußere Chloroplastenmembran ein. Geht man davon aus, daß Detergenzmizellen die Membranoberfläche und -struktur simulieren können, kann eine Proteinfaltung nur oberhalb der CMC – also in Anwesenheit von Mizellen – erfolgen. Unterhalb der CMC läßt sich eine geringe Blauverschiebung der Fluoreszenz durch Anlagerung von Detergenzmonomeren an die hydrophoben Bereiche des Proteins erklären. Möglicherweise entstehen dabei bereits Teilstrukturen, die sich aber nicht zur nativen Struktur zusammenlagern können. Der bereits gezeigte breite Peak oberhalb der CMC von β-OG deutet an, daß auch hier mehrere Faltungszustände existieren könnten. Offensichtlich ist die Faltung unvollständig. 52 β-DM hingegen zeigt bei hohen Konzentrationen einen weiteren Effekt. Es scheint, als könnten auch hohe Detergenzkonzentrationen Fehlfaltung verursachen. Deutlich zu sehen ist ein Doppelpeak im Spektrum bei einer Detergenzkonzentration von 1%. Offensichtlich liegt hier zu etwa gleichen Teilen gefaltetes und ungefaltetes Protein vor. Interessant ist auch die Zunahme der Fluoreszenz bei steigender Detergenzkonzentration. Die Ursache hierfür könnte eine Abnahme der Proteinaggregation bei steigender Detergenzmenge sein. In diesem Fall würde die Fluoreszenz weniger gequencht. Die Detergenzien mit Etherkopfgruppe zeigen ein ganz anderes Bild. Hier sind die Fluoreszenzintensitäten praktisch unabhängig von der Detergenzkonzentration (Abbildung 15 zeigt deshalb nur je eine beispielhaft ausgewählte Konzentration), und auch die Unterschiede zwischen den Detergenzien unterschiedlicher Alkylkettenlängen und Kopfgruppengrößen sind geringer. Die beiden Detergenzien C10E6 und C8E4 zeigen eine noch stärkere Blauverschiebung als die beiden langkettigen Tenside und auch stärker als die Verschiebung in Liposomen. Leider trübten diese Lösungen bei jedem Versuch, höhere Proteinkonzentrationen zu erreichen, stark ein, was eine Eignung zur korrekten Faltung unwahrscheinlich macht (Aggregatbildung). Die hohe Verschiebung der Fluoreszenz kommt vermutlich durch Anlagerung der kleinen Detergenzmoleküle im Bereich der Tryptophanreste zustande. 53 Abbildung 16: Schematische Darstellung der Faltung von OEP16 mit Nebenreaktionen. Abbildung 16 zeigt ein einfaches Modell für die Vorgänge beim Falten von OEP16. Aus den Inclusionbodies, die sehr große Proteinaggregate sind, wird monomeres, entfaltetes Protein hergestellt. Durch Versetzen mit Detergenz oder Lipid kann dieses Protein in seine native Struktur überführt werden. Hierbei enstehen unbekannte Mengen an Aggregaten als unerwünschtes Nebenprodukt. Diese zeigen sich in der Fluoreszenz durch Verbreiterung der Fluoreszenzpeaks bzw. durch Nebenmaxima. In Liposomen lassen sich die Aggregate druch IR-Spektroskopie nachweisen (siehe dort). Außer Acht gelassen wird in der Abbildung die Möglichkeit von Intermediaten, die nur zum Teil die korrekte Struktur annehmen. Es ist denkbar, daß diese unterhalb der CMC (z.B. bei Octylglucosid) durch Anlagerung monomerer Detergenzmoleküle entstehen können. Die kurzkettigen Etherdetergenzien C10E6 und C8E4, 54 die die Fluoreszenz trotz offensichtlicher Aggregation des Proteins oberhalb ihrer CMC stark verschieben, lagern sich möglicherweise als Monomere in die Aggregate ein. Geht man davon aus, daß für eine vergleichsweise gute Rekonstitutionsrate der Fluoreszenzpeak von OEP16 in Detergenz möglichst schmal sein soll (also keine Nebenmaxima haben darf, die auf Fehlfaltung hindeuten), dieselbe Verschiebung wie das Spektrum in Liposomen haben soll (wo die Proteinaktivität nachgewiesen wurde) und eine möglichst hohe Intensität haben sollte (weil auch Fluoreszenzquenching auf Aggregation des Proteins hinweist), scheinen C12E8 und C12E6 besonders geeignet. Dies gilt es nun mittels anderer Methoden zu überprüfen. CD-Spektroskopie Bei der CD-Spektroskopie nutzt man die Tatsache, daß optisch aktive Substanzen nicht nur mit linear, sondern auch mit zirkular polarisiertem Licht wechselwirken können. Die Extinktionskoeffizienten εL und εR für links und rechts zirkular polarisiertes Licht unterscheiden sich, die eigentliche Meßgröße ist die Differenz der Extinktionskoeffizienten, die positive und negative Werte annehmen kann. Praktisch gibt man die sogenannte Elliptizität Θλ an, die wie folgt definiert ist: tan Θλ = IR − IL IR + IL Hierbei sind I die Intensitäten des rechts und links zirkular polarisierten Lichts nach der Absorption durch die Probe. Die Elliptizität ist wellenlängenabhängig (daher der Index λ) und erlaubt somit das Aufnehmen von Spektren. Unter Berücksichtigung von Schichtdicke und Probenkonzentration kann man auch eine molare Elliptizität ΘM in Abhängigkeit von der Wellenlänge angeben. CD-aktive Substanzen zeichnen sich durch große, übergeordnete Strukturen aus. Insbesondere bei Proteinen kann die CD-Spektroskopie wertvolle Informationen über den Sekundärstrukturgehalt liefern. Während ein denaturiertes, ungeordnetes Protein nur wenig Auslenkung des CD-Signals zeigt, haben α-Helices und β-Faltblätter deutlich voneinander unterscheidbare Maxima und Minima im CD-Spektrum. Der Meßbereich liegt hierbei etwa zwischen 250 und 180 nm. Die Untergrenze des Meßbereichs wird hierbei durch Geräteparameter festgelegt. Wird die UV-Absorption der Probe zu hoch, verschlechtert sich 55 das Signal-Rausch-Verhältnis. Proben, die unter 200 nm gemessen werden sollen, dürfen keine im UV absorbierenden Substanzen (außer dem Protein) enthalten und sollten möglichst verdünnt und in geringen Schichtdicken verwendet werden. Problematisch ist ebenfalls die UV-Absorption durch Luftsauerstoff in diesem Wellenlängenbereich, weshalb die Apparatur ständig mit Stickstoff gespült wird. Die Proben für die Fluoreszenzspektroskopie enthalten viele störende Substanzen, z.B. NaCl und Reste von Harnstoff. CD-Spektren dieser Proben sind deshalb bei niedrigen Meßwellenlängen verrauscht, in 6M Harnstoff läßt sich ein CD-Spekrum z.B. nur bis zu einer Wellenlänge von etwa 220 nm aufnehmen. Enthält ein Protein α-Helices, was für OEP16 postuliert wurde, zeigen diese jedoch bereits in einem Wellenlängenbereich zwischen 230 bin 220 nm ein deutliches CD-Signal. Für eine erste Einschätzung der Sekundärstrukturbildung mit Hilfe von Detergenzien kann es also genügen, Spektren in diesem Wellenlängenbereich aufzuzeichnen, um schnell und einfach viele Proben miteinander vergleichen zu können. Abbildung 17: CD-Spektren von OEP16. A: in 6M Harnstoff; B: in 1% ß-OG; C: in 0,5% ß-DM; D: in 1% SB12; E: in 0,3% C12E8. Abbildung 17 zeigt CD-Spektren von OEP16 in verschiedenen Detergenzien. Selbst in 6M Harnstoff ist im untersuchten Wellenlängenbereich ein schwaches CD-Signal zu sehen. Offensichtlich sind selbst in 6 M Harnstoff Teilstrukturen ausgebildet, oder es liegen zum Teil Aggregate vor, die (wie im Kapitel IR-Spektroskopie deutlich wird) geordnete Strukturen ausbilden können. Die unterschiedlichen Detergenzien ergeben bei gleicher Proteinkonzentration sehr unterschiedliche CD-Signale. Offensichtlich ist die Sekundärstrukturbildung für das Tensid C12E8 besonders ausgeprägt, dicht gefolgt von SB12. Die beiden glykosidischen Detergenzien β-OG und β-DM zeigen nur wenig Änderung gegenüber dem Spektrum in Harnstoff. Verschiedene Aspekte sind jedoch zu beachten: 56 Die Proben wurden zwar gleich behandelt, wurden aber nach der Rekonstitution mit Konzentratoren, also Ultra-Filtrationseinheiten, ankonzentriert. Substanzverluste an den Filtern oder den Kunststoffgehäusen der Zentrifugationseinheiten könnten also zumindest teilweise mitverantwortlich sein für die unterschiedlichen Auslenkungen der CD-Spektren. Da eine Proteinbestimmung in dem verwendeten Puffersystem praktisch nicht durchführbar ist (Detergenzien, Harnstoff und Reduktionsmittel wie β-Mercaproethanol stören praktisch alle Methoden der kolorimetrischen Proteinbestimmung), kann dies jedoch nicht quantitativ nachvollzogen werden. Die Proben könnten Aggregate enthalten, die keine korrekte Struktur ausgebildet haben, aber dennoch einen Beitrag zum CD-Spektrum liefern. Tatsächlich war in vielen der Proben eine schwach Trübung erkennbar, die auf Aggregation hinweist. Um ein CD-Spektrum zu erhalten, das auf den Sekundärstrukturgehalt von OEP16 quantitative Schlüsse zuläßt, musste die Probe anders vorbereitet werden. Es galt, sämtliche UV-aktiven Substanzen zu entfernen. Dies geschah mit Hilfe von Dialysezellen und einer Dialysemembran von 3.500 kDa Porengröße, die weder für OEP16 noch für Mizellen des Detergenz (hier C12E8) durchlässig ist. Harnstoff, Reduktionsmittel, Salze und Puffersubstanzen werden durch einen Puffer aus 10 mM Natrium-Cacodylat und 50 mM NaSO4 ersetzt. Die Probe wird zur Entfernung potentiell noch enthaltener Aggregate zusätzlich filtriert. Das resultierende CD-Spektrum, aufgenommen in einer Tonnenküvette mit 0,1 mm Schichtdicke, ist in Abbildung 18 gezeigt. 57 6 Elliptizität [mdeg] 4 2 0 -2 -4 180 190 200 210 220 230 240 250 260 270 Wellenlänge [nm] Abbildung 18: CD-Spektrum von 0,5 mg/ml OEP16 in 0,3% C12E8. Als Puffersystem wurde 50 mM Natriumcacodylat, pH 7,0 mit 50 mM Natriumsulfat verwendet. Man sieht in dem Spektrum, aufgenommen in 0,3% C12E8, deutlich, daß sich immer noch eine hohe UV-Absorption oder Lichtstreuung, vermutlich ausgelöst durch das Detergenz, im Bereich unterhalb von 200 nm Wellenlänge störend auswirkt. Dennoch läßt sich mit Hilfe der Auswertsoftware des CD-Spektrometers oder anderen im Internet zur Verfügung stehenden Programmen der Anteil der verschiedenen Sekundärstrukturelemente berechnen. Je nach verwendeter Software liegt der α-Helixgehalt von OEP16 demnach bei 35-50%, bei variablem Gehalt an Loops und Turns. Anteile von β-Faltblattstrukturen sagte keines der verwendeten Programme voraus. Wegen der Ungenauigkeit der Methode nicht nur wegen des verrauschten Spektrums, sondern auch wegen der Tatsache, daß sämtliche CD-Rechenalgorithmen auf Vergleichsdaten löslicher Proteine basieren, sind diese Ergebnisse für das Membranpotein OEP16 mit Vorsicht zu betrachten. Der Befund, daß OEP16 keine β-Faltblattanteile besitzt, widerspricht den existenten Strukturmodellen. Daher wurde zur Verifizierung eine weitere Methode, die Auskunft über den Sekundärstrukturgehalt eines Proteins geben kann, angewendet. 58 IR-Spektroskopie Bei der Fourier-Transform-Infrarotspektroskopie (FTIR) wird anders als in gewöhnlichen IRSpektrometern nicht der Wellenlängenbereich abgetastet, sondern simultan ein großer Wellenlängenbereich bestrahlt. Mit einem Interferometer werden die Änderungen von Interferenzen erfaßt, die durch Absorption einzelner IR-Banden entstehen. Dieses Interferogramm kann mittels Fouriertransformation in ein komplettes IR-Spektrum umgerechnet werden. Hauptvorteil dieser Methode ist die Geschwindigkeit, mit der ein Spektrum aufgezeichnet werden kann, sowie die hohe Strahlintensität und damit ein geringeres Rauschen. Proteine haben charakteristische IR-Absorptionsbanden. Insbesondere die Amid-I-Bande (gemessen in D2O im Wellenzahlenbereich von 1600-1700 cm-1), die hauptsächlich von den C=O-Streckschwingungen der Carbonylgruppe im Polypeptidrückrad herrührt, wird maßgeblich von der Sekundärstruktur des Proteins beeinflußt. Dies rührt daher, daß die Carbonylgruppe je nach Sekundärstruktur unterschiedliche Wasserstoffbrückenbindungen eingehen kann. α-Helices zeigen charakteristische Amid-I-Banden im Bereich von 1650-1658 cm-1, während typische β-Faltblattstrukturen im Bereich um 1620-1640 cm-1 absorbieren. Loopstrukturen (1670-1680 cm-1) und ungeordnete Bereiche (1640-1650 cm-1) haben ebenfalls charakteristische Absorptionsbanden. 59 Abbildung 19: Zweite Ableitung des Infrarotspektrums von OEP16 in Phosphatidylcholinvesikeln. Die Proteinkonzentration betrug nach Lyophillisieren und Wiederaufnehmen in D2O mindestens 10 mg/ml Gezeigt ist ein typisches FTIR-Spektrum von OEP16 in seiner zweiten Ableitung. Das in Liposomen rekonstituierte und in D2O überführte Protein zeigt vier markante Banden bei 1658, 1648, 1622 und 1512 cm-1. Eine weitere Bande (bei 1587 cm-1) ist möglicherweise auf die Lipidkopfgruppen in den Liposomen zurückzuführen. Für Proteine ist eine Absorption in diesem Wellenzahlenbereich nicht bekannt(Winter, 1998). Die Bande bei 1512 cm-1 entspricht der Schwingung der Hydroxylgruppe der Tyrosine in OEP16. Diese Bande wird durch unterschiedliche Sekundärstrukturen nicht beeinflußt und gibt Auskunft über die Proteinmenge. Die im Folgenden diskutierten Banden entsprechen alle der Carbonyl-Streckschwingung der Amidbindung im Proteinrückgrat, die sich nur durch ihre unterschiedliche chemische Umgebung unterscheiden. Die Bande bei 1648 cm-1 liegt in einem Bereich, der typisch für Loop-Strukturen ist, wie sie als Verbindungen zwischen transmembranen Segmenten zu erwarten sind. Bei 1658 cm-1 absorbieren α-Helices. Diese Bande ist sehr markant und entspricht dem Ergebnis aus der 60 CD-Spektroskopie, daß OEP16 praktisch ausschließlich aus helikalen Strukturen besteht. Die letzte Absorptionsbande bei 1622 cm-1 liegt in einem Wellenzahlenbereich, der üblicherweise β-Faltblattstrukturen vorbehalten ist. Dieses Ergebnis ist zunächst unerwartet. Betrachtet man jedoch mehrere Spektren unterschiedlich präparierter Liposomenproben, stellt man fest, daß das Verhältnis der beiden Banden bei 1648 cm-1 und 1658 cm-1 zu der β-Faltblattbande (normiert auf die Tyrosinbande) variabel ist. Das bedeutet: der Sekundärstrukturgehalt der Probe in Liposomen variiert mit der Probenpräparation. FTIR-Messungen in Detergenzlösung zum direkten Vergleich sind nicht möglich, weil in Detergenz die notwendigen Probenkonzentrationen nicht erreicht werden können. Mißt man eine OEP16-Probe in Detergenz, die bis zur Aggregation ankonzentriert wurde (also stark getrübt ist), sieht man neben der Tyrosinbande praktisch nur die Bande bei 1622 cm-1. Wie im Kapitel über die Fluoreszenz bereits andiskutiert, enthalten insbesondere die Liposomen-Proben also größere Mengen aggregiertes und fehlgefaltetes Protein. Vermutlich sind diese Aggregate nicht in die Lipiddoppelschichten eingebaut, sondern nur lose daran assoziiert. Diese Aggregation zeigt sich im IR als Bande bei 1622 cm-1, eine Wellenzahl, bei der typischerweise antiparallele β-Faltblattstrukturen absorbieren, z.B. solche aus Aggregationsfibrillen. Solche Fibrillen entstehen aus fehlgefalteten Membranproteinen unter anderem bei Prionenkrankheiten (Scrapie(Callahan, 2001), BSE und die Creutzfeld-JakubKrankheit, aber auch Alzheimer und Parkinson(Conway, 2000)). Transmembrane Faltblattstrukturen, wie sie hauptsächlich in Porinen vorkommen, absorbieren bei höheren Wellenzahlen (ab 1630 cm-1)(Abrecht, 2000). Während für OEP16 in Detergenzlösung mittels CD-Spektroskopie eine rein α-helikale Struktur nachgewiesen werden konnte, sind in Liposomen-Proben noch beträchtliche Anteile an ungefaltetem bzw. fehlgefaltetem Protein enthalten. Diese zeigen sich in der Fluoreszenzspektroskopie als eine Nebenbande bei höherer Wellenlänge, die das Gesamtspektrum scheinbar verbreitert. In der IR-Spektroskopie sind die Aggregate als antiparallele β-Faltblattstrukturen mit einem Absorptionsmaximum von 1622 cm-1 nachweisbar. Offensichtlich handelt es sich bei den Aggregaten um Strukturen, wie sie auch von vielen anderen aggregierten Membranproteinen bekannt sind. Es wurde gezeigt, daß sich OEP16 in Lösung wie in Liposomen korrekt falten läßt. Spektroskopische Methoden zeigten auch, daß OEP16 hauptsächlich aus α-Helices besteht. In 61 den folgenden Abschnitten werden physikalisch-chemische Experimente zur Proteinstabilität und Faltung vorgestellt. Biophysikalische Daten des gefalteten Proteins DSC Die Differenzkalorimetrie beruht auf der Messung der Wärmekapazität einer Probe gegenüber der bekannten Wärmekapazität einer Referenz. Probe und Referenz werden während der Messung kontinuierlich aufgeheizt, wobei die Heizquellen so eingestellt sind, daß die Temperatur in der Probenzelle etwas langsamer ansteigt als in der Referenzzelle. Ein Thermoelement kontrolliert die resultierende Temperaturdifferenz zwischen den Meßkammern und regelt eine Hilfs-Heizquelle. Die Heizleistung P (Energie pro Zeit), die benötigt wird, um die Temperaturdifferenz zwischen Referenz und Probe auszugleichen, wird genutzt, um die Wärmekapazität bei konstantem Druck cP zu bestimmen. In die Berechnung geht die Geschwindigkeit der Temperaturerhöhung χ=∆T/t wie folgt ein: cP = Pχ −1 Man erhält eine Kurve, die die Änderung der Wärmekapazität cP in Abhängigkeit von der Temperatur darstellt. Eine solche Änderung erwartet man zum Beispiel bei einem Phasenübergang. Da cP als partielle Ableitung der Enthalpie ∆H nach der Temperatur bei konstantem Druck definiert ist, kann man durch Integration der Fläche unter der gemessenen Kurve die Enthalpie eines Phasenüberganges berechnen. Spektroskopische Methoden haben gezeigt, daß OEP16 eine dem nativen Zustand entsprechende Konformation annehmen kann, wenn es in detergenzhaltigen Puffer eingebracht wird. Da dieser Faltungsprozeß freiwillig abläuft, muß er mit einem Gewinn an freier Energie verbunden sein. Diese freie Energie setzt sich aus einem Enthalpie- und einem Entropieanteil zusammen, es gilt: ∆G( Faltung ) = ∆H ( Faltung ) − T∆S( Faltung ) 62 Die Entropieänderung für den betrachteten Prozeß dürfte in erster Linie aus dem hydrophoben Effekt entstehen. Das hydrophobe Protein begibt sich in die hydrophobe Umgebung der Mizelle, während es zuvor dem Wasser eine geordnete Struktur um seine hydrophoben Bereiche aufgezwungen hat. Die Enthalpieänderung setzt sich aus verschiedenen Anteilen zusammen. 1. Das Protein faltet sich in seine Sekundärstrukturelemente. Hierbei werden viele Wasserstoffbrückenbindungen gebildet. Unabhängig davon, ob es sich um α-Helices oder βFaltblattstrukturen handelt, dürfte dies den größten Anteil der Enthalpieänderung ausmachen. 2. Das Protein "löst" sich im Detergenz, die neuen Wechselwirkungen mit der Proteinumgebung werden sich in der Enthalpieänderung niederschlagen. 3. Eventuell lagern sich mehrere Proteineinheiten unter Ausbildung unterschiedlicher Wechselwirkungen zusammen. Erhitzt man das gefaltete Protein in Detergenzlösung in einem geeigneten Kalorimeter, kann man die Denaturierungswärme des Proteins bestimmen. Diese entspricht dem Umkehrprozeß der genannten Effekte, mit dem Unterschied, daß das hitze-denaturierte Protein möglicherweise in der Detergenzmizelle verbleibt - oder aggregiert und aus der Lösung ausfällt. In einem Diferenziellen "Scanning"-Kalorimeter (DSC) wurden 0,55 mg/ml OEP16 in verschiedenen Detergenzlösungen graduell bis auf 95°C erwärmt. Gemessen wurde die Änderung der Wärmekapazität der Lösung gegenüber einer Referenzlösung, die nur die detergenzhaltige Pufferlösung ohne Protein enthielt. Die Enthalpieänderung entspricht bei dieser Messung der Fläche unter einem eventuell auftretenden Denaturierungspeak. Vor allem Proteinkomplexe mit mehreren Untereinheiten können schrittweise danaturieren, haben also mehrere Denaturierungspeaks. Das Detergenz C12E8 lieferte ein starkes, aber extrem verrauschtes Denaturierungssignal bei ca. 85°C. Da das Detergenz in diesem Temperaturbereich bei der gegebenen Konzentration von 0,3% selbst eine Phasenumwandlung durchmacht(Mitchell, 1983), ist die Enthalpieänderung in diesem Fall praktisch nicht auswertbar. 63 Das Detergenz SB12 hingegen zeigt keine Phasenumwandlungen im genannten Temperaturbereich. In SB12 läßt sich die Denaturierungswärme von OEP16 somit bestimmen. Abbildung 20: DSC-Diagramme von 0,3 mg/ml OEP16 in 0,5% SB12. Das obere Bild zeigt die Denaturierungskurve ohne Zusatz von Harnstoff. Im unteren Bild verschiebt sich der Denaturierungspeak durch die Zugabe von 1,5 M Harnstoff zu einer geringeren Temperatur. Teil A der Abbildung 20 zeigt die Denaturierungskurve von OEP16 in 1% SB12. Die Denaturierungstemperatur liegt bei 85°C, und entspricht damit der gemessenen Denaturierungstemperatur für C12E8. Um zu zeigen, daß der auftretende Peak tatsächlich auf das Protein und dessen Entfaltung zurückzuführen ist, wurde eine vergleichbare Probe in 1% SB12 mit 1,5 M Harnstoff versetzt (Teil B der Abbildung). Die Denaturierungstemperatur wird durch den Harnstoff auf 67°C gesenkt, bei praktisch gleicher Denaturierungenthalpie von 580 kJ/mol. Harnstoff ist als chaotropes Reagenz dafür bekannt, intramolekulare Wechselwirkungen in Proteinen aufbrechen zu können. Die Konzentration von 1,5 M Harnstoff reicht dazu bei Raumtemperatur nicht aus (Siehe Kapitel Fluoreszenz). Während die Energie der Denaturierung gleich bleibt, wird das Protein bereits bei einer geringeren Wärmezufuhr entfaltet. Der Harnstoffpuffer gemessen gegen Wasser zeigte keinerlei Änderung der gemessenen Wärmekapazität über den gesamten Temperaturbereich. 64 Die Faltungsenthalpie von OEP16 liegt bei ca. 600 kJ/mol. Die Hitzedenaturierung erfolgt in einem einzigen Schritt und ist irreversibel, weil das Protein anschließend aggregiert und ausfällt (zu sehen an der Trübung der Probe). Der umgekehrte Prozeß, die Faltung des Proteins, läßt sich demnach kalorimetrisch nicht verfolgen. Messen läßt sich allerdings bei geeignetem Versuchsaufbau die Geschwindigkeit der Proteinfaltung. Dadurch sind Rückschlüsse auf die Aktivierungsenergie des Faltungsprozesses und auf seine Reaktionsordnung möglich. Zeitaufgelöste Spektroskopie Um Prozesse wie die hier untersuchte Proteinfaltung besser verstehen zu können, ist es hilfreich, nicht nur statische Spektren des gefalteten und entfalteten Zustandes zu messen, sondern auch die Veränderung während dem Prozeß zu verfolgen. Im Prinzip sind bei geeignetem Versuchsaufbau solche zeitaufgelösten Messungen mit jeder spektroskopischen Methode möglich. Oft macht aber eine zu geringe Empfindlichkeit der notwendigen Detektoren das Messen schneller Prozesse sehr schwierig. Im Verlauf dieser Arbeit wurden zeitaufgelöste Messungen mit Fluoreszenz- und CDDetektion durchgeführt. Die Meßprinzipien dieser beiden spektroskopischen Methoden wurden bereits erläutert. Der Versuchsaufbau ist abgesehen vom unterschiedlichen Detektor für beide Methoden identisch. Zur Vereinfachung der Messung wird nur eine feste Wellenlänge detektiert, anstatt zu jedem Zeitpunkt ein komplettes Spektrum aufzunehmen. Sinnvollerweise wählt man diese Wellenlänge in einem spektralen Bereich, in dem die größten Änderungen zwischen Anfangs- und Endzustand zu erwarten sind. Der Übergang von einem Zustand zum anderen wird durch schnelles Vermischen zweier Lösungen in einer druckbetriebenen Mischkammer, einer sogenannten "stopped-flow" Apparatur erreicht. Diese Mischkammer dient gleichzeitig als Meßküvette, in der nach einer gerätebedingten Totzeit die Änderung des Meßsignals erfaßt werden kann. Zeitaufgelöste Fluoreszenzspektroskopie Es konnte bereits gezeigt werden, daß sich die Fluoreszenz der Tryptophanreste in OEP16 signifikant ändert, wenn sich die native Struktur des Proteins bildet. Der Faltungsprozeß ist jedoch so schnell, daß sich mit einem herkömmlichen Spektrometer lediglich der Anfangs65 und Endzustand der Strukturbildung sichtbar machen läßt. Der zeitliche Verlauf der Faltung kann aber wertvolle Hinweise auf Übergangszustände liefern. Messungen bei hoher Zeitauflösung werden durch das Verfolgen der Fluoreszenzänderung von OEP16 bei 334 nm Wellenlänge in einer „stopped-flow“ Apparatur ermöglicht. Es zeigt sich, daß der Faltungsprozeß innerhalb von 100 ms vollständig abläuft. 7,6 Fluoreszenz [a.u.] 7,4 7,2 -1 k1 = 809 ± 74 s -1 k2 = 127 ± 7 s 7,0 -1 k3 = 10.3 ± 0.3 s 6,8 6,6 0,0 0,1 0,2 0,3 0,4 0,5 Zeit [s] Abbildung 21: Stopped-flow-Experiment mit Fluoreszenzdetektion. Gezeigt ist ein typisches Signal für die Mischung einer 0,7 mg/ml OEP16-Lösung in 6 M Harnstoff, 1:10 verdünnt mit 0,01% C12E8 bei Raumtemperatur. Gezeigt ist hier die Fluoreszenzänderung bei der schnellen Mischung einer OEP16-Lösung (0,7 mg/ml) in 6 M Harnstoff mit Detergenzpuffer (hier 0,01% C12E8). Mehrere Prozesse können unterschieden werden. Sie lassen sich durch nichtlineare Regression mathematisch erfassen. Die besten Anpassungen an die Meßkurve erhält man mit einer Näherungskurve aus drei exponentiellen Prozessen erster Ordnung. Der schnellste Prozeß hat dann (für 0,01% C12E8) eine Zeitkonstante von k1 = 809 ± 74 s-1. Dieser Prozeß wird bei steigender Detergenzkonzentration schneller als die Zeitauflösung des Geräts und kann somit nicht mehr 66 erfaßt werden. Um seinen Einfluß auf die Berechnung der anderen beiden Prozesse zu minimieren wurden alle Näherungskurven erst ab t = 3 ms angepaßt; zu diesem Zeitpunkt ist der schnellste Prozeß vollständig abgelaufen. Die beiden weiteren Prozesse haben für die gezeigte Detergenzkonzentration die Zeitkonstanten k2 = 127 ± 7 s-1 und k3 = 10,3 ± 0,3 s-1. Vor der Auswertung und Erklärung der einzelnen Prozesse muß nun zuerst einmal verifiziert werden, daß es sich bei den Fluoreszenzänderungen tatsächlich um strukturbildende Veränderungen handelt. Hierzu werden die Messungen mit zeitaufgelöster CD-Detektion wiederholt. Zeitaufgelöste CD-Spektroskopie -11 k1 = 1785 ± 450 s Ellipticity [mdeg] -12 k2 = 86 ± 23 s -1 -1 k3 = 14.6 ± 2.5 s -1 -13 -14 -15 0,00 0,05 0,10 0,15 0,20 Time [s] Abbildung 22: Stopped-flow-Experiment mit CD-Detektion. Gezeigt ist ein typisches Signal für die Mischung einer 0,7 mg/ml OEP16-Lösung in 6 M Harnstoff, 1:10 verdünnt mit 0,01% C12E8. Abbildung 22 zeigt eine typische Meßkurve für die Strukturbildung von OEP16, erfaßt mit einem CD-Detektor. Die mittels nichtlinearer Regression ermittelten Zeitkonstanten entsprechen den Zeitkonstanten, die mittels Fluoreszentdetektion gewonnen wurden. Damit ist gezeigt, daß alle als Fluoreszenzänderung erfaßten Prozesse mit einer Strukturbildung 67 einhergehen und nicht etwa allein durch das Mischen mit detergenzhaltigem und damit hydrophobem Puffer zustandekommen. Zeitkonstanten und Aktivierungsenergien Es konnte gezeigt werden, daß sich Faltungs-Teilprozesse einzeln erfassen lassen. Dies funktioniert gut für das Detergenz C12E8 bis zu Konzentrationen um 0,03% w/v. Bei höheren Detergenzkonzentrationen werden die Prozesse so schnell, daß eine präzise Berechnung von Zeitkonstanten nicht mehr möglich ist (jedenfalls nicht mit den gegebenen Meßgeräten). Ähnliches gilt auch für andere Detergenzien, der Faltungsprozeß läßt sich im Prinzip auch bei β-Dodecylmaltosid und SB12 verfolgen, ebenfalls nur bei niedrigen Konzentrationen. Da die Faltungsausbeute bei diesen Detergenzien etwas niedriger ist, sind die Signalintensitäten entsprechend geringer und die Berechnungen ungenauer. Den schnellsten Prozeß (und eventuell noch schnellere, gar nicht erfaßte Prozesse) kann man bei diesen Detergenzien wie auch bei relativ hohen C12E8-Konzentrationen gar nicht beobachten. Trotz dieser Einschränkungen lassen sich eine Reihe von Ergebnissen aus den zeitaufgelösten Messungen gewinnen. Diese werden im Folgenden ausschließlich für das Detergenz C12E8 näher ausgeführt, da es sich als das für die Faltung von OEP16 geeignetste Detergenz erwiesen hat. Zunächst wird die Änderung der Zeitkonstanten mit steigender Detergenzkonzentration betrachtet: 68 70 60 50 -1 1/τ [s ] 40 30 CMC klangsam 20 10 0 0,000 0,005 0,010 0,015 0,020 0,025 0,030 C12E8 [% w/v] 800 -1 1/τ [s ] 600 400 CMC kschnell 200 0 0,000 0,005 0,010 0,015 0,020 0,025 0,030 C12E8 [% w/v] Abbildung 23: Abhängigkeit der errechneten Zeitkonstanten von der Detergenzkonzentration. Der dritte, schnellste Prozeß ist nur bei einer Detergenzkonzentration um 0,01% sichtbar und ist hier nicht berücksichtigt. 69 In Abbildung 23 kann man deutlich erkennen, daß die Geschwindigkeitskonstanten der Prozesse 2 und 3 linear von der Detergenzkonzentration abhängen. Über einen Konzentrationsbereich von einer Größenordnung (gemessen in einem Konzentrationsbereich von 0,08 bis 0,8 mg/ml OEP16 Ausgangskonzentration) sind sie jedoch unabhängig von der Proteinkonzentration. Unterhalb der CMC von C12E8 läßt sich keine Fluoreszenzänderung messen, was darauf hindeutet, daß das Vorhandensein von Mizellen (und nicht von Detergenz-Monomeren) entscheidend für eine erfolgreiche Faltung von OEP16 ist. In Abbildung 24 werden nun die Amplituden der Teilprozesse in Abhängingkeit von der Detergenzkonzentration betrachtet. 45 40 Amplitude [mV] 35 30 25 20 Amplitude (schneller Prozeß) Amplitude (langsamer Prozeß) CMC 15 10 5 0 0,000 0,005 0,010 0,015 0,020 0,025 0,030 C12E8 [% w/v] Abbildung 24: Amplituden der Faltungsprozesse von OEP16. Der dritte, schnellste Prozeß ist nicht berücksichtigt. Während die Zeitkonstanten lediglich Auskunft über die Geschwindigkeit der einzelnen Prozesse geben, veranschaulichen die Amplituden der Näherungsfunktionen den Anteil der einzelnen Prozesse am Gesamtsignal. 70 Es wird deutlich, daß Prozeß 2 erst bei höheren Detergenzkonzentrationen dominiert, während der langsamste Prozeß 3 dort praktisch nicht mehr meßbar ist. Beide Amplitudenänderungen lassen sich als exponentieller Zusammenhang zwischen Meßgröße und Detergenzkonzentration darstellen. In beiden Fällen nähern sich die exponentiellen Kurven nicht der Abszisse, sondern der kritischen mizellaren Konzentration (CMC) asymptotisch an. Unterhalb dieser Konzentration – also ohne die Gegenwart von Detergenzmizellen – kann der Faltungsprozeß nicht stattfinden, die Amplituden und die Zeitkonstanten selbst betragen 0. Oberhalb dieser Konzentration werden die Prozesse um so schneller, je mehr Detergenz im Puffer zur Verfügung steht. Bei noch höheren Detergenzkonzentrationen stirbt der langsamere der beiden Prozesse aus. Möglicherweise handelt es sich hierbei um einen Übergangszustand, der nur unter relativem Detergenz-Mangel bzw. bei einem Mangel an verfügbaren Detergenzmizellen auftritt. Zuletzt soll die Temperaturabhängigkeit der Geschwindigkeitskonstanten gezeigt werden. Aus der Abhängigkeit der Reaktionsgeschwindigkeit von der Temperatur läßt sich die Aktivierungsenergie eines Prozesses nach Arrhenius berechnen: k = A∗e − EA RT ⇔ EA = −R ∗ ln k1 − ln k 2 1 − 1 T1 T2 Hierbei ist EA die Aktivierungsenergie des Teilprozesses, A der sogenannte Stoßfaktor oder Arrhenius-Faktor, eine Größe aus der statistischen Themodynamik, und R die allgemeine Gaskonstante. Durch Auftragung der logarithmierten Zeitkonstanten gegen den Kehrwert der Temperatur läßt sich die Aktivierungsenergie als Steigung der resultierenden Geraden ablesen (Abbildung 25). 71 5,2 5,0 ln klangsam 4,8 4,6 4,4 4,2 4,0 0,0032 0,0033 0,0034 0,0035 0,0036 1/T [1/K] 7,2 7,0 ln kschnell 6,8 6,6 6,4 6,2 6,0 5,8 0,0032 0,0033 0,0034 0,0035 0,0036 1/T [1/K] Abbildung 25: Arrhenius-Darstellungen der Temperaturabhängigkeit der Geschwindigkeitskonstanten. Gemessen wurde in einem Temperaturbeteich zwischen 10° und 35°C 72 Die Aktivierungsenergien betragen, abgelesen aus Abbildung 25 bzw. gewonnen aus den Daten der liearen Regression der Datenpunkte, EA = 27 ± 4 kJ mol-1 für den schnelleren Prozeß und 20 ± 3 kJ mol-1 für den langsameren Prozeß. Das Protein wird sichtbar Bisher wurde gezeigt, daß OEP16 in E.coli überexprimiert und in denaturiertem Zustand gereinigt werden kann, um es anschließend in seine native Form zurückzufalten. Die zugehörigen strukturbildenden Prozesse konnten detailliert untersucht werden. All dies sind notwendige Voraussetzungen, um die Struktur des Proteins im Detail aufklären zu können. Die folgenden Untersuchungen widmen sich direkt der Strukturbestimmung. Elektronenmikroskopie Bei der Elektronenmikroskopie macht man sich zu nutze, daß sich Elektronen nach De Broglie auch wie Wellen verhalten können. Die Wellenlänge eines Elektrons ist umgekehrt proportional zu seinem Impuls p = mev : λ= h me v wobei h das Plancksche Wirkungsquantum und me die Masse des Elektrons sind. Die Geschwindigkeiten der Elektronen bei dieser Methode sind so regelbar, daß man Wellenlängen um 10-3 nm erreicht. Bei einer Apertur von etwa 10-3 für Elektronenmikroskope ergibt sich eine um etwa einen Faktor von 1000 bessere Auflösung gegenüber einem Lichtmikroskop. Anders als in der Lichtmikroskopie muß der optische Weg des Elektronenmikroskops evakuiert sein, da Elektronen durch Gase sehr stark gestreut werden. Ansonsten ist der Aufbau eines Elektronenmikroskops mit dem eines Lichtmikroskops durchaus vergleichbar. Anstelle einer Lichtquelle wird eine Glühkathode als Elektronenquelle eingesetzt. Kondensor, Objektiv und Okular werden durch elektromagnetische Linsen ersetzt, und sichtbar gemacht wird das Abbild der Probe mittels eines durch Elektronen anregbaren Leuchtschirms. Kontrast entsteht in der Transmissions-Elektronenmikroskopie durch die Streuung und Absorption von Elektronen an dem Untersuchungsobjekt in Abhängigkeit von dessen Masse und Dicke. Der 73 Kontrast kann durch Zugabe von geeigneten Kontrastmitteln verstärkt werden. Im Falle von Protein-Proben benutzt man häufig Schwermetalle, die bei der Probenvorbereitung an die Moleküle binden und sowohl Streuung als auch Absorption den Elektronenstrahls verstärken. Man spricht in diesem Fall von „negative stain“, da man ein Negativabbild des Proteins erhält. Transmissions-Elektronenmikroskopie kann, bei geeigneter Wahl eines Kontrastmittels, einzelne Proteinpartikel sichtbar machen und – wenn auch bei vergleichsweise niedriger Auflösung – Strukturinformationen liefern. Besonders geeignet ist diese Methode, wenn es gelingt, aus dem elektronenmikoskopischen Abbild des Proteins auf dessen Orientierung im Raum zu schließen. In diesem Fall kann man mit Hilfe moderner Computermethoden hunderte von Aufnahmen mitteln und so ein dreidimensionales Bild des Proteins generieren. OEP16, rekonstituiert in C12E8, wurde mit Phospho-Wolframsäure als Kontrastmittel in einem Kryo-Elektronenmikroskop bei maximaler Vergrößerung (siehe Material und Methoden) abgebildet. Das Ergebnis ist in Abbildung 26 gezeigt. Abbildung 26: Elektronenmikroskopische Aufnahme von OEP16-Partikeln. Der Balken entspricht 30 nm. Man sieht deutlich die einzelnen Proteinpartikel, der Maßstab in der unteren rechten Bildecke entspricht 30 nm. Die Partikel haben also einen Durchmesser von etwa 5 nm. Dieser Wert ist für ein Protein von 16-48 kDa Größe (je nach dem ob es sich um ein Monomer, Dimer oder Trimer handelt), sinnvoll. Bemerkenswerterweise taucht derselbe Wert als röntgenkristallographische Größe im Folgenden nocheinmal auf (siehe Abschnitt Kristallisation). Bedauerlicherweise sind die Partikel damit zu klein für detailliertere Strukturaussagen oder 3D-Rekonstitutionsmethoden. Die Methode der 3D-Rekonstitution aus 74 Einzelbildern wird ständig verbessert, höher auflösende Elektronenmikroskope und automatisierte Bildbearbeitung werden möglicherweise schon in naher Zukunft bessere Resultate auch mit kleinen Proteinen ermöglichen. Aus dem Experiment lassen sich aber dennoch Strukturinformationen gewinnen. Man kann bei einzelnen Partikeln eine Kleeblatt-ähnliche Form, also eine dreizählige Symmetrieachse ausmachen. Bisherige Strukturmodelle gehen von einem Dimer (mit gemischter α-Helix/βFaltblattstruktur(Pohlmeyer, 1997a)) oder von einem Tetramer (reiner β-Faltblattkanal mit assoziierten Helices(Steinkamp, 2000)) aus. Beides macht eine dreizählige Symmetrieachse unmöglich. Der Partikeldurchmesser von 5 nm würde zu einem Trimer passen, betrachtet man das durchschnittliche Volumen von Proteinen entsprechender Größe (etwa 50 kDa). Die bisher diskutierten spektroskopischen Messungen erlauben keine Aussage über die Oligomerisierung von OEP16. Es ist denkbar, daß einer der kinetischen Prozesse aus den zeitaufgelösten Messungen einer Oligomerisierung von OEP16-Monomeren entspricht. Auch die Kalorimetrie zeigte keinen separaten Monomerisierungs-Prozeß, durch den sich auf die Enthalpie der Oligomer-Bildung hätte schließen lassen. Möglicherweise geschehen Denaturierung und Aggregation in der Hitze ohne vorherigen Zerfall in Monomere. Um das Problem des Oligomerisierungszustandes von OEP16 zu lösen, wurde versucht, das Protein zu kristallisieren und seine Struktur mittels Röntgenstrukturanalyse zu bestimmen. Kristallisation Die Kristallisation und anschließende Röntgenstrukturanalyse ist nach wie vor die effektivste Methode, um zu hochauflösenden Proteinstrukturen zu gelangen. Inzwischen gibt es allerdings eine ganze Reihe von Strukturen, die mittels Elektronenmikroskopie und – kristallographie sowie mit Kernspinresonanzmethoden (NMR) gelöst wurden. Hauptnachteil der klassischen Kristallisationsmethoden ist der enorme Zeit- und Materialaufwand. Die Kristallisation von Membranproteinen folgt im Prinzip denselben Regeln wie die löslicher Proteine. Die Kristallisation erfolgt aus einer übersättigten Lösung, wenn die freie Enthalpie ∆G für diesen Vorgang einen negativen Wert annimmt. Die Übersättigung kann sowohl durch Erhöhung der Proteinkonzentration als auch durch andere Faktoren, die die Löslichkeit des Proteins beeinflussen, erreicht werden. 75 Detergenzien Bei der Kristallisation von Membranproteinen wird deren Löslichkeit natürlich maßgeblich von den verwendeten Detergenzien beeinflußt. Dies geschieht auch durch Wechselwirkung des Detergenz mit den verschiedenen Salzen und Kristallisationszusätzen. Oft kristallisieren Membranproteine dadurch, daß die Löslichkeitsgrenze des Detergenz (und nur indirekt die des darin gelösten Proteins) unterschritten wird. Auf diesem Prinzip beruht auch die Kristallisation von OEP16. Erste Kristallisationsexperimente wurden mit OEP16, rekonstituiert in C12E8, durchgeführt. Um eine möglichst hohe Proteinkonzentration zu erreichen, wurde das gefaltete Protein in Puffer mit gesättigter Ammoniumsulfatlösung im Verhältnis 1:1 versetzt und dabei präzipitiert. Das Protein wurde in Wasser wiederaufgenommen, so daß das Endvolumen einem zehntel des Ausgangsvolumens entsprach. Die erhaltene Lösung wurde abzentrifugiert, um Aggregate abzutrennen und mit den Pufferlösungen der Kristallisationsansätze versetzt. Es wurde die Methode der hängenden Tropfen genutzt. Hierbei wird ein kleiner Tropfen der Proteinlösung mit Puffer hängend an einem Deckglas angebracht, der mittels Dampfdiffusion mit einem Pufferreservoir in Kontakt steht. Die Salzkonzentration im Reservoir ist höher als im Tropfen, so daß Salz- und Proteinkonzentration während des Diffusionsprozesses im Tropfen zunehmen. Hierbei wird idealerweise eine Übersättigung der Proteinlösung erreicht und so die Bildung von Kristallen ermöglicht. Variiert werden die Parameter pH, Salztyp und Salzkonzentration, die Konzentration von Präzipitationsadditiven wie Polyethylenglykol oder hydrophoben Alkoholen und – bei Membranproteinen – potentiell auch das Detergenz und dessen Konzentration. Für OEP16 in C12E8 zeigten sich folgende Änderungen der Löslichkeit in Abhängigkeit von physikochemischen Parametern: pH Der pH-Wert beeinflußt direkt die Oberflächenladung des Proteins. Saure und basische Aminosäurereste können protoniert oder deprotoniert werden. Häufig ist die Löslichkeit eines Proteins am geringsten im pH-Bereich um seinen isoelektrischen Punkt. Hier hat das Protein 76 nach außen keine Nettoladung mehr und wandert entsprechend nicht mehr im elektrischen Feld. OEP16 hat einen berechneten isoelektrischen Punkt von 9, seine Löslichkeit sollte mangels eigener Nettoladung bei einem pH um etwa 9 am geringsten sein. Bei den Kristallisationsexperimenten konnte Präzipitation und die Bildung von Mikrokristallen bei allen untersuchten pH-Werten im Bereich von 4,5 bis 9,5 beobachtet werden. Dabei zeigte sich jedoch wie erwartet, daß die Präzipitation bei höheren pH-Werten bei niedrigeren Fällungsmittelkonzentrationen erfolgt. Temperatur Wie praktisch bei allen Lösungen hängt die maximale Löslichkeit von Proteinen auch von der Temperatur ab. Es läßt sich nicht sicher vorhersagen, ob ein Protein bei höheren Temperaturen besser oder schlechter löslich ist als bei niedrigen. Da auch die meisten Kristallisationszusätze abhängig von der Temperatur das Phasendiagramm des Proteins unterschiedlich beeinflussen, werden in der Praxis meist Kristallisationsansätze parallel bei verschiedenen Temperaturen gemacht, um empirische Daten über das Temperaturverhalten zu bekommen. OEP16 wurde bei verschiedenen Temperaturen kristallisiert. Zur Verfügung standen ein Temperierschrank bei 18°C und ein Kühlraum mit 4°C Innentemperatur. Im allgemeinen waren bei 4°C Phasentrennung und Proteinpräzipitation deutlich ausgeprägter. Die Zitratansätze (siehe später), die doppelbrechende OEP16-Kristalle lieferten, wurden ebenfalls bei den verscheidenen Temperaturen angesetzt. Die deutlich besseren Kristalle wurden bei 18°C erhalten. Möglicherweise ging die Phasentrennung bei 4°C so schnell, daß eine geordnete Kristallisation des Proteins dort verhindert wurde. Präzipitationszusätze So genannte Kristallisationszusätze sind zumeist organische Moleküle oder Lösungsmittel, die Wasser binden oder ordnen (hydrophober Effekt). Dem Protein steht weniger Wasser zur Verfügung, seine Löslichkeit wird herabgesetzt. Typische Kristallisationszusätze dieser Art sind mehrwertige Alkohole wie Glyzerin oder MPD (2-Methyl-2,4-Pentandiol) oder Polyethylenglykole. 77 In Gegenwart von Polyethylenglykolen kurzer Kettenlänge (z.B. PEG 400) bildeten sich in den OEP16-Ansätzen zwei nicht mischbare flüssige Phasen aus, während Zusatz von sehr langkettige PEGs (ab etwa PEG 6000) meist zu amorpher Präzipitation des Proteins führten. PEGs mittlerer Kettenlänge verursachten im allgemeinen Beides, d.h. Phasentrennung bei gleichzeitigem amorphem Niederschlag. Die Löslichkeit des Proteins nahm mit steigendem pH auch hier ab. Dennoch konnte in keinem Fall mit PEG Kristallwachstum induziert werden. Zusatz von Alkoholen wie MPD (2-Methyl-2,4-Paentandiol) verursachten eine Trübung der Proteinlösung bei 4°C, bei 18°C einen amorphen Niederschlag. Es ist anzunehmen, daß die Trübung von einer Denaturierung und anschließenden Aggregation der Proteinmoleküle herrührt. Ionenstärke Die Ionenstärke einer Lösung beeinflußt die Löslichkeit von Proteinen maßgeblich. Ionen wechselwirken mit geladenen und polaren Gruppen auf der Oberfläche des Proteins. Typischerweise haben Proteine ihre höchste Löslichkeit bei mittleren Ionenstärken. Bei hohen Ionenstärken konkurrieren die Ionen mit dem Protein um das verfügbare Wasser zur Hydratation. Hierbei spielt nicht nur die absolute Ionenstärke, sondern auch der Typ des Ions eine große Rolle, auch weil entstehende Kristallkontakte durch entsprechende Ionen erst vermittelt werden können. Bei niedrigen Ionenstärken hingegen werden Gegenionen der geladenen Aminosäurereste im Protein abgelöst, die durch sie vermittelte Abschirmung entfällt und das Protein kann durch direkte Kontakte aggregieren bzw. kristallisieren. Komplettes Entfernen aller ionischen Pufferkomponenten durch Dialyse gegen Wasser führte nicht zu einer ausreichenden Verringerung der Löslichkeit von OEP16, eingesetzt in einer Konzentration von ca. 1 mg/ml. Als Kristallisiationsmethode kommt diese Methode also nur bei noch höheren (bei OEP16 z.Z. nicht erreichbaren) Proteinkonzentrationen in Betracht. Starkes Anheben der Ionenstärke hatte im Gegensatz dazu dramatische Effekte auf die Löslichkeit von OEP16. Die Löslichkeit ist unter den beobachteten Bedingungen generell bei 4°C niedriger als bei 18°C. Mikrokristalle bildeten sich in Gegenwart verschiedener Salze, wobei die Art des Salzes ebenso wichtig ist wie seine Konzentration. Es konnte gezeigt werden, daß der Einfluß verschiedener Anionen auf die Löslichkeit des Proteins deutlich ausgeprägter als der der verwendeten Kationen ist. Am schwächsten ist der Einfluß von Chlorid, stärker der von Phosphat und Sulfat-Ionen. Am deutlichsten senkte Citrat die 78 Löslichkeit von OEP16. Kleine Kristalle von OEP16 konnten mit Citrat in einem pH-Bereich von 6,5 bis 9,5 beobachtet werden, wobei die Größe der Kristalle mit steigendem pH zunahm. Betrachtete man die Kristallisationsansätze regelmäßig, so konnte man feststellen, daß nach etwa 48 Stunden eine Phasentrennung eintritt, bei der sich zähe, ölige Tropfen in der wäßrigen Lösung ausbildeten, die vermutlich in erster Linie aus dem Detergenz C12E8 bestehen. Manche dieser Tropfen wandelten sich dann im Laufe von Tagen langsam in kantige Kristalle um. Citratkonzentrationen unter 1M führten nicht zu Phasentrennung bei 4°C. Bei 18°C genügte zur Phasentrennung eine Konzentration von 800 mM Citrat. Die erhaltenen Kristalle wurden fotografiert, zum Teil röntgenkristallographisch untersucht und mittels SDS-Gelelektrophorese analysiert. Abbildung 27: Gelelektrophoretische Analyse der OEP16-Kristalle. Rechts sind die Banden der Markerproteine angedeutet. Spur A enthielt den Überstand der Kristallisationsansätze. Spur B enthält die plättchenförmigen Kristalle, aufgenommen in SDS-Probenpuffer. Spur C enthält die Tröpfchen (siehe auch Abbildung 25), soweit sich diese vom Überstand trennen ließen. Im Gel sieht man neben den Markerproteinen eine Lösung aus den Kristallen, dem Überstand des Ansatzes und der kleinen, nicht polarisierenden öligen Tropfen, jeweils vor dem Auftragen in SDS-Probenpuffer erhitzt. Nur die Kristalle enthalten nennenswerte Mengen an OEP16. Die öligen Tropfen wurden beim Erhitzen so zäh, daß sie sich kaum auf das Gel auftragen ließen. Es ist anzunehmen, daß diese Tropfen aus einer detergenzreichen Phase bestehen. Der Überstand enthält praktisch kein Protein mehr. 79 Abbildung 28: Kristallisationsansatz von OEP16 in 1 M Natriumzitrat. Bild A zeigt den Ansatz in normalem Licht, Bild B unter polarisiertem Licht. Abbildung 28 zeigt OEP16-Kristalle. Sie wurden mit 1 M Natriumcitrat und 100 mM CAPSO-Puffer bei pH 9,5 in C12E8 gezüchtet. Oben wurden die Kristalle unter normalem Licht fotografiert, unten unter polarisiertem Licht. Deutlich zu sehen ist, daß die kantigen 80 Kristalle die Ebene des polarisierten Lichts drehen können und somit leuchten, während die kleinen, „öligen“ Tropfen das nicht tun. Die Kristalle sind sehr flach und haben eine Abmessung von 100-200 µm Länge, 50-100 µm Breite und nur etwa 10 µm Dicke. Die gezeigten Kristalle ergaben nur ein extrem schwaches Beugungsbild. Röntgendiffraktion konnte bis zu einer Auflösung von 2 nm beobachtet werden. Schon ein zweites Beugungsbild nach Drehen des Kristalls um 1° zeigte praktisch keine Diffraktion mehr, der Kristall wurde im Röntgenstrahl also zerstört. Dennoch läßt sich aus den ersten Beugungsbildern die Gitterdimension der Elementarzelle in einer der Raumrichtungen auf 5,7 nm abschätzen. Dies paßt sehr gut zu dem elektronenmikroskopisch gefundenen Partikeldurchmesser. Um bessere Beugungsbilder zu erhalten müssen Bedingungen gefunden werden, unter denen die Kristalle größer und vor allem stabiler werden. Auch eine geeignete Kryolösung, in der sich die Kristalle ohne Eisbildung einfrieren lassen, konnte bisher nicht gefunden werden. Getestet wurden Lösungen mit 10-30% Glyzerin, 1-2 M Sucrose oder Glukose sowie Trehalose. In jeder dieser Lösungen waren die Kristalle nicht stabil. Bei weiterführenden Kristallisationsversuchen sollte der Augenmerk vor allem auf die Detergenzkonzentration gelegt werden. Die durch das Detergenz mit Citrat verursachte Phasentrennung ermöglicht zwar erst die Bildung der gezeigten Kristalle. Das in den Kristallen in großer Menge vorhandene Detergenz und möglicherweise auch das überschüssige Detergenz in Lösung dürften aber auch verantwortlich für die weiche Konsistenz und die geringe Stabilität der Kristalle gegen typische Kryoreagenzien sein. Eine Verringerung der Detergenzkonzentration auf Werte, die eine Kristallisation gerade noch erlauben, dürfte stabilere und möglicherweise auch größere Kristalle liefern. Theoretische Ansätze zur Strukturaufklärung In Verlauf dieser Arbeit konnte mit spektroskopischen Methoden gezeigt werden, daß OEP16 eine rein α-helikale Struktur aufweist. Dies widerspricht allen bisherigen Vorstellungen vom Aufbau dieses integralen Membranproteins(Pohlmeyer, 1997a; Steinkamp, 2000). Auch wenn elektronenmikroskopische Untersuchungen und Kristallisationsversuche noch nicht zu einer Auflösung führen, die eine detaillierte Aussage über die Struktur von OEP16 erlaubt, kann aufgrund theoretischer Überlegungen ein neues Strukturmodell erstellt werden. 81 Auch wenn die genaue Vorhersage einer Proteinstruktur allein aus der Primärsequenz zum jetzigen Zeitpunkt unmöglich ist, lassen sich aus den bereits verfügbaren Modellen und Algorithmen viele nützliche Informationen gewinnen. Hilfreich ist es hierbei, mehrere Sequenzen eines Proteins aus unterschiedlichen Organismen zur Verfügung zu haben. Multiple Sequence Alignment Grundvoraussetzung jeder theoretischen Strukturvorhersage ist eine Aminosäuresequenz. Diese ist für OEP16 aus den Organismen Erbse, Gerste und der Ackerschmalwand vollständig bekannt. Da theoretische Ansätze an der Sequenz aus Erbse bisher offensichtlich zu falschen Annahmen führten, sollen im folgenden die Sequenzen aus allen drei Organismen für die Erstellung eines neuen Modells herangezogen werden. Grundvoraussetzung hierfür ist das „Multiple Sequence Alignment“, bei dem die Sequenzen verglichen und homologe Aminosäuren untereinander gestellt werden. Erbse Gerste Arabidopsis 1 1 1 2222222222 2334444444 4444444444 4444444443 2333444444 Homologie Erbse Gerste Arabidopsis MPRSSFSGSL SSPKLDVVID MGNPFLNLTV DGFLKIGAVA ATRSVAEDTF MPTAGLAAG- -SNKVDVAID LGNPLLNRTV DGFLKIGAVG ACRVVAEDAF MPSSTFSGTV STPKLSVAVD MGNPFLNLTV DAFLKIGAVG VTKSLAEDTY 51 49 51 HIIRKGSISS NDFEKSLKKM CKEGAYWGAI AGVYVGMEYG VERIRGTRDW DCLHRGDISK RQLEETLKKM CKEGAYWGAV AGVYVGMEYG VERVRGDRDW KAIDKGSLSK STLEHALKKL CKEGVYWGAA GGVYIGTEYG IERIRGSRDW Homologie 3333333333 3333333555 5555555553 3555555555 5555555555 Erbse 101 Gerste 99 Arabidopsis 101 KNAMFGGAVT GALVSAASNN KKDKIAVDAI TGAAIATAAE FINYLT-KNALIGGIAT GALVSAASNN KGNKIAQDAI TGGAIATAVE FINYLT-KNAMLAGAAT GAVLSAVGKK GKDTIVIDAI LGGALATASQ FVNNHYFY Homologie 5555555335 5555552222 2222222333 3333333333 333222-- Abbildung 29: Die Abbildung zeigt die Sequenzen von OEP16 der verschiedenen Pflanzen. Die Zeile „Homologie“ gibt die Übereinstimmung im betreffenden Bereich an. Augenscheinlich ist die Sequenzhomologie über den gesamten Bereich hoch. Welche Funktion den am besten konservierten Bereichen zukommt (Homologie-Werte von 4-5) und warum, soll im Folgenden geklärt werden. 82 Hydropathie und Vorhersage transmembraner Segmente Hydrophatieplots der OEP16-Sequenz aus Erbse ließen den Schluß zu, daß OEP16 aus drei transmembranen Helices und zwei β-Faltblattstrukturen besteht. Ermittelt man die mittleren Hydrophobizitäten der Aminosäuren aus den bekannten Sequenzen, kann man aus den Mittelwerten einen Hydrophobizitätsplot erstellen, der ein besseres Bild von potentiellen transmembranen Segmenten liefert. In diesem Plot überschreitet der Sequenzbereich etwa um die Aminosäuren 25-43 deutlich den gesetzten Schwellenwert für ein transmembranes Segment, ein Befund, der sich allein aus der Erbsensequenz, aus der die vermeintlichen Faltblattstrukturen abgeleitet wurden, nicht ergibt(Steinkamp, 2000). Die drei transmembranen Segmente in den Sequenzbereichen 70-91, 102-118 und 125-144 bestätigen sich, zusätzlich tritt ein weiterer, hydrophober Bereich am n-Terminus der Sequenz zu Tage. Abbildung 30: Gezeigt ist die mittlere Hydropathie der Aminosäurereste des „multiple sequence alignments“ aus Abbildung 29 83 Was bedeutet das für das Strukturmodell? Da transmembrane (hydrophobe) Sequenzbereiche nach bisherigen Erkenntnissen ausschließlich aus Helices und in Sonderfällen aus antiparallel angeordneten β-Faltblättern bestehen können, OEP16 aber ausschließlich helikalen Charakter hat, sollten die transmembranen Segmente jeweils membranspannende Helix-Strukturen ausbilden. Um dies zu verifizieren, wurde der Algorithmus TMPred angewandt, der erlaubt, Sequenzen mit einer Datenbank bekannter Helix-Strukturen zu vergleichen. Die Ergebnisse dieser Datenbankabfrage sind in Abbildung 29 durch Unterstreichung der entsprechenden Sequenzbereiche dargestellt. Demnach besteht OEP16 aus mindestens vier transmembranen Helices in den Bereichen 25-43, 70-91, 102-118 und 125-144, von hier an Helix I-IV genannt. Der hydrophobe Bereich im n-Terminus ergibt nur für die Arabidopsis-Sequenz eine positive Vorhersage (Aminosäuren 1-19). Vermutlich handelt es sich hier um den Signalbereich, der in Kontakt mit der äußeren Chloroplastenmembran beim Proteinimport eine Helix ausbildet und damit das Einfädeln in die Lipiddoppelschicht initiiert(Pinnaduwage, 1996). Gegen ein echtes transmembranes Segment in diesem Bereich spricht vor allem der experimentelle Befund, daß sich von OEP16 in nativen Erbsenmembranen durch Proteasebehandlung ein etwa 1 kDa großes Stück (etwa 10 Aminosäuren) abspalten läßt(Pohlmeyer, 1997b). Dies kann nur am nTerminus geschehen, da der c-Terminus nach allen bisherigen Ergebnissen in die Membran eingebettet sein muß bzw. kaum aus ihr herausragt. Die bereits postulierten drei transmembranen Helices in den Sequenzbereichen 70-91, 102118 und 125-144 bestätigen sich. Helices III und IV können mittels Mutagenese entfernt werden, ohne die Kanalaktivität zu beeinflussen, ebenso wie der Signalbereich (Reste 1-20). Helix II hingegen wurde lange als entscheidend für die Kanalaktivität betrachtet. Sie hat große Ähnlichkeiten mit Helices aus vielen Aminosäuretransportproteinen aus Bakterien und Säugetieren. Mit diesen gemeinsam hat sie vor allem einen Bereich von fünf jeweils durch drei Aminosäuren getrennten Gylcinresten(Pohlmeyer, 1997b). Auch enthält sie das einzige Cystein der Sequenz (Cys71), das unter oxidativen Bedingungen den Kanal zu schließen vermag – möglicherweise über eine Dimerisierung von OEP16-Untereinheiten. Mutagenese an hydrophilen Resten dieser Helix änderten jedoch nichts an der Kanalaktivität, lediglich ein Austausch des Cysteins gegen einen Serinrest verhinderte die oxidative Zerstörung der Kanalfunktion. Es stellte sich sogar heraus, daß die Helix komplett mittels Mutagenese durch die ebenfalls sehr lange Helix 4 ersetzt werden kann, ohne die Kanalaktivität zu verändern. Damit dürfte ihr lediglich eine strukturelle Bedeutung für den Kanal zukommen, die Selektivität muß von einem anderen Sequenzbereich gesteuert werden. 84 Für den Sequenzbereich 25-43 ist das Ergebnis von TMPred nicht eindeutig. Für die Gerstesequenz wurde hier kein transmembraner Bereich vorhergesagt. Dies liegt vermutlich an der Häufung geladener und polarer Aminosäuren in diesem Bereich, der in der Gerstensequenz noch stärker ausgeprägt ist als in den anderen beiden Sequenzen. Diese polaren Reste dürften auch für die niedrige Hydropathie der Erbsensequenz verantwortlich sein, die dort auf transmembrane β-Faltblätter hindeutete. Tatsächlich dürfte es sich um eine amphiphile Helix handeln, die nur zum Teil in Kontakt mit der hydrophoben Lipidmembran steht, während die hydrophilen Reste das Innere (oder Teile des Inneren) der Kanalstruktur bilden, die den Aminosäuretransport von OEP16 ermöglichen. Bei 3,6 Aminosäuren pro Helixwindung kann auf diese Weise jeder dritte bis vierte Aminosäurerest polar sein – und damit die Helix den klassischen Analysemethoden entgehen. Hydrophobe Cluster-Analyse Die Hydrophobe Cluster-Analyse (HCA) erlaubt, sich ein zweidimensionales Bild der dreidimensionalen Hydropathie-Verhältnisse in einem Protein zu machen. Eine Aminosäure in einer Helix, zum Beispiel, ist nicht nur von ihren „Sequenznachbarn“ umgeben, sondern auch von Aminosäuren, die etwa 3-4 Positionen vor oder hinter ihr in der Sequenz angeordnet sind. Durch geeignete zweidimensionale Darstellung der Sequenz können solche Nachbarschaftsverhältnisse aufgezeigt werden. Hydrophobe Bereiche werden markiert. Ergeben sich großflächige hydrophobe Bereiche, handelt es sich mit hoher Wahrscheinlichkeit um transmembrane Helices. Auch transmembrane β-Faltblätter können mit dieser Methode sichtbar gemacht werden. Sie zeichnen sich durch ein Alternieren von hydrophilen und hydrophoben Aminosäureresten aus und werden durch Zickzack-Linien im HCA-Plot dargestellt. 85 Abbildung 31: Hydrophobe Cluster-Analyse von OEP16. In der Gerstesequenz wurden zur besseren Veranschaulichung bzw. Vergleichbarkeit die beiden Prolin-Reste 10 und 11 eingeführt (Rot markiert). Die Gerstesequenz ist in diesem Bereich zwei Reste kürzer, siehe auch Abbildung 29). Gezeigt sind die HCA-Plots für die Sequenzen aus Ackerschmalwand, Gerste und Erbse. Grau unterlegt wurden die Bereiche, die laut TMPred transmembrane Helices darstellen. Hydrophobe Bereiche sind umrahmt. Prolinreste sind durch einen Stern, Glycinreste durch eine Raute und Serin- und Threoninreste durch ein Quadrat (mit bzw. ohne Punkt darin) gekennzeichnet. Diese besondere Markierung hebt ebenso wie die Hervorhebung der Cysteinreste die besonderen Struktureigenschaften dieser Aminosäuren hervor. Während Prolin oft am Beginn oder Ende einer Helix steht, ermöglicht das kleine Glycin Knicke in Helix- und Faltblattstrukturen. Serin- und Threoninreste können durch Wasserstoffbrückenbindungen ihrer Hydroxylreste mit dem Proteinrückrat unter Umständen ihren hydrophilen Charakter innerhalb einer Membran verbergen – wiederum ist ein Knick in einer α-Helix die Folge. 86 Klar zu sehen ist eine Häufung hydrophober Cluster in den vorhergesagten transmembranen Segmenten. Putative Faltblattstrukturen sind kurz und nicht in Kernbereichen angeordnet, die als transmembrane Helix in Frage kommen. Nur ein kurzer Faltblattbereich am Ende von Helix zwei wird in allen drei Sequenzen sichtbar – in einem Bereich von fünf Aminosäuren, zu kurz für ein transmembranes Strukturelement. Schön zu sehen in dieser Darstellung ist der Bereich von fünf nebeneinander liegenden Gylcinresten in Helix II, dem vermutlich eine wichtige Rolle bei der Kanalbildung zukommt (möglicherweise bei der Oligomerisierung). Auffällig sind auch die praktisch identischen Hydrophobizitätsmuster in Helix I, was für ihre besondere Rolle für die Kanalselektivität spricht, und die auffällige Übereinstimmung der Muster im Loopbereich zwischen den ersten beiden Helices. Für viele Kanal- und Transportproteine wurde beschrieben, daß Substraterkennung und –selektivität durch Loops vermittelt wird(Slotboom et al., 2001), die zum Teil in die Membran hineinragen. Es ist denkbar, daß dies auch bei OEP16 der Fall ist. Topologie Zusammengenommen ergeben die genannten theoretischen Untersuchungen folgendes Bild: 87 S D T F H E A F I R K L S K K M V S R T V I G F T F A G I W K II D N L K G V G M D I E III I V G Y A Y A V N K K D M G K W R P M S R P S S F S G S L S A L I V D I N S V T G E V V D L K K N A G E P N C A Y E N G A L V L S S N D K I A I G G A A S G A A M F A G IV A I A A D T A T E N V A F Y T I I L C R R G T Abbildung 32: Topologiemodell von OEP16 Nach Proteolyseexperimenten ist der n-Terminus von OEP16 im Chloroplsten dem Cytosol zugewandt(Pohlmeyer, 1997b). Das OEP16-Monomer bildet vier transmembrane Helices aus, wobei Helix I vermutlich die Reste enthält, die die Selektivität des Aminosäurekanals bestimmen. Die Helix beginnt nach einem Prolinrest. Sie enthält (gezeigt für die ErbsenSequenz) die hydrophilen Aminosäuren Asparagin 28, Aspartat 32 und Lysin 36. Besonders die beiden geladenen Reste Asp32 und Lys36 dürften für zukünftige Mutageneseexperimente ein interessantes Ziel darstellen, da sie aus thermodynamischen Gründen unbedingt in das Innere des Kanals ragen müssen. Helix II scheint ein gemeinsames Strukturmotiv vieler Aminosäuretransporter darzustellen und hat offensichtlich für den Kanal vor allem eine strukturgebende Bedeutung. Ob das erwähnte Cystein Cys71 in vivo regulatorisch für die Kanalaktivität wirkt, bleibt eine interessante Fragestellung für weitere Untersuchungen. Der „Loop“ zwischen den Helices I und II ist in Gerste möglicherweise durch eine Disulfidbrücke (Cys40-Cys50) stabilisiert. Helices III und IV haben keine Bedeutung für die Bildung des Kanals. Möglicherweise sind sie an der Oligomerisierung von OEP16-Monomeren beteiligt. 88 OEP16 muß als intakter Kanal ein Oligomer bilden, da zwei α-Helices für sich genommen noch keinen Kanal bilden können. 89 Zusammenfassung der Ergebnisse In der vorliegenden Arbeit wurde die biophysikalischen Eigenschaften eines kleinen Kanalproteins aus der äußeren Chloroplastenmembran der Erbse, genannt OEP16 („outer envelope Protein 16 kDa“), untersucht und ein neues Strukturmodell entwickelt, auf dessen Basis die Funktion des Proteins mit molekularbiologischen Methoden nun genauer erforscht werden kann. OEP16 ist ein Membranprotein mit ungewöhnlichen Eigenschaften. Als Protein der äußeren Chloroplastenmembran insertiert es selbständig in geeignete Lipiddoppellschichten und in Detergenzmizellen. Bei vielen eukaryontischen Membranproteinen kommt eine bakterielle Überexpression zur Gewinnung großer Proteinmengen nicht in Frage, da zumeist ein korrekter Einbau in eine Membran mangels der komplexen eukaryontischen Faltungsmaschinerie in diesen Systemen nicht gegeben ist. OEP16 hingegen erlaubt es, aufgrund seiner selbsttätigen Renaturierung das Protein ohne Rücksicht auf die native Struktur in E.coli überzuexprimieren und erst anschließend rückzufalten. Es konnte gezeigt werden, daß man große Mengen korrekt gefalteten Proteins erhalten kann, indem man in chaotropen Puffersystemen aufgereinigtes Protein durch einen Verdünnungsschritt in einen detergenzhaltigen Puffer überführt. Der Nachweis, daß sich OEP16 in Detergenzmizellen in eine native Form faltet, ist schwierig, da die Funktion des Proteins, seine Kanalaktivität, nur in einem Membransystem meßbar ist. Durch den Vergleich von Fluoreszenz- und CD-Spektren von detergenzhaltigen Proteinlösungen und dem in Liposomen eingebautem Protein (mit nachgewiesener Funktionalität) konnte gezeigt werden, daß die Struktur von OEP16 in den auf unterschiedliche Weise rekonstituierten Proben übereinstimmte. Zeitaufgelöste Messungen mit denselben spektroskopischen Methoden lieferten Daten über den Verlauf und die Geschwindigkeit der Proteinfaltung bei dieser Renaturierungsmethode, einschließlich der Aktivierungsenergien für den Prozeß. Kalorimetrische Messungen (DSC) erlaubten eine Abschätzung der Faltungsenthalpie. Durch hochauflösende CD-Messungen und Infrarotspektroskopie wurde schließlich am in vitro gefalteten Protein gezeigt, daß es sich bei OPE16 entgegen bisheriger Voraussagen um ein rein α-helikales Membranprotein handelt. Dieser Befund konnte durch theoretische Methoden der Strukturbestimmung bestätigt werden. Ein neues Strukturmodell wurde erstellt. Erste vielversprechende Ansätze der Proteinkristallisation und der Elektronenmikroskopie zeigen, daß eine detaillierte Struktur von OEP16 in absehbarer Zeit erhältlich sein könnte. Dies wäre 90 weltweit die erste hochaufgelöste Struktur eines im Reagenzglas gefalteten Membranproteins. In einer Zeit, in der Proteomics, also das Überexprimieren und Analysieren von Proteinen, die Arbeit der größtenteils abgeschlossenen Sequenzierungprojekte fortführen sollen, konnte mit OEP16 ein Modellsystem für die detaillierte Struktur- und Funktionsanalyse von Membranproteinen etabliert werden. 91 Literatur Abrecht, H., Goormaghtigh, E., Ruysschaert, J.-M., and Homble, F. (2000) Structure and Orientation of Two Voltage-dependent Anion-selective Channel Isoforms: An Attenuated Total Reflection Fourier-Trnasform Infrared Spectroscopy Study. Journal of Biological Chemistry, 275, 40992-40999. Allen, J., Feher, G., Yeates, T., Komiya, H., and Rees, D. (1987) Structure of the reaction center from Rhodobacter sphaeroides R-26: The protein subunits. Proceedings of the National Academy of Science, USA, 84, 6162-6166. Arabidopsis Genome Initiative. (2000) Analysis of the genome sequence of the flowering plant Arabidopsis thaliana. Nature, 408, 796-815. Baldi, P., Grossi, M., Pecchioni, N., Vale G., and Cattivelli, L. (1999) High expression level of a gene coding for a chloroplastic amino acid selective channel protein is correlated to cold acclimation in cereals. Plant Molecular Biology, 41, 233-243. Bechinger, B. (2000) Understanding peptide interactions with the lipid bilayer: a guide to membrane protein engineering. Current Opinion in Chemical Biology, 4, 639-644. Benning, C. (1998) Biosynthesis and Funktion of the Sulfolipid Sulfoquinovosyldiacylglycerol. Annual Reviews of Plant Physiology and Plant Molecular Biology, 49, 53-75. Blankenship, R.E., and Hartman, H. (1998) The origin and evolution of oxygenic photosynthesis. Trends in Biochemical Science, 23, 94-97. Block, M.A., Dorne, A.-J., Joyard, J., and Douce, R. (1983) Preparation and Characterization of Membrane Fractions Enriched in Outer and Inner Envelope Membranes from Spinach Chloroplasts. Journal of Bilogical Cemistry, 258, 13281-13286. Bölter, B., Soll, J., Hill, K., Hemmler, R., Wagner, R. (1999) A rectifying ATP-regulated solute channel in the chloroplastic outer envelope from pea. EMBO Journal, 18, 55055516. Booth, P.J., Curran, A.R. (1999) Membrane protein folding. Current Opinion in Structural Biology, 9, 115-121. Brill, L.M., Nunn, R.S., Kahn, T.W., Yeager, M., and Beachy, R.N. (2000) Recombinant tobacco mosaic virus movement protein is an RNA-binding, a-helical membrane protein. Proceedings of the National Academy of Science, USA, 97, 7112-7117. Bruce, B.D. (2000) Chloroplast transit peptides: structure, function and evolution. Trends in Cell Biology, 10, 440-447. 92 Buchanan, S.K. (1999) ß-Barrel proteins from bacterial outer membranes: structure, function and refolding. Current Opinion in Structural Biology, 9, 455-461. Burstein, E.A., Vedenkina, N.S., Ivkova, M.N. (1973) Fluorescence and the location of tryptophan residues in protein molecules. Photochemistry and Photobiology, 18, 263279. Callahan, M.A., Xiong, L.-W., and Caughey, B. (2001) Reversibility of Scrapie-associated Prion Protein Aggregation. Journal of Biological Chemistry, 276, 28022–28028. Callebaut, I., Labesse, G., Durand, P., Poupon, A., Canard, L., Chomilier, J., Henrissat B., and Mornon, J.P. (1997) Deciphering protein sequence information through hydrophobic cluster analysis (HCA): current status and perspectives. Cellular and Molecular Life Science, 53, 621–645. Cavalier-Smith, T. (2000) Membrane heredity and early chloroplast evolution. Trends in Plant Science, 5, 174-182. Chen, Y., BArkley, M.D. (1998) Toward Understanding Tryptophan Fluorescence in Proteins. Biochemistry, 37, 9976-9982. Cline, K., and Henry, R. (1996) Import and Routing of Nucleus-encoded Chloroplast Proteins. Annual Reviews of Cell and Developmental Biology, 12, 1-26. Conway, K.A., Harper, J.D., and Lansbury, P.T.Jr. (2000) Fibrils Formed in Vitro from RSynuclein and Two Mutant Forms Linked to Parkinson’s Disease are Typical Amyloid. Biochemistry, 39, 2552-2563. Cowan, S.W., Rosenbusch, J.P. (1994) Folding Pattern Diversity of Integral Membrane Proteins. Science, 264, 914-916. Deisenhofer, J., Epp, O., Miki, K., Huber, R., and Michel, H. (1985) Structure of the protein subunits in the photosynthetic reaction centre of Rhodopseudomonas viridis at 3 A resolution. Nature, 318, 618-624. Fischer, K., Weber, A., Brink, S., Arbinger, B., Schünemann, D., Borchert, S., Heldt, H.W., Popp, B., Benz, R., Link, T.A., Eckerskorn, C., and Flügge, U.-I. (1994) Porins from Plants. Journal of Biological Chemistry, 269, 25754-25760. Flügge, U.I. (1998) Metabolite transporters in plastids. Current Opinion in Plant Biology, 1, 201-206. Flügge, U.I. (2000) Transport in and out of plastids: does the outer envelope membrane control the flow? Trends in Plant Science, 5, 135-137. Froehlich, J.E., Benning, C., and Dörmann, P. (2001) The Digalactosyldiacylglycerol (DGDG) Synthase DGD1 Is Inserted into the Outer Envelope Membrane of 93 Chloroplasts in a Manner Independent of the General Import Pathway and Does Not Depend on Direct Interaction with Monogalactosyldiacylglycerol Synthase for DGDG Biosynthesis. Journal of Biological Chemistry, 276, 31806–31812. Griegorieff, N., Ceska, T.A., Downing, K.H., Baldwin, J.M., and Henderson, R. (1996) Electron-crystallographic refinement of the structure of bacteriorhodopsin. Journal of Molecular Biology, 259, 393-421. Haltia, T., and Freire, E. (1995) Forces and factors that contribute to the structural stability of membrane proteins. Biochimica et Biophysica Acta, 1228, 1-27. Harris, E.H., Boynton, J.E., and Gillham, N.W. (1994) Chloroplast Ribosomes and Protein Synthesis. Microbiological Reviews, 58, 700-754. Heiber, T., Steinkamp, T., Hinnah, S., Schwarz, M., Flügge, U.I., Weber, A., Wagner, R. (1995) Ion Channels in the Chloroplast Envelope Membrane. Biochemistry, 34, 15906-15917. Heins, L., Collinson, I., Soll, J. (1998) The protein translocation apparatus of chloroplast envelopes. Trends in Plant Science, 3, 56-61. Hirsch, A., Breed, J., Saxena, K., Richter, O.M.H., Ludwig, B., Diedrichs, K., Welte, W. (1997) The structure of porin from Paracoccus denitrificans at 3.1 A resolution. FEBS letters, 404, 208-210. Hofmann, K., and Stoffel,W. (1993) TMbase - A database of membrane spanning proteins segments. Biological Chemistry Hoppe-Seyler, 374, 166. Iwata, S., Ostermeier, C., Ludwig, B., and Michel, H. (1995) Structure at 2.8 A resolution of cytochrome c oxidase from paracoccus denitrificans. Nature, 376, 660-669. Jordan, P., Fromme, P., Witt, H.T., Klukas, O., Saenger, W., and Krauss, N. (2001) Threedimensional structure of cyanobacterial photosystem I at 2.5 angstrom resolution. Nature, 411, 909-917. Joyard, J., Block, M.A., and Douce, R. (1991) Molecular aspects of plastid envelope biochemistry. European Journal of Biochemistry, 199, 489-509. Joyard, J., Teyssier, E., Miege, C., Berny-Seigneurin, D., Marechal, E., Block, M.A., Dorne, A.-J., Rolland, N., Ajlani, G., and Douce, R. (1998) The Biochemical Machinery of Plastid Envelope Membranes. Plant Physiology, 118, 715-723. Keegstra, K. (1989) In Briggs, W. (ed.) Photosynthesis. Alan R. Liss, New York, pp. 347-357. Keegstra, K., Cline, K. (1999) Protein Import and Routing Systems of Chloroplasts. Plant Cell, 11, 557-570. 94 Kerber, B., and Soll, J. (1992) Transfer of a chloroplast-bound precursor protein into the translocation apparatus is impaired after phospholipase C treatment. FEBS Letters, 306, 71-74. Klebba, P.E., Newton, S.M.C. (1998) Mechanisms of solute transport through outer membrane porins: burning down the house. Current Opinion in Microbiology, 1, 238248. Koebnick, R. (1996) In vivo membrane assembly of split variants of the E.coli outer membrane protein OmpA. EMBO Journal, 15, 3529-3537. Koike, H., Yoshio, M., Kashino, Y., and Satoh, K. (1998) Polypeptide composition of envelopes of spinach chloroplasts: Two major proteins occupy 90% of outer envelope membranes. Plant and Cell Physiology, 39, 526-532. Kreusch, A., Schulz, G.E. (1994) Refined Structure of the Porin from Rheudopseudomonas blastica. Journal of Molecular Biology, 243, 891-905. Kühlbrandt, W., Wang, D.N., and Fujioshi, Y. (1994) Atomic model of plant kght harvesting complex by electron crystallography. Nature, 367, 614-621. Kyte, J., and Doolittle, R.F. (1982) A simple method for displaying the hydropatic character of a protein. Journal of Molecular Biology, 157, 105-132. Lam, H.M., Coschingano, K.T., Oliveira, I.C., Melo-Oliveira, R., Coruzzi, G.M. (1996) The Molecular Genetics of Nitrogen Assimilation into Amino Acids in Higher Plants. Annual Reviews of Plant Physiology and Plant Molecular Biology, 47, 569-593. Lemeshko, S.V., and Lemeshko, V.V. (2000) Metabolically Derived Potential on the Outer Membrane of Mitochondria: A Computational Model. Biophysical Journal, 79, 27852800. Leon, P., Arroyo, A. (1998) Nuclear Control of Plastid and Mitochondrial Development in Higher Plants. Annual Reviews of Plant Physiology and Plant Molecular Biology, 49, 453-480. Li, H.M., Moore, T., Keegstra, K. (1991) Targeting of Proteins to the Outer Envelope Membrane Uses a Different Pathway tha Transport into Chloroplasts. Plant Cell, 3, 709-717. Li, H.M., Chen, L.J. (1996) Protein Targeting and Integration Signal for the Chloroplastic Outer Envelope Membrane. Plant Cell, 8, 2117-2126. Lin, X., Samir Kaul, Steve Rounsley, Terrance P. Shea, Maria-Ines Benito, Christopher D. Town, Claire Y. Fujii, Tan et al. (1999) Sequence and analysis of chromosome 2 of the plant Arabidopsis thaliana. Nature, 402, 761 - 768. 95 Linke, D., Frank, J., Holzwarth, J.F., Soll, J., Boettcher, C., and Fromme, P. (2000) In Vitro Reconstitution and Biophysical Characterization of OEP16, an Outer Envelope Pore Protein of Pea Chloroplasts. Biochemistry, 39, 11050-11056. Marcos, J.C., Fonseca, L.P., Ramalho, M.T., Cabral, J.M.S. (1999) Partial purification of pennicilin acylase from Escherichia coli in poly(ethylene glycol)-sodium citrate aqueous two-phase systems. Journal of Chromatography B, 734, 15-22. Margulis, L. (1996) Archeal-eubacterial mergers in the origin of Ekarya: Phylogenic classification of life. Proceedings of the National Academy of Science, USA, 93, 10711076. Mayer, K., C. Schuller, R. Wambutt, G. Murphy, G. Volckaert, T. Pohl, A. Dusterhoft, W. Stiekema, K.-D. Entian, N. Terryn et al. (1999) Sequence and analysis of chromosome 4 of the plant Arabidopsis thaliana. Nature, 402, 769 - 777. McDermott, G., Price, S.M., Freer, A.A., Hawthornthwaite-Lawless, A.M., Papiz, M.Z., Cogdell, R.J., and Isaacs, N.W. (1995) Crystal structure of an integral membrane lightharvesting complex from photosynthetic bacteria. Nature, 374, 517-521. McFadden, G.I. (1999) Endosymbiosis and evolution of the plant cell. Current Opinion in Plant Biology, 2, 513-519. Miernyk, J.A. (1999) Protein Folding in the Plant Cell. Plant Physiology, 121, 695-703. Mitchell, D.J., Tiddy, J.T., Waring, L., Bostok, T., and McDonald, M.P. (1983) Journal of the Chemical Society, Faraday Transactions, 79, 975-1000. Morgenstern, B. (1999) DIALIGN 2: improvement of the segment-to-segment approach to multiple sequence alignment. Bioinformatics, 15, 211-218. Pinnaduwage, P., and Bruce, P.D. (1996) In vitro interaction between a chloroplast transit peptide and chloroplast outer envelope lipids is sequence-specific and lipid classdependent. Journal of Biological Chemistry, 271, 32907-32915. Pohlmeyer, K., Soll, J., Steinkamp, T., Hinnah, S., Wagner, R. (1997a) Isolation and characterization of an amino acid-selective channel protein present in the chloroplastic outer envelope membrane. Proceedings of the National Academy of Science, USA, 94, 9504-9509. Pohlmeyer, K. (1997b) Porenbildende Proteine in der äußeren Hüllmembran von Chloroplasten aus Erbse (Pisum sativum L.). Mathematisch-Natrurwissenschaftliche Fakultät. Christian-Albrechts-Universität, Kiel, p. 88. Pohlmeyer, K., Soll, J., Grimm, R., Hill, K., Wagner, R. (1998) A High-Conductance Solute Channel in the Chloroplastic Outer Envelope from Pea. The Plant Cell, 10, 1207-1216. 96 Poincelot, R.P. (1973) Isolation and Lipid Composition of Spinach Chloroplast Envelope Membranes. Archives of Biochemistry and Biophysics, 159, 134-142. Popp, B., Gbauer, S., Fischer, K., Flügge, U.I., Benz, R. (1997) Study of Structure and Function of Recombinant Pea Root Plastid Porin by Biophysical Methods. Biochemistry, 36, 2844-2852. Pyke, K.A. (1999) Plastid Division and Development. Plant Cell, 11, 549-556. Rassow, J., Dekker, P.J.T., van Wilpe, S., Meijer, M., Soll, J. (1999) Ther Preprotein Translocase of the Mitochondrial Inner Membrane: Function and Evolution. Journal of Molecular Biology, 286, 105-120. Reumann, S., Keegstra, K. (1999) The endosymbiotic origin of the protein import machinery of chloroplastic envelope membranes. Trends in Plant Science, 4, 302-307. Ridge, K.D., Lee, S.S.J., and Yao, L.L. (1995) In vivo assembly of rhodopsin from expressed polypeptide fragments. Proceedings of the National Academy of Science, USA, 92. Röhl, T., Motzkus, M., Soll, J. (1999) The outer envelope protein OEP24 from pea chloroplasts can functionally replace the mitochondrial VDAC in yeast. FEBS letters, 460, 491-494. Salanoubat, M., Lemcke K., Rieger M., Ansorge W., Unseld M., Fartmann B., Valle G., Blocker H., Perez-Alonso M., Obermaier B., Delseny M., Boutry M., Grivell L.A., Mache R., Puigdomenech P., De Simone V., Choisne N., Artiguenave F, Robert C, Brottier P, Wincker P, et.al. (2000) Sequence and analysis of chromosome 3 of the plant Arabidopsis thaliana. Nature, 408, 820-822. Seedorf, M., Soll, J. (1995) Copper chloride, an inhibitor of protein import into chloroplasts. FEBS letters, 367, 19-22. Settles, A.M., Martienssen, R. (1998) Old and new pathways of protein export in chloroplasts and bacteria. Trends in Cell Biology, 8, 494-501. Slotboom, D.J., Konings, W.N. and Lolkema, J.S. (2001) Glutamate transporters combine transporter- and channel-like features. Trends in Biochemical Science, 26, 534-9. Soll, J., Bölter, B., Wagner, R., Hinnah, S.C. (2000) response: The chloroplast outer envelope: a molecular sieve? Trends in Plant Science, 5, 137-138. Steinkamp, T., Hill, K., Hinnah, S.C., Wagner, R., Röhl, T., Pohlmeyer, K., and Soll, J. (2000) Identification of the Pore-forming Region of the Outer Chloroplast Envelope Protein OEP16. Journal of Biological Chemistry, 275, 11758–11764. Stock, D., Leslie, A.G.W., and Walker, J.E. (1999) Molecular architecture of the rotary motor in ATP synthase. Science, 286, 1700-1705. 97 Tabata, S., Kaneko T, Nakamura Y, Kotani H, Kato T, Asamizu E, Miyajima N, Sasamoto S, Kimura T, Hosouchi T, Kawashima K, Kohara M, Matsumoto M, Matsuno A, Muraki A, Nakayama S, Nakazaki N, Naruo K, Okumura S, Shinpo S, Takeuchi C, Wada T, Watanabe A, Yamada M, et.al. (2000) Sequence and analysis of chromosome 5 of the plant Arabidopsis thaliana. Nature, 408, 823-826. Theologis, A., Joseph R. Ecker, Curtis J. Palm, Nancy A. Federspiel, Samir Kaul, Owen White, Jose Alonso, et al. (2000) Sequence and analysis of chromosome 1 of the plant Arabidopsis thaliana. Nature, 408, 816 - 820. Toyoshima, C., Nakasako, M., Nomura, H., and Ogawa, H. (2000) Crystal structure of the calcium pump of sarcoplasmatic reticulum at 2.6 A resolution. Nature, 405, 647-655. Tranel, P.J., and Keegstra, K. (1996) A novel, bipartite transit peptide targets OEP75 to the outer membrane of the chloroplast envelope. Plant Cell, 8, 2093-2104. Tsuhikara, T., Aoyama, H., Yamashita, E., Tomizaki, T., Yamaguchi, H., Shinzawa-Itoh, K., Nakashima, R., Yaono, R., and Yoshikawa, S. (1996) The whole structure of the 13subunit oxidized bovine heart cytochrome c oxidase at 2.8 A resolution. Science, 272, 1136-1144. Van't Hof, R., van Klompenburg, W., Pilon, M., Kozubek, A., de Korte-Kool, G., Demel, R.A., Weisbeek, P.J., and de Kruijff, B. (1993) The transit sequence mediates the specific interaction of the precursor ferredoxin with chloroplast envelope membrane lipids. Journal of Biological Chemistry, 268, 4037-4042. von Heijne, G., and Nishikawa, K. (1991) Chloroplast transit peptides. The perfect random coil? FEBS Letters, 278, 1-3. von Heijne, G. (1996) Principles of membrane protein assembly and structure. Progress in Biophysics and Molecular Biology, 66, 113-139. Waegemann, K., Eichacker, S., and Soll, J. (1992) Outer envelope membranes from chloroplasts are isolated as right-side-out vesicles. Planta, 187, 89-94. White, S.H. (1999) Membrane Protein Folding and Stability: Physical Principles. Annual Reviews of Biophysics and Biomolecular Structure, 28, 319-365. Wiese, A., Gröner, F. , Sonnewald, U., Deppner, H., Lerchl, J., Hebbeker, U., Flügge, U.-I., and Weber, A. (1999) Spinach hexokinase I is located in the outer envelope membrane of plastids. FEBS Letters, 461, 13-18. Winter, R., and Noll, F. (1998) Methoden der Biophysikalischen Chemie. 98 Zhan, H., Oh, K.J., Shin, Y.-K., Hubbel, W.L., and Collier, R.J. (1995) Interaction of the isolated transmembrane domain of diphteria toxin with membranes. Biochemistry, 34, 4856-4863. Zouni, A., Witt, H.T., Kern, J., Fromme, P., Krauss, N., Saenger, W., Orth, P. (2001) Crystal structure of photosystem II from Synechococcus elongatus at 3.8 angstrom resolution. Nature, 409, 739-743. 99 Danksagung Ich danke Frau Prof. Dr. Petra Fromme nicht nur für die interessante Aufgabenstellung und die dafür bereitgestellten finanziellen Mittel aus ihren Projekten, sondern auch insbesondere für die große Freiheit, die ich beim Berarbeiten des Themas genossen habe. Die Arbeit wurde hauptsächlich aus Mitteln der DFG (Fördernummer Fr 320/3-1 und 3-2) finanziert. Herrn Prof. Soll (Kiel, inzwischen München) danke ich für die fruchtbare Zusammenarbeit bei mehreren Publikationen und ihm und seiner gesamten Arbeitsgruppe für das Produzieren großer Mengen „inclusion bodies“, ohne die diese Arbeit nicht möglich gewesen wäre. Herrn Prof. Wagner (Osnabrück) und seinen Mitarbeitern sind die Leitfähigkeitsmessungen an OEP16-Liposomen zu verdanken. Herrn Prof. Findenegg (TU Berlin) danke ich für die Bereitschaft, sehr kurzfristig die Begutachtung meiner Arbeit zu übernehmen. Uwe Fink, Dr. Joachim Frank, Jan Kern, Dr. Athina Zouni und Dr. Priv.Doz. Petra Fromme haben mich ständig durch Fachwissen, neue Ideen und hilfreiche Diskussionen unterstützt. Ein solch produktives und angenehmes Arbeitsumfeld kann nicht genug gewürdigt werden. Meinen Eltern, Herrn Timm Krause-Plonka sowie Erwin und Anneliese Schäuble danke ich für moralische und finanzielle Unterstützung während des gesamten Studiums. Meiner Frau Daniela gilt besonderer Dank für viel Geduld. Diese Arbeit ist meinem Sohn Lukas gewidmet, der mit knapp fünf Jahren mehr über Dinosaurier, Autos und Fische weiß als ich. 100