Momentaufnahmen aus dem Leben einer Zelle
Werbung
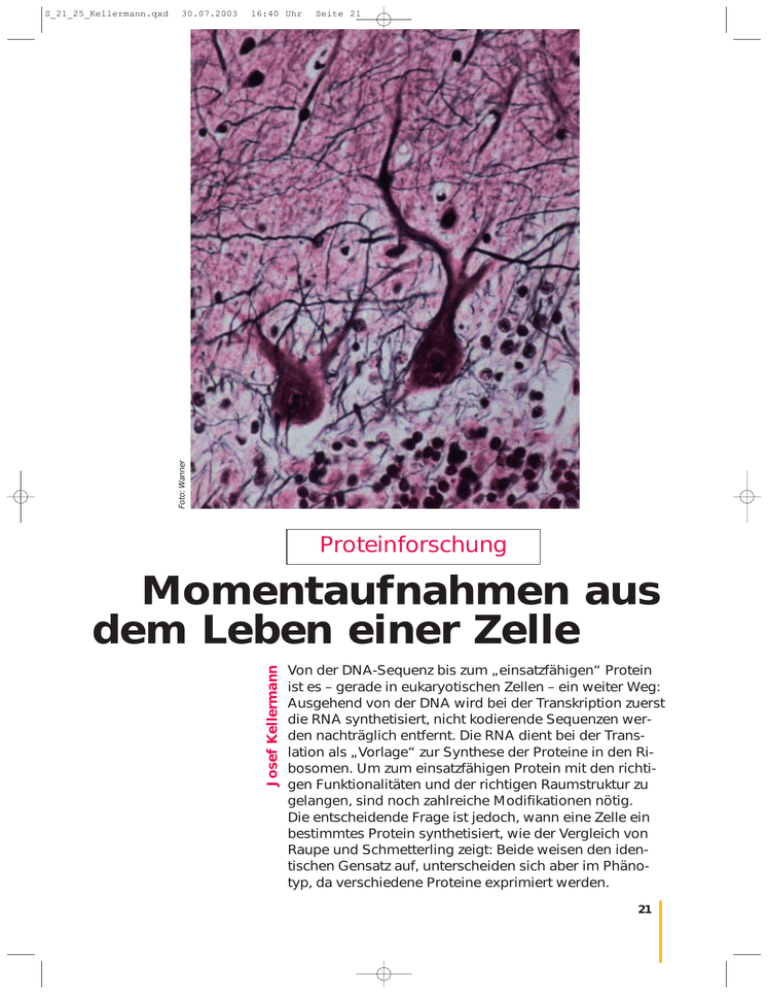
30.07.2003 16:40 Uhr Seite 21 Foto: Wanner S_21_25_Kellermann.qxd Proteinforschung Josef Kellermann Momentaufnahmen aus dem Leben einer Zelle Von der DNA-Sequenz bis zum „einsatzfähigen“ Protein ist es – gerade in eukaryotischen Zellen – ein weiter Weg: Ausgehend von der DNA wird bei der Transkription zuerst die RNA synthetisiert, nicht kodierende Sequenzen werden nachträglich entfernt. Die RNA dient bei der Translation als „Vorlage“ zur Synthese der Proteine in den Ribosomen. Um zum einsatzfähigen Protein mit den richtigen Funktionalitäten und der richtigen Raumstruktur zu gelangen, sind noch zahlreiche Modifikationen nötig. Die entscheidende Frage ist jedoch, wann eine Zelle ein bestimmtes Protein synthetisiert, wie der Vergleich von Raupe und Schmetterling zeigt: Beide weisen den identischen Gensatz auf, unterscheiden sich aber im Phänotyp, da verschiedene Proteine exprimiert werden. 21 S_21_25_Kellermann.qxd 30.07.2003 16:40 Uhr Momentaufnahmen aus dem Leben einer Zelle eueste Erkenntnisse besagen, dass Menschen wesentlich weniger Gene besitzen, als bisher vermutet wurde: „Nur“ etwa 30 000 bis 40 000 Gene reichen aus, um uns in unserer ganzen Komplexität entstehen und funktionieren zu lassen. Für viele Biochemiker ist dies kein überraschender Befund, da die Vielfalt des Lebens für sie auf der Ebene der Proteine zu suchen ist und nicht im Genom. Die Herausforderung der nächsten Jahrzehnte wird sein, zu klären, wie die Regieanweisung des Genoms von der Zelle interpretiert und in Proteine umgesetzt wird. N AABXVGHAUSMITLVGHACHTT UERENUNDLLLLLLLLLLLLLZWO ELFFENSTERNRGHHLCD… Wenn Sie sich vorstellen, dass der Architekt, den Sie für ihr neues Haus engagiert haben, ihnen eine derartige Endlosliste aus Bauteilen vorlegt, können Sie nur Seite 22 schwer daraus ableiten, wie dieses Haus aussehen oder funktionieren soll. Einer ähnlichen Liste stehen jetzt, nach der Entzifferung des menschlichen Genoms, die Wissenschaftler gegenüber, denn die Reihenfolge der über drei Milliarden Basen im menschlichen Genom sagt noch nichts aus über die Funktion der einzelnen Gene. Gerade auch, weil nur ein geringer Prozentsatz dieses Endlostextes aus vier Buchstaben wirklich den Bauplan für die daraus abgeleiteten Eiweiße, die Proteine, enthält. Proteine sind die wichtigsten Bestandteile des Körpers und die eigentlichen Träger der im Genom festgelegten Zellfunktionen. Ob als Strukturbausteine, Enzyme oder Antikörper: Sie sind es, die über die Eigenarten unserer Körperzellen bestimmen. Die Gesamtheit aller Proteine wird analog zum Genom als Proteom bezeichnet. Benötigt eine Zelle ein bestimmtes Protein, so wird im Zellkern zu Beginn der Neuproduktion eine Kopie des Bauplans des entsprechenden Gens erstellt (Transkription). Diese „Kopie“ verlässt als Datenträger den Kern und wird an die Produktionsabteilung für Proteine, die Ribosomen, verschickt. Diese fügen dem Bauplan entsprechend eine Aminosäure nach der anderen aneinander (Translation). Nach Anfügen der letzten Aminosäure wird das Protein ins Zytoplasma freigegeben und das Ribosom angelt sich eine neue Kopie des Bauplans. Dieses Prinzip der Bildung von Proteinen ist seit Anfang der sechziger Jahre bekannt. Die Vielfalt der Möglichkeiten wird aber erst jetzt klar, nachdem das Protein, dem lange Zeit die Popularität vom Gen streitig gemacht wurde, eine Renaissance erlebt. Ein Gen, ein Protein – so einfach ist es nicht Bis vor kurzem noch war man der Meinung, dass jedes Gen nur den Bauplan für ein Protein mit einer bestimmten Funktion enthält. Mittlerweile jedoch ist bekannt, dass Teile des Bauplans herausgeschnitten und mit Teilen eines anderen Bauplans, ähnlich einer Collage, zu einem völlig neuen Plan zusammengesetzt werden können. Dieser Vorgang wird als alternatives splicing bezeichnet und resultiert in einem veränderten oder neuen Protein mit anderer Funktion. So gibt es für Myosin, ein Strukturprotein der Muskelfaser, nur ein einziges Gen, obwohl Myosin beim Menschen in zahlreichen verschiedenen Formen vorkommen kann. Zusätzlich zum splicing können Trotz ihres identischen Genoms lassen die beiden Entwicklungsstadien des Schmetterlings keinerlei Verwandtschaft vermuten. Zu verschiedenen Zeitpunkten der Entwicklung werden unterschiedliche Gene exprimiert und damit unterschiedliche Proteine synthetisiert. Zeitlich und räumlich unterschiedliche Genaktivitäten wirken sich damit auf der Ebene der Proteine aus. Fotos: Kellermann 22 mensch+umwelt spezial 16. Ausgabe 2003 S_21_25_Kellermann.qxd 30.07.2003 16:40 Uhr Seite 23 Faktoren wie Stress, Medikamente und das Nährstoffangebot beitragen. Mangel oder Überangebot bestimmter Faktoren müssen ausgeglichen werden, was zu einer Mehrproduktion bestimmter Proteine führt, während andere weniger benötigt werden. Es existieren also im Gegensatz zu „dem Genom“ eine Vielzahl von Proteomzuständen, jeweils als Momentaufnahmen der Proteinzusammensetzung im Leben einer Zelle. Vielfalt macht Analysen schwierig Proteine erfüllen im Stoffwechsel vielfältige Aufgaben. Wichtigste Vertreter sind neben den strukturbildenden Proteinen, etwa in der Haut oder in den Haaren, die Enzyme. Oben dargestellt ist ein Modell der Glutamyl-tRNA-Reduktase, einem Enzym der Proteinbiosynthese. Als Biokatalysatoren ermöglichen Enzyme den Ablauf chemischer Reaktionen und steuern einzelne Stoffwechselschritte. Grafik: GBF anschließend am Protein noch Veränderungen vorgenommen werden, die nicht im Plan vorgesehen sind, die aber die Eigenschaften eines Proteins wesentlich beeinflussen (so genannte posttranslationale Modifikationen). Über hundert solcher Veränderungen sind bis heute beschrieben. Am häufigsten werden Phosphatreste oder Zuckerketten als Seitenäste an Proteine angefügt. All diese Proteine bilden nun eine dreidimensionale, kompakte Struktur, die wiederum mit anderen Proteinen in Wechselwirkung treten kann. Nicht zuletzt kann ein und dasselbe Protein mehrere unterschiedliche Funktionen in unterschiedlicher Umgebung ausüben bzw. können umgekehrt unterschiedliche Proteine sehr ähnliche Funktionen innehaben. nenten Veränderungen unterworfen, je nach Bedarf der Zelle. Sie verändert während der Entwicklung ständig ihre Proteinzusammensetzung, wozu auch äußere Die Analyse der Proteomzustände ist die Herausforderung, der die Wissenschaftler jetzt gegenüberstehen. Diese Aufgabe ist ungleich aufwendiger als die Entzifferung des Genoms. Proteine sind weitaus schwieriger handhabbar als Gene und deutlich heterogener in ihren chemischen und physikalischen Eigenschaften. Die DNA ist aus vier unterschiedlichen Basen aufgebaut. Dies lässt weniger Variationen in ihren Eigenschaften zu als bei Proteinen, die aus zwanzig Stress verändert das Bild Um die Vorgänge in einer Zelle verstehen zu können, ist es daher notwendig, die Proteine zu analysieren. Anders als das Genom, das statisch im Zellkern ähnlich einem Bauplan im Tresor vorliegt, ist das Proteom dynamisch und perma- Zweidimensionale Gelelektrophorese. In zwei Schritten werden Proteine zuerst in einem elektrischen Feld nach ihrer Ladung getrennt und dann in einem engmaschigen Netz aus Polyacrylamid nach ihrer Größe sortiert. Anschließend werden die Proteine im Gel durch Anfärben sichtbar gemacht und erscheinen dann, je nach Farbstoff, als schwarze, blaue oder fluoreszierende Punkte unterschiedlicher Größe und Intensität, abhängig von der Menge des Proteins. Grafik: Kellermann 23 S_21_25_Kellermann.qxd 30.07.2003 16:40 Uhr Seite 24 Momentaufnahmen aus dem Leben einer Zelle verschiedenen Aminosäuren zusammengesetzt sind, die zusätzlich noch durch posttranslationale Modifikationen in ihren Eigenschaften verändert werden können. Die Größe der Proteine reicht von wenigen Aminosäuren, aufgereiht wie Perlen auf einer Perlenkette, bis zu mehreren hundert Aminosäuren. Dabei werden diese Ketten, je nach Zusammensetzung der Aminosäuren, zu unterschiedlichsten dreidimensionalen Strukturen gefaltet, die so mit anderen Proteinen in Wechselwirkung treten können. Legt man die Anzahl aller gefundenen humanen Gene mit 40 000 zugrunde, kann man davon ausgehen, dass durch nachträglich eingeführte Modifikationen mindestens 200 000 verschiedene Proteinspezies mit unterschiedlicher Funktion zu erwarten sind. Das heißt, ein Gen kodiert durchschnittlich für fünf verschiedene Proteine, die jedoch nicht alle in jedem Organ oder in jedem Zelltyp gleichzeitig vorkommen. Hinzu kommen noch die sehr unterschiedlichen Mengen, in denen Proteine in einer Zelle vorliegen können. So benötigt eine Zelle von einem Protein nur wenige Moleküle zur Aufrechterhaltung ihrer Funktion, während andere Proteine in mehreren hunderttausend Kopien vorhanden sein müssen. Diese Heterogenität verlangt ein deutlich größeres Methodenspektrum als es in der hochautomatisierbaren DNA-Analyse notwendig ist. Fingerabdrücke helfen Welche Ansätze werden verfolgt, um Proteinveränderungen in einer Zelle nachweisen zu können? Es müssen Techniken gefunden werden, die sensitiv genug sind, um 24 Zur Bestimmung von Proteinen ist die instrumentelle Analytik heute unentbehrlich. Mit Hilfe eines MALDI-TOF-Massenspektrometers kann ein ionisiertes Proteinmolekül anhand seiner Flugdauer in einem evakuierten Rohr identifiziert werden. Foto: GSF/GAZ mit sehr wenig Zell- oder Gewebematerial auszukommen und es sollten Techniken sein, die Veränderungen der Proteinzusammensetzung schnell erfassen können. Die heute am weitesten verbreitete Methode, „Proteinfingerabdrücke“ einer Zelle darzustellen, ist die zweidimensionale Gelelektrophorese. Dabei werden Proteine in einem Gel aufgetrennt und angefärbt, wodurch sie als Punkte sichtbar werden. Vergleicht man die Proteinmuster unterschiedlicher Zustände einer Zelle, zum Beispiel eine Normalleber mit einer Leber unter dem Einfluss verschiedener Medikamente, so verändert sich die Intensität mancher Punkte. Um zu verstehen, welche Proteine an Regulationsnetzwerken unter dem Einfluss bestimmter Medikamente beteiligt sind, müssen die Proteine identifiziert werden, die sich hinter einem sich verändernden Punkt verbergen. Dazu wird dieses Protein aus dem Gel ausgestochen und mit „Schneide-Enzymen“, die selbst auch Proteine sind, in leichter analysierbare Fragmente zerlegt. Jedes Protein wird dabei in charak- mensch+umwelt spezial 16. Ausgabe 2003 teristische Bruchstücke zerlegt, deren Molekülmassen in sogenannten Massenspektrometern genau bestimmt werden können. Dieser „Fingerabdruck“ aus mehreren Fragmentmassen wird zur Identifizierung des Proteins in einer Datenbank verwendet. Allerdings können nicht alle Proteine auf diese Weise eindeutig identifiziert werden. In speziellen Fällen muss in einem solchen Bruchstück die Aminosäureabfolge bestimmt werden. Für eine derartige massenspektrometrische Analyse genügt heute bereits weniger als ein Millionstel eines Milligramms. Problematisch ist bei dieser Elektrophorese-basierten Methode vor allem die Reproduzierbarkeit, beginnend bei der manuellen Herstellung der Gele über die Anfärbung bis hin zur computergestützten Auswertung der Proteinmuster. Außerdem kann nur eine relativ geringe Anzahl von Eiweißen im Gel sichtbar gemacht werden, nämlich etwa 5000 von 50 000 erwarteten Proteinen. Der Rest liegt in zu geringer Menge vor, um mit dieser Technik analysiert werden zu können. S_21_25_Kellermann.qxd 30.07.2003 16:40 Uhr Nervenzellen mit ihren charakteristischen Fortsätzen, den Dendriten. Alle Zellen eines Organismus besitzen eine identische Genausstattung, unterschiedliche Zelltypen entstehen durch die Expression von verschiedenen Genen. Seite 25 mit Proteinen zusammen. So bilden sich bei der Alzheimer-Krankheit unlösliche Proteinfragmente im Gehirn, die die Zellen zerstören. Darüber hinaus erhofft man sich auch Aufschluss über die Funktion der unzähligen noch unbekannten Proteine. Mit der Buchstabenfolge der Gene kennt man auch Bauanleitungen seltener Eiweiße, die man sonst im Körper nur schwer finden würde. Noch in weiter Ferne liegt das Ziel, zu verstehen, wie all diese Proteine in Netzwerken miteinander verknüpft sind, was bei verschiedenen Krankheiten im Organismus abläuft, und wie Medikamente wirken bzw. was im Leben einer Zelle an Veränderungen auftritt. All diese Erkenntnisse, bioinformatisch abgebildet, sollen die Schaffung einer virtuellen Zelle erlauben, in der Prozesse dargestellt und simuliert werden kön- nen. Um diese schwierige Herausforderung anzugehen, müssen Wissenschaftler unterschiedlicher Fachgebiete, wie Biochemiker, Zellbiologen und Informatiker eng zusammenarbeiten. Für das Verständnis lebender Systeme könnte man aus einer funktionierenden virtuellen Zelle vieles lernen. Literaturhinweise: Hunter,T.C., Andon, N.L., Koller, A., Yates, J.R., Haynes, P.A.: (2002) The functional proteomics toolbox: methods and applications. Journal of Chromatography B 782, 1-2, 165-181 Lottspeich, F., Zorbas, H.: (1998) Bioanalytik. Spektrum Akademischer Verlag, Heidelberg Yarmush, M.L., Jayaraman, A.: (2002) Advances in Proteomic Technologies. Annual Review of Biomedical Engineering, 4, 1, 349-373 Internettipps: http://www.proteome.co.uk http://www.europroteome.com http://www.lsbc.com Foto: Wanner Deshalb wird fieberhaft nach alternativen und komplementären Methoden für die Proteomanalytik gesucht. Diese Methoden müssen besser automatisierbar sein und quantitative Aussagen liefern. Verschiedene neue Ansätze, basierend auf differentiellem Isotopenlabeling oder ProteinchipTechnologien, versprechen durchaus Fortschritte auf diesem Gebiet. Noch Zukunftsmusik: Die virtuelle Zelle Die Erwartungen an die Proteomforschung sind vielfältig: Als wichtigstes Ziel sollen krankheitsrelevante Proteine gefunden werden, die diagnostische und auch neue therapeutische Strategien in der Medizin erlauben. Viele Wissenschaftler glauben, dass im Proteom der Schlüssel zum Verständnis von Krankheiten liegt. Manche Volkskrankheiten hängen direkt Fluoreszenzmikroskopische Aufnahme von Zellen, die das Protein Huntingtin synthetisieren. Bei der erblichen Nervenkrankheit Chorea Huntington wird infolge einer Mutation des Huntingtin-Gens das entsprechende Protein Huntingtin mit einer veränderten Struktur (Amyloidstruktur) synthetisiert. Dadurch gehen Nervenzellen, speziell in den Stammganglien und der Hirnrinde, zugrunde. Foto: DHGP 25