von T-Zellen - MedUni Wien
Werbung

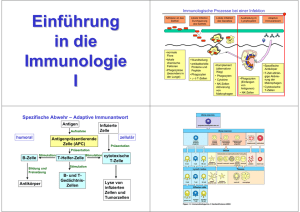
Abwehr I-II Seminar Block 8 WS 07/08 Mag. Krisztina Szalai [email protected] Abwehr I.: angeborene, natürliche Abwehr Abwehr II.: erworbene, spezifische Abwehr Immunantwort spezifische (erworbene) natürliche (angeborene) Zellulär Zellulär Humoral Phagozyten, NK-Zellen, Mastzellen, Endothelzellen, Epithelzellen... Komplements., Einige Zytokine, T-Lymph. Enzyme ... Cytotoxicity T-Helfer Zellen Zytokine APC Humoral B-Lymph. Antikörper Die spezifische Abwehr - Überblick 1. Antigenprozessierung und –präsentation von Proteinen durch APC (antigen-presenting cells) über MHC I oder MHC II an T-Zellen A) CTL : 8 CD ⇓ 2. Aktivierung von naiven T-Zellen Î werden Ag-spezifisch CD ) B 4 h1 T : ⇓ 3. diese können A) entweder töten (CTL=CD8+) B) oder andere Zellen aktivieren (CD4: Th1 und Th2!) Î Töten betroffene Zelle Î aktivieren B-Zellen zur Ig=Ak-Produktion oder MΦ aktivieren zur Phagozytose ⇓ ⇓ h2 T , Antigen presentierende Zellen Funkzion: Exogene Proteinantigene zu endozytieren, sie zum immunogenen Peptiden zu zersetzen und diese im Komplex mit Histokompatibilitätsantigene der Klasse II MHCII an ihre Oberfläche zu Th-Zellen zu presentieren. Primäre: Makrophagen Dendritische Zellen B-Lymphozyten Sekundäre: Endothelzellen der Blutgefäße Epithelzellen im Darm Antigen presentierende Zellen Töten virusbefallene Zelle (CD8+:CTL) 9 Ag-Präsentation und Aktivierung von T-Zellen Aktivieren MΦ (CD4:Th1) Aktivieren B-Zelle (CD4: Th1+Th2) Antigen presentierende Zellen - Verteilung im Lymphknoten Im Cortex des Lk. in den T-Zell-Bereich Über den gesamten Lk. In den Follikeln Antigen presentierende Zellen - Verteilung im Lymphknoten Antigen presentierende Zellen - Verteilung im Milz Antigen presentierende Zellen - Makrophagen Antigen presentierende Zellen - Dendritische Zellen stammen aus der myeloische Linie niedrigere phagozytäre Kapazität Antigenpresentation (sind änlich zu Makrophagen) in alle Gewäben, auser Gehirn Exprimieren: MHC-Klasse-I MHC-Kalsse-II Molekül B7 (costimulation) ICAM-1, ICAM-2, LFA-1, LFA-3 (Adhäsionsmoleküle) Antigen presentierende Zellen - Dendritische Zellen Formen Follikuläre dendritische: • B-Zell Zone • keine Phagozytose • exprimieren keine MHCII • Ag-Ak Komplex einzufangen Î keine Internalisierung Î Komplex bleibt auf die Oberfläche Î B-Zellen erkennen das Antigen Interdigitierende dendritische Zellen: • T-Zell-Bereich • Stimulatoren der naive T-Zellen Langerhans-Zellen: in der Epidermis der Haut Antigen presentierende Zellen - Dendritische Zellen Langerhans-Zellen (unreife Dendritische Zellen) Ag aufnähmen: • Macropinozytose • Rezeptoren: HLA-I, HLA-II, CR1, CR3 Fc, FcεR Dendritische Zellen - Der Weg zu aktiven T- und B-Zellen A. A ber ü n o i t enta s ä r P ntigen r nd e a n e r e tivi k a . . . . D DC .... r e Î n od e l n l -Ze d töte T ive L un a n T t f C f i n r C t erde P B. A iese w C. d ellen Z B r (hie n e l l e eZ z ktio u d o r P ur Ak- n) Antigen presentierende Zellen Strukture von MHC-I und –II (Polypeptidketten) MHC-I MHC-II Antigen presentierende Zellen - Dendritische Zellen - Die Antigen-Prozessierung und -Präsentation 1. MHC I: körpereigene und fremde zytosolische, z.B. virale Proteine Zytosol ER calnexin Antigen presentierende Zellen - Dendritische Zellen - Die Antigen-Prozessierung und -Präsentation 2. MHC II: extrazelluläre und vesikuläre Antigene Die Lymphozyten - Vielfalt ihrer Rezeptoren Vielfalt durch 1. Rekombination der Gensegmente für Rezeptoren 2. Kombination der Ketten (alpha, beta bzw. schwere und leichte) 3. Verknüpfung an Verbindungsstellen Transmembrane Signaltransduktionsmodule Die Lymphozyten - Vielfalt ihrer Rezeptoren TCR BCR Die Lymphozyten - Vielfalt ihrer Rezeptoren Die Antigen-Präsentation an T-Zellen Die T-Zellaktivierung - Braucht Signal 1 (MHC/TCR) und 2 (Co-Stimulation) Die Antigen-Präsentation an T-Zellen - Die Effekte Die Antigen-Präsentation an T-Zellen - Die Effekte Die Antigen-Präsentation an T-Zellen - Naive T-Zellen erhalten Effektorfunktion • nach Aktivierung Î IL-2 sezerniert Differenzierung der T-Zellen in Th1/Th2 - Zytokinmilieu und Antigen sind bestimmend Aktivierung der T-Zellen - Zytokinmilieu und Antigen sind bestimmend Das Schicksal der naiven T-Zellen im Lymphknoten wird durch 3 Signale (von DC) bestimmt: 1. MHC I-, MHC II-Peptid Liganden Erkennung durch TCR (Signal 1): a. Geringe Interaktion, Selbstpeptide Î Anergie oder Apoptose oder Treg b. Mittlere Stärke oder Dauer der Interaktion Î Effektorzellen + central memory T-Zellen c. Starke, lange Interaktion Î Effektor-Zellen, die besten werden dann zu memory Effektorzellen 2. Co-stimulatorische Moleküle (Signal 2): * Aktivierung der T-Zellen(!), Polarisierung, Beeinflussung und Timing der Zytokinbildung * In Abwesenheit dieser Signale wird die T-Zelle anerg, was zur Toleranz führen kann (wichtig bei Selbstpeptiden). 3. Zytokine (Signal 3): * Polarisierung der TH-Antwort. Die Art der gebildeten Zytokine kann vom Subtyp der DCs, von der Art des Ag, der Entzündungsreaktion und dem Mikromilieu abhängen. Antigen-präsentierende Zellen Töten virusbefallene Zelle (CTL) 9 Ag-Präsentation und Aktivierung von T-Zellen Aktivieren MΦ (CD4:Th1) Aktivieren B-Zelle (CD4: Th1+Th2) Die B-Lymphozyten - Prinzip der B-Zellfunktion: Antigenerkennung führt zu monospezifischer Antikörperproduktion Knochenmark 9 wird Isotyp und spezifität determiniert von B-Zellen 9 negative Selektion unreife B-Zellen 9 IgM und IgD an die Oberfläche Treffen mit Antigen in sekundäre lymphatische Organen Plasmazellen Die B-Lymphozyten Aktivierung führt zur Produktion von Antikörpern Die B-Lymphozyten Aktivierung führt zur Produktion von Antikörpern Die B-Lymphozyten Aktivierung führt zur Produktion von Antikörpern 1 3 2 4 Die B-Lymphozyten Treffen in Lymphorganen die spezifischen T-Zellen Die Immunglobuline - Humoraler Teil der spezifischen extrazellulären Abwehr Î Antikörper gegen Antigene Î Glykoproteine, bestehend aus Polypeptidketten mit unterschiedlichen Zuckeranteil Î B-Zellen exprimieren Ig an ihrer Oberfläche = BCR! Î Antikörper-produzierende Zellen, die Ig an Umgebung abgeben = Plasmazellen Die Funktionen der Immunglobuline Funktionen Antikörper neutralisieren binden an andere Zelltypen aktivieren das Komplement Antigene binden (jedes Immunglobulin kann dabei nur an ein bestimmtes Antigen binden an die spezifische antigene Determinante = Epitop) Î Valenz: mindestens 2, IgA = 4, IgM = 10 Î Î Î Î Die Funktionen der Immunglobuline Î Bindung eines Antikörpers an ein Antigen: oft keine unmittelbaren Auswirkungen auf das Antigen Î erst, wenn weitere Effektor-Funktionen ins Spiel kommen (abhängig von der Bindung des Antikörpers an sein Antigen und Art der Antikörper-Moleküle) Î Neutralisation: Pathogen und/oder seine Produkte binden und sie damit zu neutralisieren (bakterielle Toxine, Oberfläche von Viren oder Bakterien) Î Bindung an verschiedene Zellarten: Phagozyten, Lymphozyten, Dendritische Zellen, Thrombozyten, Mastzellen und Basophile tragen an ihrer Oberfläche Rezeptoren (Fc Rezeptoren) Î Phagozytose wesentlich besser Die Funktionen der Immunglobuline Î binden auch an derartige Rezeptoren auf den Throphoblastzellen der Plazenta Î mütterlichen Ig durch die Plazenta in den fetalen Kreislauf Î schützen das Ungeborene vor Infektionen Î Komplementbindung und – aktivierung: Antikörper können durch Bindung an bestimmte Komplementkomponenten zur Aktivierung des Komplementsystems führen Î Lyse der beladenen Mikroorganismen, dabei Freisetzung von biologisch aktiven Mediatorsubstanzen und zur Beladung der Erreger mit bestimmten Komplementkomponenten Î noch bessere Opsonisierung IgG: Der universale Antikörper Î Monomere Î universiellste Immungloblinklasse (kann die meisten Funktionen der Immunglobuline ausüben) Î häufigstes Immunglobulin im Serum: bis 75% der Antikörper Î häufigstes und wichtigstes Immunglobulin im Extravaskulärraum (Gewebe) Î einzige Ig Klasse, die Plazentaschranke überqueren kann (Subklassen können unterschiedlich gut übertreten, IgG2 am schlechtesten) Î Komplementbindung ist unterschiedlich ausgeprägt, je nach Subklasse (IgG4 bindet das Komplement nicht) Î Makrophagen, Monozyten und manche Lymphozyten haben Rezeptoren für Fc-Region von IgG (Subklassen binden unterschiedlich gut: IgG2 und IgG4 z.B. gar nicht) Î IgG ist somit ein gutes Opsonin IgM: Der erste Antikörper Î Pentamere Î jeweils alle schweren und leichten Ketten ident, die Valenz beträgt maximal 10, Aufbau des Pentamers mit J-Kette, die durch Disulfidbrücken an 2 schwere Ketten gebunden ist Î IgM wird als erstes vom Fetus produziert Î auch das erste Immunglobulin, das von einer naiven B-Zelle produziert wird, wenn sie durch ein Antigen aktiviert wird Î Aufgrund seiner pentameren Struktur kann IgM das Komplement besonders gut binden Î IgM kann gut agglutinieren: Mikroorganismen und Antikörper verklumpen miteinander, die Keime werden eliminiert IgA: Der sezernierte Antikörper Î im Serum als Monomer, in Sekreten als Dimer Î auch hier ist eine J-Kette mit den beiden schweren (alpha) Ketten verbunden Î IgA ist der wichtigste Antikörper in Sekreten wie Tränen, Speichel, Kolostrum, Schleim Î besonders wichtig zur Ausbildung der lokalen (mukosalen) Immunantwort Î In Sekreten ist IgA mit einem weiteren Protein zusammen, dem sekretorischen Stück Î für den Transport durch die Epithelzellen notwendig (wird von den Epithelzellen produziert und an ihrer basalen Seite exprimiert) Î sekretorisches Stück beschützt das sezernierte IgA davor, in den Sekreten verdaut zu werden Î IgA bindet an CD89 (FcαRI-hochaffine Rezeptor) auf eosinoplilen und neutrophilen Granulozyten, Monozyten, Makrophagen Î Antigenerkennung durch zwei IgA Î Zellen degranulieren IgD: Der unbekannte Antikörper Î nur als Monomere IgD: Î IgD nur in sehr geringen Mengen im Serum Mission unknown Î Bedeutung ist unklar Î zusammen mit IgM ist als frühe Klasse on der B-Zellen koexprimiert Î IgD wird auf der Oberfläche von reifen naiven B-Zellen gefunden und fungiert dort als Antigenrezeptor IgE: Der allergische Antikörper Î nur Monomere Î IgE ist das seltenste Immunglobulin im Serum Î auch ohne Antigen bindet es an Oberfläche von Basophilen und Mastzellen an Fc Rezeptoren für IgE (FcεRI+II) Î an allergischen Reaktionen beteiligt: bindet ein Antigen an zwei oberflächengebundene IgE-Moleküle gleichzeitig Î Quervernetzung der Fc Rezeptoren der Mastzelle Î Freisetzung von pharmakologisch aktiven Substanzen, die die klinische Symptomatik der Allergie hervorrufen Î wichtige Rolle bei der Abwehr von parasitären Wurmerkrankungen Î gute Opsonine: IgE-Moleküle binden an Antigene auf den Parasiten Î docken sie an Fc Rezeptoren von Eosinophilen an Î Abtöten der Parasiten Die Funktionen der Immunglobuline +++ ++ + * dominierend weniger wichtig sehr selten Opsonin bei bestimmten Fc-Rezeptor-Allotyp (50% der weißen Bevölkerung) Die Verteilung der Immunglobuline Toleranzmechanismen Antikörper-Moleküle und T-Zellen-Rezeptoren können jedes andere Molekül erkennen, ob fremd oder körpereigen, sogar künstlich synthetisierte Î das Immunsystem ist bezüglich seiner Eigenschaft Antigene zu erkennen vollständig Î Toleranzmechanismen gegenüber „selbst“ sowie „fremd-ungefährlich“ von entscheidender Bedeutung T-Zellen B-Zellen Zentrale Toleranz Im Thymus: mTEC-Ag erkannt Î Apoptose = klonale Deletion, Elimination Im KM: Stromazelle Î klonale Deletion= Elimination oder Î neuer Rezeptor Periphere Toleranz • klonale Anergie • mangelnde Kommunikation = Ignoranz • klonale Anergie • klonale Ignoranz Maturation von T-Zellen in Thymus Toleranzmechanismen - Zentrale Toleranz der T-Zellen Positive selection: - TCR binds with „low avidity“ to self-peptide and self-MHC Î survive - do not recognize self MHC Î apoptose Negative selection: -TCR binds strongly to self peptide with MHC Î apoptose Toleranzmechanismen - Zentrale Toleranz der T-Zellen Toleranzmechanismen - Periphere Toleranz der T-Zellen 1. 2. 3. 4. Apoptose = klonale Elimination, Deletion Anergy = funktionelle Nicht-Reaktivität Aktive Suppression durch regulatorische T-Zellen Mangelnde Kommunikation = klonale Ignoranz: isolierte Moleküle in ZNS und Augen; fehlende MHC IIMoleküle; Antigen unterhalb Schwellenwert exprimiert Î spezifische T-Zellen weder aktiviert noch deletiert Toleranzmechanismen - Periphere Toleranz der T-Zellen 1. Apoptose Induktion von Activation-induced cell death (AICD) von T-Zellen: nach Restimulierung von kürzlich aktivierten CD4+ T-Zellen kommt es zur Induktion von Fas-Ligand (FasL) und Fas Î bei Bindung dieser beiden (auf Zelle selbst) oder durch nahe T-Zellen Î Apoptose ÎVerstärkt durch IL-2, also wenn viele T-Zellen aktiviert werden Î Deletion-induzierte Toleranz (FasL auch von HIV induziert, FasL auch auf Tumorzellen exprimiert) Toleranzmechanismen- Periphere Toleranz der T-Zellen 1. Apoptose Toleranzmechanismen - Periphere Toleranz der T-Zellen 2. Anergy Geringe Interaktion von DC und T-Zellen Geringe Menge an co-stimulatorischen Molekülen und MHC Molekülen Geringe Affinität des TCR zum MHC/Peptid Komplex Antigen-Erkennung parallel mit CTLA-4 statt CD28 (auf T-Zellen) und B7 (auf DC) Toleranzmechanismen - Periphere Toleranz der T-Zellen 2. Anergy Toleranzmechanismen - Periphere Toleranz der T-Zellen 3. Regulatorische T-Zellen Exprimieren IL-2 Rezeptor-α (CD25) Sind generiert nach „self-antigen recognition” in Thymus aber kann auch in peripherisches Lymphknoten Generierung ist abhängig von IL-2, TGF-β Charakterisiert durch die Produktion von immunsuppressiven Faktoren: IL-10, TGF-β Î Lymphozyten, Makrophagen sind gehemmt T-reg werden gebildet, wenn mit DC interagierende T-Zellen wiederholt hohen Mengen an IL-10 ausgesetzt werden IL-10 wird von einigen DC-Subtypen produziert T-reg unterdrücken TH1 und TH2-Antworten Toleranzmechanismen - Periphere Toleranz der T-Zellen 3. Regulatorische T-Zellen Toleranzmechanismen - Zentrale Toleranz der B Zellen Bindung von multivalenten, membranständigen Liganden (Zellmembran-Moleküle, dsDNA...) Î Elimination im KM Î oder Veränderung des Rezeptors (2. Chance) Toleranzmechanismen - Zentrale Toleranz der B Zellen Toleranzmechanismen - Zusammenfassung