Immunologie für die Praxis - Das Immunsystem der
Werbung
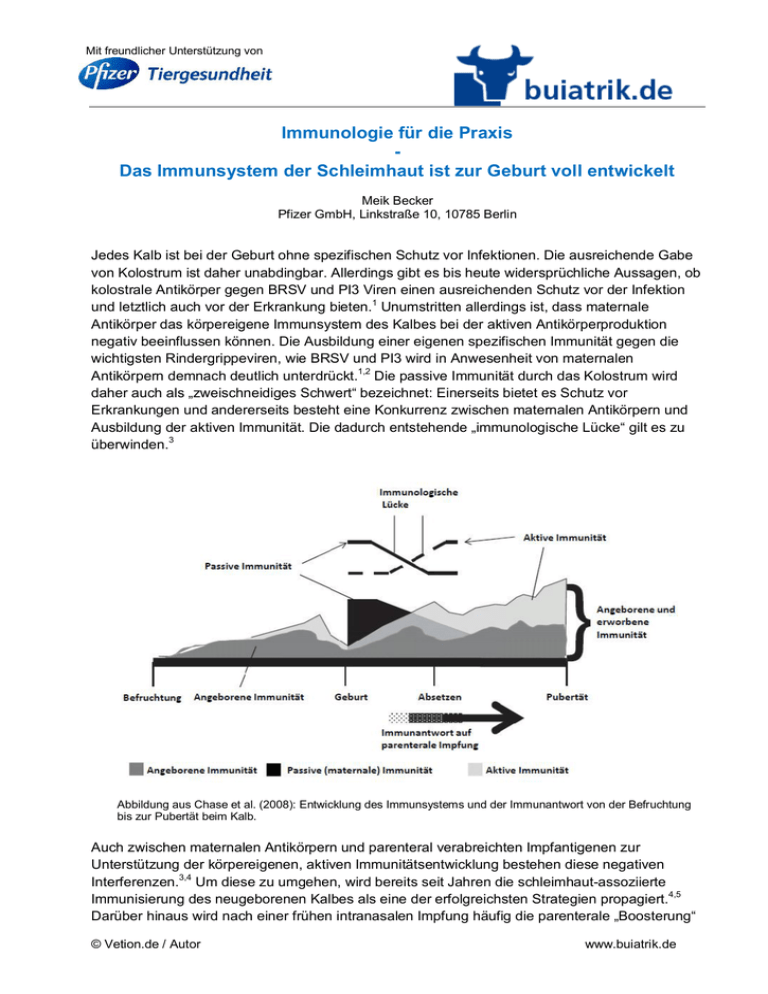
Mit freundlicher Unterstützung von Immunologie für die Praxis Das Immunsystem der Schleimhaut ist zur Geburt voll entwickelt Meik Becker Pfizer GmbH, Linkstraße 10, 10785 Berlin Jedes Kalb ist bei der Geburt ohne spezifischen Schutz vor Infektionen. Die ausreichende Gabe von Kolostrum ist daher unabdingbar. Allerdings gibt es bis heute widersprüchliche Aussagen, ob kolostrale Antikörper gegen BRSV und PI3 Viren einen ausreichenden Schutz vor der Infektion und letztlich auch vor der Erkrankung bieten.1 Unumstritten allerdings ist, dass maternale Antikörper das körpereigene Immunsystem des Kalbes bei der aktiven Antikörperproduktion negativ beeinflussen können. Die Ausbildung einer eigenen spezifischen Immunität gegen die wichtigsten Rindergrippeviren, wie BRSV und PI3 wird in Anwesenheit von maternalen Antikörpern demnach deutlich unterdrückt.1,2 Die passive Immunität durch das Kolostrum wird daher auch als „zweischneidiges Schwert“ bezeichnet: Einerseits bietet es Schutz vor Erkrankungen und andererseits besteht eine Konkurrenz zwischen maternalen Antikörpern und Ausbildung der aktiven Immunität. Die dadurch entstehende „immunologische Lücke“ gilt es zu überwinden.3 Abbildung aus Chase et al. (2008): Entwicklung des Immunsystems und der Immunantwort von der Befruchtung bis zur Pubertät beim Kalb. Auch zwischen maternalen Antikörpern und parenteral verabreichten Impfantigenen zur Unterstützung der körpereigenen, aktiven Immunitätsentwicklung bestehen diese negativen Interferenzen.3,4 Um diese zu umgehen, wird bereits seit Jahren die schleimhaut-assoziierte Immunisierung des neugeborenen Kalbes als eine der erfolgreichsten Strategien propagiert.4,5 Darüber hinaus wird nach einer frühen intranasalen Impfung häufig die parenterale „Boosterung“ © Vetion.de / Autor www.buiatrik.de Mit freundlicher Unterstützung von erst mit 2 bis 3 Monaten empfohlen. Also erst, wenn die Konzentration der maternalen Antikörper abfällt.2 Aber was passiert eigentlich bei einer Schleimhautimpfung genau? Wie reagiert das immunologisch naive Kalb auf diese Maßnahme? Dieses Thema wurde auch auf dem 23. Kongress der American Dairy Science Association im Mai dieses Jahres diskutiert. PJ Griebel von der Universität Saskatchewan in Kanada nimmt sich der bovinen Immunologie seit mehreren Jahren an. Seine Forschungsgruppe untersuchte, ob die intranasale Impfung mittels modifizierter Lebendvakzine eine geeignete Strategie sei, um neugeborene Kälber vor Atemwegserregern erfolgreich zu schützen. Die wichtigsten Resultate einer neu publizierten Studie (Hill et al. 2012) zur Immunantwort der Schleimhaut nach intranasaler Impfung beim neonatalen Kalb sind an dieser Stelle für Sie zusammengefasst: Die Schleimhaut und das dazugehörige Immunsystem sind in über 90% die erste Barriere für potenzielle Pathogene, mit denen das neonatale Kalb unmittelbar nach der Geburt im Respirations- und Verdauungstrakt konfrontiert wird. Aus diesem Grund ist es auch nicht verwunderlich, dass das mukosale Immunsystem auch beim Wiederkäuer bereits im Uterus hervorragend entwickelt ist. Bei vielen Haussäugetieren wird die Schleimhautimpfung daher routinemäßig eingesetzt. Welpen werden intranasal gegen Bordetella bronchiseptica, Katzen gegen feline infektiöse Peritonitis, Küken oral gegen Salmonellen und neugeborene Kälber gegen die wichtigsten Atemwegserreger lokal auf der Schleimhaut im oberen Respirationstrakt immunisiert. Für den antikörperbasierten Schleimhautschutz ist in erster Linie das Immunglobulin A verantwortlich (IgA). Das neonatale Kalb besitzt diese Schutzfunktion noch nicht. IgA ist zwar auf der respiratorischen Schleimhaut unmittelbar post natum nachweisbar, wird allerdings durch die mukoziliäre Clearance innerhalb weniger Tage wieder abgebaut. Die intranasale Impfung mit modifizierter Lebendvakzine (MLV) kann einen schnell einsetzenden und lang wirkenden Schutz induzieren. Unmittelbar nach der Applikation vermittelt die zelluläre Immunabwehr (CD 4+ Th1 und CD8+ Tc) den lokalen Schutz. Im Anschluss wird durch selektierte B-Zellen im respiratorischen Epithel lokal das protektive IgA produziert und über Rezeptoren an die Schleimhautoberfläche transportiert. Die Dauer der lokalen Immunität wird dabei vor allem durch die Art des Virus und dem jeweiligen Impfstamm bedingt. Wenn es als notwendig erachtet wird, kann die lokale IgA Produktion auch „geboostert“ werden. Schlussendlich ruft die IgA Produktion induziert durch die intranasale Impfung eine starke Immunantwort hervor. Dies gilt als Beweis für die ausgebildete Immunkompetenz der Schleimhaut beim neugeborenen Kalb und rechtfertigt damit auch den Einsatz einer frühen intranasalen Impfung als Prophylaxemaßnahme. Zusätzlich bietet die intranasale Impfung mit modifizierter Lebendvakzine nachweislich eine effektive Strategie, um Interferenzen zwischen Impfstoff und maternalen Antikörpern vollständig zu umgehen6. © Vetion.de / Autor www.buiatrik.de Mit freundlicher Unterstützung von Kontakt und weitere Informationen: Pfizer GmbH | Dr. Meik Becker Telefon: +49 (0)30 550055 5337 Email: [email protected] Linkstraße 10, 10785 Berlin Internet: www.pfizer-tiergesundheit.de Literatur: 1. Brodersen BW. Bovine respiratory syncytial virus. Vet Clin Food Anim 2010; 26: 323-333 2. Ellis JA. Bovine Parainfluenza-3-Virus. Vet Clin Food Anim 2010; 26: 575-593 3. Chase CCL, Hurley DJ, Reber AJ. Neonatal immune development in the calf and its impact on vaccine response. Vet Clin Food Anim 2008; 24:87-104 4. Kimman TG, Westenbrink F, Straver PJ. Priming for local and systemic antibody memory responses to bovine respiratory syncytial virus: Effect of amount of virus, virus replication, route of administration and maternal antibodies. Vet Immunopathol 1989; 22:145-160 5. Ellis J, Gow S, West K et al. Response of calves to challenge exposure with virulent bovine respiratory syncytial virus following intranasal administration of vaccines formulated for parenteral administration. JAVMA 2007; 230: 233-243 6. Hill KL, Hunsaker BD, Townsend HG et al. Mucosal immune response in newborn Holstein calves that had maternally derived antibodies and were vaccinated with an intranasal multivalent modified-live virus vaccine. JAVMA 2012; 240 (10): 1231-1240 © Vetion.de / Autor www.buiatrik.de











