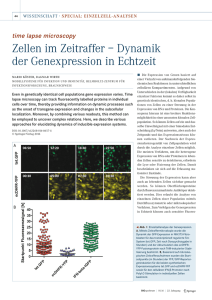
Untersuchungen zur Expression zweier FGF
Werbung

Untersuchungen zur Expression zweier FGF-bindender Proteine, des Fibroblasten-Wachstumsfaktor Bindungsproteins (FGF-BP) und des nukleolären Bindungsproteins (NoBP), während der Mausembryogenese Dissertation zur Erlangung des Grades eines Doktors der Naturwissenschaften der Fakultät für Chemie der Ruhr-Universität Bochum angefertigt an der Abteilung für Medizinische Mikrobiologie und Virologie (Leiter : Prof. Dr. H. Werchau) Arbeitsgruppe Priv.-Doz. Dr. Paul Kiefer vorgelegt von Volker Blecken aus Buxtehude Bochum Mai 2000 Tag der Disputation: 23.08.2000 Vorsitzender: Prof. Dr. W. Sander Referent: Priv. Doz. Dr. P. Kiefer Korreferent: Prof. Dr. R. Heumann 3. Prüfer: Prof. Dr. F. Stuhl Danksagung Ich danke Herrn Priv.-Doz. Dr. Paul Kiefer für die Überlassung des interessanten Themas und seine engagierte Betreuung, er war immer zu hilfreichen Diskussionen bereit. Bei Frau Dr. Marianne Antoine möchte ich mich für die vielen Tips, Tricks und die Hilfe bei den molekularbiologischen Arbeiten bedanken. Desweiteren bedanke ich mich allen jetzigen und ehemaligen Mitarbeitern der Arbeitsgruppe Kiefer, insbesondere Roman Köhl, Christian Roder und Kerstin Reimers-Fadhlaoui, für die gute Zusammenarbeit und das kollegiale Miteinander. Diese Arbeit konnte nur durchgeführt werden, weil andere Arbeitsgruppen der Medizinischen Fakultät immer bereit waren, bei technischen Engpässen auszuhelfen. Den Mitarbeitern im Schnellschnittlabor der AG Prof. Dr. Morgenroth danke ich für die Vakuumparaffinierung der Embryonen, der AG Prof. Dr. Mannherz, Frau Konieczny und Frau Klau, für die Möglichkeit, das Microtom und die Einbettungsstation zu benutzen. Besonders bedanken möchte ich mich bei der Arbeitsgruppe von Herrn Dr. H.J. Jacob, speziell bei Herrn Dr. Jacob und Frau Ritenberg, für die Bereitstellung des Präparierarbeitsplatzes und des Microtoms und ihrer Hilfe bei histologischen und entwicklungsbiologischen Fragestellungen. Den Mitarbeitern der zentralen Versuchstierhaltung danke ich für die gute Betreuung der Mäuse. Der AG Prof. Dr. Heumann danke ich für die Überlassung des BaculovirusExpressionssystems. Herrn Prof. Dr. Heumann danke ich für die Übernahme der Korreferats und Herrn Prof. Dr. Stuhl für seine Bereitschaft, als dritter Prüfer zu fungieren. Und nicht zuletzt möchte ich mich bei meinen Eltern für ihre Unterstützung bedanken, ohne die mein Studium so nicht möglich gewesen wäre. Abkürzungen A Abb. AER Amp APS BCIP C bp cDNA ddNTP DIG DMEM DNA dNTP DTT E ECL ECM EDTA EGF egr et al. FCS FGF FGF-BP FGFR FHF G g GTP h HGF his Hox HSPG Ig IGF IGFBP IPTG ISP kD LB M mAb MAPK MAPKK min Adenin Abbildung apical ectodermal ridge Ampicillin Ammoniumperoxodisulfat 5-Bromo-4-Chloro-Idolylphosphat Cytosin Basenpaare complementary DNA didesoxy Nukleintriphosphat Digoxigenin Dulbecco´s Modified Eagle Medium Desoxyribonucleinacid desoxy Nukleintriphosphat 1,4-Dithiothreitol Entwicklungstag enhanced-chemoluminiscence Extrazellulärmatrix Ethylendiamintetraessigsäure epidermal growth factor early growth response et altera fetales Kälberserum fibroblast growth factor FGF-Bindungsprotein fibroblast growth factor receptor FGF homology factor Guanin Erdbeschleunigung Guanintriphosphat Stunde hepatinocyte growth factor 6 x Histidin-Sequenz Homeobox Heparansulfatproteoglycan Immunglobulin insulin-like growth factor insulin-like growth factor binding protein Isopropyl-ß-D-1-thiogalactopyranosid Insektensignalpeptid Kilodalton Luria Bertani Mol/Liter monoklonaler Antikörper Mitogen Activated Protein Kinase Mitogen Activated Protein Kinase Kinase Minute mRNA mu NBT NLS NoBP nu-FGF3 OD p.a. PAGE PBS Pbx PCR PDGF PKA PLC RNA RT s SDS Sf Shh T TBS TEMED TGF-ß Tris Triton-X 100 Tween 20 U üN UTP UV V v/v w/v x-Gal ZPA messenger RNA murin Nitroblau, Tetrazolimsalz nuclear localization sequence Nukleoläres FGF-Bindungsprotein nukleäres FGF3 Optische Dichte pro analysis Polyacrylamid-Gelelektrophorese phosphate buffered saline pre B-cell leukemia transcription factor polymerase chain reaction plateled derived growth factor Proteinkinase A Phospholipase C Ribonucleinacid Raumtemperatur Sekunde Natriumdodecylsulfat Spodoptera frugiperda sonic hedgehog homolog Thymin tris buffered saline Tetramethylethylendiamin transforming growth factor ß Tris-(hydroxymethy-)aminomethan Octophenyl-polyethylenglycolether Polyoxy-ethylensorbitan-monolaureat Unit über Nacht Uraciltriphosphat Ultraviolett Volt Volumenprozent (volume per volume) Gewichtsprozent (weight per volume) 5-Bromo-4-Chloro-3-indolyl-ß-D-galactopyrasonid zone of polarizing activity Inhaltsverzeichnis 1 2 2.1 2.1.1 2.1.2 2.1.3 2.1.4 2.1.5 2.1.6 2.1.7 2.1.8 2.2 2.2.1 2.2.1.1 2.2.1.2 2.2.1.3 2.2.1.4 2.2.1.5 2.2.1.6 2.2.1.7 2.2.1.8 2.2.1.9 2.2.1.10 2.2.1.11 2.2.1.12 2.2.1.13 2.2.1.14 2.2.1.15 2.2.2 2.2.2.1 2.2.2.2 2.2.2.3 2.2.2.3.1 2.2.2.4 2.2.2.4.1 2.2.2.4.2 2.2.3 2.2.3.1 Einleitung Material und Methoden Materialien Chemikalien Enzyme Plasmide Verbrauchsmaterialien Geräte Antikörper Bakterienstämme und Zellen Tiere Methoden Molekularbiologische Methoden Polymerasekettenreaktion (PCR) Isolierung von Plasmid-DNA aus E.coli im kleinen Maßstab (Minipräp) Elektrophorese von DNA-Fragmenten in Agarosegelen Aufreinigung von DNA mit Phenol/Chloroform Ethanolfällung von DNA Restriktion von DNA Präparative Isolierung von DNA-Fragmenten aus Agarosegelen Alkalische Phoshatase-Reaktion Auffüllreaktion bei überhängenden Enden von DNA-Fragmenten Ligation Herstellung kompetenter Bakterien Transformation kompetenter Bakterien DNA-Sequenzierung Herstellung von Digoxigenin-RNA-Sonden Dot-Blot mit Digoxigenin-RNA-Sonden Methoden der In-situ Hybridisierung Präparation der Gewebe Einbettung der fixierten Gewebe in Paraffin In-situ Hybridsierung Protokoll der In-situ Hybridisierung in Gewebeschnitten Whole-mount In-situ Hybridisierung Herstellung von Acetonpulver zur Präabsorption des DIGAntikörpers Protokoll der Whole-mount In-situ Hybridisierung Methoden bei der Herstellung eines rekombinanten Baculovirus zur Expression von FGF-BP in Insektenzellen Selektion von transformierten DH10Bac-Klonen 1 14 14 14 15 15 15 15 16 16 16 17 17 17 18 18 19 19 19 19 20 20 20 21 21 22 23 24 24 24 25 26 27 28 29 30 30 30 2.2.3.2 2.2.3.3 2.2.3.4 2.2.3.5 2.2.3.6 2.2.3.6.1 2.2.3.6.2 2.2.3.6.3 2.2.3.6.4 2.2.4 2.2.5 3 3.1 3.1.1 3.1.2 3.1.3 3.2 3.2.1 3.2.2 3.2.3. 4 5 6 7 Aufreinigung von rekombinanter Baculovirus-DNA aus DH10BacE.coli Insekten-Zellkultur Herstellung von Virusüberstand Herstellung von FGF-BP enthaltenden Zellüberstand Methoden zum Nachweis des FGF-BP im Zellüberstand SDS-Polyacrylamid-Gelelektrophorese Silbergelfärbung Western-Blot Immunodetektion des FGF-BP Lungenorgankultur Hämatoxylin-Färbung der Lungenschnitte Ergebnisse Die Expression von FGF-BP, NoBP, FGF18 und FGF10 in verschiedenen Stadien der Mausembryogenese In-situ Hybridisierung in Gewebeschnitten im Zeitraum E 13.5 bis E 18.0 Whole-mount In-situ Hybridisierung mit Embryonen im Zeitraum E 7.0 bis E 10.5 Die Expression von FGF-BP und NoBP während der frühen Lungenentwicklung FGF-BP in der Lungenorgankultur Expression von humanem und murinem FGF-BPhis in Insektenzellen Der Überstand von huFGF-BPhis(ISP) expremierenden Zellen hemmt das FGF-induzierte Lungenwachstum Schnitte von kultivierten Lungen Diskussion Zusammenfassung Literatur Anhang 31 31 31 32 32 32 32 33 34 34 35 36 38 38 48 55 58 58 61 66 67 79 81 91 EINLEITUNG 1 1 Einleitung Die Fibroblastenwachstumsfaktoren (FGFs, fibroblast growth factors) Momentan umfaßt die Gruppe der Säugetier-FGFs 20 strukturell verwandte Proteine, die speziell während der Embryonalentwicklung eine bedeutende Rolle zu spielen scheinen, aber auch in adulten Geweben gefunden werden (eine umfangreiche Zusammenfassung zum aktuellen Stand der FGF-Forschung bieten Szebenyi und Fallon, 1999). Die verschiedenen FGFs weisen innerhalb einer etwa 120 Aminosäuren langen Kernsequenz eine 30-50%ige interspezifische Homologie der Aminosäurensequenzen und zwei konservierte Cysteine auf, die intraspezifische Homologie innerhalb der Säugetiere beträgt in der Regel über 90% (Coulier et al., 1997). Das ursprüngliche FGFGen scheint sehr alt zu sein, da man bereits in dem Fadenwurm C.elegans ein FGF nachweisen konnte (Roubin et al., 1999). An nahezu allen Prozessen, die im adulten Tier mit der Proliferation und der zielgerichteten Wanderung von Zellen verbunden sind, wie z.B. der Angiogenese, der Neovaskularisation von Tumoren und der Wundheilung, sind FGFs beteiligt. Die beiden als erste charakterisierten FGFs, FGF1 (Giminez-Gallego et al., 1985) und FGF2 (Esch et al., 1985), werden konstitutiv auch in adulten Geweben expremiert, FGF1 bevorzugt in neuronalen Zellen, während FGF2 fast überall gefunden wird. Die Expression der einzelnen FGFs, die in der Regel sekretiert werden, ist während der Embryogenese zeitlich und gewebespezifisch reguliert. Solche Expressionsdaten werden v.a. mit RNA-In-situ Experimenten in Gewebeschnitten und mit Geweben bzw. ganzen Embryonen (´Whole-mount` In-situ Hybridisierung) gewonnen. Mit einer markierten antisense-RNA Sonde können in den Zellen vorhandene RNAs indirekt nachgewiesen werden. FGFs als sekretierte Wachstumsfaktoren: hochaffine und niedrigaffine Interaktionen Wie viele andere Wachstumsfaktoren auch binden die sekretierten FGFs mit hoher Affinität an spezifische membranständige Tyrosinkinase-Rezeptoren, was die Dimerisierung und Aktivierung dieser Rezeptoren initiiert. In der Folge wird neben der Bildung bzw. Freisetzung verschiedener second messenger eine Signalkaskade eingeleitet, was schließlich zu der Aktivierung bestimmter Gene führt und damit eine Zelle anregt, sich zu teilen, zu differenzieren oder auch zu migrieren. Im Mittelpunkt dieser Signalkaskade, die in der Signaltransduktion vieler Tyrosinkinase-Rezeptoren eine wichtige Rolle spielt, steht das kleine G-Protein ras. Im aktivierten Zustand bindet ras die Kinase raf; EINLEITUNG 2 diese wiederum phosphoryliert eine andere Kinase (MAPKK), die dann ihrerseits die Kinasen MAPK 1 und 2 (mitogen-acitvated protein kinase) aktiviert. Diese Kinasen aktivieren sowohl verschiedene Proteine im Cytosol, können aber auch in den Kern translozieren (für eine aktuelle Zusammenfassung der FGFR-Signaltransduktion siehe Klint et al., 1999). Insgesamt kennt man sieben verschiedene FGF-Rezeptoren, die sich in ihrer Bindungsspezifität unterscheiden- FGFR-1, -2 und -3 in zwei Subtypen (b und c) und FGFR-4c (Ornitz et al., 1996). Die b und c Spleißvarianten der FGFR unterscheiden sich in der Struktur der dritten und letzten ihrer Immunglobulindomänen (Ig-3b bzw. Ig-3c), an die sich direkt die Transmembranregion anschließt. Für FGFR-2 konnte gezeigt werden, daß die Wahl eines der beiden Exons von Ig-3b oder Ig-3c gewebe- bzw. zelltypspezifisch ist (Shi et al., 1994). Die b-Variante wird vorzugsweise in epithelialen Zellen expremiert, während FGFR-2c in mesenchymalen Geweben gefunden wird (Orr-Urtreger et al., 1993). Das FGF7 bildet unter den FGFs insofern eine Ausnahme, indem es nur auf endodermale Zellen proliferativ wirkt und auch nur an einen Rezeptorsubtyp bindet, an FGFR-2b. Zu FGF10 existieren bis dato weniger Daten, es weist allerdings strukturell wie funktionell deutliche Parallelen zu FGF7 auf, bindet ähnlich gut an FGFR-2b, nicht aber an FGFR-1c oder FGFR-2c (Beer et al., 1997 und Igarashi et al., 1998). Im Gegensatz zu FGF7 scheint für FGF10 auch der FGFR-1b ein funktioneller Rezeptor zu sein, wenn auch bei deutlich geringer Affinität (Beer et al., 2000). FGF2 interagiert mit allen c-Varianten und zusätzlich mit FGFR-1b. FGF1 hingegen bindet an alle FGFR mit hoher Affinität (Ornitz et al., 1996). Neben den hochaffinen FGF-Rezeptoren existiert mit den Heparansulfatproteoglycanen (HSPG) eine niedrigaffine Rezeptorklasse. HSPGs sind hochglykosylierte, sulfatreiche Proteine, die ubiquitär in der Extrazellulärmatrix (ECM) und an der Zelloberfläche vieler Zelltypen vorkommen und neben ihrem Konnex zu FGFs die Fähigkeit besitzen, FGF-Rezeptoren (abhängig von der Gegenwart divalenter Kationen) zu binden (Kan et al., 1996). Speziell im Fall der in vielen embryonalen und adulten Geweben expremierten FGF1 und FGF2, scheinen die HSPG eine große Rolle zu spielen. So können einzelne HSPGs die Spezifität von FGFR-1 und FGFR-4 für FGF1 und FGF2 entscheidend verändern (Kan et al., 1999). Man vermutet, daß die Bindung der FGFs an die HSPGs im Allgemeinen zu einer besseren Verfügbarkeit der FGFs in vivo führt, weil auf diese Weise die sekretierten Wachstumsfaktoren einerseits verstärkt in der räumlichen Nähe der FGFR verbleiben und andererseits vor proteolytischen Abbau geschützt sind. Au- EINLEITUNG 3 ßerdem gilt es, spätestens nachdem man die dreidimensionale Struktur eines FGF/FGFR-Komplexes aufklären konnte, als sicher, daß HSPGs in vivo an der Bildung dieser Komplexe beteiligt sind; in einem zweifach symmetrischen Dimer, bestehend aus zwei Liganden und vier Rezeptoren, bildet sich eine Tasche, umgeben von basischen Aminosäuren, die eine gute Bindungsstelle für ein Heparansulfat darstellt (Plotnikov et al., 1999). Kürzlich konnte gezeigt werden, daß die Entwicklung des Tracheensystems in Drosophilalarven mit gestörter Bildung der HSPG gehemmt ist (Lin et al., 1999), was man in ähnlicher Weise bei dem Fehlen von branchless (Sutherland et al., 1996) – dem Drosophila-FGF – und breathless (Lee et al., 1996) – einem der beiden DrosophilaFGFR - beobachten kann. Solche Bindungsmoleküle, die ohne enzymatische Aktivität zu besitzen, aufgrund ihrer Faktoraffinität eine wichtige physiologische Aufgabe erfüllen, kennt man auch von anderen Wachstumsfaktoren. Das am besten untersuchte Beispiel bildet hier die Klasse der hochaffinen IGF (insulin-like growth factor)-Bindungsproteine (IGFBP), von denen zur Zeit sechs mit unterschiedlichen Bindungsspezifitäten bekannt sind (Ferry, 1999). Daneben kennt man noch vier niedrigaffine Bindungsproteine (IGFBP-related proteins). Je nach Protein kann die Bindung der IGFs an ihre die Signaltransdution vermittelnden membranären Rezeptoren gehemmt oder verstärkt werden. Für das IGFBP-3 existiert sogar ein eigener, spezifischer Membranrezeptor. Bindung von extrazellulärem FGF1 und FGF2 an FGF-Bindungsprotein Im Fall der FGFs kennt man ein sekretiertes Protein, das einerseits mit einer hohen Affinität verschiedene FGFs bindet, andererseits auch wie die FGFs selbst zu den Heparinbindenden Proteinen zählt. Dieses 17 kD große FGF-Bindungsprotein wurde erstmals 1991 von Wu et al. aus dem konditionierten Medium von A431 Zellen, einer humanen epidermalen Tumorzellinie, aufgrund dessen hoher Affinität zum ebenfalls von diesen Zellen sekretierten FGF2 entdeckt, aufgereinigt und charakterisiert. Der offene Leserahmen umfaßt 234 Aminosäuren. Das Protein weist, abgesehen von einer typischen hydrophoben Signalpeptidsequenz am N-Terminus keine bekannten Motive oder strukturelle Verwandtschaft mit anderen Proteinen auf. FGF-BP besitzt eine einzelne potentielle Glykosylierungsstelle an einem Asparaginrest in Position 99. Offenbar wird es in den A 431 Zellen C-terminal vor dem Methionin 168 prozessiert, da bei einer Analyse der Aminosäurenzusammensetzung des Proteins kein Methionin gefunden wurde. FGFBP mRNA wurde von der Arbeitsgruppe lediglich in normalen humanen Keratinocyten EINLEITUNG 4 und in malignen Hauttumoren gefunden, aber nicht in anderen humanen Geweben. Die transformierenden Eigenschaften von FGF1 und FGF2 auf diverse Zellinien verschwanden, wenn man gleichzeitig FGF-BP in das Kulturmedium gab. Diese Hemmung beruht, so vermuten die Autoren, darauf, daß FGF-BP gebundenes FGF nicht mehr mit den FGF-Rezeptoren interagieren kann, weil die Bindungsaffinität der FGFs zum FGFBP zu groß ist. Ein 150faches der Konzentration an FGF-BP genügte, um die mitogene Stimulation des FGF1 um die Hälfte zu verringern; im Fall des FGF2 betrug dieses Verhältnis 2400:1. Befand sich im Medium zusätzlich noch Heparin, das ähnlich den HSPGs bei einer geringen Affinität aufgrund der großen Anzahl der Bindungsstellen einen großen Anteil des FGF-Pools zu binden vermag, verschwand dieser Effekt. Interessanterweise nahm die Tumorgenität von A431 Zellen im Nacktmaus-Assay zu, wenn diese mit FGF-BP cDNA transfektiert worden waren. Die Autoren entwickeln daher die These, daß die Funktion des FGF-BP in vivo darin besteht, HSPG-gebundenes FGF2 bzw. FGF1 zu binden, dieses zu anderen Zellen oder in die Nähe der eigenen FGFRezeptoren zu transportieren, um es dort, möglicherweise verdrängt durch lösliches Heparin oder spezielle HSPGs, wieder abzugeben. Eine andere Arbeitsgruppe um Wellstein kommt in ihren Arbeiten mit dem FGF-BP von 1994 (Czubayko et al.) und 1997 (Kurtz et al.) zu einem ganz ähnlichen Schluß. Eine humane Zellinie, die FGF2 konstitutiv und stark expremiert, entwickelte erst nach der Transfektion mit FGF-BP transformierende Eigenschaften, nachgewiesen mit einem Soft-Agar und einem NacktmausHauttumorassay. Die durch die Kombination von FGF2 und FGF-BP hervorgerufenen Tumore wuchsen recht schnell und waren auffallend gut vaskularisiert. FGF1 und FGF2 werden von verschiedenen Zellinien im nur geringen Maße in das Zellmedium abgegeben, zum großen Teil bleiben die Faktoren in der Extrazellulären Matrix der Zellen, die die HSPG enthält, gebunden (Vlodavsky et al., 1991). Andere FGF wie z.B. FGF-7 dagegen bleiben im Medium gelöst. Die Expressionsstudien der Wellsteingruppe bestätigen die Ergebnisse von Wu et al. weitestgehend. Tumore, die in der Hautepidermis wachsen, expremierten viel FGF-BP, unabhängig davon, von welchem Tumorzelltyp sie sich ableiteten, während verschiedene Brusttumore kein oder nur sehr wenig FGF-BP enthielten. 1997 wurde im Wellsteinlabor das murine FGF-BP kloniert, das unprozessiert etwas größer ist als das humane FGF-BP, weil es an Position 178 einen Einschub von 17 Aminosäuren aufweist. Das murine FGF-BP erwies sich im Soft-Agar Assay als funktionell homolog zum humanen Protein; die zehn Cysteine sind allesamt konserviert, was EINLEITUNG 5 auf eine ähnliche Sekundärstruktur der beiden Homologe schließen läßt. Die Expression von FGF-BP während der Mausentwicklung wurde untersucht (Kurtz et al, 1997.). Mittels In-situ Experimenten mit 35 S-RNA konnten Transkripte von FGF-BP in Haut, Lunge und Darm nachweisen werden. Die Expression in der Haut beginnt am Entwicklungstag 9.5 und wird ab E 12 prominent, speziell in den epidermalen Basalzellen direkt an der Grenze zum locker gepackten Mesenchym, das nur schwach positiv bleibt. In späteren Entwicklungsstadien konzentriert sich die FGF-BP Expression laut Wellstein auf Zellen innerhalb der Haarfollikel. Im adulten Tier wird in der Haut nur noch wenig FGF-BP expremiert, maligne Tumore führen allerdings zu einem deutlichen Anstieg der Expression, die dann ähnlich stark ist wie während der Embryonalentwicklung. Im sich entwickelnden Darm wurde die Expression des FGF-BP im Lauf der Embryogenese spezifischer; nur die noch undifferenzierten Vorläuferzellen der Darmepidermis bilden in jungen Mäusen FGF-BP. In ihrer aktuellen Veröffentlichungen zeigte die Arbeitsgruppe, daß die Expression des FGF-BP durch die EGF-Signaltransduktion, die der der FGF stark ähnelt, aktiviert werden kann und daß diese Aktivierung durch die Hemmung der Proteinkinase C und der beiden MAPK1 und MAPK2 komplett aufgehoben wird (Harris et al., 1998 und 2000). Der Promotor des FGF-BP Gens besteht u.a. aus einer AP-1 (c-Fos/JunD) Bindungsstelle. c-Fos und JunD zählen zu den `immediate early` Genen, die sehr schnell nach der Aktivierung der ras/raf/MEKK/MAPK Signalkaskade induziert werden (Klint, 1999). Intrazelluläre und nukleäre FGF-Varianten Von mehreren FGFs wie den FGF1, -2 (Basilico und Moscatelli, 1992), -3 (Acland et al., 1990)und -11 bis -14 (Munoz-Sanjuan et al., 2000) kennt man verschiedene Isoformen, die von der Aktivierung alternativer Startcodi herrühren und von denen einige nicht mit einem Signalpeptid, aber mit einer NLS, einer nuclear localization sequence, versehen und daher im Zytoplasma und im Kern lokalisiert sind. Die biologische Rolle dieses intrazellulären Wachstumsfaktorpools ist noch nicht gut verstanden, ebenso ist noch ungeklärt, mit welchen intrazellulären Proteinen diese FGFs interagieren können. Bekannt ist, daß die mitogenen Eigenschaften des FGF1 verschwinden, wenn man die NLS entfernt, was auf eine wichtige biologische Rolle der intrazellulären FGFs hinweist (Joy et al., 1997; Mehta et al., 1998). Nur endogenes, intrazelluläres FGF2, das mit internalisierten FGF-Rezeptor 1 in der Zelle interagiert, fördert das Wachstum von Glia- EINLEITUNG 6 zellen, während von außen appliziertes FGF2 keinen proliferativen Effekt auslöst (Stuchowiak et al., 1997). Die Interaktion von nukleären FGF3 mit NoBP Die nukleäre/nukleoläre Variante des FGF3 wirkt in vitro als potenter Hemmer der Zellproliferation (Kiefer und Dixon, 1995). Stabil mit nu-FGF3 transfektierte Zellinien wachsen nur sehr langsam. Der Übergang der Zellen in die S-Phase des Zellzyklus scheint gehemmt zu sein, wobei der molekulare Mechanismus noch unbekannt ist. Deswegen wurden in der Arbeitsgruppe Kiefer in einem Hefe-Two-Hybrid System in einer humanen cDNA-Bank nach Interaktionspartnern des FGF3 gesucht (ReimersFadhlaoui, Dissertation 1999). Die am häufigsten gefundene cDNA kodiert für ein Protein mit einer Molmasse von 40 kDa, das bereits 1997 von der Arbeitsgruppe H.Busch als nukleäres Protein isoliert und sequenziert worden war und das von uns den Namen NoBP, nucleolar binding protein, erhielt. NoBP scheint nicht mit allen nukleären FGFs zu interagieren, denn ein weiterer Two-Hybrid Test mit FGF11 (ursprünglich FHF3; Smallwood et al., 1996) und FGF1 verlief im Falle des FGF11 negativ, während die Interaktion von FGF1 und NoBP recht schwach zu sein schien. Nach möglichen Homologen des NoBP wurde mittels einer Datenbankrecherche gesucht. Ein Mausprotein weist eine 82%ige Homologie der Aminosäurensequenz auf. Zwei Proteine aus dem Wurm C.elegans und der Bäckerhefe S. cerevisae ähneln dem NoBP sehr in ihrer Zentralregion mit 62 bzw. 55% Homologie und Austauschen von überwiegend äquivalenten Aminosäuren, während die C- und N-terminalen Enden stark von denen des humanen NoBP abweichen. Da NoBP ein Motiv mit einer regelmäßigen Abfolge von Lysin- und Argininresten aufweist, bindet es eventuell an DNA und/oder RNA. Ein Two-Hybrid Test mit dem putativen S.cerevisae NoBP und dem humanen FGF3 verlief dennoch positiv, und Tests mit trunkierten Versionen des NoBP identifizierten die zentrale Region als die Bindungsstelle für das FGF3. Weitere Untersuchungen zum NoBP wiesen seine nukleäre und nukleoläre Lokalisation in der Zelle nach. Mit Northern-Blots wurde die Expression des NoBP in vielen Zellinien und Geweben der adulten Maus, die insbesondere kräftig in Lunge, Herz, Milz und Nieren ist, nachgewiesen. Im Gegensatz dazu wird FGF3 kaum in adulten Geweben expremiert, die sekretierte Variante wird häufig in Brust- und Hauttumoren gefunden (Zhou et al., 1988). Interessanterweise wurden in differenzierenden HL60-Zellen, humanen multipotenten Knochenmarkszellen, keine NoBP-Transkripte entdeckt, während die undifferenzierten Zellen NoBP enthalten. Die EINLEITUNG 7 Daten, die bisher gewonnen wurden, weisen also auf eine wachstumsfördernde Funktion des NoBP hin, die teilweise auf der Bindung des nukleolären proliferationshemmenden FGF3 beruht. FGFs als Modulatoren epithelialer/mesenchymaler Interaktionen und Wachstumsprozesse während der Embryogenese: Lunge und Extremitäten Viele wichtige Organe - die Lunge, das vaskulare System, die Nieren und die meisten Drüsen- bestehen aus einem komplexen und sehr feinen Netzwerk von mit Membranen ausgekleideten Hohlräumen, durch die Gas bzw. Flüssigkeit fließt. Dieses Bauprinzip garantiert eine größtmögliche Oberfläche, wodurch ein effizienter Austausch von Stoffen über die Membranen erst möglich wird. Die Organisation und die Bildung dieser Netzwerke während der Embryonalentwicklung, insbesondere in der Lunge, fasziniert Entwicklungsbiologen und Mathematiker bereits seit Aristoteles (Metzger und Krasnow, 1999). Bei der Maus beginnt die Lungenentwicklung am Entwicklungstag 9.5, wenn epithelialendodermale Zellen aus der Wand des frühen Vorderdarms beginnen, sich vermehrt zu teilen, links und rechts in das sich seitlich ausbreitende, lockerer gepackte mesenchymale Gewebe hinein wachsen und dabei die beiden primären Lungenschläuche ausbilden (primary branching). Bereits zum Zeitpunkt 11.0 invasieren die ersten Zellen aus der Wand der Primärschläuche (secondary branching) und formen dabei ihrerseits neue sekundäre Tubuli, die kurz darauf wiederum knospen. Die Bildungsrate neuer Abzweigungen nimmt dabei laufend zu, und am Ende des Entwicklungstag 13 hat sich der linke Lungenschlauch , geformt von den epithelialen Zellen, bereits in mehrere Dutzend kleinere aufgespaltet. Anders als im humanen Embryo teilt sich der rechte Lungentubulus in der Maus früh in einen Haupt- und drei Nebenarme auf, die sich zu den vier rechten Lungenlappen der Maus weiterentwickeln. Dieser Prozeß verläuft ebenso dynamisch wie streng reguliert und wirft die Frage auf: Welche Signale bewirken auf welche Weise, daß sich bestimmte - hier epitheliale Zellen mit einer bestimmten Geschwindigkeit teilen? Bei der Beantwortung dieser Frage konnte in den letzten Jahren große Fortschritte gemacht werden, von einem vollständigen Bild ist man aber noch weit entfernt (aktuelle Zusammenfassungen zur molekularen Regulation der Knospung finden sich u.a. bei Metzger und Krasnow, 1999; Hogan und Yingling, 1998; Hogan, 1999; Warburton et al., 2000). EINLEITUNG 8 Als gesichert gilt, daß die Wechselwirkungen zwischen den epithelialen und den umliegenden mesenchymalen Zellen für die Regulation der Lungenbildung von entscheidender Bedeutung sind. So wurden neben einigen FGFs noch verschiedene andere Wachstumsfaktoren identifiziert, die im Mesenchym sekretiert werden und bewirken, daß sich die Teilungsrate im Epithel erhöht; ein gerichtetes Wachstum des Epithels wird also möglich, wenn es Zonen innerhalb des umliegenden Mesenchyms gibt, die mehr Wachstumsfaktor sezernieren als andere, oder wenn Zonen des Epithels unterschiedlich auf die einwirkenden proliferativen Signale reagieren. Die proliferativen Eigenschaften eines Wachstumsfaktors in der embryonalen Lunge lassen sich in vitro besonders deutlich dann testen, wenn man das Mesenchym um das Epithel entfernt und die Lungentubuli zu einem frühen Zeitpunkt – im Fall der Maus am Entwicklungstag 11 - in ein Gel einbettet, so daß ein Wachstum der Zellen in alle Raumrichtungen ermöglicht wird. Wenn man einen geeigneten Faktor in das Gel einbringt, bilden sich Knospen aus. Diese Technik wurde seit 1991 insbesondere von der Gruppe um Nogawa etabliert. Embryonale Lungenexplantate mit intaktem Mesenchym sind relativ einfach kultivierbar. Inzwischen wurden mehrere die Knospung auslösende Faktoren identifiziert. Dazu zählen HGF (hepatinocyte growth factor) (Ohmichi et al., 1996 und 1998), PDGF-B (platelet-derived growth factor) (Souza et al., 1994), FGF1 (Nogawa et al., 1995), FGF7 (Cardoso et al., 1997) und FGF10 (Bellusci et al., 1997). TGF-ß1 (transforming growth factor) hingegen übt einen hemmenden Einfluß auf die Expansion des Epithels aus (Serra et al., 1994). Alle drei genannten FGF binden bevorzugt an den FGFR-2b, der als einziger der FGF-Rezeptoren zu diesem frühen Zeitpunkt im Lungenepithel exprimiert wird. Gut untersucht sind insbesondere die Effekte der FGF in den Lungenorgankulturen, die sich trotz des gemeinsam genutzten Rezeptors unterscheiden lassen. Während FGF7 zunächst eine einfache Expansion des Lungenepithels auslöst, die erst nach etwa drei Tagen Kultur in eine angedeutete Knospung mündet, tritt diese bei FGF1 schon nach zwei Tagen ein, ohne daß eine vorherige Dilatation der Tubuli zu beobachten wäre (Cardoso et al., 1997). Die Applikation von FGF10 wiederum führt zu einer Expansion des Epithels und anschließend zur Ausbildung vieler großer Knospen (Bellusci et al., 1997b). In vitro wirkt FGF7 also anscheinend auf alle Epithelzellen gleichermaßen proliferativ, während FGF1 eine differentielle Wachstumsreaktion erzeugt. EINLEITUNG 9 FGF10 gilt als das stärkste Proliferationssignal für embryonale Lungenepithelzellen, das man kennt und wirkt auf diese Zellen als ein chemischer Lockstoff. Trotz einer ähnlichen Rezeptorspezifität beobachtet man bei FGF7 keinen chemotaktischen Effekt. Appliziert man ein mit FGF10 getränktes Heparin-Sepharose-Kügelchen neben einen E 11.5 Lungentubulus, bewegt sich die gesamte Struktur im Gel in die Richtung des Kügelchens, unabhängig ob mit oder ohne Mesenchym. Ist die FGF10 -Quelle erreicht, wird sie umwachsen (Park et al., 1998). Man fand, daß die Expression von FGF10 in dem frühen Stadium der murinen Lungenentwicklung sehr dynamisch reguliert wird. Am stärksten ist sie im Mesenchym direkt vor der Spitze des linken und der vier rechten Tubuli. Die Expression von FGF7 hingegen scheint weniger genau kontrolliert zu sein; es ist Lungenmesenchym viel gleichmäßiger verteilt und stärker während der späteren Embryonalentwicklung (Bellusci et al., 1997b). Anders als FGF7 wirkt FGF1 ebenfalls chemotaktisch, aber deutlich schwächer als FGF10 und scheint während der frühen Wachstumsphase der Lunge auch gar nicht expremiert zu werden (Bellusci et al., 1997b). Neben FGF7 und FGF10 kann man zu dieser Zeit noch FGF2 in dem Lungenmesenchym nachweisen (Post et al., 1996). FGF9 wird in dem frühen Epithel expremiert (Colvin et al., 1999). Von den anderen FGFs wird nur FGF18 in höheren Konzentrationen in der Lunge gefunden, etwa beginnend von E 14.5. bis zum adulten Tier (Ohbayashi et al., 1998). Auf struktureller Ebene bildet FGF18 mit FGF8 und -17 eine Subfamilie innerhalb der FGF, ihre Expressionsmuster während der frühen Embryonalentwicklung sind jedoch recht verschieden (Maruoka et al., 1998). Ein weiterer Hinweis auf die außerordentlich große Bedeutung des FGF10 für die Entwicklung der Lunge besteht darin, daß von den FGF-Knockout-Mäusen nur FGF10-/-Mäuse nicht lebensfähig sind, weil speziell die Lungenentwicklung in einem frühen Stadium gehemmt ist; die Trachea wächst zwar aus dem Endoderm des frühen Vorderdarm heraus, aber ohne daß sich Verzweigungen bildeten (Min et al., 1998; Sekine et al., 1999). Wenn die Signaltransduktion des FGFR-2b, dem hochaffinen Rezeptor des FGF10 (der auch von FGF1, -3 und –7 aktiviert wird) durch die Expression einer dominant negativen, löslichen Rezeptorvariante gehemmt wird, führt dies zu der NichtAnlage mehrerer Organe, darunter der Lunge und der Extremitäten (Peters et al., 1994; Celli et al., 1998). Ein ähnlich früher Abbruch der Lungenentwicklung tritt bei Shh(sonic hedgehog homolog; Litingtung et al., 1998) und Nkx2.1-Nullmutanten (Minoo et EINLEITUNG 10 al., 1999) auf; hier allerdings wird keine Trachea gebildet, lediglich zwei kleine tubuläre Strukturen wachsen direkt aus dem Vorderdarm heraus. Nkx2.1 ist ein Homeodomänen-Protein (früher TTF-1, thyroid transcription factor, genannt), das für die Induktion der Lunge von essentieller Bedeutung ist. Hemmt man die Expression von Nkx2.1 in kultivierten E 11-Lungen durch antisense RNA, stoppt die Proliferation des Epithels sofort, und es stirbt in der Folge sogar ab (Minoo et al., 1995). Interessanterweise entwickeln FGF7-/- -Mäuse dagegen normale Lungen und weisen lediglich Defekte bei der Haarbildung auf (Guo et al., 1996). Shh und sein Rezeptor, Patched (Ptc), wurden inzwischen als Schlüsselregulatoren vieler epithelial-mesenchymaler Wechselwirkungen dingfest gemacht. Shh wird von epithelialen Zellen expremiert und reguliert über das Signal seines Rezeptors Ptc, der im Mesenchym lokalisiert ist, die Aktivität der Gli-Transkriptionsfaktoren und damit die Expression verschiedener mesenchymaler Gene (Parisi et al., 1998). Es existieren Hinweise, daß in frühen Entwicklungsstadien die Expression von FGF10 durch die ShhSignale gehemmt wird. Daher wurde vorgeschlagen, daß ein negativer Rückkopplungsmechanismus zwischen Shh und FGF10 an der Regulierung des tubulären Wachstums beteiligt ist. Dort, wo die Konzentration an epithelialen Zellen hoch ist, befindet sich weniger FGF10 im angrenzenden Mesenchym. Das Epithel wird also bevorzugt dorthin proliferieren, wo bisher wenig epitheliale Zellen sind. Diese Hypothese wird durch den Phänotyp einer Mutante unterstützt, bei der das Shh unter der Kontrolle des surfactant protein C-Promotors während der frühen Lungenentwicklung in den epithelialen Zellen überexpremiert wird. Ohne die Shh regulierte Genexpression kommt es zu einer gleichmäßigen mesenchymalen Verteilung von FGF10 und die zu geringen Konzentrationsunterschiede führen zur unzureichenden Knospung des Epithels (Bellusci et al., 1997a). Eine interessante Erweiterung und Verfeinerung dieses Modells wurde 1999 durch die Arbeit von Lebeche et. al vorgenommen, die fanden, daß die FGF10 mRNA in E 11 Lungenexplanten durch die Applikation von TGFß-1 herunterreguliert wird, welches in geringen Mengen im Epithel exprimiert wird. Andererseits induzierte FGF10 die Expression von bmp-4 (bone morphogenic protein), einem weiteren Vertreter der TGFß-Familie, das in erster Linie in den Tubulispitzen gefunden wird (Bellusci et al., 1996) und von dem man annimmt, daß es die Expansion des Lungenepithels hemmt. Ein anderes, erst kürzlich in Mäusen entdecktes Protein, das einen hemmenden Einfluß auf die FGF-induzierte Zellproliferation ausübt und eine wichtige Rolle während der EINLEITUNG 11 Lungenentwicklung spielt, ist sprouty. Der Name sprouty stammt aus der Drosophilaforschung (Hacohen et al., 1998) und beschreibt den Phänotyp der sprouty-negativen Maden, bei denen aus der primären Tracheenanlage etwa doppelt so viele sekundäre Wege abzweigen als im Wildtyp. Eine Überexpression sproutys führt zu einem Abbruch der trachealen Entwicklung. Diese sekundäre Knospung wird von branchless, dem Drosophila-FGF induziert, dessen Rezeptor breathless in den trachealen Zellen expremiert wird. Die Expression von sprouty ist interessanterweise in den Zellklustern am stärksten, die gleichzeitig eine hohe Expression von branchless aufweisen und so den Startpunkt eines wachsenden sekundären Kanals bilden. Das hängt offenbar damit zusammen, daß branchless die Expression seines Antagonisten sprouty direkt über die Aktivierung eines Transkriptionsfaktors, pointed, induziert (Casci et al., 1999). Für das korrekte Wachstum des Tracheensystems scheint ein dynamisches Gleichgewicht zwischen sprouty und branchless essentiell zu sein. Inzwischen hat man festgestellt, daß sprouty nicht nur zu FGF, sondern auch zu EGF (epidermal growth factor) antagonistisch wirkt (Kramer et al., 1999). Offenbar moduliert sprouty die Aktivierung von ras und somit auch die MAPK (Reich et al., 1999). Der hohe Grad der Homologie zwischen den Proteinen des branch-less/breathless/sprouty Signalwegs in Drosophila und den FGF, FGFR und sprouty-Proteinen in Vertebraten (inzwischen kennt man z.B. vier murine sprouty-Varianten, siehe de Maximy et al., 1999), legt nahe, daß hier ein ähnlicher Mechanismus wirkt. Eines der ersten Ergebnisse in biologischen Assays mit den murinen sprouty-Varianten war denn auch, daß die Unterdrückung der sprouty-2 Expression in kultivierten E 11.5 Mauslungen zu einer massiven Verstärkung der Knospung führt (Tefft et al., 1998). 1999 konnte gezeigt werden, daß sprouty auch in Maus und Huhn antagonistisch zu EGF und den FGFs wirkt und durch die Signaltransduktion seiner eigenen Antagonisten aktiviert wird. Überexpression von sprouty kann z.B. zum Abbruch der Chondrozyten-Differenzierung und somit zu dem Fehlen einzelner Knochen führen (Minowada et al., 1999). Ein weitere augenfällige Mißbildung der FGF10 -Negativmutanten ist das Fehlen jeglicher Extremitäten; auch das war aufgrund der bereits bekannten Daten erwartet worden (eine aktuelle Übersicht zu diesem Thema bieten Martin, 1998; Ohuchi und Noji 1999; Xu et al., 1999). Von Experimenten mit Hühnerembryonen weiß man, daß der `zusätzliche Flügel`, der aus einer Region etwas proximal der Anlage des eigentlichen Vorderflügels erwächst, künstlich durch die Applikation von einigen FGFs (FGF1, FGF2, EINLEITUNG 12 FGF4, FGF8 und FGF10) induziert werden kann. Allerdings führt die jeweilige Nullmutation der FGF2 bis FGF9-Gene in Mäusen entweder nicht zu einer Hemmung der Gliedmaßenentwicklung (FGF2), oder die Embryonen sterben zu früh ab (FGF4 und FGF8), um Schlußfolgerungen ziehen zu können (Xu et al., 1999). In der frühen Phase der Anlage der Gliedmaßen in der Maus wurden jedenfalls zumindest FGF2 -, FGF4 - , FGF8 - und FGF9 -Transkripte im äußeren Ektoderm und der darin liegenden zentralen Zone, der apical ectodermal ridge (AER), gefunden. FGF2 und FGF10 dagegen werden im Mesenchym unterhalb der AER expremiert. Das momentan propagierte Modell der Gliedmaßenentwicklung postuliert eine stufenweisene Induktion von Proliferationssignalen (Martin, 1998; Xu et al., 1998): FGF8 aus dem die Somiten umgebenen Mesenchym induziert die FGF10-Expression in dem darüber liegenden Mesenchym, was wiederum zur Synthese von FGF8 in der äußeren ektodermalen Zellschicht führt. Das FGF8 induziert die Expression von mesenchymalen Shh nahe der Epidermis, was seinerseits zur Bildung von FGF4 führt, was die Synthese des Shh nochmals fördert. FGF4 und Shh bilden im jetzt etablierten Gliedmaß eine positive Rückkopplung aus, womit die schnelle Proliferation des mesenchymalen Gewebes gesichert ist. Wie man festgestellt hat, ist die Expressionsrate des Shh im Mesenchym der Extremität nicht symmetrisch, sondern konzentriert sich auf die caudale Seite, in der zone of polarizing activity. Die Etablierung der ZPA ist die Voraussetzung für den Aufbau der anterioren/posterioren Achse (Daumen zum kleinen Finger ) des Gliedmaß. Die hier zusammengefassten Forschungsergebnisse der letzten drei, vier Jahre belegen, daß die Regulation des Wachstums von Lunge und Gliedmaß ganz entscheidend auf der zeitlichen und örtlichen Regulation der Expression und der Aktivität verschiedener FGF-Wachstumsfaktoren beruht. Jedes Protein, das mit einem der beteiligten FGF interagiert und das mit diesem coexprimiert wird, ist somit ein potentieller Kandidat, eine Rolle innerhalb diese Regelkreise zu spielen. Ziel dieser Arbeit war es, die Expression der beiden beschriebenen FGF-interagierenden Proteine, dem sekretierten FGF-Bindungsprotein und dem nukleären Bindungsprotein, während der Mausentwicklung hinsichtlich ihrer gewebespezifischen und zeitlichen Lokalisation zu untersuchen und so Hinweise auf ihre Funktion in vivo zu erhalten. Besonderes Augenmerk wurde dabei auf die frühe Entwicklung der Lunge gelegt, da, wie beschrieben, verschiedene FGFs, davon in erster Linie FGF10, dort in einer dynami- EINLEITUNG 13 schen Weise expremiert werden und entscheidenden Anteil an der Regulation des Wachstumsprozesses haben. Dazu wurden In-situ Hybridisierungsexperimente mit den entsprechenden RNAs an Paraffinschnitten von Mäuseembryonen (Entwicklungstag 13.5 bis 18.0) durchgeführt, wie Whole-mount Hybridisierungen mit ganzen Embryonen (Entwicklungstag 7.0 bis 10.5) und frühen Lungen (Entwicklungstag 10.0 bis 13.5). Um fundierte Aussagen über mögliche Co-Expressionen mit FGF-Faktoren machen zu können, wurden für die Hybridisierungen u.a. FGF10- und FGF18-RNA-Sonden eingesetzt. Da bereits Untersuchungen zur Expression von FGF10 in den Lungen und FGF18 in Embryonen aus Whole-mount Experimenten veröffentlicht sind (Bellusci et al., 1997b; Ohbayashi et al., 1998; Hu et al., 1998), konnten diese Daten vorteilhaft zur Kontrolle der Spezifität der Hybridisierungsreaktionen herangezogen werden. Außerdem wurde damit begonnen, die Wirkung des FGF-BP auf die FGF-vermittelte Proliferation in kultivierten embryonalen Lungen zu untersuchen. Dazu wurden FGF-BP enthaltende Zellüberstände angefertigt, diese mit FGF-haltigem Medium vermischt und das Wachstum der Lungen in diesem Medium protokolliert. MATERIAL UND METHODEN 14 2 Material und Methoden 2.1 Materialien Die Herkunft der Chemikalien, Verbrauchsmaterialien, Geräte etc. ist teilweise innerhalb des Methodenabschnittes aufgeführt. Alle Lösungen sind, soweit nicht anders vermerkt, mit demineralisiertem Wasser aus der Reinstwasseranlage Seralpur PRO 90 CN der Firma Seral angesetzt. Sofern nicht anders vermerkt, wurden nur hochreine (p.a.) organische Lösungsmittel verwendet. Für Experimente mit RNA wurden alle Lösungen autoklaviert und teilweise DEPC-behandelt. 2.1.1 Chemikalien Agarose biozym, Eurogentec Bromphenolblau Serva Casein Merck EDTA Merck Ethidiumbromid Gibro BRL FCS Seromed Fettstift Daido Sangyo Formaldehyd Riedel-de Haen Gel Slick Serva Geniticin Gibco Life Gentamycin Seromed Glutaraldehyd Fluka Glycin biomol Harnstoff ICN Methylbenzoat Agros Organics SDS biomol TEMED Serva Tris biomol X-Gal bts Nicht aufgeführte Chemikalien wurden in der Regel von Sigma oder Baker bezogen. MATERIAL UND METHODEN 2.1.2 15 Enzyme Restriktionsendonukleasen Eurogentec, NEB, Promega SP6 und T7 RNA-Polymerase Eurogentec Protease K Sigma RNAse A Sigma 2.1.3 Plasmide pGem4Z Promega pMbac Stratagene pFASTBacHTa Gibco Life 2.1.4 Verbrauchsmaterialien Plastikwaren Brandt, Greiner, Nunc, Sarstedt, TPP Sterilfilter Sartorius, Gibco 2.1.5 Geräte Lambda 3 UV/VIS Spektrometer Perkin Elmer Chemie-Hybridpumpe vacuubrand Feinstwaage SBA 31 Scaltec Speed-Vac Univapo 150 H Uniequip Zellkulturbench HeraSafe Heraeus Agarosegelelektrophoresekammer Mupid 21 Eurogentec Microtom HM335E Microm Hybridisierungsofen Amersham Bakterienwarmluftschüttler Infors Brutschrank Heraeus Tischzentrifugen Beckmann pH-Meter 761 Knick Elektrogeräte Zentrifuge Mikrofuge RF Heraeus MATERIAL UND METHODEN Zentrifuge Avanti J.25 16 Beckmann mit Rotor JLA-10.500 2.1.6 Antikörper mAb Anti-Penta-His für Westernblots Qiagen mAb Anti-Maus aus Schaf; Amersham gekoppelt an Meerettich-Peroxidase mAb Anti-DIG-Antikörper, Fab-Fragmente ; Boehringer Mannheim gekoppelt an Alkalische Phosphatase 2.1.7 Verwendete Bakterienstämme und Zellen Escherichia coli DH5a supE44 ? lacU169(? 80lacZ? M15)hsdR17 recA1 endA1 gyrA96 thi-1 relA1 Escherichia coli DH10Bac Sf-21 Insektenzellen Gibco Life 2.1.8 Verwendete Tiere Auszucht-Mäuse HsdWinNMRI (Harlan Winkelmann) Die Mäuse wurden zur Zucht in der Zentralen Versuchstierhaltung der Ruhr-Universität gehalten. MATERIAL UND METHODEN 17 2.2 Methoden 2.2.1 Molekularbiologische Methoden Sofern nicht anders angegeben, wurden alle molekularbiologischen Arbeitsschritte gemäß Sambrook et al. (1989) durchgeführt. 2.2.1.1 Polymerasekettenreaktion (PCR) Die PCR wurde genutzt, um die DNA-Sequenz des huFGF-BPhis –Konstrukts zu modifizieren. Der Reaktionsansatz setzte sich zusammen aus: x µl DNA 5 µl 10x Taq-Polymerase-Puffer mit MgCl2 (Eurogentec) 5 µl DMSO 1 µl dNTP-Mix (10mM je Nukleotid) 1 µl 5´-Primer (1µg/µl) 1 µl 3´-Primer (1µg/µl) 0,5 µl Taq-Polymerase (Eurogentec) mit H2O auf 50µl auffüllen Der Ansatz wurde mit Mineralöl überschichtet. Es wurde ein PCR-Gerät (Biometra) mit Uno-Thermoblock benutzt. Der 40 Runden-Zyklus bestand aus drei Schritten: - 90 s Denaturierung bei 94°C - 3 min Primerannealing bei einer um 5-10°C unter der Schmelztemperatur des Oligonukleotid/DNA-Hybrids liegenden Temperatur, hier bei jeweils 58°C - 1-3 min DNA-Synthese (Elongation) bei 72°C, 1 min/1000bp Eine 10 minütige Inkubation bei 72°C und abschließende Kühlung auf 4°C führte zum Abbruch der PCR. Primer huFGF-BPhis 5´-3´: AGATCTAGATATCCGGATCCCATCACCATCACCAT Primer huFGF-BPhis 3´-5´: AGAGAATTCTTACAGGTCCTCCTCGCTGAT Die Primer wurden von Gibco Life bezogen. MATERIAL UND METHODEN 18 2.2.1.2 Isolierung von Plasmid-DNA aus E.coli im kleinen Maßstab (Minipräp) Um die erfolgreiche Transformation eines bestimmten Klons zu überprüfen, mußte die Plasmid-DNA isoliert werden, um eine Restriktionsanalyse durchführen zu können. Dazu wurde der Klon üN unter Schütteln in LB-Medium mit entsprechendem Antibiotikazusatz bei 37°C wachsen gelassen. 1.5 ml Bakteriensuspension wurden in der Tischzentrifuge bei 20000 g 15 s zentrifugiert und der Überstand verworfen. Das Pellet wurde in 350 µl STET-Puffer resuspendiert. Nach Zugabe von 25 µl Lysozymstammlösung (10 mg/ml in H2O) wurde 5 min bei RT inkubiert und anschließend 40 s in Wasser gekocht. Nach 30 minütiger Zentrifugation bei 20000 g und 4°C wurden die Eiweiß/Fettrückstände entfernt, die Nukleinsäuren durch die Zugabe von 420 µl Isopropanol und 0.3 M NaAc pH 7.0, gefällt und mit einer weiteren 10 minütigen Zentrifugation bei 20000 g und 4°C sedimentiert. Das Sediment wurde einmal mit eiskaltem EtOH gewaschen und vakuumgetrocknet. Anschließend wurde die DNA in 50 µl TE/RNAse-Puffer wieder gelöst. LB-Medium: 1 % (w/v) Bacto-Pepton 1 % (w/v) Hefe-Extrakt 0.5 % (w/v) NaCl autoklavieren STET: 8 % (w/v) Sucrose TE/RNAse: 0.5 % (v/v) Triton X-100 10 mM Tris/HCl pH 8.0 1 mM EDTA 50 mM EDTA 50 mg/ml RNAse A 10 mM Tris/HCl pH 7.0 2.2.1.3 Elektrophorese von DNA-Fragmenten in Agarosegelen Je nach erwarteter Größe der DNA-Fragmente wurden diese in 0.8 bis 1.2 %igen TAEAgarosegelen (von Eurogentec, mit 1µg/ml Ethidiumbromid) im elektrischen Feld bei 100 V getrennt und unter UV-Licht visualisiert. TAE: 40 mM Tris 5 mM NaOAc 1 mM EDTA autoklavieren MATERIAL UND METHODEN 19 2.2.1.4 Aufreinigung von DNA mit Phenol/Chloroform Der in einer wäßrigen Phase gelösten DNA wurde ein gleiches Volumen einer Mischung aus Phenol, Chloroform und Isoamylalkohol (25:24:1) zugesetzt. Nach Zentrifugation (20000 g, 10 min) wurde die wäßrige Phase in ein neues Eppendorfreaktionsgefäß überführt und gleichvolumig mit Chloroform/Isoamylalkohol versetzt. Nach erneuter Zentrifugation und Überführung der wäßrigen Phase in ein neues Eppendorfreaktionsgefäß wurde die DNA mit Ethanol gefällt. 2.2.1.5 Ethanolfällung von DNA Der DNA-Suspension wurden zwei Volumen EtOH und ein zehntel Volumen 3 M NaAc pH 5.2 zugesetzt. Nach einer Inkubation von 20 min bei –80°C wurde zentrifugiert (20000 g, 15 min, 4°C), der Überstand verworfen und das Sediment mit EtOH gewaschen. Nach erneuter Zentrifugation wie oben wurde das Sediment 5 min vakuumgetrocknet und anschließend in TE oder Wasser gelöst. 2.2.1.6 Restriktion von DNA Die Restriktion von DNA erfolgte mit Restriktionsendonuklease verschiedener Hersteller mit den dazugehörigen Puffersystemen bei den empfohlenen Temperaturen (meist 37°C) für 2-3h. Das Reaktionsvolumen betrug 20-50 µl, wobei je Ansatz etwa 1-2.5 U Enzym eingesetzt wurden. Die Reaktion wurde durch Zugabe von 1/6 Volumen DNA-Auftragspuffer gestoppt, die Proben auf einem Agarosegel aufgetrennt und – je nach Zweck der Restriktion – die DNA Fragmente aus dem Gel eluiert. 2.2.1.7 Präparative Isolierung von DNA-Fragmenten aus Agarosegelen Für die Isolierung von DNA-Fragmenten aus Agarosegelen wurde das Geneclean IIIKit (Bio/101-Inc) nach Herstellerangaben verwandt. MATERIAL UND METHODEN 20 2.2.1.8 Alkalische Phosphatase-Reaktion Vektoren wurden für die Ligation dephosphoryliert, indem gegen Ende der Restriktion 1 µl = 10 U Alkalische Phosphatase (Eurogentec) in den Ansatz gegeben und 30 min bei 37°C inkubiert wurde. 2.2.1.9 Auffüllreaktion bei überhängenden Enden von DNA-Fragmenten Um bei der Restriktion entstandene überhängende Enden aufzufüllen, wurde die T4 DNA Polymerase (Eurogentec) oder das Klenow-Fragment ohne 5´-3´ Exonukleaseaktivität verwandt. Die Inkubation erfolgte in einem 30 µl Ansatz 1 h bei RT. 23 µl H2O, inklusive DNA 2 µl dNTP-Mix (2mM, jeweils) (TaKaRa) 3 µl 10x Reaktionspuffer 2 µl Enzym Anschließend wurde die DNA mit einer Agarosegelelektrophorese vom Enzym getrennt und aus dem Gel eluiert. 2.2.1.10 Ligation Für die Ligation wurden sowohl die DNA-Fragmente wie der dephosphorylierte Vektor über ein Agarosegel gereinigt. Die Ligation des Inserts in die Vektoren erfolgte über Nacht bei 16°C oder in 2 h bei RT in einem 20 µl Ansatz: 2 µl 10x Ligationspuffer x µl Insert-DNA y µl Vektor-DNA 1 µl T4-DNA-Ligase mit H2O auf 20 µl auffüllen Das molare Konzentrationsverhältnis Vektor/Insert sollte etwa 1:3 betragen. Als Kontrolle diente eine Ligation ohne den Zusatz des Inserts. MATERIAL UND METHODEN 21 2.2.1.11 Herstellung kompetenter Bakterien (Hanahan, 1983) 3 ml einer E.coli-DH5a bzw. DH10 Übernachtkultur wurden in 200 ml LB-Medium im Warmluftschüttler bei 37°C bis zu einer Dichte von OD600 ˜ 0.3 wachsen gelassen. Die Bakterienkultur wurde 15 min auf Eis abgekühlt, dann 5 min bei 3000 g und 4°C zentrifugiert. Die sedimentierten Bakterien wurden in 16 ml Transformationspuffer I resuspendiert und 15 min auf Eis inkubiert. Nach erneuter Zentrifugation (wie oben) wurden die Bakterien in 16 ml Transformationspuffer II resuspendiert und sofort in Aliquots zu 210 µl in flüssigem Stickstoff schockgefroren. Die kompetenten Bakterien wurden bei –80°C gelagert. Transformationspuffer I: 100 mM RbCl 50 mM MnCl2 30 mM KOAc pH 7.5 10 mM CaCl2 15 % (w/v) Glycerin pH 5.8 mit 0.2 M HAc einstellen steril filtrieren Transformationspuffer II: 2 % (v/v) 0.5 M MOPS pH 6.8 10 mM RbCl 75 mM CaCl2 15 % (w/v) Glycerin steril filtrieren 2.2.1.12 Transformation kompetenter Bakterien Pro Transformation wurden 100 µl der kompetenten Bakterien aufgetaut, zu dem Ligationsansatz bzw. einer Plasmidlösung gegeben, 30 min auf Eis inkubiert und danach 90 s bei 42°C hitzegeschockt. Die Transformationsansätze wurden mit 500 µl kaltem LB-Medium versetzt und für 2 h bei 37°C inkubiert. Die gesamten Transformationsansätze wurden auf vorgewärmten LB-Platten, die 100 µg/ml Ampicillin enthielten, trokken ausgestrichen und über Nacht bei 37°C inkubiert. LB-Platten: 1.5 % Agar in LB-Medium autoklavieren, Lagerung bei 4°C MATERIAL UND METHODEN 22 2.2.1.13 DNA-Sequenzierung Die Sequenzierungen wurden nach der Dideoxy-Kettenabbruch-Methode von Sanger (1977) durchgeführt. Verwendet wurde das T7 Sequenase Version 2.0 DNA sequenzing kit von USB. Für jede Sequenzierreaktion wurden 18 µl Minipräp-DNA mit 2 µl 2 M NaOH/ 2 mM EDTA-Lösung 5 min bei RT und 20 s bei 68°C inkubiert, dann auf Eis gekühlt. Nach Zugabe von 7 µl Wasser, 3 µl 3 M NaAc pH 5.2 und 75 µl kaltem EtOH wurde die DNA durch 30 min Inkubation bei –80°C und Zentrifugation (20000 g, 15 min, 4°C) gefällt und sedimentiert. Nach einmaligen Waschen mit kaltem EtOH wurde die DNA vakuumgetrocknet und in 7 µl Wasser gelöst. Die DNA wurde mit 2 µl 5x Sequenase Buffer und 1 µl Sequenzierungsprimer (10 ng/µl) gemischt. Für das Annealing der Sequenzierungsprimer wurden die Ansätze 2 min bei 75-80°C inkubiert und dann langsam auf unter 35°C abkühlen gelassen. Zu den 10 µl DNA-Lösung wurden dann 1 µl 0.1 M DTT, 2 µl 1:5 verdünnter GTP-Labeling-Mix, 0.5 µl [a-35S]-dATP und 2 µl 1:8 verdünnte Sequenase gegeben und 5 min bei RT inkubiert. In die Vertiefungen einer Nunc-Mitrotiterplatte wurde für jede Reaktion jeweils 2.5 µl der vier ddNTP-Lösungen vorgelegt und jeweils 3.5 µl der Labeling-Reaktion dazupipettiert. Nach 5 min Inkubation bei 37°C wurde zu den Sequenzierungsreaktionen 4 µl Stop-Lösung gegeben. Vor dem Auftrag auf das Gel wurden die Proben 2 min bei 90°C denaturiert. Für das Sequenziergel wurden 36.8 g Harnstoff in 32 ml Wasser auf 60°C erwärmt und gelöst, auf Eis gekühlt und 12 ml 40 % 19:1 Acrylamid/Bis-Mix und 8 ml 10 x TBE dazugegeben. Direkt vor dem Gießen des Gels in eine Gelapparatur von Serva, wurden 140 µl 25%ige APS-Lösung und 85 µl TEMED hinzupipettiert. Vor dem Auftrag von 4 µl der Sequenzierungsproben wurde das Gel für 10 min einer Vorelektrophorese unterworfen. Die Elektrophorese wurde bei einer Stromstärke von 40 mA und bei einer Spannung von ca. 1.0 kV durchgeführt. Nach der Elektrophorese wurde das Gel direkt auf ein Whatman-Papier übertragen und bei 80°C im Vakuum getrocknet. Ein Röntgenfilm wurde aufgelegt und nach ein bis drei Tagen entwickelt. TBE: 90 mM Tris 90 mM Borsäure 1 mM EDTA autoklavieren MATERIAL UND METHODEN 23 2.2.1.14 Herstellung von Digoxigenin-RNA-Sonden Von den in den pGem4Z klonierten cDNA-Fragmenten wurden mit Hilfe der T7- und der SP6-Polymerasen unter Verwendung eines DIG-RNA-Labelingmixes (Boehringer Mannheim) digoxigenierte RNA-Kopien erstellt. Die Reaktion und die Aufreinigung der RNA-Sonden erfolgte nach Angaben des Herstellers (Boehringer Mannheim - Nonradioactive In-situ Hybridization - Application manual). Zunächst wurde das Plasmid per Restriktion linearisiert und mit einer Phenol/Chloroform-Extraktion vom Restriktionsenzym gereinigt. Folgender Ansatz wurde zusammenpipettiert: 1 µg linearisierte Plasmid-DNA in 10µl H2O 2 µl 10x Biotin RNA Labeling Mix : 10 mM ATP, 10 mM CTP, 10 mM GTP, 6.5 mM UTP, 3.5 mM Biotin-16-UTP (Boehringer Mannheim) in Tris/HCl pH 7.5 2 µl 10x Transcription Buffer (400 mM Tris/HCl pH 8.0, 60 mM MgCl2, 100 mM Dithiothreitol (DTT), 20 mM Spermidin 2 µl RNA-Polymerase SP6 bzw. T7 4 µl H2O Nach zweistündiger Inkubation bei 37°C wurden 2 µl 0.2 M EDTA pH 8.0 hinzupipettiert, um die Reaktion zu stoppen. Um die markierte RNA zu fällen, wurden 2.5 µl 4 M LiCl und 75 µl eiskaltes EtOH hinzugegeben und 30 min bei –80°C gefällt. Anschließend wurde die RNA mittels einer Zentrifugation (13000 g, 15 min, 4°C) sedimentiert und der Überstand verworfen. Das Sediment wurde mit eiskaltem 70%igen EtOH gewaschen, wiederum wie oben für 5 min zentrifugiert, 5 min vakuumgetrocknet und anschließend in frisch autoklaviertem Wasser gelöst. Die Konzentration der synthetisierten RNA wurde abgeschätzt, indem 2 µl der Lösung einer Gelelektrophorese in einem 1%igem TBE-Agarosegel unterworfen wurden. Dazu wurde die ElektrophoreseApparatur mindestens 2 h in 3% H2O2 inkubiert und danach dreimal mit autoklaviertem Wasser gewaschen. Puffer und Gel waren frisch autoklaviert. Die cDNAs der untersuchten Gene waren durch PCR aus einer Maus-RNAAufreinigung amplifiziert und in der Regel in den pGem4Z-Vektor kloniert worden (Dr. Marianne Antoine). Das egr2 Konstrukt war eine freundliche Gabe aus dem Labor von David Wilkinson, London. Die folgende Tabelle stellt die Konstruktion der DigRNAs dar (+ = antisense, - = sense): MATERIAL UND METHODEN 24 DIG-RNA Quelle Basenpaare Vektor FGF-BP (+) mus 1-755 pGem4Z (-) FGF-10 (+) pGem4Z human 1-630 pGem4Z NoBP mus 178-839 pGem4Z FGF-18 mus 1-624 pGem4Z FGF-1 mus 1-484 pGem7Zf(+) shh (+) mus 604-1314 pGem4Z (-) (-) egr2 1-604 mus 750bp blueskript 2.2.1.15 Dot-Blot mit Digoxigenin-RNA-Sonden Um die effektive Konzentration der digoxigenierten RNAs, d.h. die Menge des eingebauten Digoxigenins abschätzen zu können, wurden Dot-Blots durchgeführt, bei der eine Verdünnungsreihe der zu untersuchenden DIG-RNA und eine Verdünnungsreihe mit einer digoxigenierten DNA (Boehringer Mannheim), deren Konzentration bekannt war, auf einer Nitrocellulosemembran (bezogen von Schleicher & Schuell, Porengröße 45 µm) aufgetragen wurde. Der Dot-Blot wurde gemäß den Herstellerangaben durchgeführt. Nach mehreren, voneinander unabhängigen Experimenten, erwies sich, daß die relative Konzentration des gebundenen Digoxigenins stets konstant im Verhältnis zur gesamten Dig-RNA (ermittelt per Gelelektrophorese, siehe 2.2.1.15) blieb. Daher wurde im Folgenden auf die regelmäßige Durchführung von Dot-Blots verzichtet, und die Digoxigenierung nur noch stichprobenartig überprüft. 2.2.2 Methoden der In-situ Hybridisierung 2.2.2.1 Präparation der Gewebe HsdWinNMRI-Mäuse wurden angepaart und die erfolgte Paarung durch Kontrolle des Vaginalplaques überprüft. Trächtige Mäuse wurden durch zervikale Dislokation getötet, die Bauchdecke geöffnet und der Embryonenschlauch entnommen. Zur Bestimmung der Entwicklungsstufe eines Embryos, die innerhalb eines Wurfes erheblich differieren MATERIAL UND METHODEN 25 kann, wurden während der Präparation die Somiten gezählt (Entwicklungstag 8 bis 10), die Größe der Lunge oder der Gliedmaßen herangezogen (Entwicklungstag 10 bis 13), oder die Körpergröße gemessen (ab Tag 14). Die E 18 Embryonen wurden dekapitiert und ihr Brustkorb wurde eröffnet, um die effiziente Perfusion der Gewebe zu ermöglichen. Zur Lungenpräparation wurden die Embryonen auf Eis gekühlt und möglichst schnell in kaltem PBS --, d.h. innerhalb von zwei Stunden, präpariert. Je nach Größe der Lunge bzw. des Embryos lag die Dauer der Fixierung in eiskaltem 4% Paraformaldehyd/PBS -- zwischen einer und 24 h. PBS-- 137 mM NaCl 2.7 mM KCl 1.5 mM KH2PO4 4.3 mM Na2HPO4 pH 7.4, autoklavieren 2.2.2.2 Einbettung der fixierten Gewebe in Paraffin Zur Einbettung der Gewebe in Paraffin (rotiplast von Roth, Schmelztemperatur 62°C) wurden diese zunächst in PBS -- und 0.85%iger Kochsalzlösung je eine Stunde gewaschen und in einer aufsteigenden Alkoholreihe (0.85%ige NaCl-Lösung/Ethanol mit 50, zweimal 70, 85, 95 und zweimal 100% Ethanol) entwässert und entfettet. Anschließend folgten je zwei Waschungen in Isopropanol und in Rotihistol (Roth), einem XylolErsatz. Je nach Größe des Embryos betrug die Dauer jedes Waschschrittes zwischen zwei und 24 h. Große Embryonen ab dem Entwicklungstag 16 wurden zusätzlich nach dem Isopropanol über Nacht in Methylbenzoat gewaschen und so geschmeidig gemacht. Embryonen ab E 13 wurden anschließend über Nacht im Vakuum mit dreifachem Paraffinwechsel paraffiniert (im Tissue-Tek, Miles Scientific, Schnellschnittlabor der AG Prof. Morgenroth) und danach in einem Ofen im Paraffin auf 68°C erhitzt. Kleinere Embryonen wurden über Nacht im Ofen bei 68°C und drei bis vier Wechseln paraffiniert. Anschließend wurden die Embryonen, möglichst exakt ausgerichtet, in Formen unter Paraffin eingegossen. Die über Nacht erstarrten Paraffinblöcke wurden bei 4°C gelagert. Mit der HM 335 E (AG Prof. Dr Mannherz) wurden 3 µm dicke Schnitte angefertigt und direkt auf den Objektträgern (superfrost plus, Firma menzel-gläser) über Nacht bei MATERIAL UND METHODEN 26 42°C getrocknet. Ab diesem Arbeitsschritt bis zur Hybridisierungsreaktion waren alle Lösungen autoklaviert, das Wasser DEPC-behandelt. Alle Glaswaren wurden 6 h bei 180°C gebacken und so RNAse-frei gehalten. 2.2.2.3 In-situ Hybridisierung Die In-situ Hybridisierung in den Gewebeschnitten wurde nach einem selbst erstellten Protokoll durchgeführt, das auf den Protokollen von Baumgart et. al (1997) und Wilkinson und Nieto (1993) basierte. Die Konzentration der Dig-RNAs wurde abgeschätzt, indem ein Teil davon auf ein Agarose-Gel aufgetragen und mit Ethidiumbromid angefärbt wurde. Die optimale Verdünnung der Probe wurde in Vorversuchen ermittelt und betrug in der Regel 1:100 bis 1:1000. Die Konzentration der Protease K betrug immer 25µg/ml, und in Vorversuchen wurde die jeweils optimale Dauer des Verdaus eines Gewebes mit einer Zeitreihe ermittelt, typischerweise 0, 2, 5, 10, 15, 20 und 30 Minuten. Als Test-RNA wurde in der Regel antisense-FGF-10 benutzt. In den meisten Fällen ergab sich eine optimale Inkubationszeit von zwei bis 15 Minuten. Als Kontrolle diente eine Reaktion mit einer sense-RNA. Die einzelnen Schnitte wurden mit einem hydrophoben Film aus einem Fettstift umrandet, um ein Verlaufen der Proben zu verhindern. Das Volumen der Hybridisierungslösung betrug etwa 0.1 bis 0.4 µl/mm². MATERIAL UND METHODEN 27 2.2.2.3.1 Protokoll der In-situ Hybridisierung in Gewebeschnitten Deparaffinierung Rotihistol über Nacht Rehydrierung absoluter EtOH, 95%, 85%, 70%, aqua bidest jeweils 5 min Postfixierung 4% Paraformaldehyd/ PBS--- Deproteinierung 10 min PBS 2 x 5 min 0.1M HCl 10 min -- PBS 2 x 5 min Proteinase K , 20 µg/ml in 50mM Tris/HCl, 2 bis 15 min 5mM EDTA, pH 8.0 PBS-Acetylierung 2 x 5 min Essigsäureanhydrid 0.25% (v/v) in 0.1M 20 min Triethanolamin Dehydrierung PBS-- 2 x 5 min 70%, 85%, 95% EtOH jeweils 5 min an der Luft trocknen Hybridisierung Waschschritte Prähybridisierungslösung mindestens 2 h, 42°C Hybridisierungslösung 5 bis 10 h, 48°C 2 x SSC 2 x 30 min, 58°C 1 x SSC, 50% Formamid 1 h, 58°C 0.5 x SSC 2 x 10 min 0.2 x SSC 10 min -- PBST: PBS , 0.1% Tween 20 (v/v) Blockieren unspezifischer 10% hitzeinaktiviertes (1 h bei 65°C) 10 min 2 bis 4 h, 4°C Antikörperbindungsstellen Schafserum (Sigma), in PBST Antikörperreaktion Anti-DIG-Antikörper, Fab-Fragmente (Boeh- über Nacht, 4°C ringer Mannheim), 1:1000 in PBST PBST 4 x 10min NTMT: 100mM NaCl, 100mM Tris, 50mM 2 x 5min MgCl2, 2mM Levamisol, 0.1% Tween 20 (v/v), pH 9.5 Farbreaktion Eindeckeln 4-Nitroblau-tetrazoliumchlorid (NBT), 0.35 bei 37°C unter ständiger mg/ml Beobachtung, oder über 5-Bromo-4-chloro-3-indolyl-phosphat Nacht bei 4°C, vor Licht (BCIP) 0.18 mg/ml in NTMT schützen TE 1 x 10 min Kaiser´s Glyceringelatine (Merck) MATERIAL UND METHODEN 28 Um die Hintergrundfärbung in den Zellen und Zellkernen zu verringern, wurde bei einigen Experimenten auf eine Acetylierung verzichtet. Das führte aber gleichzeitig zu einer deutlichen Abschwächung der Färbung des Cytosols. Prehybridisierungslösung 50 % deionisiertes Formamid (Sigma) 50 mM Tris 25 mM EDTA 20 mM NaCl 250 µg/ml Hefe-tRNA (Sigma) 2.5x Denhardts-Lösung (Sigma) Hybridisierungslösung 3-10 ng/µl Dig-RNA 50 % deionisiertes Formamid 20 mM Tris 1 mM EDTA 330 mM NaCl 500 µg/ml Hefe-tRNA 1x Denhardts-Lösung 2.2.2.4 Whole-mount In-situ Hybridisierung Die Whole-mount In-situ Hybridisierung wurde gemäß Sasaki et. al (1995) durchgeführt, modifiziert nach Wilkinson und Nieto (1993) und Coulon und Herrmann (1993). Statt TBST diente MABT als Waschlösung. Alle Waschschritte erfolgten unter Schwenken. Embryonen jenseits des Entwicklungstags 10 befanden sich in 2ml-, kleinere in 1.5ml Eppendorf-Reaktionsgefäßen. Die Konzentration der eingesetzten DIGRNA Proben betrug - nach Abschätzung auf einem Agarose-Gel - etwa 1 µg/ml. 2.2.2.4.1 Herstellung von Acetonpulver zur Präabsorption des DIG-Antikörpers (Wilkinson und Nieto, 1993) Die Körper der bei der Präparation der Lungen getöteten Embryonen wurden in flüssigem Stickstoff schockgefroren und mit einem Mörtel zerstoßen, dabei ständig mit Stickstoff gekühlt. Das Pulver wurde in eiskaltem Aceton (techn.) zweimal 10 min unter gelegentlichem Schütteln und zwischenzeitiger Zentrifugation bei 4000g und 4°C inkubiert. Es wurde wiederum per Zentrifugation sedimentiert und das Aceton verworfen. MATERIAL UND METHODEN 29 Das Pulver wurde luftgetrocknet auf ein Stück Whatman-Papier verteilt und mit dem Mörtel nochmals weiter verfeinert. Die Lagerung erfolgte bei 4°C. 2.2.2.4.2 Protokoll der Whole-mount In-situ Hybridisierung Fixierung Embryonen/ 4% Paraformaldehyd/ PBS-- der 45 min bis 4 h, 4°C Gewebe PBST 4 x kurz Waschen, 1 h bei 4°C MeOH 2 x 5 min, Lagerung bei –20°C Bleichung 5:1 MeOH/30% H2O2 4-5 h MeOH 4 x 20 min, Lagerung bei – 20°C Rehydrierung Deproteinierung Postfixierung 75%, 50%, 25% MeOH in PBST jeweils 5 min PBST 2 x 5 min Proteinase K (25µg/ml) in PBST 3-12 min Glycin (2mg/ml) in PBST 2 x 5 min 0.2% Glutaraldehyd/4% Paraformal- 20 min dehyd in PBST PBST Prähybridisierung 3 x 5 min in 50% Formamid, 5 x SSC pH 5.0, 1 x 5 min 50 µg/ml Hefe-RNA (Sigma), 1% 1 x 1 h, 70°C SDS, 50µg/ml Heparin 1 x 5 min Hybridisierung s.o. über Nacht, 65-70°C Waschungen Sol I: 50% Formamid, 5x SSC pH 5.0, 2 x 30 min, 70°C 1% SDS 1:1 Sol I/ Sol II 10 min, 70°C Sol II: 0.5M NaCl, 10mM Tris pH 7.5, 3 x 5 min 0.1% Tween 20 (v/v) RNAse-Verdau RNAse A (100µg/ml) in SolII 2 x 30 min, 37°C Sol III: 50% Formamid, 2xSSC pH 2 x 30 min, 65°C 5.0 MABT: 100mM Maleinsäure, 150mM 3 x 10 min NaCl, 0.1% Tween 20 (v/v), pH 7.5 Blockierung unspezifischer 10% hitzeinaktiviertes (1 h, 65°C) 2-3 h Antikörperbindungsstellen Schafserum, 2% Blockierungsreagenz in MABT MATERIAL UND METHODEN 30 Reinigung der Antikörperlö- Zentrifugation bei 10000g, sung 5 min, 4°C, abdekantieren Antikörperreaktion 2% hitzeinaktiviertes Schafserum, über Nacht, 4°C 0.1% Blockierungsreagenz in MABT Waschungen MABT/ 2 mM Levamisol 3 x 5 min 6x1h NTMT 2 x 20 min Farbreaktion NBT/BCIP in NTMT 37°C im Dunkeln Stopreaktion PBST/1 mM EDTA 3 x 5 min darin bei 4°C im Dunkeln lagern 2.2.3 Methoden bei der Herstellung eines rekombinanten Baculovirus zur Expression von FGF-BP in Insektenzellen (Manual zum Bac-to-Bac Baculovirus Expressionssystem, Life Technologies) Die dabei benötigten Sf-21 Insektenzellen, die DH10Bac E.coli und die HT-Vektoren wurden freundlicherweise von der Arbeitsgruppe von Prof. Dr. Heumann, Bochum, zur Verfügung gestellt. 2.2.3.1 Selektion von transformierten DH10Bac-Klonen Bis zu diesem Arbeitsschritt sind die Methoden für DH5a und DH10Bac-Zellen gleich, bis auf die Wahl der Antibiotika. Für die Selektion wurden LB-Platten mit 50 µg/ml Kanamycin, 7 µg/ml Gentamicin, 10 µg/ml Tetracyclin, 100 µg/ml X-Gal (Stammlösung 20 mg/ml in DMSO) und 40 µg/ml IPTG angesetzt. Nachdem die transformierten DH10Bac-Zellen in die Platten eingearbeitet wurden, wurde für 24h bei 37°C inkubiert. Ein freistehender, großer und vollkommen weißer Klon wurde ausgewählt und über Nacht auf dem Warmluftschüttler in LB-Medium mit 50 µg/ml Kanamycin, 7 µg/ml Gentamicin und 10 µg/ml Tetracyclin amplifiziert. Um sicherzustellen, daß dieser Klon keine ß-Galactosidase-Aktivität mehr aufwies (weil Fremd-DNA dort integrierte), wurde etwas der amplifizierten E.coli erneut auf eine LB-Platte aufgetragen und erneut auf Blaufärbung getestet. MATERIAL UND METHODEN 31 2.2.3.2 Aufreinigung von rekombinanter Baculovirus-DNA aus DH10Bac-E.coli Da es sich bei dieser DNA um ein ca. 30 kBp großes Plasmid handelt, darf es unter keinen Umständen größeren Scherkräften ausgesetzt werden. Die E.coli wurden wie bereits in 2.2.1.2 beschrieben, abzentrifugiert und der Überstand verworfen. Das Bakteriensediment wurde vorsichtig in 0.3 ml der Lösung I (15mM Tris/HCl pH 8.0, 10 mM EDTA, 50 µg/ml RNAse A) resuspendiert. Dazu wurden 0.3 ml der Lösung II (0.2 N NaOH, 1 % SDS) gegeben, die Lösung gemischt und 5 min inkubiert. Mit der Zugabe von 0.3 ml einer 3 M Kaliumacetat-Lösung pH 5.0, wurden die Proteine gefällt. Der Ansatz wurde 10 min auf Eis gekühlt und 10 min bei 14000 g und 4°C zentrifugiert. Der Überstand wurde in ein neues Gefäß mit 0.8 ml Isopropanol überführt und 10 min auf Eis inkubiert. Die Lösung wurde 15 min bei 14000 g zentrifugiert, der Überstand verworfen und das Sediment mit kaltem Ethanol gewaschen. Es wurde wie eben geschildert nochmal zentrifugiert, der Überstand verworfen. Das Sediment trocknete kurz an der Luft und wurde schließlich in 40 µl sterilem TE aufgenommen und über Nacht lösen gelassen. 2.2.3.3 Insekten-Zellkultur Sf-21 Insektenzellen wurden in Monolayerkultur (auf Zellkulturschalen von TPP) bei 25°C in TC-100 Medium (Gibco) mit 5% FCS gehalten. Die Zellen wurden bis zu ca. 80-90% iger Konfluenz wachsen gelassen und dann 1:3 geteilt. 2.2.3.4 Herstellung von Virusüberstand Die aufgereinigte Baculovirus-DNA wurde mit dem FastGene-Reagenz von Gibco in die Sf-21 Zellen eingeschleust. 4,5 µl des Reagenz wurden in 100 µl serumfreiem TC-100 Medium gelöst, vorsichtig gemixt und 10 min stehen gelassen. Anschließend wurde der Ansatz langsam auf die sterile, in Wasser gelöste Bacmid-DNA (ca. 3 µg in 6 µl H2O) geträufelt, vorsichtig gemischt und 20 min bei RT inkubiert. Die Lösung wurde auf frisch ausgesäte, etwa 50% konfluente Sf-21 Zellen in dem Well einer TPP-6Wellschale pipettiert und nach 2 h Inkubation bei RT wurden 2 ml 5% TC-100 Medium addiert. Nach 120 h wurde der Überstand abgenommen und der Zelldebris durch Zentrifugation (10000 g, 4°C, 5 min) sedimentiert. Der gewonnene, Baculovirus enthaltende Überstand, wurde nun auf eine neue, größere Platte mit Sf-21 Zellen pipettiert und die MATERIAL UND METHODEN 32 Zellen wie oben beschrieben weiterbehandelt. Nach 120 h wurde der Überstand, jetzt mit einem ausreichend hohem Virustiter, wiederum vom Zelldebris per Zentrifugation befreit und aliquotiert bei –80°C eingefroren. 2.2.3.5 Herstellung von FGF-BP enthaltenden Überstand Zur Induktion einer Proteinexpression wurde der Virusstock 1:20 in serumfreiem TC-100 Medium verdünnt und jeweils 2ml der Verdünnung auf eine 100 mmZellkulturschale mit ca 50% konfluenten, frisch ausgesäten Sf-21 Zellen gegeben und 2 h bei RT inkubiert. Anschließend wurden 10 ml serumhaltiges TC-100 in die Schale gegeben und bei 25°C inkubiert. Nach zwei Tagen wurde das Medium gegen 4 ml serumfreies TC-100 ausgetauscht. Nach weiteren 3 1/2 Tagen Inkubation wurde der Mediumüberstand abgenommen, Zellen und Zelldebris durch Zentrifugation entfernt und der gereinigte Überstand bei –20°C gelagert. 2.2.3.6 Methoden zum Nachweis des FGF-BP im Zellüberstand 2.2.3.6.1 SDS-Polyacrylamid-Gelelektrophorese nach Laemmli (1970) Die SDS-PAGE wurde mit dem Minigel-System von Biometra nach Herstellerangaben durchgeführt. Das Sammelgel enthielt 3% und das Trenngel 12% Acrylamid. Sammelgel Trenngel 3% (w/v) Acrylamid 12% Acrylamid 125 mM Tris/HCl, pH 6.8 350 mM Tris/HCl, pH 8.8 0.1% (w/v) SDS 0.1% (w/v) SDS Die 40%ige Acrylamid:Bisacrylamid-Stammlösung im Konzentrationsverhältnis 37.5:1 stammte von Serva. Laufpuffer 2 x Probenpuffer 25 mM Tris 55 mM Tris/HCl pH 6.8 192 mM Glycin 4% (w/v) SDS 0.1% (w/v) SDS 40% (v/v) Glycerin 4.3% (v/v) ß-Mercaptoethanol 0.1% (w/v) Bromphenolblau MATERIAL UND METHODEN 33 Die Proben wurden 1:1 mit Probenpuffer versetzt, 5 min gekocht, kurz in der Tischzentrifuge zentrifugiert und auf Eis gekühlt, bis sie auf das Gel aufgetragen wurden. Um die apparente Molgröße der aufgetrennten Proteine abschätzen zu können, wurde als Marker die vorgefärbte Benchmark Prestained Protein Ladder von Gibco mit auf das Gel aufgetragen. Mit dem Blue-Power 500 Elektrophoresegerät von Serva wurde eine Spannung von 100V angelegt. Die Elektrophorese wurde beendet, kurz nachdem das Bromphenolblau des Probenpuffers aus dem Gel ausgetreten war. 2.2.3.6.2 Silbergelfärbung nach Heukeshoven und Dernick (1985) Um den Proteingehalt der Insektenzellüberstände abschätzen zu können, wurden die aufgetrennten Proteine mit Silber angefärbt. Nach der Elektrophorese wurden die Gele über Nacht in 30% (v/v) Ethanol (techn.) und 10% (v/v) Essigsäure fixiert. Anschließend wurden die Gele 1 h in 30% (v/v) Ethanol (techn.), 0.5 M Natriumacetat, 0.5% (w/v) Glutaraldehyd und 0.2% (w/v) Natriumthiosulfat in H2O inkubiert. Die Gele wurden dreimal 10 min in H2O gewaschen und danach 1 h in 0.1% Silbernitrat und 0.01% Formaldehyd inkubiert, kurz in H2O gewaschen und die Farbreaktion schließlich durch die Zugabe von 2.5% Natriumcarbonat und 0.005% Formaldehyd gestartet. Als Stoplösung diente 50 mM EDTA pH 8.0. Das fertige Gel wurde um es dauerhaft haltbar zu machen, im Ölpumpenvakuum bei 80°C auf Whatman-Papier getrocknet. 2.2.3.6.3 Western-Blot, modifiziert nach Towbin (1982) Um die Expression des FGF-BP nachzuweisen, wurde ein Western-Blot nach Herstellerangaben angefertigt. Dazu wurde das Modell 200/ 2.0 Power Supply von BioRad verwandt. Bei einer Stromstärke von 2.5 mA/cm² wurden die Proteine innerhalb von 40 min auf die Nitrocellulosemembran (Protran BA 85, Porengröße 45 µm, Schleicher&Schuell) transferiert. Vor dem Blotten wurden das Gel und die Nitrocellulosemembran getrennt 10 min in dem Transferpuffer (25 mM Tris, 192 mM Glycin, 10% (w/v) Methanol, pH 8.3) inkubiert. MATERIAL UND METHODEN 34 2.2.3.6.4 Immundetektion des FGF-BP Zur Immundetektion des mit einem His-Tag versehenen FGF-BP wurde der murine monoklonale Penta-His Antikörper von Qiagen nach Herstellerangaben verwandt. TBS: 10 mM Tris/HCl, pH 7.5, 150 mM NaCl 2 x 10 min Blockierungslösung: 1 % (w/v) Casein (Merck) in TBS, pH 7.5 2h TBST: 20 mM Tris/HCl, pH 7.5, 500 mM NaCl, 2 x 10 min 0.05 % Tween20 (Sigma), 0.2 % Triton X-100 (Sigma) anti-Penta-His, 0.15µg/ml in Blockierungslösung über Nacht bei 4°C TBST 2 x 10 min TBS 10 min anti-Maus Peroxidase-gekoppelter Zweitantikörper aus Schaf 2h (Amersham), 1:4000 in Blockierungslösung TBST 4 x 10 min ECL-Reagenz (Amersham) 1 min Abschließend wurde das Fluoreszierungssignal mit einem Hyperfilm ECL (Amersham) aufgenommen und der Film entwickelt. 2.2.4 Lungenorgankultur Die Kultur von embryonalen Mauslungen basierte auf der Methode von Nogawa und Ito (1995). Embryonen der Entwicklungstage 11 bis 12 wurden auf Eis gekühlt, die Lungen in kaltem HBSS-Puffer (Hanks´Balanced Salt Solution, Gibco) mit feinen Pinzetten (Dumont No5) unter dem Lichtmikroskop (Leica Wild M10) herauspräpariert und jeweils eine bis zwei pro Eppendorfgefäß auf Eis in HBSS gesammelt. Das HBSS wurde so gründlich wie möglich abgenommen und die Lungen in 200 µl eiskaltem Matrigelansatz in einen Millicell-CM Zellkultureinsatz (12 mm Durchmesser, Porengröße 4 µm, Millipore) überführt. Das Matrigel wurde 30 min bei 5% CO2 und 37°C im Brutschrank inkubiert, bis es fest war. Anschließend wurden 200 µl des vorgewärmten Mediums auf das Matrigel gegeben und bei 5% CO2 und 37°C inkubiert. Matrigel ist ein Extrakt von extrazellulären Matrixproteinen, wie Laminin, Collagen und HSPGs, der aus einem Maustumor gewonnen wird. Das von Beckton-Dickinson vertriebenene Wachstumsfaktor-reduzierte Matrigel enthält dennoch nach Herstellerangaben noch Faktoren, v.a. noch TGF-ß mit einer Konzentration von 1.7 ng/ml. Am Tag vor der Präparation wurde MATERIAL UND METHODEN 35 das bei –20°C gelagerte Matrigel über Nacht auf Eis langsam aufgetaut. 100 µl des reinen Matrigels wurden mit 100 µl einer 3:2 Mischung von DMEM-Medium mit 0.2% FCS und dem in 2.2.3.5 beschriebenen FGF-BP enthaltenden Überstand der Sf21-Insektenzellen vermischt. Da dieser Überstand einen pH von ca. 6.2 aufweist, wurde die Mischung mit Spuren von 1 M NaOH versetzt, bis das Phenolrot des DMEMs wieder einen physiologischen pH-Wert durch das farbliche Umschlagen nach rot anzeigte. Das Medium bestand entsprechend aus einer 4:1 Mischung von DMEM/0.1% FCS mit dem Insektenzellüberstand. Eine Versuchsreihe mit den Lungen eines Wurfs bestand aus vier Ansätzen: mit Überstand von FGF-BP mit oder ohne Insektensignalpeptid produzierenden Insektenzellen mit oder ohne Wachstumsfaktor. Die Konzentration des FGF-10 im fertigen Gel betrug 50 ng/ml, die des FGF-1 500 ng/ml. Beide Proteine , jeweils die humanen Formen, wurden von PeproTech bezogen und mit PBS-- auf Arbeitskonzentrationen verdünnt. Im Verlauf der Inkubation wurde die Veränderung der äußeren Morphologie der Lungen durch die Anfertigung von Diaserien lichtmikroskopisch dokumentiert (Kamera: Nikon F-601 M, Film: Kodak Epy 64T). Nach 90 h wurden die Lungen mitsamt Microcell-Inlet in eiskaltem HBSS 3 h inkubiert, bis sich das Matrigel soweit verflüssigt hatte, daß die Lungen entnommen und nach 1 h fixiert und paraffiniert werden konnten. Von den Lungen wurden 5 µm dicke Schnitte angefertigt, die wie in 2.2.5 beschrieben weiterbehandelt wurden. 2.2.5 Hämatoxylin-Färbung der Lungenschnitte Nach der abschließenden Rehydrierung wurden die Schnitte in Hämatoxylin-Lösung nach Gill (Sigma) 10 min inkubiert und mit Leitungswasser gespült, bis sie gebläut waren. Abschließend wurden die Schnitte unter Kaiser´s Glyceringelatine eingedeckelt. ERGEBNISSE 36 3 Ergebnisse Ziel dieser Arbeit war es, die Expression zweier FGF-bindender Proteine, des sekretierten FGF-Bindungsproteins (FGF-BP) und des nukleolären Bindungsproteins (NoBP), während der Embryonalentwicklung auf ihre zeitliche und gewebespezifische Lokalisation hin zu untersuchen. Ein spezielles Augenmerk sollte dabei auf die frühe Lungenentwicklung gelegt werden, weil verschiedene FGF-Wachstumsfaktoren dort in einer dynamischen Weise expremiert werden und entscheidend zur Regulation des Lungenwachstums beitragen. Dazu wurden In-situ Hybridisierungen mit digoxigenierten RNAs an Paraffinschnitten von Mäuseembryonen zwischen dem Entwicklungstag 13 und 18 und Whole-mount Hybridisierungen mit Embryonen und Lungen ab dem Entwicklungstag 7 bzw. 10 durchgeführt. Um bessere Aussagen über die Co-Expression von NoBP und FGF-BP und den FGFs machen zu können, wurden zusätzlich Hybridisierungen mit FGF10 und FGF18 antisense RNA vorgenommen. Da bereits Daten über die Verteilung von FGF10 und FGF18 in embryonalen Mäusen veröffentlicht wurden, konnten die Ergebnisse dieser Hybridisierungen zur Beurteilung der Selektiviät der gewählten Hybridisierungsmethode herangezogen werden. Von FGF10 und FGF18 ist bekannt, daß sie in der embryonalen Lunge expremiert werden. Neben dem Nachweis der Proteinexpression wurde damit begonnen, in der Lungenorgankultur den Einfluß des FGF-BP auf die FGF-vermittelte Proliferation von embryonalen Lungengewebe zu untersuchen. In-situ Hybridisierung Das Problem der Spezifität Ein Hauptproblem der In-situ Hybridisierung besteht darin, falsch negative Ergebnisse zu erkennen und die Spezifität der Signale zu beurteilen. Daher wurden bei jedem Insitu Experiment mit Digoxigenin markierten sense RNAs Negativkontrollen durchgeführt, in der Regel eine auf zwei bis fünf antisense RNA-Hybridisierungen. Einige Mock-Versuche, d.h. eine In-situ Hybridisierung ganz ohne RNA-Sonde, zeigten, daß der benutzte Digoxigenin-Antikörper unter den gegebenen Versuchsbedingungen keinen Hintergrund auslöst, also nicht unspezifisch bindet. Allerdings führten alle senseRNA Sonden zu einer teilweise vernachlässigbar schwachen Hintergrundfärbung, teilweise zu einer, gegenüber den antisense-RNA Sonden zwar klar schwächeren, aber deutlichen Färbung der Schnitte. Dies wurde v.a. bei FGF18 und FGF-BP beobachtet. ERGEBNISSE 37 Es ist bekannt und allgemein akzeptiert (Wilkinson und Nieto, 1993), daß sense-RNA Sonden zu Signalen führen können, dennoch zählt die Reduzierung dieser – vermutlich unspezifischen – Färbung zu den wichtigsten Aufgaben bei der Optimierung eines Insitu Protokolls. Im Wesentlichen können die Hybridisierungsbedingungen spezifischer gemacht werden, indem die Hybridisierungstemperatur und/oder der Anteil der Formamids im Hybridisierungspuffer angehoben wird. Auch die Reduzierung der Hybridisierungsdauer auf vier bis sechs Stunden hat sich in dieser Arbeit als nützlich erwiesen. Die Einführung eines RNAse-Verdaus nach der Hybridisierung, um unvollständig bindende RNA in kleine Stücke zu schneiden und anschließend abwaschen zu können, erwies sich allerdings als weitestgehend ungeeignet, um spezifischere Ergebnisse zu erzielen. Das Problem der nicht bekannten Spezifität der benutzten RNA-Sonden konnte nicht vollständig gelöst werden, daher soll zu jedem Ergebnis repräsentative Kontrollschnitte gezeigt werden. Als problematisch erwies sich auch, daß die benutzen antisense-Proben der FGFs und des FGF-BP immer recht ähnliche Signalmuster hervorriefen. Allerdings unterschieden sich FGF-NoBP- und shh-Sonden deutlich hiervon. Ein Hybridisierungssignal wurde als spezifisch gewertet, wenn - die Zellkerne nicht oder nur schwach gefärbt waren, d.h. die hoch konzentrierten Kern-RNAs nicht an die Sonde banden - die dunkelbraun/violett/schwarze Färbung des NBT/BCIP-Präzipitats ausschließlich im Zytosol gefunden wurde - ungefärbt gebliebene Zellen und Gewebe sich in der direkten Nachbarschaft des gefärbten Gewebes befanden. Die Konzentration der sense-RNA wurde in der Regel noch etwas höher gewählt als die der korrespondierenden antisense-RNA, der Positivprobe. Die Konzentrationsbestimmung der Dig-RNAs erfolgte mit einer schnellen Agarosegelelektrophorese, gleichzeitig kann man durch das Anfärben der Nukleinsäuren mit EtBr überprüfen, ob eventuelle Verunreinigungen mit kurzer, unvollständig synthetisierter RNA oder der TemplateDNA vorliegen. In Vorversuchen wurde festgestellt, daß diese Abschätzung der Konzentration der RNA recht zuverlässige Werte liefert. Dazu wurden Dot-Blots mit Verdünnungsreihen markierter RNA durchgeführt, und die relative Konzentration der DigMarkierung durch den Vergleich mit einer definiert markierten DNA (Boehringer Mannheim) bestimmt. Nachdem sich mehrfach in unabhängigen Experimenten bestätigt hatte, daß die Konzentration der Sonde mit der Konzentration der Markierung gut übereinstimmte, daß also der Anteil des Dig-UTP gegenüber dem nicht-markierten UTP ERGEBNISSE 38 konstant bleibt, wurde die Qualität der Dig-Markierung in den RNA-Sonden nur noch stichprobenartig per Dot-Blot untersucht. Bei der Whole-mount In-situ-Hybridisierung wurden auch sense-RNAs als Negativkontrollen eingesetzt. Zusätzlich wurden Hybridisierungen mit egr2 antisense-RNA (die egr2 DNA war eine freundliche Gabe aus dem Labor von Prof. Dr. D. Wilkinson, London) durchgeführt. Egr2 (early growth response, früher auch krox-20) ist ein Zinkfingerprotein und ein bekannter Marker der Hindbrain-Region, die Expression ist stark und sehr spezifisch (Wilkinson et al., 1989a). Als weitere Kontroll-Sonde wurde zum einen FGF18 antisense-RNA benutzt, dessen Expression in Mäuseembryonen 1998 von Maruoka et. al bereits mittels Whole-mount In-situ-Hybridisierung untersucht worden war. Zur Überprüfung der Experimente mit den Lungen wurden Proben von FGF10 (Bellusci et al., 1997b) und Shh (Bellusci et al., 1996) benutzt, die in spezifischen Regionen der embryonalen Lungen expremiert werden. Die Auswertung der gefärbten Gewebeschnitte und der Embryonen erfolgte mit der Hilfe des Atlas of Mouse Development von M. H. Kaufman (2. Auflage der revidierten Ausgabe von 1995, Academic Press, London 1998) und der Cytologie, Histologie und mikroskopischen Anatomie des Menschen von O. Bucher und H .Wartenberg (Nachdruck der 11., vollständig überarbeiteten Ausgabe von 1989, Verlag Hans Huber, Bern 1991). Um dem interessierten Leser die Orientierung in den Gewebeschnitten zu erleichtern, ist dem Anhang ein illustrierter Sagittalschnitt beigefügt. 3.1 Die Expression von FGF-BP, NoBP, FGF18 und FGF10 in verschiedenen Stadien der Mausembryogenese 3.1.1 In-situ Hybridisierungen in Gewebeschnitten im Zeitraum E 13.5 bis E 18.0 Entwicklungstag 13.5 Wie bereits erwähnt, ähnelten sich die Hybridisierungssignale der untersuchten FGFs und des FGF-BP. Am prominentesten fiel stets die Färbung der sich entwickelnden Knochen aus. Die proliferierenden Chondroplasten um die Knorpelmasse der Wirbel herum waren stets gefärbt. Die inneren Organe Herz, Leber, Darm und Lunge blieben zu diesem Zeitpunkt im wesentlichen ungefärbt. Auffallend war die – auch bei Schnitten von älteren Embryonen beobachtete - Färbung vieler mesenchymaler Gewebe, wogegen epidermale Zellen, z.B. die Epidermis im Nasen/Rachenraum, ungefärbt blieben. ERGEBNISSE 39 Das Rückenmark und andere neuronale Zellen waren negativ, die Zellen unter der äußeren Hautepidermis dagegen positiv. Abb. 1 A: Schräger Sagittalschnitt durch ein E 13 Embryo. Der Pfeil weist auf den Ausschnitt, der in B vergrößert dargestellt ist. Caudal sind die Anlagen der Wirbel gut zu erkennen. Herz und Leber in der Bauchhöhle sind ungefärbt. Hybridisiert mit antisense FGF-BP Dig-RNA. B: Der Pfeil unten links zeigt auf das Epithel einer Arterie, vermutlich der Aorta carotis. Oberhalb davon schließt sich die Cochlea an (Gehörschnecke), umgeben von einer Knochenanlage. Es folgen eine weitere Arterie und mesenchymales Gewebe. Der zweite Pfeil weist auf die Epidermis des Oesophagus (Luftröhre). C: Gezeigt sind Wirbel, hybridisiert mit antisense FGF10-Sonde. Die Zone mit höher differentierten Chondroplasten ist von weniger fortgeschrittenen Zellen umkränzt. Rechts unten ist ein Teil der Lunge zu sehen. D: Eine Hybridisierung mit antisense FGF1-RNA. Gekennzeichnet ist das gefärbte Gewebe zwischen den Somiten. Rechts unten sieht man einen Wirbel. Alle drei Schnitte sind nicht mehr als 50 µm voneinander entfernt. Entwicklungstag 16 FGF10: Die Ergebnisse der FGF10 in-situ Hybridisierung ähnelte der bei FGF-BP. Allerdings fiel die Färbung der Haut und der Knochen deutlich stärker aus, während die sonst so auffällig gefärbten Ganglien nur schwach positiv waren. Auch andere neuronale Zellen waren, wenn überhaupt, nur ganz schwach positiv. Das Epithel im vorderen Nasenraum war, zumindest teilweise, relativ stark gefärbt. In der Lunge konzentrierte sich die Färbung auf das Mesenchym. Anders als bei den anderen Sonden fiel die Hybridisierung in der Leber recht kräftig aus und war stärker als in der Lunge. ERGEBNISSE Abb. 2 40 A: Sagittalschnitt durch ein E 16 Embryo, hybridisiert mit antisense FGF10 RNA. Bei der Hybridisierung wurde auf eine Acetylierung (siehe ) verzichtet. Als positiv detektiert wurden v.a. Haut und Knochen. Mesenchymale Zellen wurden im Allgemeinen stärker angefärbt als epitheliales Gewebe. Die Pfeile deuten auf die gezeigten Ausschnitte B-D. B: Das Epithel im Eintritt zur Nasenhöhle ist nur direkt angrenzend an das Mesenchym wirklich negativ. C: Die FGF10 mRNA wurde ganz bevorzugt im Mesenchym der Lunge gefunden. D: Dieser Ausschnitt verdeutlich das starke Farbsignal in der Haut. V.a. die ektodermale Zellschicht ist FGF10 positiv. Das im Vergleich zu den anderen Abbildungen fadenförmige Aussehen des Farbniederschlags erklärt sich aus dem Verzicht auf eine Acetylierung (siehe 2.2.2.3). FGF18: Der gezeigte Längsschnitt durch ein E16-Embryo ist recht stark gefärbt, andere In-situ Experimente ergaben aber ein ganz ähnliches Signalmuster. Am prominentesten sticht die Färbung des Trigeminalganglions und des Thymus heraus, die während der Entwicklung der Farbreaktion sehr früh zu sehen waren. Weiterhin fällt die Färbung der neuronalen Zellen im Rückenmark auf, die nur bei Hybridisierungen mit FGF18 antisense-RNA stark ausfiel. Das Nasenepithel blieb wiederum vollständig negativ, wäh- ERGEBNISSE 41 rend die sich entwickelnden Knochen stark gefärbt waren. Die Haut war ebenfalls deutlich positiv, in ihrer Gänze. In der Lunge war das Mesenchym deutlich stärker gefärbt als das Epithel. Insgesamt sind sich die Hybridisierungsmuster der beiden Proben von FGF18 und FGF-BP relativ ähnlich. Abb.3 A1: Sagittalschnitt eines E16 Embryos, als Sonde diente antisense FGF18-RNA. Folgende Gewebe wurden mit abnehmender Intensität bzw. Geschwindigkeit gefärbt: Trigeminalganglion, Thymus, Knochen/Knorpel, Epithel der Blutgefäße, Lunge, Epithel des Dünndarms, Haut, der frühe Neocortex, Penis, Rückenmark. Keine und nur wenig FGF18 Transkripte wurden in Herz, Leber , Dickdarm, dem caudalen Abschnitt des Rückenmarks und weiten Teilen des Gehirns detektiert. Die Pfeile zeigen auf die Ausschnitte in A-D. A: Links außen die Haut, darunter Bindegewebe und das Rückenmark. Speziell das äußere Endothel der Haut ist intensiv gefärbt. B: In der Mitte die Nasenhöhle, ausgekleidet mit epithelialen Zellen. Etwas rostral davon befindet sich ein Drüsengang (Pfeil). Zwischen dem umgebenen Mesenchym und dem Nasenepithel wurde eine FGF18 positive Zellschicht detektiert (Pfeil). Am linken Rand der Abbildung zeigen sich Teile der Gesichts-/Schädelknochen. C: Ein Ausschnitt der Lunge aus einem anderen FGF18 Schnitt (ohne Acetylierung, siehe 2.2.2.3.1). Das Epithel um die Bronchioen (Pfeil) enthält offenbar weniger FGF18 Transkripte als die mesenchymalen Zellen. D: In der oberen Hälfte sind zwei Schlingen des Dünndarms zu sehen, darunter ein Zeh. Das den Dünndarm umkleidende Endoderm wurde nicht angefärbt (Pfeil). ERGEBNISSE 42 FGF-BP: Abbildung 4-A zeigt einen Längsschnitt durch ein Embryo am Entwicklungstag 16. Die prominenteste Färbung findet sich in dem Thymus, dem Trigeminalganglion und in der inneren Zellschicht des Darms. Die Lunge und die neuronalen Zellen in den DRGs (dorsal root ganglia) sind ebenfalls klar FGF-BP positiv. Weiterhin positive Zellen befanden sich z.B. in den unteren Schichten der Haut, in den Knochenanlagen, in den frühen Muskeln und in der Wand der frühen Gallenblase. Mittelstark gefärbt erscheinen neuronalen Zellen in den zu diesem Zeitpunkt proliferierenden Abschnitten des Großhirns, im Midbrain (direkt über der Anlage der Cerebellums) und im Striatum und den proliferierenden neuronalen Zellschichten darüber, die später den Neocortex ausbilden werden. Interessant ist die Abb, die das Epithel im Innern des Nasenrachenraumes zeigt. Die Epithelzellen selber waren negativ, einige Zellen unterhalb der obersten Zellschicht jedoch positiv. Die Lunge war im Bereich des Mesenchyms deutlich stärker gefärbt als in den epidermalen Zellen, die die Tubuli ausbilden und als kreisförmige Gebilde zu erkennen sind. Epitheliale Zellen, die Blutgefäße auskleiden, gehören zu den klar positiven Zellen. ERGEBNISSE Abb. 4 43 A: Sagittalschnitt durch ein E 16 Embryo, hybridisiert mit antisense FGF-BP RNA. Drei der stärksten Signale entwickelten (1) das Trigeminalganglion, (2) der Thymus und (3) die DRGs. Die Pfeile deuten die vergrößerten Ausschnitte an, die in C-F gezeigt sind. Folgende Gewebe wurden als FGF-BP positiv detektiert, in der Reihenfolge der Signalstärke: Trigeminalganglion, Thymus, DRGs, Lunge, Epithel des Darms, proliferierende Knochenzellen, neuronale Zellen des Striatums, Neocortex und Midbrains, Penis, Gefäßepithel, Blase, Muskel und Haut. B: Dies ist der angrenzende Schnitt zu A, hybridisiert mit sense FGF-BP RNA. Die höchste Hintergrundfärbung findet sich in der Leber. C: Ein schon recht weit entwickelter Knochen an der Schädelbasis. Die proliferierenden Zellen im Perichondrium sind gefärbt (Pfeil). Im Muskel darunter sind einige Zellen ebenfalls positiv (Pfeil). D: Im Mesenchym der Lunge wurde mehr FGF-BP Transkript detektiert als im Epithel um die Aerosolen (Pfeil). E: Das Epithel des Darms ist an der Basis etwas stärker gefärbt als in den frühen Zotten (jeweils durch Pfeile gekennzeichnet). F: Einige Zellen in der Haut wurden als stark FGF-BP positiv detektiert. Insgesamt fiel das Signal der Haut relativ schwächer aus als bei FGF10 und FGF18. ERGEBNISSE 44 NoBP: Die Sonde des NoBP ergab bei den in-situ Experimenten in den Schnitten leider immer nur schwache Signale, häufig verbunden mit einer recht hohen, scheinbar unspezifischen Färbung der Zellen und teilweise auch der Zellkerne. Interessanterweise traten weniger Probleme dieser Art, etwa ein hoher Hintergrund, bei den whole-mount Experimenten auf, siehe Abb. 9. Am stärksten gefärbt wurden epitheliale Zellen der Blutgefäße und des Dünndarms, mesenchymales Gewebe in der Lunge, in der Zunge, im Kiefer und im Kopfbereich, sowie wie bei den anderen Sonden auch, proliferierende Chondroplasten. Neuronale Zellen blieben negativ. Abb. 5 A: Sagittalschnitt durch eine E 16 Lunge, hybridisiert mit antisense NoBP-RNA. V.a. mesenchymale Zellen sind im Cytosol gefärbt. Das Epithel zeigt eine hohe Hintergrundfärbung. B: Ein zu A direkt benachbarter Schnitt der Lunge, hybridisiert mit sense NoBP-RNA C: Längsschnitt entlang eines Abschnittes des Dünndarms, hybridisiert mit antisense NoBPRNA, ebenso wie D und E. Der Pfeil weist auf positive Zellen des Darmepithels. D: Das Epithel einer großen Ader ist NoBP-positiv. E: Knorpeliges Gewebe zwischen zwei Wirbeln wurde stark angefärbt. ERGEBNISSE 45 Entwicklungstag 18 FGF 18: Die detektierte Expression von FGF18 am Entwicklungstag 18 entsprach ziemlich genau der am Tag 16. Zwischen Tag 16 und 18 differenziert u.a die Haut weiter, und die Expression von FGF18 konzentrierte sich jetzt auf die oberste Zellschicht, war aber auch in den Haarwurzeln zu sehen. Lunge und Darm waren weiterhin die am stärksten gefärbten inneren Organe. Die Färbung der Lunge war im Mesenchym weiter etwas intensiver als im Epithel. Im Darm waren wiederum die – jetzt fast ausdifferenzierten – inneren epithelialen Zellen am prominentesten gefärbt. Die Expression scheint in den neuronalen Zellen des Großhirns wie des Rückenmarks etwas weniger stark zu sein als zwei Entwicklungstage zuvor. Abb. 6-F verdeutlicht eine interessante Differenzierung innerhalb des Rückenmarks hinsichtlich der FGF18-Expression. Die Negativprobe mit sense FGF18-Dig-RNA rief allerdings im Parallelversuch v.a. in Darm und Lunge ebenfalls eine deutliche Färbung hervor. ERGEBNISSE Abb. 6 46 A: Aus einem Sagittalschnitt eines E 18 Kopfes, hybridisiert mit antisense FGF18-RNA. Gezeigt ist ein Abschnitt des Neocortex. B: Der zu A direkt benachbarte Schnitt, hybridisiert mit sense FGF18-RNA. C-G: Ausschnitte eines Sagittalschnittes eines E 18 Torsos, hybrisisiert mit antisense FGF18Sonde C: Speziell die äußerste epidermale Schicht der Haut ist intensiv gefärbt. Weiterhin ist eine prominente Färbung in der Basis der Haarwurzel zu sehen (Pfeil). D: Die Lunge war das am intensivsten gefärbte Organ. Das Mesenchym scheint noch etwas mehr FGF18 Transkripte zu enthalten als das Epithel (siehe den linken Saum des Flügels). E: Gefärbte Zellen in den Darmzotten F: Ein Abschnitt aus dem Rückenmark. Bei den intensiv gefärbten Zellen könnte es sich um Ependymzellen, epitheliale Neuroglia, handeln. G: Proliferierende Knochen-Stammzellen (Pfeil) expremieren FGF18, die ausdifferenzierten Osteoblasten links und rechts sind FGF18- negativ. FGF-BP: Hier war die Intensität der Färbung allgemein eher geringer als zum Zeitpunkt E16 und konzentrierte sich auf einige wenige Gewebe. In der Lunge scheinen weniger Zellen, dafür aber relativ stärker, FGF18 zu expressionieren. Diese Zellen finden sich v.a. im Mesenchym. Daneben waren die Haut, das Darmepithel und ein DRG die einzigen klar positiven Gewebe in den untersuchten Schnitten. Allerdings trat analog zu FGF18 das ERGEBNISSE 47 Problem der `positiven` Negativprobe mit FGF-BP - auf, d.h. auch hier waren, wenn auch schwächer, die Haut und der Darm gefärbt; am deutlichsten war der Unterschied der Färbung aber bei der Lunge. Abb. 7 Aus einem Sagittalschnitt durch den Torso eines E 18 Embryos A, C, E und F sind mit antisense FGF-BP –RNA hybridisiert, B und D mit der entsprechenden sense RNA A: Die Hautepidermis ist relativ deutlich stärker gefärbt als bei FGF18 (Abb. 6A). Die Haarwurzeln sind nur schwach NoBP-positiv. B: Ein zu A entsprechender Hautabschnitt bei etwas geringerer Vergrößerung. Die FGF-BP sense-RNA hybridisiert ebenfalls in der Epidermis. C und D: Der mesenchymale Saum der Lungenflügel (Pfeil) ist in C FGF-BP –positiv, innerhalb des Flügels fällt die Färbung weniger stark aus. Die Kontrolle in D bleibt weitesgehend negativ. E: Von den inneren Organen enthielt nur der Darm bzw. das Darmepithel detektierbare Mengen an FGF-BP mRNA. F: Die stärkste FGF-BP Expression wurde neben der Haut in den DRGs, caudalen peripheren Ganglien, detektiert. NoBP: Es konnten keinen eindeutigen Signale mit der NoBP-antisense-RNA detektiert werden. Das Mesenchym der Lunge schien aber etwas positiv zu sein. ERGEBNISSE 48 3.1.2 Whole-mount In-situ Hybridisierung mit Embryonen im Zeitraum E 7.0 bis E10.5 Bei der Whole-mount Hybridisierung, bei der keine Gewebeschnitte, sondern ganze Organe und Embryonen mit den Dig-RNA Sonden inkubiert werden, ist es oft besser möglich, den Expressionsort eines Genes zu bestimmen. Allerdings darf z.B. ein Embryo nicht zu groß sein. Die größten Mäuseembryonen, die häufig zur noch zum Wholemount Hybridisierung benutzt werden, stammen in der Regel vom Entwicklungstag 10.5, maximal bis E 11.5. Bei noch größeren Embryonen kann man nicht mehr davon ausgehen, daß die RNA-Sonde und/oder der Antikörper gut genug auch an die inneren Körperpartien, speziell im Kopf, herankommt. Ab dem Entwicklungstag 10 wurden daher den Embryonen während der Präparation der Kopf leicht eröffnet, um eine bessere Durchlässigkeit zu den Gehirnregionen zu gewährleisten. Es traten deutlich weniger Probleme mit der unspezifischen Färbung durch sense-Dig-RNA auf als in den Gewebeschnitten. Mit der egr2-RNA stand zusätzlich eine sehr gute Kontroll-Dig-RNA zur Verfügung, bei der ausschließlich zwei Segmente im Hindbrain gefärbt sein sollten, die Rhombomere 3 und 5 (Nieto et al., 1991). Desweiteren wurden Kontrollen mit shh- und FGF18-Sonden durchgeführt. Hybridisierungsexperimente mit FGF-BP- und NoBPDig-RNA wurden mindestens zweimal mit möglichst ähnlich weit entwickelten Embryonen wiederholt. Allerdings muß betont werden, daß die Expression eines Proteins während der frühen Embryogenese sehr dynamisch verlaufen kann und nie auszuschließen ist, daß eine kurze, transiente Expression in einem Gewebe übersehen wird. Das Alter der untersuchten Embryonen lag zwischen E 7.0 und E 10.5. Dabei konnte mit den benutzen RNA-Sonden von FGF-BP, NoBP und FGF10 keine Expression bis zum Zeitpunkt 8.0 detektiert werden (Daten nicht gezeigt). Die Entwicklungsstufe eines Embryos bis zu E 9.5 läßt sich recht gut an der Zahl der Somiten abschätzen, deren Genese ab E 7.5 bis 7.75 beginnt und etwa 100-120 Minuten pro Somitenpaar benötigt. Die Zahl der Somiten liefert in den meisten Fällen zwar ein gutes Maß für die Entwicklung eines Embryos, aber nicht immer, denn die Genese der Organe und der Gewebe läuft nicht unbedingt synchron. Das bedeutet, daß Embryonen mit der gleichen Anzahl an Somiten sich z.B. im Fortschritt der Herzentwicklung morphologisch deutlich unterscheiden können. Positivkontrollen mit egr2- und FGF18-Sonden (Embryonen) Bei jeder whole-mount Hybridisierung wurde immer auch mindestens ein Embryo mit egr2- bzw. FGF18-Dig-RNA inkubiert, um die Selektivität der Färbesignale einschätzen ERGEBNISSE 49 zu können. Die Ergebnisse der Hybridisierungsexperimente von Nieto et. al im Fall des egr2 und von Maruoka et. al für FGF18 konnten nachvollzogen werden. Egr2-RNA wurde immer nur im Hindbrain detektiert, zum Zeipunkt 8.0 in den Rhombomeren 3 und 5, siehe Abb. 9-B. FGF18 wird in der Übergangsregion zwischen dem Midbrain und dem Hindbrain sowie in den zuletzt generierten Somiten und dem sich direkt anschließenden undifferenzierten Schwanzgewebe expremiert, siehe Abb. 8-B. Positivkontrollen mit FGF10- und Shh-Dig-RNA-Sonden (Lungen) Die Expression von FGF10 und Shh während der frühen Lungenentwicklung ist bereits gut untersucht (siehe Einleitung), daher eignen sich diese RNAs gut für eine Kontrolle der Ergebnisse der Hybridisierungsexperimente. Die Expression von FGF10 verläuft dabei sehr dynamisch. Ähnlich wie bei dem NoBP findet man die Transkripte in dem Mesenchym vor der Wachstumszone des Epithels, so wie in Abb. 12-A dargestellt. Shh dagegen wird im Epithel expremiert, siehe Abb. 8-A. Um zu überprüfen, ob FGF18 auch während der frühen Lungenentwicklung dort expremiert wird, wurden Lungen bis zum Entwicklungstag 12.0 mit antisense FGF18-RNA hybridisiert. Es konnte aber kein lokal definierbares Signal detektiert werden, lediglich eine gewisse Grundfärbung. Abb. 8 A: E 12.5 Lunge , hybridisiert mit antisense Shh-RNA. Das Shh wird v.a. in den distalen Enden der Tubuli expremiert. B: ein Embryo zum Zeitpunkt 10.0, hybridisiert mit antisense FGF18-RNA. Das FGF18 findet sich an der Grenze zwischen Hindbrain und Midbrain (Pfeil), dem Forebrain, in den jüngsten Somiten und dem angrenzenden Gewebe im distalen Schwanz. ERGEBNISSE 50 NoBP: Zum Zeitpunkt E 8.25-8.5 (Embryonen mit etwa 8-14 Somitenpaaren) wurde eine starke NoBP-Expression in frühen Anlagen des Hindbrains, des Forebrains und in der Neuralleiste detektiert. Die Begriffe Fore-, Mid- und Hindbrain (d.h. vorderes, mittleres und hinteres Gehirn) basieren auf anatomischen Kriterien, beschreiben also zunächst nur die Lage der Zentren der neuronalen Proliferation in der Embryonalentwicklung. Im Laufe des Entwicklungstag 8 teilt sich das Hindbrain in sieben Segmente, die Rhombomere, auf (Wilkinson, 1993), zwischen denen Furchen verlaufen (siehe Abb. 9-C). Der Vergleich der segmentierten Expression des egr2 und des NoBP im Hindbrain in Abb. 9-A und 9-B verdeutlicht, daß NoBP-RNA in diesem Embryo in den Segmenten 1, 4 und 6 detektiert wurde. Die Zellen der Neuralleiste sind besonders für die Bildung des peripheren Nervensystems wichtig (LeDouarin und Smith, 1988). Die Somiten waren kaum, die frühen Anlagen von Darm und Herz gar nicht und das undifferenzierte Gewebe im Schwanzbereich etwas gefärbt. Etwas später, um den Entwicklungstag 9.5 herum (Embryonen mit etwa 20-25 Somitenpaaren), haben sich der erste und der zweite Kiemenbogen deutlich ausgebildet. Weiterhin erkennt man dorsal zu den Kiemenbögen die kreisförmige Anlage des Innenohres, den otischen Vesikel. Die Zellmasse der Seitenleiste neben den Somiten hat deutlich zugenommen, und die erste Andeutung der vorderen Extremität (forelimb) ist zu erkennen. Zu diesem Zeitpunkt lieferte der erste Kiemenbogen (frühe Anlage des Kieferbereichs) das prominenteste Hybridisierungssignal mit der NoBP antisense-RNA. Das stärkste Hybridisierungssignal in der Hirnanlage fand sich im Forebrain, weniger stark im Midbrain und nur schwach im Hindbrain. Der zweite Kiemenbogen, in den jetzt Zellen aus der Neuralleiste migrieren, die später u.a. den Facialisnerven ausbilden, war deutlich schwächer gefärbt. Im Bereich des Schwanzextremität war, weniger stark, das Schwanzende und der ventrale Bereich gefärbt. Die inneren Organe wie der Darm und das Herz waren negativ. Etwas später, wenn das Embryo ca. 25 Somiten aufweist und die vordere Extremität als Verdickung der Seitenleiste gut zu erkennen ist, wird diese, zusätzlich zu den eben beschriebenen Geweben, vollständig angefärbt. Die apical ectodermal ridge, die ektodermale Zellschicht über dem Mesenchym an der Spitze der Extremität (siehe Einleitung), scheint eher weniger NoBP zu expremieren; die Zone der stärksten Hybridisierung lag zu diesem Zeitpunkt an dem Ansatz der Extremität, nicht an der Spitze. Abb. 9-F zeigt die hintere Extremität eines E 10.25-10.5 Embryos, die spezifisch in der der ZPA (zone ERGEBNISSE 51 of polarizing activity) gegenüber liegenden Zone gefärbt ist. Ab diesem Entwicklungsstadium wurde auch die Zellwand des otischen Vesikels, der Anlage des Innenohres, etwas stärker gefärbt. Am Tag E 10.5 war das detektierte Hybridisierungssignal in den drei Gehirnabschnitten in Hindbrain und Midbrain fast verschwunden; im Forebrain waren Zellen aus der optical placode, die u.a. an der Bildung der endokrinen Gewebe des Gehirns beteiligt sind (Tarazzo et al., 1995), am kräftigsten gefärbt. Die lateral-rostrale Zone des Schwanzes blieb positiv, ebenso die vorderen wie die hinteren Extremitäten. Die inneren Organe zeigten wiederum keine Hybridisierungssignale. Zusammenfassend läßt sich also sagen, daß NoBP-RNA von E 8.0 bis E 10.5 vor allem in der Neuralleiste und dem frühen Gehirn, dort in erster Linie im Hindbrain, und ganz besonders stark in dem ersten Kiemenbogen detektiert wurde. Während sich das Signal im Gehirn von älteren Embryonen abschwächte, nahm es im Schwanz und in den entstehenden Extremitäten, speziell auf der rostralen Seite gegenüber der ZPA, zu. ERGEBNISSE Abb. 9 52 A und C-F sind mit antisense NoBP-RNA hybridisiert, B mit antisense egr2-RNA A: Embryo zum Zeitpunkt E 8.0-8.25, mit 10 Somiten. Die Position der gefärbten Hindbrainsegmente, der Rhombomere 1, 4 und 6 ist gekennzeichnet. Die Neuralleiste ist als dunkle Linie zwischen den Rhombomeren zu erkennen. Im Bereich des Forebrains wurde ebenfalls Gewebe angefärbt. B: Embryo zum Zeitpunkt 8.0-8.25, mit 12 Somiten. Die Rhombomere 3 und 5 sind egr2-positiv. C: Embryo zum Zeitpunkt E 8.0, mit 8 Somiten. Die Aufnahme der dorsalen Kopfpartie verdeutlicht die Segmentierung des Hindbrains. D: Embryo zum Zeitpunkt E 9.5, mit 24 Somiten. Die detektierte Expression des NoBP konzentriert sich auf das Forebrain, den ersten Kiemenbogen, die (vordere) Extremität, die dorsale Seite des Schwanzes und das undifferenzierte mesenchymale Gewebe am Schwanzende. E: Embryo zum Zeitpunkt E 10.25-10.5. Eine starke NoBP-Expression wurde in den Kiemenbögen sowie der optical placode, den Extremitäten, und der dorsalen Schwanzseite detektiert. F: Aufnahme einer hinteren Extremitätenanlage eines E 10.25 Embryos. Die detektierte NoBP-Expression konzentriert sich auf die proximale Seite der Anlage (Pfeil), gegenüber der ZPA. ERGEBNISSE 53 FGF-BP: Mit der FGF-BP antisense-Dig-RNA wurden weniger eindeutige Expressionsorte gefunden als mit der NoBP-Sonde. Embryonen vom Entwicklungstag 8.0 bis 9.0 (10-20 Somiten) zeigten lediglich ein schwaches Hybridisierungssignal im Midbrain, im Hindbrain und an der Spitze des ersten Kiemenbogens. In Embryonen vom Entwicklungstag 9.5 allerdings, wurde in zwei Embryonen (mit 25 bzw. 26 Somiten) eine sehr starke Expression im caudalen Bereich der Neuralleiste, in der frühen Anlage des proximalen Rückenmarks und im distalen Part des Hindbrains, festgestellt. Dies war im Falle eines der beiden Embryonen die heftigste Farbreaktion, die überhaupt in allen Whole-mount Experimenten beobachtet wurde. Als ebenfalls positiv wurden das corticale mesenchymale Gewebe, das Forebrain, der optische Vesikel und der erste Kiemenbogen identifiziert. Die inneren Organanlagen wie Herz, Leber und Darm blieben negativ, ebenso die frühe Vorderextremität und der Schwanz. Zwei andere Embryonen mit 29 bzw. 30 Somiten zeigten wiederum nur schwache und vage Signale. Bei einem späterem Embryo, E 10.25 bis E 10.5, wurden FGF-BP-Transkripte im Bereich des nasalen Mesenchyms, der caudalen Zone der Kiemenbögen und der Extremitätenanlagen detektiert. Die Färbung im Schwanzende konzentrierte sich auf die lateraldorsale Seite der Somiten. Die inneren Organe wurden nicht gefärbt. Zu diesem Zeitpunkt ähnelt das Expressionsmuster des FGF-BP also dem des NoBP, abgesehen davon, daß keine Hybridisierungssignale in neuronalen cervicalen Zellen gefunden wurden. ERGEBNISSE Abb.10 54 A: Embryo mit 25 Somiten, Entwicklungstag 9.5, hybridisiert mit antisense FGF-BP RNA. Die benachbarten Abschnitte des Rückenmarks und des Hindbrains sind äußerst intensiv gefärbt. Weiterhin wurden das mesenchymale corticale Gewebe, das Forebrain (mehr rostral als caudal), der optische Vesikel (Pfeil) und der erste Kiemenbogen als FGF-BP positiv detektiert. B: Blick auf die dorsale Seite von A. C: Embryo von 10.25 bis 10.5, hybridisiert mit antisense FGF-BP RNA. Die detektierte Expression befindet sich in der olfactory lobe, der Spitze der Kiemenbögen, den Extremitäten und im Schwanzende. Expression von FGF-BP, NoBP und FGF18 in Hand und Fuß am Tag E 14.0 Abb. 11 zeigt einen Vergleich der Hybridisierungssignale von FGF-BP (A), NoBP (B) und FGF18 (C) in Hand und Fuß einer Maus am Entwicklungstag 14.0. Zu diesem Zeitpunkt ist die Hand (stets rechts) sichtlich noch etwas größer als der Fuß. Das Expressionsmuster der drei Gene ist nahezu identisch. Maruoka et. al fanden für FGF18 eine ganz ähnliche Expression. ERGEBNISSE 55 3.1.3 Die Expression von FGF-BP und NoBP während der frühen Lungenentwicklung Am Entwicklungstag 9.5 beginnt in Mäusen das sichtbare Wachstum der primären Lungentubuli aus dem Endoderm des frühen Vorderdarms. Die jüngsten zur whole-mount Hybridisierung verwendeten Lungen stammten aus E 10.0 Mäusen, die ältesten aus E 14.0 Mäusen. Zum Zeitpunkt E 10.0 gibt es noch keine morphologischen Anzeichen der sekundären Knospung. Die erste eindeutige Expression von FGF-BP und NoBP konnte erst dann in den Lungen detektiert werden, wenn die sekundäre Knospung bereits verstärkt eingesetzt hatte, ab dem Entwicklungstag 11.0 und darüber hinaus. NoBP: Abb. 12-D zeigt eine E 11.5 Lunge, hybridisiert mit der antisense-Dig-RNA des NoBP. Das Hybridisierungssignal fand sich in den Bereichen des Mesenchyms, die die Wachstumszone der endodermalen Tubuli umschließen. Charakteristisch war, daß die Färbung in dem Mesenchym vor den sekundären Tubuli stärker ausfiel als vor der Spitze der Lungenhauptschläuche, im linken wie im rechten Lungenflügel. Auch in einem bereits fortgeschrittenen Stadium der Knospung, am Tag 13.5, blieb das Mesenchym direkt vor den Tubuli NoBP-positiv, siehe Abb. 12-C. Abb. 12-A und 12-B verdeutlichen die Unterschiede in der Verteilung des FGF-10- und des NoBP-Transkripts. Die Pfeile deuten auf die Spitzen der sekundären Tubuli (Abb. 12-A und –B sind zueinander spiegelbildlich). Während FGF-10 im Mesenchym zwischen dem Epithel expremiert wird, gilt für NoBP das genaue Gegenteil, denn die Expression konzentriert sich auf das direkt die Tubulispitze umfassende Mesenchym. ERGEBNISSE Abb. 12 56 A: Lunge vom Entwicklungstag 12.5, hybridisiert mit antisense FGF10-RNA. Die Pfeile deuten auf die Spitzen der Tubuli. In dem Mesenchym dazwischen wurde das FGF10 detektiert. B-D sind mit antisense NoBP-RNA hybridisiert B: Lunge vom Entwicklungstag 12.5, spiegelbildlich zu A. Die Pfeile zeigen wiederum auf die Spitzen der Tubuli. Hier ist das Mesenchym direkt um die distalen Tubuli gefärbt. C: Linker Lungenflügel vom Entwicklungstag 13.0. Das Mesenchym um und vor den distalen Tubuli ist gefärbt. D: Lunge vom Entwicklungstag 11.5. Das Mesenchym um die sekundären Tubuli zeigt stärkere Signale als das Mesenchym um die primären distalen Tubuli. FGF-BP Das zum Zeitpunkt 11.0 detektierte Expressionsmuster erinnert sehr an die Lokalisation des NoBP-Signales. Wiederum wurden die mesenchymalen Zellen vor der Spitze der sekundären Knospen am stärksten angefärbt (Abb. 13-A). Verglichen mit NoBP und FGF10, scheint die Expression des FGF-BP aber deutlich geringer zu sein. Tatsächlich wurden Lungen vom Entwicklungstag 11.0 bis 12.5 in einigen Fällen hier nur sehr schwach angefärbt. Bei drei größeren Lungen, etwa vom Tag 13.5 bis 14.0, wurde die FGF-BP RNA nur in drei bis vier Flecken ganz am äußeren Ende des wachsenden Mesenchyms detektiert. Die Abb. 13-B zeigt einen solchen Flügel, 13-C eine Vergrößerung des interessanten Ausschnittes. Die Färbung konzentriert sich auf Bereiche direkt vor den äußeren epithelialen Tubuli. Die gekennzeicheten Hybridisierungssignale befanden sich vor solchen Knospen, die scheinbar gerade im Begriff waren, sich in zwei Hälften ERGEBNISSE 57 zu teilen. Dies deutet darauf hin, daß das FGF-BP in dieser Phase der Proliferation des Lungenepithels entgegenwirkt. Abb. 13 Beide Lungen sind mit antisense FGF-BP -RNA hybridisiert. A: Lunge vom Entwicklungstag 11.0. Das mesenchymale Hybridisierungssignal befindet sich nicht direkt vor, sondern eher lateral der Knospenspitze. Die sekundären Verzweigungen sind stärker gefärbt als die primären Enden. B: Lunge vom Entwicklungstag 13.5. Der Rand des rechten Flügels ist in C vergrößert dargestellt. C: Die Pfeile deuten auf zwei der drei epithelialen Knospen, vor denen FGF-BP expremierende mesenchymale Zellen detektiert wurden. Beide erscheinen an der Spitze etwas abgeflacht und verbreitert. Zwischen diesen Knospen ist ein schmaler Tubulus zu sehen. Es läßt sich festhalten, daß das NoBP konstant in dem das Epithel unmittelbar benachbarten Mesenchym expremiert wird, beginnend ab E 11.0. Dagegen wird die Expression des FGF-BP im Mesenchym nach dem Zeitpunkt E 11.5 sehr schwach. Erst ab etwa E 13 findet man wieder FGF-BP mRNA, aber (bei drei unabhängigen Versuchen) nur in der äußeren lateralen Wachstumszone der Flügel, direkt in der Nähe der äußersten epithelialen Knospen. ERGEBNISSE 58 3.2 FGF-BP in der Lungenorgankultur Mit Hilfe der In-situ Hybridisierungen konnte nachgewiesen werden, daß FGF-BP während der frühen Lungenentwicklung expremiert wird und daß diese Expression auf spezifische Zonen im Mesenchym, dicht an der Spitze der wachsenden Tubuli, beschränkt ist. Um den Effekt von FGF-BP auf die FGF-Signaltransduktion in der frühen Lunge zu untersuchen, wurden Lungenorgankulturen angelegt, wobei die Lungen in Matrigel über mehrere Tage gehalten werden können. FGF-BP Protein wurde mit Hilfe des Bac-toBac Expressionssystems in Sf-21 Insektenzellen expremiert und in den Überstand sekretiert. Dieser Überstand wurde dem Matrigel beigemischt und die Lungen in Anwesenheit von FGF1 bzw. FGF10 inkubiert. 3.2.1 Expression von humanem und murinem FGF-BPhis in Insektenzellen Die vollständige cDNA des murinen FGF-BP wurde von Frau Dr. Marianne Antoine mit Hilfe einer RT-PCR amplifiziert und in den pGem4Z Vektor kloniert. Der Leserahmen des Proteins kodiert für 251 Aminosäuren. Aus diesem Plasmid wurde die FGF-BP cDNA von Dr. Antoine in den pFASTBacHTa-Vektor (Gibco Life) einkloniert, wodurch N-terminal die ersten 20 Aminosäuren mit dem Signalpeptid des FGF-BP abgetrenntwurden und eine für ein 6xHis-Tag kodierende Sequenz an das 5´-Ende vor die insertierte cDNA gelangte. Mit diesem Konstrukt wurden DH10 E.coli transformiert. Diese Bakterien tragen das funktionelle Genom eines Insektenvirus (Baculovirus) in sich. Transformierte Zellen wurden aufgrund ihrer Eigenschaft, über keine ß-Galoctisidaseaktivität mehr zu verfügen, als weiße Klone in einem X-Gal-Assay identifiziert. Die aufgereinigte Virus-DNA aus diesen Zellen wurde mit Hilfe eines Lipidreagenzes in Sf-21 Insektenzellen transfiziert. Innerhalb von vier Tagen befanden sich Viren im Zellüberstand, die weiter in der Insektenzellkultur vermehrt wurden, bis ein ausreichend hoher Virustiter erreicht war. Das das den Virus enthaltende Medium wurde aliquotiert und eingefroren. Infizierte Insektenzellen wurden nach jeweils ein bis fünf Tagen gesammelt und Zellysate angefertigt. Durch Western-Blot Analysen mit dem Penta-His Antikörper wurde die Expression eines etwa 35 kD großen Proteins nachgewiesen. In Lysaten von nicht infizierten Insektenzellen zeigte der Antikörper keinerlei Kreuzaktivität (Daten nicht gezeigt). Dies ist deutlich größer, als das erwartete Molekulargewicht von etwa 27 kD. Durch das Aufkochen des Zellysats und die Durchführung der SDSGelelektrophorese unter nicht-reduzierenden Bedingungen sollten aber alle nicht- ERGEBNISSE 59 kovalenten Bindungen und Cysteindisulfidbrücken zerstört sein. Möglicherweise ist das Protein glykosyliert (siehe Einleitung). Um das FGF-BPhis in den Überstand der Insektenzellen zu dirigieren, wurde eine spezifische Insektensignalpeptidsequenz, die für 25 Aminosäuren kodiert, samt Startcodon aus dem pMBac Vektor (Stratagene) vor die cDNA des humanen FGF-BPhis kloniert (die 6xHis-Sequenz war von Dr. Antoine 5´ von Serin 37 mit einer PCR eingesetzt worden; laut den Sequenzanalysen von Wu et al. befindet sich am N-Terminus des reifen huFGF-BP das Lysin 34). Dazu mußten zunächst zwei Basenpaare an der 5´-Seite der cDNA über eine PCR mit entsprechenden Primern eingefügt werden, um den Leserahmen zwischen dem Signalpeptid und dem FGF-BPhis nicht zu verschieben. Die ISP-Sequenz wurde zunächst als 5´-Ende eines KpnI/NheI-Fragmentes in den mit KpnI/XbaI geschnittenen pGem4Z-Vektor kloniert. Nichtkompatible überhängende 5´Enden wurden mit Klenow-Fragment aufgefüllt. Im zweiten Schritt wurde das PCRProdukt über Restriktion mit EcoRV/EcoRI (beide Schnittstellen stammen aus dem Vektor) an das 3´-Ende der mit SmaI geschnittenen Signalpeptidsequenz gesetzt. Der korrekte Anschluß des FGF-BPhis an das ISP und die Sequenz der benutzten Primer wurde mit einer Sequenzierung überprüft. Das FGF-BPhisISP Fragment wurde per Restriktion mit HindIII/EcoRI in den mit CpoI und EcoRI geschnittenen pFASTBacHTaVektor kloniert. Durch die Nutzung der CpoI-Schnittstelle wurden das Startcodon und die 6xHis-Sequenz aus dem HTA-Vektor entfernt. Mit diesem Konstrukt wurden wiederum DH10 E.coli transfiziert und, wie für FGF-BPhis beschrieben, weiterverfahren, und es wurde ein entsprechender Insektenvirus hergestellt. Sf-21 Insektenzellen wurden parallel mit die Expression von murinen FGF-BPhis bzw. humanen FGF-BPhis(ISP) induzierenden Viren infiziert. Nach 48 Stunden Kultur wurde das 5% FCS enthaltende TC-100 Medium gegen 4 ml serumfreies Medium pro 100mm-Zellkulturschale ausgetauscht, um über weitere drei Tage die von den Zellen sekretierten Proteine in möglichst wenig Medium aufzunehmen. Einen ganz ähnlichen Ansatz wählten Ohbayashi et al. 1998, um FGF18-haltiges Medium herzustellen. Der Proteingehalt der Zellüberstände und der Zellysate aus beiden Ansätzen wurde per SDS-PAGE und anschließender Silberfärbung bzw. Westernblot analysiert. Im Silbergel konnte kein Unterschied detektiert werden (Daten nicht gezeigt). Das Ergebnis des Westernblots ist in Abb. 14 dargestellt. In den Zellüberständen befand sich kein detektierbares His-Protein. Das mit dem Insektensignalpeptid ausgestattete huFGF-BPhis wurde aber offenbar von den Zellen ERGEBNISSE 60 synthetisiert. Das apparente Molekulargewicht der Hauptfraktion beträgt etwa 27 kD, was dem aus der Größe des offenen Leserahmens zu erwartenden Wert entspricht, wenn man das Signalpeptid mit einbezieht. Da das Molekulargewicht der Hauptvariante des murinen FGF-BP ohne Insektensignalpeptid um ca. 8 kD größer als erwartet ist, werden beide Formen offenbar unterschiedlich modifiziert. Die kleineren detektierten HisProteine bei 22 und 15 kD sind vermutlich am C-Terminus prozessiert. Es war aber anhand des Western-Blots nicht möglich zu entscheiden, ob, und wenn ja, wieviel, N-prozessiertes huFGF-BP im Zellüberstand vorhanden war. Da das Startcodon des Proteins aus dem Insektensignalpeptid stammt, muß ein unprozessiertes, His-Tag modifiziertes FGF-BP auf jeden Fall ein ISP im richtigen Leserahmen aufweisen. Sollte das Protein trotz der Modifikationen N-terminal der 34 Aminosäure gespalten worden sein, bestünde der His-Tag nur noch aus drei Histidinen. hu FG FB mu Ph FGF is( IS BPh P) is 62 kD 50 kD 37 kD 25 kD 20 kD 14 kD Abb. 14 Expression des humanen und des murinen FGF-BP in Sf-21 Insektenzellen Das Lysat der Zellen wurde in einem 12%igem SDS-Gel aufgetrennt, und nach einem Western-Blot wurden die 6xHis-markierten Proteine mit Penta-His-Antikörper (Zweitantikörper a-Maus-IgG POD) und der ECL-Technik immunodetektiert. Links sind die apparenten Molekulargewichte der mitgelaufenen Markerproteine aufgetragen. ERGEBNISSE 3.2.2 61 Der Überstand von huFGF-BPhis(ISP) expremierenden Zellen hemmt das FGFinduzierte Lungenwachstum Obwohl nicht bewiesen werden konnte, daß die Sf-21 Insektenzellen huFGF-BP in den Zellüberstand abgeben, wurden die Überstände weiter verwendet, um zu überprüfen, ob damit die Wirkung von FGF10 und FGF1 in der Lungenorgankultur moduliert werden kann. In zwei unabhängigen Versuchen wurden jeweils die Lungen aus einer E 11.5 -Präparation auf sechs Matrigel-Ansätze verteilt. Das Matrigel bestand zu 50% aus dem reinen Matrigel, zu 30% aus DMEM/0.2% FCS und zu 20% aus Zellüberstand. Das Medium setzte sich dementsprechend aus 80% DMEM/0.1% FCS und 20% Zellüberstand zusammen. Im Gel und im Medium befanden sich entweder 50 ng/ml FGF10, 500 ng/ml FGF1 oder gar kein exogen addiertes FGF. Als Kontrolle diente der Überstand der das murine FGF-BPhis expremierenden Insektenzellen. Auf die beiden parallelen Ansätze wurden möglichst ähnlich weit entwickelte Lungen verteilt, um ihr Wachstum über einen Zeitraum von 90 h besser vergleichen zu können. Abgesehen von dem Zeitpunkt 0 h sind alle Aufnahmen der Lungen bei der gleichen Vergrößerung gemacht worden. ERGEBNISSE 62 huFGF-BPhis(ISP) muFGF-BPhis 0h 12 h 40 h 72 h 90 h Abb. 15 Wachstum von E 11.5 Lungen in Matrigel mit (links) Überstand von huFGF-BPhis(ISP) expremierenden Insektenzellen bzw. mit (rechts) Überstand von muFGF-BPhis expremierenden Insektenzellen. Bis auf 1 und 6 ist die Vergrößerung stets die gleiche. ERGEBNISSE 63 huFGF-BPhis(ISP) muFGF-BPhis 0h 12 h 40 h 72 h 90 h Abb. 16 Wachstum von E 11.5 Lungen in Matrigel mit (links) Überstand von huFGF-BPhis(ISP) expremierenden Insektenzellen bzw. mit (rechts) Überstand von muFGF-BPhis expremierenden Insektenzellen, jeweils supplementiert mit 50 ng/ml FGF10. Bis auf 1 und 6 ist die Vergrößerung stets die gleiche. Die Pfeile in 16-8 deuten auf wachsendes Epithel. ERGEBNISSE 64 huFGF-BPhis(ISP) muFGF-BPhis 0h 12 h 40 h 72 h 90 h Abb. 17 Wachstum von E 11.5 Lungen in Matrigel mit (links) Überstand von huFGF-BPhis(ISP) expremierenden Insektenzellen bzw. mit (rechts) Überstand von muFGF-BPhis expremierenden Insektenzellen, jeweils supplementiert mit 500ng/ml FGF1. Bis auf 1 und 6 ist die Vergrößerung stets die gleiche. Die Pfeile in 17-9 und 17-0 deuten auf knospendes Epithel. ERGEBNISSE 65 In allen drei miteinander verglichenen Fällen entwickelten die Lungen, je nachdem in welchem Überstand sie inkubiert wurden, dezidierte Unterschiede, hinsichtlich der Größe des Explantats und/oder der Knospung des Epithels. Wenn dem Gel kein Wachstumsfaktor zugegeben wurde, begannen nach 40stündiger Inkubation mit dem Überstand aus huFGF-BPhis(ISP) expremierenden Insektenzellen vermutlich abgestorbene Zellen, sich aus dem Verband zu lösen (Abb. 15-1 bis 15-5). Dagegen blieb die äußere Morphologie der Lunge, die in Gel mit Überstand von muFGF-BPhis expremierenden Zellen inkubiert wurde, über 90 h weitestgehend intakt (Abb. 15-6 bis 15-0). Wenn zu den Ansätzen 50 ng/ml FGF10 addiert wurde, blieb bei der Inkubation mit huFGF-BPhis(ISP) Überstand ein vermehrtes Absterben aus (Abb. 16-1 bis 16-5) und im Falle des muFGF-BPhis Überstands konnte sogar eine gewisse Expansion des Epithels durch das Mesenchym hindurch in das Gel hinaus beobachtet werden (Abb. 16-6 bis 16-0). Am frappierendsten war allerdings der Unterschied bei Inkubation mit 500 ng/ml FGF1. Während mit huFGF-BPhis(ISP) Überstand kein epitheliales Wachstum induziert wurde und sogar nach 90 h ein verstärktes Zellsterben einsetzte (Abb. 17-1 bis 17-5), proliferierte das Lungenepithel in Anwesenheit von muFGF-BP Überstand. Nach 72 h hatte sich eine große Knospe im Bereich der sekundären Tubuli etabliert (Abb. 17-9), und nach 90 h erschienen viele kleine Knospen aus der Zone der primären Tubulispitzen (Abb 17-0). In der zweiten, identisch aufgebauten Versuchsreihe mit etwas weiter entwickelten Lungen (etwa E 12) waren die Ergebnisse ähnlich, aber weniger poignant im Hinblick auf die Unterschiede zwischen den beiden verschiedenen Insektenzellüberständen. ERGEBNISSE 66 3.2.3 Schnitte von kultivierten Lungen Um die innere Struktur der Lungen zu untersuchen, und um zu zeigen, daß die Knospen tatsächlich von den epithelialen Zellen gebildet wurden, wurden die Lungen nach 90stündiger Inkubation aus dem durch Abkühlung verflüssigten Matrigel entnommen, fixiert und in Paraffin eingegegossen. 3 µm dicke Schnitte wurden mit HämatoxylinLösung angefärbt. Abb. 18 A: Längsschnitt durch die in Anwesenheit von 50 ng/ml FGF10 und huFGF-BPhis(ISP) Überstand inkubierte Lunge; mehrere kleine Knospen aus offenbar epithelialen Zellen haben sich gebildet (Pfeil). B: Querschnitt durch die in Anwesenheit von 500 ng/ml FGF1 und muFGF-BPhis Überstand inkubierte Lunge; es hat sich eine große Knospe etabliert, die aus einer einfachen Schicht epithelialer Zellen besteht (Pfeil). Es fällt auf, daß das Mesenchym in A deutlich dichter gepackt ist als in B und das im Gegenzug die Dichte der von den Fibroblasten des äußeren Mesenchyms gebildeten Interzellularsubstanz (Bucher und Hartenberg, 1991), hier blaß rosa angefärbt, viel größer ist. DISKUSSION 67 4 Diskussion Das korrekte Wachstum komplexer Organe und Körperstrukturen während der Embryogenese hängt von der kontrollierten Proliferation, Migration und Differenzierung der daran beteiligten Zellen ab. Bei einem Organ wie der Lunge, bestehend aus dem Epithel der Tubuli und dem darum gepackten Mesenchym, spielen die Interaktionen zwischen epithelialen und mesenchymalen Zellen eine entscheidende Rolle. Viele Hinweise lassen vermuten, daß die komplex regulierte, lokale Konzentration und Aktivität der Fibroblastenwachstumsfaktoren (FGFs) in diesen Geweben großen Einfluß auf den Wachstumsprozeß ausübt. Proteine, die mit FGFs interagieren bzw. sie binden, sind als potentielle Modulatoren des FGF-kontrollierten Zellwachstums daher wahrscheinlich an dieser Regulation beteiligt – unter der Voraussetzung, daß sie auch in den entsprechenden Zellen vorhanden sind. Das nukleäre Bindungsprotein NoBP und das sekretierte FGF-Bindungsprotein gehören, anders als FGF-Rezeptoren und Heparansulfatproteoglycane zu den "nicht-klassischen" FGF-interagierenden Proteinen. Ihre Expression und Funktion während der Embryogenese ist noch nicht gut untersucht. Diese Arbeit sollte dazu beitragen, dies zu ändern. Dazu wurden RNA-In-situ Hybridisierungen an Paraffinschnitten von embryonalen Mäusen (vom Entwicklungstag E 13.5, 16.0 und 18.0) und ganzen Embryonen (E 7.0 bis 10.5) und Lungen (E 10.0 bis 13.5) durchgeführt (`Whole-mount In-situ Hybridisierung´). Zur Kontrolle der Spezifität der detektierten Signale wurden, v.a. bei Experimenten mit Gewebeschnitten, parallel digoxigenierte sense-RNAs als Negativprobe eingesetzt. Bei Whole-mount Hybridisierungen dienten in erster Linie antisense-Sonden von FGF10, Shh, FGF18 und erg2 als Kontrollen. Ihre spezifische Expression in den Lungen bzw. den Mäuseembryonen ist in der Literatur bereits beschrieben worden (siehe Einleitung) und konnte in jedem Fall in den hier diskutierten Experimenten nachvollzogen werden. Jedes diskutierte Ergebnis wurde in mindestens zwei unabhängigen Experimenten erzielt. Etwas schwerer fällt die Auswertung der gefärbten Schnitte, da v.a. die sense-RNA Sonden von FGF-BP und FGF18 dazu neigten, wenn auch in einem deutlich geringeren Maße, in den gleichen Zonen zu hybridisieren wie die komplementären antisense-RNAs. Die Hybridisierungssignale fanden sich auch hier spezifisch im Zytosol der Zellen. Die FGF10 sense-RNA verursachte dagegen nur sehr wenig Hintergrund. Der Diskussion der NoBP und der FGF-BP Expression soll daher ein Vergleich DISKUSSION 68 der detektierten Expression von FGF18 und FGF10 mit der in der Literatur beschriebenen vorangestellt werden. Die Expression des FGF18 in Mäuseembryonen Ohbayashi et al. benutzten 1998 für ihre In-situ Hybridisierungen S35-markierte antisense-RNA. Damit detektierten sie in E 14.5 Ratten (was in etwa E 14 Mäusen entspricht) Transkripte in verschiedenen Geweben und die stärksten Signale befanden sich in der Zunge, dem Rückenmark, der Hypophyse, den Knochen und den DRGs. Hu et al. untersuchten 1998 ebenfalls mit radioaktiv markierten Sonden die FGF18 Expression in E 15.5 Mäusen. Die kräftigsten Signale wurden in der Lunge, dem die Knochen umgebenen Mesenchym und in dem sich entwickelnden Neocortex detektiert. Verschiedene andere Gewebe, darunter das Rückenmark und die Haut, waren ebenfalls positiv. Leber und Herz scheinen laut beiden Autoren kein FGF18 zu expremieren. Damit werden die Ergebnisse, die in dieser Arbeit mit der antisense-Sonde des FGF18 erzielt worden, durchaus bestätigt. In Schnitten von E 16 Embryonen wurden die stärksten Hybridisierungssignale in dem Trigeminalganglion, dem Thymus und der Lunge detektiert, gefolgt von den Knochen, dem Darmepithel, der Haut, dem frühen Neocortex und dem Rückenmark. Die einzige wirkliche Differenz zwischen den hier beschriebenen Ergebnissen und den Angaben in der Literatur scheint die FGF18 Expression im Darmepithel zu betreffen, die von Ohbayashi und von Hu nicht beschrieben wird. In der frühen Lunge von E 11 bis E 12.5 wird FGF18 den Whole-mount Hybridisierungen zur Folge nicht expremiert, weswegen die Annahme, daß FGF18 an der Organisation des frühen Lungenwachstums beteiligt sein könnte (Lebeche et al., 1999), wohl nicht zutrifft. Die Expression des FGF10 in Mäuseembryonen Yamasaki et. al detektierten 1996 mit radioaktiv markierten Sonden FGF10 Transkripte in der E 14 Ratte spezifisch in der Hirnanhangdrüse, der Lunge, dem Dünndarm und dem caudalen Rückenmark. In dieser Arbeit hingegen wurde die stärkste FGF10Expression in Haut und Knochen der E 16 Mäuse detektiert. Unter den inneren Organen war die Leber am kräftigsten angefärbt. In der Lunge war das Mesenchym positiv, während im Epithel keine FGF10 mRNA gefunden wurde (siehe Abb. 2-C). Auch in anderen mesenchymalen Geweben wurden FGF10-Transkripte detektiert, und die Intensität der Signale war der in den Lungen vergleichbar. DISKUSSION 69 Da mit der benutzten digoxigenierten antisense-FGF10 RNA die Ergebnisse von Bellusci et al. von 1997 bestätigt werden konnten, die bei Whole-mount Hybridisierungen mit den Lungen erzielt worden waren, war die Sonde offenbar in der Lage, spezifisch zu binden. Es ist nicht auszuschließen, daß das Muster der Expression in Ratte und Maus voneinander differiert, zumal wenn sich die untersuchten Stadien um zwei Entwicklungstage unterscheiden. Aktuelle Forschungsergebnisse implizieren, daß FGF10 durchaus eine Rolle bei der Entwicklung der Knochen und der Haut spielen könnte. Adulte Mäuse synthetisieren v.a. in der Lunge, dem Gehirn und der Haut FGF10 (Beer et al., 1997), und FGFR2b Knockout-Mäuse weisen u.a. Mißbildungen der Haut auf (De Moerlooze et al., 2000). FGFR2b, der bevorzugte FGF10-Rezeptor, wird ebenso in proliferierenden Osteoblasten der Maus expremiert (Rice et al., 2000). Insgesamt widersprechen also die Ergebnisse der In-situ Hybridisierungen im Falle von FGF10 und FGF18 nicht den veröffentlichten Daten. Im Allgemeinen, das gilt auch für das FGF-BP und das NoBP, wurden viele Gewebe mit einer geringen Intensität angefärbt, wohingegen in der Literatur häufig ganz spezifische Expressionsorte beschrieben werden. Diese unterschiedlichen Ergebnisse mögen zumindest teilweise dadurch erklärbar sein, daß in vielen Arbeiten S35- oder P33-markierte RNA-Sonden zur Hybridisierung verwandt werden. Da bei dieser Methode ein strahlungssensitiver Film benutzt wird, um die Signale zu dokumentieren, dessen Empfindlichkeit nicht linear ist und so schwächere Signale ausblenden kann, kommen oft nur die prominenten Signale zur Geltung. Die Expression des NoBP in Mäuseembryonen Das NoBP wurde bei einem Two-Hybrid Screen als FGF3 bindendes Protein identifiziert (Reimers-Fadhlaoui, Dissertation 1999). Weitere Studien bestätigten diese Bindung, und es konnte nachgewiesen werden, daß das NoBP im Kern lokalisiert ist. Alle FGFs werden zumindest zum Teil sekretiert; von den FGF1, -2, -11 bis -14 und eben auch -3 kennt man aber Spleißvarianten, die in den Kern translozieren. Abgesehen von internalisierten FGF-Rezeptoren (Stuchowiak et al., 1997) ist das NoBP das einzige Protein, das bisher als (potentieller) nukleärer Bindungspartner für die FGFs charakterisiert wurde. Offen ist noch, mit welchen weiteren FGF das NoBP interagieren kann; der Nachweis einer FGF11–Bindung, ebenfalls im Two-Hybrid-System, konnte jedenfalls nicht erbracht werden und mit FGF2 interagierte NoBP nur schwach. Wie weitere Un- DISKUSSION 70 tersuchungen in unserem Labor zeigten, wird das NoBP offenbar in vielen Geweben der adulten Maus expremiert, v.a. in Herz, Lunge, Milz und Nieren. Auch in allen untersuchten sekundären Zellinien fand sich NoBP mRNA, während in differenzierten HL-60 Zellen kein NoBP detektiert wurde. Diese Ergebnisse ließen uns eine Funktion des NoBP als Teil der Zellzyklusmaschinerie schnellwachsender Zellen vermuten. Solch ein Protein würde im Embryo womöglich ubiquitär expremiert. Die Ergebnisse dieser Arbeit zeigen jedoch, daß diese ursprüngliche Annahme zu pauschal ist und so nicht zutrifft. Die Expression des NoBP ist während der Mausembryogenese zeit- und gewebespezifisch kontrolliert. Aus den Experimenten mit den Paraffinschnitten läßt sich festhalten, daß das NoBP bevorzugt in mesenchymalen Zellen expremiert wird. Die stärkste Expression wurde zu E 16 in dem Epithel der Blutgefäße, der inneren Zellschicht des Dünndarms und proliferativen Chondroplasten bzw. Osteoblasten gefunden. Außerdem wurden viele mesenchymale Gewebe als schwach NoBP-positiv detektiert. FGF3, der einzige bisher identifizierte Bindungspartner (in seiner nukleären Form) des NoBP , wird dagegen während der späteren embryonalen Entwicklung nur in den frühen Purkinje-Zellen des Cerebellums und in differenzierenden Zellen in der Retina expremiert (Wilkinson et al., 1989). In der frühen embryonalen Phase scheint FGF3 jedoch eine wichtige Rolle zu spielen, zu E 7.5 wird es z.B. in migrierenden Zellen des Mesoderms gefunden und etwas später , zu E 8.5, im Neuroepithel des caudalen Hindbrains, im otischen Vesikel, der Anlage des Innenohrs, und im Ende des Schwanzes (Wilkinson et al., 1988; Mahmood et al., 1996). Die Expression ist im Rhombomer 6 am stärksten, und das Rhombomer 4 ist nur noch schwach FGF3-positiv. In E 9.5 Embryonen hat die Expression in den Rhombomeren nachgelassen, aber im ventralen Teil des Forebrains und in den Kiemenbögen zugenommen. Die FGF3-Knockout Mäuse weisen Defekte in der Entwicklung des Innenohres und des Schwanzes auf und sterben häufig noch vor der Geschlechtsreife (Mansour et al., 1993). In dem Zeitraum der Hindbrainsegmentierung wurden zu E 8.25-8.5 v.a. in den Rhombomeren 1, 4 und 6 und in der Neuralleiste, sowie im Forebrain und am Schwanzende NoBP-Transkripte detektiert. Somit überschneidet sich hier die Expression von FGF3 und NoBP zumindest teilweise. Möglicherweise ist das NoBP also an der Organisation des Innenohres beteiligt. Einen Tag später, zu E 9.5, ergeben sich im ventralen Forebrain, in den Kiemenbögen und im Schwanz Co-Expressionen von FGF3 und NoBP. DISKUSSION 71 Zusätzlich wurde hier noch ein Signal in der frühen Anlage der vorderen Extremität entdeckt, in der FGF3 nicht expremiert wird. Am Entwicklungstag 10.5 nimmt im Cortex die Expression des NoBP weiter ab. Interessanterweise scheint das NoBP im diesen Stadium spezifisch an der rostralen Seite des hinteren Gliedmaß expremiert zu werden, also gegenüber der durch die Expression von Shh gekennzeichneten ZPA. In der Lunge wurde die NoBP mRNA von E 11.0 bis E 13.5 ausschließlich in dem Mesenchym, das die distalen Tubuli umgibt, detektiert. NoBP wird also in drei Geweben, im Hindbrain, im Gliedmaß und in der Lunge entlang einer anterioren/posterioren Achse expremiert. Dies gilt ebenso für Genfamilie der Hox-Gene, die in Arthropoden offenbar entscheidend zur Initiierung und v.a. Aufrechterhaltung asymmetrischer Wachstumsvorgänge beitragen. Diese Transkriptionsfaktoren besitzen innerhalb einer hochkonservierten Sequenz ein Homeoboxmotiv, das die Bindung an spezifische DNA-Sequenzen vermittelt. Obwohl man für viele der mehreren Dutzend Hox-Proteine spezifische Aufgaben ermitteln konnte, sind sich die DNA-Bindungseigenschaften der Hox-Proteine recht ähnlich, so daß man annimmt, daß die Bindungen anderer Proteine wie z.B. von einem der drei Pbx-Varianten an Hox nötig sind, um die Selektivität der Hox/DNAInteraktion entscheiden zu erhöhen (zusammengefaßt von Chariot et al., 1999). Eine interessante Eigenschaft der Hox-Proteine besteht darin, daß sie die Expression von Shh und somit z.B die Etablierung der ZPA initiieren können. Das größte Maß an Coexpression tritt scheinbar mit Hoxb-2 (früher Hox-2.8) und Hoxb-5 (Hox-2.1) auf. Beide werden in der Lunge (E 10.5 bis E 13.5) wie NoBP ausschließlich im Mesenchym um die distalen Tubuli expremiert, wobei die Stärke der Expression gleichermaßen mit der Zeit abnimmt (Bogue et al., 1996). Hoxb-5 wurde in E 10.5 Mäusen ebenso wie NoBP im proximalen Teil der Extremitäten detektiert (Wall et al., 1992). Knockout-Mäuse bilden eine rostral verschobene Schulter aus (Rancourt et al., 1995), ein Phänotyp, den man auch bei Menschen schon beobachtet hat (SprengelSyndrom). Desweiteren wird Hoxb-5 im Hindbrain nicht expremiert, sondern in der sich caudal anschließenden Region des Rückenmarks (Holland und Hogan, 1988), sowie im ersten Kiemenbogen (Hunt et al., 1991). Hoxb-2 wird dagegen zwar nicht im Gliedmaß expremiert, aber zu E 8.5 in den Rhombomeren 3 bis 6 (Barrow et al., 2000), wobei die Expression anterior/posterior bzw. rostral/caudal ähnlich wie bei FGF3 immer stärker wird. Hoxb-2 wird ebenso wie NoBP in den Zellen der Neuralleiste gebildet, von wo aus mesenchymale Zellen in die Kiemenbögen einwandern (Rossel et al., 1999) und die Bildung der Brust-, Kiefer- und Gesichtsknochen einleiten (Vieille-Grosjean et al., DISKUSSION 72 1997). Die Hoxb-2 Knockout-Mäuse, die lebend geboren werden, besitzen keine Gesichtsknochen und sterben früh (Barrow und Capecchi, 1996). Das einzige NoBP-Signal während der frühen Embryonalentwicklung, das nicht mit der Expression von HoxGenen verknüpft ist, wurde im Bereich des ersten Rhombomers nachgewiesen, wo man bis jetzt keine Hox-Proteine finden konnte und der vermutlich die gesamte frühe Anlage des Cerebellums darstellt. Kürzlich hat man nachgewiesen, daß die Zellen zwar HoxProteine bilden können, die Expression aber durch die Wirkung von FGF8 gehemmt wird (Irving und Mason, 2000). Die in dieser Arbeit nachgewiesene spezifische, asymmetrische Expression des NoBP läßt also vermuten, daß es während der frühen Embryogenese eine wichtige Rolle bei der Organisation des Wachstumsprozesses übernimmt. Das in Lunge, Gliedmaß und Hindbrain detektierte Expressionsmuster ist dem eines Hox-Proteins (konkret Hoxb-2 und Hoxb-5) sehr ähnlich. Möglicherweise ist NoBP Teil der Hox-/ShhSignaltransduktion oder interagiert direkt oder mittelbar mit den Hox- Transkriptionsfaktoren. Die Suche nach weiteren Bindungspartnern des NoBP z.B. im Two-Hybridsystem sollte zunächst im Vordergrund stehen, um diesen Überlegungen eine konkrete Grundlage zu verleihen. Auch könnte das Studium von Knockout-Mäusen einen großen Beitrag zur Erforschung der Funktion dieses interessanten Proteins leisten. Die Expression von FGF-BP in Mäuseembryonen Die Ergebnisse der In-situ Hybridisierungen in den Paraffinschnitten zeigen, daß FGF-BP in vielen Geweben expremiert wird, in denen auch FGF-Transkripte gefunden werden. Das Muster der Expression von FGF-BP, FGF10 und FGF18 war z.B. im Kieferbereich weitgehend identisch. Während endodermale Zellen FGF-BP negativ sind, enthalten die mesenchymalen Zellen im Bindegewebe detektierbare Mengen an FGFBP mRNA. Bei zunehmender Differenzierung zu Chondrozyten und Osteoblasten nimmt die Expression ab und die FGF-BP positiven mesenchymalen Zellen bilden einen Kranz um die Zentren der Ossifikation. Das höchste Expressionsniveau wurde in der Lunge, v.a. im Mesenchym, dem Epithel im Dünndarm, im Thymus, im Trigeminalganglion und in den DRGs (dorsal root ganglia) gefunden. Die Expression im Gehirn der E 16 Embryonen scheint dagegen schwächer zu sein. Hier sind die fortgeschrittenen Zentren der neuronalen Differenzierung angefärbt. In der Haut wurden erst ab dem Entwicklungstag 18 größere Mengen an FGF-BP mRNA detektiert, während das Signal in der Lunge abnimmt und im Darmepithel etwa gleich stark bleibt. DISKUSSION 73 Kurtz et al. dagegen fanden 1997, indem sie Hybridisierungen mit radioaktiven Sonden durchführten, daß sich die Expression des FGF-BP in embryonalen Mäusen, beginnend von E14 bis zur Geburt, ganz auf nur drei Gewebe, die Haut, den Darm und die Lunge konzentriert und dort in späteren Stadien zunimmt. In den 70er Jahren hat man erstmals FGF1 und FGF2 aus der Hirnanhangdrüse von Rindern isoliert (Gospodarowicz et al., 1974). FGF1 und FGF2 sind die einzigen FGFs, deren Bindung an das FGF-BP bisher zweifelsfrei nachgewiesen wurde (Wu et al., 1991). Interessanterweise zeigen FGF1- (Fu et al., 1991) und FGF2-Protein (Gonzalez et al., 1990) in älteren Ratten-Embryonen eine Lokalisation, die der hier beschriebenen FGF-BP mRNA Verteilung sehr ähnlich ist. Das FGF2 befindet sich v.a. in der Extrazellulärmatrix von mesenchymalen Zellen. FGF1 wird ebenfalls v.a. in mesenchymalen Gewebe gefunden. Eine Besonderheit stellt die weite Verbreitung des FGF1 in neuronalen Gewebe dar, dessen Konzentration erst einige Wochen postnatal die höchsten Werte erreicht und im adulten Tier auf einem hohen Niveau verharrt (Ozawa et al., 1996). Aus den hier präsentierten Ergebnissen ließe sich nicht schließen, daß die Expression von FGF-BP in älteren Mausembryonen ab dem Entwicklungstag 13 auf wenige Gewebe beschränkt ist, so wie es die Wellsteingruppe propagiert. Die Whole-mount Hybridisierung ergab im Hinblick auf die FGF-BP Expression ebenfalls interessante Ergebnisse. Während in E 7.0 bis 9.0 Embryonen keine, bzw. nur diffuse Signale gefunden wurden, wurden zwei Embryonen mit 25-26 Somiten, d.h. zum Zeitpunkt E 9.5 bis 10.0, kräftig im gesamten neuroepithelialen Gewebe des Hindbrains gefärbt; im Falle des Embryos, das in Abb. 10-A gezeigt wird, war dies die wohl stärkste Farbreaktion, die in allen Whole-mount Experimenten beobachtet wurde. Da dieses Signal in einen Tag älteren Embryonen schon wieder nahezu verschwunden war, scheint es sich um eine transiente Expression zu handeln. In diesem Zusammenhang sind die Ergebnisse einer Arbeit aus dem Jahre 1993 von Nurcamb et al. sehr interessant. Die Autoren konnten zeigen, daß das Neuroepithel am Embryonaltag 9 FGF2 expremiert, aber nicht FGF1, dessen mRNA erst in E 11 Embryonen detektiert wurde. In der Zwischenzeit ändert sich die Bindungsspezifität eines der hier produzierten HSPGs aufgrund der Bildung einer anderen Heparansulfatkette (Brickman et al., 1998). Zum Zeitpunkt E 9 wird FGF2 besser gebunden, zum Zeitpunkt E 11 aber FGF1. Dieses etwa 460 kD große HSPG wird von kultivierten neuroepithelialen Zellen in den Mediumüberstand sekretiert. Wenn das HSPG mit geeigneten Anti- DISKUSSION 74 körpern aus diesem Überstand entfernt wird, verlieren exogen zugegebenes FGF1 und FGF2 ihre mitogene Wirkung, die sie in Kulturen von E11 Neuroepithelium besitzen. Offenbar reagieren die Zellen des Neuroepithels auch mit der Bildung von FGF-BP auf die bevorstehende Expression des FGF1. Da FGF-BP eine sehr viel höhere Affinität zu FGF1 als zu FGF2 aufweist (siehe Einleitung), könnte es eine Schlüsselrolle bei der Aktivierung des neu synthetisierten FGF1 spielen. Wie könnten das sekretierte HSPG und das ebenfalls sekretierte FGF-BP zusammenwirken? Die Experimente von Wu et al. von 1991 (siehe Einleitung) deuten darauf hin, daß an FGF-BP gebundenes FGF1 und FGF2 inaktiv ist und daß diese Bindung und Inaktivierung durch die Zugabe von Heparin aufgehoben werden kann. Möglicherweise ist FGF-BP in der Lage, die Verteilung des FGF1 zu verändern, weil es viel kleiner als das FGF-spezifische HSPG ist und so aufgrund einer erleichterten Diffusion mehr Zellen erreichen kann. Dort wo das FGF1 von Heparin/HSPGs aus der Bindung zu FGF-BP befreit wird, könnte das FGF1 ein Differenzierungssignal setzen. Zum Zeitpunkt E 11 beginnt das Rückenmark verstärkt zu differenzieren, ebenso die Zellen in den Ganglien des peripheren Nervensystems (Kaufman, The Atlas of Mouse Development, 1995). Der optische Vesikel, das mesenchymale neuronale Gewebe und die Kiemenbögen waren ebenfalls gefärbt. Die Anlage der Extremitäten und der gesamte caudale Bereich des Embryos waren FGF-BP negativ. Interessanterweise hat man kein FGF1 oder FGF2 in den frühen Gliedmaßen der Maus gefunden (Chan et al., 1995), wohl aber FGF2 in den Extremitäten des Huhns (Savage und Fallon, 1995). Zum Zeipunkt E 11 wurde eine geringe Expression des FGF-BP in den Extremitäten, dem caudalen Teil des Schwanzes und den Kiemenbögen detektiert. Neuronales Gewebe wurde nicht gefärbt. 1997 hatten Kurtz et al. berichtet, daß FGF-BP zum Zeitpunkt E 14 bis E 18 in der Lunge expremiert wird, ohne weitere Angaben zur genaueren Lokalisation zu machen. In dieser Arbeit konnte gezeigt werden, daß sich die FGF-BP Transkripte zum Zeitpunkt E 16 in vielen mesenchymalen Zellen detektieren lassen. Die Ergebnisse der Whole-mount In-situ Hybridisierungen lassen dagegen auf eine ganz spezifische Expression des FGF-BP in frühen embryonalen Lungen bis zum Embryonaltag 13.5 schließen. Zum Zeitpunkt E 11 konnte die FGF-BP mRNA in kleinen Zonen im Mesenchym detektiert werden, etwas lateral der Spitze der sekundären Tubuli. Diese Expression nahm im folgenden ab, und in E 12 bis E 12.5 Lungen wurde mehrfach keine oder eine nur sehr geringe Färbung beobachtet. Erst in späteren Stadien, etwa ab dem Ent- DISKUSSION 75 wicklungstag 13 bis 13.5, wenn sich im linken bzw. im größten der rechten Lungenflügel bereits 6 bis 7 parallel angeordnete Tubuli etabliert haben, wurden wieder definierte Zonen FGF-BP positiver Zellen entdeckt. Die Abb. 13-B zeigt einen solchen rechten Lungenflügel. Zwei der Zonen, in denen FGF-BP expremiert wird, befinden sich direkt vor der Wachstumsspitze eines solchen Tubulis, die dritte verläuft etwas seitlich davon. Die Tubuli, die in die Richtung der FGF-BP Expression wachsen, sind an ihrer Spitze deutlich abgeflacht und verbreitert. Offenbar geht von dem Expressionsort des FGF-BP ein - vermutlich anti-proliferierendes - Signal an die epithelialen Zellen aus. Es mag Zufall sein, aber gerade zu E 13 beginnt die Expression des FGF1 in den Lungen detektierbar zu werden (Bellusci et al., 1997). Das FGF1 ist relativ gleichmäßig im Mesenchym verteilt, findet sich aber auch im Epithel. FGF-BP in der Lungenorgankultur Nachdem gezeigt werden konnte, daß FGF-BP während der frühen Lungenentwicklung expremiert wird und die Expression streng lokalisiert ist, sollte überprüft werden, ob FGF-BP in vitro die FGF-Signaltransduktion modulieren kann. Dazu wurde mit Hilfe eines Baculovirus-Expressionssystems zum einen murines FGF-BP und zum anderen humanes FGF-BP, das durch ein an den N-Terminus angehängtes Insektensignalpeptid in den Überstand dirigiert werden sollte, in Insektenzellen hergestellt. Beide Proteine waren N-Terminal zusätzlich mit einem His-Tag versehen, um sie mit einem spezifischen Antikörper im Westernblot detektieren zu können. Es war aber leider nicht möglich, auf diese Weise das humane FGF-BP im Überstand der Insektenzellen nachzuweisen, obwohl es von den Zellen synthetisiert wurde, wie Analysen des Zellysats zeigten. Da das Startcodon dieses FGF-BP Konstruktes aus dem Signalpeptid stammt, müssen Proteine mit His-Tag ein im Prinzip funktionelles Insektensignalpeptid aufweisen. Entweder war also die Sekretion des huFGF-BPhis(ISP) sehr uneffektiv, oder der His-Tag des sekretierten Proteins ist durch N-terminale Prozessierung abgetrennt worden. Es kann auch nicht ausgeschlossen werden, daß das Protein in der ECM der Insektenzellen gebunden vorliegt, auch wenn es von humanen Zellinien in den Überstand sekretiert wird (Wu et al., 1991; Kurtz et al., 1997). Dennoch wurden Lungenorgankulturen angelegt, um die Auswirkungen der Überstände der die beiden FGF-BP Formen expremierenden Zellen auf die Lungen miteinander zu vergleichen. Ohne Signalpeptid sollte das murine FGF-BP ausschließlich in den Zellen verbleiben. Intakte Mäuselungen (einmal E 11.5 bzw. einmal E 12.0) wurden dabei in DISKUSSION 76 Matrigel, einer kommerziell erhältlichen Mischung aus Extrakten eines Maustumors, die in erster Linie aus Bestandteilen der Extrazellulären Matrix besteht, über mehrere Tage inkubiert. Gel und Medium setzten sich zu 20% aus den Überständen zusammen und waren entweder supplementiert mit 50 ng/ml FGF10 bzw. 500 ng/ml FGF1 (jeweils die humanen Formen), oder ohne den Zusatz von Wachstumsfaktoren. Dabei konnte in allen drei Fällen bei den E 11.5 Lungen beobachtet werden, daß das Wachstum sowohl der mesenchymalen wie der epithelialen Zellen unter dem Einfluß des huFGF-BPhis(ISP) -Überstandes deutlich reduziert war, bzw. die Zahl der sich aus dem Zellverband lösenden und anscheinend absterbenden Zellen deutlich zunahm. Speziell bei der Inkubation mit FGF1, das kombiniert mit muFGF-BPhis-Überstand innerhalb von 70 bis 90 h ein deutliches Wachstum des Epithels und die Bildung vieler epithelialer Knospen eingeleitet hatte, während mit huFGF-BPhis(ISP)-Überstand nach 90 h lediglich ein verstärktes Absterben der Zellen zu beobachten war, wurden die Unterschiede deutlich. Im Fall des FGF10 fiel dieser Effekt viel kleiner aus: keine Knospung im Falle des huFGF-BPhis(ISP)-Überstandes gegenüber einer geringen mit muFGF-BPhis. Ohne den Zusatz eines FGFs kam es mit huFGF-BPhis(ISP), ähnlich wie bei dem Versuch mit FGF1, zu einem Ablösen vieler Zellen vom Zellverband, während dies mit muFGF-BPhis -Überstand nicht beobachtet wurde. Da die Insektenzellen, deren Überstand eingesetzt wurde, parallel und völlig gleich behandelt worden waren bzw. sich nur in der Wahl des infizierenden Virus unterschieden, ist es wahrscheinlich, daß der beobachtete antiproliferative Effekt auf die Anwesenheit von huFGF-BP zurückzuführen ist. Zweifellos müßten weitere Versuchsreihen mit verschiedenen Konzentrationen des huFGF-BPhis(ISP) -Überstandes und FGF1 unternommen werden, um diese Annahme zu stützen. Diese wäre aber auch konsistent mit den Ergebnissen von Wu et. al aus dem Jahr 1991 (siehe Einleitung). Sie hatten beobachtet, daß FGF-BP die FGF1- und FGF2-induzierte Proliferation einer Fibroblastenzellinie in vitro hemmt und daß diese Wirkung durch die Zugabe von Heparin unterdrückt werden kann. In weiteren Versuchen wäre es also nötig, den Effekt von Heparin auch in der Lungenorgankultur zu testen, sowie das eben beschriebene Experiment von Wu mit den beiden verschiedenen Überständen und FGF1 durchzuführen. Das Matrigel selbst enthält (nach Angaben des Herstellers Becton-Dickinson) nur wenig HSPGs. Obwohl die Lungenzellen auch HSPGs zum Zeitpunkt E 11.5 expremieren (David et al., 1992; Lories et al., 1992), ist nicht klar, ob solche darunter sind, die zur Aktivierung des FGF1 benötigt werden, das ja erst ab E 13 in der Lunge nachgewiesen wird und in DISKUSSION 77 erster Linie im Zytosol wie in der ECM der gesamten mesenchymalen Zellen zu finden ist (Fu et al., 1991). Die Expression des FGF-BP in dem Mesenchym vor den epithelialen Tubuli könnte daher dazu dienen, dort die lokale Konzentration des extrazellulären FGF1 durch die Bindung zu verringern, um so das Wachstum des Epithels in die Zonen seitlich der FGF-BP expremierenden Zellen zu lenken. Erstaunlicherweise konnte man in FGF1-Knockout Mäusen aber keinerlei Defekte entdecken (Miller et al, 2000), und Mäuse, die weder FGF1 noch FGF2 expremieren, weisen den gleichen milden Phänotyp wie die FGF2-Knockout-Mäuse auf (Dono et al., 1998), d.h. in erster Linie Störungen der Cortexentwicklung und einen erhöhten Blutdruck. Andererseits z.B. konnte in vitro und mit Expressionsstudien gezeigt werden, daß FGF1 und FGF2 ganz entscheidend an der Induktion der Leberentwicklung beteiligt sind (Jung et al., 1999). Möglicherweise sind aber noch andere FGF an diesem Prozess beteiligt, die dann FGF1 und FGF2 funtionell ersetzen können. Die weite Verbreitung des FGF1 im Embryo und seine Fähigkeit, an alle bekannten FGFR mit hoher Affinität zu binden, lassen ebenfalls spezifisch durch FGF1 regulierte Wachstumsprozesse als unwahrscheinlich erscheinen. Eine wirklich essentielle Rolle des FGF-BP während der Embryonalentwicklung ist daher zweifelhaft, wenn man davon ausgeht, daß die Aufgabe des Proteins ausschließlich in der Bindung und dem Transport von FGF1 und FGF2 liegt. Wichtig wäre es, nach der Bindung von FGF-BP an andere FGF zu suchen. Da es bis jetzt keinen Antikörper gegen FGF-BP gibt und auch die Wellstein-Arbeitsgruppe, die seit 1994 mehrere Arbeiten zum FGF-BP veröffentlicht hat, noch kein modifiziertes, im Western-Blot detektierbares FGF-BP beschrieben hat, ist der experimentelle Nachweis einer solchen Bindung aber direkt, z.B. über Co-Immunopräzipitation, schwer zu führen. Das verminderte epitheliale Wachstum bei Zugabe von FGF10 und das verstärkte Absterben zumindest des Mesenchyms ohne FGFs, welches unter dem Einfluß von huFGF-BPhis(ISP)-Überstand beobachtet wurde, könnte durch die Bindung von FGF10 und anderer FGF an das FGF-BP hervorgerufen sein. Es sollte mit epithelialen Zellinien getestet werden, ob die Insektenzellüberstände die FGF10-induzierte Zellproliferation hemmen können. FGF10 scheint trotz seines Signalpeptids ähnlich wie FGF1 in verschiedenen Formen sowohl im Zytosol wie auch in der ECM lokalisiert zu sein (Beer et al., 1997). FGF9, das im Lungenepithel expremiert wird (Colvin et al., 1999), und das mesenchymale FGF7 werden hingegen effektiv als lösliche Proteine sekretiert (Giri et al., 1999; Panos et al., 1993). DISKUSSION 78 Es konnte in dieser Arbeit gezeigt werden, daß die Expression des FGF-BP in der frühen Embryonalentwicklung im Allgemeinen recht schwach ist, aber transient sehr stark sein kann. Am Tag E 9.5, bevor die Zellen des Neuroepithels des Hindbrains beginnen, FGF1 zu expremieren, wird hier kurzfristig viel FGF-BP synthetisiert. Offenbar ist hier die Aktivierung beider Gene über einen unbekannten Mechanismus miteinander gekoppelt. Die Ergebnisse der In-situ Hybridisierungen belegen, daß FGF-BP, FGF1 und FGF2 in vielen Geweben von älteren Embryonen co-expremiert werden. Die Expression des FGF-BP in der Lunge scheint mit der Hemmung des epithlialen Wachstums verbunden zu sein, wie auch die Hemmung des FGF1-induzierten Lungenwachstums durch Überstände von Insektenzellen, die ein mit einem spezifischen Insektensignalpeptid versehenes FGF-BP expremieren, nahelegt. Ob FGF-BP auch mit anderen FGF als FGF1 und FGF2 interagieren kann, muß offen bleiben und sollte zum Gegenstand nachfolgender Untersuchungen gemacht werden. ZUSAMMENFASSUNG 79 5 Zusammenfassung Im Rahmen dieser Arbeit konnten Daten zur Expression zweier FGF-bindender Proteine während der Embryogenese der Maus gesammelt werden, die es erlauben, Rückschlüsse auf die biologische Bedeutung dieser Proteine zu ziehen. Dazu wurden In-situ Hybridisierungen mit Gewebeschnitten von Embryonen der Entwicklungstage 13.5 bis 18, mit ganzen Embryonen der Entwicklungstage 7 bis 10.5 und mit ganzen Lungen der Entwicklungstage 10.5 bis 13.5 durchgeführt. Das nukleäre Bindungsprotein NoBP, das aufgrund seiner Bindung zu FGF3 identifiziert worden war, wurde ab E 8.0 in den Embryonen detektiert. Es wird hier v.a. in der Neuralleiste und in den Rhombomeren 1, 4 und 6 expremiert. In der Folgezeit nimmt die Expression dort ab. Zu E 10.5 hat sich der Schwerpunkt der Expression auf die Kiemenbögen und die dorsale Seite des Schwanzes verlagert. Im hinteren Gliedmaß wird NoBP spezifisch im proximalen Mesenchym gebildet. In der Lunge sind ausschließlich die mesenchymalen Zellen um die distalen Tubuli NoBP positiv. Auch hier nimmt die Expression in späteren Entwicklungsstadien ab. Damit wurde NoBP in drei verschiedenen Strukturen spezifisch entlang einer anterioren/posterioren Achse detektiert. Die Etablierung solcher Strukturen basiert in Vertebraten auf der Aktivität von Homeobox-Transkriptionsfaktoren, namentlich den Hox-Proteinen. Aufgrund der nukleären Lokalisation des NoBP, seiner Anwesenheit in schnell wachsenden Zellen der Zellkultur und der Lokalisation der Expression, die partiell der von Hoxb-2 und Hoxb-5 sehr ähnlich ist, wird die Hypothese aufgestellt, daß NoBP ähnlich wie die HoxProteine eine Funktion bei der Wachstumskontrolle unsymmetrischer Körperstrukturen hat. In den älteren Embryonen wurde NoBP in erster Linie in mesenchymalen Zellen, differenzierenden Osteoblasten, dem Epithel des Dünndarms und Gefäßepithel detektiert, ist also auch hier in schnell wachsenden Zellen anzutreffen. Das sekretierte Fibroblasten-Wachstumsfaktor-Bindungsprotein FGF-BP interagiert mit FGF1 mit hoher und mit FGF2 mit niedrigerer Affinität. Von FGF-BP gebundenes FGF kann den hochaffinen FGFR vermutlich nicht mehr effektiv aktivieren und muß zunächst durch die Interaktion mit spezifischen HSPGs oder Heparin freigesetzt werden. In den Hybridisierungsexperimenten konnte nachgewiesen werden, daß die FGF-BP mRNA etwa einen Tag, bevor das Neuroepithel des Hindbrains mit der Synthese von FGF1 beginnt, dort massiv hochreguliert wird und dieser Effekt weniger als 24 Stunden andauert. Offenbar ZUSAMMENFASSUNG 80 reagieren die Zellen auf die bevorstehende Expression des FGF1. Gleichzeitig ist auch die Expression in dem mesenchymalen corticalen Gewebe und dem Neuroepithel des optischen Vesikels stark erhöht. Zum Zeitpunkt E 10.5 wurde eine moderate Expression in dem distalen Part der Kiemenbögen, dem dorsalen Schwanzende und dem das Forebrain überlagernden mesenchymalen Gewebe detektiert. Konträr zu in der Literatur veröffentlichen Daten wurde zu E 16 die FGF-BP mRNA nicht nur in der Haut, der Lunge und dem Darm detektiert, sondern in vielen mesenchymalen Geweben. Die kräftigsten Signale wurden in dem Trigeminalganglion, den DRGs, dem Mesenchym der Lunge, dem Darmepithel und in differenzierenden Osteoblasten gefunden. Das Signal in der Haut wurde erst zu E 18 prominent. Weiterhin konnte gezeigt werden, daß das FGF-BP in der frühen E 11 Lunge expremiert wird, im Mesenchym seitlich der distalen Tubuli. Die Expressionsrate ist sehr niedrig und erst in E 13.5 Lungen, wenn die FGF1 Expression begonnen hat, konnte wieder ein eindeutiges Signal, in einer Zone direkt vor sich offenbar in zwei Wege teilenden Tubuli, detektiert werden. Offenbar ist die Expression des FGF-BP also mit der Aussendung eines antiproliferativen Signals an die Epithelzellen verknüpft. Um die antiproliferative Wirkung des FGF-BP in den Lungen in vitro zu testen, wurden Lungenorgankulturen angelegt und ein mit einem Insektensignalpeptid versehenes FGF-BP in Insektenzellen expremiert. Lungen, die in Anwesenheit des Überstandes dieser Zellen inkubiert wurden, entwickelten sich signifikant schlechter als solche, die mit Überstand von Zellen, die ein FGF-BP ohne Signalpeptid synthetisieren, gehalten wurden. Das galt in besonderem Maße, wenn das Medium mit FGF1 supplementiert wurde. Die hier präsentierten Daten zeigen, daß die FGF-BP Expression während der frühen Embryogenese recht spezifisch und möglicherweise an die Synthese von FGF1 gekoppelt ist. In älteren Embryonen ist FGF-BP weit verbreitet, genau wie FGF1. Im Konzert mit den hochaffinen FGFR und spezifischen HSPGs scheint FGF-BP an der Verteilung und Aktivierung/Deaktivierung von FGF1 entscheidend beteiligt zu sein. Von FGF18, dessen Sonde zur Kontrolle der Hybridisierungen eingesetzt wurde, war spekuliert worden, daß es an der Regulation der frühen Lungengenese beteiligt ist. Es konnte gezeigt werden, daß dies nicht zutrifft, weil FGF18 von E 11 bis E 12.5 nicht in der Lunge expremiert wird. LITERATUR 81 6 Literatur A Guide to the Bac-to-Bac Baculovirus Expression System. Life Technologies Procedures for Labeling DNA, RNA, and Oligonucleotides with DIG, Biotin, or Fluorochromes (1996), in: Nonradioactive In Situ Hybridization, Application Manual 2nd Edition, Boehringer Mannheim Acland, P., Dixon, M., Peters, G., und Dickson, C. (1990). Subcellular fate of the int-2 oncoprotein is determined by choice of initiation codon. Nature 343, 662-5. Barrow, J. R., und Capecchi, M. R. (1996). Targeted disruption of the Hoxb-2 locus in mice interferes with expression of Hoxb-1 and Hoxb-4. Development 122, 3817-28. Basilico, C., und Moscatelli, D. (1992). The FGF family of growth factors and oncogenes. Adv Cancer Res 59, 115-65. Baumgart, E., Schad, A., Volkl, A., und Fahimi, H. D. (1997). Detection of mRNAs encoding peroxisomal proteins by non-radioactive in situ hybridization with digoxigeninlabelled cRNAs. Histochem Cell Biol 108, 371-9. Beer, H. D., Florence, C., Dammeier, J., McGuire, L., Werner, S., und Duan, D. R. (1997). Mouse fibroblast growth factor 10: cDNA cloning, protein characterization, and regulation of mRNA expression. Oncogene 15, 2211-8. Bellusci, S., Furuta, Y., Rush, M. G., Henderson, R., Winnier, G., und Hogan, B. L. (1997a). Involvement of Sonic hedgehog (Shh) in mouse embryonic lung growth and morphogenesis. Development 124, 53-63. Bellusci, S., Grindley, J., Emoto, H., Itoh, N., und Hogan, B. L. (1997b). Fibroblast growth factor 10 (FGF10) and branching morphogenesis in the embryonic mouse lung. Development 124, 4867-78. Bellusci, S., Henderson, R., Winnier, G., Oikawa, T., und Hogan, B. L. (1996). Evidence from normal expression and targeted misexpression that bone morphogenetic protein (Bmp-4) plays a role in mouse embryonic lung morphogenesis. Development 122, 1693-702. Bogue, C. W., Lou, L. J., Vasavada, H., Wilson, C. M., und Jacobs, H. C. (1996). Expression of Hoxb genes in the developing mouse foregut and lung. Am J Respir Cell Mol Biol 15, 163-71. Brickman, Y. G., Ford, M. D., Gallagher, J. T., Nurcombe, V., Bartlett, P. F., und Turnbull, J. E. (1998). Structural modification of fibroblast growth factor-binding heparan sulfate at a determinative stage of neural development. J Biol Chem 273, 4350-9. Bucher, O. und Wartenberg, H.: Cytologie, Histologie und mikroskopischen Anatomie des Menschen (Nachdruck der 11., vollständig überarbeiteten Ausgabe von 1989, Verlag Hans Huber, Bern 1991) LITERATUR 82 Cardoso, W. V., Itoh, A., Nogawa, H., Mason, I., und Brody, J. S. (1997). FGF-1 and FGF-7 induce distinct patterns of growth and differentiation in embryonic lung epithelium. Dev Dyn 208, 398-405. Celli, G., LaRochelle, W. J., Mackem, S., Sharp, R., und Merlino, G. (1998). Soluble dominant-negative receptor uncovers essential roles for fibroblast growth factors in multi-organ induction and patterning. Embo J 17, 1642-55. Chan, D. C., Wynshaw-Boris, A., und Leder, P. (1995). Formin isoforms are differentially expressed in the mouse embryo and are required for normal expression of fgf-4 and shh in the limb bud. Development 121, 3151-62. Chariot, A., Gielen, J., Merville, M. P., und Bours, V. (1999). The homeodomain-containing proteins: an update on their interacting partners. Biochem Pharmacol 58, 1851-7. Colvin, J. S., Feldman, B., Nadeau, J. H., Goldfarb, M., und Ornitz, D. M. (1999). Genomic organization and embryonic expression of the mouse fibroblast growth factor 9 gene. Dev Dyn 216, 72-88. Conlon, R. A., und Herrmann, B. G. (1993). Detection of messenger RNA by in situ hybridization to postimplantation embryo whole mounts. Methods Enzymol 225, 37383. Coulier, F., Pontarotti, P., Roubin, R., Hartung, H., Goldfarb, M., und Birnbaum, D. (1997). Of worms and men: an evolutionary perspective on the fibroblast growth factor (FGF) and FGF receptor families. J Mol Evol 44, 43-56. Czubayko, F., Smith, R. V., Chung, H. C., und Wellstein, A. (1994). Tumor growth and angiogenesis induced by a secreted binding protein for fibroblast growth factors. J Biol Chem 269, 28243-8. David, G., van der Schueren, B., Marynen, P., Cassiman, J. J., und van den Berghe, H. (1992). Molecular cloning of amphiglycan, a novel integral membrane heparan sulfate proteoglycan expressed by epithelial and fibroblastic cells. J Cell Biol 118, 961-9. de Maximy, A. A., Nakatake, Y., Moncada, S., Itoh, N., Thiery, J. P., und Bellusci, S. (1999). Cloning and expression pattern of a mouse homologue of drosophila sprouty in the mouse embryo. Mech Dev 81, 213-6. De Moerlooze, L., Spencer-Dene, B., Revest, J., Hajihosseini, M., Rosewell, I., und Dickson, C. (2000). An important role for the IIIb isoform of fibroblast growth factor receptor 2 (FGFR2) in mesenchymal-epithelial signalling during mouse organogenesis. Development 127, 483-92. Dono, R., Texido, G., Dussel, R., Ehmke, H., und Zeller, R. (1998). Impaired cerebral cortex development and blood pressure regulation in FGF-2-deficient mice. Embo J 17, 4213-25. Esch, F., Baird, A., Ling, N., Ueno, N., Hill, F., Denoroy, L., Klepper, R., Gospodarowicz, D., Bohlen, P., und Guillemin, R. (1985). Primary structure of bovine pituitary basic fibroblast growth factor (FGF) and comparison with the amino-terminal sequence of bovine brain acidic FGF. Proc Natl Acad Sci U S A 82, 6507-11. LITERATUR 83 Ferry, R. J., Jr., Katz, L. E., Grimberg, A., Cohen, P., und Weinzimer, S. A. (1999). Cellular actions of insulin-like growth factor binding proteins. Horm Metab Res 31, 192-202. Fu, Y. M., Spirito, P., Yu, Z. X., Biro, S., Sasse, J., Lei, J., Ferrans, V. J., Epstein, S. E., und Casscells, W. (1991). Acidic fibroblast growth factor in the developing rat embryo. J Cell Biol 114, 1261-73. Gimenez-Gallego, G., Rodkey, J., Bennett, C., Rios-Candelore, M., DiSalvo, J., und Thomas, K. (1985). Brain-derived acidic fibroblast growth factor: complete amino acid sequence and homologies. Science 230, 1385-8. Giri, D., Ropiquet, F., und Ittmann, M. (1999). FGF9 is an autocrine and paracrine prostatic growth factor expressed by prostatic stromal cells. J Cell Physiol 180, 53-60. Gonzalez, A. M., Buscaglia, M., Ong, M., und Baird, A. (1990). Distribution of basic fibroblast growth factor in the 18-day rat fetus: localization in the basement membranes of diverse tissues. J Cell Biol 110, 753-65. Gospodarowicz, D., Jones, K. L., und Sato, G. (1974). Purification of a growth factor for ovarian cells from bovine pituitary glands. Proc Natl Acad Sci U S A 71, 2295-9. Guo, L., Degenstein, L., und Fuchs, E. (1996). Keratinocyte growth factor is required for hair development but not for wound healing. Genes Dev 10, 165-75. Hacohen, N., Kramer, S., Sutherland, D., Hiromi, Y., und Krasnow, M. A. (1998). sprouty encodes a novel antagonist of Fgf signaling that patterns apical branching of the Drosophila airways. Cell 92, 253-63. Hanahan, D. (1983). Studies on transformation of Escherichia coli with plasmids. J Mol Biol 166, 557-80. Harris, V. K., Coticchia, C. M., Kagan, B. L., Ahmad, S., Wellstein, A., und Riegel, A. T. (2000). Induction of the angiogenic modulator fibroblast growth factor-binding protein by epidermal growth factor is mediated through both MEK/ERK and p38 signal transduction pathways. J Biol Chem 275, 10802-11. Harris, V. K., Liaudet-Coopman, E. D., Boyle, B. J., Wellstein, A., und Riegel, A. T. (1998). Phorbol ester-induced transcription of a fibroblast growth factor-binding protein is modulated by a complex interplay of positive and negative regulatory promoter elements. J Biol Chem 273, 19130-9. Hecht, D., Zimmerman, N., Bedford, M., Avivi, A., und Yayon, A. (1995). Identification of fibroblast growth factor 9 (FGF9) as a high affinity, heparin dependent ligand for FGF receptors 3 and 2 but not for FGF receptors 1 and 4. Growth Factors 12, 223-33. Heukeshoven, J., und Dernick, R. (1985). Characterization of a solvent system for separation of water-insoluble poliovirus proteins by reversed-phase high-performance liquid chromatography. J Chromatogr 326, 91-101. Hogan, B. (1999). Morphogenesis. Cell 96, 225-33. Hogan, B. L., und Yingling, J. M. (1998). Epithelial/mesenchymal interactions and branching morphogenesis of the lung. Curr Opin Genet Dev 8, 481-6. LITERATUR 84 Holland, P. W., und Hogan, B. L. (1988). Spatially restricted patterns of expression of the homeobox-containing gene Hox 2.1. during mouse embryogenesis. Development 102, 159-74. Hu, M. C., Qiu, W. R., Wang, Y. P., Hill, D., Ring, B. D., Scully, S., Bolon, B., DeRose, M., Luethy, R., Simonet, W. S., Arakawa, T., und Danilenko, D. M. (1998). FGF-18, a novel member of the fibroblast growth factor family, stimulates hepatic and intestinal proliferation. Mol Cell Biol 18, 6063-74. Hunt, P., Whiting, J., Muchamore, I., Marshall, H., und Krumlauf, R. (1991). Homeobox genes and models for patterning the hindbrain and branchial arches. Dev Suppl 1, 18796. Igarashi, M., Finch, P. W., und Aaronson, S. A. (1998). Characterization of recombinant human fibroblast growth factor (FGF)-10 reveals functional similarities with keratinocyte growth factor (FGF-7). J Biol Chem 273, 13230-5. Irving, C., und Mason, I. (2000). Signalling by FGF8 from the isthmus patterns anterior hindbrain and establishes the anterior limit of Hox gene expression. Development 127, 177-86. Joy, A., Moffett, J., Neary, K., Mordechai, E., Stachowiak, E. K., Coons, S., Rankin-Shapiro, J., Florkiewicz, R. Z., und Stachowiak, M. K. (1997). Nuclear accumulation of FGF-2 is associated with proliferation of human astrocytes and glioma cells. Oncogene 14, 171-83. Jung, J., Zheng, M., Goldfarb, M., und Zaret, K. S. (1999). Initiation of mammalian liver development from endoderm by fibroblast growth factors. Science 284, 1998-2003. Kan, M., Wang, F., To, B., Gabriel, J. L., und McKeehan, W. L. (1996). Divalent cations and heparin/heparan sulfate cooperate to control assembly and activity of the fibroblast growth factor receptor complex. J Biol Chem 271, 26143-8. Kan, M., Wu, X., Wang, F., und McKeehan, W. L. (1999). Specificity for fibroblast growth factors determined by heparan sulfate in a binary complex with the receptor kinase. J Biol Chem 274, 15947-52. Kaufman, M. H.: The Atlas of Mouse Development (2. Auflage der revidierten Ausgabe von 1995, Academic Press, London 1998) Kiefer, P., und Dickson, C. (1995). Nucleolar association of fibroblast growth factor 3 via specific sequence motifs has inhibitory effects on cell growth. Mol Cell Biol 15, 436474. Klint, P., und Claesson-Welsh, L. (1999). Signal transduction by fibroblast growth factor receptors. Front Biosci 4, D165-77. Kramer, S., Okabe, M., Hacohen, N., Krasnow, M. A., und Hiromi, Y. (1999). Sprouty: a common antagonist of FGF and EGF signaling pathways in Drosophila. Development 126, 2515-25. LITERATUR 85 Kurtz, A., Wang, H. L., Darwiche, N., Harris, V., und Wellstein, A. (1997). Expression of a binding protein for FGF is associated with epithelial development and skin carcinogenesis. Oncogene 14, 2671-81. Laemmli, U. K. (1970). Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature 227, 680-5. Le Douarin, N. M., und Smith, J. (1988). Development of the peripheral nervous system from the neural crest. Annu Rev Cell Biol 4, 375-404. Lebeche, D., Malpel, S., und Cardoso, W. V. (1999). Fibroblast growth factor interactions in the developing lung. Mech Dev 86, 125-36. Lee, T., Hacohen, N., Krasnow, M., und Montell, D. J. (1996). Regulated Breathless receptor tyrosine kinase activity required to pattern cell migration and branching in the Drosophila tracheal system. Genes Dev 10, 2912-21. Lin, X., Buff, E. M., Perrimon, N., und Michelson, A. M. (1999). Heparan sulfate proteoglycans are essential for FGF receptor signaling during Drosophila embryonic development. Development 126, 3715-23. Litingtung, Y., Lei, L., Westphal, H., und Chiang, C. (1998). Sonic hedgehog is essential to foregut development [see comments]. Nat Genet 20, 58-61. Liu, M., Liu, J., Buch, S., Tanswell, A. K., und Post, M. (1995). Antisense oligonucleotides for PDGF-B and its receptor inhibit mechanical strain-induced fetal lung cell growth. Am J Physiol 269, L178-84. Lories, V., Cassiman, J. J., Van den Berghe, H., und David, G. (1989). Multiple distinct membrane heparan sulfate proteoglycans in human lung fibroblasts. J Biol Chem 264, 7009-16. Lories, V., Cassiman, J. J., Van den Berghe, H., und David, G. (1992). Differential expression of cell surface heparan sulfate proteoglycans in human mammary epithelial cells and lung fibroblasts. J Biol Chem 267, 1116-22. Lories, V., David, G., Cassiman, J. J., und Van den Berghe, H. (1986). Heparan sulfate proteoglycans of human lung fibroblasts. Occurrence of distinct membrane, matrix and secreted forms. Eur J Biochem 158, 351-9. Mahmood, R., Kiefer, P., Guthrie, S., Dickson, C., und Mason, I. (1995). Multiple roles for FGF-3 during cranial neural development in the chicken. Development 121, 1399-410. Mahmood, R., Mason, I. J., und Morriss-Kay, G. M. (1996). Expression of Fgf-3 in relation to hindbrain segmentation, otic pit position and pharyngeal arch morphology in normal and retinoic acid-exposed mouse embryos. Anat Embryol (Berl) 194, 13-22. Mansour, S. L., Goddard, J. M., und Capecchi, M. R. (1993). Mice homozygous for a targeted disruption of the proto-oncogene int-2 have developmental defects in the tail and inner ear. Development 117, 13-28. Martin, G. R. (1998). The roles of FGFs in the early development of vertebrate limbs. Genes Dev 12, 1571-86. LITERATUR 86 Maruoka, Y., Ohbayashi, N., Hoshikawa, M., Itoh, N., Hogan, B. L. M., und Furuta, Y. (1998). Comparison of the expression of three highly related genes, Fgf8, Fgf17 and Fgf18, in the mouse embryo. Mech Dev 74, 175-7. Mehta, V. B., Connors, L., Wang, H. C., und Chiu, I. M. (1998). Fibroblast variants nonresponsive to fibroblast growth factor 1 are defective in its nuclear translocation. J Biol Chem 273, 4197-205. Metzger, R. J., und Krasnow, M. A. (1999). Genetic control of branching morphogenesis. Science 284, 1635-9. Miller, D. L., Ortega, S., Bashayan, O., Basch, R., und Basilico, C. (2000). Compensation by fibroblast growth factor 1 (FGF1) does not account for the mild phenotypic defects observed in FGF2 null mice. Mol Cell Biol 20, 2260-8. Min, H., Danilenko, D. M., Scully, S. A., Bolon, B., Ring, B. D., Tarpley, J. E., DeRose, M., und Simonet, W. S. (1998). Fgf-10 is required for both limb and lung development and exhibits striking functional similarity to Drosophila branchless. Genes Dev 12, 315661. Minoo, P., Hamdan, H., Bu, D., Warburton, D., Stepanik, P., und deLemos, R. (1995). TTF-1 regulates lung epithelial morphogenesis. Dev Biol 172, 694-8. Minoo, P., Su, G., Drum, H., Bringas, P., und Kimura, S. (1999). Defects in tracheoesophageal and lung morphogenesis in Nkx2.1(-/-) mouse embryos. Dev Biol 209, 60-71. Minowada, G., Jarvis, L. A., Chi, C. L., Neubuser, A., Sun, X., Hacohen, N., Krasnow, M. A., und Martin, G. R. (1999). Vertebrate Sprouty genes are induced by FGF signaling and can cause chondrodysplasia when overexpressed. Development 126, 4465-75. Munoz-Sanjuan, I., Smallwood, P. M., und Nathans, J. (2000). Isoform diversity among fibroblast growth factor homologous factors is generated by alternative promoter usage and differential splicing. J Biol Chem 275, 2589-97. Nieto, M. A., Bradley, L. C., und Wilkinson, D. G. (1991). Conserved segmental expression of Krox-20 in the vertebrate hindbrain and its relationship to lineage restriction. Development Suppl 2, 59-62. Nogawa, H., und Ito, T. (1995). Branching morphogenesis of embryonic mouse lung epithelium in mesenchyme-free culture. Development 121, 1015-22. Nogawa, H., und Takahashi, Y. (1991). Substitution for mesenchyme by basementmembrane-like substratum and epidermal growth factor in inducing branching morphogenesis of mouse salivary epithelium. Development 112, 855-61. Nurcombe, V., Ford, M. D., Wildschut, J. A., und Bartlett, P. F. (1993). Developmental regulation of neural response to FGF-1 and FGF-2 by heparan sulfate proteoglycan. Science 260, 103-6. Ohbayashi, N., Hoshikawa, M., Kimura, S., Yamasaki, M., Fukui, S., und Itoh, N. (1998). Structure and expression of the mRNA encoding a novel fibroblast growth factor, FGF-18. J Biol Chem 273, 18161-4. LITERATUR 87 Ohmichi, H., Koshimizu, U., Matsumoto, K., und Nakamura, T. (1998). Hepatocyte growth factor (HGF) acts as a mesenchyme-derived morphogenic factor during fetal lung development. Development 125, 1315-24. Ohmichi, H., Matsumoto, K., und Nakamura, T. (1996). In vivo mitogenic action of HGF on lung epithelial cells: pulmotrophic role in lung regeneration. Am J Physiol 270, L10319. Ohuchi, H., und Noji, S. (1999). Fibroblast-growth-factor-induced additional limbs in the study of initiation of limb formation, limb identity, myogenesis, and innervation. Cell Tissue Res 296, 45-56. Ornitz, D. M. (2000). FGFs, heparan sulfate and FGFRs: complex interactions essential for development. Bioessays 22, 108-12. Ornitz, D. M., Xu, J., Colvin, J. S., McEwen, D. G., MacArthur, C. A., Coulier, F., Gao, G., und Goldfarb, M. (1996). Receptor specificity of the fibroblast growth factor family. J Biol Chem 271, 15292-7. Orr-Urtreger, A., Bedford, M. T., Burakova, T., Arman, E., Zimmer, Y., Yayon, A., Givol, D., und Lonai, P. (1993). Developmental localization of the splicing alternatives of fibroblast growth factor receptor-2 (FGFR2). Dev Biol 158, 475-86. Ozawa, K., Uruno, T., Miyakawa, K., Seo, M., und Imamura, T. (1996). Expression of the fibroblast growth factor family and their receptor family genes during mouse brain development. Brain Res Mol Brain Res 41, 279-88. Parisi, M. J., und Lin, H. (1998). The role of the hedgehog/patched signaling pathway in epithelial stem cell proliferation: from fly to human. Cell Res 8, 15-21. Park, W. Y., Miranda, B., Lebeche, D., Hashimoto, G., und Cardoso, W. V. (1998). FGF-10 is a chemotactic factor for distal epithelial buds during lung development. Dev Biol 201, 125-34. Peters, K., Werner, S., Liao, X., Wert, S., Whitsett, J., und Williams, L. (1994). Targeted expression of a dominant negative FGF receptor blocks branching morphogenesis and epithelial differentiation of the mouse lung. Embo J 13, 3296-301. Plotnikov, A. N., Schlessinger, J., Hubbard, S. R., und Mohammadi, M. (1999). Structural basis for FGF receptor dimerization and activation. Cell 98, 641-50. Post, M., Souza, P., Liu, J., Tseu, I., Wang, J., Kuliszewski, M., und Tanswell, A. K. (1996). Keratinocyte growth factor and its receptor are involved in regulating early lung branching. Development 122, 3107-15. Rancourt, D. E., Tsuzuki, T., und Capecchi, M. R. (1995). Genetic interaction between hoxb5 and hoxb-6 is revealed by nonallelic noncomplementation. Genes Dev 9, 108-22. Reich, A., Sapir, A., und Shilo, B. (1999). Sprouty is a general inhibitor of receptor tyrosine kinase signaling. Development 126, 4139-47. LITERATUR 88 Reimers-Fadhlaoui, K. (1999). Identifizierung von Bindungsproteinen des Fibroblast growth factor (FGF) 3 mit Hilfe der Hefe-Two-Hybrid-Methode. Dissertation an der RuhrUniversität Bochum Rice, D. P., Aberg, T., Chan, Y., Tang, Z., Kettunen, P. J., Pakarinen, L., Maxson, R. E., und Thesleff, I. (2000). Integration of FGF and TWIST in calvarial bone and suture development. Development 127, 1845-55. Rossel, M., und Capecchi, M. R. (1999). Mice mutant for both Hoxa1 and Hoxb1 show extensive remodeling of the hindbrain and defects in craniofacial development. Development 126, 5027-40. Roubin, R., Naert, K., Popovici, C., Vatcher, G., Coulier, F., Thierry-Mieg, J., Pontarotti, P., Birnbaum, D., Baillie, D., und Thierry-Mieg, D. (1999). let-756, a C. elegans fgf essential for worm development. Oncogene 18, 6741-7. Sambrook, J., Fritsch, E.F., und Maniatis, T. (1989). Molecular cloning- A laboratory manual 2nd edition. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York Sanger, F., Nicklen, S., und Coulson, A. R. (1977). DNA sequencing with chain-terminating inhibitors. Proc Natl Acad Sci U S A 74, 5463-7. Savage, M. P., und Fallon, J. F. (1995). FGF-2 mRNA and its antisense message are expressed in a developmentally specific manner in the chick limb bud and mesonephros. Dev Dyn 202, 343-53. Sekine, K., Ohuchi, H., Fujiwara, M., Yamasaki, M., Yoshizawa, T., Sato, T., Yagishita, N., Matsui, D., Koga, Y., Itoh, N., und Kato, S. (1999). Fgf10 is essential for limb and lung formation. Nat Genet 21, 138-41. Serra, R., Pelton, R. W., und Moses, H. L. (1994). TGF beta 1 inhibits branching morphogenesis and N-myc expression in lung bud organ cultures. Development 120, 2153-61. Shi, D. L., Fromentoux, V., Launay, C., Umbhauer, M., und Boucaut, J. C. (1994). Isolation and developmental expression of the amphibian homolog of the fibroblast growth factor receptor 3. J Cell Sci 107, 417-25. Simonet, W. S., DeRose, M. L., Bucay, N., Nguyen, H. Q., Wert, S. E., Zhou, L., Ulich, T. R., Thomason, A., Danilenko, D. M., und Whitsett, J. A. (1995). Pulmonary malformation in transgenic mice expressing human keratinocyte growth factor in the lung. Proc Natl Acad Sci U S A 92, 12461-5. Smallwood, P. M., Munoz-Sanjuan, I., Tong, P., Macke, J. P., Hendry, S. H., Gilbert, D. J., Copeland, N. G., Jenkins, N. A., und Nathans, J. (1996). Fibroblast growth factor (FGF) homologous factors: new members of the FGF family implicated in nervous system development. Proc Natl Acad Sci U S A 93, 9850-7. Souza, P., Sedlackova, L., Kuliszewski, M., Wang, J., Liu, J., Tseu, I., Liu, M., Tanswell, A. K., und Post, M. (1994). Antisense oligodeoxynucleotides targeting PDGF-B mRNA inhibit cell proliferation during embryonic rat lung development. Development 120, 2163-73. LITERATUR 89 Stachowiak, E. K., Maher, P. A., Tucholski, J., Mordechai, E., Joy, A., Moffett, J., Coons, S., und Stachowiak, M. K. (1997). Nuclear accumulation of fibroblast growth factor receptors in human glial cells--association with cell proliferation. Oncogene 14, 220111. Sutherland, D., Samakovlis, C., und Krasnow, M. A. (1996). branchless encodes a Drosophila Fgf homolog that controls tracheal cell migration and the pattern of branching. Cell 87, 1091-101. Szebenyi, G., und Fallon, J. F. (1999). Fibroblast growth factors as multifunctional signaling factors. Int Rev Cytol 185, 45-106. Tarozzo, G., Peretto, P., und Fasolo, A. (1995). Cell migration from the olfactory placode and the ontogeny of the neuroendocrine compartments. Zoolog Sci 12, 367-83. Tefft, J. D., Lee, M., Smith, S., Leinwand, M., Zhao, J., Bringas, P., Jr., Crowe, D. L., und Warburton, D. (1999). Conserved function of mSpry-2, a murine homolog of Drosophila sprouty, which negatively modulates respiratory organogenesis. Curr Biol 9, 219-22. Towbin, H., Ramjoue, H. P., Kuster, H., Liverani, D., und Gordon, J. (1982). Monoclonal antibodies against eucaryotic ribosomes. Use to characterize a ribosomal protein not previously identified and antigenically related to the acidic phosphoproteins P1/P2. J Biol Chem 257, 12709-15. Vieille-Grosjean, I., Hunt, P., Gulisano, M., Boncinelli, E., und Thorogood, P. (1997). Branchial HOX gene expression and human craniofacial development. Dev Biol 183, 49-60. Vlodavsky, I., Bar-Shavit, R., Ishai-Michaeli, R., Bashkin, P., und Fuks, Z. (1991). Extracellular sequestration and release of fibroblast growth factor: a regulatory mechanism? Trends Biochem Sci 16, 268-71. Wall, N. A., Jones, C. M., Hogan, B. L., und Wright, C. V. (1992). Expression and modification of Hox 2.1 protein in mouse embryos. Mech Dev 37, 111-20. Warburton, D., Schwarz, M., Tefft, D., Flores-Delgado, G., Anderson, K. D., und Cardoso, W. V. (2000). The molecular basis of lung morphogenesis. Mech Dev 92, 55-81. Wilkinson, D. G. (1993). Molecular mechanisms of segmental patterning in the vertebrate hindbrain and neural crest. Bioessays 15, 499-505. Wilkinson, D. G., Bhatt, S., Chavrier, P., Bravo, R., und Charnay, P. (1989a). Segmentspecific expression of a zinc-finger gene in the developing nervous system of the mouse. Nature 337, 461-4. Wilkinson, D. G., Bhatt, S., und McMahon, A. P. (1989b). Expression pattern of the FGFrelated proto-oncogene int-2 suggests multiple roles in fetal development. Development 105, 131-6. Wilkinson, D. G., und Nieto, M. A. (1993). Detection of messenger RNA by in situ hybridization to tissue sections and whole mounts. Methods Enzymol 225, 361-73. LITERATUR 90 Wu, D. Q., Kan, M. K., Sato, G. H., Okamoto, T., und Sato, J. D. (1991). Characterization and molecular cloning of a putative binding protein for heparin-binding growth factors. J Biol Chem 266, 16778-85. Xu, X., Weinstein, M., Li, C., und Deng, C. (1999). Fibroblast growth factor receptors (FGFRs) and their roles in limb development. Cell Tissue Res 296, 33-43. Yamasaki, M., Miyake, A., Tagashira, S., und Itoh, N. (1996). Structure and expression of the rat mRNA encoding a novel member of the fibroblast growth factor family. J Biol Chem 271, 15918-21. Zhou, D. J., Casey, G., Cline, M. J. (1988). Amplification of human int-2 in breast cancers and squamous carcinomas. Oncogene 2, 279-82 ANHANG 7 Anhang Sagittalschnitt durch ein E 15.5 Embryo aus Kaufman, The Atlas of Mouse Development 91 ANHANG 92 Lebenslauf Volker Blecken 11. Oktober 1971 geboren als Sohn der Industriekauffrau Johanne Blecken und des Tischlers Klaus Blecken in Stade 1977 bis 1981 Grundschule in Buxtehude-Hedendorf 1981 bis 1983 Orientierungsstufe im Schulzentrum Süd in Buxtehude 1983 bis 1987 Gymnasium im Schulzentrum Süd in Buxtehude 1987 bis 1990 Halepaghen-Gymnasium in Buxtehude 14. Mai 1990 Abitur Juli 1990 bis September 1991 Ableisten der Grundwehrdienstes 1991 bis 1996 Studium der Biochemie an der Ruhr-Universität Bochum Diplom-Arbeit: "Intrazelluläre Signaltransduktion von Neurotrophinen in kultivierten Neuronen des zentralen Nervensystems", angefertigt am Lehrstuhl für Molekulare Neurobiochemie (Leiter: Prof. Dr. R. Heumann) der RuhrUniversität Bochum 12. September 1996 Diplom in Biochemie Oktober 1996 bis Juni 2000 Promotion im Rahmen der Tätigkeit als wissenschaftlicher Mitarbeiter in der Abteilung für Medizinische Mikrobiologie und Virologie (Leiter: Prof. Dr. H. Werchau)