Das Immunsystem
Werbung

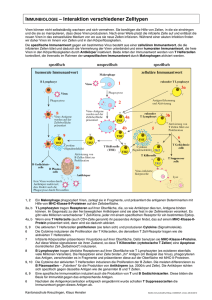
Das Immunsystem Vorlesung System-Biophysik 21. Jan. 2008 • Grundlagen nativ/adaptiv; humoral/zellulär • Klonale Selektionstheorie • Basis der Antikörpervielfalt • Die Jernesche Netzwerktheorie Künstliche Immunsysteme (AIS) Literatur Skript H. Gaub: Immunologie N.A. Campbell: Biologie Es gibt eine Vielfalt von „Krankheitserregern“ Phatogene: •Bakterien •Viren •Phatogene Pilze •Parasiten Ebola Virus Immunsystem & Systembiophysik Das Immunsystem verteidigt den Körper gegen Eindringlinge und falsch funktionierende Zellen Eigenschaften des Immunsystems • Mustererkennung (kognitiv) • Lernfähigkeit, anpassungsfähig (adaptiv) • Gedächtnis • kann zwischen „selbst“ und „fremd“ unterscheiden • robust, autonom • delokalisiert & vielschichtig Aufrechterhaltung des internen Körperzustandes (Homöostase) Das Immunsystem ist in seiner Funktion dem Nervensystem und dem endokrinen System verwandt: =>Psychoneuroimmunologie Early Attempts at Immunisation • Plagues & pandemics, esp. bubonic plague (Pasteurella pestis) & smallpox. • Thucydides (430 B.C.) observed people who recovered were protected from reinfection. • Causes of disease were unknown until 19th C. (Pasteur). Thought to be caused by poisons = “virus” (latin). • Mithridates VI (Roman King) took increasing daily doses of poisons. • Immunisation against Smallpox:– Chinese: dried matter from pustules on cotton inserted in nostrils. – Turks: used variolation, hence Variola Virus. History of Immunisation • 1798: Dr. Edward Jenner – Inoculated 7 subjects with cowpox. 2 challenged with smallpox. All O.K. – Cowpox = Vaccinia virus, hence vaccination ® general term. Edward Jenner inoculating James Phipps with cowpox • 1978: Smallpox completely eradicated worldwide. Abwehrsystem des Menschen Physikalische Barrieren (Haut, Haare, Schleim etc.) Biochemische Barrieren (Magensäure, Lysozme, etc.) Angeborene (innate) Immunsystem Phagozyten angeboren Granulozyten Neutrophils Eosinophils Erworbene (adaptive) Immunsystem Immunsystem Makrophagen Basophils erworben Lymphozyten Lymphozyten B-Zellen T-Zellen Leukozyten (weiße Blutzellen) Die Zellen des Immunsystems lassen sich in Phagozyten und Lymphozyten einteilen. Phagozyten sind unspezifische Freßzellen -Bei einer Invasion des Organismus mit Erregern sind diese Zellen die erste Stufe der Immunantwort. -Sie fressen die befallenen Zellen und mit ihnen einige Erreger auf und tragen dann Bruchstücke der fremden Moleküle in die Lymphknoten zu den hochspezifischen Lymphozyten, um diese auf die Gefahr aufmerksam zu machen. -Indem sie bestimmte Klassen von Antikörpern in ihre Membran aufnehmen, können sie sich dann im späteren Verlauf der Immunantwort multiple Spezifitäten aneignen: Makrophagen IgG Leukozyten IgE Mastzellen, Basophile IgE totes Gewebe (Viren) Bakterien Parasiten (Allergien) Makrophage, der nach einem Bakterium (Pfeil) "greift" Phagozyten sind der älteste Teil unseres Immunsystems; für die meisten Nichtvertebraten ist es die einzige Form der Abwehr. Das adaptive Immunsystem besteht aus 1012 Lymphozyten Lymphozyten sind eine Klasse der weißen Blutzellen, die in den lymphoiden Organen, Thymus und Knochenmark (gelb), hergestellt werden und im lymphoiden Gewebe (blau) verteilt werden. B: Knochenmark (bone marrow) T: Thymus B-Zellen : Antikörperproduktion THelfer : Stimulation und Regulation der B-Zellen TSuppressor : Unterdrückung der Autoimmunantwort TCytotoxisch : Direkte Bekämpfung von Erregern durch Lyse Neutral Killer Cells: Bekämpfung von Tumoren Lymphozyten sind die Träger der Immunität - Schlüsselexperiment - Der Verlust der Immunantwort durch Bestrahlung kann in Mäusen durch Injektion von Lymphozyten aus genetisch identischen Tieren wiederhergestellt werden. Die Zellen des Immunsystems Granulozyten Monozyten Lymphozyten platelets T-dth haemopoietic stem cell T-cytotoxic eosinophil megacariocyte T-helper neutrophil common myeloid progenitor basophil common lymphoid progenitor T-suppressor Mastzellen B cells mast cell plasma cell monocyte macrophage third population cells T und B-Lymphozyten Ruhende, immunkompetente B-Lymphozyten Aktivierte B-Lymphozyten sekretieren Antikörper Aktive T-Zellen zerstören infizierte Zellen site of inflammation tissue damage and immune reactions Die meisten Zellen des Immunsystems sind in der Lage, die Blutgefäße, in denen sie normalerweise zirkulieren, zu öffnen, um diese am Entzündungsherd zu verlassen Theories of Immunity: Humoral v. Cellular • Cellular Theory:- Elie Metchnikoff (Pasteur Inst.) – Phagocytes in starfish larvae surround a splinter; phagocytosis & digestion of bacteria by MFs & polymorphs ® Phagocytic Theory (innate immunity). – G.B. Shaw, “The Doctor’s Dilemma” – “Stimulate the phagocytes”. • Humoral Theory:- Koch, Ehrlich et al. (Berlin) – protection by soluble cmpnts. of blood. Showed serum from immunised animals kill bacteria. Nobel Prize in Physiology or Medicine to Metchnikoff & Ehrlich Die Immunantwort - das ganz grobe Bild B-Lymphozyten sezernieren Antikörper Die humorale oder Antikörper-Immunantwort beseitigt extrazelluläre Fremdkörper T-Lymphozyten zerstören infizierte Zellen Die zelluläre Immunantwort beseitigt in körpereigene Zellen eingedrungene Fremdlinge Die Immunantwort der Lymphozyten ist vernetzt Makrophagen sind Antigenpräsentierende Zellen (APC) und vermögen die passenden B-Lymphozyten zu aktivieren. Zellkommunikation T-Helfer Zellen stimulieren die B-Lymphozyten Der Antikörper Eine Substanz, die eine Immunantwort hervorrufen kann, nennt man Antigen (Antikörper-Generator). Antikörper sind Proteine und gehören als Stoffklasse zu den Immunoglobulinen (Ig). Sezernierte Antikörper Antikörper haben zwei identische, hochspezifische Antigen-Bindungsstellen Wie Antikörper arbeiten Opsonization Es gibt fünf Klassen von Antikörpern Die Immunglobuline unterscheiden sich in ihrer konstanten Fußregion, welche für die Effektorfunktion des Antikörpers zuständig ist. Früher Antikörper mit niedriger Affinität „Normaler“ & häufigster Antikörper Antikörper zur Neutralisation von Bakterien in Schleimhäuten B-Zell Oberflächenrezeptor Aktiviert Mastzellen und Basophile Ig-M sind die erste Klasse der während einer Immunreaktion synthetisierten Antikörper Die hohe Zahl an Bindungsstellen erhöht die Affinität (Avidität) von Ig-M um bis zu einem Faktor 104 gegenüber Ig-G. Dies ist besonders deshalb wichtig, weil die erste Klasse noch nicht so optimiert auf das Antigen ist, wie spätere Generationen Ig-E und Allergien Mast-Zellen sind auf die Parasitenbekämpfung spezialisiert. Eine Theorie darüber, warum in modernen Industriegesellschaften so viele Allergien auftauchen, besagt, daß dieser Teil des Immunsystems unterbeschäftigt ist und sich gegen harmlose Substanzen richtet. Antigen-Antikörper Erkennung V: variable C: constant Schlüssel-Schloß-Prinzip : Paratop-Epitop Die Bindungstasche (besteht je zur Hälfte aus den Ende der schweren und leichten Kette Die Struktur der Antikörper Die Affinität eines Antikörper k1 k1:Bindungsrate oder on-Rate. Einheit M-1 s-1 k"1 k-1:Dissoziationsrate oder off-Rate. Einheit s-1 A + B! AB d[ AB] dt = [ A][ B] ! k1 " [ AB] ! k"1 Die Affinitäts-Konstante : [ AB] =:K k1 = A k!1 [A][ B] Typische Antikörperaffinität: KA~104 - 1011 M-1 Dissoziationskonstante 1 k!1 K d := = K eq k1 Mehrere Antikörper können ein Antigen binden und ein Antikörper kann (leicht) unterschiedliche Antigene erkennen. (Kreuzreaktionen) Abschätzung der Antigen-Vielfalt Größe der antigenen Determinante (Epitop) : 10Åx20Åx20Å (Der Teil des fremden Proteins, der „erkannt“ wird) Ca. 109 verschiedene Moleküle sind so denkbar. Ähnliche Antigene binden den gleichen Antikörper (Reduktion um einen Faktor 100) Damit ergibt sich eine Zahl von 107 verschiedenen Antikörper. -> Es kann nicht für jeden Antikörper ein Gen vorliegen !! Wie schaffte es eine endliche Zahl von Zellen diese Zahl von Antigenen zu erkennen ? Die Genetische Basis der Antikörpervielfalt Schlüsselexperiment S. Tonegawa (Nobelpreis 1987) Die Keimbahn DNA hat Gruppen von Gensequenzen für die Kodierung der Ig-Ketten V: variable D: diversity J: junction C: constant Genetische Basis der Antikörpervielfalt Jede V-Region wird durch 3 Gensegmente (V,J,D) codiert Kombinatorische Vielfalt bei der Gen-Rekombination: Für die leichten Ketten stehen 300 V- Segmente und 4 JSegmente zur Verfügung (1200 Kombinationen) Für die schweren Ketten stehen 500 V- Segmente und 4 J-Segmente und 12 D-Segmente zur Verfügung (24000 Kombinationen) Gesamt ca. 1200x24000 ca. 3*107 Kombinationen Verknüpfungsvielfalt Der Verbindungsmechanismus arbeitet zusätzlich sehr “schlampig” (zusätzliche Nukleotide werden zufällig eingefügt oder welche weggelassen. Hypermutation Gesamte mögliche Vielfalt ca. 1015 PAUSE How are Antibodys made ? Selective v. Instructive Theories (20th C) Are Abs pre-made (selective) or “moulded” by ag (instructive)? Historical introduction • • • • Ehrlich’s Side Chain Theory (selective) Pauling - Instructive Theory Landsteiner: Specificity & diversity; blood group ags. Abs as proteins Porter & Edelman: 1st Description of structure of IgG, Nobel Prize (1972) • Köhler & Milstein: Monoclonal Abs • Sir MacFarlane Burnet – Clonal Selection Theory. • Niels Jerne – Selection of preformed Abs.; Network Theory Köhler, Milstein & Jerne shared Nobel Prize (1984) Klonale Selektionstheorie Annahmen: 1. Die Population der Lymphozyten besteht aus Untergruppen identischer Zellen (Klone), die je Klon nur für ein Antigen zuständig sind. 2. Klone gegen eigene Moleküle wurden in frühen Entwicklungsstadien ausgemerzt oder sind unterdrückt. 3. Die Diversität wird durch Genrekombination in der Entwicklungsphase erzeugt. Schlüsselexperimente zur klonalen Selektionstheorie Zu jedem beliebigen Antigen (Fremdkörper) existiert bereits ein Klon von Zellen, die im Fall der Immunantwort aktiviert werden. Die Population der Lymphozyten besteht aus Untergruppen identischer Zellen (Klone), die je Klon nur für ein Antigen zuständig sind. 2. Schlüsselexperimente zur Klonalen Selektionstheorie Klone gegen eigene Moleküle wurden in frühen Entwicklungsstadien ausgemerzt oder sind unterdrückt. Klonale Selektion Fremde Antigene Self-Antigen Klonale Expansion Klonale Ignoranz Unberührte Zelle Negative Selektion Klonale Löschung Zelltod ODER Rezeptor-Edition Klonale Expansion + Affinitätsreifung führt zu schneller Adaption von B-Zellen durch Evolutionsprozess Affinitäts-Reifeprozess Die B-Zellen durchlaufen eine “immunologischen Mikroevolution” Die Affinitätskonstante nimmt im Laufe der Immunantwort zu Die Jernsche Netzwerktheorie (Jerne, 1974) Niels Jerne Die Jernsche Netzwerktheorie (Jerne, 1974) * Die Immunantwort wird durch ein zelluläres Netzwerk dargestellt * Immun-Netzwerk ist ein dynamischer Zustand (d.h. auch ohne äußere Reize ständiges Bilden und Vernichten von Zellen) • Gegenseitiges Erkennen von Antikörpern/B Zellen durch Idiotope =>„idiotyp-Netzwerk“ * Erzeugt immunologisches Gedächtnis Suppression Negativeresponse Paratope Ag 1 2 Idiotope 3 Antibody Activation Positiveresponse Die Netzwerk-Theorie der Immunreaktion Ein Antigen Ag X (mit einer Determinanten) stimuliert die Synthese eines Antikörpers Ab1 (den sog. Idiotyp), der seinerseits antigene Wirkung zeigt und einen zweiten Klon zur Produktion eines Antikörpers Ab2 (den sog. AntiIdiotyp) anregt, der zu Ab1 komplementär ist. Ab2 stimuliert dann Ab3 usw. Schematische Darstellung eines verzweigten Immunnetzwerkes. Abn+1 TH-Zellen Abn Ab3 Ab2 T-Zellen Ab1 Ab1 Ag-X Ab1 B-Zellen Ein mathematische Modell des Immun-Netzwerks (Richter, Hoffmann et al.) Im Folgenden bezeichnen die Spezien Xi die Zahl der Lymphozyten des Klons bzw. die Konzentration der dazugehörigen Antikörper Abi. Das zeitliche Verhalten der Lymphozytenpopulation ist durch eine Evolutionsgleichung beschrieben: dx i = [bi ! di ]X i dt Die Rückkopplungsmechanismen !1 $ bi = # & f b (Xi '1 , Xi , X i+1 ); "Tb % di = !1 $ f X ,X ,X #" Td &% d ( i '1 i i +1 ) bi „birthrate“ di : „death-rate“ Die Rückkopplungsmechanismen 1Die Unterdrückung (Suppression) der Spezies i durch den anti-Idiotyp (i+1): Dieser Prozeß basiert auf einer Zerstörung der Lymphozytenpopulation Abi durch Zellen des Klons i+1. Die Funktion könnte durch Killer-Zellen erfüllt werden. Die Pufferung durch Ab-Ab-Wechselwirkung. Bei einer hohen Konzentration an Abi im Serum binden diese an die Spezies Abi-1 und Abi+1 und reduzieren so die Zahl der für die Kopplung mit Abi-Lymphozyten zur Verfügung stehenden Antikörper. Die Hemmung (I) der Stimulation der Abi-Produktion durch die Spezies Abi-1. Dieser Prozeß basiert auf einer Besetzung der Rezeptoren Abi durch Abi+1. Er spielt jedoch keine Rolle gegenüber einer anderen Hemmung (II), welche die Unterdrückung von Abi durch Abi+1 reduziert. Ursache dafür ist Unterdrückung des Unterdrückers Abi+1 durch Abi+2. Diese Hemmung hat jedoch propagierende Wirkung. Die Lymphozyten Abi+2 spielen somit die Rolle von TH-Zellen. Implementierung von Schwellwertverhalten und Rückkopplung 1 '% ' Bi $ "" bi = 1 + %% Tb % & X i !1 # & m $ " " # !1 1 '% ' Di $ "" di = 1 + %% Tb % & X i +1 # & m $ " " # !1 m bestimmt die Steilheit der Schwelle, Bi und Di die Schwellenwerte Stabile Lösungen erfordern Di>Bi #1 Bi = B0 [1+ X i+1 ] [1+ "X i+1 ] [1+ $X i ] #1 Di = D0 [1+ X i+1 ] [1+ "X i+1 ] [1+ $X i ] ! ! Der Term (1 + βXi-1)-1 berücksichtigt die Hemmung Ergebnis des Modells: 1. Die Niedrigzonen-Toleranz (Low-Zone-Tolerance, LZT) Time Das Antigen stimuliert die Spezies Ab1, dessen Konzentration zunimmt. Nach Überschreiten der Schwellkonzentration der Spezies Ab2 wird diese aktiviert. Gleichzeitig wird Ab1 unterdrückt, d.h. [Ab1] −> 0. Ergebnis des Modells: 2. Die normale Immunantwort Die Unterdrückung der Ab1 durch Ab2 wird (durch Bindung von AgX an Ab1) soweit gehemmt, daß die Unterdrücker Ab2 durch Ab3 selbst eliminiert werden. Auch spätere Zugaben von AgX werden durch Ab1 (B-Zellen) leicht eliminiert. Ergebnis des Modells: 3. Die Hochzonen-Toleranz (High-Zone-Tolerance = HZT) Wie die Abbildung zeigt, toleriert das Immunsystem eine hohe Konzentration Ax durch Elimination der B-Zellen. Der Grund für diese Toleranz ist die Elimination der "Helfer-Zellen" Ab3 durch deren Aggressoren Ab4: Die Ereigniskette endet mit der Stufe 4. Das Immunsystem besitzt ein Gedächtnis Die Immunantwort auf eine zweite Begegnung mit dem Antigen A ist stärker und schneller als die erste. Primäre und Sekundäre Immunantwort Die Unterscheidung von „Selbst“ und „Fremd“ Das Unvermögen gegen Selbst-Antigene zu reagieren, beruht auf erworbener immunologischer Toleranz. Es gibt zwei Arten von molekularen „Markern“ (membranständige Glykoproteine) = Haupthistokompatibilitätskomplex (MHC, mayor histocompatibility complex) MHC-Klasse-I Auf allen körpereigenen Zellen MHC-Klasse-II Auf Zellen des Immunsystems MHC-I Moleküle aktivieren TC-Zellen und finden sich auf jeder Körperzelle MHC-II Moleküle aktivieren TH -Zellen und finden sich nur auf speziellen Immunzellen, wie Makrophagen und B-Zellen. Aktivierung der T-Helferzellen Wirkungsweise der cytotoxischen Zellen Cytotoxische T-Zelle zerstört einen Eindringling Überblick zum synergistischen Zusammenwirken der Zellen des Immunsystems Die immunologische „Synapse“ der T-Zellen Wie präsentiert der MHC I Komplex das im Zellinneren synthetisierte Protein an der Zelloberfläche? Exkurs: Das Proteasom Wolfgang Baumeister 30% aller neu synthetisierten Proteine sind fehlerhaft und werden sofort wieder im Proteasom degradiert. Zusammenfassung Das Immunsystem ist ein sehr komplexer Abwehrmechanismus, der in einer ständigen Wechselwirkung mit mit dem gesamten Organismus steht Angeborenes IS (Phagozyten) und adaptives IS (B- und T-Lymphozyten) Eigenschaften adaptiven IS durch klonale Selektion • spezialisiert durch Antikörper/Selektion • vielfältig durch genetische Antikörpervielfalt • Gedächnis • Selbst-Fremd Erkennung (T-Zellen) Die Jernsche Netzwerktheorie beschreibt die Dynamik der Lymphozyten Population