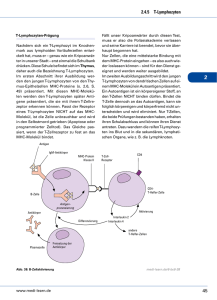
Membrankontakte von T-Lymphozyten mit dendritischen Zellen in
Werbung

Aus der Abteilung für Funktionelle und Angewandte Anatomie und aus dem Institut für Versuchstierkunde der Medizinischen Hochschule Hannover Membrankontakte von T-Lymphozyten mit dendritischen Zellen in den sekundär lymphatischen Organen der Ratte INAUGURAL-DISSERTATION zur Erlangung des Grades einer DOKTORIN DER VETERINÄRMEDIZIN durch die Tierärztliche Hochschule Hannover Vorgelegt von Andrea Sahle aus Münster/ Westf. Hannover 2001 II Wissenschaftliche Betreuung: Univ.-Prof. Dr. J. Westermann Univ.-Prof. Dr. R. Pabst 1. Gutachter: Univ.-Prof. Dr. H.- J. Hedrich 2. Gutachter: PD Dr. H.- J. Schuberth Tag der mündlichen Prüfung:30.05.2001 Diese Arbeit wurde mit der finanziellen Unterstützung des Graduierten Kollegs „Charakterisierung von regulatorischen Peptiden und ihrer Zielproteine“ angefertigt. III Meiner Mutter und meinem Sonnenschein Y a na -Ma r ie Man sieht nur mit dem Herzen gut, das Wesentliche ist für die Augen unsichtbar. Antoine de Saint-Exupery IV Inhaltsverzeichnis Verzeichnis der verwendeten Abkürzungen................................................... 7 I. Einleitung........................................................................................................ 9 II. Literaturübersicht...................................................................................... 11 1. Das Immunsystem....................................................................................................... 11 2. Die lymphatischen Organe.......................................................................................... 14 3. Aktivierungsstadien von T-Lymphozyten im Laufe einer Immunantwort ................. 18 4. Die Migration von Lymphozyten................................................................................ 21 5. Antigenpräsentation oder: die Kontrolle der Immunantwort...................................... 24 III. Material und Methoden ........................................................................... 31 1. Geräte und Laborbedarf.............................................................................................. 31 2. Puffer, Medien und Materialien ................................................................................. 32 3. Antikörper .................................................................................................................. 35 4. Versuchstiere.............................................................................................................. 37 5. Gewinnung, Aufbereitung und Injektion von Subpopulationen der Lymphozyten ... 38 6. Darstellung der Membrankontakte auf immunhistologisch gefärbten Gewebeschnitten ................................................................................................................................... 40 7. Immunhistologisch gefärbte Gewebeschnitte in der konfokalen Mikroskopie.......... 45 8. Darstellung von Membrankontakten zwischen T-Lymphozyten und IDC im Mausmodell ............................................................................................................... 46 9. Auswertung ................................................................................................................ 48 10. Verwendete Computerprogramme und Statistik ...................................................... 50 IV. Ergebnisse .................................................................................................. 52 A. Untersuchung der Membrankontakte von T-Lymphozyten mit interdigitierenden dendritischen Zellen in den sekundär lymphatischen Organen der Ratte........................................................................................... 52 1. Injizierte T-Lymphozyten und interdigitierende dendritische Zellen können auf immunhistologisch gefärbten Gewebeschnitten identifiziert werden. ...................... 52 6 2. In den sekundär lymphatischen Organen befinden sich 80% der injizierten TLymphozyten in Membrankontakt mit interdigitierenden dendritischen Zellen. ...... 55 3. Zu verschiedenen Zeitpunkten nach der Injektion der T-Lymphozyten lassen sich gleiche Anteile von Membrankontakten beobachten. ............................................... 57 4. Endogene T-Lymphozyten zeigen über 60% Membrankontakte zu DC.................... 60 5. Membrankontakte zu IgD-positiven B-Lymphozyten befinden sich vorwiegend im äußeren Bereich der periarteriolären lymphatischen Begleitscheide der Milz .......... 60 6. Membrankontakte von injizierten T-Lymphozyten mit dendritischen Zellen lassen sich auch mit konfokaler Mikroskopie aufzeigen. .................................................... 63 7. In der Maus werden interdigitierende dendritische Zellen über den spezifischen Marker DEC-205 nachgewiesen................................................................................ 67 B. Effektor T-Lymphozyten in Zellzyklus und Proliferation ..................... 70 1. Ki-67+ T-Lymphozyten im Blut ................................................................................. 70 2. BrdU+ T-Lymphozyten in der Milz ............................................................................ 72 3. Die Anteile der Ki-67+ und BrdU+ T-Lymphozyten sind erhöht zu finden, wenn Membrankontakte mit IDC in der Milz vorliegen..................................................... 72 V. Diskussion.................................................................................................... 80 1. Membrankontakte zwischen T-Lymphozyten und IDC stellen ein konstantes Phänomen dar. ........................................................................................................... 80 2. Funktion von LFA-1 bei Membrankontakten im Mausmodell .................................. 88 3. Membrankontakte beeinflussen den Anteil der Ki-67+ und BrdU+ T-Lymphozyten. 88 VI. Zusammenfassung..................................................................................... 92 VII. Summary .................................................................................................. 95 VIII. Literaturverzeichnis .............................................................................. 97 IX. Anhang ..................................................................................................... 117 7 Verzeichnis der verwendeten Abkürzungen Abb. AP APAAP APC Abbildung Alkalische Phosphatase Alkalische Phosphatase-Anti-Alkalische Phosphatase antigen presentating cell, Antigen-präsentierende Zelle BrdU BSA 5’-Brom 2’-Desoxyuridin bovines Serumalbumin ca. CD CO2 CSFE CTLA-4 circa Cluster of Differentiation, Differenzierungskluster Kohlendioxid 5-,6-carboxyfluorescein diacetat succinimidyl ester cytotoxic T lymphocyte antigen-4, zytotoxisches T-Zellantigen-4 DC Dig d.h. DMSO DNS dendritic cell, dendritische Zelle Digoxigenin das heißt Dimethylsulfoxid Desoxyribonukleinsäure etc. et cetera FACS fluorescence activated cell sorter, fluoreszenzaktivierter Zellsortierer fetal calf serum, fetales Kälberserum FCS GM-CSF Granulocyte/ Macrophage-colony-stimulating factor, Granulozyten/ Makrophagen-Kolonie-stimulierender Faktor h HEV hora, Stunde high endothelial venule, hochendotheliale Venule ICAM-1 IDC Ig IL- 2 i.v. intercellular adhesion molecule-1, interzelluläres Zelladhäsionsmolekül-1 interdigitating dendritic cell, interdigitierende dendritische Zelle Immunglobulin Interleukin-2 intravenös Ko Kontrolle LFA-1 Lymphocyte function-associated antigen-1, lymphozytenfunktionsassoziiertes Antigen-1 mAb MAdCAM-1 monoclonal antibody, monoklonaler Antikörper mucosal addressin-cell adhesion molecule-1, mukosales Addressin-Zelladhäsionsmolekül-1 8 MCP Min MIP1-α MHC mLN macrophage chemotactic protein, Makrophagen chemotaktisches Protein macrophage colony-stimulating factor, Makrophagen Kolonie-stimulierender Faktor Molecular Institute of Borstel, Antikörper gegen nukleäres Antigen des Zellzyklus (in der Ratte während der G1-M2-Phase exprimiert) Minute macrophage inflammatory protein 1-alpha Major histocompatibility complex, Haupthistokompatibilitätskomplex mesenterial lymph node, mesenterialer Lymphknoten MLR mixed lymphocyte reaction, gemischte Lymphozytenreaktion MS Mäuseserum NaCl NK-Zelle Natriumchlorid Natürliche Killerzelle PALS periarteriolar lymphatic sheath, periarterioläre lymphatische Begleitscheide Peroxidase-Anti-Peroxidase Phosphat-gepufferte Salzlösung Phycoerythrin Paraformaldehyd negativer Logarithmus der Wasserstoffionenkonzentration Peyersche Platten M-CSF Mib5 PAP PBS PE PFA pH PP RANTES RT regulated on activation, normally T cell expressed and secreted, durch Aktivierung reguliertes, normalerweise von T-Zellen exprimiertes und sezerniertes Chemokin Raumtemperatur s. S. sec SPF siehe Seite Sekunde spezifisch pathogenfrei TH1/2 TDL TNF-α TTBS TCR T-Helfer1/ 2 thoracic duct lymphocytes, Lymphozyten aus dem Ductus thoracicus tumor necrosis factor-alpha Trisgepufferte Salzlösung mit Tween T cell receptor, T-Zellrezeptor VCAM-1 VLA-4 vascular cell adhesion molecule-1, vaskuläres Zelladhäsionsmolekül-1 very late antigen-4, sehr spätes Antigen-4 z.B. zum Beispiel 9 I. Einleitung Das Immunsystem beschäftigt sich tagtäglich mit der Abwehr möglicher Pathogene. Im Laufe der Evolution haben sich dabei eine angeborene und eine erworbene Immunabwehr entwickelt, die ineinandergreifend effektiv den Organismus zu schützen imstande sind. TLymphozyten und B-Lymphozyten als Träger der erworbenen Immunabwehr erkennen über spezialisierte Rezeptoren Antigene. Um eine T-Zellabhängige Immunantwort auszulösen, benötigen T-Lymphozyten ihr spezifisches, in Peptide „zerlegtes“ (prozessiertes) Antigen, das mit dem Hauptgewebeverträglichkeitskomplex (MHC) zusammen präsentiert werden muss. Da sich Immunantworten auch gegen das eigene Gewebe richten können (Autoimmunität), müssen sie reguliert werden (VAN PARIJS u. ABBAS, 1998). In verschiedenen Modellen konnte gezeigt werden, wie wichtig die Interaktion zwischen T-Lymphozyten, aber auch BLymphozyten mit dendritischen Zellen (DC) für die Auslösung von Immunantworten, die Induktion und das Aufrechterhalten von peripherer Toleranz (BANCHEREAU u. STEINMAN, 1998) und das Überleben der Lymphozyten in den peripheren Geweben ist (BROCKER, 1997; INGULLI et al., 1997). In den sekundär lymphatischen Organen wird durch die spezialisierte Einteilung in Kompartimente das Zusammentreffen von Antigenen aus dem Blut oder den Geweben und der T-Lymphozyten und DC ermöglicht. Interdigitierende dendritische Zellen (IDC) stellen DC eines reifen Phänotyps (Fähigkeit zur Auslösung primärer T-Zellabhängiger Immunantworten) dar, die sich in den T-Zellarealen der sekundär lymphatischen Organe befinden und mit ihrer charakteristischen Morphologie mit zahlreichen dendritischen Ausläufern ein dichtes Netzwerk ausbilden. Durch eine hohe Expression von MHC Klasse II und kostimulatorischen Molekülen lassen sich diese Zellen in den Geweben nachweisen (STEINMAN et al., 1997). Obwohl der Interaktion zwischen T-Lymphozyten und DC verschiedene wichtige Funktionen bei der Einleitung und Regulierung von Immunantworten zugeschrieben wird, ist nicht bekannt, in welchem Ausmaß sich die Zellen in einem in vivo Modell in Kontakt zueinander befinden. Um diese Interaktion besser verstehen zu lernen, wurden in der vorliegenden Arbeit durch die Auswertung von Immunhistologien nach Injektion von T-Lymphozyten in einem kongenen Rattenmodell folgende Aspekte untersucht: 10 - Welcher Anteil von injizierten kongenen T-Lymphozyten befindet sich in Membrankontakt zu IDC in den T-Zellarealen der Milz, der mesenterialen Lymphknoten und der Peyerschen Platten? - Haben die verschiedenen Aktivierungsstadien (naive, Effektor und „Gedächtnis“T-Lymphozyten) der T-Lymphozyten einen Einfluss auf die Anzahl der Kontakte? - Lassen sich die Membrankontakte mittels weitergehender Techniken (konfokaler Mikroskopie) nachweisen? - Welchen Anteil von Membrankontakten zwischen T-Lymphozyten und dendritische Zellen lassen sich in der Maus mit einem spezifischen Marker für dendritische Zellen feststellen? - Welchen Einfluss hat eine LFA-1-Defizienz der T-Lymphozyten auf die Membrankontakte? - Welchen Einfluss haben immunhistologisch nachgewiesene Membrankontakte auf den Zellzyklus oder den Einbau von BrdU während der S-Phase des Zellzyklus für die T-Lymphozyten? 11 II. Literaturübersicht 1. Das Immunsystem Jeder Organismus muss tagtäglich gegenüber einer Vielzahl von Mikroorganismen und anderen Substanzen geschützt werden. Im Laufe der Evolution haben sich verschiedene Mechanismen entwickelt, die der effektiven Abwehr dienen. Die Aufgabe des Immunsystems ist es, die Integrität des Körpers gegen das Eindringen dieser Fremdstoffe von außen zu gewährleisten. Diese Abwehrreaktionen des Organismus gegen Pathogene werden einerseits durch die unspezifische (angeborene) und durch die spezifische (erworbene) Abwehr vermittelt (JANEWAY et al., 1999). Diese komplexen Vorgänge werden hier allerdings nur vereinfacht dargestellt. Die erste Verteidigungslinie gegen Infektionen ist die unspezifische Immunität, die direkt Effektorfunktionen zur Bekämpfung der Pathogene einleitet. Physikalisch-chemische Barrieren wie der natürliche Säuremantel der Haut und den Epithelien der Schleimhäute reduzieren ein Eindringen von fremden Substanzen bereits auf ein Minimum. Daneben haben Granulozyten und Makrophagen die Aufgabe, schnell alle eingedrungenen Erreger zu beseitigen. Makrophagen gehören zu einer Familie von langlebigen Zellen, die in fast allen Geweben verteilt sind und ein frühes Warnsystem gegenüber dem Eindringen exogener Agentien darstellen. Lösliche, zirkulierende Moleküle wie die Komplementfaktoren sind in der Lage, sich an Mikroorganismen anzuheften und zu einer verbesserten Erkennung und Phagozytose (Aufnahme von Fremdstoffen und Bakterien) zu führen (Opsonisierung) (GORDON, 1999). Natürliche Killerzellen (NK-Zellen) nehmen eine Zwischenstufe zwischen der unspezifischen und spezifischen Immunität ein, da sie einerseits Virus-infizierte Zellen aufspüren und eliminieren können, obwohl ihnen andrerseits Antigen-spezifische Rezeptoren fehlen. Die Verteidigungsstrategien der unspezifischen Immunität laufen stets gleichartig ab und sind unabhängig von einem vorherigen Kontakt mit den Erregern. Wenn diese Abwehr durchbrochen wird, ist die spezifische Immunität gefordert, die sich mit der Höherentwicklung der Wirbeltiere etabliert hat und vorwiegend von T- und B-Lymphozyten vermittelt wird. Die Spezifität der Antigen-spezifischen Antwort ergibt sich aus dem 12 Repertoire von Antigenrezeptoren, die von den T- und B-Lymphozyten exprimiert werden. Jeder individuelle T- oder B-Lymphozyt trägt Antigenrezeptoren auf seiner Zelloberfläche, die in einzigartiger Weise fähig sind, spezifische Strukturdeterminanten (Epitope) oder Antigen zu erkennen. Die Verschiedenheit (Diversität) der Antigenrezeptoren wird durch eine kombinatorische Neuordnung einer Varietät von Immunglobulin- oder T-ZellrezeptorGensegmenten und somatischer Mutation gewährleistet. Dieses breit angelegte Immunrepertoire erlaubt der Lymphozytenpopulation, auf jedes virtuelle, potentiell pathogene Agens reagieren zu können. Die selektive Vermehrung eines Lymphozytenklons, die durch ein Antigen hervorgerufen wird, ermöglicht es dem Immunsystem, die Immunantwort an häufig vorkommende Pathogene anzupassen und ein immunologisches Gedächtnis zu entwickeln. Durch eine erhöhte Frequenz von Antigen-spezifischen Lymphozyten und eine erhöhte Sensibilität gegenüber dem Antigen können die sogenannten „memory“ Lymphozyten bei erneutem Eindringen des Antigens schneller reagieren. Zusätzlich werden durch die spezifische Immunabwehr auch die Schutzmechanismen der unspezifischen Abwehr verstärkt, indem z.B. durch Botenstoffe (Zytokine, Chemokine) Phagozyten an den Ort der Entzündung gelockt werden können, die bei der Eliminierung der Fremdstoffe unterstützend wirken (HALE u. HAYNES, 1999). B-Lymphozyten sind die Vorläufer von Antikörper-sezernierenden Plasmazellen, die eine humorale Immunität vermitteln. Antikörper haften an eingedrungenen Antigenen, aktivieren das Komplementsystem und führen zur verbesserten Aufnahme durch Makrophagen. Besonders Bakterien und deren Toxine, die sich im extrazellulären Raum befinden, werden durch diesen Mechanismus eliminiert. T-Lymphozyten vermitteln hingegen die Antigen-spezifische zelluläre Immunität und regulieren gleichzeitig auch die Funktion der B-Lymphozyten und Makrophagen durch zelluläre Interaktionen und die Produktion von Zytokinen. Die Wichtigkeit der T- und B-Lymphozyten zur allgemeinen Funktion des Immunsystems wird durch die Vielzahl der infektiösen Erkrankungen reflektiert, die bei einer verminderten Anzahl oder dem Fehlen dieser Zellen eintreten (z.B. kongenitale Immundefizienz, Infektion mit dem humanen Immundefizienz Virus, HIV) (HALE u. HAYNES, 1999; JANEWAY et al., 1999). 13 Der T-Zellrezeptor erkennt keine strukturellen Determinanten oder Epitope in ihrer nativen Form. Stattdessen erkennen T-Lymphozyten proteolytisch zerteilte Peptidfragmente des Antigens, die an den polymorphen Anteil der Moleküle des Hauptgewebeverträglichkeitskomplexes (major histocompatibility complex, MHC) auf der Oberfläche einer Antigen-präsentierenden Zelle gebunden sind. Der Prozess, durch den Antigene in Peptide abgebaut und an die MHC-Moleküle gebunden werden, wird als Antigenprozessierung bezeichnet. Dabei existieren spezialisierte Abbauwege für Antigene, die aus dem extra- oder intrazellulären Raum stammen. Extrazelluläre Antigene wie Bakterien und Viren werden durch Antigen-präsentierende Zellen aufgenommen, nach ihrem Abbau an Moleküle des MHC Klasse II gebunden, auf der Oberfläche exprimiert und von CD4+ T-Lymphozyten erkannt. CD4+ T-Lymphozyten werden auch als T-Helferzellen bezeichnet, da sie durch direkte Zellinteraktionen und die Ausschüttung von Zytokinen Makrophagen und B-Lymphozyten aktivieren können. Antigene innerhalb der Zellen, wie sie nach Infektion durch Viren, obligaten intrazellulären Pathogenen oder Tumorantigenen entstehen, werden nach proteolytischem Abbau in Zusammenhang mit Molekülen des MHC Klasse I präsentiert und von CD8+ T-Lymphozyten erkannt. CD8+ T-Lymphozyten werden auch zytotoxische T-Lymphozyten genannt, da sie eine immunvermittelte Zerstörung von Virus-infizierten Zellen oder Tumorzellen einleiten. Der prädominante Ort der Sensibilisierung von Lymphozyten gegenüber neuem Antigen sind die sekundär lymphatischen Organe, in denen die T-Lymphozyten und Antigenpräsentierenden Zellen, wie z.B. dendritische Zellen, in einem besonderen Mikromilieu kolokalisiert sind (GUNN et al., 1999). In den lymphatischen Organen werden den Lymphozyten Antigene aus dem Blut und den peripheren Geweben präsentiert und damit die Wahrscheinlichkeit des Zusammentreffens eines spezifischen Lymphozyten mit seinem Antigen erhöht. Dendritische Zellen (DC) nehmen dabei in den peripheren Geweben Antigen auf, zerteilen es in kleine Peptide, wandern in die lymphatischen Organe und präsentieren es dort zusammen mit dem MHC-Komplex auf ihrer Oberfläche. Durch zahlreiche Oberflächenmoleküle (kostimulatorische oder akzessorische Moleküle) können sie TLymphozyten optimal stimulieren und Immunantworten einleiten. Die Schlüsselrolle für die Kontrolle der Immunantwort durch die DC liegt hierbei im Wechsel des Phänotyps: von der 14 effektiven Antigenaufnahme (unreifer Phänotyp) zur effektiven Antigen-Präsentation (reifer Phänotyp) (BANCHEREAU u. STEINMAN, 1998). Um die Regulation und die Einleitung von Immunantworten besser nachvollziehen zu können, werden im folgenden Abschnitt der Aufbau und die Funktion der lymphatischen Organe erläutert. 2. Die lymphatischen Organe Lymphozyten stammen von lymphoiden Vorläuferzellen ab, die sich frühzeitig aus hämatopoetischen Stammzellen aus dem Knochenmark entwickeln. Das Knochenmark dient der Vermehrung der Lymphozyten, im Thymus wird die Entscheidung über die weitere Entwicklung der T-Lymphozyten getroffen. Im Gegensatz zum Knochenmark und dem Thymus, die als primäre oder zentrale lymphatische Organe gelten, werden die Milz, die Lymphknoten und Darm-, Mukosa- oder Bronchus-assoziierte lymphatische Gewebe (GALT, respektive MALT und BALT), zu denen auch die Peyerschen Platten zählen, als sekundär oder peripher lymphatische Organe bezeichnet. Bei lymphatischen Organen handelt es sich um organisierte Gewebe, in denen die Lymphozyten Interaktionen mit nicht-lymphatischen Zellen eingehen, die zur Einleitung einer adaptiven Immunantwort führen können. 2.1 Die Milz Die Milz ist ein beim Menschen etwa faustgroßes, bei der Ratte ein circa 3 cm langes, kompaktes Organ, das als Blutfilter fungiert. Das Parenchym der Milz besteht aus zwei Kompartimenten: die rote und die weiße Pulpa. In der roten Pulpa werden alternde Erythrozyten phagozytiert, die durch die enge Passage der Milzgefäße nicht wieder in die Blutbahn gelangen können, und zur Wiederverwertung in ihre Bestandteile zerlegt. Die weiße Pulpa repräsentiert den Teil des Organs mit der höchsten Dichte an Lymphozyten und umfasst drei Unterkompartimente: die periarterioläre lymphatische Begleitscheide, kurz PALS genannt (T-Zellareal), die Follikel (B-Zellareal) und die Marginalzone. Die PALS ist konzentrisch um 15 die Zentralarteriolen, die durch die gesamte Milz ziehen, gelagert. Sie beinhaltet vorwiegend T-Lymphozyten und dendritische Zellen, die hier aufgrund ihrer Morphologie mit zahlreichen Ausläufern interdigitierende dendritische Zellen genannt werden (STEINMAN et al., 1997). B-Lymphozyten befinden sich nur zu einem geringen Anteil in der PALS und sind dann bevorzugt im äußeren Anteil (äußere PALS) anzutreffen. An diesem Übergang zwischen T- und B-Zellareal finden Antigen-spezifische Interaktionen zwischen T-Lymphozyten und wandernden B-Lymphozyten während primärer und sekundärer Immunantworten statt. Antigen-spezifische B-Lymphozyten wandern aus der Marginalzone in die angrenzende äußere PALS. Durch eine gegenläufige Wanderung wird das Zusammentreffen von Antigen-spezifischen T- und B-Lymphozyten optimiert. B-Lymphozyten können so die notwendige T-Zellhilfe erhalten und sich in der Marginalzone zu Antikörper-produzierenden Plasmazellen entwickeln (VAN ROOIJEN, 1990). Die angrenzenden Follikeln beinhalten vorwiegend B-Lymphozyten und nur wenige CD4+ T-Lymphozyten. Follikuläre dendritische Zellen, die vermutlich nicht von Vorläufern aus dem Knochenmark stammen, halten auf ihrer Oberfläche Antigen in nativer Form als Immunkomplex zurück und präsentieren es B-Lymphozyten in den Keimzentren (STEINMAN et al., 1997). Die Marginalzone umgibt PALS und Follikel und bildet ein breites, gut demarkiertes Band zwischen weißer und roter Pulpa. In dieser Zone befinden sich vorwiegend eine Population von memory BLymphozyten, die durch eine sofortige Antikörperantwort auf Polysaccharidkomponenten aus Bakterienkapseln einen Schutz vor Sepsis bieten (STEINIGER u. BARTH, 2000). 2.2 Lymphknoten Lymphknoten sind in die Lymphbahnen eingeschaltete Filterstationen, die in ihrer Größe und ihrer Anzahl im Körper variieren können. In den meisten Geweben befinden sich lymphatische Gefäße, die als afferente Lymphbahnen die Lymphknoten speisen. Lymphknoten bestehen aus einer Bindegewebskapsel, von der aus Trabekel in das Innere einstrahlen und den Lymphknoten segmentieren. Von außen wird die Kapsel von den Vasae afferentiae, den zuleitenden Lymphgefäßen, unterbrochen, von denen aus die Lymphe unter der Kapsel weiter über die Intermediärsinus in den Marksinus und abschließend in die Vasae efferentiae weitergeleitet wird. Der Lymphknoten wirkt hierbei als Filter sowohl für inerte Partikel (z.B. 16 Farbpartikel nach Tätowierungen) als auch für Bakterien oder Zellreste, die von den Fressund Immunzellen aufgenommen werden. Im Lymphknoten werden 3 Kompartimente unterschieden: der Kortex, der Parakortex und die Medulla. Im Kortex sind die Lymphozyten in primäre und sekundäre Follikel mit Keimzentren angeordnet, die in der Hauptsache von BLymphozyten und wenigen CD4+ T-Helferzellen besiedelt sind. Der Parakortex besteht vorwiegend aus T-Lymphozyten und dendritischen Zellen. Eine Besonderheit des Parakortex ist das Vorkommen von hochspezialisierten, postkapillären Venulen mit einem kubischen Epithel (hochendotheliale Venulen, HEV), die es den Lymphozyten in hoher Anzahl ermöglichen, aus dem Blut in die Lymphknoten einzuwandern. (PABST, 1994). 2.3 Peyersche Platten Die Schleimhäute des Verdauungstraktes besitzen eine besonders große Oberfläche und ein dünnes Epithel zur effektiven Resorption von Nährstoffen. Beides ermöglicht es aber auch Pathogenen wie Bakterien oder Viren die Schleimhautbarriere zu überwinden, in das Gewebe einzudringen und es zu schädigen. Das Darm-assoziierte, lymphatische Gewebe vermindert das Eindringen und die Vermehrung der Mikroorganismen. Es setzt sich aus vielen vereinzelt (solitär) gelegenen Follikeln und aus Follikeln mit spezialisiertem Epithel, den Peyerschen Platten, auch „Plaques“ genannt, zusammen. Letztere sind im Bereich des gesamten Dünndarmes anzutreffen und zeichnen sich dadurch aus, dass sie keine afferenten Lymphgefäße besitzen. Zum Darmlumen hin sind sie mit einem spezialisierten Epithel bedeckt, das den Antigenkontakt und die -aufnahme ermöglicht. In der Histologie sind auch hierbei deutlich abgrenzbare Kompartimente zu erkennen: bei den Follikeln handelt es sich ausschließlich um Sekundärfollikel mit aktiven Keimzentren und einem Randwall aus kleineren Lymphozyten. In der zwischen den Follikeln gelegenen Interfollikulärregion befinden sich in der Hauptsache dicht gepackt liegende T-Lymphozyten, DC und HEVs. Zum Darmlumen hin kommt es zu einer kappenartigen Ansammlung von T- und B-Lymphozyten, die Dom-Epithel genannt wird. Aufgrund seiner Funktion zeichnet sich das Epithel dort mit einigen Besonderheiten aus: es hat weder Krypten noch Zotten, kaum oder keine Becherzellen und ist somit nicht von einer Schleimschicht geschützt, trägt keine IgA-Rezeptoren und zwischen den Epithelzellen finden sich Zellen, die zum Lumen hin eine membranförmige 17 Faltung haben und aufgrund ihrer Form M-Zellen („membranous cells“) genannt werden. Durch Transzytose sind diese Zellen in der Lage, große Moleküle, Bakterien und Viren aufzunehmen und mit den räumlich nahe gelegenen Immunzellen in Kontakt zu bringen (PABST, 1994; GEBERT, 1997; BEIER u. GEBERT, 1998). 2.4. Morpholgie der sekundär lymphatischen Organe in LFA-1-defizienten Mäusen LFA-1 (CD11a-/-/CD18) aus der β2- Integrinrezeptorfamilie wird vor allem auf Leukozyten exprimiert und nimmt eine Schlüsselrolle in der Funktion, wie z. B. bei der Adhäsion dieser Zellen an andere Zellen oder das Epithel, ein. LFA-1 setzt sich aus zwei Ketten zusammen, die auf unterschiedlichen Genen kodiert werden: Integrin alpha L (CD11a, Ly 15, Ly 29) wird auf dem Chromosom 7 kodiert, Integrin beta 2 auf Chromosom 10 (CD18). Die Produkte beider Gene formen das funktionelle LFA-1. Wird die Expression eines der beiden Produkte unterdrückt wie im vorliegenden Fall die Expression von CD11a, so liegt eine Defizienz des LFA-1-Moleküls vor. Im Vergleich zu Wildtypmäusen, die eine normale Expression des LFA1-Moleküls auf der Oberfläche der Zellen aufweisen, konnte bei LFA-1-defizienten Mäusen eine Vergrößerung der Milz bei männlichen Tieren um das 1,7 fache, bei weiblichen Tieren um das 1,2 fache festgestellt werden. Die peripheren Lymphknoten hingegen sind um etwa 30% kleiner als bei Wildtypmäusen, wohingegen weder die mesenterialen Lymphknoten, noch weitere Lymphknoten diese Veränderung aufwiesen. Bei der Analyse der T- und BLymphozyten konnte ein deutlicher Verlust von CD4+ und CD8+ T-Lymphozyten in den peripheren Lymphknoten nachgewiesen werden, in der Milz hingegen fanden sich signifikant mehr T-Lymphozyten. Diese LFA-1-Defizienz resultierte in einer Reduktion der Einwanderung von T-Lymphozyten in die peripheren Lymphknoten und in die Peyerschen Platten auf etwa 30% (BERLIN-RUFENACH et al., 1999). In den sekundär lymphatischen Organen werden die Funktionen der spezifischen Immunabwehr eingeleitet. Nach Antigenkontakt durchlaufen die Lymphozyten verschiedene Phasen der Reifung und werden in naive, Effektor und memory T-Lymphozyten eingeteilt, die im folgenden näher erläutert werden. 18 3. Aktivierungsstadien von T-Lymphozyten im Laufe einer Immunantwort 3.1. Naive T-Lymphozyten Nach ihrer Entstehung im Knochenmark wandern Prä-T-Lymphozyten in den Thymus ein. Das T-Zellrepertoire muss weitgehend tolerant gegenüber körpereigenen Strukturen und Proteinen sein. Um diese „zentrale Toleranz“ zu gewährleisten, werden während der Entwicklung im Thymus körpereigene Proteine auf MHC-Molekülen von dendritischen Zellen präsentiert. Zum einen werden Thymozyten darauf getestet, ob sie den Hauptgewebeverträglichkeitskomplex (major histocompatibility complex, MHC) auf den körpereigenen Zellen erkennen (positive Selektion), zum anderen, ob sie eine verstärkte Affinität auf körpereigenes Protein zeigen (negative Selektion). Etwa 95% der TLymphozyten überstehen diesen Prozess nicht und sterben im Thymus (SPRENT et al., 1996). Nach ihrer Differenzierung im Thymus tragen naive T-Lymphozyten auf ihrer Oberfläche bestimmte Moleküle, die dem Anheften an bestimmten Oberflächen (Adhäsion) oder der Bindung von Proteinen aus der Zirkulation oder auf anderen Zellen (Rezeptoren) dienen. Zu diesen Molekülen werden der T-Zellrezeptor, CD28 und CD4 oder CD8 gezählt, die sich auch bei einer Aktivierung des Lymphozyten nur wenig in ihrer Expression verändern. Andere Moleküle wie CD45RC und L-Selektin werden nach einem spezifischen Antigenkontakt weniger oder nicht mehr exprimiert (BODE, 1998). Diese Moleküle werden auch zur Unterscheidung des Aktivierungszustandes herangezogen. Diese T-Lymphozyten, die den Thymus verlassen haben, aber noch nicht mit ihrem spezifischen Antigen in Kontakt gekommen sind, werden auch als naive T-Lymphozyten bezeichnet, deren Lebensspanne in der Maus etwa 6 Monate beträgt (DI ROSA et al., 1999). 19 3.2. Aktivierung und Effektorphase Durch den T-Zellrezeptor (TCR) erkennen und binden T-Lymphozyten Peptide in Zusammenhang mit MHC-Molekülen. Die Antigen-abhängige Stimulation des TCR resultiert in einer komplexen Kaskade von biochemischen Signalereignissen, die drei mögliche Folgen hat: Proliferation und klonale Expansion, Apoptose oder Anergie. Einige Ergebnisse lassen vermuten, dass in Abhängigkeit des gebundenen Liganden, der Zeit oder anderen Eigenschaften der physikalischen Bindung eine qualitativ und quantitativ unterschiedliche Antwort hervorgerufen wird (LORD et al., 1999). Die Avidität der TCR-Bindung wird durch die Moleküle CD4 oder CD8 verstärkt und es kommt zu einer Stabilisierung des Kontaktes und einer Veränderung des Schwellenwertes durch ein direktes Signal oder Induktion der IL2-Transkription. Die Bindung weiterer kostimulatorischer Moleküle wie beispielsweise B7.1 (CD80), B7.2 (CD86) oder des interzellulären Zelladhäsionsmoleküls-1 (ICAM-1, CD54) auf der Zelloberfläche wird benötigt, damit T-Lymphozyten proliferieren können (HALE u. HAYNES, 1999). B7 wird dabei eine zentrale Rolle in der Regulation der Proliferation zugeschrieben. Einerseits führt es zum Überleben der Zellen (DEETHS u. MESCHER, 1999), andrerseits kommt es durch die Bindung an das zytotoxische T-Zellantigen-4 (cytotoxic T lymphocyte antigen-4, CTLA-4) zu einer Hemmung der Proliferation (CHAMBERS, 2001). Aber auch durch die Neuanordnung von weit über die Oberfläche herausragenden Molekülen wie CD45 und CD43 (Sialophorin, 45nm), durch die eine Interaktion des kleinen TCR (15nm) mit dem MHC ermöglicht wird, kann die Aktivierung beeinflussen (SHAW u. DUSTIN, 1997). Integrine, u.a. LFA-1, werden dabei für den initialen Zell-Zell-Kontakt und kostimulatorische Moleküle (CD28) zur Ausbildung eines stabilen Kontaktes benötigt. Eine Bindung des TCR an den MHC-Peptid-Komplex ohne die gleichzeitige Bindung der kostimulatorischen Moleküle führt zu Anergie oder „unresponsiveness“ des T-Lymphozyten, d.h. die Zelle ist zwar weiterhin überlebensfähig, aber reagiert nicht weiter auf sein spezifisches Antigen. Eine vollständige Aktivierung führt zur Differenzierung der Zelle. Die Funktion der Zelle wechselt vom Erkennen des Antigens zum Eliminieren der Mikroorganismen (ABBAS et al., 1994). Bereits innerhalb von Sekunden nach der Bindung des TCR kommt es zur Auslösung der Signalkaskade. Biochemische Veränderungen, die mit der Aktivierung des TCR 20 einhergehen, dauern über mehrere Stunden und bieten die Möglichkeiten der Beeinflussung durch zusätzliche regulative Wege. Nach der TCR-Aktivierung werden innerhalb von etwa 2h Zytokine sezerniert, zur DNS-Replikation kommt es nach 24h, eine Zellteilung erfolgt nach 48h, die Differenzierung in Effektorzellen benötigt einige Tage (HALE u. HAYNES, 1999). Bei den Effektor T-Lymphozyten handelt es sich um große, blastoide Zellen, die eine hohe Synthese von DNS zeigen. Es kommt zu einem Wechsel des auf der Oberfläche getragenen Molekülmusters, die zum einen die Zytokinrezeptoren betreffen und zum anderen die Adhäsionsmoleküle, die für das Anheften der Zellen am Endothel entscheidend sind (SPRINGER, 1994). Durch die Interaktion mit dendritischen Zellen differenzieren sich CD4+ T-Lymphozyten in zwei Klassen T-Helferzellen: TH1-Lymphozyten, die bevorzugt Interferon-γ (IFN-γ) exprimieren, welches bei Entzündungsprozessen eine wichtige Rolle spielt, und die sich durch Hyperaktivierung von Makrophagen bei der Abwehr von intrazellulären Pathogenen beteiligen. TH2-Lymphozyten sezernieren IL-4, Il-5, IL-6 und IL-10 (MOSMANN et al., 1991) und aktivieren B-Lymphozyten zur Produktion und Sekretion von spezifischen Antikörpern (DEFRANCO, 1988). In Abhängigkeit des Zytokins kommt es bei den B-Lymphozyten zur Synthese von verschiedenen Antikörperklassen (SWAIN et al., 1996). Der Mechanismus der Differenzierung der T-Helferzellen ist nicht vollständig geklärt. Es wird jedoch vermutet, dass DC nicht nur die Signale zur klonalen Expansion der Helferzellen geben, sondern selektive Signale von unterschiedlichen funktionellen Subpopulationen von DC zur Differenzierung der T-Helferzellen führen (BOTTOMLY, 1999; RISSOAN et al., 1999). CD8+ T-Lymphozyten differenzieren sich in zytotoxische Zellen, die durch infizierte Zellen angreifen und in die Apoptose treiben können (JANEWAY et al., 1999). 3.3 Memory T-Lymphozyten Die von den differenzierten Zellen sezernierten Zytokine können sich auf den gesamten Körper schädlich auswirken. Aus diesem Grunde muss nach einer erfolgreichen Eliminierung des Antigens die Immunantwort streng reguliert werden und die potentiell gefährlichen Zellen beseitigt werden (VAN PARIJS u. ABBAS, 1998). Ein Hauptteil der Effektor T- 21 Lymphozyten, etwa 70%, wird dabei durch einen induzierten Zelltod, die Apoptose, unschädlich gemacht (SMITH et al., 1980; BINNS et al., 1992; BOISE et al., 1995). Dabei wird das auf der Oberfläche von Effektor T-Lymphozyten getragene Molekül Fas (CD95) von seinem Liganden (Fas-L, CD95L) auf den dendritischen Zellen oder den Makrophagen aktiviert und führt über eine Signalkaskade zum Abbau der DNS in den T-Lymphozyten (NAGATA, 1997). Nach Abklingen einer Immunantwort überleben einige Antigenspezifische T-Lymphozyten und bilden das immunologische Gedächtnis („memory“). Memory T-Lymphozyten werden in der Ratte durch den phänotypischen Verlust des Markers CD45RC und in der Maus über die Kombination der Marker CD45low, L-Selektinlow und CD44high identifiziert (TIETZ u. HAMANN, 1997). Sie kommen in höherer Frequenz als naive T-Lymphozyten vor und haben eine längere Lebensdauer als diese. Bei einem sekundären Kontakt zum spezifischen Antigen läuft die Immunabwehr schneller ab. Um sowohl eine möglichst breite Reihe an Antigenen erkennen zu können, aber auch gleichzeitig eine effektive Immunantwort auslösen zu können, bedarf es eines Gleichgewichtes zwischen dem naiven und dem memory T-Zellpool. Die Aufrechterhaltung des T-Zellpools ist ein aktiver Prozess, der eine kontinuierliche Bindung des TCR durch MHC auf z.B. dendritischen Zellen erfordert. Diese Interaktion scheint über die Expression von Bcl-2 das Überleben der T-Lymphozyten vermitteln zu können (TANCHOT u. ROCHA, 1998). 4. Die Migration von Lymphozyten Eine charakteristische und zum Auffinden des spezifischen Antigens wichtige Eigenschaft von Lymphozyten ist ihre Fähigkeit, in nahezu alle Organe und Gewebe ein- und auswandern zu können („Migration“). Die Rezirkulation von Lymphozyten ist ausschlaggebend für die Interaktion zwischen T-Lymphozyten und den dendritischen Zellen zur kontinuierlichen Präsentation des gesamten Antigenrepertoires im Körper und damit zur Einleitung von Immunantworten (WESTERMANN u. PABST, 1990). Dabei herrscht ein reger Verkehr zwischen dem Blut, den Geweben und der Lymphe. Etwa 5 x 1011 Lymphozyten wandern beim Menschen jeden Tag aus dem Blut aus und wieder zurück. Das Blut enthält nur 2% der 22 gesamten Lymphozyten, die sich im Durchschnitt nur etwa 30 Min dort aufhalten. Die meisten Lymphozyten wandern in Organe wie die Lunge, Milz, Leber, Knochenmark und nur ein geringerer Anteil, unter physiologischen Bedingungen, auch in die Haut, die Synovia, die Muskulatur oder das Gehirn. Durch Entzündungsgeschehen oder chronische Erkrankungen kann sich diese Situation aber deutlich verändern (WESTERMANN et al., 1988; WESTERMANN u. PABST, 1996). Ein Antigen, das die angeborene Immunabwehr durchbrochen hat, wird von dendritischen Zellen aufgenommen und zu den lymphatischen Organen transportiert, wo optimale Bedingungen für die Antigenerkennung herrschen (MONDINO et al., 1996). Ein Großteil der naiven T-Lymphozyten gelangt über Adhäsionsmoleküle wie L-Selektin über die hochendothelialen Venulen (HEV) in die sekundär lymphatischen Organe und durchwandert das Gewebe. Findet in dieser Zeit keine Antigenerkennung statt, so wandern die naiven TLymphozyten über die efferente Lymphe (SMITH u. FORD, 1983) aus und gelangen wieder in die Zirkulation (GIRARD u. SPRINGER, 1995). Die Anheftung an das Epithel und die anschließende Einwanderung in das Gewebe umfasst dabei mehrere Schritte und wird durch die Interaktion der Adhäsionsmoleküle auf den T-Lymphozyten und den spezifischen Rezeptoren auf den Endothelzellen vermittelt. Dabei werden in der Literatur immer wieder sogenannte „Homingrezeptoren“ diskutiert, die für den Eintritt der Lymphozyten in bestimmte Gewebe verantwortlich sein sollen, wie z.B. L-Selektin für den Eintritt in periphere Lymphknoten (GALLATIN et al., 1983), α4β7-Integrin für den Eintritt in die Peyerschen Platten (HAMANN et al., 1994). In LFA-1-defizienten Mäusen konnte gezeigt werden, dass die Migration von T-Lymphozyten in die peripheren Lymphknoten zwar bis auf 30% des Wertes bei Wildtypmäusen abfällt, jedoch andere α4-Integrine wie α4β7 oder α4β1 das Fehlen eines funktionellen LFA-1-Moleküls teilweise kompensieren können (BERLIN-RUFENACH et al., 1999). Für die Milz konnte kein spezifisches Molekül identifiziert werden. Zusätzlich zu den lymphatischen Geweben wandern naive T-Lymphozyten auch in die Leber (LUETTIG et al., 1999) und die Lunge ein. Findet bei der Durchwanderung z.B. des Lymphknotens eine Antigenerkennung statt, so stellt die Bindung des TCR ein Stopsignal für den T-Lymphozyten da und führt zur Beendigung der Migration (DUSTIN et al., 1997). Dieses Phänomen wird als ein Mechanismus angesehen, um 23 Antigen-spezifische Lymphozyten im drainierenden Lymphknoten anzureichern. Dabei ist die Bindung des membrangebundenen LFA-1 mit seinen Liganden ICAM-1, -2 oder –3 auf den T-Lymphozyten ein früher und essentieller Schritt in der Zellaktivierung. LFA-1 gehört zur Familie der β2-Integrine und vermittelt eine Antigen-unabhängige Bindung der TLymphozyten mit dendritischen Zellen, aber auch mit dem Endothel von Gefäßen (SPRINGER, 1990). Durch die Rezeptor-Ligandenpaare LFA-1/ ICAM, ICAM/ LFA-1, CD2/ LFA-3 und CD28/ CD80 wird eine transiente Adhäsion zwischen CD4+ T-Lymphozyten und DC vermittelt, wie durch monoklonale Antikörper nachgewiesen werden konnte (HAUSS et al., 1995). Die Interaktion mit der DC erfordert mehrere Stunden zur Initiierung der Zytokinproduktion, zum Eintritt in den Zellzyklus und zur Differenzierung. Einige dieser Effektor TLymphozyten wandern vom Parakortex in die Follikel ein und initiieren dort eine BZellantwort, die zur Ausbildung von Keimzentren führt (FULLER et al., 1993). Andere TLymphozyten verlassen auch über die efferente Lymphe den Lymphknoten auf dem Weg in das Blut (AGER, 1994). Mit der Aktivierung der T-Lymphozyten sind phänotypische Veränderungen der Zellen verbunden, die u.a. zu einer Funktionsänderung, aber auch zu einem veränderten Wanderungsverhalten führen. Auf aktivierten T-Lymphozyten werden Adhäsionsmoleküle wie LFA-1, VLA-1 und CD2 verstärkt exprimiert, von denen angenommen wird, dass sie eine erhöhte Interaktion mit dem Endothel bewirken. Dadurch könnte eine verbesserte Einwanderung in nicht-lymphatische Gewebe und eine erhöhte Kapazität in entzündete Gewebe einwandern zu können, erklärt werden (SPRENT, 1994). Entgegen der Annahme, dass über diesen Mechanismus Antigen-spezifische T-Lymphozyten so an den Ursprung der Entzündung wandern (DUNON et al., 1996), konnte gezeigt werden, dass Effektor TLymphozyten in alle Gewebe einwandern, aber nur in ihrem Herkunftsmilieu bevorzugt proliferieren und vermindert der Apoptose anheim fallen (BODE et al., 1999). Effektor TLymphozyten finden sich vorwiegend in nicht-lymphatischen Geweben wie Lunge, Leber und Darm wieder (HAMANN u. REBSTOCK, 1993; LUETTIG et al., 1999). Es konnten aber auch Effektor T-Lymphozyten im Lymphknoten und in den Peyerschen Platten nachgewiesen 24 werden (BODE et al., 1999), obwohl auf vielen Effektor T-Lymphozyten kein oder nur geringe Mengen L-Selektin exprimiert wird (DAILEY et al., 1985), das für den Eintritt über HEV in Lymphknoten verantwortlich gemacht wird. T-Lymphozyten, die nach der Aktivierung und Differenzierung entstehen und eine Immunantwort überleben, werden als „memory“ Lymphozyten bezeichnet. Es konnte jedoch gezeigt werden, dass sowohl naive wie auch memory T-Lymphozyten in der Lage sind, über HEV in lymphatische Gewebe einzuwandern. Beide Subpopulationen wandern ebenfalls in BZellareale und Keimzentren ein. Dabei wandern T-Lymphozyten vom memory-Phänotyp schneller durch die T-Zellareale und lassen sich deshalb in geringer Anzahl im Gewebe auffinden (WESTERMANN et al., 1997). Für andere Spezies wie der Maus wird beschrieben, dass sich memory T-Lymphozyten, wie auch Effektor T-Lymphozyten, vorwiegend in Leber und Lunge ansammeln, aber nicht von der Migration in lymphatische Gewebe ausgeschlossen sind (TIETZ u. HAMANN, 1997). 5. Antigenpräsentation oder: die Kontrolle der Immunantwort T- und B-Lymphozyten sind zwar die Botschafter der Immunabwehr, aber ihre Funktion steht unter der Kontrolle der DC, die zu den effektivsten Antigen-präsentierenden Zellen zählen (BANCHEREAU u. STEINMAN, 1998). B-Lymphozyten als Vorläufer der Antikörper sezernierenden Plasmazellen können über ihren B-Zellrezeptor natives Antigen direkt erkennen. Zur Auslösung einer T-Zellabhängigen Immunantwort benötigt der T-Lymphozyt sein spezifisches Antigen in einer prozessierten und präsentierten Form in einem MHCPeptid-Komplex und kostimulatorischen Molekülen wie CD28 und LFA-1. Dabei müssen die CD8+ T-Lymphozyten Fremdpeptide auf der Oberfläche von infizierten Körperzellen finden, die sich überall im Körper befinden können. Die Menge spezifischen MHC-Peptid-Komplexe auf infizierten und Tumorzellen ist gering (100 oder weniger pro Zelle), es fehlen meistens kostimulatorische Moleküle und die Zellen müssen von seltenen T-Zellklonen (1: 100.000 oder weniger) erkannt werden, die T-Zellrezeptoren mit niedriger Affinität besitzen (BANCHEREAU u. STEINMAN, 1998). DC haben alle phänotypischen und funktionellen 25 Eigenschaften, die zur effizienten Einleitung einer zellulären Immunantwort nötig sind: in den meisten Geweben vertreten, binden sie in der Peripherie Antigen, prozessieren es und präsentieren es in einem MHC-Peptid-Komplex in Zusammenhang mit kostimulatorischen Molekülen wie ICAM-1 und der B-7-Familie. Im Gegensatz zu Makrophagen liegt ihre Aufgabe jedoch nicht in der Beseitigung der eingedrungenen Pathogene, sondern in der Alarmierung des Immunsystems (STEINMAN u. BHARDWAJ, 1999). Dendritische Zellen sind unverwechselbare Antigen-präsentierende Zellen (APC), die drei Hauptfunktionen haben: 1. DC sind überaus potente APC. In vitro und in vivo sind nur einige DC notwendig, um eine starke T-Zellantwort einzuleiten. DC induzieren eine sogenannte gemischte Leukozytenreaktion (mixed leucocyte reaction, MLR), wobei nur eine DC notwendig ist, um 100-3000 T-Lymphozyten zu stimulieren. DC aktivieren T-Lymphozyten nicht nur gegenüber körperfremden MHC-Molekülen, sondern auch gegenüber einer Reihe von Fremdproteinen und mikrobiellen Proteine wie Superantigenen, die ohne Prozessierung direkt an die MHC-Moleküle binden (BHARDWAJ et al., 1993), oder den „Standardproteinen“, die eine Prozessierung erfordern einschließlich Entzündungsprodukten (INABA et al., 1993) und Tumorantigenen (MAYORDOMO et al., 1995; ZITVOGEL et al., 1996). 2. DC induzieren als einzige Zellen primäre T-Zellabhängige Immunantworten, die sich anschließend in T-Helfer oder zytotoxische Zellen differenzieren. 3. Nach der Aktivierung durch DC können T-Lymphozyten effizient mit Makrophagen und BLymphozyten interagieren. Der Wechsel von der Prozessierung des aufgenommenen Antigens und der Präsentation mit anschließender Aktivierung von naiven T-Lymphozyten wird allgemein als „Reifung“ bezeichnet. DC, die sich in fast alle Geweben befinden, weisen einen „unreifen“ Phänotyp auf, d.h. sie haben nur eine schwache stimulatorische Aktivität für T-Lymphozyten, die des weiteren mit einer niedrigeren oder abwesenden Expression von Oberflächenmolekülen wie MHC Klasse II, CD40, ICAM-1 oder B7-1 assoziiert ist. So ist MHC Klasse II bis zu 10 mal niedriger exprimiert. Nach Isolierung aus Geweben und Organen reifen sie jedoch in der Kultur schnell aus, was durch eine koordinierte Reihe von Veränderungen wie der Hochregulierung der MHC-Moleküle und kostimulatorischer Moleküle deutlich wird (STEINMAN u. BHARDWAJ, 1999). Der Prototyp der unreifen DC ist die Langerhanszelle in der Haut, die auch unter Zugabe von M-CSF nicht zu Makrophagen ausdifferenziert. In 26 vielen verschiedenen Kultursystemen sind die Stimuli untersucht worden, die zu einer Ausreifung der DC führen. So werden DC durch Entzündungsstimuli und infektiöse Agentien, wie z.B. LPS aus Bakterienwänden, aktiviert und produzieren Chemokine (MIP-1α, MIP-2, MCP-1, TNFα), die Makrophagen, NK-Zellen, Neutrophile Granulozyten und weitere unreife DC an den Ort der Entzündung locken. Danach erst durchlaufen sie ein induziertes Reifungsprogramm, in dem sie irreversible Veränderungen von der Antigenaufnahme (unreifer Phänotyp) über eine intermediäre Phase von 24-48h bis zur Auslösung von Immunantworten (reifer Phänotyp) durchlaufen (RESCIGNO et al., 1999). Verglichen mit anderen Leukozyten sind DC ungewöhnlich reich an Genprodukten des MHC Klasse II, das sich in intrazellulären endozytotischen Vakuolen, MHC II reiche Kompartimente (MIIC) genannt, befindet. Nach einem Stimulus erfolgt eine erhöhte Synthese der MHC Klasse II und die Fusion der Vesikel. Das Antigen wird an das MHC-Molekül gebunden und auf die Oberfläche der Zelle ausgeschleust, wobei die Halbwertszeit der Komplexe über 100h beträgt und sie so über mehrere Tage T-Lymphozyten stimulieren können. Der Wechsel der Kompartimentalisierung aus den MIIC an die Oberfläche erfolgt in 24h bis 48h nach den Antigenaufnahme (PIERRE et al., 1997). Die Gegenwart der MIIC erklärt, warum der unreife Phänotyp das Stadium in der Entwicklung der DC ist, in dem DC aktiv Proteine aufnehmen und zur Präsentation für T-Lymphozyten prozessieren. Diese endgültige Ausreifung der DC nach Stimulierung durch Entzündungsprodukte, virale und bakterielle Komponenten oder durch CD40Ligand wird als der Kontrollpunkt zur Einleitung von Immunantworten oder Toleranz angesehen (STEINMAN et al., 2000). Dabei werden kostimulatorische und Adhäsionsmoleküle wie B7-2, MHC II und CD40 bereits nach 1-2h hochreguliert, B7-1 und MHC I hingegen erst nach 4-6h initiiert und das Maximum nach 18h erreicht. Die Expression der Chemokinrezeptoren (u.a. CCR1, CCR5) wechselt von der Erkennung von Entzündungschemokinen (SLC, ELC) zu konstitutiv im Gewebe exprimierten Chemokinen. Diesem Wechsel wird auch die erhöhte Wanderungsaktivität in lymphatische Gewebe zugeschrieben, wo sie in den T-Zellarealen zurückgehalten werden und sich auf die Suche nach Antigen-spezifischen T-Lymphozyten machen (RESCIGNO et al., 1999). Wie es auch der Fall bei anderen Zellen von myeloider Abstammung ist, ist die Morphologie zur Identifizierung der DC nützlich. So weisen DC lange, blattähnliche Ausläufer, die auch 27 Lamellipodia oder „veiled“ genannt werden, auf, die in verschiedene Richtungen vom Zellkörper ausstrahlen. Im lebenden Zustand werden diese Ausläufer ständig neu geformt und aktiv bewegt. Diese ungerichteten Bewegungen sind bei anderen Leukozyten nicht zu beobachten. Obwohl diese Zelleigenschaften nicht so diagnostisch sind wie die gefärbten Granula von eosinophilen oder basophilen Granulozyten, so ist doch die Morphologie der DC ausreichend charakteristisch, um die Identifikation und Aufreinigung zu erlauben. In humanem Blut, afferenter Lymphe und Haut von Mäusen, Affen und Menschen, aber auch in den lymphatischen Organen von Mäusen, Ratten und Menschen sind DC untersucht worden. Die einzigartige Morphologie der DC wurde dazu herangezogen, Methoden zur Gewinnung von großen Mengen von DC zu etablieren. Durch FACS-Untersuchungen konnte gezeigt werden, dass neben zahlreichen anderen Molekülen vor allem MHC-Produkte auf der Oberfläche von DC exprimiert werden. Besonders MHC Klasse II ist überreichlich exprimiert. Quantitative Bindungsstudien mit monoklonalen Antikörpern ergaben mehr als 106 Bindungsstellen pro Zelle (CELLA et al., 1997). Durch die Expression von MHC Klasse I, sowie MHC Klasse II präsentieren DC sowohl Antigene aus dem Zytosol der Zelle, wie auch aus endozytotischen Vesikeln (JANEWAY et al.,1999). DC exprimieren die meisten der bekannten akzessorischen oder kostimulatorischen Moleküle für T-Lymphozyten wie CD40, ICAM-1 (CD54), CD58, B7.1 (CD80) und B7.2 (CD86). Diese Moleküle erklären die Effizienz, mit der DC T-Lymphozyten binden und stimulieren. Die Interaktion ist bidirektional in dem Sinne, dass die Bindung der T-Lymphozyten zu Veränderungen des TLymphozyten wie auch der DC führen. Dies ist besonders kennzeichnend für die Bindung von CD40. Nach Interaktion mit CD40L auf aktivierten T-Lymphozyten bleibt die Lebensfähigkeit der DC erhalten und sie produzieren große Mengen an IL-12 (HOWLAND et al., 2000; KOCH et al., 1996; TAKASHIMA u. KITAJIMA, 1998). Spezifische Marker für andere Leukozyten fehlen auf DC wie CD14 für Makrophagen, CD16 für NK-Zellen, CD19 und CD20 für B-Lymphozyten. Zellspezifische Marker waren bislang aufgrund geringer verfügbarer Anzahl an DC nur sehr schwierig zu identifizieren. Für den Menschen werden 3 Antigene zur Identifizierung verwendet: S100b, p55 und CD83, die jedoch nicht zellspezifisch sind, da sie ebenfalls auf Zellen im Neuralgewebe exprimiert werden (STEINMAN u. BHARDWAJ, 1999). 28 Die Charakterisierung der DC macht die Separation von anderen Leukozyten, im besonderen aber von den Makrophagen notwendig. Diese Separation ist aufwendig, da DC in nur sehr geringer Anzahl vorkommen, wie z.B. im humanen Blut, in dem sich das Verhältnis von Monozyten zu DC auf 20-50:1 belaufen. Durch die Entwicklung von Kulturprotokollen ist es neuerlich möglich (CRAWFORD et al., 1999; TALMOR et al., 1998), größere Mengen von DC zu gewinnen und in der aktiven Immuntherapie gegen Tumorzellen oder virale Antigene einzusetzen (HIRAO et al., 2000; LUDEWIG et al., 1999a; MANICKASINGHAM u. REIS, 2000; SCHULER u. STEINMAN, 1997). So konnten aus CD34+ humanen Blutzellen und aus Monozyten durch die Zugabe von GM-CSF und Zytokinen Zellen mit DC-Charakter gewonnen werden (TALMOR et al., 1998). DC sind in vivo in den meisten Geweben (z.B. Langerhanszellen in der Epidermis, in der afferenten Lymphe, in Herz, Nieren, IDC in den T-Zellarealen der lymphatischen Organe) vorhanden und können aus den verschiedenen Kompartimenten über die afferente Lymphe oder das Blut in die T-Zellareale der lymphatischen Organe einwandern. DC stellen jedoch keine einheitliche Gruppe von Zellen dar. So konnte gezeigt werden, dass DC aus mehreren verschiedenen Vorläuferzellen, aber auch verschiedene funktionelle Phänotypen von DC aus der gleichen Vorläuferzellen in Abhängigkeit von den Kulturbedingungen gewonnen werden können (GRABBE et al., 2000). Auch im Blut, in der Milz (STEINMAN et al., 1997), den Lymphknoten (DE ST GROTH, 1998; SALOMON et al., 1998) und den Peyerschen Platten (ANJUERE et al., 1999; VREMEC u. SHORTMAN, 1997) sind verschiedene Subtypen von DC anwesend. Die speziellen Fähigkeiten der DC scheinen nur in Relation zur Expression der Oberflächenmoleküle und zu ihrer Regulierung vor und während der Immunantworten zu stehen (BANCHEREAU u. STEINMAN, 1998). Im Vergleich zu anderen Antigenpräsentierenden Zellen wie B-Lymphozyten oder Makrophagen werden MHC- Produkte und MHC- Peptid-Komplexe auf den DC 10-100mal höher exprimiert. Des weiteren synthetisieren DC hohe IL-12-Spiegel, die die angeborene wie erworbene Immunabwehr stimulieren (CELLA et al., 1996; KOCH et al., 1996; SOUSA et al., 1997). Durch Freisetzung von Chemokinen können sie T- und B-Lymphozyten anlocken und das Überleben der rezirkulierenden T-Lymphozyten sichern. DC befinden sich in der afferenten Lymphe, sind aber nicht in der efferenten Lymphe nachzuweisen (INGULLI et al., 1997). So sind DC 48h 29 nach enger Interaktion mit T-Lymphozyten nicht mehr nachzuweisen. DC erhalten während einer Antigen-spezifischen Interaktion mit T-Lymphozyten auch Signale durch die TLymphozyten, u.a. durch Bindung des Fas-L, das die Apoptose der DC vermittelt (MATSUE et al.,). Der aktive Zelltod der DC stellt einen Mechanismus zur Herunterregulierung einer Immunantwort dar, um eine ständige Aktivierung von Antigen-spezifischen T-Lymphozyten zu vermeiden (VAN PARIJS u. ABBAS, 1998). Auch die Einleitung und das Aufrechterhalten der peripheren Toleranz benötigt ein Absuchen der DC durch die T-Lymphozyten. Die Kontakte sind notwendig, um potentiell reaktive Klone zu deletieren oder die Anergie zu versetzen. So sind DC in der Lage, apoptotische Zellen aus dem Intestinaltrakt, die beim physiologischen Zelluntergang anfallen, von Tumoren, nach Transplantationen oder nach Virusinfektion aufzunehmen, über die afferente Lymphe in die Lymphknoten zu transportieren und dort den rezirkulierenden T-Lymphozyten zu präsentieren (ALBERT et al., 1998a; ALBERT et al., 1998b; HUANG et al., 2000). Diese Wanderung tritt auch in Abwesenheit von Antigen oder Entzündungen auf, wie in SPF-Tieren gezeigt werden konnte. Im Gegensatz zur Nekrose führt die Aufnahme der apoptotischen Zellen jedoch nicht zur Ausreifung der DC. Diese sind deshalb nur in geringem Ausmaß fähig, eine Immunantwort gegenüber dem Selbstantigen auszulösen (SAUTER et al., 2000; STEINMAN et al., 2000b). Obwohl DC von großem Interesse für die Wissenschaft sind, ist der physikalische Kontakt in vivo in den lymphatischen Organen nicht weiter untersucht worden. Gerade bei klinischem Einsatz von DC bei neu entwickelten Impfschemata (DNS-Vakzinierung) oder in der Tumorbehandlung ist es von Interesse, Immunantworten über die Charakterisierung der Kontakte, das Wissen über die Funktion und die beteiligten Moleküle besser verstehen zu lernen und beeinflussen zu können. So ist nicht weiter bekannt, ob die Mikroumgebung wie die verschiedenen Kompartimente in den lymphatischen Organen die Interaktion beeinflusst, wie es für die Einwanderung über HEV in die lymphatischen Organe berichtet wurde. Auch der Einfluss der Oberflächenmoleküle auf die Interaktion von T-Lymphozyten und DC ist bislang nicht weiter untersucht worden. Es wurde in der vorliegenden Arbeit versucht zu klären, welcher Anteil der durch die lymphatischen Organe wandernden T-Lymphozyten Kontakte zu dendritischen Zellen ausbildet. Durch ein kongenes Rattenmodell konnten 30 injizierte Zellen auf Immunhistologien nachgewiesen werden und damit das Verhalten in vivo in den Kompartimenten aufgeklärt werden. 31 III. Material und Methoden 1. Geräte und Laborbedarf Geräte Autoklav Memmert, Schwabach Coulter Counter Coulter Counter Electronics, England Durchlichtmikroskop Fa. Carl Zeiss Jena GmbH, Jena Okular: Kpl W 12,5 Objektive: Zeiss 10x/ 0,22 Neofluar 25x/ 0,60 Zeiss 40x/ 0,65 IKA Schüttler, KS 501 D Fa. Janke u. Kunkel, IKA-Labortechnik, Staufen konfokales Mikroskop Objektive: Leica TCS, Benzheim Plan Apo, Immersionsöl 40x/ 1,0 Plan Apo, Immersionsöl 100x/ 1,4 Filtersätze: N2.1 für TRITC, Cy3, Alexa 568 I3 für FITC, Cy2, Alexa 488 Kryostat, Typ 1720 Leitz, Wetzlar pH-Meter, CG 840 Schott, Wiesbaden Photomikroskop Zeiss, Oberkochem +Mikroskopkamera MC 80DX Pipetten, einstellbar Zeiss, Oberkochem Eppendorf, Fa. Hinz, Hamburg (100-1.000µl, 20-200µl, 10-100µl, 1-20µl) Tischventilator FT-30 Salco, Bensheim Zentrifuge Universal 30 RF Hettich, Tuttlingen Zytozentrifuge Typ Cytospin Shandon INC., Pittsbourgh, USA 32 Geräte für Zellkulturarbeiten CO2-Brutschrank Heraeus, Hanau Pinzette, gebogen, anatomisch Aesculap, Tuttlingen Sterile Werkbank Mahl, Neuss Drahtnetz (Porengröße 0,4mm) Forschungswerkstatt der Medizinischen Hochschule Hannover Laborbedarf Kulturflaschen , 260ml Greiner, Frickenhausen Objektträger, 76 x 25mm, geputzt Menzel, Braunschweig Pipettenspitzen, gelb und blau Sarstedt, Nümbrecht PAP-Pen (Wachsstift) science service Blue caps, 50ml Falcon, Dänemark Becton Dickinson, Heidelberg 2. Puffer, Medien und Materialien PBS (Phosphat gepufferte Salzlösung) Serva, Heidelberg TBS (Tris gepufferte Salzlösung) Serva, Heidelberg TTBS (TBS mit 0,05% Tween) Merck, Darmstadt EDTA-Puffer (1mmol/l EDTA auf 1l Aqua dest., 0,372mg EDTA-Puffer, mit 1mol/l NaOH auf pH7,2 einstellen) Antiklotting-Medium ( 0,9% NaCl + 2,5mmol/l EDTA + 5%BSA, auf pH7,2 einstellen) 33 Schwinzerlyse (8,3g NH4Cl + 0,1g EDTA + 1,0g KHCO3 auf 1l Aqua dest.) in vitro Stimulation Kulturmedium (KM): RPMI 1640 Biochrom KG, Berlin mit 4mmol/l Glutamin Biochrom KG, Berlin 15 µmol/l Hepes ICN flow, Eschwege 100 U/ml Penicillin + 100µmol/lStreptomycin Biochrom KG, Berlin 0,1 nmol/l beta-Mercaptoethanol Merck, Darmstadt Medium 199/ Hanks’ Biochrom KG, Berlin fetales Kälberserum (FCS) Biochrom KG, Berlin 5’-Brom-2’-Desoxyuridin (BrdU) Sigma, Deisenhofen Trypanblau, 0.16% in NaCl Serva, Heidelberg 2% hitzeinaktiviertes Rattenserum in PBS laboreigene Herstellung: gepooltes Blut von LEW (RT7a) und LEW.7B(BH) Ratten wurde für 30 Min bei RT stehen gelassen, anschließend für 30 Min bei 800xg (RT) zentrifugiert, der Überstand in Blue caps aufgenommen und erneut für 30 Min bei 800xg (RT) zentrifugiert. Das so erhaltene Serum wurde in 5ml Portionen für 30 Min bei 56°C in Wasser inaktiviert und anschließend bei -20°C bis zur Verwendung gelagert Markierung der Mauszellen 2µmol/l 5-,6-carboxyfluorescein diacetat succinimidyl ester (CSFE 557) in PBS Molecular probes, USA DIG-NHS Boehringer Mannheim, Mannheim 34 (DIG-antibody labeling Kit Nr.1367200) Dimethylsulfoxid (DMSO) Immunhistologie PAP-Substrat 280mmol/l 3,3’-Diaminobenzidin Tetrahydrochlorid in 0,2% H2O2 in TTBS Sigma, Deisenhofen APAAP-Substrat 540µmol/l Naphthol-AS-MX-phospat Sigma N4875, Deisenhofen 2,5mmol/l Fast Blue oder 1mMol Fast Red Sigma, Deisenhofen 2% N,N-Dimethylformamid Fluka 40240, Buchs 1mmol/l Levamisol Sigma L 9756, Deisenhofen 0,1 mol/l Tris, pH 8,2 Fixierung: Paraformaldehyd (PFA) 4%ig: 8g Paraformaldehyd auf 200ml PBS pH 7,2 Methanol, z.A. (6009) Merck, Darmstadt Aceton, z.A. (14.2500) Merck, Darmstadt Hämatoxylin Fluka, Buchs Glycergel (Einschlußmittel C 563) Dako, Hamburg Moviol (4-88) Hoechst AG, Frankfurt 35 3. Antikörper Primäre Antikörper Tabelle 1 zeigt Antikörper (Spalte 2), die in der vorliegenden Arbeit für die Charakterisierung in der Immunhistologie eingesetzt worden sind. Soweit nicht anders beschrieben, wurden monoklonale Antikörper aus der Maus eingesetzt. Die Antikörper wurden mit verschiedenen Konjugationen eingesetzt (Spalte 3). Des weiteren wird die Verdünnung, der Isotyp des Antikörpers und die Veröffentlichung angegeben, in der der Einsatz des Antikörpers beschrieben wurde. Spezifität Antikörper/ Konjugat Isotyp Spezies Verdünnunga Referenz IgG1 Ratte 1:2, 1:5 Klon Anti-TCR R73b (HUNIG et al., 1989) Anti-CD28 JJ319 b IgG1 Ratte 1:2, 1:5 (TACKE et al., 1997) B-Lymphozyten HIS 14 IgG1 Ratte 1:50 (KROESE et al., 1987) Ratte 1:100 IgG1 Ratte 1:100 (KAMPINGA 1990) α-IgD CD45RC c His 41 biotinyliert et al., MHC Klasse II Ox 6 IgG1 Ratte 1:500 (FUKUMOTO et al., 1982) ICAM-1 1A29 IgG1 Ratte 1:300 1:500 (konfokal) (TAMATANI u. MIYASAKA, 1990) Ki-67 Antigen MIB5 IgG1 Ratte 1:5000 (SCHLUTER 1993) Interdigitierende dendritische Zellen NLDC-145d IgG 2a Maus 1:50 (KRAAL et al., 1986) (BREEL et al., 1987) Alkalische Phosphatase IgG Maus 1:150 biotinyliert IgG1 Maus 1:5000 Anti-DigoxigeninAP Anti-Fluoreszin B13-DE-1 biotinyliert a et al., (RIGBY et al., 1977) Die Verdünnung erfolgte, soweit nicht anders aufgeführt, für die primären Antikörper in der Ratte in 0,9% NaCl + 5% Rattenserum, 1:2. In der Maus erfolgte die Verdünnung in PBS + 5% Mäuseserum, zu gleichen Teilen. Die Verdünnung der biotinylierten Antikörper erfolgte in PBS und 20% Mäuseserum. b Zur Stimulierung der T-Lymphozyten wurden die Zellkulturüberstände dieser Hybridome eingesetzt. c Nachweis des RT7b Molekül nach Injektion von Zellen in kongene LEW (RT7a) d Wird in der Literatur auch als Multilektin-Rezeptor DEC-205 bezeichnet. Antikörper und sekundäre Nachweisreagenzien 36 Tabelle 2 zeigt die Antikörper und die sekundären Reagenzien, die in der vorliegenden Arbeit für den Nachweis gebundener Antikörper eingesetzt wurden. Soweit nicht anders beschrieben, wurden monoklonale Antikörper aus der Maus eingesetzt. Zusätzlich wird die Verdünnung, der Isotyp des Antikörpers und die Firma angegeben, die diesen Antikörper vertreibt. Spezifität Antikörper Konjugat Isotyp Verdünnunga Firma/ Vertrieb Kaninchen-Ig Alexa 568 CyTM 5 IgG 1:100 Dianova, Hamburg CyTM 3 IgG 1:100 Dianova, Hamburg Ig-Fraktion 1:50 Dako, Hamburg polyklonal (Ziege) Hamster-Ig Alexa 488 polyklonal (Ziege) Maus-Ig Z259, polyklonal (Kaninchen) Maus-Ig Ratten-Ig D651 APAAP 1:50 (in TTBS) Z494, polyklonal Dako, Hamburg b Dako, Hamburg 1:100 b Dako, Hamburg 1:100 Boehringer 1:100 (Kaninchen) Ratten-Ig D488 BrdU APAAP Peroxidase IgG1 Mannheim, Mannheim Alkalische Phosphatase- 1:50 Dako, Hamburg 1:50 Dako, Hamburg 1:500 Dianova, Hamburg Anti-Alkalische Phosphatase (APAAP) Peroxidase-AntiPeroxidase (PAP) Streptavidin-Peroxidase (SAAP) a die Verdünnung erfolgte, wenn nicht anders angegeben, in PBS und 5% Rattenserum b in TTBS + 5% Mäuseserum 37 4. Versuchstiere Als Versuchstiere wurden kongene Lewis-Rattenstämme eingesetzt. Durch den Polymorphismus im Gen RT7 (Allele RT7a und RT7b) exprimieren LEWIS (RT7a) und LEW.7B(BH) Rattenstämme zwei unterschiedliche Varianten der Protein-Tyrosin- Phosphatase, Rezeptor Typ C (Ptprc, CD45) (WONIGEIT, 1979). Das Gen RT7 wurde auch als ART-1, RT-Ly-1, T200 oder Leucocyte common antigen (L-ca) bezeichnet. Dabei kann das RT7B-Molekül durch den monoklonalen Antikörper His41 nachgewiesen werden (KAMPINGA et al., 1990). Bei einer Transplantation oder einer Injektion von Zellen eines Stammes in den anderen findet keine Abstoßungsreaktion statt und Zellen lassen sich in einem in vivo Modell verfolgen. Die Ratten wurden unter spezifiziert pathogenfreien Bedingungen (SPF) im Tierlabor der medizinischen Fakultät der Universität Manchester (naive, memory T-Lymphozyten-Versuche) und im Tierhaus der Medizinischen Hochschule Hannover (Effektor T-Lymphozyten-Versuche) gezüchtet und gehalten. Die Ratten wurden in Gruppen bis zu drei Tieren in Makrolonkäfigen Typ III auf staubfreiem Weichholzgranulat gehalten. Die in den Kontrollversuchen zum Nachweis der DC eingesetzten C57BL/6 Mäuse wurden in Makrolonkäfigen Typ II gehalten. Die Raumtemperatur lag bei 22±2°C, die relative Luftfeuchtigkeit bei 55±5%, die Belichtung fand von 07.00 bis 19.00 Uhr MEZ statt. Die Tiere wurden mit einem pelletierten, autoklavierten Haltungsfutter für Ratten/Mäuse der Firma Altromin GmbH (Lage) [Inhaltsstoffe: Rohprotein 19,00%, Rohfett 4%, Rohfaser 6,00%, Rohasche 7,00%, Rohwasser 10% und N-freie Extraktstoffe 54%; Zusatzstoffe (je kg): Vit. A 15.000 IE, Vit. D3 600 IE, Vit. E 75 mg, Kupfer 5 mg] gefüttert. Zur Wasserversorgung wurde steriles Leitungswasser aus Tränkeflaschen ad libitum bereitgestellt. Die Tiere wurden regelmäßig jedes Quartal auf das Vorkommen von Erregern entsprechend der Liste GV-SOLAS (1986) untersucht. Lymphozyten-Funktionsantigen-1-defiziente (LFA-1, αL/ β2, CD11a-/-/ CD18) Mäuse wie sie von BERLIN-RUFENACH et al. (1999) beschrieben wurden, wurden freundlicherweise von Frau Dr. N. Hogg, England, zur Verfügung gestellt. LFA-1-defiziente Mäuse wurden im Tierlabor des „Lymphocyte Molecular Biology Labratory“, London, gezüchtet und unter spezifisch pathogenfreien Konditionen in Übereinstimmung mit Regulationen des „United 38 Kingdom Home Office“ gehalten. Sie wurden routinemäßig auf Parasiten, Bakterien und Pilze untersucht und wurden für pathogenfrei befunden. Das Gewicht richtete sich nach dem Verwendungszweck und lag bei den Ratten zwischen 250-350g, bei den Mäusen zwischen 20-30g. Genehmigung: Das Tierversuchsvorhaben wurde von der Bezirksregierung Hannover unter der Nummer 60442502-94/716, ein Fortsetzungsantrag unter der gleichen Nummer und ein Neuantrag unter der Nummer 604-42502-99/166 genehmigt. 5. Gewinnung, Aufbereitung und Injektion von Subpopulationen der Lymphozyten 5.1. Naive und memory CD4+ T-Lymphozyten Durch die Kanülierung des Ductus thoracicus von Spendertieren konnte die Lymphe über mehrere Stunden gesammelt werden. Nach der von WESTERMANN et al. (1996) beschriebenen Aufbereitung der Zellen wurden jedem kongenen Empfängertier 20 x 106 naive (CD45RC+) oder memory (CD45RC-) CD4+ T-Lymphozyten in die Schwanzvene injiziert Die Empfängertiere wurden nach 30 Min (jeweils n=5 für Ratten mit naiven oder memory CD4+ T-Lymphozyten), nach 2 Stunden (n= 6, jeweils naive und memory), nach 24 Stunden (n=6 für naive, n=5 für memory) und nach 48 Stunden (n= 2 für naive, n= 1 für memory) unter Etheranästhesie durch Entbluten aus der Bauchaorta getötet. Es wurden die Milz, die mesenterialen Lymphknoten, sowie die Peyerschen Platten entnommen, in flüssigem Stickstoff eingefroren und bei -80°C gelagert. Von diesen Organen wurden anschließend Gefrierschnitte in einer Dicke von 5µm angefertigt, luftgetrocknet und bis zur weiteren Verwendung (s. 6.1.) in Aluminiumfolie gewickelt bei -20°C gelagert. 39 5.2. Effektor T-Lymphozyten Zwei LEW.7B(BH) Ratten wurden nach CO2-Begasung durch Herzpunktion entblutet. Die axillären, zervikalen, brachialen und mesenterialen Lymphknoten wurden unter sterilen Bedingungen entnommen und in einem Metallsieb (0,4mm Porendurchmesser) in maximal 50ml Medium-199/Hanks zerzupft und in ein 50ml Blue Cap aufgenommen. Anschließend wurde die Zellsuspension für 10 Min bei 400xg (bei 4°C) zentrifugiert, der Überstand verworfen und das Pellet in 20ml (4°C) neues Medium wieder aufgenommen. Nekrotische Zellen wurden beseitigt, indem die Zellsuspensionen mit 5ml FCS unterschichtet und danach bei 400xg für 10 Min (bei 4°C) zentrifugiert wurden. Nach zweimaligem Waschen in M199 wurde das Pellet in 10ml aufgenommen. Anschließend wurden die Zellen mit 0,16% Trypanblau in NaCl angefärbt und mikroskopisch eine Zellzählung der vitalen Zellen durchgeführt. Danach erfolgte eine Antikörperinkubation für 30 Min auf Eis. Dazu wurden die Zellen erneut zentrifugiert (200xg, 10 Min, 4°C) und mit den Kulturüberständen der Hybridome R73 (Antikörper gegen den αβ-T-Zellrezeptor gerichtet) und JJ319 (Antikörper gegen CD28 gerichtet) inkubiert, wobei für eine vollständige Antikörperanlagerung 1ml der optimalen Konzentration (1:2 bis 1:5 in M199, abhängig von der verwendeten Charge, durch Titration im Facs kontrolliert, beschrieben von BODE, 1998) des Kulturüberstandes auf 10 x 106 Zellen eingesetzt wurden. Nach erneutem Waschen und Zentrifugation bei 200xg für 10 Min bei 4°C wurde zur Markierung der aktivierten Zellen, wie bereits beschrieben (FRITZ et al., 1990) dem Kulturmedium 5µmol/l BrdU zugesetzt, das als Thymidinanalogon während der SPhase des Zellzyklus in die DNS eingebaut wurde. Zur Kreuzvernetzung der Antikörper wurden 260ml Kulturflaschen vor dem Gebrauch mit Ziegenantikörpern gegen Mausimmunglobuline (Maus-Ig, 3µg/ml) in PBS über Nacht bei 4°C beschichtet. Der überschüssige Antikörperanteil wurde vor der Eingabe der Zellen zweimal mit PBS ausgewaschen (TACKE et al., 1995). Die jeweiligen Zellsuspensionen mit einer Zelldichte von 1 x 106 Zellen/ml wurden bei 37°C und einer 5% CO2-Konzentration für 72 Stunden im Brutschrank inkubiert. BODE (1998) konnte mit dieser Methode 78,8 ± 6,1% der Zellen nachweisen, die BrdU eingebaut hatten. Von diesen Zellen war der überwiegende Teil 40 T-Lymphozyten, die jeweils etwa zur Hälfte CD4+ und CD8+ gewesen sind. Kontrollexperimente zur Messung des BrdU-Einbaus wurden im ELISA durchgeführt und ebenfalls von BODE (1998) beschrieben. Um die mit BrdU markierten 20-100 x 106 Lymphknotenzellen zu injizieren, wurden männliche LEW-Ratten (RT7a) mit Ethylether narkotisiert und die Zellen intravenös (i.v.) in 1ml M199 in die Schwanzvene gegeben. Die Ratten wurden nach 1h (n=3), 9h (n=4), 24h (n=8), 72h (n=4) und 96h (n=3) erneut narkotisiert und durch Öffnen der Aorta abdominalis entblutet. Die Lymphknoten, die Peyerschen Platten und die Milz wurden entnommen, in flüssigem Stickstoff eingefroren und bei -80°C gelagert. Von diesen Organen wurden 5-7µm dicke Gewebeschnitte angefertigt, an der Luft getrocknet und anschließend bis zur weiteren Verwendung (s. 6.2.) in Aluminiumfolie bei -20°C gelagert. 6. Darstellung der Membrankontakte auf immunhistologisch gefärbten Gewebeschnitten 6.1. Darstellung der Membrankontakte zwischen naiven oder memory CD4+ TLymphozyten mit interdigitierenden dendritischen Zellen in den T-Zellarealen der lymphatischen Organe Die Färbung und Fixierung der Präparate erfolgte nach bereits etablierter Methode (WESTERMANN et al., 1997). Die Fixierung wurde durch eine 10 minütige Inkubation (bei -20°C) in Methanol und Azeton zu gleichen Teilen vorgenommen. Anschließend erfolgte eine Spülung mit 0,05% Tween 20 in TBS. In einem ersten Schritt wurde der monoklonale Antikörper gegen das interzelluläre Adhäsionsmolekül-1 (ICAM-1, 1A29) in einer Verdünnung von 1:300 (in 0,9% NaCl und 5% Rattenserum) für 30 Min auf die Objektträger aufgebracht, das sowohl von dendritischen Zellen wie auch von B-Lymphozyten exprimiert wird. Alternativ dazu wurde der monoklonale Maus-Antikörper anti-IgD in einer Verdünnung von 1:100 (in 0,9% NaCl und 5% Rattenserum) verwendet. Nach zweimaligem Waschen in PBS erfolgte eine zweite Inkubation für 30 Min mit einem Brückenantikörper Kaninchen-anti- 41 Maus in der Verdünnung von 1:50 (in PBS und 5% Rattenserum). Nach zweimaligem Waschen in PBS wurde der Brückenantikörper erneut für 15 Min aufgetragen und wieder abgespült. Anschließend wurde zur Wiedererkennung der injizierten Spender-T-Lymphozyten des PVG.7B Stammes der biotinylierte Antikörper His 41 (1:100, 30 Min, in PBS und 20% Mäuseserum), gefolgt von Avidin-Peroxidase (30 Min) verwendet. Für die Anfärbung der Spenderzellen in braun wurde Diaminobenzidin eingesetzt. Die dendritischen Zellen (s.Abb.1, S. 53), beziehungsweise die B-Lymphozyten (s.Abb.4, S. 60) wurden mit dem Substrat Fast Blue in blau sichtbar gemacht. Anschließend wurden die Gewebeschnitte in 70%igem Ethanol (30 Min) fixiert und luftgetrocknet. Hämatoxylin diente in den meisten Fällen als Gegenfärbung. Die Präparate wurden mit Dako-Glycergel eingedeckelt und wie in 9.1. beschrieben ausgewertet. 6.2. Darstellung der Membrankontakte von Effektor T-Lymphozyten mit IDC in den TZellarealen der lymphatischen Organe Die Gewebeschnitte der Milz, der Lymphknoten und der Peyerschen Platten der Empfängertiere nach Injektion von aktivierten Lymphknotenzellen wurden untersucht. Diese wurden bei -20°C für 10 Min in gleichen Teilen Methanol/Aceton fixiert und danach in TTBS gewaschen. Alle nachfolgenden Inkubationsschritte erfolgten 30 Min bei Raumtemperatur (RT) in einer feuchten Kammer. Die Objektträger wurden mit dem primären Antikörper inkubiert, um die injizierten LEW.7B(BH)-Lymphozyten (mAb His41) und die Expression von ICAM-1 (mAb 1A29) auf den dendritischen Zellen darzustellen. Nach zweimaligem Waschen in TTBS wurden die Zellen mit dem sekundären Antikörper Z259 (Kaninchen-anti-Maus, 1:50 in PBS + 5% RS) inkubiert. Nach erneutem Waschen in TTBS wurde der tertiäre Antikörper (D651, Maus-APAAP, 1:50 in TBS-Tween) auf die Präparate gegeben. Zur Verstärkung des Signals wurde die Inkubation mit dem sekundären und tertiären Antikörper für jeweils 15 Min wiederholt. Das Oberflächenantigen, an das der primäre Antikörper (His41) gebunden hatte, wurde durch die Inkubation des APAAP-Substrates mit Fast Blue in blau visualisiert (WESTERMANN u. PABST, 1996; WILLFUHR et al., 1989). Nach gründlichem Spülen 42 wurden die Präparate in 70%igem Ethanol für 30 Min fixiert und für weitere 30 Min vor dem Ventilator getrocknet. Um das eingebaute BrdU zu detektieren, wurden die Präparate mit Formamid und NaOH denaturiert. Dazu wurden 190ml Formamid auf 70°C erwärmt und dann 8 Min mit 100mmol/l NaOH gemischt. In diesem Gemisch wurden die Objektträger 30 sec inkubiert. Nach Waschen in 70°C warmen TTBS wurden die Präparate für 15 Min in 70°C warmen Formamid mit 7,5mmol/l Trinatriumcitrat inkubiert. Darauf erfolgte ein Spülen in eiskaltem TBS für 15 Min und eine Fixierung mit 1% Formaldehyd bei RT. Des weiteren wurden sie mit TTBS gewaschen und 10 Min mit 0,2% Glutaraldehyd bei RT fixiert. Nach erneutem Spülen in TTBS wurden die Objektträger über Nacht mit 50µl Anti-BrdU-Antikörper (1:500, in TBS + 5% Rattenserum, 1:2) im Kühlschrank inkubiert. Nach Abspülen des überschüssigen Antikörpers mit TTBS wurden die Objektträger mit dem APAAP-Komplex inkubiert und die Inkubationsschritte ein zweites Mal für jeweils 15 Min wiederholt. Zur Darstellung des BrdU wurden 2mg Fast Red mit 3ml APAAP vorsichtig vermischt und für 10 Min bei RT stehen gelassen. Anschließend wurden die Präparate für genau 25 Min damit inkubiert. Wie in Abb.10 (s. S. 73) zu erkennen ist, waren die injizierten T-Lymphozyten nach dieser Färbung in blau, BrdU+ Zellen anhand eines roten Kernes zu erkennen. Dendritische Zellen stellten sich durch den Nachweis des ICAM-1 auf ihrer Oberfläche in braun dar. Nach gründlichem Waschen mit TTBS wurden die Präparate mit Hämatoxylin gegengefärbt. Die fertigen Präparate wurden mit Dako Glycergel eingedeckelt. 6.3. Herstellung und Färbung von Blutzytospots Um die injizierten Zellen im Blut der Empfängertiere zu detektieren und auszuzählen, wurden 500µl Blut mit 10ml Schwinzerlyse versetzt und für 10 Min inkubiert. Anschließend wurden die Leukozyten zentrifugiert (400xg, 10 Min, RT). Diese Zellen (1 x 106 Zellen/ml) wurden in Antiklotting-Medium (0,9%NaCl, 2,5mmol/l EDTA, 5% BSA bei pH 7,2) aufgenommen und bei 200xg für 8 Min bei RT in einer Zytozentrifuge auf Objektträger aufgebracht. Anschließend wurden diese getrocknet und bis zur immunzytologischen Färbung (s. 6.4.) bei 20°C gelagert. 43 6.4. Darstellung der Zellen im Zellzyklus Der monoklonale Antikörper MIB5 reagiert mit dem nukleären Protein „Ki-67“, das während aller aktiven Phasen des Zellzyklus (G1-M2) in der Ratte exprimiert wird und mit der Zellproliferation assoziiert wird (GERLACH et al., 1997). Die Spezifität des Antikörpers in der Immunhistochemie und bei anderen Analysen ist von CATTORETTI et al. (1992) und SCHLUTER et al. (1993) beschrieben worden. Zur Darstellung der Ki-67+-Zellen wurden Zytospots vom Blut (s. 6.3.) und 5-7µm dicke Gefrierschnitte der Milz und der Lymphknoten nach Injektion von naiven, memory (s. 5.1.) und aktivierten (s. 5.2.) T-Lymphozyten immunhistochemisch angefärbt. Dabei wurde, wie bereits für die Darstellung von BrdU (siehe 6.2.) beschrieben, zuerst eine Oberflächenfärbung und nach Denaturierung die Färbung des Zellkernantigens durchgeführt. Nach dem Trocknen der Gewebeschnitte und Einkreisen mit dem PAP-Pen wurden die Präparate für 10 Min bei -20°C in einem Gemisch von Methanol/Aceton zu gleichen Teilen fixiert und danach zweimalig in PBS gewaschen. Im weiteren wurden die Objektträger für 30 Min bei RT mit 50µl des primären Antikörpers inkubiert, um auf der Oberfläche der Zellen ICAM-1 (1A29, 1:300, in 0,9%NaCl und Rattenserum, zu gleichen Teilen) zu identifizieren. Nach zweimaligem Spülen in PBS wurden die Präparate bei 4°C für 45 Min in Paraformaldehyd (PFA) fixiert und anschließend zweimal in TBS gewaschen. Daraufhin wurden die Gefrierschnitte mit dem sekundären Antikörper, einem Kaninchenantikörper gegen Maus-Ig (1:50, in PBS und 5%Rattenserum, 1:2) für 30 Min auf dem Schüttler inkubiert und einmal in TBS/Tween abgewaschen. Eine weitere Inkubation erfolgte mit einem Maus-APAAPAntikörper für 30 Min bei RT. Die letzten beiden Inkubationsschritte wurden jeweils für 15 Min wiederholt. Die Identifizierung der injizierten LEW.7B(BH) Lymphozyten erfolgte durch die Inkubation mit dem biotinylierten, monoklonalen Antikörper His41 (His41-Biotin in PBS und 20% Mäuseserum, 1:100), wie bereits unter 6.2. beschrieben. Die Inkubation erfolgte für 1h bei 4°C in einer feuchten Kammer. Zur Visualisierung des biotinylierten His41 wurden die Präparate für 45 Min bei RT mit Streptavidin alkalische Phosphatase (in PBS und 5% Rattenserum) inkubiert, in TBS gewaschen und für 10 Min in Benzidin (4ml TBS/Tween mit 80µl H2O2 und 160µl Benzidin) inkubiert. Anschließend wurden die Oberflächenantigene 44 durch 25minütige Inkubation des APAAP-Substrates und Fast Blue in blau visualisiert, gewaschen, für 30 Min mit 70%igem Ethanol fixiert und anschließend getrocknet. Zur Darstellung des Zellkernantigens Ki-67 wurden die Zellen in EDTA (0,372g/l, pH 7,2) in 90°C warmen Wasserbad für 45 Min denaturiert. Daraufhin erfolgte ein zweimaliges Spülen in eiskaltem TBS für jeweils 10 Min. Über Nacht wurde der Antikörper zur Darstellung von Ki-67 (Mib5, 1:5000, in PBS, 1% BSA und 0,1NaN3) auf die Objektträger aufgebracht. Nachdem der überschüssige Antikörper durch Spülen mit PBS entfernt worden ist, erfolgte die Visualisierung des APAAP-Komplexes mit Fast Red, so dass proliferierende Zellen durch einen roten Kern zu identifizieren waren. Wie in der Darstellung des BrdU in 6.2. stellen sich dendritische Zellen durch die Expression von ICAM-1 in braun, injizierte T-Lymphozyten in blau dar. Mib+ Zellen lassen sich durch einen roten Zellkern differenzieren (ähnlich der Abb.10, S.73, keine eigene Darstellung). Nach einer Gegenfärbung für 30 sec mit Hämatoxylin wurden die fertigen Präparate mit Glycergel eingedeckelt. 6.5. Darstellung der BrdU+ Effektor T-Lymphozyten Wie unter 5.2. beschrieben, wurden Lymphknotenzellen gewonnen und mit Antikörpern gegen den TCR und CD28 (1:2 bis 1:5 abhängig von der Charge) für 30 Min auf Eis inkubiert. Um herausfinden zu können, welcher Anteil der injizierten T-Lymphozyten sich innerhalb der untersuchten Organe in der S-Phase befindet, wurde abweichend von dieser Beschreibung dem Kulturmedium kein BrdU zugesetzt. Zur Kreuzvernetzung der Antikörper wurden die Zellen für 72h bei 37°C und einer 5% CO2-Konzentration in Kulturflaschen inkubiert, die zuvor mit Ziegenantikörpern gegen Maus-Ig (3µl/ml) beschichtet worden waren. Die Injektion erfolgte wie in 5.2. beschrieben in die Schwanzvene. Nach 24h (n=2) und 72h (n=10) wurden die Tiere durch Entbluten getötet und die Organe entnommen. Eine Stunde vor der Entblutung erfolgte unter Ethernarkose eine intravenöse Injektion von 5mg BrdU/ 100g Körpergewicht. Alle Zellen, die sich innerhalb dieser Stunde in der S-Phase befunden haben, haben BrdU eingebaut. Es wurden Gewebeschnitte angefertigt und die Darstellung der Zellen erfolgte wie bereits in 6.2. beschrieben. 45 7. Immunhistologisch gefärbte Gewebeschnitte in der konfokalen Mikroskopie Naive und memory T-Lymphozyten wurden, wie bereits unter 5.1. beschrieben, gewonnen und die Milz 24h nach Injektion der Spenderlymphozyten aufbereitet (jeweils n=3). Es wurden 14µm dicke Gewebeschnitte der Milz angefertigt und auf Gelatine-beschichtete Objektträger aufgebracht. Die Gefrierschnitte wurden dabei mit einem Wachsstift (PAP-Pen) umrandet und 1-2 Stunden bei Raumtemperatur getrocknet. Die Präparate wurden für 10 Min in einem Gemisch von Methanol/Aceton zu gleichen Teilen fixiert und anschließend für 3 x 5 Min in TBS mit Tween 20 gewaschen. Anschließend wurde die Vorinkubationslösung (PBS+BSA+1% NaN3+10% Ziegenserum) auf die Schnitte aufgetragen und diese für 1 h in einer feuchten Kammer bei RT inkubiert. Nach der Inkubation wurden die Objektträger 3 x 5 Minuten in TBS + Tween gewaschen und danach der in PBS+1%BSA+0,1%NaN3 verdünnte primäre Antikörper (ICAM-1, 1:500) aufgegeben. Der nichtgebundene Anteil des primären Antikörpers wurde nach einer Stunde durch erneutes Waschen in TTBS entfernt und anschließend der fluorochrom-markierte sekundäre Antikörper (Alexa 568, 1:100, in PBS+5% Rattenserum) aufgegeben und in einer feuchten Kammer 1 h im Dunkeln inkubiert. Zur Darstellung der injizierten T-Lymphozyten wurde der zweite primäre Antikörper (His41bio, 1:100, in PBS+10% Mäuseserum) auf die Objektträger aufgegeben und für 1h inkubiert. Nach wiederholtem Waschen wurde der zweite, Fluorochrom-markierte sekundäre Antikörper, Alexa 488 (1:100, in PBS+5% Rattenserum) für 1h aufgetragen. Nach 3 x 5 Min Spülen in TTBS wurden die Objektträger mit Moviol eingedeckelt. Wie in Abb.6 (S.63/ 64) zu erkennen ist, stellten sich die injizierten T-Lymphozyten anschließend in der roten Fluoreszenz, die ICAM-1+ DC in der grünen Fluoreszenz dar. Die Schnitte wurden mittels konfokaler Laserscanning-Mikroskopie untersucht. Nach Anregung der Fluorochrome bei 488nm und 568nm mit einem Laser wurden für die Übersichtsaufnahmen 11-17 Schnitte im Abstand von 0,5µm mit dem 40er Objektiv bei unterschiedlichen Nachvergrößerungen aufgenommen und im ‘extended focus’-Modus übereinander projiziert. Zur Dokumentation von Detailaufnahmen der Membrankontakte zwischen den injizierten, kongenen T-Lymphozyten und dendritischen Zellen wurde ein 100 x 46 Ölimmersions-Objektiv (numerische Apertur 1,4) verwendet und einzelne Schnitte im 0,5µm Abstand gespeichert. Diese wurden als Einzelschnitte untersucht oder in einer Projektion betrachtet. Die Bilder wurden digital nachbearbeitet (Adobe Photoshop 4.0). Zur photographischen Dokumentation wurden Ekta Chrom 64 Filme von Kodak verwendet. 8. Darstellung von Membrankontakten zwischen T-Lymphozyten und IDC im Mausmodell 8.1 Darstellung der Expression des Multilektin-Rezeptors DEC-205 auf interdigitierender dendritischer Zelle im T-Zellareal der Milz Die Milz von 12 Wochen alten C57BL/6 Mäusen wurde entnommen, tiefgefroren und daraus Gewebeschnitte hergestellt. Diese wurden für 10 Min bei -20°C in einem Gemisch von Methanol/Aceton fixiert und danach gewaschen. Die Objektträger wurden für 30 Min mit dem primären Antikörper NLDC-145 (non-lymphoid dendritic cell antigen of 145 kDa, 1:50) inkubiert, um die dendritischen Zellen im T-Zellareal der Milz über die Expression des Multilektinrezeptors DEC-205 darzustellen. Nach erneutem Waschen wurden die Präparate mit dem sekundären Antikörper Z494 (1:100 mit PBS und 5% Mäuseserum) für 30 Min inkubiert, gewaschen und mit dem tertiären Antikörper D488 (1:100) für weitere 30 Min inkubiert. Zur Verstärkung der Bindung wurde die Inkubation mit dem sekundären und tertiären Antikörper für jeweils 15 Min wiederholt. Die Darstellung des Oberflächenantigens des primären Antikörpers erfolgte durch die Inkubation des APAAP-Substrates mit Fast Blue. Nach gründlichem Spülen wurden die Präparate mit Hämatoxylin für 30 Min gegengefärbt und anschließend mit Dako-Glycergel eingedeckelt. Wie in Abb.8 (S.68) zu erkennen, stellen sich die dendritischen Zellen in blau dar. 47 8.2 Nachweis von Membrankontakten zwischen markierten Wildtyp- oder LFA-1-defizienten Zellen und DC in der PALS der Maus Zur Markierung der Zellen wurden C57BL/6 und LFA-1-defiziente (CD11a-/-/ CD18) Mäuse im Alter von 12 Wochen durch Genickbruch getötet und die Milz und der mesenteriale Lymphknoten entnommen. In einem engmaschigen Drahtnetz (Porengröße 0,4mm), bedeckt mit Medium 199, wurde vorsichtig das Fett entfernt und die Organe zerzupft. Die so gewonnenen Zellsuspensionen wurden bei 400xg für 10 Min bei RT zentrifugiert, der Überstand abgesaugt und die Zellen in M199 wieder aufgenommen. Durch die Zugabe von 25ml Schwinzerlyse für 10 Min wurden die Erythrozyten lysiert und durch Zentrifugation bei 400xg für 10 Min entfernt. Die Zellen wurden wiederholt in PBS gewaschen und in 12ml resuspendiert. Nach Zugabe von 10ml PBS pH7,2 wurden die Zellen erneut für 10 Min bei 400xg zentrifugiert, anschließend in 1ml PBS aufgenommen und bis 2ml aufgefüllt. Anschließend wurden die Zellen mit 0,16% Trypanblau in NaCl angefärbt und mikroskopisch eine Zellzählung der vitalen Zellen (80-210 x 106 Zellen) durchgeführt. Zum Nachweis der Zellen in den Empfängermäusen wurde ein Teil der Zellsuspension mit Fluoreszenzmarker CSFE markiert. Da gleichzeitig Spenderzellen aus LFA-1-defizienten Mäusen, aber auch von Wildtypmäusen intravenös in Wildtypmäuse injiziert wurden, wurden die Zellsuspensionen mit zwei unterschiedlichen Markierungen (CSFE und DIG-NHS) versehen. Dazu wurden 50 x 106 Zellen (in 2ml) mit einer 2µmol/l CSFE-Lösung (in PBS) für 30 Min bei 37°C inkubiert. Zur Markierung des anderen Anteils der Zellsuspension mit DIGNHS wurden 50 x 106 Zellen in 60µg DIG-NHS für 15 Min bei RT inkubiert. Nach der Markierung wurden die Zellen in PBS gewaschen, bei 400xg für 10 Min bei RT zentrifugiert und in 1200µl PBS+0,1%BSA resuspendiert. Um einen Einfluss der Markierung auf das Wanderungsverhalten der Zellen ausschließen zu können, wurde die Markierung für die LFA-1-defizienten Zellen und die Wildtypzellen gewechselt. Als Empfängertiere dienten 12 Wochen alte männliche Wildtypmäuse (C57BL/6), die 300µl eines Gemisches aus CSFE- und DIG-NHS-markierten (Wildtypzellen und LFA-1defiziente Zellen in wechselnder Markierung) Zellen i. v. in die Schwanzvene erhalten haben. Nach 2h wurden die Empfängermäuse durch Genickbruch getötet, die Milz entnommen und tiefgefroren. Wie unter 8.1. beschrieben, wurden Gewebeschnitte hergestellt und nach einer 48 Fixierung in Methanol/Aceton der primäre Antikörper NLDC-145 (1:50) und im Falle der Darstellung der CSFE-Markierung der Antikörper B13-DE-1bio (1:5000) aufgegeben. Nach gründlichem Waschen wurden die Objektträger mit dem sekundären (Z494, 1:100 in TTBS + 5% Mäuseserum) und dem tertiären (D488, 1:100 in TTBS + 5% Mäuseserum) Antikörper für jeweils 30 Min inkubiert und beide Schritte nach erneutem Waschen für jeweils 15 Min wiederholt. Zuzüglich zu den DC in der PALS wurden die vor der Injektion markierten Zellen dargestellt. Um Zellen darzustellen, die mit DIG-NHS markiert worden sind, wurden die Präparate mit anti-Dig P (1:150 in PBS + 5% Mäuseserum) für 30 Min inkubiert, gewaschen und für 10 Min mit Benzidin inkubiert. Durch die anschließende Inkubation des APAAPSubstrates mit Fast Blue für 25 Min wurde das Oberflächenantigen des primären Antikörpers visualisiert. Zellen, die mit CSFE markiert worden waren, wurden für 30 Min mit Streptavidin-Phosphatase inkubiert, im weiteren, wie zuvor beschrieben, mit Benzidin und anschließend Fast Blue dargestellt. Injizierte Zellen wiesen damit eine braune Färbung auf. Dendritische Zellen waren in blau zu erkennen (siehe Abb.8, S.68). Alle Präparate wurden mit Dako-Glycergel eingedeckelt. 9. Auswertung 9.1. Ermittlung der Anzahl von Membrankontakten zwischen den injizierten TLymphozyten und den dendritischen Zellen in den sekundär lymphaischen Organen In den T-Zellarealen der Milz, des Lymphknotens und der Peyerschen Platten wurden mindestens 200 injizierte T-Lymphozyten gezählt und von diesen der Anteil ermittelt, die sich in direktem Membrankontakt zu ICAM-1+ dendritischen Zellen befinden. Dabei wurden 3-6 Gewebeschnitte eines jeden Organs des jeweiligen Empfängertieres begutachtet und in die Auswertung einbezogen. Für den Zeitpunkt 24h nach Injektion wurden für naive (n=6), für memory (n=5) und für Effektor (n=7) Empfängertiere ausgewertet und aus diesen Mittelwert und Standardabweichung errechnet. Für die weiteren Zeitpunkte wurden 3 bis 5 unabhängige Versuche ausgewertet. 49 9.2. Ermittlung der Anzahl von Membrankontakten mit der konfokalen Mikrospkopie In einer 100er Vergrößerung der PALS wurden in der Teilprojektion (computergestützte Übereinanderlagerung von 9 Einzelschnitten) einzelne injizierte Lymphozyten ausgewählt und eingeteilt, ob sie einen Membrankontakt mit einer DC aufweisen (mit/ohne Kontakt). Diese Zellen wurden über die Einzelschnitte verfolgt, um festzustellen, in wie vielen Schichten die Zellen Kontakt haben und wie der Kontakt ausgebildet ist. Durch Einzelschnitte, die ober- und unterhalb der Teilprojektion gelegt worden waren, konnte zudem analysiert werden, ob die ausgewählten T-Lymphozyten weitere Membrankontakte aufwiesen. Es wurden 24h nach Injektion Präparate von naiven und memory T-Lymphozyten (je n=3) ausgewählt. Es wurden pro Tier 3 bis 5 Ausschnitte der PALS ausgewertet. 9.3. Ermittlung der Membrankontakte im Mausmodell Milz- und Lymphknotenzellen aus Wildtypmäusen und aus LFA-1-defizienten Mäusen wurden wechselweise mit CSFE oder Digoxigenin markiert und gleichzeitig zu gleichen Anteilen in Wildtypmäuse injiziert. Zwei Stunden nach der Injektion wurde die Milz der Empfängertiere entnommen und die unter 8.2. beschriebenen Immunhistologien ausgewertet. Dabei wurde zum einen der Anteil der empfängereigenen (endogenen) Zellen bestimmt, die Membrankontakt zu DC in der PALS aufgewiesen haben. Zum anderen wurde die Anzahl der markierten Zellen ausgewertet und unter diesen der Anteil der Zellen mit einem Kontakt zu DC bestimmt. Es wurden jeweils n=6 Tiere für die Markierung mit CSFE und Digoxigenin ausgewertet, wobei für jeden Versuch mindestens 3 Schnitte ausgewertet wurden. Es wurden Mittelwert und Standardabweichung errechnet. 9.4. Ermittlung des Prozentsatzes von T-Lymphozyten im Zellzyklus oder in der S-Phase im Blut Nach 24h und 72h wurde der Prozentsatz der Lymphozyten im Zellzyklus (Ki-67+) oder in der S-Phase (BrdU+) ermittelt. Dazu wurden mindestens 100 His41+ injizierte Lymphozyten 50 identifiziert und der prozentuale Anteil daran bestimmt, der sowohl His41+, als auch BrdU+ oder Mib+ war. Aufgrund des geringen Prozentsatzes BrdU+ Lymphozyten wurden nur etwa 20-40 dieser Zellen ermittelt. Es wurden Mittelwert und Standardabweichung von 2-10 Versuchen errechnet. 9.5. Ermittlung von Membrankontakten von T-Lymphozyten im Zellzyklus oder in der S-Phase mit DC in der Milz In immunhistologischen 3-fach Färbungen der Milz sind 1h, 9h, 24h, 72h und 96h nach Injektion der kongenen Spenderzellen die His41+ T-Lymphozyten analysiert worden, die einen Kontakt zu einer DC hatten und daran der Anteil ausgewertet, der sich im Zellzyklus (Mib+) befand. Zum Vergleich dazu wurde der Anteil der His41+-Mib+ ermittelt, die keinen Kontakt mit DC hatten. In der Milz wurde zuzüglich zwischen einem inneren und äußeren Anteil der PALS unterschieden. Mit dem gleichen Prinzip sind Präparate von Tieren ausgewertet worden, die eine Stunde vor der Organentnahme BrdU intravenös erhalten hatten. Es sind die Zeitpunkte 24h und 72h nach Injektion ausgewertet worden. Es wurden mehrere Organschnitte von jeweils 2-10 unabhängigen Versuchen ausgewertet. 10. Verwendete Computerprogramme und Statistik Zur Auswertung der computergespeicherten konfokalen Bilder wurde das Programm confocal assistant und Adobe Photoshop, Version 4.0 verwendet. 10.1. Statistik Die Daten wurden mit SPSS für Windows Version 6.0 oder Version10.0 (SPSS Inc., Chicago, IL, USA) erfasst. Mittelwerte und Standardabweichung wurden errechnet. Als nichtparametrische Tests dienten entweder der Mann-Whitney-U-Test oder der Wilcoxon Test. 51 Unterschiede wurden als statistisch signifikant angesehen, wenn in einem der Tests p<0,05 erreicht wurde. 10.2. Graphik Die graphische Verarbeitung der Daten erfolgte mit Sigma Plot Version 5.0 (Scientific Graphing Software, Jandel Cooperation, Erkrath). 52 IV. Ergebnisse A. Untersuchung der Membrankontakte von T-Lymphozyten mit interdigitierenden dendritischen Zellen in den sekundär lymphatischen Organen der Ratte Als prädominanter Ort der Sensibilisierung von T-Lymphozyten gegenüber ihrem spezifischen Antigen und der Regulation vieler T-Zellabhängigen Immunantworten sind die sekundär lymphatischen Organe bekannt. Die Ausübung dieser Funktionen setzt die Kolokalisation von 2 verschiedenen Populationen von Leukozyten voraus: die TLymphozyten und die dendritischen Zellen. Aus diesem Grunde war es wichtig, im vorliegenden in vivo Modell sowohl die T-Lymphozyten, als auch die interdigitierenden dendritischen Zellen immunhistologisch in der Milz, den Lymphknoten und den Peyerschen Platten identifizieren zu können. 1. Injizierte T-Lymphozyten und interdigitierende dendritische Zellen können auf immunhistologisch gefärbten Gewebeschnitten identifiziert werden. Im kongenen Rattenmodell konnte festgestellt werden, welche Anzahl von T-Lymphozyten in Membrankontakt zu den interdigitierenden dendritischen Zellen lag. Durch die Separation von naiven und memory T-Lymphozyten über die Expression der hohen (CD45RChigh) oder niedrigen (CD45RClow) Isoform des allgemeinen Leukozytenantigens und die polyklonale Aktivierung über den T-Zellrezeptor und CD28 konnten verschiedene Aktivierungszustände beobachtet werden. In Abb. 1A ist die Milz zu erkennen. Um die Zentralarterie herum befindet sich die periarterioläre lymphatische Begleitscheide (PALS), in der sich vorwiegend T-Lymphozyten und nur wenige B-Lymphozyten befinden. Angrenzend sind Follikel zu erkennen, die sich durch die gut demarkierte Marginalzone von der roten Pulpa unterscheiden lässt. Auch im 53 Lymphknoten und in den Peyerschen Platten sind T-Zellareale zu sehen, in denen sich zahlreiche injizierte T-Lymphozyten differenzieren lassen. Im Lymphknoten (Abb. 1C) lassen sich die T-Lymphozyten überwiegend im Parakortex ausmachen. Angrenzend ist der Kortex mit einem Follikel zu sehen. Die Medulla ist in diesem Anschnitt nicht zu erkennen. Betrachtet man einen vergrößerten Ausschnitt der PALS in Abb. 1B, so lassen sich zahlreiche injizierte, in braun angefärbte T-Lymphozyten erkennen. Daneben sind über die Expression des interzellulären Adhäsionsmolekül-1 (ICAM-1) in blau angefärbte Zellen zu erkennen, die interdigitierende dendritische Zellen darstellen. Bei der Auswertung von Immunhistologien der lymphatischen Organe wurden verschiedene Kriterien zur Identifizierung der DC zu Grunde gelegt, da bislang kein monoklonaler Antikörper in der Ratte zur Verfügung steht. Reife DC exprimieren auf ihrer Oberfläche das Molekül ICAM-1 sowie MHC II. Diese lassen sich über monoklonale Antikörper (1A29, respektive Ox6) nachweisen. Ein zweites Kriterium ist die charakteristische Morphologie der DC, die zur Unterscheidung herangezogen wurde. Neben einem großen Zellkern besitzen DC zahlreiche blattähnliche Zellausläufer, die sich in alle Richtungen von der Zelle aus erstrecken und die diesen Zellen ihren Namen verliehen haben. Die Lokalisation der ICAM-1+-DC im T-Zellareal der lymphatischen Organe stellt das dritte Kriterium dar. B-Lymphozyten und auch Makrophagen exprimieren ebenfalls ICAM-1 und MHC II auf ihrer Oberfläche. Wie in Abb.1A zu erkennen ist, ist die Expression von ICAM-1 auf den BLymphozyten jedoch schwächer und ermöglicht eine deutliche Abgrenzung der Kompartimente. Aus diesem Grunde wurden in den nachfolgenden Versuchen DC über die Expression von ICAM-1 nachgewiesen. Des weiteren weisen B-Lymphozyten eine zumeist runde Morphologie auf und sind deutlich kleiner als die DC und befinden sich in der Hauptsache in den an die PALS grenzenden Follikeln. B-Lymphozyten erleichtern so die Abgrenzung zwischen roter und weißer Pulpa. Makrophagen lassen sich aufgrund ihrer unregelmäßigen Konturen von DC und B-Lymphozyten unterscheiden und sind in der PALS nur selten anzutreffen. 54 Abb. 1 Im kongenen Rattenmodell können die den Empfängertieren injizierten T-Lymphozyten durch den mAb His41 und interdigitierende dendritische Zellen durch die hohe Expression von ICAM-1 nachgewiesen werden. Dargestellt sind immunhistologisch gefärbte Gewebeschnitte der Milz, des mesenterialen Lymphknotens und der Peyerschen Platten. Naive (CD45RChigh) und memory (CD45RClow) CD4+ T-Lymphozyten wurden in kongene Empfängertiere injiziert. Die lymphatischen Organe wurden 24h später entnommen. T-Lymphozyten wurden durch den mAb His41 immunhistologisch in braun dargestellt. Zusätzlich sind interdigitierende dendritische Zellen über ihre hohe Expression des interzellulären Adhäsionsmoleküls-1 (ICAM-1) in blau dargestellt und durch ihre charakteristische Morphologie und ihre Lokalisierung im T-Zellareal identifiziert worden. (A) In der Übersichtsvergrößerung der Milz sind die rote (RP) und weiße Pulpa zu erkennen, wobei sich die letztere weiter in die um die Zentralarterie (Za) gelegene periarterioläre lymphatische Begleitscheide (PALS), die Follikel (F) und die Marginalzone (Mz) einteilen läßt. (APAAP-Technik, 250fache Vergrößerung) (B) Deutlich sind zahlreiche Membrankontakte (schwarze Pfeile) zwischen den injizierten T-Lymphozyten und interdigitierenden dendritischen Zellen zu erkennen. (APAAP-Technik, 1000fache Vergrößerung). (C) Im Lymphknoten lassen sich ein Follikel (Fo) im Kortex und der Parakortex (Pk), das T-Zellareal, unterscheiden (400fache Vergrößerung). (D) In den Peyerschen Platten lassen sich das Domepithel (Do), die Krypten (Kr), Follikel (Fo) und Interfollikulärregion (Ifr) abgrenzen (400fache Vergrößerung). 55 2. In den sekundär lymphatischen Organen befinden sich 80% der injizierten T-Lymphozyten in Membrankontakt mit interdigitierenden dendritischen Zellen. In der PALS, deutlicher zu erkennen in der höheren Vergrößerung (Abb.1B), befindet sich ein großer Anteil der injizierten T-Lymphozyten in enger Nachbarschaft zu stark ICAM-1+ interdigitierenden dendritischen Zellen. Durch ihre zahlreichen langen Ausläufer bilden IDC ein Netzwerk, durch das die T-Lymphozyten wandern. Die Pfeile weisen auf Membrankontakte zwischen den einzelnen Zellen hin. Ausgewertet wurde im folgenden der Anteil der T-Lymphozyten, die in Membrankontakt zu IDC liegen, als Prozentsatz an den injizierten kongenen T-Lymphozyten, die im Organ zu identifizieren sind. Es sind keine Zellanhäufungen (Kluster) der injizierten T-Lymphozyten um die IDC zu beobachten, wenn sich auch häufig mehr als ein T-Lymphozyt an einer IDC befindet. Wie in Abb.2 zu erkennen ist, befinden sich in der Milz über 80% His41+ T-Lymphozyten in Membrankontakt mit IDC. Die untersuchten Subpopulationen der T-Lymphozyten, d.h. die naiven, memory und Effektor T-Lymphozyten, unterscheiden sich hinsichtlich des prozentualen Anteils der Kontakte nicht. Für alle Subpopulationen liegt der Mittelwert des Prozentsatzes bei 80%±10%. Betrachtet man daraufhin den mesenterialen Lymphknoten oder die Peyerschen Platten, so findet sich das gleiche Bild auch dort wieder. Die Membrankontakte zwischen T-Lymphozyten mit IDC stellen ein konstantes Phänomen dar, das vermutlich von den Subpopulationen der T-Lymphozyten nicht beeinflusst wird, obwohl BODE (1998) zeigen konnte, dass sich die Expression von z.B. L-Selektin und des IL-2Rezeptors deutlich auf naiven und aktivierten T-Lymphozyten unterscheidet. Auch die unterschiedliche Mikroumgebung in den sekundär lymphatischen Organen scheint keinen Einfluss auf das Ausmaß der Membrankontakte zwischen den T-Lymphozyten mit den IDC zu haben. Eine mögliche Erklärung dieses Phänomens ist das dichte Netzwerk, dass durch die DC mit ihren zahlreichen Ausläufern gebildet wird, wie es sich auch in der Immunhistologie in Abb.1 zu sehen ist. Gelangen T-Lymphozyten in die sekundär lymphatischen Organe, müssen sie auf ihrer Wanderung durch dieses Netzwerk hindurch und bekommen so zahlreichen Kontakt zu den DC. 56 100 Milz 80 Anteil der T-Lymphozyten in Membrankontakt mit IDC an injizierten T-Lymphozyten [%] 60 40 20 100 Lymphknoten 80 60 40 20 100 Peyersche Platten 80 60 40 20 naiv memory E effektor Subpopulationen der T- Lymphozyten Abb. 2 In der Milz, dem mesenterialen Lymphknoten und den Peyerschen Platten befinden sich über 80% der injizierten T-Lymphozyten in Membrankontakt mit interdigitierenden dendritischen Zellen. Zum Zeitpunkt 24h nach Injektion von kongenen naiven, memory und Effektor T-Lymphozyten wurden die Milz, der mesenteriale Lymphknoten und die Peyerschen Platten entnommen und Gewebeschnitte angefertigt (siehe 5.1 und 5.2). Immunhistologisch wurden die injizierten TLymphozyten mit dem mAb His41 und IDC über ICAM-1 dargestellt. Die Membrankontakte der TLymphozyten mit IDC wurden ermittelt und der Anteil der Kontakte als Prozentsatz an den injizierten T-Lymphozyten aufgeführt. Es sind Mittelwert und Standardabweichung von n=5-7 unabhängigen Versuchen aufgeführt. 57 Neben den Kriterien der Lokalisation und ihrer charakteristischen Morphologie wurde die hohe Expression von ICAM-1 zur Identifikation der IDC verwendet. Auf ausgereiften interdigitierenden dendritischen Zellen ist jedoch MHC Klasse II sehr hoch exprimiert, ein Molekül, das bei der Antigenerkennung durch CD4+ T-Lymphozyten eine entscheidende Rolle spielt. Bei der Auswertung der Membrankontakte über einen anti-MHC Klasse IIAntikörper (s.III.3.) befinden sich in allen untersuchten lymphatischen Organen über 80% der injizierten T-Lymphozyten in Membrankontakt zu IDC (s. Tabelle 1). Bei der Verwendung von MHC Klasse II als Nachweis für die IDC findet sich kein signifikanter Unterschied dieser Anteile zwischen naiven, memory und Effektor T-Lymphozyten oder zwischen den verschiedenen sekundär lymphatischen Organen, was die bisherigen Ergebnisse bestätigt. Da beide Nachweise für die DC zu gleich guten Ergebnissen führten, die Abgrenzung der Kompartimente mit der Färbung des ICAM-1 jedoch deutlicher zu sehen war, wurde dieser im folgenden zur Färbung der DC herangezogen. 3. Zu verschiedenen Zeitpunkten nach der Injektion der T-Lymphozyten lassen sich gleiche Anteile von Membrankontakten beobachten. Um die Frage zu beantworten, ob sich zu früheren oder späteren Zeitpunkten der Anteil der Kontakte verändert, wurden zu verschiedenen Zeitpunkten nach Injektion der kongenen T-Lymphozyten die Membrankontakte analysiert. Abb. 3 zeigt verschiedene Zeitpunkte von 0,5h bis 96h nach Injektion der T-Lymphozyten. Obwohl vermutet wird, dass die Wanderung der Subpopulationen der T-Lymphozyten durch die Gewebe verschieden lange dauert und sich das Migrationsverhalten deutlich unterscheidet, befinden sich bereits nach einer halben Stunde naive und memory T-Lymphozyten in Membrankontakten zu IDC. Zu diesem frühen Zeitpunkt finden sich absolut gesehen weniger kongene T-Lymphozyten in den T-Zellarealen der Milz (Daten nicht gezeigt). Festzustellen ist jedoch, dass sich der Anteil der injizierten T-Lymphozyten, die sich in Membrankontakt mit IDC befinden, auf 80±10% beläuft. Auch Effektor T-Lymphozyten, deren Verhalten nach 1h analysiert wurde, weisen ebenfalls in der großen Mehrheit Membrankontakte auf. Zu allen weiteren untersuchten Zeitpunkten (2h, 9h, 58 24h, 48h, 72h und 96h) nach der Injektion lassen sich die gleichen Anteile der Kontakte feststellen. Damit erscheinen die Membrankontakte ein von der Zeit unbeeinflusstes Phänomen darzustellen, die unabhängig von der absoluten Anzahl der im Organ nachzuweisenden T-Lymphozyten in großer Mehrheit nachzuweisen sind. In der Zeitkinetik konnte kein unterschiedliches Verhalten von naiven, memory oder Effektor T-Lymphozyten festgestellt werden. Sie sind aus diesem Grunde in der Graphik gemeinsam dargestellt. Tabelle 1. Membrankontakte zwischen T-Lymphozytena und interdigitierenden dendritischen Zellenb, die über die Oberflächenexpression von MHC Klasse II in den sekundär lymphatischen Organen nachgewiesen worden sind. Subpopulationen injizierter T-Lymphozyten Organec naive memory Effektor Milz 80,6 ± 10,5d 82,7 ± 7,1 71,6 ± 9,5 Lymphknoten 82,7 ± 4,6 80,7 ± 6,9 83,0 ± 5,5 Peyersche Platten 84,5 ± 3,7 84,5 ± 8,8 84,4 ± 6,9 Aus dem Ductus thoracicus wurden naive (CD45RC+) und memory (CD45RC-) T-Lymphozyten separiert. T-Lymphozyten aus Lymphknoten wurden über den T-Zellrezeptor und CD28 in Gegenwart von BrdU für 72h polyklonal aktiviert. LEW.7B(BH) T-Lymphozytensubpopulationen sind LEW (RT7a)-Empfängertieren in die Schwanzvene injiziert worden b Interdigitierende dendritische Zellen wurden über ihre hohe Oberflächenexpression MHC Klasse II, ihre charakteristische Form und ihrer Lokalisation in den T- Zellarealen der peripheren lymphatischen Organe identifiziert. c Die Organe wurden 24 Stunden nach der Injektion der T-Lymphozyten entnommen und durch immunhistochemische Färbungen von Gefrierschnitten ausgewertet. In den T-Zellarealen der Milz, der Lymphknoten und den Peyerschen Platten wurde der Anteil der injizierten T-Lymphozyten mit einem Membrankontakt mit interdigitierenden dendritischen Zellen an den injizierten Zellen ermittelt. d Die Werte sind Mittelwert und Standardabweichung von n=4-7 unabhängigen Experimenten. a Anteil der T-Lymphozyten in Membrankontakt mit interdigitierenden dendritischen Zellen an injizierten T- Lymphozyten [%] 59 100 90 80 70 60 50 40 0.5 1 2 3 4 5 6 7 8 9 24 48 72 96 Zeit nach Injektion [h] Abb. 3 Zu verschiedenen Zeitpunkten nach Injektion der T-Lymphozyten befinden sich gleiche Anteile der Zellen in Membrankontakt zu DC. Nach Injektion von naiven und memory T-Lymphozyten wurden nach 30min, 2h und 48h (•) und nach Injektion von aktivierten T-Lymphozyten nach 1h, 9h, 24h, 72h und 96h (■) die Milz entnommen und Gewebeschnitte hergestellt. Die kongenen T-Lymphozyten wurden über den mAb His41, die DC über ihre Expression des ICAM-1 immunhistologisch identifiziert. Es wurde die Anzahl der injizierten TLymphozyten ermittelt und davon der Anteil bestimmt, der sich in Membrankontakt zu den DC in der PALS befindet. Da sich für die Anteile der Membrankontakte von naiven und memory TLymphozyten keine signifikanten Abweichungen ergeben haben, sind diese in der Zeitkinetik zusammengefasst dargestellt. Angegeben sind Mittelwert und Standardabweichung von n=3-7 unabhängigen Versuchen. 60 4. Endogene T-Lymphozyten zeigen über 60% Membrankontakte zu DC Endogene T-Lymphozyten liegen dicht gedrängt in den T-Zellarealen der lymphatischen Organe, durch die IDC mit ihren zahlreichen Ausläufern ein Netzwerk bilden. Wenn kongene naive, memory und Effektor T-Lymphozyten zu gleichen Anteilen Membrankontakte ausbilden, so müssten auch endogene, empfängereigene T-Lymphozyten einen hohen Anteil an Kontakten aufweisen. In einer Gegenfärbung mit Hämatoxylin und über den Nachweis der IDC konnten auch Membrankontakte zwischen endogenen T-Lymphozyten und IDC ausgewertet werden. Nach der Injektion von naiven, memory und Effektor T-Lymphozyten wurden auch die Anzahl der Membrankontakte der endogenen T-Lymphozyten ausgewertet. In der Milz befand sich der größte Anteil, 65,9±3,8%, der endogenen Zellen in Membrankontakt zu IDC. 5. Membrankontakte zu IgD-positiven B-Lymphozyten befinden sich vorwiegend im äußeren Bereich der periarteriolären lymphatischen Begleitscheide der Milz Neben den IDC gelten auch B-Lymphozyten als Antigen-präsentierende Zellen, die sowohl MHC, als auch ICAM-1 schwach auf ihrer Zelloberfläche exprimieren. Dabei steht jedoch nicht die Auslösung einer T-Zellabhängigen Immunantwort im Mittelpunkt, sondern die B-Lymphozyten benötigen die Interaktion mit Antigen-spezifischen T-Helfer-Zellen zur Enddifferenzierung in Antikörper-sezernierende Plasmazellen. In Abbildung 4A und B sind im inneren Anteil der PALS nur vereinzelt B-Lymphozyten zu erkennen, im äußeren Anteil und zu den Follikeln hingegen sind jedoch zahlreiche, dicht beieinander liegende B-Lymphozyten zu sehen. Der Hauptteil der injizierten T-Lymphozyten befindet sich gleichmäßig verteilt sowohl im inneren, als auch im äußeren Anteil der PALS. Einige T-Lymphozyten sind auch in den Follikeln zu erkennen. Abb.5 zeigt den Anteil der injizierten T-Lymphozyten, die einen Membrankontakt zu den IgD+ B-Lymphozyten im inneren Anteil der PALS aufweisen und 20±5% ausmacht. Im äußeren Teil der PALS 61 hingegen beläuft sich der Kontakt auf über 70%, eine vergleichbare Größenordnung zu den Membrankontakten mit IDC. Lässt sich zwischen den Membrankontakten zwischen den Tund B-Lymphozyten ein deutliches Gefälle zwischen innerem und äußerem Anteil der PALS feststellen, so sind die Kontakte zwischen T-Lymphozyten und IDC gleichmäßig über die gesamte PALS verteilt (hellgraue Balken). Auch in den Anteilen der Membrankontakte zu BLymphozyten lässt sich kein Unterschied zwischen naiven, memory und Effektor TLymphozyten finden (Daten nicht gezeigt). Membrankontakte zwischen T- und BLymphozyten sind vorwiegend im äußeren Bereich der PALS anzutreffen. Abb.4 Membrankontakte zwischen injizierten T-Lymphozyten und IgD+B-Lymphozyten finden vorwiegend im äußeren Anteil der PALS statt. (A) Gezeigt ist ein immunhistologisch gefärbter Gewebeschnitt der Milz 24h nach Injektion von kongenen naiven (CD45RChigh) T-Lymphozyten. Die periarterioläre lymphatische Begleitscheide (PALS), Follikel (F), Marginalzone (MZ) und die rote Pulpa (Rp) lassen sich durch die Darstellung der B-Lymphozyten mit einem anti-IgD-Antikörper in blau deutlich abgrenzen. Die Pfeile weisen auf den äußeren Anteil der PALS, in dem der Hauptteil der T-Lymphozyten Membrankontakt zu B-Lymphozyten zeigt. (B) Injizierte T-Lymphozyten zeigen im vergrößerten Ausschnitt durch die Anfärbung mit dem mAb His41 eine intensive braune Membranfärbung (Pfeilspitzen). Vorwiegend im äußeren Anteil der PALS sind zahlreiche Membrankontakte zu deutlich blau gefärbten B-Lymphozyten zu sehen (schwarze Pfeile). Anteil der T-Lymphozyten in Membrankontakt mit IDC oder B-Lymphozyten an injizierten T-Lymphozyten [%] 62 100 B-Lymphozyten IDC 80 60 40 20 innerer äußerer Anteil der PALS Abb. 5 Die Anteile der Membrankontakte von T-Lymphozyten mit IDC oder mit B-Lymphozyten unterscheiden sich hinsichtlich ihrer Verteilung in der PALS. Bei der Auswertung der in Abb. 4 gezeigten Gewebeschnitte wurde ein innerer (Mitte) und ein äußerer (Peripherie) Anteil der PALS unterschieden. Gezeigt ist die Auswertung der Membrankontakte zwischen den naiven T- und den B-Lymphozyten (schwarze Balken), die sich vorwiegend im äußeren Teil der PALS nachweisen lassen. Die grauen Balken geben zum Vergleich die Membrankontakten zwischen naiven T-Lymphozyten und IDC in einer ICAM-1-Färbung wieder. Im inneren Bereich der PALS befinden sich signifikant mehr T-Lymphozyten in Membrankontakt zu IDC als zu B-Lymphozyten (p<0,05; Wilcoxon-Test). Dargestellt sind Mittelwert und Standardabweichung von n=5 unabhängigen Versuchen. 63 6. Membrankontakte von injizierten T-Lymphozyten mit dendritischen Zellen lassen sich auch mit konfokaler Mikroskopie aufzeigen. In der bei den Immunhistologien verwendeten APAAP-Technik kommt es zur Verwendung von Brückenantikörpern, die optisch einen erhöhten Farbniederschlag vorspiegeln können. Dadurch könnten Überlagerung der Farbniederschläge in der Auswertung zu einem höheren Anteil an Membrankontakten führen. In der konfokalen Mikroskopie werden Fluorochromgekoppelte Antikörper verwendet, die den primären Antikörper erkennen und durch einen Laser zur Emission angeregt werden und somit einen deutlich geringeren Farbniederschlag aufweisen. Ein weiterer Vorteil der konfokalen Mikroskopie liegt darin, dass durch einen immunhistologischen Schnitt mehrere Ebenen gelegt werden können, die bei einer computergestützten Projektion ein dreidimensionales Bild der Kontakte wiedergibt. Es ist also, wie in Abb.6 gezeigt, möglich, den Verlauf und die Lokalisation der Membrankontakte zu verfolgen und des weiteren Überlagerungen ober- oder unterhalb der Schnittebene auszuschließen. Im grünen Kanal lassen sich deutlich die mit His41 angefärbten injizierten TLymphozyten (siehe Abb.6A) erkennen. Im roten Kanal ist der Zellkörper einer IDC mit einer hohen Expression von ICAM-1 und zu mehreren Seiten abgehenden dendritischen Zellausläufern zu sehen (Abb.6B). In der Projektion sind einige der T-Lymphozyten in direkter Nähe zu der IDC zu erkennen, der gelbe Saum entsteht durch eine Überlagerung des roten und grünen Kanals. Auf den folgenden, 0,5µm auseinander liegenden Schnitten lässt sich ein Membrankontakt zwischen der IDC und einem T-Lymphozyten verfolgen (Sternchen). Auch andere T-Lymphozyten weisen einen Membrankontakt auf, sind aber nicht als ganze Zelle im Schnitt enthalten. Mit einem Dreieck gekennzeichnet ist ein T-Lymphozyt, der über die gesamte Schnittebene keinen Kontakt aufweist. In den Immunhistologien, die mittels konfokaler Mikroskopie ausgewertet worden sind, haben sich 60±5% der injizierten T-Lymphozyten in engem Membrankontakt zu den IDC befunden. Die Kontakte, die sich schichtweise pro Zelle verfolgen lassen, sind dabei gleichmäßig verteilt. Durch einen T-Lymphozyt konnten 9,5±1,9 Schichten gelegt werden, was einem berechneten Durchmesser von etwa 5µm entspricht. In einem Hauptteil der verfolgten Kontakte haben die T-Lymphozyten über alle Schichten Kontakt, was in Abb.7 dargestellt ist. 64 Zellen, die sich komplett im Schnitt befunden haben, wurden dabei von oben bis unten durchgemustert. Dabei hatten 33 von 84 ausgewerteten T-Lymphozyten in allen Schichten (100%) Membrankontakt zu einer IDC. In nur weniger als 5% der untersuchten Zellen konnten Überlagerungsartefakte festgestellt werden, d.h. in den Einzelschnitten konnte kein Kontakt festgestellt werden, obwohl in der Projektion die Zelle als positiv (mit Kontakt) gewertet worden war (falsch positiv). Hingegen konnte mit Hilfe der konfokalen Mikroskopie festgestellt werden, dass fast 50% der Zellen ohne Kontakt ober- oder unterhalb der Schnittebene Kontakte aufgewiesen haben (falsch negativ). Abb. 6 In der konfokalen Mikroskopie lassen sich die Membrankontakte über den ganzen Kontakt verfolgen. Gezeigt ist eine Immunhistologie der Milz 24h nach Injektion von CD4+ Gedächtnis T-Lymphozyten im kongenen Modell. Bei den Einzelbildern handelt es sich um Ausschnitte aus der PALS (1000fache Vergrößerung). a) Im grünen Kanal sind T-Lymphozyten (T) über Fluorochromfarbstoff-gekoppelte Antikörper (mAb His41) in grüner Fluoreszenz dargestellt, der gegen den LEWIS RT7b-Phänotyp gerichtet ist. Es sind mehrere T-Lymphozyten zu erkennen. b) Im roten Kanal ist durch eine Markierung mit anti-ICAM-1 (Antikörper 1A29) eine interdigitierende dendritische Zelle dargestellt, deren Zellkörper und einige dendritische Ausläufer zu sehen sind. c) Die Abbildung zeigt eine konfokale Gesamtprojektion des grünen und roten Kanals durch computergestützte Übereinanderlagerung der optischen Einzelschnitte. Durch die Übereinanderlagerung der Kanäle erscheinen die Membrankontakte zwischen T-Lymphozyten und IDC in gelb. d-l) Optische konfokale Folgeschnitte im Abstand von 0,5µm durch den Ausschnitt der PALS der Milz. Mit einem Stern (*) gekennzeichnet ist ein T-Lymphozyt, der durch alle optische Einzelschnitte hindurch verfolgt werden kann und einen deutlichen Membrankontakt zur dendritischen Zelle aufweist. Mit einem Dreieck (∆) gekennzeichnet ist hingegen ein T-Lymphozyt, bei dem über alle Einzelschnitte kein Kontakt zu beobachten ist. Die Pfeile (→) weisen exemplarisch auf Membrankontakte zwischen den injizierten T-Lymphozyten und den dendritischen Zellen (mit einer gelb erscheinenden Überlappungszone) hin. 65 Anzahl der injizierten T-Lymphozyten 66 35 30 25 20 15 10 5 0 10 20 30 40 50 60 70 80 % 100 Ausmaß der Membrankontakte in Prozent Abb. 7 Membrankontakte zwischen T-Lymphozyten und IDC lassen sich in der Mehrzahl über mehrere Schichten verfolgen. Auf Gewebeschnitten wurden die injizierten naiven (CD45RChigh) und memory (CD45RClow) TLymphozyten mit dem fluorochrom-markierten Antikörper His41 in grün dargestellt. Über die Expression von ICAM-1 wurden IDC in der PALS in roter Fluoreszenz nachgewiesen. Mit Unterstützung eines bildgebenden Verfahrens am Computer wurden insgesamt 9 (Z-Dicke = 0,5µm) durch einen Ausschnitt der PALS gelegte Einzelschnitte übereinander gelagert und als Teilprojektion definiert. In dieser Darstellung wurden in der PALS injizierte T-Lymphozyten ausgewählt, die einen Membrankontakt zu einer IDC aufgewiesen haben und über die Einzelprojektionen der Kontakt verfolgt. Es wurden bei der Auswertung nur Zellen genommen, die sich mit ihrer gesamten Zelloberfläche innerhalb des Gewebeschnittes befunden haben. Die y-Achse zeigt dabei die Anzahl der T-Lymphozyten an, die x-Achse den prozentualen Anteil der Schichten, in denen die TLymphozyten einen Membrankontakt aufweisen, an allen Schichten der Zelle. Dabei sind TLymphozyten, die in allen Schichten Membrankontakt aufweisen, unter 100% aufgeführt. Zellen, die nur in der Hälfte ihrer Schichten Kontakte hatten, sind in der Kategorie 50% aufgeführt. Angegeben sind nur die T-Lymphozyten (n=84), die in der Teilprojektion wie auch den Einzelschnitten Membrankontakte gezeigt haben. 67 7. In der Maus werden interdigitierende dendritische Zellen über den spezifischen Marker DEC-205 nachgewiesen. Um herauszufinden, ob es sich bei der beobachteten Größenordnung von Membrankontakten um speziesspezifische Effekte handelt, die sich nur in der Ratte darstellen lassen, wurden im weiteren auch Mäuse untersucht. In der Maus sind spezifische Marker für IDC bekannt. Ein Beispiel ist der Nachweis des Multilektinrezeptors DEC-205, der sich in den T-Zellarealen der lymphatischen Organe identifizieren lässt. Auch weitere spezifische Marker, Mac-1 und CD11c, für IDC wurden auf den Immunhistologien getestet, erbrachten jedoch keine zufrieden stellenden Ergebnisse. So war Mac-1auf Gewebeschnitten nur auf Makrophagen in der roten Pulpa exprimiert und konnte zum Nachweis der IDC nicht weiter eingesetzt werden. CD11c konnte nicht in gleicher Intensität wie NLDC-145 in der Maus oder ICAM-1 in der Ratte nachgewiesen werden (Daten nicht gezeigt). In Abb.8 ist im inneren Bereich der PALS eine deutliche Markierung von Zellen mit IDCCharakter zu beobachten, die sich zum äußeren Bereich der PALS hin verliert. Die Abgrenzung zu den Follikeln im äußeren Anteil der PALS ist nicht so deutlich ausgeprägt, wie es bei der Verwendung von ICAM-1 (s.Abb.1) oder MHC Klasse II (nicht gezeigt) in der Ratte der Fall ist. Endogene T-Lymphozyten liegen zu 55,7 ± 2,7% in Membrankontakt mit IDC. Die Membrankontakte von endogenen T-Lymphozyten mit IDC in der Ratte und in der Maus liegen in einer vergleichbaren Größenordnung. Das Mausmodell eröffnet hingegen eine Reihe weiterer Untersuchungsmöglichkeiten. 7.1. LFA-1-defiziente Zellen weisen eine unverändert hohe Anzahl von Membrankontakten zu DC auf. Durch die Verwendung von genetisch veränderten Mäusen ist es möglich, die Beteiligung von Oberflächenmolekülen bei der Ausbildung der Membrankontakte zu untersuchen. LFA-1 ist als ein wichtiges Molekül bei der Migration der Lymphozyten aus den Blutgefäßen bekannt, spielt aber auch eine entscheidende Rolle in der Vermittlung von transienten Zell-Zell- 68 Interaktionen. Um herauszufinden, welche Rolle LFA-1 in der Ausbildung von Membrankontakte zwischen T-Lymphozyten und IDC hat, wurden Wildtypmäusen gleichzeitig markierte Wildtypzellen und LFA-1-defiziente (αL-/-/ β2, CD11a-/-/ CD18) Lymphozyten injiziert. Immunhistologisch konnten Membrankontakte zu IDC, die über den spezifischen Antikörper NLDC-145 nachgewiesen wurden, in der Milz ausgewertet werden. Dabei befanden sich Zellen aus Wildtyptieren zu gleichen Anteilen (59,9±5,2%) in Membrankontakt zu IDC wie die Zellen aus LFA-1-defizienten Tieren (59,0±5,3%). Eine mögliche Erklärung dieses Ergebnis ist die Expression von LFA-1 auf den Dendritischen Zellen und des ICAM-1 auf den T-Lymphozyten, die den Kontakt gewährleisten könnten. Auch andere Ligand-Rezeptorbindungen wie CD2/ LFA-3 oder CD28/ CD80 können Antigen-unabhängige Membrankontakte vermitteln. Durch eine zusätzliche Blockierung mit einem Antikörper, der gegen ICAM-1 gerichtet ist, könnte in einer weiteren Untersuchung der Einfluss des LFA-1 auf die Membrankontakte deutlicher gezeigt werden. Ob das fehlende LFA-1-Molekül Auswirkungen auf die Signaltransduktion für die T-Lymphozyten mit sich bringt, bleibt in weiteren Studien mit diesen genetisch veränderten Mäusen zu zeigen. 69 Abb. 8 In der Maus lassen sich IDC über den spezifischen Marker DEC-205 nachweisen. Gewebeschnitt der Milz einer Wildtypmaus. IDC lassen sich über die Expression des Multilektinrezeptors DEC-205 (Antikörper NLDC-145) in blau darstellen. (A) Im inneren Anteil der PALS heben sich die DC durch die Färbung besonders hervor, zum äußeren Bereich der PALS hin ist die Färbung schwächer ausgeprägt. Endogene T-Lymphozyten zeigen durch eine Gegenfärbung mit Hämalaun eine schwach blaue Färbung. Es ist zu erkennen, dass sie dicht gedrängt in der PALS liegen. Angrenzend an die PALS sind Follikel (F) schwach zu erkennen. (250 x Vergrößerung, APAAP-Technik) (B) In der Ausschnittsvergrößerung sind einzelne T-Lymphozyten aus einer Wildtypmaus zu erkennen, die vor der Injektion in Wildtypmäuse mit Digoxigenin markiert worden ist. Die schwarzen Pfeile weisen auf T-Lymphozyten hin, die einen Membrankontakt zu einer DC aufweisen. (1000 x) 70 B. Effektor T-Lymphozyten in Zellzyklus und Proliferation Eine wesentliche, in der Literatur beschriebene Funktion der DC liegt in der Auslösung von primären oder sekundären T-Zellabhängigen Immunantworten. Dabei wird einem T-Lymphozyt sein spezifisches Antigen in einem MHC-Peptid-Komplex verbunden mit kostimulatorischen Molekülen präsentiert, d.h. es erfolgt eine vollständige Aktivierung der Zelle. Diese führt zur Proliferation und zur klonalen Expansion des spezifischen T-Lymphozyten. Als ein Nachweis für Proliferation gilt der Einbau von BrdU, eines Thymidinanalogons, in die DNS. Als eine weitere wichtige Funktion der DC wird das Überleben von aktivierten, aber auch von naiven und memory T-Lymphozyten beschrieben. In verschiedenen Modellen konnte gezeigt werden, dass T-Lymphozyten ohne den regelmäßigen Kontakt zu DC nicht lange überleben können, sondern vermutlich durch eine Grundaktivierung im Zellzyklus gehalten werden müssen. Aus diesem Grunde ist im zweiten Teil der Arbeit der Fokus auf den Zellzyklus und die Proliferation in Abhängigkeit von Membrankontakten gerichtet worden. 1. Ki-67+ T-Lymphozyten im Blut Um Hinweise auf die Funktion der morphologisch beobachteten Membrankontakte zu erhalten, wurde die Expression des nukleären Zellantigens Ki-67 von aktivierten TLymphozyten ausgewertet. Ki-67, das durch den spezifischen Marker Mib5 nachzuweisen ist, wird in der Ratte in der G1-Phase, der M1-Phase, der S-Phase und der M2-Phase exprimiert. Diese Phasen werde im weiteren als „Zellzyklus“ referiert. Nach Aktivierung der TLymphozyten wie unter 5.2 beschrieben, sind etwa die Hälfte der T-Lymphozyten im Inokulum Ki-67+, d.h. sie befinden sich im Zellzyklus. Wie in Abb.9 zu erkennen ist, befinden sich nach intravenöser Injektion in die Schwanzvene von Empfängertieren bereits nach einer Stunde davon nur noch ein Fünftel, d.h. 10% der im Blut identifizierten Zellen, im Zellzyklus. Dieser Wert bleibt über 9h, 24h und 96h konstant. Es ist nicht geklärt, ob sich nach einer Stunde oder zu späteren Zeitpunkten vermehrt T-Lymphozyten in den Organen im Zellzyklus 71 befinden und ob die Membrankontakte zwischen T-Lymphozyten und dendritischen Zellen Anteil der Zellen im Zellzyklus von den injiziertenT-Lymphozyten im Blut einen Einfluss darauf haben. 60 Blut 50 % 40 30 20 10 0 Inokulum 1h 9h 24h 96h Zeit nach Injektion Abb. 9 Zeitkinetik von injizierten T-Lymphozyten im Zellzyklus im Blut Kongene T-Lymphozyten aus den Lymphknoten wurden über den TCR und CD28 polyklonal aktiviert und Empfängertieren i.v. in die Schwanzvene injiziert (siehe 5.2). Nach 1h, 9h, 24h und 96h wurden jeweils Tiere durch Entbluten getötet. Auf Blutzytospots (siehe 6.3 und 6.4) wurden durch den monoklonalen Antikörper His41 die injizierten T-Lymphozyten identifiziert. Unter diesen wurde der Anteil der Zellen ermittelt, die Mib+ waren. Dieser Antikörper erkennt das nukleäre Zellantigen Ki67, das während des Zellzyklus (G1-M2) exprimiert wird. Es sind Mittelwert und Standardabweichung aus n= 3-7 unabhängigen Versuchen gezeigt. 72 2. BrdU+ T-Lymphozyten in der Milz Während das nukleäre Zellantigen Ki-67 während des gesamten Zellzyklus über alle Phasen außer G0 exprimiert wird, wird das Thymidinanalogon BrdU nur während der S-Phase des Zellzyklus in die DNS eingebaut. Befindet sich eine Zelle in der S-Phase, so durchläuft sie in den meisten Fällen eine aktive Zellteilung, wohingegen der Zellzyklus vorher an bestimmten Checkpunkten gestoppt werden kann, um unkontrollierte Proliferation verhindern zu können. Um festzustellen, inwiefern sich die eingewanderten, aktivierten Lymphozyten in der Milz teilen, wurde den Ratten eine Stunde vor dem Entbluten BrdU appliziert (siehe 6.5). Dadurch haben nur solche Zellen BrdU in ihre DNS einbauen können, die sich in den Organen in der S-Phase befunden haben. Bereits 24h nach i.v. Injektion der aktivierten T-Lymphozyten waren 2,2% BrdU+ T-Lymphozyten zu finden, 72h nach der Injektion war der Anteil auf 3,3% angestiegen. Aufgrund sehr niedriger Zellzahlen wurden die Rohdaten für 24h (n=2), für 72h (n=10 unabhängige Versuche) zu einer Summe zusammengezogen und daran der Anteil der BrdU+ Zellen ermittelt. Wie zu erwarten gewesen war, lag der Anteil der BrdU+ Zellen deutlich unter den Anteilen der Ki-67+ T-Lymphozyten. Von Interesse ist für diese Arbeit gewesen, ob die Membrankontakte zwischen den injizierten T-Lymphozyten und den IDC in der PALS den Anteil der Zellen im Zellzyklus (Expression von Ki-67) und den Anteil der proliferierenden Zellen (Einbau von BrdU) beeinflussen können. 3. Die Anteile der Ki-67+ und BrdU+ T-Lymphozyten sind erhöht zu finden, wenn Membrankontakte mit IDC in der Milz vorliegen Wie im ersten Teil beschrieben, befinden sich 80±10% der injizierten T-Lymphozyten, aber auch 60±5% der endogenen T-Lymphozyten in Membrankontakt mit den IDC. Abb.10 zeigt eine 3fach Färbung der Milz, in der deutlich die T-Lymphozyten in blau und die IDC mit ihrer charakteristischen Morphologie in braun zu erkennen sind. Die schwarzen Pfeilköpfe weisen 73 auf injizierte His41+ T-Lymphozyten hin, die in Membrankontakt zu einer IDC liegen. Deutlich zu erkennen ist ein T-Lymphozyt mit Membrankontakt zu einer IDC, der sich durch einen roten (BrdU+) Zellkern hervorhebt (schwarzer Pfeil). Auch endogene Zellen sind zu beobachten, die eine rote Zellkernfärbung aufweisen (weiße Pfeilköpfe). Sie sind ein Indiz dafür, dass sich sowohl injizierte, als auch empfängereigene Zellen zum Zeitpunkt der Organentnahme in der S-Phase des Zellzyklus befunden haben. Im folgenden wurde ausgewertet, ob sich vermehrt T-Lymphozyten in der S-Phase des Zellzyklus oder in allen Phasen des Zellzyklus außer G0 nachweisen lassen, wenn sie einen Membrankontakt zu IDC aufweisen. Dabei wurden die Zeitpunkte 24h und 72h nach der Injektion der T-Lymphozyten ausgewählt, da sich frühestens nach 24h die DNS-Replikation und nach 48h die Zellteilung nachweisen lassen. 3.1. T-Lymphozyten, die in der Milz einen Membrankontakt zu IDC aufweisen, befinden sich signifikant erhöht im Zellzyklus und in der S-Phase Vergleicht man in der Milz die injizierten T-Lymphozyten, die einen Membrankontakt mit IDC haben, mit solchen, die keinen haben, so lässt sich sowohl bei Ki-67+ Zellen, wie auch bei den BrdU+ Zellen ein signifikanter Unterschied feststellen. Wie es in Abb.11 zu erkennen ist, sind bereits 24h nach der Injektion 28,9±7,3% der T-Lymphozyten mit einem Kontakt Ki67+ gegenüber 20,2±8,9% T-Lymphozyten ohne Kontakt zu einer IDC. In der Darstellung der Einzeltiere wird deutlich, dass zwar die Anteile der Zellen im Zellzyklus zwischen 20 bis 50% schwanken können, aber doch deutlich mehr Zellen mit Kontakt das Ki-67-Antigen exprimieren. 72h nach der Injektion sinkt der Anteil der Zellen im Zellzyklus auf 13±5,1% ab, aber auch hier befinden sich signifikant mehr Zellen im Zellzyklus, wenn sie gleichzeitig einen Membrankontakt zu einer IDC aufweisen. Der Anteil der T-Lymphozyten, die während der S-Phase BrdU eingebaut haben, liegt deutlich niedriger: nach 24h bei etwa 8%, nach 72h bei noch etwa 4%. Doch auch hier lässt sich ein signifikanter Unterschied feststellen, wenn man Zellen mit und ohne Kontakt vergleicht. Diese Ergebnisse scheinen darauf hinzuweisen, 74 dass T-Lymphozyten auf Kontakte zu IDC angewiesen sind, um im Zellzyklus zu verbleiben und in geringerem Maße zu proliferieren. Abb. 10 Injizierte, proliferierende T-Lymphozyten befinden sich in Membrankontakten zu IDC. Auf einem Gewebeschnitt der Rattenmilz ist ein Ausschnitt der PALS gezeigt. Die Milz wurde 72 Stunden nach Injektion von polyklonal über den TCR und CD28 aktivierten T-Lymphozyten entnommen (s.5.2. und 5.3.). Eine Stunde zuvor wurde den Tieren BrdU i.v. in die Schwanzvene injiziert, um die Proliferation von Zellen nachweisen zu können. Die injizierten T-Lymphozyten zeigen durch die Anfärbung mit dem mAb His41 eine intensive blaue Membranfärbung. IDC sind über ihre hohe Expression des ICAM-1 in braun dargestellt. Proliferierende Zellen zeigen durch den Nachweis des während der S-Phase in die DNS eingebauten BrdU eine intensive rote Kernfärbung. Deutlich zu erkennen ist ein injizierter T-Lymphozyt in Membrankontakt zu einer IDC, der einen intensiv roten, BrdU+ Zellkern aufweist (schwarzer Pfeil). Die schwarzen Pfeilköpfe verweisen auf Membrankontakte zwischen den injizierten T-Lymphozyten und den IDC. Auch endogene Zellen haben BrdU eingebaut und weisen eine rote Kernfärbung auf (weiße Pfeilköpfe). (APAAP-Technik, 1000fache Vergrößerung) 75 * 50 |__________| 40 28.9 + 7.3 30 20 20.2 + 8.9 10 1.2 0.8 ohne m it 72h nach Injektion * 20 |___________| 15 13.0 + 5.1 10 + K i-67 T-Lym phozyten an den injizierten T-Lym phozyten [%] 24h nach Injektion 8.6 + 4.4 5 ohne m it M em brankontakt zu dendritischen Zellen Abb. 11 T-Lymphozyten mit einem Membrankontakt mit IDC weisen einen erhöhten Anteil von Ki-67+Zellen auf. Jeweils 24h und 72h nach Injektion von aktivierten T-Lymphozyten wurde die Milz entnommen, tiefgefroren und T-Lymphozyten und IDC immunhistochemisch anfärbt. Zusätzlich wurden Zellen, die sich im Zellzyklus befinden, über das nukleäre Zellkernantigen Ki-67 (mAb Mib5) nachgewiesen. Der Prozentsatz (y-Achse) gibt an, welcher Anteil der His41+ Lymphozyten sich im Zellzyklus befindet. Die x-Achse gibt Auskunft, ob die T-Lymphozyten Membrankontakt gezeigt haben. Signifikant mehr T-Lymphozyten befinden sich im Zellzyklus, wenn sie einen Kontakt zu einer IDC aufweisen. Zusätzlich sind Daten nach Injektion von naiven und memory T-Lymphozyten erhoben worden, die allerdings aufgrund von sehr geringen Zellzahlen aus n=5 Versuchen zu einer Summe zusammengefasst worden sind (schwarze Raute). Gezeigt sind Einzeltiere aus n=5-6 unabhängigen Versuchen. Das Sternchen (*) verweist auf eine Signfikanz von p<0,05, die mit dem Wilcoxon-Test berechnet wurde. 24h nach Injektion 10 8 7.8 + 1.1 6 4.9 + 1.1 4 2 0.8 0.5 ohne 10 mit 72h nach Injektion * 8 |__________| BrdU+ T-Lymphozyten unter den injizierten T-Lymphozyten [%] 76 6 3.9 + 1.0 4 2 2.0 + 0.5 ohne mit Membrankontakt zu dendritischen Zellen Abb. 12 T-Lymphozyten mit einem Membrankontakt mit IDC sind zu einem erhöhten Anteil BrdU+. Wie für Abb. 11 beschrieben wurden T-Lymphozyten polyklonal aktiviert, injiziert und nach 24h und 72h die Milz entnommen und tiefgefroren. Injizierte T-Lymphozyten wurden über den mAb His41 und die IDC über ICAM-1 identifiziert. Zusätzlich wurden Zellen, die sich in der S-Phase befanden, über das Thymidinanalogon BrdU nachgewiesen. Der Prozentsatz gibt an, welcher Anteil der His41+ Lymphozyten, die einen Membrankontakt zu IDC haben, sich in der S-Phase befindet. Signifikant mehr T-Lymphozyten proliferieren, wenn sie einen Kontakte zu einer IDC aufweisen. Zusätzlich sind Daten nach Injektion von naiven und memory T-Lymphozyten erhoben worden, die allerdings aufgrund von sehr geringen Zellzahlen aus n=5 Versuchen zu einer Summe zusammengefasst worden sind (schwarze Raute). Gezeigt sind Einzeltiere aus n=2-10 unabhängigen Versuchen. (*, p<0,05; Wilcoxon-Test) 77 3.2. Ki-67+ T-Lymphozyten sind gleichmäßig über die PALS verteilt, T-Lymphozyten mit BrdU-Einbau befinden sich hingegen vorwiegend im äußeren Anteil der PALS. Wie in Abb.5 gezeigt wurde, finden Membrankontakte von T-Lymphozyten zu BLymphozyten vorwiegend im äußeren Anteil der PALS statt. Auf ihrer Wanderung gelangen sowohl T-, als auch B-Lymphozyten in diesen Randbereich zwischen Follikeln und PALS. Die Kontakte zwischen CD4+ T-Lymphozyten und B-Lymphozyten sind entscheidend für die Einleitung einer humoralen Immunantwort, also der Enddifferenzierung der B-Lymphozyten in Plasmazellen und der Produktion von spezifischen Antikörpern. Nach ihrer Aktivierung im inneren Anteil der PALS wandern T-Helferzellen in den äußeren Anteil der PALS und in die Follikel, wo sich Antigen-spezifische B-Lymphozyten befinden. Betrachtet man nun in Abb.13 den Anteil der injizierten Lymphozyten, die einen Membrankontakt zu IDC aufweisen, in Abhängigkeit von der Lokalisation, also dem inneren oder äußeren Anteil der PALS, so lässt sich feststellen, dass sich im äußeren Anteil mehr Lymphozyten in der S-Phase (BrdU+) befinden als im inneren Anteil. Im Gegensatz dazu lässt sich bei Lymphozyten im Zellzyklus (Mib5+) kein signifikanter Unterschied feststellen. Etwa 30% der T-Lymphozyten befinden sich in der gesamten PALS gleichmäßig verteilt im Zellzyklus. Eine mögliche Erklärung für dieses Ergebnis könnte die gegenseitige Aktivierung der CD4+ T-, wie auch der B-Lymphozyten in diesem Randbereich der PALS sein, der zu einem erhöhten Anteil an BrdU+ Zellen unter den injizierten T-Lymphozyten führen könnte. 78 + BrdU T-Lymphozyten 72h nach Injektion 12 12 10 10 8 8 6 6 4 4 2 2 ** |____________| Anteil der BrdU + T-Lymphozyten an injizierten T-Lymphozyten 24h nach Injektion + Anteil der Mib + T-Lymphozyten an injizierten T-Lymphozyten Ki-67 T-Lymphozyten 50 50 40 40 30 30 20 20 10 10 innere äußere innere äußere Lokalisation der injizierten T-Lymphozyten in der PALS der Milz 79 Abb. 13 In der äußeren PALS befinden sich signifikant mehr BrdU+ T-Lymphozyten als in der inneren PALS, wohingegen sich kein Unterschied der Verteilung der Ki-67+ T-Lymphozyten feststellen lässt. Jeweils 24h und 72h nach Injektion von kongenen, polyklonal aktivierten T-Lymphozyten wurde die Milz entnommen und Immunhistologien angefertigt. Der Nachweis der T-Lymphozyten wurde über den mAb His41, der DC über die Expression von ICAM-1 geführt. Zellen in der S-Phase wurden durch den Einbau von BrdU, das eine Stunde vor der Organentnahme i.v. injiziert wurde, nachgewiesen. Zellen im Zellzyklus wurden hingegen durch das Zellzyklus-assoziierte Zellkernantigen Ki-67 (Antikörper Mib5) identifiziert. Es wurde ausgewertet, welcher prozentuale Anteil der injizierten T-Lymphozyten, die einen Kontakt zu DC aufweisen, sich in der S-Phase oder im Zellzyklus befindet. Bei der Auswertung wurde zusätzlich unterschieden, ob sich die injizierten Zellen im inneren (Mitte) oder äußeren Bereich (Peripherie) der PALS befanden. Angegeben sind die Werte von Einzeltieren aus jeweils n=2-10 unabhängigen Versuchen. Die Signifikanz (**, p<0,02) wurde mit dem Wilcoxon-Test für nicht parametrische Tests ermittelt. Für 24h (BrdU) ließ sich aufgrund der geringen Anzahl der Versuche keine Signifikanz ermitteln. 80 V. Diskussion Ziel der vorliegenden Arbeit war es, die Anzahl der Membrankontakte zwischen TLymphozyten und dendritischen Zellen (DC) in vivo in den T-Zellarealen der sekundär lymphatischen Organen zu untersuchen. DC werden eine essentielle Rolle in der TZellaktivierung (BANCHEREAU u. STEINMAN, 1998)), dem Überleben der TLymphozyten in Abhängigkeit der peripheren MHC-Präsentation (BEUTNER u. MACDONALD, 1998; BROCKER, 1997; DANIEL et al., 1998), der peripheren Toleranz (STEINMAN et al., 2000a), der Tumorimmunität (SCHULER u. STEINMAN, 1997) und der Entwicklung von Autoimmunität (DELEMARRE et al., 1999; LUDEWIG et al., 1999b) zugeschrieben. Um diese vielfältigen Aufgaben wahrnehmen zu können, benötigen die Zellen jedoch den Kontakt zueinander. Bisherige Daten zur physikalischen Interaktion sind vorwiegend aus Kultursystemen in vitro (GEIJTENBEEK et al., 2000; POPE et al., 1995) oder aus adoptiven Transfermodellen (TANCHOT u. ROCHA, 1998) bekannt geworden. In diesen, wie auch in anderen Untersuchungen zur Interaktion von T-Lymphozyten mit dendritischen Zellen (BOTTOMLY, 1999; RISSOAN et al., 1999; SCHUHBAUER et al., 2000), aber auch zur Interaktion mit B-Lymphozyten (DEFRANCO, 1988; GARSIDE et al., 1998; KUSHNIR et al., 1998), mit Makrophagen (UNDERHILL et al., 1999), mit Mastzellen (MEKORI u. METCALFE, 1999) oder mit Endothelzellen (JANCIC et al., 1998) bleibt unbekannt, welche Anzahl von Membrankontakten stattfindet. Diese Größenordnung der Membrankontakte kann zu einem grundlegenden Verständnis über die Kommunikation der TLymphozyten mit ihrer Umgebung führen. 1. Membrankontakte zwischen T-Lymphozyten und IDC stellen ein konstantes Phänomen dar. Identifizierung der T-Lymphozyten und der interdigitierenden dendritischen Zellen Bei den Untersuchungen für diese Arbeit wurde auf Gewebeschnitten der Rattenmilz die Membrankontakte von T-Lymphozyten mit DC in vivo analysiert. Als Grundlage dieser Arbeit wurde das etablierte, kongene Modell (WONIGEIT, 1979) eingesetzt, da es eine 81 Identifizierung injizierter T-Lymphozyten erlaubte, ohne eine vorherige Markierung der Zellen vornehmen zu müssen. So blieben die Oberflächenmoleküle auf den Zellen unbeeinträchtigt und ermöglichten immunhistochemische Mehrfachfärbungen. Durch die Verwendung von immunhistologischen Färbungen konnten T-Lymphozyten, sowie DC in den Kompartimenten und die Anzahl der Membrankontakte zwischen den beiden Zelltypen in vivo nachgewiesen werden. DC in den T-Zellarealen der lymphatischen Organe, auf die in dieser Arbeit Bezug genommen wurde, werden aufgrund ihrer charakteristischen Morphologie mit zahlreichen Zellausläufern auch als interdigitierende dendritische Zellen (IDC) bezeichnet (STEINMAN et al., 1997). Neben der Morphologie und der Lokalisation exprimieren IDC, die durch ihre Kapazität zur Auslösung einer T-Zellabhängigen Immunantwort einen reifen Phänotyp der DC darstellen, MHC Klasse II und Adhäsionsmoleküle wie das interzelluläre Adhäsionsmolekül-1 (ICAM-1) auf ihrer Zelloberfläche. Mit Antikörpern gegen ICAM-1 oder gegen den MHC Klasse II konnten so die IDC gut identifiziert werden, obwohl bisher kein spezifischer Antikörper in der Ratte bekannt ist. Es konnten mit beiden Antikörpern gleiche Anteile an Membrankontakten festgestellt werden (etwa 80%), wobei im weiteren der Antikörper gegen ICAM-1 verwendet worden ist. Bei der Auswertung von Immunhistologien bleibt die Morphologie der Organe erhalten und ermöglicht so eine Zuordnung der Zellen in bestimmte Kompartimente. Im Gegensatz hierzu werden beim Einsatz von durchflußzytometrischen (FACS) Messungen die Zellen aus ihren Gewebeverbänden herausgelöst betrachtet (WESTERMANN u. PABST, 1992). Membrankontakte, wie sie im Falle dieser Arbeit beschrieben werden, können so nicht ausgewertet werden. Probleme beim Nachweis der Membrankontakte Wenn man 24h nach der Injektion die periarterioläre lymphatische Begleitscheide (PALS) der Milz immunhistologisch betrachtet, befinden sich 80% der T-Lymphozyten in Membrankontakt zu IDC. Die bei der Darstellung der Zellen verwendete APAAP-Technik kann durch die Signalverstärkung über Brückenantikörper zu einem Farbniederschlag führen. Es ist nicht auszuschließen, dass sich dadurch ein Farbring um die Zellen bildet, der in die Wertung der Zellkontakte eingeht und zu falsch-positiven Ergebnissen führt. Der Einsatz der 82 konfokalen Mikroskopie ermöglicht die Darstellung ganzer T-Lymphozyten und eine Minimierung der Farbniederschläge. In der konfokalen Mikroskopie konnten über 60% Membrankontakte zwischen den T-Lymphozyten und IDC beobachtet werden. Um eine bessere Vergleichbarkeit der Ergebnisse der Immunhistologie mit der konfokalen Mikroskopie zu erreichen, wurden computergestützt durchschnittlich 15 Schichten von 0,5µm Dicke durch eine Histologie gelegt (gescannt). Davon wurden die 9 mittleren Schichten ausgewählt und übereinander projiziert, so dass diese „Teilprojektion“ einem Gewebeschnitt im Durchlichtmikroskop entsprach. Dieses Vorgehen ermöglichte es, einzelne Zellen auszuwählen, erst in der Teilprojektion Membrankontakte festzustellen und diese nachfolgend in den unter- und oberhalb liegenden Schichten zu verfolgen. Interessanterweise ließ sich bei diesem Vorgehen feststellen, dass von den 40% der T-Lymphozyten, die in der Teilprojektion keinen Membrankontakt hatten, noch etwa die Hälfte unter- und oberhalb der Teilprojektion Membrankontakt zu einer IDC hatte. Finden wir also in der Immunhistologie 80% Membrankontakte, die zum Teil durch Farbniederschläge um die Zellen zustande kommen können, so können wir doch aus den Ergebnissen der konfokalen Mikroskopie schließen, dass weit über 60% der T-Lymphozyten Membrankontakte aufweisen müssen. Überlappungen (falsch-positive Ergebnisse), d.h. dass durch die Lichtführung im Mikroskop Zellen einen Kontakt aufweisen, die sich auf unterschiedlichen Ebenen befinden, ließen sich in nur weniger als 5% der Fälle nachweisen. Die Vorhersage, dass sich eine T-Zelle in der Teilprojektion in Kontakt zu einer DC befindet, trifft mit sehr hoher Wahrscheinlichkeit zu. Durch diese Untersuchungen konnte bestätigt werden, dass sich der Hauptteil der in der Milz einwandernden naiven T-Lymphozyten in Membrankontakt zu IDC befindet. Naive, Effektor und CD4+ Gedächtnis T-Lymphozyten weisen in allen lymphatischen Organen zu 80% Membrankontakte mit IDC auf. Übereinstimmend mit der Beobachtung, dass in allen sekundär lymphatischen Organen ein dichtes Netzwerk von IDC durch die T-Zellareale ausgebildet wird, durch das die TLymphozyten kontinuierlich rezirkulieren (STEINMAN et al., 1997), befinden sich jeweils etwa 80% Membrankontakte zwischen injizierten T-Lymphozyten und den IDC. Keinen Einfluss scheint auch die Herkunft der Antigene zu haben, da die Milz Antigene aus dem Blut, 83 die Lymphknoten aus den von ihnen drainierten Geweben und die Peyerschen Platten über MZellen aus dem Darm erhalten (JANEWAY et al., 1999). Den sekundär lymphatischen Organe ist die Aufgabe gemein, durch ihre spezialisierte Aufteilung in T- und B-Zellkompartimente die Auslösung und Regulation von Immunantworten zu unterstützen und zu erleichtern. In den lymphatischen Organen wird ein konzentriertes Zusammentreffen von T-Lymphozyten auf der Suche nach ihrem spezifischen Antigen und Antigen-spezifischen IDC ermöglicht. Mit der Aktivierung der T-Lymphozyten gehen phänotypische Veränderungen einher, die mit einer Veränderung der Expression von Adhäsionsmolekülen und Aktivierungsmarkern verbunden ist (BODE, 1998). Damit unterscheiden sich Effektor T-Lymphozyten deutlich von naiven T-Lymphozyten. Memory T-Lymphozyten in der Ratte werden durch die niedrige Expression des CD45RC von naiven T-Lymphozyten unterschieden, wobei nach neueren Erkenntnissen ein Teil der memory T-Lymphozyten wieder die hohe Isoform des CD45RC exprimieren kann (BELL u. SPARSHOTT, 1990). Da Adhäsionsmoleküle für die spezifische Einwanderung in lymphatische oder nicht-lymphatische Organe und für die Interaktion mit anderen Zellen wie auch den DC verantwortlich gemacht werden, wurden naive, Effektor und memory T-Lymphozyten auf die Anzahl ihrer Membrankontakte zu IDC untersucht. Bislang gibt es in der Literatur keine Daten zu der Anzahl der Membrankontakte zwischen TLymphozyten und DC. Aufgrund der Reexpression der hohen Isoform des CD45RC kann eine „Verunreinigung“ der hier betrachteten naiven Zellpopulation nicht vollständig ausgeschlossen werden. Da sich aber die Membrankontakte zwischen naiven und memory TLymphozyten mit den IDC nicht signifikant unterscheiden, ist diese Verunreinigung höchstwahrscheinlich nicht relevant. Membrankontakte endogener T-Lymphozyten Da sich kongene, injizierte T-Lymphozyten wie empfängereigene T-Lymphozyten verhalten, müssten auch endogene T-Lymphozyten in hohem Maße Membrankontakte zu DC aufweisen. In den T-Zellarealen liegen endogene T-Lymphozyten dicht gedrängt beieinander, was sich durch eine Gegenfärbung mit Hämatoxylin darstellen lässt. Ein Hauptteil der endogenen TLymphozyten (über 60%) liegt ebenfalls in Membrankontakt mit den ICAM-1-positiven IDC. Dieses unterstützt die aus der Elektronenmikroskopie gewonnenen Beobachtungen, dass IDC ein Netzwerk formen, durch das die T-Lymphozyten kontinuierlich rezirkulieren und so 84 spezifische Klone für das präsentierte Antigen herausfiltern können (STEINMAN et al., 1997). Die niedrigere Frequenz (60% versus 80%) der Membrankontakte im Vergleich zu den injizierten T-Lymphozyten kann teilweise durch die fehlende Färbung der T-Lymphozyten erklärt werden, da nur die IDC durch den ICAM-1 Antikörper nachgewiesen werden. Auswirkung der Membrankontakte auf die T-Lymphozyten Interessant sind diese Ergebnisse im Hinblick darauf, dass die Aktivierungsstadien der TLymphozyten, wie sie hier beobachtet worden sind, unterschiedliche Ansprüche an die Membrankontakte stellen. So sind naive T-Lymphozyten abhängig von der Präsentation ihres spezifischen Antigens in Zusammenhang mit einem MHC-Peptid-Komplex und kostimulatorischen Molekülen, um zu proliferieren, sich in Effektorzellen zu differenzieren (BANCHEREAU u. STEINMAN, 1998) und benötigen damit den ständigen Kontakt zu zahlreichen IDC in den lymphatischen Organen. Effektor T-Lymphozyten sind bereits aktiviert und potentiell schädlich für den Organismus. Nach erfolgreicher Eliminierung des Antigenstimulus ist es wichtig, die Ansammlung einer großen Anzahl von Effektorzellen zu verhindern. Zur Aufrechterhaltung der Homöostase wird nach Aktivierung des TCR das FasMolekül (CD95) hochreguliert. Die Bindung von Fas/CD95 durch FasL/CD95L auf den IDC führt zur Aktivierung des programmierten Zelltods (Apoptose) und damit zur Beendigung der Immunantwort (VAN PARIJS u. ABBAS, 1998). Memory T-Lymphozyten, die bei einer Sekundärantwort schneller Effektorfunktionen (Sekretion von IFN-γ, IL-4, IL-5 nach 12-24h, Proliferation bei geringen AntigenKonzentrationen) exprimieren können, könnten durch die Membrankontakte mit IDC in Abwesenheit des Antigens überleben (LONDON et al., 1999). Aber auch für die Auslösung einer sekundären Immunantwort benötigen memory T-Lymphozyten die Präsentation des spezifischen Antigens durch eine IDC. Auch die unterschiedliche Herkunft und Behandlung der naiven, memory (Ductus thoracicus durch Separation) und Effektor (Lymphknoten durch polyklonale Aktivierung über den T-Zellrezeptor und CD28) T-Lymphozyten scheint für das Phänomen der Membrankontakte eine untergeordnete Rolle zu spielen. 85 Dynamik der Membrankontakte Die T-Zellareale können nach Betrachtung der Membrankontakte von naiven, memory und Effektor T-Lymphozyten mit IDC als Kompartimente eingeordnet werden, in denen die Membrankontakte ein sehr robustes Phänomen darstellen. IDC bilden dabei ein dichtes Netzwerk aus, durch das sich die T-Lymphozyten während ihrer Wanderung bewegen und zahlreiche Kontakte aufnehmen können. GUNZER et al. (2000) konnten in einem 3-DKollagengel ebenfalls zeigen, dass sich T-Lymphozyten in ständigem Kontakt zu IDC befinden. Interessanterweise konnten sie zeigen, dass die Kontakte dynamischer Natur (im Minutenbereich) sind und T-Lymphozyten von einer IDC zur nächsten wandern, bevor sie aktiviert werden. Dieses Modell könnte eine Erklärung für die hohe Anzahl Membrankontakte bieten, die sich in vivo finden lassen. LORD et al., (1999) berechnen über die Dissoziationskonstanten der beteiligten Moleküle ein kinetisches Modell, in dem durch die niedrige Affinität viele verschiedene Antigen-präsentierende Zellen abgesucht werden können. Die von uns gemachte Beobachtung, dass zu verschiedenen Zeitpunkten 80% der TLymphozyten Membrankontakte mit IDC in einem Antigen-unspezifischen Modell aufweisen, unterstützt diese dynamische Sicht. Die Anzahl der Membrankontakte ist unabhängig von den verschiedenen beobachteten Zeitpunkten (24h, 48h, 72h und 96h) der Untersuchung. Diese Feststellung lässt vermuten, dass diese Kontakte zu jeder Zeit stattfinden. Übereinstimmend mit der hohen Anzahl der Membrankontakte ist die Beobachtung von vorübergehenden, kurz andauernden (transienten) Kontakten zwischen T-Lymphozyten und DC, wenn kein spezifisches Antigen präsentiert wird (HAUSS et al., 1995; INGULLI et al., 1997). Die transiente Bindung der Zellen könnte erklären, wie T-Lymphozyten während ihrer Wanderung durch die lymphatischen Gewebe eine möglichst hohe Anzahl von DC nach ihrem Antigen absuchen können. Keine Ausbildung von Zellaggregaten (Kluster) von T-Lymphozyten mit IDC im in vivo Modell Die Möglichkeit zur physikalischen Überwachung und Beobachtung der anatomischen Lokalisation von T-Lymphozyten und IDC in den Kompartimenten der lymphatischen Organen erlaubt einige Schlussfolgerungen in Hinblick auf die Antigen-Präsentation in vivo in den Geweben. So wird aus verschiedenen Studien berichtet, dass IDC Zellaggregate (Kluster) 86 mit T-Lymphozyten (INGULLI et al., 1997; KUDO et al., 1997) oder B-Lymphozyten (DUBOIS et al., 1997; KUSHNIR et al., 1998) ausbilden. In dieser Miniaturumgebung können IDC die Proliferation von ruhenden T-Lymphozyten einleiten, wobei die Ausbildung der Zellaggregate ein Adhäsionsmolekül abhängiges Phänomen zu sein scheint. In der untersuchten Antigen-unspezifischen Situation lassen sich hingegen keine oder nur sehr kleine Kluster (weniger als 5 T-Lymphozyten/IDC) zwischen den injizierten T-Lymphozyten und den IDC finden. Das Fehlen von großen Klustern mit mehr als 5 T-Lymphozyten an einer IDC im Gewebe kann durch verschiedene Beobachtungen erklärt werden. Die Wanderungsdynamik der T-Lymphozyten im Gewebe vermindert das stabile Binden an die IDC und favorisiert das Ablösen der Zellen. Die Beweglichkeit der T-Lymphozyten ist stark erhöht und ist in der Gegenwart von IDC verlängert, vermutlich hervorgerufen durch Zytokine, die von den IDC sezerniert werden (TANG und CYSTER, 1999). Diese locken nicht nur naive oder Effektor T-Lymphozyten in IDC-enthaltende Kompartimente, sondern fördern auch eine ungerichtete Migration in den Kompartimenten. Auch wurde vorwiegend aus Antigen-spezifischen in vitro Kulturen über die Ausbildung von Klustern berichtet. In diesen Kulturen fehlt jedoch die dreidimensionale Miniaturumgebung mit extrazellulärer Matrix und retikulären Zellen, die das Grundgerüst der Organe stellen und die Wanderungsdynamik und die Position von wandernden Zellen deutlich beeinflusst. GUNZER et al. (2000) konnten in einem, dem Gewebe nachgeahmten 3D-Kulturgel ebenfalls keine Ausbildung von Klustern feststellen. Vergleich der Membrankontakte im Rattenmodells mit einem Mausmodell Es stellt sich die Frage, ob es sich bei den bisher nachgewiesenen Membrankontakten zwischen T-Lymphozyten und IDC um speziesspezifische Effekte in der Ratte handeln kann. Um einen Vergleich zu den Immunhistologien der Ratte erstellen zu können, wurden die Membrankontakte der endogenen T-Lymphozyten (Gegenfärbung mit Hämatoxylin) mit IDC in der Maus ausgewertet, die über einen Antikörper gegen DEC-205 (NLDC-145) nachgewiesen worden sind. Endogene T-Lymphozyten in der Maus weisen zu etwa 60% Membrankontakte zu diesen IDC in der Milz auf. Dabei ist allerdings zu beachten, dass DC keine phänotypisch oder funktional einheitliche Gruppe bilden (GRABBE et al., 2000). Diskutiert wird dabei zum einen die Abstammung von einer myeloiden Stammzelle, die sich 87 unter verschiedenen Kulturbedingungen sowohl in Makrophagen (M-CSF), als auch bei Zugabe des GM-CSF und verschiedenen Zytokinen wie IL-4 oder TGF-β in dendritische Zellen differenzieren kann. Aber auch die Abstammung von einer lymphoiden Stammzelle, die sich in Lymphozyten und DC differenzieren kann, konnte nachgewiesen werden. In der Milz werden lymphoide und myeloide DC-Populationen aufgrund der Expression von CD8α, 33D1 und DEC-205 unterschieden (SALOMON et al., 1998). So sind DC der myeloiden Abstammung, Cd8α-, DEC-205-/low CD11b+, vorwiegend in der Marginalzone anzutreffen. Diese führen zur Produktion eines unterschiedlichen Zytokinprofils in T-Lymphozyten und sind verantwortlich für die Einleitung von T-Zellabhängigen Immunantworten. Lymphoide DC, Cd8α+, DEC-205+ CD11b-, die zu hohen Anteilen in Milz, Thymus, Lymphknoten und Peyersche Platten anzutreffen sind, sind für die Induktion von Toleranz zuständig (CELLA et al., 1997). Finden wir also in der Maus eine Größenordnung von 60% Membrankontakten, so könnte eine Begründung sein, dass der verwendete Antikörper DEC-205 nur DC der myeloiden Abstammung erfasst. Im Gegensatz zu den spezifischen Markern in der Maus, exprimieren alle IDC eines reifen Phänotyps ungeachtet ihrer Herkunft oder Funktion hohe Level an MHC Klasse I und II und kostimulatorische Moleküle wie ICAM-1 (BANCHEREAU u. STEINMAN, 1998). Aufgrund der Schwierigkeiten bei der Definition der IDC und einem einheitlichen spezifischen Marker für IDC in der Ratte ist deshalb die Arbeit auf den ausgereiften Phänotyp beschränkt und ermöglicht dadurch eine eindeutige Identifikation. In diesem Sinne ist es von Vorteil gewesen, sich die Expression von ICAM-1 und MHC Klasse II zunutze zu machen, die, unabhängig von der myeloiden oder lymphoiden Abstammung oder den Kulturbedingungen, auf allen IDC des reifen Phänotyps einheitlich ist. In der Ratte scheint der Unterschied zwischen verschiedenen Phänotypen der DC keinen Einfluss auf die Anzahl der Membrankontakte zu haben. 88 2. Funktion von LFA-1 bei Membrankontakten im Mausmodell Um besser verstehen zu können, wie die Membrankontakte zwischen T-Lymphozyten und DC, die bisher in der Immunhistologie und der konfokalen Mikroskopie betrachtet worden sind, in vivo zustande kommen und zu bewerten sind, wurde die Rolle des Leukozytenfunktionsantigens-1 (LFA-1) untersucht. Mit Fluoreszenzfarbstoff markierte Wildtypzellen und LFA-1-defiziente Zellen wurden gleichzeitig in Wildtypmäuse injiziert. Nach 2h wurden die Membrankontakte zu DC in der Milz betrachtet. Obwohl LFA-1 eine Schlüsselrolle bei der Zelladhäsion zugeschrieben wird (DEETHS u. MESCHER, 1999), befanden sich sowohl die Wildtypzellen, als auch die LFA-1-defizienten Zellen zu etwa 60% in Membrankontakt zu DC. Das fehlende LFA-1 auf den T-Lymphozyten scheint den Anteil der Membrankontakte nicht zu beeinflussen. Eine Erklärung für diese Befunde könnte sein, dass auch DC das LFA-1-Molekül und T-Lymphozyten den Bindungspartner ICAM-1 exprimieren. Erst durch den zusätzlichen Einsatz von Antikörpern gegen LFA-1 oder ICAM-1 könnte in einem weiteren Versuchsansatz der Einfluss des LFA-1 auf die Kontakte deutlicher gezeigt werden. Aber wie SWARTE et al. (1998) zeigen konnten, wird auch über L-Selektin ein Kontakt zwischen Zellen ausgebildet, was auf eine gewisse Redundanz der Zelladhäsion schließen läßt. Auch weitere Liganden-Rezeptorenpaare wie CD2/ LFA-3, CD28/ CD80 und CD40/ CD40L können die Antigen-unabhängige, transiente Bindung zwischen T-Lymphozyten und DC in Abwesenheit des LFA-1-Moleküls vermitteln (HAUSS et al., 1995). 3. Membrankontakte beeinflussen den Anteil der Ki-67+ und BrdU+ T-Lymphozyten Die Proliferation der injizierten Effektor T-Lymphozyten wurde über die Expression des Zellzyklus-assoziierten Zellkernantigen Ki67 dargestellt, das über den gesamten Zellzyklus (G1-M2) hindurch exprimiert wird (GERLACH et al., 1997). Ein weiterer Nachweis der Proliferation ist der Einbau von BrdU, das während der S-Phase des Zellzyklus in die DNS 89 eingebaut wird. Bei der Untersuchung der Proliferation der injizierten Effektor TLymphozyten zeigte sich, dass zu allen Beobachtungszeitpunkten Proliferation in der PALS nachweisbar war (Daten nicht gezeigt). Im Inokulum befindet sich ein Anteil von 50% der TLymphozyten im Zellzyklus, jedoch sind im Blut nach bereits 1h und zu späteren Zeitpunkten nur noch 10% der injizierten T-Lymphozyten im Zellzyklus nachzuweisen. Das entspricht der Beobachtung, dass nach Aktivierung von T-Lymphozyten etwa 70% dieser Zellen innerhalb von 24h nach Injektion absterben (BINNS et al., 1992; SMITH et al., 1980). Betrachtet man diesen Anteil der proliferierenden T-Lymphozyten näher und in Abhängigkeit zu den Membrankontakten, so war festzustellen, dass sich signifikant mehr injizierte T-Lymphozyten im Zellzyklus und auch in der S-Phase befanden, wenn sie gleichzeitig einen Membrankontakt mit einer DC aufwiesen. Nach 24h befanden sich etwa 30% der injizierten T-Lymphozyten mit Kontakt zu einer DC im Zellzyklus, jedoch nur 20% der T-Lymphozyten, die keinen Kontakt zu einer DC aufwiesen. Individuelle Schwankungen zwischen den Tieren sind von 20-40% zu finden, die Tendenz zeigt sich jedoch in allen untersuchten Tieren. Die Hälfte der T-Lymphozyten ohne Membrankontakt konnte mit der Hilfe des konfokalen Mikroskops als falsch-positiv erkannt werden. Korrigiert man die 20% der T-Lymphozyten im Zellzyklus um diese Erkenntnis, so liegt man bei etwa 10% der injizierten Zellen im Zellzyklus, die sich auch im Blut wiederfinden lassen. Auch für die T-Lymphozyten in der S-Phase konnten gleiche Tendenzen gefunden werden. Es war ein Anstieg der Zellen im Zellzyklus oder der S-Phase um 50% zu verzeichnen, wenn die T-Lymphozyten in Membrankontakt zu IDC lagen. Auch nach 72h ist der Einfluss der Membrankontakte auf den Zellzyklus und die S-Phase der T-Lymphozyten noch nachzuweisen. Im Vergleich zu den Werten nach 24h sind die Werte auf etwa die Hälfte abgefallen, bleiben in der Tendenz jedoch gleich. Auch hier finden sich signifikante Unterschiede von T-Lymphozyten mit Membrankontakt zu IDC. In diese Ergebnisse kann auch die Überlegung einbezogen werden, die mit dem konfokalen Mikroskop gezeigt werden konnte. So ist zu vermuten, dass auch die Hälfte der TLymphozyten im Zellzyklus oder in der S-Phase, die keinen Membrankontakt aufgewiesen haben, ober- oder unterhalb der Schnittebene durchaus in Membrankontakt liegt. Eine weitere Erklärung für den Prozentsatz der T-Lymphozyten im Zellzyklus ohne Kontakt kann die Dynamik der Zell-Zellkontakte bieten, die von GUNZER et al. (2000) gefunden wurden. So 90 können die T-Lymphozyten durch zahlreiche Kontakte zu verschiedenen DC aufeinanderfolgende Signale akkumulieren und so weiter im Zellzyklus verbleiben oder weiter durch die S-Phase geleitet werden. Die Gewebeumgebung unterstützt die Ansammlung von Einzelsignalen, die schlussendlich zu einer Aktivierung und Auslösung einer Immunantwort führen kann. Da sich im äußeren Anteil der PALS vermehrt auch B-Zellen aufhalten (STEINIGER et al., 2000), die zu ihrer Enddifferenzierung in Plasmazellen die Hilfe von aktivierten, Antigen-spezifischen T-Lymphozyten benötigen (DEFRANCO, 1988), stellte sich die Frage, ob sich die Membrankontakte zwischen dem äußeren und inneren Anteil der PALS unterscheiden und nachfolgend zu einer erhöhten Proliferation führen. Die Membrankontakte zwischen T-Lymphozyten und B-Lymphozyten belaufen sich im äußeren Bereich auf über 70%. Im inneren Bereich der PALS haben nur 20% der injizierten T-Lymphozyten Membrankontakt zu B-Lymphozyten. Es lässt sich also vermuten, dass am Übergang der PALS zu den Follikeln T-Lymphozyten sowohl zu DC, als auch gleichzeitig zu BLymphozyten Membrankontakte haben. Diese Mikroumgebung nimmt eine Schlüsselrolle für die Funktion der T- und B-Lymphozyten, sowie den DC während einer Immunantwort ein (VAN ROOIJEN, 1990). T-Lymphozyten, die sich im Zellzyklus befinden, sind gleichmäßig über beide Bereiche der PALS verteilt. Im inneren, wie im äußeren Bereich befinden sich 30% der injizierten T-Lymphozyten im Zellzyklus, wenn sie einen Membrankontakt zu DC aufweisen. Betrachtet man hingegen die T-Lymphozyten, die sich in der S-Phase befinden, also eine Zellteilung durchlaufen, so finden sich nach 24h im inneren Anteil 6% der TLymphozyten in der S-Phase, im äußeren sind es jedoch über 8%. Deutlicher wird dieser Unterschied nach 72h, wenn sich nur noch 2% im inneren Bereich, aber mehr als die doppelte Anzahl im äußeren Bereich in der S-Phase befindet. Auch zahlreiche endogene Lymphozyten, bei denen allerdings nicht zwischen T- oder B-Lymphozyten unterschieden werden konnte, proliferieren im äußeren Bereich der PALS. Nach Kontakt zu DC können stimulierte THelferzellen im äußeren Anteil der PALS auf B-Zellen treffen und diese zur Antikörperproduktion stimulieren. Im Zusammenspiel mit CD8+ T-Lymphozyten können sie diese zu einer zytotoxischen Immunantwort „lizenzieren“ (LANZAVECCHIA, 1998) oder aber Makrophagen unterstützen bei der Eliminierung von Fremdkörpern (GORDON, 1999; JANEWAY et al.,1999). 91 Membrankontakte finden unabhängig von der Lokalisation, dem Aktivierungsstatus der TLymphozyten und unabhängig vom Zeitpunkt auf einem sehr hohen Niveau statt. Mit diesen Ergebnissen können die in verschiedenen Zelltransfermodellen ermittelten Daten in anderem Licht betrachtet werden. So produzieren DC Chemokine, die verschiedene Aktivierungsstadien von T-Lymphozyten, andere DC oder weitere Zelltypen anlocken können wie z.B. das secondary lymphoid tissue chemokine (SLC) (GUNN et al., 1999). Durch ständig im Gewebe (konstitutiv) exprimierte Chemokine können DC Lymphozyten in T- und BZellkompartimente unterteilen. In Anbetracht der erhobenen Daten ist es jedoch fraglich, ob die Anlockung von T-Lymphozyten ausschließlich durch die von DC sezernierten Chemokine zustande kommt oder ob nicht die Mikroumgebung der Kompartimente und das Netzwerk der DC zu ersten Membrankontakten zwischen den Zellen führen. Chemokine könnten die Art und Funktion des Kontaktes zwischen T-Lymphozyten und DC bestimmen und Immunantworten regulieren. Dieser Frage wäre in der Fortsetzung dieser Arbeit weiter nachzugehen. 92 VI. Zusammenfassung Andrea Sahle Membrankontakte von T-Lymphozyten mit dendritischen Zellen in den sekundär lymphatischen Organen der Ratte Bisher sind nur wenige in vivo Daten zu den Kontakten zwischen T-Lymphozyten und DC erhoben worden, obwohl dem Zusammenspiel von T-Lymphozyten und dendritischen Zellen eine ausschlaggebende Rolle bei der Kontrolle von Immunantworten und zahlreichen weiteren Funktionen zugeschrieben wird. Dendritische Zellen werden als besonders potente Antigenpräsentierende Zellen beschrieben, da sie in der Peripherie Antigen aufnehmen, es prozessieren und durch ihre sehr hohe Expression von MHC und kostimulatorischen Molekülen primäre und sekundäre T-Zellabhängige Immunantworten auslösen können. T-Lymphozyten, die vom Blut in die Gewebe und zurück wandern können, nehmen in den sekundär lymphatischen Organen vielfachen Kontakt zu den Antigen-tragenden DC auf. Durch dieses System wird aus weiten Gebieten des Körpers Antigen konzentriert in den lymphatischen Organen angeboten. Um ein sensibles Zusammenspiel zu gewährleisten, benötigen die Zellen direkten physikalischen Kontakt und Interaktion miteinander. Es ist jedoch bislang in keinem System analysiert worden, in welcher Anzahl die Kontakte in einer physiologischen Situation in vivo in den Kompartimenten der lymphatischen Organe vorkommen und durch welche Parameter sie beeinflusst werden. Diese Erkenntnis könnte zu einem besseren Verständnis der Regulation von Immunantworten beitragen. Um immunhistologisch nachweisen zu können, welcher Anteil von T-Lymphozyten sich in Membrankontakt zu IDC befindet, wurden CD4+ T-Lymphozyten des kongenen Rattenstammes LEW.7B(BH) in naive (CD45RC+) und memory (CD45RC-) Zellen separiert. Des weiteren wurden aus dem Lymphknoten stammende T-Lymphozyten mit monoklonalen Antikörpern über den T-Zellrezeptor und CD28 aktiviert und während der Inkubation mit 5’-Brom-2’Desoxyuridin (BrdU) markiert. Diese Zellpopulationen wurden intravenös in LEW-Ratten (RT7a) injiziert. Nach 24h wurden die Milz, die Lymphknoten und die 93 Peyerschen Platten entnommen. Außerdem wurde die Milz zu weiteren Zeitpunkten (1h, 9h, 72h 96h) gewonnen. Es erfolgte die immunhistologische Darstellung der Membrankontakte zwischen den T-Lymphozyten und DC in den jeweiligen T-Zellarealen (PALS, Parakortex, interfollikuläre Region). Es zeigte sich, dass sich in vivo 80±10% der injizierten T-Lymphozyten in Membrankontakt zu DC befindet. Dieses Phänomen lässt sich unabhängig vom lymphatischen Organ, unabhängig vom Zeitpunkt nach Injektion und unabhängig vom Aktivierungsstadium der injizierten T-Lymphozyten beobachten. Auch die dem Empfänger eigenen, endogenen T-Lymphozyten befinden sich zu über 60% in Membrankontakt zu IDC. Durch ihre langen Ausläufer bilden IDC ein dichtes Netzwerk in den T-Zellarealen und ermöglichen eine effektive Überwachung des aus der Peripherie stammenden Antigens durch die wandernden T-Lymphozyten. Um ausschließen zu können, dass der hohe Anteil der Membrankontakte durch eine Übereinanderlagerung des Farbniederschlags auf den Zelloberflächen zustande kommt, erfolgte im weiteren eine Aufarbeitung der Immunhistologien in der konfokalen Mikroskopie. Durch die Verwendung von Fluorochrom-markierten Farbstoffen kommt ein geringerer Farbniederschlag zustande. Es konnte auch mit dieser Methode ein Anteil von über 65% Membrankontakte aufgezeigt werden. Die Kontakte waren in mehr als der Hälfte der durch die Zelle gelegten Schichten ausgebildet. In etwa 50% der Fälle ließen sich auch ober- oder unterhalb der Schnittebene noch Kontakte feststellen. Damit konnten die hohen Anteile an Membrankontakten in der lichtmikroskopischen Methode bestätigt werden. Um Hinweise auf die Funktion der bislang morphologisch nachgewiesenen Membrankontakte zu erhalten, wurden T-Lymphozyten im Zellzyklus und in der S-Phase immunhistologisch identifiziert. Es zeigte sich, dass sich signifikant mehr T-Lymphozyten im Zellzyklus (Ki-67+) oder in der S-Phase (BrdU+) befanden, wenn sie einen Kontakt zu einer IDC aufwiesen. Unter Verwendung eines spezifischen Markers für DC im Mausmodell konnte gezeigt werden, dass auch spezies-unspezifisch der Hauptteil der endogenen T-Lymphozyten in der Milz Membrankontakt zu DC aufweist. Im Mausmodell wurde die Rolle des Leukozytenfunktionsantigen-1 (LFA-1) getestet. Vor der Injektion in Wildtypmäuse wurden Zellen von LFA-1-defizienten (CD11a-/-/CD18) Mäusen, aber auch Wildtypzellen markiert und immunhistologisch in den Kompartimenten der Milz 94 nachgewiesen. Die Membrankontakte erwiesen sich als unabhängig von der LFA-1Expression auf den T-Lymphozyten. Da jedoch auch dendritische Zellen LFA-1 und T-Lymphozyten das ICAM-1-Molekül auf ihrer Zelloberfläche exprimieren, müsste in weiteren Versuchen durch den Einsatz eines anti-ICAM-1-Antikörpers der Einfluss von LFA1 auf die Membrankontakte zwischen den Zellen untersucht werden. Aber auch weitere Liganden-Rezeptorpaare wie CD2/ LFA-3 und CD28/ CD80 können transiente, Antigenunabhängige Kontakte vermitteln. Diese Redundanz der Moleküle weist darauf hin, wie wichtig die Interaktion der Zellen im Organismus ist. Die Wanderung der T-Lymphozyten durch das enge Netzwerk von DC in den T-Zellarealen der sekundär lymphatischen Organe ermöglicht das Absuchen von möglichst vielen Oberflächen (DC) nach spezifischem Antigen und damit der Regulierung und Kontrolle von Immunantworten. Fraglich bleibt die Rolle der Chemokine bei der Anlockung der Antigen-spezifischen T-Lymphozyten. Möglich wäre auch dynamische Aufnahme von zahlreichen Kontakten, deren Signale kumuliert würden, um T-Lymphozyten zu aktivieren. Die Ergebnisse der vorliegenden Arbeit zeigen eine einfache Möglichkeit auf, wie die Regulierung und Kontrolle einer Immunantwort gewährleistet werden kann. 95 VII. Summary Andrea Sahle Interaction of T-lymphocytes with dendritic cells in the secondary lymphoid organs of the rat The interaction between T lymphocytes and dendritic cells (DC) plays a major role in the control of the immune response and in many other functions. However, few in vivo data have been collected so far on this interaction. Dendritic cells are very potent antigen presenting cells since they take up antigen in the periphery, process it, and thus initiate primary and secondary T cell dependent immune responses. They do this through their high expression of MHC and costimulatory molecules. T lymphocytes, which migrate from the blood to the tissue and back, interact in lymphatic organs with the antigen bearing DC. Antigen from all areas of the organism is presented in a concentrated way via this system. In order to ensure interaction the cells need direct physical contact. It has not been studied in animals or humans how many such contacts occur in the physiological situation in vivo in the compartments of lymphatic organs and what parameters influence these contacts. These investigations could lead to a better understanding of the regulation of the immune response. In order to investigate what proportion of T lymphocytes have direct physical contact with DC in the T cell areas of lymphatic organs, lymphocytes of congenic LEW.7B(BH) rats were separated into naïve (CD45RC+) and memory (CD45RC-) cells. Furthermore, lymph node T cells were stimulated with monoclonal antibodies against the T cell receptor and CD28 in the presence of BrdU to show proliferation. These cell populations were injected iv into LEW (RT7a) rats. Spleen, lymph node, and Peyer’s patches were removed after 24h. Additionally, spleen was removed at various time points (1h, 9h, 72h, 96h). An immunohistological demonstration of the membrane contacts between T lymphocytes and DC in the respective T cell area (PALS, paracortex, interfollicular region) followed. It was shown in the congenic rat model that in vivo 80±10% of the injected T cells had membrane contact with DC. This phenomenon was observed independent of the lymphatic organ and T lymphocyte subset studied. It was also independent of the time following cell injection. More 96 than 60% of the endogenous T cells also had membrane contact with DC building a network via their long dendritic branches. Then an analysis of the immunohistologies using a confocal microscope was performed. It was shown that more than half of the sections through a cell revealed contact between the cells. Furthermore, in 50% of the cases contact could still be observed above and below the projection. Using a mouse model the role of leukocyte function antigen-1 (LFA-1) was investigated. Before injection into wild type mice, wild type cells or cells from LFA-1 deficient (CD11a-//CD18) mice were labelled. These cells were then analysed immunohistologically in the spleen compartments. In the mouse model, using a specific DC marker, the majority of injected T lymphocytes also had membrane contact with DC. This contact was not dependent on LFA-1 expression on T lymphocytes. To exclude a redundant expression of surface molecules it would be interesting to use a monoclonal antibody against ICAM-1 or LFA-1 showing the influence of LFA-1. Meanwhile other receptor/ligand pathways, CD2/ LFA-3, CD28/ CD80 or Cd40/ CD40L could be involved in the transient, antigen independent contacts between T lymphocytes and DC. Furthermore, T lymphocytes were immunohistogically identified in cell cycle (Ki-67+) and in the S-phase (BrdU+). Significantly more T lymphocytes were in cell cycle or S-phase, ie proliferating, when contact with a DC was observed. Contact is important for the survival of T lymphocytes and DC and for tolerance. It is a constant phenomenon that is not dependent on cell surface molecules such as L-selectin, IL-2, which change upon activation of T lymphocytes and molecules such as LFA-1. During migration T lymphocytes take up dynamic contact with DC allowing them to control the immune response against foreign and most likely self proteins. The migration of T lymphocytes through the tight network of DC in the secondary lymphoid organs could show a simple mechanism to regulate and control immune responses. 97 VIII. Literaturverzeichnis ABBAS, A. K., A. H. LICHTMAN, J. S. POBER (1994): Cellular and molecular immunology. W.B. Saunders Company AGER, A. (1994): Lymphocyte regulation and homing: roles of adhesion molecules and chemoattractants. Trends Cell. Biol. 4, 326-33 ALBERT, M. L., B. SAUTER, N. BHARDWAJ (1998a): Dendritic cells acquire antigen from apoptotic cells and induce class I-restricted CTLs. Nature 392, 86-89 ALBERT, M. L., S. F. PEARCE, L. M. FRANCISCO, B. SAUTER, P. ROY, R. L. SILVERSTEIN, N. BHARDWAJ (1998b): Immature dendritic cells phagocytose apoptotic cells via alphavbeta5 and CD36, and cross-present antigens to cytotoxic T lymphocytes. J. Exp. Med. 188, 1359-1368 ANJUERE, F., P. MARTIN, I. FERRERO, M. L. FRAGA, G. M. DEL HOYO, N. WRIGHT, C. ARDAVIN (1999): Definition of dendritic cell subpopulations present in the spleen, Peyer's patches, lymph nodes, and skin of the mouse. Blood 93, 590-598 BANCHEREAU, J. u. R. M. STEINMAN (1998): Dendritic cells and the control of immunity. Nature 392, 245-252 98 BEIER, R. u. A. GEBERT (1998): Kinetics of particle uptake in the domes of Peyer's patches. Am. J. Physiol. 275, G130-G137 BELL, E. B. u. S. M. SPARSHOTT (1990): Interconversion of CD45R subsets of CD4 T cells in vivo. Nature 348, 163-166 BERLIN-RUFENACH, C., F. OTTO, M. MATHIES, J. WESTERMANN, M. J. OWEN, A. HAMANN, N. HOGG (1999): Lymphocyte migration in lymphocyte function-associated antigen (LFA)-1- deficient mice. J. Exp. Med. 189, 1467-1478 BEUTNER, U. u. H. R. MACDONALD (1998): TCR-MHC class II interaction is required for peripheral expansion of CD4 cells in a T cell-deficient host. Int. Immunol. 10, 305-310 BHARDWAJ, N., J. W. YOUNG, A. J. NISANIAN, J. BAGGERS, R. M. STEINMAN (1993): Small amounts of superantigen, when presented on dendritic cells, are sufficient to initiate T cell responses. J. Exp. Med. 178, 633-642 BINNS, R. M., S. T. LICENCE, R. PABST (1992): Homing of blood, splenic, and lung emigrant lymphoblasts: comparison with the behaviour of lymphocytes from these sources. Int. Immunol. 4, 1011-1019 BODE, U. (1998): Charakterisierung von aktivierten T-Lymphozyten aus den peripheren und mesenterialen Lymphknoten der Ratte: Regulation der Migration in vivo. 99 Verlag Cuvillier, Göttingen. (Dissertation) BODE, U., C. DUDA, F. WEIDNER, M. RODRIGUEZ-PALMERO, K. WONIGEIT, R. PABST, J. WESTERMANN (1999): Activated T cells enter rat lymph nodes and Peyer’s patches via high endothelial venules: survival by tissue-specific proliferation and preferential exit of CD8+ T cell progeny. Eur. J. Immunol. 29, 1487-1495 BOISE, L. H., A. R. GOTTSCHALK, J. QUINTANS; C. B. THOMPSON (1995a): Bcl-2 and Bcl-2-related proteins in apoptosis regulation Curr. Top. Microbiol. Immunol. 200, 107-21 BOISE, L. H., A. J. MINN, C. B. THOMPSON (1995b): Receptors that regulate T-cell susceptibility to apoptotic cell death. Ann. N. Y. Acad. Sci. 766, 70-80 BOTTOMLY, K. (1999): T cells and dendritic cells get intimate. Science 283, 1124-1125 BREEL, M., R. E. MEBIUS, G. KRAAL (1987): Dendritic cells of the mouse recognized by two monoclonal antibodies. Eur. J. Immunol. 17, 1555-1559 BROCKER, T. (1997): Survival of mature CD4 T lymphocytes is dependent on major histocompatibility complex class II-expressing dendritic cells. J. Exp. Med. 186, 1223-1232 CATTORETTI, G., M. H. BECKER, G. KEY, M. DUCHROW, C. SCHLUTER, J. GALLE, J. GERDES (1992): Monoclonal antibodies against recombinant parts of the Ki-67 antigen (MIB 1 and MIB 3) detect proliferating cells in microwave-processed formalin-fixed paraffin sections. J. Pathol. 168, 357-363 100 CAUX, C., C. MASSACRIER, B. VANBERVLIET, B. DUBOIS, C. VAN KOOTEN, I. DURAND, J. BANCHEREAU (1994): Activation of human dendritic cells through CD40 cross-linking. J. Exp. Med. 180, 1263-1272 CELLA, M., A. ENGERING, V. PINET, J. PIETERS, A. LANZAVECCHIA (1997): Inflammatory stimuli induce accumulation of MHC class II complexes on dendritic cells. Nature 388, 782-787 CELLA, M., D. SCHEIDEGGER, K. PALMER-LEHMANN, P. LANE, A. LANZAVECCHIA, G. ALBER (1996): Ligation of CD40 on dendritic cells triggers production of high levels of interleukin-12 and enhances T cell stimulatory capacity: T-T help via APC activation. J. Exp. Med. 184, 747-752 CHAMBERS, C. A. (2001): The expanding world of co-stimulation: the two signal-model revisited. Trends in Immunol. 22, 217-223 CRAWFORD, K., D. GABUZDA, V. PANTAZOPOULOS, J. XU, C. CLEMENT, E. REINHERZ, C. A. ALPER (1999): Circulating CD2+ monocytes are dendritic cells. J. Immunol. 163, 5920-5928 DAILEY, M. O., W. M. GALLATIN, G. KRAAL, E. BUTCHER, I. WEISSMAN (1985): T cell clones: a model of a non-recirculating phase of T cell differentiation. Adv. Exp. Med. Biol. 186, 621-627 DANIEL, P. T., C. SCHOLZ, J. WESTERMANN, B. DORKEN, A. PEZZUTTO (1998): Dendritic cells prevent CD95 mediated T lymphocyte death through costimulatory signals. Adv. Exp. Med. Biol. 451, 173-177 101 DEETHS, M. J. u. M. F. MESCHER (1999): ICAM-1 and B7-1 provide similar but distinct costimulation for CD8+ T cells, while CD4+ T cells are poorly costimulated by ICAM-1. Eur. J. Immunol. 29, 45-53 DEFRANCO, A. L. (1988): Cell-cell interactions in the antibody response. Nature 334, 199-200 DELEMARRE, F. G., P. J. SIMONS, H. J. DE HEER, H. A. DREXHAGE (1999): Signs of immaturity of splenic dendritic cells from the autoimmune prone biobreeding rat: consequences for the in vitro expansion of regulator and effector T cells. J. Immunol. 162, 1795-1801 DE ST GROTH, B. F. (1998): The evolution of self-tolerance: a new cell arises to meet the challenge of self-reactivity. Immunol. Today 19, 448-454 DI ROSA, F., S. RAMASWAMY, J. P. RIDGE, P. MATZINGER (1999): On the lifespan of virgin T lymphocytes. J. Immunol. 163, 1253-1257 DUBOIS, D., J. M. BRIDON, J. FAYETTE, C. BARTHELEMY, J. BANCHEREAU, C. CAUX, F. BRIERE (1999): Dendritic cells directly modulate B cell growth and differentiation. J. Leukoc. Biol. 66, 224-230 DUNON, D., L. PIALI, B. A. IMHOF (1996): To stick or not to stick:the new leukocyte homing paradigm. Curr. Opin. Cell. Biol. 8, 714-723 102 DUSTIN, M. L., S. K. BROMLEY, Z. KAN, D. A. PETERSON, E. R. UNANUE (1997): Antigen receptor engagement delivers a stop signal to migrating T lymphocytes. Proc. Natl. Acad. Sci. U S A 94, 3909-3913 FRITZ, F. J., R. PABST, R. M. BINNS (1990): Lymphocyte subsets and their proliferation in a model for a delayed-type hypersensitivity reaction in the skin. Immunology 71, 508-516 FUKUMOTO,T., W. R. MCMASTER, A. F. WILLIAMS (1982): Mouse monoclonal antibodies against rat major histocompatibility antigens. Two Ia antigens and expression of Ia and class I antigens in rat thymus. Eur. J. Immunol. 12, 237-243 FULLER, K. A., O. KANAGAWA, M. H. NAHM (1993): T cells within germinal centers are specific for the immunizing antigen. J. Immunol. 151, 4505-4512 GALLATIN, W. M., I. L. WEISSMAN, E. C. BUTCHER (1983): A cell-surface molecule involved in organ-specific homing of lymphocytes. Nature 304, 30-34 GARSIDE, P., E. INGULLI, R. R. MERICA, J. G. JOHNSON, R. J. NOELLE, M. K. JENKINS (1998): Visualization of specific B and T lymphocyte interactions in the lymph node. Science 281, 96-99 GEBERT, A. (1997): The role of M cells in the protection of mucosal membranes. Histochem. Cell. Biol. 108, 455-470 103 GEIJTENBEEK, T. B., R. TORENSMA, S. J. VAN VLIET, G. C. VAN DUIJNHOVEN, G. J. ADEMA, Y. VAN KOOYK, C. G. FIGDOR (2000): Identification of DC-SIGN, a novel dendritic cell-specific ICAM-3 receptor that supports primary immune responses. Cell 100, 575-585 GERLACH, C., M. GOLDING, L. LARUE, M. R. ALISON, J. GERDES (1997): Ki-67 immunoexpression is a robust marker of proliferative cells in the rat. Lab. Invest. 77, 697-698 GIRARD, J. P. u. T. A. SPRINGER (1995): High endothelial venules (HEVs): specialized endothelium for lymphocyte migration. Immunol. Today 16, 449-457 GORDON, S. (1999): Kapitel 3: Development and distribution of mononuclear phagozytes: relevance to inflammation. In: J. I. CALLIN u. R. SNYDERMAN (Hrsg.): Inflammation: basic principles and clinical correlates. Verlag Lippincott Williams u. Wilkins, Philadelphia, USA, 2.Auflage, S.35-48 GRABBE, S., E. KAMPGEN, G. SCHULER (2000): Dendritic cells: multi-lineal and multi-functional. Immunol. Today 21, 431-433 GUNN, M. D., S. KYUWA, C. TAM, T. KAKIUCHI, A. MATSUZAWA, L. T. WILLIAMS, H. NAKANO (1999): Mice lacking expression of secondary lymphoid organ chemokine have defects in lymphocyte homing and dendritic cell localization. J. Exp. Med. 189, 451-460 104 GUNZER, M., A. SCHAFER, S. BORGMANN, S. GRABBE, K. S. ZANKER, E. B. BROCKER, E. KAMPGEN, P. FRIEDL (2000): Antigen presentation in extracellular matrix: interactions of T cells with dendritic cells are dynamic, short lived, and sequential. Immunity 13, 323-332 HALE, L. P. u. B. F. HAYNES (1999): Kapitel 8: Overview of development and function of lymphocytes In: J. I. CALLIN u. R. SNYDERMAN (Hrsg.): Inflammation: basic principles and clinical correlates. Verlag Lippincott Williams u. Wilkins, Philadelphia, USA, 2.Auflage, S.119-135 HAMANN, A. u. S. REBSTOCK (1993): Migration of activated lymphocytes. Curr. Top. Microbiol. Immunol. 184, 109-124 HAMANN, A., D. P. ANDREW, D. JABLONSKI-WESTRICH, B. HOLZMANN, E. C. BUTCHER (1994): Role of alpha 4-integrins in lymphocyte homing to mucosal tissues in vivo. J. Immunol. 152, 3282-3293 HARGREAVES, M. u. E. B. BELL (1997): Identical expression of CD45R isoforms by CD45RC+ 'revertant' memory and CD45RC+ naive CD4 T cells. Immunology 91, 323-330 HAUSS, P., F. SELZ, M. CAVAZZANA-CALVO, A. FISCHER (1995): Characteristics of antigen-independent and antigen-dependent interaction of dendritic cells with CD4+ T cells. Eur. J. Immunol. 25, 2285-2294 105 HEALY, J. I. u. C. C. GOODNOW (1998): Positive versus negative signaling by lymphocyte antigen receptors. Annu. Rev. Immunol. 16, 645-670 HIRAO, M., N. ONAI, K. HIROISHI, S. C. WATKINS, K. MATSUSHIMA, P. D. ROBBINS, M. T. LOTZE, H. TAHARA (2000): CC chemokine receptor-7 on dendritic cells is induced after interaction with apoptotic tumor cells: critical role in migration from the tumor site to draining lymph nodes. Cancer Res. 60, 2209-2217 HOWLAND, K. C., L. J. AUSUBEL, C. A. LONDON, A. K. ABBAS (2000): The roles of CD28 and CD40 ligand in T cell activation and tolerance. J. Immunol. 164, 4465-4470 HUANG, F. P., N. PLATT, M. WYKES, J. R. MAJOR, T. J. POWELL, C. D. JENKINS, G. G. MACPHERSON (2000): A discrete subpopulation of dendritic cells transports apoptotic intestinal epithelial cells to T cell areas of mesenteric lymph nodes. J. Exp. Med. 191, 435-444 HUNIG, T., H. J. WALLNY, J. K. HARTLEY, A. LAWETZKY, G. TIEFENTHALER (1989): A monoclonal antibody to a constant determinant of rat T cell antigen receptor that induces T cell activation. Differential reactivity with subsets of immature and mature T lymphocytes. J. Exp. Med. 169, 73-86 INABA, K., M. INABA, M. NAITO, R. M. STEINMAN (1993): Dendritic cell progenitors phagocytose particulates, including bacillus Calmette-Guerin organisms, and sensitize mice to mycobacterial antigens in vivo. J. Exp. Med. 178, 479-488 106 INGULLI, E., A. MONDINO, A. KHORUTS, M. K. JENKINS (1997): In vivo detection of dendritic cell antigen presentation to CD4(+) T cells. J. Exp. Med. 185, 2133-2141 JANCIC, C., H. E. CHULUYAN, A. MORELLI, A. LARREGINA, E. KOLKOWSKI, M. SARACCO, M. BARBOZA, W. S. LEIVA, L. FAINBOIM (1998): Interactions of dendritic cells with fibronectin and endothelial cells. Immunology 95, 283-290 JANEWAY, C. A., P. TRAVERS, M. WALPORT, J. D. CAPRA (1999): Kapitel 1: Basic Concepts in Immunology In: Immunobiology, The Immune System in Health and Disease. Verlag Elsevier Science, USA, 4.Auflage, S. 1-33 KAMPINGA, J., F. G. KROESE, G. H. POL, D. OPSTELTEN, H. G. SEIJEN, J. H. BOOT, B. ROSER, P. NIEUWENHUIS, R. ASPINALL (1990): RT7-defined alloantigens in rats are part of the leucocyte common antigen family. Scand. J. Immunol. 31, 699-710 KOCH, F., U. STANZL, P. JENNEWEIN, K. JANKE, C. HEUFLER, E. KAMPGEN, N. ROMANI, G. SCHULER (1996): High level IL-12 production by murine dendritic cells: upregulation via MHC class II and CD40 molecules and downregulation by IL-4 and IL-10. J. Exp. Med. 184, 741-746 KRAAL, G., M. BREEL, M. JANSE, G. BRUIN (1986): Langerhans' cells, veiled cells, and interdigitating cells in the mouse recognized by a monoclonal antibody. J. Exp. Med. 163, 981-997 107 KROESE, F. G., A. S. WUBBENA, D. OPSTELTEN, G. J. DEENEN, E. H. SCHWANDER, L. DE LEIJ, H. VOS, S. POPPEMA, J. VOLBERDA, P. NIEUWENHUIS (1987): B lymphocyte differentiation in the rat: production and characterization of monoclonal antibodies to B lineage-associated antigens. Eur. J. Immunol. 17, 921-928 KUDO, S., K. MATSUNO, T. EZAKI, M. OGAWA (1997): A novel migration pathway for rat dendritic cells from the blood : hepatic sinusoidslymph translocation. J. Exp. Med. 185, 777-784 KUSHNIR, N., L. LIU, G. G. MACPHERSON (1998): Dendritic cells and resting B cells form clusters in vitro and in vivo: T cell independence, partial LFA-1 dependence, and regulation by cross-linking surface molecules. J. Immunol. 160, 1774-1781 LANZAVECCHIA, A. (1998): Immunology. Licence to kill. Nature 393, 413-414 LONDON, C. A., V. L. PEREZ, A. K. ABBAS (1999): Functional characteristics and survival requirements of memory CD4+ T lymphocytes in vivo. J. Immunol. 162, 766-773 LORD, G. M., R. I. LECHLER, A. J. GEORGE (1999): A kinetic differentiation model for the action of altered TCR ligands. Immunol. Today 20, 33-39 108 LUDEWIG, B., S. OEHEN, F. BARCHIESI, R. A. SCHWENDENER, H. HENGARTNER, R. M. ZINKERNAGEL (1999a): Protective antiviral cytotoxic T cell memory is most efficiently maintained by restimulation via dendritic cells. J. Immunol. 163, 1839-1844 LUDEWIG, B., B. ODERMATT, A. F. OCHSENBEIN, R. M. ZINKERNAGEL, H. HENGARTNER (1999b): Role of dendritic cells in the induction and maintenance of autoimmune diseases. Immunol. Rev. 169, 45-54 LUETTIG, B., L. PAPE, U. BODE, E. B. BELL, S. M. SPARSHOTT, S. WAGNER, J. WESTERMANN (1999): Naive and memory T lymphocytes migrate in comparable numbers through normal rat liver: activated T cells accumulate in the periportal field. J. Immunol. 163, 4300-4307 MANICKASINGHAM, S. u. E. S. REIS (2000): Microbial and T Cell-Derived Stimuli Regulate Antigen Presentation by Dendritic Cells In Vivo. J. Immunol. 165, 5027-5034 MATSUE, H., D. EDELBAUM, A. C. HARTMANN, A. MORITA, P. R. BERGSTRESSER, H. YAGITA, K. OKUMURA, A. TAKASHIMA (1998): Dendritic cells undergo rapid apoptosis in vitro during antigen- specific interaction with CD4+ T cells. J. Immunol. 162, 5287-98 MATSUNO, K. u. T. EZAKI (2000): Dendritic cell dynamics in the liver and hepatic lymph. Int. Rev. Cytol. 197, 83-136 109 MAYORDOMO, J. I., T. ZORINA, W. J. STORKUS, L. ZITVOGEL, C. CELLUZZI, L. D. FALO, C. J. MELIEF, S. T. ILDSTAD, W. M. KAST, A. B. DELEO (1995): Bone marrow-derived dendritic cells pulsed with synthetic tumour peptides elicit protective and therapeutic antitumour immunity. Nat. Med. 1, 1297-1302 MEKORI, Y. A. u. D. D. METCALFE (1999): Mast cell-T cell interactions. J. Allergy Clin. Immunol. 104, 517-523 MONDINO, A., A. KHORUTS, M. K. JENKINS (1996): The anatomy of T-cell activation and tolerance. Proc. Natl. Acad. Sci. U S A 93, 2245-2252 MOSMANN, T. R., J. H. SCHUMACHER, N. F. STREET, R. BUDD, A. O' GARRA, T. A. FONG, M. W. BOND, K. W. MOORE, A. SHER, D. F. FIORENTINO (1991): Diversity of cytokine synthesis and function of mouse CD4+ T cells. Immunol. Rev. 123, 209-229 NAGATA, S. (1997): Apoptosis by death factor. Cell 88, 355-365 PABST, R. (1994): Kapitel 11: Die Systematik und Organe der Abwehr. In: DRENCKHAHN u. ZENKER (Hrsg.): Benninghoff Anatomie, Makrsokopische Anatomie, Embryologie und Histologie des Menschen. Verlag Urban u. Schwarzenberg, München, 15.Auflage, S. 733-756 PIERRE, P., S. J. TURLEY, E. GATTI, M. HULL, J. MELTZER, A. MIRZA, K. INABA, R. M. STEINMAN, I. MELLMAN (1997): Developmental regulation of MHC class II transport in mouse dendritic cells. Nature 388, 787-792 110 POPE, M., M. G. BETJES, H. HIRMAND, L. HOFFMAN, R. M. STEINMAN (1995): Both dendritic cells and memory T lymphocytes emigrate from organ cultures of human skin and form distinctive dendritic-T-cell conjugates. J. Invest. Dermatol. 104, 11-17 RESCIGNO, M., F. GRANUCCI, S. CITTERIO, M. FOTI, P. RICCIARDI-CASTAGNOLI (1999): Coordinated events during bacteria-induced DC maturation. Immunol. Today 20, 200-203 RIGBY, P. W., M. DIECKMANN, C. RHODES, P. BERG (1977): Labeling deoxyribonucleic acid to high specific activity in vitro by nick translation with DNS polymerase I. J. Mol. Biol. 113, 237-251 RISSOAN, M. C., V. SOUMELIS, N. KADOWAKI, G. GROUARD, F. BRIERE, M. DE WAAL, Y. J. LIU (1999): Reciprocal control of T helper cell and dendritic cell differentiation. Science 283, 1183-1186 SALOMON, B., J. L. COHEN, C. MASURIER, D. KLATZMANN (1998): Three populations of mouse lymph node dendritic cells with different origins and dynamics. J. Immunol. 160, 708-717 SAUTER, B., M. L. ALBERT, L. FRANCISCO, M. LARSSON, S. SOMERSAN, N. BHARDWAJ (2000): Consequences of cell death: exposure to necrotic tumor cells, but not primary tissue cells or apoptotic cells, induces the maturation of immunostimulatory dendritic cells. J. Exp. Med. 191, 423-434 111 SCHLUTER, C., M. DUCHROW, C. WOHLENBERG, M. H. BECKER, G. KEY, H. D. FLAD, J. GERDES (1993): The cell proliferation-associated antigen of antibody Ki-67: a very large, ubiquitous nuclear protein with numerous repeated elements, representing a new kind of cell cyclemaintaining proteins. J. Cell. Biol. 123, 513-522 SCHUHBAUER, D. M., N. A. MITCHISON, B. MUELLER (2000): Interaction within clusters of dendritic cells and helper T cells during initial Th1/Th2 commitment. Eur. J. Immunol. 30, 1255-1262 SCHULER, G. u. R. M. STEINMAN (1997): Dendritic cells as adjuvants for immune-mediated resistance to tumors. J. Exp. Med. 186, 1183-1187 SHAW, A. S. u. M. L. DUSTIN (1997): Making the T cell receptor go the distance: a topological view of T cell activation. Immunity 6, 361-369 SMITH, M. E. u. W. L. FORD (1983): The recirculating lymphocyte pool of the rat: a systematic description of the migratory behaviour of recirculating lymphocytes. Immunology 49, 83-94 SMITH, M. E., A. F. MARTIN, W. L. FORD (1980): Migration of lymphoblasts in the rat. Preferential localization of DNS-synthesizing lymphocytes in particular lymph nodes and other sties. Monogr. Allergy 16, 203-232 112 SOUSA, C. R., S. HIENY, T. SCHARTON-KERSTEN, D. JANKOVIC, H. CHAREST, R. N. GERMAIN, A. SHER (1997): In vivo microbial stimulation induces rapid CD40 ligand-independent production of interleukin 12 by dendritic cells and their redistribution to T cell areas. J. Exp. Med. 186, 1819-1829 SPRENT, J. (1994): T and B memory cells. Cell 76, 315-322 SPRENT, J., H. KISHIMOTO, Z. CAI, C. D. SURH, A. BRUNMARK, M. R. JACKSON, P. A. PETERSON (1996): The thymus and T cell death. Adv. Exp. Med. Biol. 406, 191-198 SPRINGER, T. A. (1990): Adhesion receptors of the immune system. Nature 346, 425-434 SPRINGER, T. A. (1994): Traffic signals for lymphocyte recirculation and leukocyte emigration: the multistep paradigm. Cell 76, 301-314 STEINIGER, B. u. P. BARTH (2000): Kapitel 3: Microanatomical compartments of the rat spleen In: Microanatomy and function of the spleen. Advances in Anatomy, Embryology and Cell Biology 151 Springer Verlag, Berlin, Heidelberg, New York, S. 9-22 STEINMAN, R. M., M. PACK, K. INABA (1997): Dendritic cells in the T-cell areas of lymphoid organs. Immunol. Rev. 156, 25-37 113 STEINMAN, R. M. u. N. BHARDWAJ (1999): Kapitel 4: Dendritic cells In: J.I. CALLIN u. R.SNYDERMAN (Hrsg.): Inflammation: basic principles and clinical correlates. Verlag Lippincott Williams u. Wilkins, Philadelphia, USA, 2.Auflage, S.49-59 STEINMAN, R. M., S. TURLEY, I. MELLMAN, K. INABA (2000): The induction of tolerance by dendritic cells that have captured apoptotic cells. J. Exp. Med. 191, 411-416 SWAIN, S. L., M. CROFT, C. DUBEY, L. HAYNES, P. ROGERS, X. ZHANG, L. M. BRADLEY (1996): From naive to memory T cells. Immunol. Rev. 150, 143-167 SWARTE, V. V., R. E. MEBIUS, D. H. JOZIASSE, D. H. VAN DEN EIJNDEN, G. KRAAL (1998): Lymphocyte triggering via L-selectin leads to enhanced galectin-3-mediated binding to dendritic cells. Eur. J. Immunol. 28, 2864-2871 TACKE, M., G. J. CLARK, M. J. DALLMAN, T. HUNIG (1995): Cellular distribution and costimulatory function of rat CD28. Regulated expression during thymocyte maturation and induction of cyclosporin A sensitivity of costimulated T cell responses by phorbol ester. J. Immunol. 154, 5121-5127 TACKE, M., G. HANKE, T. HANKE, T. HUNIG (1997): CD28-mediated induction of proliferation in resting T cells vitro and in vivo without engagement of the T cell receptor: evidence for functionally distinct forms of CD28. Eur. J. Immunol. 27, 239-47 114 TAKASHIMA, A. u. T. KITAJIMA (1998): T cell-mediated terminal maturation of dendritic cells, a critical transition into fully potent antigen presenting cells. Pathol. Biol. 46, 53-60 TALMOR, M., A. MIRZA, S. TURLEY, I. MELLMAN, L. A. HOFFMAN, R. M. STEINMAN (1998): Generation or large numbers of immature and mature dendritic cells from rat bone marrow cultures. Eur. J. Immunol. 28, 811-817 TAMATANI, T. u. M. MIYASAKA (1990): Identification of monoclonal antibodies reactive with the rat homolog of ICAM-1, and evidence for a differential involvement of ICAM-1 in the adherence of resting versus activated lymphocytes to high endothelial cells. Int. Immunol. 2, 165-171 TANCHOT, C. u. B. ROCHA (1998): The organization of mature T-cell pools. Immunol. Today 19, 575-579 TANG, H. L. u. J. G. CYSTER (1999): Chemokine Up-regulation and activated T cell attraction by maturing dendritic cells. Science 284, 819-822 TIETZ, W. u. A. HAMANN (1997): The migratory behavior of murine CD4+ cells of memory phenotype. Eur. J. Immunol. 27, 2225-2232 UNDERHILL, D. M., M. BASSETTI, A. RUDENSKY, A. ADEREM (1999): Dynamic interactions of macrophages with T cells during antigen presentation. J. Exp. Med. 190, 1909-1914 115 VAN PARIJS, L. u. A. K. ABBAS (1998): Homeostasis and self-tolerance in the immune system: turning lymphocytes off. Science 280, 243-248 VAN ROOIJEN, N. (1990): Antigen processing and presentation in vivo: the microenvironment as a crucial factor. Immunol. Today 11, 436-439 VREMEC, D. u. K. SHORTMAN (1997): Dendritic cell subtypes in mouse lymphoid organs: cross-correlation of surface markers, changes with incubation, and differences among thymus, spleen, and lymph nodes. J. Immunol. 159, 565-573 WESTERMANN, J. u. R. PABST (1990): Lymphocyte subsets in the blood: a diagnostic window on the lymphoid system? Immunol. Today 11, 406-410 WESTERMANN, J. u. R. PABST (1992): Distribution of lymphocyte subsets and natural killer cells in the human body. Clin. Investig. 70, 539-544 WESTERMANN, J. u. R. PABST (1996): How organ-specific is the migration of 'naive' and 'memory' T cells? Immunol. Today 17, 278-282 WESTERMANN, J., Z. PUSKAS, R. PABST (1988): Blood transit and recirculation kinetics of lymphocyte subsets in normal rats. Scand. J. Immunol. 28, 203-210 116 WESTERMANN, J., T. SMITH, U. PETERS, T. TSCHERNIG, R. PABST, G. STEINHOFF, S. M. SPARSHOTT, E. B. BELL (1996): Both activated and nonactivated leukocytes from the periphery continuously enter the thymic medulla of adult rats: phenotypes, sources and magnitude of traffic. Eur. J. Immunol. 26, 1866-1874 WESTERMANN, J., U. GEISMAR, A. SPONHOLZ, U. BODE, S. M. SPARSHOTT, E. B. BELL (1997): CD4+ T cells of both the naïve and the memory phenotype enter rat lymph nodes and Peyer’s patches via high endothelial venules: within the tissue their migratory behavior differs. Eur. J. Immunol. 27, 3174-3181 WILLFÜHR, K. U., J. WESTERMANN, R. PABST (1989): Immunohistological localization and characterization of FITC-labelled lymphocytes. A rapid and inexpensive method for studying migration. J. Immunol. Methods 120, 29-36 WONIGEIT, K. (1979): Characterization of the RT-Ly-1 and RT-Ly-2 alloantigenic systems by congenic rat strains. Transplant. Proc. 11, 1631-1635 ZITVOGEL, L., J. I. MAYORDOMO, T. TJANDRAWAN, A. B. DELEO, M. R. CLARKE, M. T. LOTZE, W. J. STORKUS (1996): Therapy of murine tumors with tumor peptide-pulsed dendritic cells: dependence on T cells, B7 costimulation, and T helper cell 1-associated cytokines. J. Exp. Med. 183, 87-97 117 IX. Anhang Erklärung: Hiermit erkläre ich, dass ich die Dissertation „Membrankontakte von T-Lymphozyten mit dendritischen Zellen in den sekundär lymphatischen Organen der Ratte“ selbständig verfasst habe. Bei der Anfertigung wurden folgende Hilfen Dritter in Anspruch genommen: - die Versuche zur Kanülierung des Ductus thoracicus mit anschließender Aufreinigung der CD4+T-Lymphozyten wurden von Frau Ulrike Geismar, Frau Dr. rer. nat. Ulrike Bode und Herrn Prof. Dr. med. J. Westermann durchgeführt. - Die Gewinnung von T-Lymphozyten aus peripheren und mesenterialen Lymphknoten und anschließender Aktivierung in vitro wurde von Frau Dr. rer. nat. Ulrike Bode, geb. Peters, als Methode etabliert und mit ihr als Verantwortlicher zusammen durchgeführt. - Die Gefrierschnitte der Organe und die immunhistologische Färbung derselbigen wurden mit der tatkräftigen Unterstützung von Frau I. Dressendörfer und Frau S. Lopez-Kostka angefertigt. - Die Konfokale Mikroskopie wurde methodisch von Frau Dr. med. Astrid Markus etabliert. In Zusammenarbeit mit ihr wurden die immunhistochemischen Färbungen zur Auswertung mit der konfokalen Mikroskopie erstellt. - LFA-1-defiziente Mäuse wurden im Institut von Frau N. Hogg etabliert und gezüchtet. LFA-1-defiziente T-Lymphozyten wurden der Arbeitsgruppe von Herrn Prof. Dr. J. Westermann zur Verfügung gestellt. Ich habe keine entgeltliche Hilfe von Vermittlungs- bzw. Beratungsdiensten (Promotionsberater oder andere Personen) in Anspruch genommen. Niemand hat von mir unmittelbar oder mittelbar entgeltliche Leistungen für Arbeiten erhalten, die im Zusammenhang mit dem Inhalt der vorgelegten Dissertation stehen. 118 Ich habe die Dissertation an der folgenden Institution angefertigt: - Abteilung für Funktionelle und Angewandte Anatomie der Medizinischen Hochschule Hannover Die Dissertation wurde bisher nicht für eine Prüfung oder Promotion oder für einen ähnlichen Zweck zur Beurteilung eingereicht. Ich versichere, dass ich die vorstehenden Angaben nach bestem Wissen vollständig und der Wahrheit entsprechend gemacht habe. Eigenhändige Unterschrift: 119 Aus Prioritätsgründen wurden Teilergebnisse der vorliegenden Arbeit vorgestellt: Vorträge SAHLE, A., U. BODE, E. B. BELL, R. PABST, J. WESTERMANN Interaktion von naiven, aktivierten und memory T-Lymphozyten mit dendritischen Zellen in T-Zellarealen von lymphatischen Organen. 94. Arbeitstagung der Anatomischen Gesellschaft, Hamburg, 26.-29.03.1999 WESTERMANN, J., A. SAHLE Interaktion von dendritischen Zellen und T-Lymphozyten Subpopulationen in vivo. 22. Arbeitstagung Norddeutscher Immunologen, Borstel, 10.12.1999 Poster SAHLE, A., U. BODE, E. B. BELL, R. PABST, J. WESTERMANN Interaction of naive, activated and memory T cells with interdigitating dendritic cells in lymphoid organs. 30. Tagung der Deutsche Gesellschaft für Immunologie, Hannover , 29.09.-02.10.1999 (Immunobiol. 200, S.445-6, 1999) 120 Danksagung Herrn Prof. Dr. med. R. Pabst danke ich für die freundliche Überlassung des Themas, die guten technischen Voraussetzungen bei der Durchführung dieser Arbeit und die Bereitstellung der notwendigen Räumlichkeiten. Bei Herrn Prof. Dr. med. vet. H.-J. Hedrich möchte ich mich für die freundliche Übernahme der wissenschaftlichen Betreuung bedanken. Bei Herrn Prof. Dr. med. J. Westermann möchte ich mich ganz besonders für die gute Betreuung und die stete, auch kurzfristige Bereitschaft zur Diskussion und Kritik bedanken. Ich habe in dieser Zeit nicht nur wissenschaftlich, sondern auch menschlich viel gelernt. Meinen Kobetreuern im Graduierten Kolleg, Herrn Prof. Dr. med. H.-G. Forssmann und Herrn Priv.-Doz. Dr. med. H. Holtmann möchte ich danken, dass sie mir die Möglichkeit gegeben haben, in diesem Rahmen zu promovieren. Ganz herzlich möchte ich mich bei meinen Kolleginnen Frau Dr. U. Bode und Frau Dr. B. Lüttig bedanken, mit deren Geduld, Wissen und moralischer Unterstützung ich jederzeit rechnen konnte. Frau Dr. A. Markus danke ich für die viele Zeit und Mühe, die sie sich mit der Anfertigung und Verarbeitung der konfokalen Bilder gemacht hat. Herrn Priv.-Doz. Dr. med. A. Gebert danke ich für die Unterstützung bei der Auswertung der konfokalen Bilder und für seine Unterstützung in allen graphischen und computerrelevanten Fragen. Frau I. Dressendörfer und Frau S. Lopez danke ich für die tatkräftige Hilfe und die Geduld bei der Anfertigung zahlreicher Präparate und Immunhistologien. Allen Mitarbeitern der Abteilung, deren freundliche Unterstützung, Ratschläge und Geduld eine angenehme und motivierende Arbeitsatmosphäre schaffte, möchte ich herzlich danken. Meiner Mutter, meinem Bruder und meiner Schwägerin möchte ich für das offene Ohr und die telefonische Aufbauarbeit in den kritischen Momenten dieser Arbeit danken. Frau med. vet. U. Raschke und Frau med. vet. A. Heipke danke ich für den konstanten moralischen Beistand, ohne den ich so manches Mal verzweifelt wäre. Abschließend danke ich meiner Tochter, dass sie mir in den schwierigsten Momenten geholfen hat, das Lachen nicht zu verlernen.