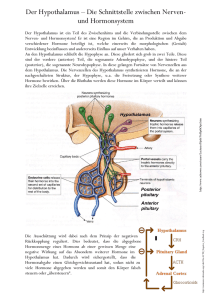
Formen der Signalübertragung
Werbung

Kommunikation von Zellen • Direkte Kommunikation Rezeptor - Ligand Gap-Junctions (Connexone) • Neuronale Kommunikation • Hormonale Kommunikation ? Pheromone (gleiche Art) ? ? Allomone (unterschiedliche Arten) ? VERGLEICH Nervensystem - Neuroendokrines System - Hormonsystem Wirkung schnell Wirkung mittelschnell Wirkung langsam kurz andauernd länger andauernd lang andauernd über Axone & Blutgefäße über Blutgefäße über Nerven „digitale“ Wirkung „variable“ Wirkung Endokrine Kommunikation Blut Unterschiedliche Endokrine Zellen Zielzellen (target cell) Parakrine Sekretion Hormon-sezernierende Zelle Zielzelle Beispiele Prostaglandine Immunsystem: IL-4 Autokrine Sekretion Hormon-sezernierende Zelle und Zielzelle Beispiele Immunsystem: IL-2 Muskelzellen: Myokine Formen der Signalübertragung Klassische endokrine Drüsen Chemische Einteilung der Hormone • Steroidhormone Cholesterin, Carrier, orale Supplementation, 10-6 – 10-11 mol/L, enzymatische Biosynthese & Abbau • Aminosäure – Derivate T3, T4, Katecholamine enzymatische Biosynthese & Abbau • Peptidhormone werden im Magen hydrolisiert, 10-9 – 10-12 mol/L genetisch gesteuerte Biosynthese LipidLöslichkeit Biosynthese, Transport & Wirkungsweise Biosynthese von Peptidhormonen Sekretionsdynamik Einfache Regulation (negative Rückkoppelung) Regulation im neuroendokrinen Hormonsystem (effektorisch – regulatorisch) Pathogenese Choleratoxin Aktiviert G-Protein cAMP , Cl- - Sekretion Durchfälle (Cholera) Onkogene (mutierte Gene): •Tyrosinkinasen, Ras, Raf... •Unkontrollierte Teilung •Fehlende Inaktivierbarkeit •Hemmung der Apoptose Push-pull Mechanismus Antwortverhalten gegenüber mehreren Hormonen ist größer als die Summe der einzelnen Antworten Die Antwort gegenüber mehreren Hormonen kann Additiv (Glucagon & Adrenalin) oder Synergistisch (Glucagon, Adrenalin & Cortisol) sein. Rezeptor und Signalübertragung Rezeptoren besitzen eine Domäne für die Hormonerkennung sowie eine für die Signalübertragung. Welches Signal entsteht, hängt vom Rezeptor und nicht vom Hormon ab! Regulation der Rezeptoren • Rezeptoraffinität • Rezeptoranzahl • Rezeptordichte •Homologe Regulation durch Konzentrationsveränderungen •Heterologe Regulation über andere Hormone Up- & Down-Regulation Down-Regulation = Hyposensitivität (C) Up-Regulation = Hypersensitivität (A) Das Antwortverhalten gegenüber Hormonen wird durch den ED50 Wert angegeben. Rezeptor-gekoppelte Signalübertragung • Rezeptor-gekoppelte Ionenkanäle • Rezeptoren mit intrinsischer Enzymaktivität • Tyrosinkinase • MAP-Kinase (wirkt auf Transkriptionsfaktoren, z.B: c-Fos) • 2nd Messenger • G-Proteine (a, b, g-Untereinheiten) • cAMP (Adenylatcyclase) • cGMP (Guanylatcyclase) • DAG & IP3 (PLC) • Ca2+ & Calmodulin • Eikosanoide über PLA2 • Ceramide • Stickoxid (NO), Superoxid (O2-) • „Zellvolumen“ (Zellschwellung, Zellschrumpfung) Nachweisverfahren • Biologische Methoden – Nur die biol. Aktivität wird gemessen – sehr komplex, aufwendig & störanfällig, schlecht reproduzierbar • Chemische Methoden – Großer Aufwand, geringe Spezifität • Immunologische Methoden (Immunoassay) – Einfache Durchführung & hohe Empfindlichkeit – Nachteil: oftmals Detektion von Vorstufen & Abbauprodukten Prinzip eines Immunoassays (z.B.: RIA, ELISA) Aufgaben des Hypothalamus (vegetativ-nervös & humoral) • • • • Stabilisierung & Steuerung des Stoffwechsels Homöostase (T, RR, Atmung, H2O, Elektrolyte) Wachstum & Reifung Überwachung der Funktion der Fortpflanzungsorgane Rezeptoren des Hypothalamus Zentren – Nutritiv („trophotrope“ Reaktionen) – Abwehr & Aggression (limbisches System, NNM, „ergotrope“ Reaktionen) – Reproduktiv (Pheromone z.B.: Bombykol) • Wärmerezeptoren • Osmorezeptoren • Hormonrezeptoren Hypothalamohypophysäres System Humorale Verbindungen des ZNS mit der Peripherie 1... Sekretion in den Portalkreislauf 2... Direkte Sekretion in die Zirkulation 3... Blut-Hirn-Schranke 4... Diffusion für lipophile Hormone 5... Rezeptorvermittelte Zytose Hypothalamus – Hypophyse Hypothalamus • Liberine (Releasinghormone RH) • Statine (Inhibitinghormone IH) Adenohypophyse (HVL) •Glandotrope Hormone •Nicht-glandotrope Hormone (GH, Prolactin) Neurohypophyse (HHL) •ADH •Oxytocin Hormone der Neurohypophyse • Antidiuretisches Hormon = ADH = Vasopressin (VP) = AVP =Adiuretin • Oxytocin ADH Gly Arg Pro Cys Asp Glu Phe Tyr Cys Oxytocin Leu Arg Pro Cys Asp Glu Ile Tyr Cys Neurohypophyse (HHL) • ADH & Oxytocin (je 9 As) • Vorläufermoleküle in Soma von Nc. supraopticus & Nc. paraventricularis produziert • axonaler Transport und enzymatische Spaltung im HHL • Ausschüttung erfolgt gekoppelt mit einem Aktionspotential („Elektrosekretionskoppelung“) • Weitere biolog. aktive Peptide „Neurophysine“ Aus Vasotocin (Träume!!) wird ADH & Oxytocin ADH = Adiuretin = Antidiuretisches Hormon = Vasopressin = AVP ADH als Neurotransmitter, Neuromodulator & Hormon Facts zu ADH • • • • • • • Osmorezeptoren im Hypothalamus ADH-produzierende Zellen sind selbst osmorezeptiv Barorezeptoren (Hochdruck) Volumenrezeptoren (Niederdruck) Henry-Gauer-Reflex (Orthostase) Temperatur & Gedächtnis Alkohol & ANP hemmen ADH • Diabetes insipidus Oxytocin – gr.: „schnelle Geburt“ Stimuli: •Dehnung (Uteruszervix, Vagina) „Ferguson-Reflex“ •Berührung (Mamillen) •Schreien des Säuglings •„snuggle hormone“ Wirkung: •Uteruskontraktion (Orgasmus, Geburt) •Milchdrüsenkontraktion (Stillen, Laktation) Adenohypophyse • Effektorisch bzw. nicht glandotrop: – Prolaktin – STH • Regulatorisch bzw. glandotrop: – TSH – ACTH – FSH – LH Prolactin (199 As) Für Galaktogenese mRNA für Casein Rezeptoren aber in fast allen Organen „Stresshormon“ Zirkadianer Rhythmus (2te Nachthälfte ) Unterdrückt Follikelsprung nach Orgasmus (♀ & ♂) PRH: mehrere Proteine (TRH, VIP, AT2, b-Endorphin) Östrogene PIH: Dopamin?? Fällt Dopamin aus: Spontanes Einschiessen d. Milch Somatostatin Prolactin Stress, Umwelteinflüsse STH – Somatotropin – Growth Hormone (GH) 191 As Streng artspezifisch (CJD!!) Schubweise Sekretion (Schlaf) Kurze HWZ (20min.) Anabole Wirkung (Doping, Basketball) Substitution im Alter Somatomedine (engl.: Insulin like growth factors) Somatomedin C (IGF-1), SM A (IGF-2) Stimulieren die Mitose Nicht rein effektorisch, auch glandotrop Starke negative Rückkoppelung mit Glucosespiegel Hypothalamus STH Stimuli: •Somatoliberin •Somatostatin Wirkung: •Proteinaufbau (Leber) •Lipolyse •Erythropoese •Wachstum (Zellproliferation) •Elektrolytretention •Glucoseverbrauch Hyperglykämie Rhythmus von STH Angriffsorte von SIH (Hypothalamus, Pankreas) „Octreotid“ STH und Wachstumsanomalien • Mangel: – – – – Oft bei Hypophyseninsuffizienz Bei Leberinsuffizienz (zu wenig Somatomedine) Bei Kindern: „Zwergwuchs“ Bei Adulten: vermehrter Proteinabbau – geschwächtes Immunsystem (meist unerkannt) • Überschuss: „Rübezahl-Krankheit“ – Riesenwuchs: „Gigantismus“ - „Akromegalie“ (an Weichteilen und Akren, wie Kinn, Nase, Extremitäten, Eingeweide) – Makroglossie Akromegalie Liberine & Statine aus dem Hypothalamus • TRH (Thyreotropin-Releasinghormon) – • TRH regt zur Ausschüttung von TSH an. CRH (Corticotropin-Releasinghormon oder -faktor) – CRH stimuliert die Ausschüttung von ACTH. • Gn-RH (Gonadotropin-Releasinghormon) – ist ein Hormon, das zur Ausschüttung von zwei Sexualhormonen anregt, dem FSH und LH. • GH-RH (Growth Hormone-Releasinghormon) – regt die Ausschüttung von Wachstumshormon an. • GH-IH (Growth Hormone-Inhibitinghormon oder Somatostatin) – • hemmt die Ausschüttung von Wachstumshormon. MSH-RH (MRH oder Melanoliberin) – bewirkt die Freisetzung von Melanotropin (MSH). • MSH-IH (MIH oder Melanostatin) – bewirkt als Gegenspieler von MSH-RG eine verminderte Ausschüttung von MSH. • PRL-RH (Prolaktin-Releasinghormon oder Prolaktoliberin) – stimuliert zur Ausschüttung von Prolaktin. • PRL-IH (Prolaktin-Inhibitinghormon oder Prolaktostatin) – hemmt die Prolaktinausschüttung. Adenohypophyse • Regulatorisch bzw. glandotrop: – ACTH • Adrenocorticotropes Hormon • Corticotropin – TSH – FSH – LH Hypothalamus – Hypophyse - NN Corticoliberin (Corticotropin-Releasing Hormon – CRH) Corticotropin (Adrenocorticotropes Hormon – ACTH) Corticoide (Cortisol, Aldosteron, Androgene) CRH - Corticotropin-Releasing Hormone (Corticoliberin) Synthese: Nc. paraventricularis Hirnstamm Lunge NN GI • Endogener Rhythmus • Feed-back mit dem limbischen System • Stressantwort • (Sympathikus) • Störung - Depression • POMC-Synthese Biosynthese von Proopiomelanocortin (POMC) Synthese in kortikotropen Zellen POMC: • ACTH (1-39) • b-Endorphin • MSH ACTH Stimulation der Lipolyse – LDL Cholesterin Corticoide • Stimulierung der NN – Corticoide – Androgene – Catecholamine • Hautpigmentierung • Mb. Addison (NNR-Insuffizienz) Nebenniere Negativer Feedback-Mechanismus (lipophil !!) Cortisol & Stress Facts zum Cortisol • • • • HWZ: 90 min. Transport über CBG & Albumin Zirkadianer Rhythmus (EEG, Arousal, Jetlag) Gluconeogenese (Stress, körperliche Arbeit) – Proteolyse – katabole Wirkung!!! – Lipolyse & Glykogenbildung • Immunsupressiv (hemmt PLA2) – Einschränkung der unspezifischen Abwehr – Hemmt die Produktion & Freisetzung von Zytokinen & Enzymen (COX2) – Allergie, Transplantation, Chemotherapie • Permissiver Effekt (z.B.: Sympathomimeticum) – Rezeptoraffinität – Katecholamine & Glucagon • ZNS (neg. Feedback, Wahrnehmung, Emotionen) • Wirkung auf Organe – GFR Magensaftsekretion Knochenabbau Cortisol & Katecholaminsynthese TH....... Tyrosinhydroxylase DBH..... Dopamin-b-Hydroxylase PNMT.. Phenyläthanolamin-N-Methyltransferase Stress-Antworten Reiz aktiv • Amygdala-Kerne passiv • Hippokampus-Areal • Abwehrverhalten (Aggression) • Vermeidung • Sympathisch-adrenalmedulläres System • • • • • Catecholamine Oxytocin, Prolaktin Renin Testosteron Endorphine • Hypophysär-adrenalkortikales System • ACTH • Kortisol Cushing-Syndrom - Hyperkortisolismus – – – – – – – – Hyperglykämie (Gluconeogenese!!) Hypertonie Osteoporose Atrophie der Muskulatur Fettumverteilung (Stammfettsucht) „Vollmondgesicht“ H2O-Einlagerungen „Büffelnacken“ Ursachen – NNR-Tumore – Vermehrte ACTH-Produktion durch hypophysäre Mikroadenome Cushing-Syndrom Morbus Addison (peripher oder zentral) • Zerstörung der NNR (autoimmun) • Hyponatriämie & Hyperkaliämie • Hypotonie • Metabolische Azidose • Muskelschwäche • lebensbedrohlich • ACTH (Pigmentierung von Haut & Schleimhäuten) • Behandelbar durch lebenslange Substitution • • • • • • • • Aldosteron „Salzsparhormon“ Mineralocorticoid Zona glomerulosa HWZ: 20 min. Teil von RAAS Na-Rückresorption (distaler Tubulus, Sammelrohr) Kalium- & Säure-Ausscheidung Schweiß- & Speicheldrüsen, Dünn- & Dickdarm Antagonist vom ANP • Stimuli: – Hyponatriämie – Hyperkaliämie – AT II Hyperaldosteronismus • Überproduktion – bei Schwangerschaft – Herzinsuffizienz – Gestörter Abbau (Leberstörungen) • Behandelbar mit Rezeptorblocker (Spironolakton) Adenohypophyse • Regulatorisch bzw. glandotrop: – TSH – FSH – LH Hypothalamus – Hypophyse Thyroidea TRH Thyreotropin-Releasing Hormon Thyreoliberin TSH Thyroidea stimulierendes Hormon Thyreotropin T3, T4 & reverse T3 Wirkungen von TRH • Hypophysär: – Biosynthese & Sekretion von TSH – Sekretion von Prolaktin & STH • Extrahypophysär: – Temperaturregulation – Retina – Regeneration von Neuronen TSH • Glykoprotein • kontrolliert alle Funktionen der Thyreoidea – Blutversorgung – aktive Jod-Aufnahme – Synthese & Sekretion • Hormone • Transportproteine (TBG, TBPA) – Chronische Stimulation • Hyperplasie • Struma T3, T4 & rT3 (lipophil!!!) • • • • • • Biosynthese: Aktive Aufnahme von J (Na+ gekoppelt) J + Tyrosin MJT (Jodination) J + J + Tyrosin DJT MJT + DJT T3 Trijodthyronin DJT + DJT T4 Tetrajodthyronin = Thyroxin • T3 – 85% extrathyreoidal durch Dejodierung von T4 • rT3 – in der Peripherie gebildet – biologisch inaktiv – setzt Schilddrüsenhormonwirkung herab Charakteristika der Schilddrüsenhormone Stoffwechsel, Wachstum & Entwicklung • • • • • • Permissiver Effekt auf Proteinsynthese Entwicklung des Nervensystems (Kretinismus) Erhöhung des Grundumsatzes Thermogenese Erhöhung des O2-Verbrauches Utilisation der Kohlenhydrate – Aufnahme im GI – Glykogenolyse – Gluconeogenese • Lipolyse (braunes Fettgewebe) • Permissiver Effekt auf Sympathikus & Catecholamine (Herz!!!) – Anzahl der b-Rezeptoren • • • • • • • • • Hypothyreose Jodmangel Enzymatische Effekte (Biosynthese) Verlangsamung aller Stoffwechselvorgänge „müdes“ Aussehen – Leistungsfähigkeit Bradykardie Neigung zum Frieren Obstipation Pathologische Hypertrophie des Herzens Reduzierte Nierenfunktion, reduzierter GAG-Abbbau Myxödem • Struma (kompensatorische Hypertrophie) • Kretinismus • Behandlung durch Substitution (T3 & T4) Hyperthyreose • oft eine Autoimmunerkrankung – Autoantikörper geg. TSH-Rezeptoren – (Mb. Basedow „Graves disease“) Hashimoto-Struma • Autonomes Wachstum von Schilddrüsengewebe – – – – – – – Körpertemperatur , Hitzeintoleranz Überregbarkeit & Tachykardie, systolischer Hypertonus Schwitzen, Diarrhö, „feuchte“ Haut Gewichtsabnahme (erhöhter Grundumsatz) Schlaflosigkeit, Haarausfall Exophtalmus (retrobulbäre Entzündung) Basedow-Struma (durch die Stimulation) • Behandlung mit Thyreostatika (Nebenwirkungen!!!) • Plummerung (Behandlung mit hochdosiertem Jodid (Lugolsche Lösung Durchblutung ) Pankreas • • • • Insulin Glucagon Somatostatin Pankreatisches Polypeptid Blutzucker: 4,0 - 5,5 mMol/l (70-100mg/dl) > 5,5 Hyperglykämie < 4,0 Hypoglykämie < 4,6 Insulinspiegel sinkt < 3,8 Glukagon, Adrenalin < 3,7 STH < 3,2 Kortisol 3,7 Glukoseaufnahme des Gehirns 3,0 Schweißausbruch, Heißhunger, Unruhe, Zittern 2,7 (<50mg/dl) Bewusstlosigkeit Insulin (51 As) • • • • • • Parakrine & endokrine Wirkung B-Zellen (Langerhans-Inseln) Proinsulin C-Peptid (Somatomedine – IGF´s) Pulsatile Sekretion, HWZ ~5min. Biphasischer Verlauf („kiss & run“ Exocytose) Autonomes NS • • • • Senkung des Blutzuckerspiegels Leber, Muskel, Fettgewebe Ausgeprägte Rezeptorregulation (Down) GTF (CrIII) – Stimulation über b-Rezeptoren & Vagus – Inhibierung über a-Rezeptoren Stimuli für die Insulinfreisetzung • Blutzuckerspiegel • Amino- & Fettsäuren • gastrointestinale Hormone • Parasympathikus Nahrungsaufnahme Insulin liefert liefert ein anorexigenes Signal „push & pull“ • Glucoseaufnahme & Glykolyse • Hemmt Gluconeogenese • Hemmt Proteolyse, Gluconeogenese & stimuliert Proteinsynthese – antikatabol & anabol!!! • Hemmt Lipolyse & stimuliert Fettspeicherung – Antiketogen & lipogen!!! • Aufnahme von As, Fs, Mg2+, K+ & freie Phosphate – Synthese von Glykogen, TG, Proteine – Zellschwellung, zelluläre Alkalose, Glykolyse, Zellteilung • Agonistisch mit STH für das Längenwachstum • Inotrope Wirkung GTT Diabetes Mellitus • Insulinmangel • Verminderte Insulinwirkung • Hyperglykämie & Glukoseintoleranz – Glukosurie & Polyurie („osmotische Diurese“) – Gefäßschäden (Mikro- & Makroangiopathien Retinopathien) – Arteriosklerose – Ketoazidose & Kussmaulatmung (Hungerstoffwechsel) – Elektrolytstörungen (intrazellulärer K+ & Pi-Verlust) – Neurologische Erkrankungen – Coma diabeticum Hypertoniker haben Insensitivität gegenüber Insulin sowie eine reduzierte Glucosetoleranz!!! Diabetes im Alter 54,3 prozentuelle Häufigkeit 60 50 40 30 17,8 20 10 6,2 1,3 0 <25 45 55-59 Jahre 65-74 Diabetes mellitus Diabetes -Typen • IDDM – juveniler Typ (Typ1-Diabetes) – Insulinproduktion – Infektionen (z.B.: Mumps-Viren) – HLA-Antigene • NIDDM – (Typ2-Diabetes) – – – – – Keine Substitution notwendig – Diäten Resistenz der Rezeptoren (Adipositas) Mangelnde Aktivierung (C-Peptid) Störung der B-Zellen Hyperinsulinämie • Erhöhter Körperfettanteil • Hypertonie Glucagon (29 As) • • • • • • • • Direkter Antagonist vom Insulin (Leber, Fettgewebe) A-Zellen Ähnlichkeit mit VIP & GIP (Prähormon) Glykogenolyse Proteolyse Gluconeogenese b-Oxidation (lipolytische Wirkung) Stimuli – – – – – Blutzuckerspiegel, freie Fs As-Konzentration lang-andauernde Anstrengungen Hunger Stress Somatostatin (D-Zellen) • Ubiquitäres Vorkommen – Hypothalamus, ZNS, Darm • Hemmt Insulin, Glucagon, Renin & Prolactin • Parakrine Wirkung (ZNS, GI, Pankreas) • Hemmt GI-Motilität – bessere Absorptionsrate über die Mukosa Nahrungsaufnahme Neuropeptide & Essverhalten Stimulierend (orexigen) – – – – – – NPY Galanin MSH b-Endorphin Orexin A und B GABA Hemmend (anorexigen) – – – – – – – – – – Leptin Insulin MSH Neurotensin TRH CCK Oxytocin Histamin Serotonin Dopamin Adipokine (etwa 100 verschiedene Vertreter bekannt) • • • • • • • • • Adiponektin (ApN-Agonisten pharmazeutisch als „Insulinsensitizer“) Resistin (Insulinresistenz – „Resistin-Antagonisten“) Leptin (Appetit) Adipsin Visfatin TNF-α RAAS (alle Teile) Interleukine etc. Adipokine Leptin (167 As) gr.: leptos = dünn • Gebildet in den Fettzellen • Ausschüttung ist proportional der Fettmasse • Hemmt die Nahrungsaufnahme im Hypothalamus (Transzytose!!!) • Hemmt NPY (orexigene Wirkung!!!) • Steigert den Grundumsatz (entkoppelnde Wirkung) • Hemmt Insulin • Leptinmangel – massive Fettsucht • Immunsystem & Fruchtbarkeit (Anorexie) • Schützt nicht vor zuviel Nahrungsaufnahme sondern verhindert Nahrungsmangel!!! Resistin resistant to insulin HGO: Hepatic Glucose Output Resistin wirkt antagonistisch zum Insulin Muskulatur & Fettgewebe können weniger Glucose aufnehmen ??? • Regulieren: • • • • • • Adipokine Glukose- und Lipidstoffwechsel (Energiestoffwechsel) Insulinsensitivität Hämostase Blutdruck Immunsystem zentralnervöse Prozesse wie Appetit • Stehen in Verdacht mit: • • • • Diabetes mellitus Typ-2 KHK Adipositas Arteriosklerose Myokine (Proteine, Zytokine, Glykoproteine, Proteoglykane) • Werden bei Muskelkontraktion aus der Muskulatur abgegeben • Derzeit ~400 verschiedene Vertreter bekannt – Myostatin (hemmt die Myogenese) – IL-6, IL-7, IL-8, IL-15 – Neutrophine (ähnlich den NGF´s) • BDNF (brain derived neurotropic factor) – Myonektin – Follistatin – Dekorin (bindet Myostatin, fördert Myogenese) Gendoping & Bodybuilding auto- para- & endokrine Effekte der Myokine • • • • • • Geweberegeneration & Reparaturmechanismen Immunmodulation - antiinflammatorisch Lipolyse & Glykogenolyse Muskelwachstum – anabole Wirkung Neurogenese & Neuroplastizität Angiogenese (bessere Kapillarisierung der Muskulatur) Wirkung von Myokinen Nach: Fiuza-Luces C et al, Exercise is the real polypill. Physiology 2013; 28: 330-58 Calcium (25.000mmol/l) Serumgehalt: 2,2 – 2,7mmol/l – ~40% gebunden an Proteine • nicht diffusibel & stark pH-Wert abhängig, weniger H+ Affinität • Alkalose Hypocalzämie (Muskelspasmen Tetanie) – ~10% komplexiert mit anorganischen Anionen • (Citrat, Phosphat, Sulfat) – ~50% (1,2mmol/l) als freie Ionen (diffusibel) • Wird exakt reguliert!!! • Biologisch aktiv – Nur 0,1% des gesamten Ca2+ befindet sich extrazellulär, etwa 1% intrazellulär – 99% gespeichert im Knochen • 500mmol/l für rasches „Speichern“ – „Entspeichern“ Aufgaben • Kontraktion – Skelettmuskulatur, Herzmuskulatur, glatte Muskulatur • Blutgerinnung • Weiterleitung von Nervensignalen – Hypercalzämie Hemmung des ZNS – Hypocalzämie Übererregbarkeit, Schwelle Tetanie – Pfötchenstellung, Kribbeln in den Händen „Karpopedalspasmen“ (Streckkrämpfe der Beine) – Osteoporose, Rachitis • Signaltransduktion • Knochen- & Zahnbildung Karpopedalspasmen Ca2+ - Metabolismus Aufnahme ~25mmol/l (¼ wird resorbiert) 10% vom resorbierten Ca2+ wird renal ausgeschieden Ca2+ gebunden an Proteine wird nicht filtriert Renale Rückresorption: • 60% proximaler Tubulus (passiv) • 30% Henle´sche Schleife (passiv) • 8% distaler Tubulus (aktiv & variabel über Parathormon) Ca2+ – Verlust: • Schweiß • plazentarer Kreislauf • Milch •Starke renale Ausscheidung (1g/d) • „Nephrolithiasis“ (Calcium-Oxalat) Calcium-Homöostase • Parathormon (PTH) Parathyrin • Vitamin D3 – Calcitriol • Calcitonin Calcium-Bestand 700 mg Aufnahme Knochen (als Apatit*): 1300 g Parathormon Extrazellulär: 2 g Niere 200 mg Plasma-Ca2+ = 2,5 mM (50% ionisiert) Intrazellulär: 5 g 500 mg (Stuhl) 200 mg * 3Ca3(PO4)2 ∙ Ca(OH, F, Cl)2 • Parathormon – Parathyrin - PTH (84 As) Stimuli: – Absinken der freien Ca2+ - Konzentration – Langandauernder Stimulus – Hyperplasie – Adrenalin • Ca2+-Rezeptoren an der Parathyreoidea • „Osteolyse“ durch Osteoklastenaktivierung - Demineralisierung – rasche Mobilisierung von Ca2+ & Phosphat aus Knochen • • • • • Über Calcitriol fördert es die intestinale Resorption Kann langfristig Ca2+-Haushalt nicht ausgleichen Geht auf Kosten der Knochen Stimuliert Umwandlung von Calcitriol in Niere schneller Ca2+ Hoch-Regulator!!!! !!!Keine Steuerung über HVL und Hypothalamus sondern direkte (konstitutive) Sekretion!!! Primärer Hyperparathyreoidismus • • • • • • • • Nebenschilddrüsenadenom Überproduktion von PTH Massiv erhöhte Ca2+-Konzentration Osteoporose Entmineralisierung der Knochen Kalkeinlagerung in Gefäßen & Niere Nierensteine „Stein-, Bein- und Magenpein“ Sekundärer Hyperparathyreoidismus (Vitamin D3- bzw. Kalziummangel) • PTH (1000fach erhöht!!!) • Meist durch chronisches Nierenversagen (kein Calcitriol – keine Hemmwirkung auf PTH) • Hyperphosphatämie – Phosphat kann nicht ausgeschieden werden (Löslichkeitsprodukt) • • • • • • Phosphat bindet Calcium - Hypokalzämie (freies Ca2+ ) Kompensatorische Hyperplasie der Parathyroidea Skelettveränderungen Kristallbildung in Gelenken (Gelenksschmerzen) Juckreiz durch Ca2+-Ablagerungen in der Haut Toxische Wirkung auf Herz & Muskulatur Pseudohypoparathyreoidismus „Martin-Albright-Syndrom“ • Hypoparathyreoidismus ohne Mangel an PTH • Genetischer Defekt des PTH-Rezeptors – Zielzellen können nicht auf PTH reagieren • Hypokalzämie & Hyperphosphatämie • Gestörter Knochenstoffwechsel – „paradoxe Verkalkungen“ • Augenlinsen • Basalganglien • Erhöhte neuromuskuläre Erregbarkeit • Muskelzuckungen • Krampfanfälle - Tetanie Calcium-Bestand 700 mg Aufnahme Knochen (als Apatit): 1300 g Parathormon Extrazellulär: 2 g Niere 200 mg 200 mg Plasma-Ca2+ = 2,5 mM (50% ionisiert) Intrazellulär: 5 g Calcitriol 500 mg (Stuhl) Calcitriol: Synthese Osteoporose 7-Dehydro-cholesterol (Leber) Hemmen Osteoklastenaktivität! Cholecalciferol = Vitamin D3 (Haut, UV) Nahrung, Supplemente Őstrogene 25(OH)-Cholecalciferol (Leber) 1α-Hydroxylase 1,25(OH)2-Cholecalciferol (= D-Hormon = Calcitriol) (Niere, prox. Tubulus) PTH Calcitriol • Darm: Stimulation der Calcium- und Phosphat-Resorption (stark altersabhängig) “enterale Calciumresorption“ • Niere: Stimulation der Calcium- und Phosphat-Reabsorption • Knochen: Aufbau von Knochenmatrix, Kochenmineralisierung • beständiger Ca2+-Auffüller in Knochen – Remineralisierung!!! • Mangel: – Rachitis (Kinder) – Osteomalazie (adulte Rachitis) – Osteoporose • Speicherung im Fettgewebe (½ Jahr) Calcium-Bestand 700 mg Aufnahme Knochen (als Apatit): 1300 g (Calcitonin) Extrazellulär: 2 g Niere Parathormon 200 mg Plasma-Ca2+ = 2,5 mM (50% ionisiert) Intrazellulär: 5 g 500 mg (Stuhl) 200 mg Calcitonin - Thyreocalcitonin (32 As) • • • • • • • • • Senkt freien Ca2+-Spiegel Aus C-Zellen der Thyreoidea, Thymus & Parathyreoidea Direkter Gegenspieler zum PTH am Knochen Erst seit ~50 Jahren bekannt, HWZ ~20 min. Verhindert postprandiale Hyperkalzämie Wichtig für Mineralisierung des fetalen & juvenilen Skeletts schneller Ca2+ Herunter-Regulator - Erhalt der Mineralisierung Eigentlich nur relevant bei Schwangerschaft & beim Stillen Relativ schwache Wirkung • Bedeutung für Ca2+ Homöostase beim Menschen gering (s. Thyreoidektomie) Klotho - „Anti-aging-Protein“ gr. Κλωθώ „Spinnerin“ des Lebensfadens • Produziert im distalen Tubulus, Parathyreoidea & Plexus choroideus • Hemmt die renale Ca2+-Ausscheidung • Hemmt Calcitriolsynthese • Reguliert die Ca2+-Aufnahme von Zellen (spez. Ca2+Kanal - TRPV5) • Mangel führt zu rapidem Altern – – – – – Verkalkungen - Arteriosklerose - Osteoporose Endotheliale Dysfunktionen Nierenversagen (GFR ) Muskel- & Hautatrophie kardiovaskuläre Komplikationen Blutdruckregulatorische Hormone • Kurzfristig (Sekunden) – Adrenalin • Umverteilung des HMV • Inotrop, chronotrop • Mittelfristig (Minuten) – ANP • Vasodilatation, erhöhte Permeabilität – Adrenomedullin • Vasodilatation, antagonistisch zum Sympathikus • Längerfristig ( ab ¼ Stunde) – Blutvolumenregulatorische Hormone • RAAS • ADH • ANP • Lokal wirksame Hormone Lokale Durchblutungsregulation – – – – – Mechanische Reizung (Druck, Verletzung) Temperatur Blutstillung Entzündungen Schubspannung • Gewebehormone aus: – Parenchym – Makrophagen – Endothel Vasodilatatorische Gewebshormone • erhöhen Permeabilität (lokale Ödeme – anaphylaktischer Schock) – Kinine • Bradykinin • Kallidin – Histamin – Adrenomedullin – Nukleotide • Adenosin, ADP, AMP – Konzentration von freien Ionen (metabolische Dilatation) • K+ & H+-Ionen • Gewebeosmolalität • Zunahme von PCO2 - Abnahme von PO2 – Stickoxid (EDRF) – Prostaglandine (Cyclooxygenasen – COX-1 & COX-2) • PGE2 • PGI2 (Prostacyclin) NO aus Nitroglycerin • Extrem kurzlebiges und reaktives Radikal (HWZ ~5 Sek.) • Abbauprodukt von L-Arginin (NOS) – iNOS, eNOS, nNOS • Stimuli: – Schubspannung (durchblutungsabhängige Vasodilatation) – Gewebshormone • • • • • Erschlaffung der glatten Muskulatur (cGMP) kontrolliert Blutfluss und reguliert so Blutdruck (Viagra) Potenter Vasodilatator in der Lunge (Hypoxie) hemmt Blutgerinnung & verhindert Thrombosen wirkt als Neurotransmitter (nicht in Vesikeln gespeichert) – Lernen, Gedächtnis & Geruchsempfinden • antimikrobielle Wirkungen (Nitritsalze NO2-) • Hohe Affinität für Hb (Blue-Baby - Syndrom) Cyclooxygenasen COX-1 & COX-2 • COX-1: – – – – – Bildung von PGE2, Thromboxan A2 & Prostazyklin gastrointestinale Schleimhautprotektion Nierenfunktion Thrombozytenaggregation Hemmung führt zu Appetitlosigkeit, Übelkeit, Erbrechen, Nierenschäden • COX-2: – Durch Entzündungsprozesse aktiviert – Bildung von inflammatorischen Prostaglandinen Schmerz Fieber (Sollwert im Hypothalamus wird verstellt) Rötung (Vasodilatation) • NSAID´s (z.B. Aspirin) – non steroidal anti–inflammatory drugs (antientzündliche Medikamente) – Hemmen COX-1 & COX-2 Vasokonstriktorische Gewebshormone • Prostaglandine der F-Gruppe – PGF2a – Thromboxane (TXA2 & TXB2) • Serotonin (Lunge, Niere) – wird in Melatonin umgewandelt (Schlaf-Wach-Rhythmus) • Angiotensin II (verstärkt auch Sympathikus) • Endotheline (stärkste Vasokonstriktoren) – ET-1, ET-2, ET-3 – Gefahr von (zerebralen) Vasospasmen – ECE aktiviert das „Big-ET-1“ Erythropoetin • Glykoprotein • Bildungsort: Peritubuläre Zellen der Niere, (Leber) • Messung des O2 Partialdruckes in der Niere durch Häm-enthaltendes Protein Wirkung von Erythropoetin • Retikulozyten werden früher ins Blut abgegeben • Generationszeit und DNA Synthesezeit werden reduziert • Erythrozyten erhöhen Hämsynthese • Wirkung auf Reservepool