Kernwaffen - Eine Einführung
Werbung

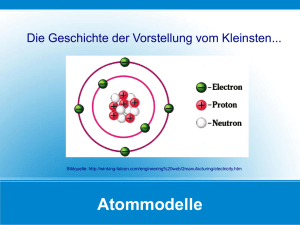
Kernwaffen - Eine Einführung S. E. Erickson Kernwaffen – Eine Einführung © Stefan E. Erickson Erste Auflage: Dezember 2015 ISBN: 978-3-7375-9102-7 2 Es gibt sie erst seit Mitte des letzten Jahrhunderts, doch gelten sie seither als das ultimative Mittel totaler Vernichtung: Kernwaffen. Seit ihrer Erfindung sind Kernwaffen mit einer Brisanz behaftet, die aufgrund ihres Bedrohungspotenzials, ganze Staaten und Zivilisationen in kürzester Zeit auslöschen zu können, stets aktuell ist. Der Besitz von Kernwaffen verspricht enorme politische und moralische Verantwortung und kann weitreichenden Einfluss in der Weltpolitik verleihen. Das Prinzip der nuklearen Abschreckung ist nach wie vor ein fundamentaler Bestandteil der Beziehungen zwischen vielen Staaten. Solange die Menschheit dazu bereit ist Kriege gegeneinander zu führen, stellen Kernwaffen zu einem bestimmten Grad eine Rückversicherung gegen einen militärischen Konflikt dar. Während die Abrüstung von Kernwaffen unter diesem Gesichtspunkt nicht absehbar ist, zieht allein deren Existenz stets die Gefahr ihres tatsächlichen Einsatzes mit sich. Gewinnen Sie in diesem Buch einen Einblick in wissenschaftliche und technische Aspekte, die es überhaupt ermöglichen, Kernenergie nutzbar zu machen. Lernen Sie grundlegende Konzepte der Kernwaffentechnik sowie Nuklearstrategien kennen. Erfahren Sie unter anderem wie Kernwaffen funktionieren, welche strategischen Optionen sie mit sich bringen, wie sich Nuklearexplosionen auswirken und welchen Einfluss diese Waffen auf historische Ereignisse ausübten. © S. E. Erickson, Dezember 2015 3 INHALTSVERZEICHNIS Teil I - Die Wissenschaft hinter Kernwaffen 6 9 19 25 33 37 - Atome - Die vier Grundkräfte der Physik, Materie und Energie - Kernkräfte und Massendefekt - Kernzerfall und Radioaktivität - Nukleare Fission (Kernspaltung) - Kernfusion (Verschmelzung von Kernen) Teil II - Kernwaffentechnik 41 42 46 50 - Explosionen - Kernwaffendesign - Mehrstufige Kernwaffen - Zivile Nutzung Teil III - Globale Thermonukleare Kriegsführung 54 54 59 64 67 74 - Kernwaffen als Machtinstrument - Staaten im Besitz von Kernwaffen - Trägersysteme von Nuklearsprengköpfen - Arten von Sprengköpfen - Abwehrsysteme gegen nukleare Angriffswaffen - Nuklearstrategien Teil IV - Folgen eines nuklearen Schlagabtauschs 87 94 100 - Auswirkungen einer Nuklearexplosion - Biologische Schäden durch ionisierende Strahlung - Weltweite Auswirkungen Teil V - Historisches 103 103 106 116 122 130 135 - Wissenschaftliche Erkenntnisse - Wettforschen während des zweiten Weltkrieges (1939 - 1945) - Die Kapitulation Japans - Die Anfänge des Kalten Krieges - Die Kubakrise - Der Kalte Krieg in vollem Gange - Das Ende des Kalten Krieges 138 149 Appendix Quellenverzeichnis 4 Teil I – Die Wissenschaft hinter Kernwaffen "Das Ganze ist mehr als die Summe seiner Teile." – Aristoteles 5 Atome Wenn Sie sich umsehen, werden Sie feststellen, dass wir von zahllosen, verschiedenen Stoffen und Substanzen umgeben sind; von Metallen und Kunststoffen zu Menschen und Pflanzen und sogar der Luft, die Sie atmen. Alle diese Substanzen bestehen aus einer Auswahl von rund einhundert verschiedenen Arten von Bausteinen, welche miteinander verbunden sind. Diese Bausteine sind winzige Partikel, die man Atome nennt. Atome sind so klein, dass selbst ein kaum sichtbares Staubkorn aus mehr als einer Million mal einer Million Atomen besteht. Das sind mehr als 1.000.000.000.000, also eine Billion bzw. eintausend Milliarden Atome in einem einzigen Staubkorn. Manche Stoffe, wie Eisen oder Gold, bestehen aus nur einer einzigen von rund einhundert in der Natur vorkommenden verschiedenen Atomsorten. Andere Substanzen, wie Wasser oder Holz, sind eine Verbindung aus zwei oder mehreren, verschiedenen Atomarten und werden als Moleküle bezeichnet. Moleküle können sehr komplex sein und aus Dutzenden, Hunderten und Tausenden Atomen bestehen, wie es bei verschiedenen Kunststoffen, organischem Gewebe oder Nanopartikeln der Fall ist. Wasser hingegen ist ein sehr simples Molekül, welches lediglich aus drei Atomen besteht: z ei Wasserstoffato e H droge u d ei e Sauerstoffato O ge ; H₂O. Alle Stoffe, it denen der Mensch unerlässlich in Berührung kommt, bestehen aus einer Anordnung von zahllosen Molekülen, welche sich wiederum aus den noch kleineren Atomen zusammensetzen. Aufbau eines Atoms So winzig die Atome bereits sein mögen, bestehen diese aus noch viel kleineren, subatomaren Teilchen. Ein Atom ist durch einen dichtbepackten Kern aus positiv geladenen Protonen und elektrisch neutralen Neutronen aufgebaut, um welchen negativ geladene Elektronen mit hoher Geschwindigkeit herumschwirren. Die negativ geladenen Elektronen sind durch ihre elektrische Ladung, der elektrostatischen Anziehung, an die positiv geladenen Protonen im Atomkern gebunden. Proton (positive Ladung) Atomkern (Nukleus) Neutron (keine Ladung) Elektron (negative Ladung) } Aufbau eines gewöhnlichen Heliumatoms Wiegt man die Ladungen der Protonen (+1), Neutronen (0) und Elektronen (-1) gegeneinander auf, erhält man als Ergebnis Null, was elektrischer Neutralität entspricht. Atome sind in ihrem Grundzustand immer elektrisch neutral, da sie immer die gleiche Anzahl an positiv geladenen Protonen und negativ geladenen Elektronen haben. Kommt es dazu, dass durch eine Reaktion ein Elektron fehlt oder sich eines zu viel in der Hülle befindet, bezeichnet man dieses elektrisch nicht neutrale und daher chemisch sehr reaktionsfreudige Atom als Ion. Die Neutronen, die keine elektrische Ladung haben, wirken sich auf die elektrischen bzw. chemischen Eigenschaften nicht aus, wohl aber auf die nuklearen Eigenschaften. 6 Elektron Ein Elektron hat eine rund 1845 Mal kleinere Masse als ein Proton, ist jedoch trotz dieses Masseunterschieds mit der gleichstarken, entgegengesetzten Ladung von minus Eins behaftet. Sein Orbit findet in einer Elektronenschale mit einer bestimmten Entfernung zum Kern statt. Nur wenige Elektronen können sich zusammen in ein und demselben Abstand zum Kern aufhalten, weshalb ein Atom mit vielen Elektronen sich wie die Schale einer Zwiebel aufbaut. Dabei ist der Begriff "Elektronenschale" irreführend. Die Schalen existieren in Wirklichkeit nicht in Form einer soliden, kugelförmigen Wand, sondern bezeichnen vielmehr ein Energieniveau, auf welchem sich das Elektron fortbewegt. Je nach Anzahl und Konfiguration der in den äußeren Elektronenschalen befindlichen Elektronen, können sich zwei oder mehr Atome diese äußeren Elektronen teilen, was einer chemischen Verbindung entspricht. Atome, denen als Folge verschiedener Reaktionen Elektronen entrissen werden, sind elektrisch nicht mehr neutral und suchen sich eine chemische Verbindung oder ein anderes freies Elektron, um wieder zu elektrischer Neutralität zurückzukehren. Elektronen sind die kleinsten Teilchen ihrer Art, die, anders als Protonen und Neutronen, nicht aus noch kleineren Teilchen bestehen. Proton Das Proton ist ein positiv geladenes Teilchen im Atomkern. Die Anzahl der Protonen im Kern ist zugleich die Kernladungszahl, d.h. die Anzahl geladener Teilchen im Kern und bestimmt das Element des Atoms, ob es sich um Wasserstoff, Helium, Kohlenstoff, Eisen oder eines der anderen rund einhundert Elemente handelt. Die positive Ladung der Protonen sorgt für eine Anziehung zwischen Protonen und Elektronen, wodurch das Atom zusammengehalten wird. Neutron Das Neutron trägt keine elektrische Ladung. Seine Zahl im Atomkern kann bei jedem der Elemente variieren, ohne sich dabei auf die Kernladungszahl auszuwirken. Ein Element kann mit einer unterschiedlichen Anzahl an Neutronen im Kern vorkommen. So gibt es beispielsweise verschiedene Arten von Helium, die im Kern neben die für Helium spezifischen zwei Protonen ein bis acht Neutronen aufweisen. Elemente mit abweichender Neutronenzahl nennt man Isotope oder Nuklide. Atomkern (Nukleus) Über 99,95 % der Masse und damit auch des Energiepotentials eines Atoms macht der Kern aus, obwohl dieser weniger ein Hundertstel der Größe eines Atoms ausmacht. Die Elektronen, die um den Kern sausen, sind für chemische Prozesse zwischen mehreren Atomen verantwortlich, spielen jedoch bei Nuklearvorgängen kaum eine Rolle. Obwohl die freigesetzten Kräfte durch chemische Reaktionen, d.h. Wechselwirkungen der Elektronen in der Elektronenhülle, immens sein können, werden sie von den Kräften im Atomkern weit übertroffen. Änderungen innerhalb des Atomkerns können das gesamte Element verändern, und zur Umwandlung von Masse in gewaltige Energiemengen führen. Nukleon Ein Nukleon ist ein Teilchen, welches Teil des Nukleus ist. Nur Protonen und Neutronen werden als Nukleonen bezeichnet. Nukleonen sind nicht die kleinsten Teilchen ihrer Art, sondern bestehen aus noch viel kleineren Teilchen. Wie die Elektronenschale, haben Protonen und Neutronen keine feste Hülle um sich herum, sondern generieren Abstände durch ihre Ladungen Allgemein macht jegliche Materie leerer Raum aus, der lediglich durch Ladungen voneinander abgetrennt wird. 7 Elemente / Periodensystem Mit den Elementen sind nicht die klassischen Elemente Wasser, Feuer, Luft und Erde gemeint, sondern Elemente im Sinne des Periodensystems. Jedes Element wird durch seine Anzahl an Protonen im Kern, bzw. der Kernladungszahl bestimmt. Die Kernladungszahl bezeichnet die Anzahl der geladenen Teilchen im Kern eines Atoms, also Protonen. Beginnend mit dem kleinsten Element, dem Wasserstoff mit nur einem einzigen Proton als Atomkern, gibt es in der Natur noch weitere 91 vorkommende Elemente, die bis zum schwersten Element Uran mit 92 Protonen und über 140 Neutronen reichen. Darüber hinaus gibt es über zwei Dutzend weiterer Elemente, die künstlich erzeugt werden können. Isotope/Isobare/Nuklide, Massen- und Kernladungszahl Element ist nicht immer gleich Element, da die Anzahl der Neutronen im Kern variieren kann. Isotope bzw. Nuklide sind verschiedene Arten ein und desselben Elements. Die Begriffe "Isotop" und "Nuklid" bezeichnen jeweils ein Element mit einer unterschiedlichen Anzahl an Neutronen, jedoch fokussiert sich der Begriff "Isotop" auf ein bestimmtes Element einschließlich seiner chemischen Eigenschaften, wohingegen der Begriff "Nuklid" die Beschaffenheit des Atomkerns betont. Die Anzahl an Protonen in einem Isotop ist immer gleich, allerdings kann die Anzahl der Neutronen im Atomkern unterschiedlich sein, was physikalische Auswirkungen auf die Dichte oder die Stabilität des Kerns sowie dessen Zerfall haben kann. Isobare hingegen haben die gleiche Anzahl an Neutronen mit unterschiedlich vielen Protonen. In der Nuklidkarte (Seite 138 - 146) stehen Isotope horizontal nebeneinander, Isotone vertikal. Die Massenzahl bezeichnet die Summe aller Protonen und Neutronen eines Atomkerns. Aufgrund der variierenden Neutronenzahl kann die Massenzahl eines Elementes schwanken. Die Kernladungszahl bezeichnet die Anzahl aller geladenen Teilchen in einem Atomkern, d.h. alle Protonen. Die ausgeschriebene Form zur Identifizierung eines individuellen Nuklids sieht folgendermaßen aus: X bezeichnet das Element, A die Massenzahl (Protonen + Neutronen) und Z die Kernladungszahl (nur Protonen). Beispiel der ausgeschriebenen Form: Das Element Uran, abgekürzt durch das chemische Symbol U, hat eine Kernladungszahl von 92. Es befinden sich also 92 Protonen im Kern. Anhand der Massenzahl 235, die für die Gesamtzahl an Nukleonen steht, lässt sich die Zahl der Neutronen errechnen. 235 Nukleonen – 92 Protonen = 143 Neutronen. Oftmals wird die Kernladungszahl ausgelassen, da die Protonen ohnehin dem Element entsprechen, wofür das chemische Symbol steht: oder vereinfacht U-235. Uran ist ein sehr wichtiges, schweres Element zur Herbeiführung nuklearer Reaktionen und hat eine ganze Reihe an Isotopen: . Diese Nuklide haben entsprechend der vorangegangenen Aufzählung 140, 141, 142, 143, 144, 145, 146 und 147 Neutronen im Kern. 8 Mit steigender Massenzahl der Elemente, erhöht sich das Missverhältnis zwischen Protonen und Neutronen. Während die stabilen Elemente bis Chlor-35in ihrem Nukleus ein etwa gleiches Verhältnis aus Protonen wie Neutronen aufweisen, steigt die Anzahl der Neutronen im Vergleich zu Protonen der im Periodensystem folgenden Elemente deutlich an. Die Neutronen helfen dabei, die Protonen im Kern zusammenzuhalten. Wegen ihrer gleichen elektrischen Ladung würden sich Protonen untereinander stärker abstoßen, wenn keine Neutronen präsent wären. Alle Elemente außer Wasserstoff, der nur aus einem Proton besteht, würden auseinanderbrechen, wenn es in ihren Atomkernen keine Neutronen als Puffer gäbe. Die vier Grundkräfte der Physik, Materie und Energie Während Materie alles beschreibt, was Raum einnimmt und daher aus winzigen Atomen bzw. deren subatomaren Teilchen besteht, die sich auf vielfältige Weise miteinander verbinden können und so verschiedenste Stoffe bilden, ist eine physikalische Kraft eine Art von Energie, die Materie umfasst, sie dazu veranlasst in Bewegung zu geraten, sich zu verändern oder zu reagieren. Materie kann in Energie übergehen und umgekehrt Energie in Materie. Nimmt man Materie bis hin zu ihren kleinsten Bausteinen, den subatomaren Partikeln, auseinander, stellt man fest, dass diese kleinen, nicht weiter unterteilbaren Elementarteilchen die eigentliche Materie ausmachen. Jedoch fängt Materie bei diesen winzigen Maßstäben an, mit physikalischen Kräften zu verschwimmen, welche jegliche Strukturen zusammenhalten und deren Existenz überhaupt ermöglichen. So ziehen sich beispielsweise das positiv geladene Proton und das negativ geladene Elektron an. Diese Anziehungskraft hält die beiden Teilchen in einander Nähe. Doch was mach diese Anziehungskraft tatsächlich aus; woher weiß das Elektron, dass sich ein Proton in seiner Nähe befindet, zu welchem es angezogen wird, während dies bei einem Neutron nicht der Fall ist? Die Antwort auf diese Frage ist, dass das Proton und Elektron den Raum um sich herum mit zahllosen kleinsten Partikeln erfüllen, die nur sehr flüchtig existieren. Da es elektrisch neutral ist, sendet ein Neutron keine solche Partikel aus. Diese sogenannten virtuellen Teilchen werden von ihrem jeweiligen Elternteilchen blitzschnell ausgesandt und fungieren als Austauschteilchen bzw. Vermittler physikaElektron Proton lischer Kräfte. Elementarteilchen sind mit ihren vielen virtuellen Partikeln pulsierende Körper, die Felder um sich herum generieren. Geraten die virtuellen Partikel eines Elementarteilchens mit denen eines anderen Elementarteilchens aneinander, können diese Die Felder aus virtuellen Teilchen (ge- sich untereinander verflechten, austaupunktete Linien) bewirken Anziehung schen oder abstoßen. Das Elementaroder Abstoßung teilchen erfährt diese Wechselwirkung als physikalische Kraft. Die Physik unterscheidet vier fundamentale Kräfte, die Gravitation, die elektromagnetische Kraft, sowie die starke und die schwache Kernkraft, wovon jeder einzelnen ihr charakteristisches, virtuelles Austauschteilchen zugrunde liegt. Je mehr Energie und Masse diese Austauschteilchen haben, umso geringer ist die Zeitspanne, in der sie existieren können. Die Reichweite einer 9 Kraft ist daher von der Masse ihres Austauschteilchens abhängig. Manche dieser Teilchen sind masselos und in ihrer Reichweite unbegrenzt. Die vier Grundkräfte der Physik funktionieren allesamt durch den Austauschmechanismus von virtuellen Teilchen. Neben vielen Elementarteilchen, aus denen alles besteht, was wir kennen und wahrnehmen, existieren auch Antiteilchen mit gleicher Masse, aber entgegengesetzter elektrischer Ladung oder einer anderen entgegengesetzten Eigenschaft. Beispielsweise ist das entsprechende Antiteilchen des elektrisch negativen Elektrons das Positron mit positiver Ladung. Treffen Elektron und Positron aufeinander, annihilieren sie sich, d.h. zerstrahlen zu elektromagnetischer Strahlung. Bei Aufeinandertreffen von anderen Partikeln mit deren Antiteilchen, zersplittern die Teilchen in kleinere Teilchen. Gravitation Die Gravitationskraft, hält uns nicht nur auf dem Boden, sondern erklärt auch wie Planeten, Sterne und Galaxien sich bewegen. Dank der Gravitation ist die Entstehung und Existenz ganzer Galaxien, Sonnen und Planeten möglich. Die Gravitation, die wir Menschen alltäglich erfahren, ist die Erdanziehungskraft, die Gravitation zwischen Mond und Erde, die für Ebbe und Flut verantwortlich ist, sowie der Lauf der Erde um die Sonne, der die Jahreszeiten ausmacht und sich in perfektem Abstand vollzieht, sodass die Bedingungen Leben auf unserem Planeten ermöglichen. Auch wenn wir die Gravitationskraft jederzeit als Erdanziehungskraft wahrnehmen, ist sie weitaus komplexer als einen Stein zu Boden fallen zu lassen. Alles im Universum, was Masse hat, von den kleinsten Partikeln bis hin zu Galaxien, zieht einander an. Diese Anziehungskraft zwischen jeglicher Masse ist die Gravitationskraft. Die Stärke der Gravitationskraft ist abhängig von der Masse der Objekte und deren Entfernung zueinander. Je mehr Masse ein Objekt hat, desto mehr Anziehungs- bzw. Gravitationskraft übt es auf ein anderes Objekt aus. Die Gravitationskraft sinkt jedoch stark ab, je weiter die Objekte voneinander entfernt sind. Allerdings ist die Gravitation nicht nur eine Eigenschaft von Masse, sondern auch von Raum und Zeit. Gemäß Albert Einstein sind Raum und Zeit das, woraus das Universum besteht, und seine allgemeine Relativitätstheorie besagt, dass Objekte mit Masse oder Energie das Gefüge aus Raum und Zeit verzerren. Anhand der Raumzeit wird deutlich, wie sehr die Gravitation und die elektromagnetische Kraft miteinander verknüpft sind. Doch was genau ist die Raumzeit, wie können zwei so scheinbar unterschiedliche Maße wie Raum und Zeit miteinander verbunden sein und was hat Gravitation mit der elektromagnetischen Kraft zu tun? Blickt man in den Nachthimmel, sieht man Sterne, die teils Millionen von Lichtjahren entfernt sind. [Erläuterung: Ein Lichtjahr entspricht der Entfernung, die Licht in einem Jahr zurücklegt. Elektromagnetische Strahlung, wie Licht, breitet sich mit einer Geschwindigkeit von 299.792,458 km/Sek im Vakuum aus und legt in Zahlen ausgedrückt pro Jahr (365,25 Tage)9.460.730.472.580,800 km zurück = 1 Lichtjahr.] Es braucht Zeit, bis das Licht der Sterne bei uns auf der Erde ankommt, weshalb wir die Sterne nicht in ihrem aktuellen Zustand sehen, sondern wie zu jener Zeit, als ihr Licht sich auf die Reise Richtung Erde machte. Je weiter ein Stern entfernt ist, desto weiter blickt man bei seinem Anblick in die Vergangenheit zurück, nämlich so weit wie es braucht, bis uns sein Licht erreicht. Stellt man sich einen Stern in 2.000 Lichtjahren Entfernung vor, auf welchem Menschen leben, sähen wir diese, wie sie vor 2.000 Jahren lebten. Umgekehrt sähen diese Menschen auch uns, wie wir vor 2.000 Jahren lebten. Die Gegenwart lässt sich für die Erde, den entfernten Stern und das Licht nicht einheitlich definieren. Raum und Zeit sind also miteinander verknüpft: je weiter man durch den Raum sieht, umso weiter blickt man in die Zeit zurück. Gravitation verzerrt jedoch das Gefüge aus Raum und Zeit. 10 Abbildung links: Die Raumzeit zweidimensional dargestellt. Abbildung rechts: Massereiche Objekte verzerren die Raumzeit und ziehen andere Objekte (rot) an. Die Gravitation ist neben der Eigenschaft von Objekten mit Masse auch eine Eigenschaft von masseloser Energie, wie z.B. Licht. Demnach sind Masse und Energie zwei unterschiedliche Arten von ein und derselben Sache und wirken sich aufeinander aus. Besonders Massereiche Objekte, wie die Sonne, üben eine solch starke Gravitation aus, dass sie das Licht, um sich herum biegen. Beispiel: Die direkte Sicht auf einige Sterne wird durch die Sonne versperrt. Durch die enorme Masse der Sonne wird das Licht der Sterne gebogen wenn es in die Nähe ihres Gravitationsfeldes gerät. Dadurch bleiben die Sterne sichtbar, obwohl sie sich tatsächlich hinter der Sonne befinden. Licht durchstreift das Gravitationsfeld Sterne hinter der Sonne Sonne Erde Ein Objekt mit genügend kompakter Masse kann so gravitationsstark werden und die Raumzeit so stark verformen, dass nicht einmal Licht die extreme Gravitationskraft überwinden kann und in ihr gefangen bleibt. Diese extrem massereichen Objekte, sogenannte schwarze Löcher, können die millionen- bis milliardenfache Masse der Sonne haben. Für jede der physikalischen Grundkräfte gibt es ein Teilchen, welches als Austauschteilchen fungiert und eine bestimmte Kraft zwischen Materie vermittelt. Für die Gravitationskraft übernimmt diese Aufgabe das sogenannte Graviton. Wenn selbst masselose Energie bzw. Licht auf Gravitation reagiert, muss das Graviton noch deutlich kleiner als alle anderen virtuellen Teilchen sein und wird wie auch Licht als masseloser Partikel beschrieben. Allerdings wurden Gravitonen im Gegensatz zu den Austauschteilchen der anderen drei Grundkräfte der Physik noch nie entdeckt, gelten als nicht nachweisbar und existieren nur in der Theorie. Elektromagentische Kraft Wie der Name schon verrät, tritt die elektromagnetische Kraft in zwei Formen auf, die auf den ersten Blick völlig unterschiedlich zu sein scheinen, nämlich in Elektrizität und Magnetismus. Darüber hinaus ist die elektromagnetische Kraft auch verantwortlich für viele grundlegende physikalische Erscheinungen, denen wir tagtäglich begegnen. Dazu zählen unter anderem jegliche Arten elektromagneti11 scher Strahlung wie Wärme oder Licht. Alles was wir sehen ist eine Information, die durch elektromagnetische Strahlung übertragen wird. Sie ist aber auch für alle chemischen Prozesse verantwortlich, tritt in diversen Erscheinungsformen auf und wird im allgemeinen Sprachgebrauch als Energie bezeichnet. Der elektromagnetischen Wechselwirkung ist es zu verdanken, dass Strom fließen kann, geladene Teilchen von Molekülen bis hin zu Protonen und Elektronen einander anziehen oder abstoßen und die Atome nicht in ihre einzelnen subatomaren Partikel auseinanderfliegen. Das Austauschteilchen für die elektromagnetische Kraft ist das Photon, welches sich als Träger elektromagnetischer Wellen mit Lichtgeschwindigkeit fortbewegt (299.792,458 km/Sek), als masselos gilt und daher in seiner Reichweite unbegrenzt ist. Photonen können sowohl die Eigenschaften von Partikeln als auch Wellen haben und sich in ihrer Stärke erheblich unterscheiden. Hierzu gehören alle Arten von elektromagnetischer Strahlung, die sich anhand ihrer Frequenzen und Wellenlängen charakterisieren lassen. Das elektromagnetische Wellenspektrum reicht von theoretisch von unendlich langen Wellen zu unendlich kurzen Wellen. Dabei gilt: Je kürzer die Welle ist, desto energetischer ist sie auch. Als Indikator für die Energiemenge ist die Temperaturskala der folgenden Abbildung heranzuziehen. Ultraviolette Strahlen 0,000 000 01 Meter Gammastrahlen 0,000 000 000 000 1 Meter Infrarotstrahlen (Wärme) 0,000 05 Meter Radiowellen 100 Kilometer bis 0,3 Meter Sichtbares Licht 0,000 000 5 Meter Mikrowellen 0,3 Meter bis 0,001 Meter Röntgenstrahlen 0,000 000 000 01 Meter Äquivalente Temperatur von Materie, dieStrahlung mit einer bestimmten Wellenlänge emittiert 1°C 100°C 10.000°C 10.000.000°C Elektromagnetische Strahlung entsteht, wenn ein Elektron in einem Atom Energie verliert und auf ein tieferes Energieniveau fällt. Dies setzt eine Schwingung elektrischer Energie frei, die sich in Form eines Photons sowie elektrischer und magnetischer Felder durch den Raum ausbreitet. Wenn das Photon bzw. die elektromagnetische Welle auf ein anderes Atom trifft, kann dort ein Elektron die Energie gewinnen und auf ein höheres Energieniveau springen, bis es wie das Elektron im vorhergehenden Atom wieder zurückfällt und einen Teil der Energie abgibt. Auf diese Weise transportiert eine elektromagnetische Welle Energie. Da der Maßstab für die Energieniveaus, auf welche die Elektronen springen, so klein ist, gehen sie nicht fließend ineinander über, sondern verlaufen sprunghaft in den sogenannten Quanten. Eine einzelne Stufe Energie, ein Quantum, entspricht dabei immer dem geringstmöglichen Energiebetrag. Der Bruchteil eines Quantums ist nicht möglich. Die Weitergabe von Energie erfolgt daher in winzigen, schnell aufeinanderfolgenden Portionen. 12 Elektronen springen auf höhere Energieniveaus, wenn sie Energie (Photonen) aufnehmen(Abb. links) und geben die Energie wieder in Form von Photonenemissionen ab, wenn sie wieder auf ein tieferes Energieniveau fallen (Abb. rechts). Je nach Intensität der erhaltenen Energie, werden Photonen mit entsprechender Wellenlänge freigesetzt. Jeder Körper sendet elektromagnetische Strahlung aus, wenn seine Temperatur oberhalb des absoluten Nullpunktes von minus 273,15 Grad Celsius liegt, egal ob es sich dabei um Metalle, Kunststoffe, Luft, organisches Gewebe oder jeglichen anderen Stoff handelt. In diesem Zusammenhang bedeutet Wärme (thermische Strahlung bzw. Infrarotstrahlung), dass sich die Atome mitsamt ihren Ladungsträgern in Bewegung befinden, was zur Folge hat, dass elektromagnetische Strahlung frei wird. Welche Intensität und Wellenlänge die elektromagnetische Strahlung hat, hängt von der Energiemenge ab, der ein Atom ausgesetzt wird. Erhitztes Eisen veranschaulicht die Abgabe von Energie sehr gut. Je höher die Temperatur von Eisen ist, desto kürzer ist die Wellenlänge der ausgesendeten thermischen Strahlung. Mit steigender Temperatur strahlt das Eisen zunächst Strahlung ab, die für das menschliche Auge zwar nicht sichtbar ist, jedoch über die Haut durchaus wahrgenommen wird. Bis etwa 400°C liegt diese Strahlung im Infrarotbereich. Wird das Eisen über diese Temperatur weiter erhitzt, verkürzt sich auch weiterhin die Wellenlänge und verschiebt sich in den sichtbaren Bereich, mit der Folge, dass die Strahlung als Licht wahrgenommen wird. Das Eisen beginnt zu glühen, zuerst dunkelrot, orange, gelb, bis hin zu gleißendem weiß. Elektromagnetische Strahlung kann nicht nur durch Quantensprünge der Elektronen freigesetzt werden, sondern auch durch Reaktionen im Atomkern hervorgerufen werden. Die bei Kernreaktionen freiwerdende elektromagnetische Strahlung ist die sehr kurzwellige Gammastrahlung, welche so energetisch ist, dass sie bei Interaktion mit einem Atom, dessen Elektronen aus seinem Orbit herausschlagen kann. Starke Kernkraft Die starke Kernkraft hält die Atomkerne zusammen und sorgt dafür, dass die im Nukleus befindlichen Neutronen und Protonen trotz ihrer gleichen positiven Ladung nicht auseinanderfliegen. Wohingegen sich Elektronen nicht in kleinere Teilchen aufteilen lassen, bestehen Protonen und Neutronen aus jeweils drei kleineren Partikeln, den sogenannten Quarks. Diese nicht weiter unterteilbaren Teilchen, auch Elementarteilchen genannt, sind ein fundamentaler Bestandteil der Materie. Jedes einzelne Quarkteilche i ei e Nukleo trägt e t eder ei e elektris he Ladu g o plus ⅔ Up-Quark) 13 oder i us ⅓ Do -Quark). Entsprechend ihrer elektrischen Eigenschaften gilt für die Bestimmung eines Protons oder Neutrons die Quarkkonfiguration. Zwei Up-Quarks +⅔ u d ei Down-Quark (-⅓ ergeben in ihrer Summe eine Ladung von plus Eins, was das Nukleon als Proton definiert. Im Gegenzug gleichen sich die Ladungen zweier Down-Quarks (-⅓ u d ei es Up-Quarks +⅔ aus, as si h als elektrisch neutrales Neutron auszeichnet. -⅓ +⅔ -⅓ +⅔ Ein Neutron hat zwei Down-Quarks und ein Up-Quark. Beim Proton ist es genau umgekehrt, weshalb es positiv ist. +⅔ -⅓ Neutron Proton Neben dieser elektrischen Eigenschaft tragen Quarks auch eine Farbladung, welche Teil der starken Kernkraft ist. Mit der Farbladung wird der Quantenzustand eines Quarks beschrieben und hat mit der Farbe des alltäglichen Sprachgebrauchs nichts zu tun. Diese Quantenzustände der Quarks unterteilen sich in die drei Farbladungen Rot, Blau und Grün. Darüber hinaus gibt es Antiquarks mit den entsprechenden Antifarbladungen, die jedoch kein Bestandteil von Nukleonen sind, jedoch eine wichtige Rolle im Austausch der starken Kernkraft spielen. Alle Protonen und Neutronen sind gemäß der Farbladung neutral bzw. farblos (weiß), weshalb die Farbladungen der drei Quarks sich gegenseitig stets aufheben. Da jedes Proton und Neutron aus drei Quarks besteht, trägt jedes einzelne dieser drei Quarks immer eine andere Farbladung als die anderen beiden Quarks. Schematische Darstellung von Quarks mit den Farbladungen Rot, Blau und Grün, den zwischen ihnen wechselnden Gluonen mit Farbe und Antifarbe, sowie der neutralen Summe alle Farbladungen (weiß). Quarks ändern ständig ihre Farbladung untereinander. Der Vorgang, der ihnen zu diese Änderung ermöglicht, ist auch dafür verantwortlich, weshalb die Quarks auf engem Raum zusammengehalten werden: Die Wechselwirkung durch das Austauschteilchen der starken Kernkraft, des Gluons. Das Gluon ist masselos, trägt keine elektrische Ladung, aber es trägt Farbladungen und existiert nur als virtuelles Teilchen, wenn zwei Quarks miteinander interagieren. Es gibt verschiedene Arten von Gluonen, die je eine andere Kombination aus einer Farbladung und beliebigen Antifarbladung tragen. Während des Austausches von Gluonen zwischen den Quarks, ändern die Gluonen die Farbladungen der Quarkteilchen, die sie verlassen und bei denen sie ankommen. Gleichzeitig sorgt der Austausch von Gluonen zwischen den Quarkteilchen, dass diese eng miteinander verbunden bleiben. Da Gluonen nämlich ihre eigene Farbladungen haben, sind sie nicht nur bloße Austauschteilchen, die eine Kraft vermitteln, sondern nehmen an der starken Wechselwirkung teil und generieren sekundä14 re virtuelle Gluonen um sich, welche wiederum weitere virtuelle Gluonen um sich generieren können. Dieser Prozess kann sich endlos wiederholen, d.h. zwischen den Quarkteilchen findet regelrecht ein Sturm an Gluonen statt. Je weiter sich die Quarkteilchen voneinander entfernen, umso mehr Gluonen generieren sich selbst und umso stärker wird die Kraft, die die Quarks aneinander bindet. Die Quarks sind durch die Gluonen wie ein Gummiband miteinander verbunden. Die Bezeichnung "starke Kernkraft" verrät bereits, dass diese Kraft enorm stark sein muss. In den Atomkernen drängt sich die Frage auf, weshalb die Nukleonen im Kern so eng zusammengehalten werden. Die gleiche elektrische Ladung der dicht beieinander liegenden Protonen sollte eigentlich dafür sorgen, dass sich die Nukleonen voneinander abstoßen und es den Kern in seiner dicht bepackten Form nicht geben kann. Diese Folgerung ist korrekt, jedoch wird die starke Kernkraft ihrem Namen gerecht, indem sie die elektrischen Abstoßungskräfte unter den Protonen bei weitem übertrifft und dafür sorgt, dass der Atomkern zusammenhält. Spaltet man den Atomkern, dann wird genau diese immense Kraft frei. Auf sehr kurzen Distanzen wirkt die Kernkraft abstoßend, weshalb Protonen und Neutronen einen gewissen Abstand zueinander halten und sich nicht ineinander verheddern. Gleichzeitig übt sie bei geringfügig größeren Entfernungen, die sich auf den gesamten Nukleus bezieht, die oben beschriebene starke Anziehung aus. Die Nukleonen werden daher von der gleichen Kraft gleichzeitig voneinander abgetrennt und auf engstem Raum gehalten. Hierbei nimmt die Farbladung wieder eine tragende Rolle ein, welche Quarks innerhalb von Protonen und Neutronen verbindet. Nicht nur Kräfte innerhalb der Nukleonen werden ausgetauscht, sondern auch zwischen den Protonen und Nukleonen untereinander. Diese Kraft wird über Pionen vermittelt, die virtuell aus der starken Kernkraft erschafft werden, ein Vorgang bei welchem aus wechselwirkenden Kräften Materie und Antimaterie gebildet wird. Pionen bestehen aus einem normalen Quarkteilchen und dessen Antiteilchen. Da die Teilchen innerhalb des Pions eine Farbladung tragen und die Pionen zwischen Protonen und Neutronen ausgetauscht werden, ermöglichen Pionen den Austausch von Farbladungen zwischen Protonen und Neutronen untereinander. Die drei Quarks in einem Nukleon ändern nicht nur untereinander ihre Farbladungen, sondern auch durch Einfluss von anderen Nukleonen in unmittelbarer Nähe. Durch diesen Austausch wird auch die elektrische Ladung von Quarkteilchen in ein anderes Nukleon getragen, wodurch sich zeitgleich Neutronen in Protonen und umgekehrt verwandeln. Das Pion übernimmt die Rolle eines Vermittlers zwischen den Nukleonen und überträgt die in ihm beherbergten Quarks mit elektrischer Ladung, Farbladung und Gluonen, ähnlich in der Funktion eines Schiffes, ohne dessen Hilfe die Passagiere einen gewissen Bestimmungsort nicht erreichen können. Ist das Pion angekommen, zerstrahlt das Antiteilchen mit einem Quark am Bestimmungsort. Das ursprüngliche Quarkteilchen wird in dem Zielnukleon integriert. 15 Folgende Abbildung veranschaulicht den Austausch eines Pions zwischen einem Proton und einem Neutron: Proton Neutron Proton Neutron Neutron Neutron Neutron Proton Neutron Proton Interaktion von Nukleonen untereinander durch ein Pion 1. Ein Up-Quark löst sich aus dem Proton, kann jedoch aufgrund der kräftevermittelnden Gluonen nicht als freies Quarkteilchen existieren. 2. Im Prozess der starken, wechselwirkenden Farbladungen bildet sich aus den Kräften neue Materie in Form eines Quarkteilchens und seines Anti-Quarkteilchens. Hier ein Down-Quark und ein Anti-Down-Quark. 3. Das neu geschaffene Down-Quark verbleibt im Proton, während das neue Antiquark und das sich lösende Quarkteilchen gemeinsam als Pion das Proton verlassen. Durch diesen Vorgang verliert das Proton ein Up-Quark und gewinnt ein Down-Quark, wodurch sich seine elektrische Ladung ändert. Aus dem Proton wird ein Neutron. 4. Das Pion trifft auf ein in der Nähe befindliches Neutron. Dabei annihiliert ein Down-Quark das Anti-Down-Quarkteilchen. Das Up-Quarkteilchen ersetzt das annihilierte DownQuarkteilchen. 5. Die Ladungsverhältnisse im Atomkern wurden ausgetauscht, sind aber wieder hergestellt. Proton und Neutron haben über den Kräfte- und Ladungsaustausch ihre Position verändert. Schwache Kernkraft Ohne die schwache Kernkraft würde die Sonne nicht scheinen, es gäbe keine schweren Elemente wie Uran oder Plutonium und es gäbe auch keine Kohlenstoff-14-Analyse. Auch ist die schwache Kernkraft für den Betazerfall verantwortlich (Seite 25/26).All diese Vorgänge werden erst dadurch ermöglicht, dass sich ein Partikel in einen anderen Partikel umwandelt, was auch als Zerfall bezeichnet wird. Während die starke Kernkraft auf ein Proton oder Neutron wirkt, sodass seine Quarks durch den Austausch von Farbladungen zusammengehalten werden, bewirkt die schwache Kernkraft statt des Austausches der Farbladung, den Austausch des Flavors (Flavor = englisch für Geschmack). Es gibt sechs verschiedene Quark-Fla ors: Erd eere, )itro e, Apfel, Wal uss, S hlu pf u d Marzipa … Nei , kleiner Scherz. 16 Die Flavors bezeichnen keinen Geschmack, wie ihr Name vermuten lässt, sondern Quarks und Leptonen mit unterschiedlicher Masse und Ladungen. Neben Up- und Down-Quarks gibt es noch Charm-, Strange-, Top- und Bottom-Quarks. Up-Quarks tragen eine positive Ladung und DownQuarks eine negative Ladung. Diese beiden Quark-Arten haben die geringste Masse aller Quarks. Die anderen Quarks – Charm, Strange, Top und Bottom – tragen ebenfalls eine Ladung, sind jedoch weitaus massereicher und kommen nur sehr selten vor, da sie rapide in ein Up- oder Down-Quark zerfallen. Nicht nur Quarks unterliegen der schwachen Kernkraft, auch Leptonen (Elektronen und Neutrinos) interagieren durch sie. Genau wie die Quarks kommen auch Elektronen und Neutrinos in unterschiedlichen Flavors bzw. Massen vor. Deren massereicheren Teilchen sind jedoch ebenfalls sehr kurzlebig. All diese Materie-Teilchen nennt man zusammen Ferimonen. Die unterschiedlichen Materie-Teilchen (Ferimonen) im Vergleich: Ferimon Masse Up-Quark (u) 2,3 MeV/c Charm-Quark (c) 1,275 GeV Top-Quark (t) 173,07 GeV Down-Quark (d) 4,8 MeV Strange-Quark (s) 95 MeV Bottom-Quark (b) 4,18 GeV Elektron (e) 0,511 MeV Myon (µ) 105,7 MeV Tau τ 1,777 GeV Elektron-Neutrino( ) < 2 eV < 0,19 MeV Myon-Neutrino ( ) Tau-Neutrino ( ) < 18,2 MeV Ladung +⅔ +⅔ +⅔ -⅓ -⅓ -⅓ -1 -1 -1 0 0 0 Die schwache Kernkraft verändert den Flavor und damit auch die Masse und Ladung von Quarks. Wenn ein Quark seine Ladung ändert, verändert dies die Ladung des Nukleons, was sich auf die gesamte Identität des Atoms auswirkt. Wird ein Proton zu einem Neutron oder umgekehrt, ändert sich auch die Kernladungszahl, wodurch ein anderes Element mit anderen Eigenschaften entsteht. Wie bei den drei anderen Grundkräften der Physik, findet die Interaktion der schwachen Wechselwirkung durch virtuelle Austauschteilchen statt, einerseits den W-Bosonen, die positiv oder negativ geladen sind, andererseits durch neutrale Z-Bosonen. Die schwache Kernkraft wird als schwach bezeichnet, da sie nur auf sehr kurze Entfernungen von etwa 0,1 % des Durchmessers eines Protons wirkt. Ihre Austauschteilchen sind massereich und daher in ihrer Reichweite extrem begrenzt. Die wechselwirkenden Partikel müssen also sehr dicht aneinander geraten, um über die schwache Kernkraft in Interaktion zu treten. Wenn beispielsweise ein Neutrino ganz in die Nähe eines Neutrons gelangt, kann die schwache Wechselwirkung in Erscheinung treten. Ein positiv geladenes Boson verlässt das Neutrino und wechselwirkt mit dem Neutron. Genau diese Wechselwirkung ist die schwache Kernkraft. Das Neutrino, welches ein positives Austauschteilchen verloren hat, wird zum negativ geladenen Elektron. Das positiv geladene Boson trifft auf eines der beiden Down-Quarks des Neutrons und ändert dessen Ladung von -⅓ zu +⅔, as das Neutro i ei Proto u a delt. 17 Verschiedene Möglichkeiten des Zerfalls aufgrund der schwachen Wechselwirkung. Die Dicke der Pfeile stellt die Wahrscheinlichkeit des Zerfalls in ein bestimmtes anderes Quark dar. Deutlich erkennbar sind die Sprünge zwischen den Ladungen o +⅔ zu -⅓ u d zurück, sowie die enormen Massenunterschiede der Quarks. Dabei beschreiben die Pfeile nach links eine Emission von positiv geladenen Bosonen und nach rechts eine Emission von negativ geladenen Bosonen. Ein umgekehrter Austausch ist nicht möglich, da über die Bosonen nur entgegengesetzte Ladungen an die Quarks herantragen können. Die Quarks können hingegen nur die positive oder negative Ladung emittieren, die sie tragen. Anhand der Abbildung erklärt sich, dass ein Neutron mehr Masse als ein Proton hat, da Down-Quarks massereicher als Up-Quarks sind. Es gibt eine ganze Reihe an unterschiedlichen Teilchen, die aus den verschiedenen Quark-Flavors aufgebaut sind. Nicht nur uud (Proton) oder udd (Neutron), sondern einen ganzen Teilchenzoo aus über siebzig Kompositionen von Quark-Flavors gibt es, z. B. uus, udc, dsc und viele weitere. Alle diese Kompositionen sind sehr kurzlebig und zerfallen schnell in Up- oder Down-Quarks, welche besonders langlebig sind. Allerdings gibt es auch hier Unterschiede. Ein freies Neutron (udd), welches mit keinem Proton verbunden ist, zerfällt nach spätestens 14 Minuten und 42 Sekunden unter Emission eines Elektrons und Antineutrinos in ein Proton, während der Zerfall von Protonen noch nie beobachtet wurde. Bei diesem Zerfall muss sich ein Down-Quark in ein Up-Quark umwandeln, was nicht nur unter der oben beschriebenen Absorption eines Bosons von einem nahe vorbeifliegenden Neutrino geschehen kann. Das Down-Quark kann ein Boson emittieren und sich somit zu einem Up-Quark umwandeln. Dabei ist jedoch das emittierte Boson instabil und zerfällt schnell. ron und ein Antineutrino, Bosonen in ein Positron und Neutrino. Bosonen zerfallen in ein Elekt- Weitere Informationen zur schwachen Kernkraft finden Sie unter dem Thema Betazerfall (S. 25/26). 18 Kernkräfte und Massendefekt Wie im vorangegangenen Abschnitt beschrieben, wechselwirken Atome bzw. ihre Bestandteilemiteinander durch alle vier Grundkräfte der Physik. Während die Elektronen und damit die chemischen Eigenschaften nur der Gravitation und elektromagnetischen Kraft unterliegen, wirken auch die starke und schwache Kernkraft auf den Nukleus. Im Nukleus sind die starke Kernkraft und die elektromagnetische Kraft von besonderer Bedeutung, da diese beiden eine entgegengesetzte Kraft auf die Nukleonen auswirken. Während die positiv geladenen Protonen im Kern einander bei geringem wie auch größerem Abstand durch die elektromagnetische Kraft abstoßen, hält die starke Kernkraft die Nukleonen trotzdem dicht bepackt zusammen, wirkt jedoch nur auf sehr geringe Entfernungen. Die starke Kernkraft stellt eine Art Superkleber auf gleichpoligen Magneten dar; kommen sie nah genug aneinander, kleben sie miteinander fest, obwohl sie einander bereits bei größeren Abständen abstoßen. Protonen stoßen sich bei größerer Entfernung aufgrund ihrer gleichen Ladung (blau) ab. Bei geringer Entfernung wirkt die starke Kernkraft (rot) und hält die Protonen trotz der sich abstoßenden elektromagnetischen Kräfte zusammen. Die starke Kernkraft ist stärker als die elektromagnetische Abstoßung. Die elektrischen Abstoßungskräfte zwischen den Protonen haben eine unendliche Reichweite, auch wenn diese mit größerem Abstand abnimmt. Die starke Kernkraft hingegen wirkt nur auf eine Entfernung von etwa 2,5 Diametern eines Nukleons. Die elektrischen Abstoßungskräfte sind zwar schwächer als die starke Kernkraft, jedoch wirken sie auf alle Protonen im Kern. Je größer ein Nukleus als 2,5mal dem Durchmesser eines Nukleons ist, bzw. je mehr Protonen bzw. Nukleonen ein Nuklid über dieses Maß hinaus hat, umso instabiler wird es. Die einander abstoßenden Kräfte werden mit jedem Proton immer stärker, während die starke Kernkraft gleich bleibt. Ab einem bestimmten Punkt kann die starke Kernkraft den einander abstoßenden Kräften der Nukleonen nicht mehr gerecht werden, was eine Instabilität nach sich zieht. Wie stark die Nukleonen zusammengehalten werden ist von Nuklid zu Nuklid verschieden. Bindungsenergie und Massendefekt Wie im vorangehenden Abschnitt beschrieben, wirken zwei Kräfte auf den Nukleus ein: Die starke Wechselwirkung hält die Nukleonen zusammen, während die von den Protonen ausgehende elektromagnetische Wechselwirkung den Nukleus auseinander zu drücken versucht. Die starke Wechselwirkung ist dabei sehr viel stärker als die elektromagnetische Wechselwirkung, wirkt jedoch auf eine Distanz von nur etwa 2,5 Durchmessern eines Nukleons, während die elektromagnetische Wechselwirkung mit abnehmender Stärke unendlich weit wirkt. Die Bindungsenergie in einem Nukleus ist die Menge an Energie, die benötigt wird, um die darin enthaltenen Nukleonen voneinander vollständig zu trennen, bzw. die Differenz aus der starken Wechselwirkung und elektromagnetischer Wechselwirkung, die sich auf die Nukleonen auswirkt. 19 Abbildung links: Leichte Nuklei lassen sich deutlich schwerer in ihre einzelnen Nukleonen aufspalten, da in ihnen wenige Protonen enthalten sind, welche die einzelnen Bestandteile des Kerns auseinanderdrängen (blauer Pfeil). Die ins Zentrum des Kerns wirkendende, starke Wechselwirkung (roter Pfeil), ist dieser elektromagnetischen Wechselwirkung deutlich überlegen. Die Differenz zwischen diesen beiden Wechselwirkungen (gelb gestrichelte Linie) wird jedoch mit steigender Massenzahl immer geringer. Dies bedeutet, dass i er s h erere Nuklide au h i er „u ruhiger“ werden, da die einzelnen Nukleonen nicht so stark aneinander gebunden sind. Je mehr Nukleonen auf einem Haufen sind und sich versuchen auseinander zu drängen, desto geringer fällt ihre Bindungsenergie aus, weshalb auch immer weniger Energie benötigt wird, um diese Nukleonen sich spalten zu lassen. Entgegen aller Erwartungen ist die Bindungsenergie eigentlich eine Freigabe von Energie. Doch wie kann die Freigabe von Energie das Atom zusammenhalten? Sollte nicht Energie benötigt werden, um die einzelnen Komponenten im Kern zusammenzuhalten? Die Antwort lautet Ja und Nein zugleich: Sind Protonen und Neutronen zu einem Kern miteinander verbunden, wird Energie benötigt, um ihre Verbindung in einzelne Nukleonen aufzubrechen. Die Menge an benötigter Energie entspricht der Bindungsenergie, die jedes einzelne Nukleon umfasst und mit den anderen Nukleonen zusammenhält. Protonen und Neutronen zusammen in einem Kern, haben ein geringeres Energieniveau und sind daher stabiler als freie Protonen und Neutronen. Indem sie zusammenkommen, gehen sie in einen geringeren Energiezustand über. Wenn sie in diesen geringeren Energiezustand übergehen, wird überschüssige Energie wird frei, d.h. ein kleiner Teil der Masse der Nukleonen wird in Energie umgewandelt. Partikel, die Energie gewinnen oder verlieren, gewinnen oder verlieren dabei auch Masse. Wenn also ein Proton und Neutron zusammenkommen, wandelt sich ein Teil der Teilchen in Energie um. Beispielsweise besteht ein4He-Kern aus zwei Protonen und Neutronen und sollte eigentlich die gleiche Masse aus seinen zwei Protonenmassen und Neutronenmassen haben – er ist allerdings leichter. Ein einzelnes Proton wiegt 1,672622 x 10-27 kg, ein einzelnes Neutron 1,674927 x 10-27 kg. Bei jeweils zwei einzelnen Protonen und Neutronen ergibt die Summe dieser vier einzelnen Massen 6,695098 x 10-27 kg. Der 4He-Kern hat jedoch eine Masse von 6,644656 x 10-27 kg, ist also um 0,050442 x 10-27 kg masseärmer als die Summe der Massen der einzelnen Teilchen. Genau dieser Unterschied an Masse ist der Massendefekt bzw. die Bindungsenergie. Der einzige Ort, an welchem auf natürlichem Wege einzelne Nukleonen miteinander verschmelzen, ist ein Stern Sonne. Nur dort, wirken genügend starke Ener6,695098 x 10-27 kg 6,644656 x 10-27 kg gien, welche die einzelnen Nukleonen nahe genug Differenz: 0,050442 x 10-27 kg aneinanderpressen, damit die starke Kernkraft wirken 2p/2n 20 kann. Beim Zusammenschluss von einzelnen Protonen und einzelnen Neutronen wird ein kleiner Teil ihrer Masse in Energie umgewandelt. Durch diesen Verlust an Masse, und damit durch die abgegebene Energie, wird die Bindung der Nukleonen aneinander ermöglicht. Gemäß Albert Einsteins berühmter Gleichung E=mc² kann bestimmt werden, wie viel Energie einer bestimmten Masse und umgekehrt entspricht. Dabei wird deutlich, dass kleinste Mengen an Masse ein enorm hohes Energiepotential haben. Beim 4He-Kern entspricht der Massendefekt von 0,050442 x 10-27 kg einer Energiemenge von 0,4535 x 10-11 Joule. Umgerechnet in Elektronenvolt (Seite 23/24) sind das 28,3 MeV. Dies ist die Bindungsenergie, die auf den gesamten Kern wirkt. Bei der Entstehung des 4He-Kerns aus seinen vier einzelnen Nukleonen wurden also 28,3 MeV abgegeben. Pro Nukleon entfällt rein rechnerisch eine Bindungsenergie von 7,075 Mev (28,3 Mev geteilt durch die Anzahl der Nukleonen im Kern).Im Umkehrschluss bedeutet dies: Um den 4He-Kern in seine einzelnen Nukleonen zu spalten, wird mindestens die gleiche Menge an Energie benötigt, die er bei seiner Entstehung freigesetzt hat, d.h. 7,075 MeV pro Nukleon. Der Massendefekt zeigt, wie sehr Masse und Energie miteinander verknüpft und austauschbar sind. Masse und Energie sind in diesem Sinne zwei verschiedene Erscheinungsformen ein und derselben Sache. n p 28,3 MeV 4 p He n n 28,3 MeV p wird zu 4 He p n Zwei Protonen plus zwei Neutronen minus der Freigabe von Energie in Höhe von 28,3 Mev, um miteinander zu verschmelzen, entsprechen einem 4HeKern.Ein 4He-Kern plus 28,3 MeV entspricht seinen vier einzelnen Nukleonen (zwei Protonen und zwei Neutronen).Bei Entstehung des 4He-Kerns beträgt der Masseverlust 7,075 MeV pro Nukleon, genauso stark sind die Nukleonen miteinander verbunden, und genau diese Energie wieder benötigt wird, um die Nukleonen aus ihrer Bindung auseinanderzubrechen. Jedes Nuklid hat seine eigene charakteristische Bindungsenergie. Je mehr Nukleonen sich in einem Kern befinden, umso stärker wird die Bindungsenergie. Ab den Elementen Eisen und Nickel tritt jedoch ein Wendepunkt ein. Ab diesem Punkt wird das Missverhältnis von Protonen und Neutronen größer, der Nukleus hat einen größeren Radius als 2,5 Nukleonen-Durchmesser und die elektromagnetischen Kräfte im Kern beginnen über die starke Wechselwirkung zu dominieren. Werden jenseits dieser Nuklide weitere Nukleonen in den Kern gefügt, beginnt die auseinanderdrängende elektromagnetische Kraft die starke Kernkraft zu übertrumpfen. Jedes weitere hinzugefügte Nukleon ist etwas weniger im Kern gebunden bzw. hat weniger Bindungsenergie. Werden so viele Nukleonen hinzugefügt, bis man bei den Elementen Blei und Bismuth ankommt (207 Nukleonen), gewinnt die elektromagnetische Kraft die Überhand. Atomkerne jenseits dieser Elemente sind instabil und wandeln sich selbst durch Strahlung in stabile Elemente um, auch wenn diese Umwandlung je nach Nuklid bis zu mehrere Milliarden Jahre dauern kann. 21 Bindungsenergie per Nukleon in MeV Massenzahl Die obige Abbildung zeigt die mittlere Bindungsenergie per Nukleon in Abhängigkeit von der Massenzahl. Mittelschwere Kerne mit den Massenzahlen 40 bis 100 (gelber Abschnitt) haben die höchsten Werte an Bindungsenergie und sind daher allgemein sehr stabil. Der Kern mit der höchsten Bindungsenergie ist Eisen-56. Bis zu diesem Kern neigen leichtere Nuklide dazu, zu fusionieren (roter Abschnitt), schwerere neigen eher dazu instabil zu werden (blauer Abschnitt). Für die Nutzung der Kernenergie sind die äußersten Enden dieser Kurve am brauchbarsten, da diese weniger Bindungsenergie als die mittelschweren Atomkerne haben und am ehesten dazu zu veranlassen sind, ihren Kern zu ändern, damit dieser in den sehr stabilen, gelb markierten Abschnitt gerät: Sehr leichte Kerne werden miteinander verschmolzen und bilden somit einen neuen, schwereren Kern, dessen Nukleonen stärker aneinander gebunden sind. Mit dem einhergehenden Masseverlust, ist dieser Vorgang mit einer enormen Freigabe von Energie verbunden. Die Fusion zweier leichteren Kerne zu einem schwereren Kern geschieht im Inneren der Sonne und wird in der Zündung von Wasserstoffbomben künstlich herbeigeführt. Besonders schwere, instabile Atomkerne hingegen, werden in zwei mittelgroße Kerne gespalten. Da die Bindungsenergie bei sehr schweren Kernen ebenfalls geringer ist, als bei mittelschweren Kernen, tritt auch hier der Massenverlust auf und es wird Energie freigesetzt. Kernspaltungen finden Anwendung zur Energiegewinnung in Kernkraftwerken, finden aber auch in Kernwaffen statt. Jenseits des Elementes Eisen steigen die Abstoßungskräfte mit jedem weiteren Proton im Kern an, wohingegen die starke Kernkraft gleichbleibt. Die Bindungsenergie pro Nukleon wird durch die sich abstoßenden Protonen immer mehr aufgehoben und der Effekt der Instabilität nimmt zu. Ab dem Element Polonium, das 84 Protonen im Kern beherbergt, können die Nukleonen ihre enorme positive Ladung nicht mehr arrangieren. Um wieder in einen stabileren Zustand zu gelangen, werden überschüssige Protonen in Form von Alphastrahlung abgestoßen. (siehe Alphazerfall Seite 25) 22 Nuklid Gesamte Bindungsenergie in MeV Bindungsenergie pro Nukleon in MeV H-2 2,23 1,11 He-4 28,29 7,07 Li-7 40,15 5,74 Be-9 58,13 6,46 O-16 127,62 7,98 Cl-35 298,20 8,52 Fe-56 492,24 8,79 Ag-107 915,23 8,55 I-127 1072,53 8,45 Pb-208 1636,46 7,87 Po-210 1645,16 7,83 U-235 1783,80 7,59 U-238 1801,63 7,57 Die höchsten Werte der Bindungsenergie pro Nukleon liegen bei Eisen-56. Nukleosynthese Die Nukleosynthese beschreibt die Entstehung von Elementen in Sternen. Je nach der Größe eines Sterns, bewirken Hitze und der entsprechende Gravitationsdruck die Fusion von leichten Kernen zu schwereren Kernen. Bei der Entstehung von Nukliden bis Eisen-56 wird Energie freigesetzt (exotherme Reaktion). Insbesondere sehr leichte Isotope mit geringer Bindungsenergie wie Wasserstoff, Helium oder Lithium lassen sich vergleichsweise leicht zu schwereren Nukliden fusionieren (siehe Kernfusion Seite 36 ff.). Von allen Nukliden verfügt Eisen-56 über die stärkste Bindungsenergie pro Nukleon. Elemente, die schwerer als Eisen sind, setzen bei ihrer Entstehung weniger Energie frei als sie zu ihrer Bildung verbrauchen (endotherme Reaktion). Beim Kollaps von sehr massereichen Sternen zu einer Supernova, entstehen durch Fusionsprozesse und Neutroneneinfänge sehr schwere Elemente. Die heute auf unserer Erde befindlichen Elemente wie Blei, Gold, Silber, Uran und andere schwere Elemente jenseits von Eisen-56, sind Spuren eines vor Billionen von Jahren explodierten Sterns. Bis Eisen-56 lassen sich alle leichteren Nuklide fusionieren, während schwerere Nuklide sich eher spalten lassen. Prinzipiell lassen sich Elemente umso leichter spalten, desto schwerer sie als Eisen sind. Der Grund, weshalb Eisen-56 einen Wendepunkt in der Energiefreigabe von Zusammenschlüssen für leichtere Kerne und Spaltungen für schwerere Kerne darstellt, liegt an der mit steigender Protonenzahl wachsenden positiven Ladung im Kern. Die sich gegenseitig abstoßende elektromagnetische Kraft zwischen den Protonen wirkt sich auf den gesamten Kern aus, während die starke Kernkraft nur einen Effekt auf eine Entfernung von rund 2,5 Nukleonen hat. Im konkreten Fall des Eisens stößt sich jedes Proton von den anderen 25 in der Nähe befindlichen Protonen ab, während die starke Kernkraft jedes einzelnen Nukleons auf jedes andere Nukleon wirkt. 23 Energieeinheiten Elektronenvolt, Joule und Watt Anders als der Name verrät, ist eV (Elektronenvolt) eine Energieeinheit und keine Einheit für Spannung wie Volt. Die genaue Definition lautet: Ein Elektronenvolt ist die Energie, die ein Teilchen mit der Ladung 1e (Elementarladung bzw. Ladung eines Elektrons) erhält, wenn es im Vakuum die Spannung von einem Volt durchläuft, dadurch beschleunigt wird und somit kinetische Energie gewinnt. Im Bereich der Kernkraft treten sehr kleine Energiewerte auf, die durch das Elektronenvolt gut veranschaulicht werden können. Für den alltäglichen Gebrauch ist das Elektronenvolt jedoch eine viel zu kleine Einheit. Hier finden eher die Energieeinheiten Joule und Watt Anwendung, die untereinander und in Elektronenvolt umgerechnet werden können. Ein Joule entspricht dabei etwa der Energie, die benötigt wird, um einen 100 Gramm schweren Gegenstand, wie eine handelsübliche Tafel Schokolade oder einen kleinen Apfel, einen Meter in die Höhe zu heben. Die gleiche Energie von einem Joule wird wiederum freigesetzt, wenn die Schokolade bzw. der Apfel aus einem Meter Höhe zu Boden fallengelassen wird. Ein Joule entspricht ebenfalls der Beschleunigung eines ein Kilogramm schweren Gegenstandes auf eine Geschwindigkeit von einem Meter pro Sekunde (3,6 Km/h) über eine Strecke von einem Meter. Die mathematische Formel lautet also: Joule ist damit eine Einheit, die eine gewisse Arbeit in Zahlen ausdrückt. Eine andere Möglichkeit festzustellen wie viel Arbeit in welcher Zeit erledigt werden kann, liefert das Watt. Generell gilt: die geleistete Energie entspricht der verrichteten Arbeit geteilt durch die dafür benötigte Zeit. Ein Watt gleicht einem Joule pro Sekunde. Watt ist also die Energie, die eine Vorrichtung in Höhe von einem Joule pro Sekunde verbraucht. Beispielsweise verbraucht eine Glühbirne mit 25 Watt umgerechnet 25 Joule pro Sekunde. Der im Alltag oft verwendete Begriff "Kilowattstunde" kWh sind 1.000 Watt, die im Zeitraum von einer Stunde bzw. 3.600 Sekunden verbraucht werden. Eine kWh rechnet sich demnach wie folgt in Joule um: 24 1 kWh = 1.000 Watt * 3.600 Sekunden = 3.600.000 Joule = 3.600 Kilojoule (KJ) = 3,6 Megajoule (MJ) Einheit Joule Kilowattstunde Elektronenvolt Abkürzung J kWh eV J 1 3,60 * 6 1,60 * 10-19 Faktor zu Umrechnung in kWh eV 2,78 * 10-7 6,24 * 1018 1 2,25 * 1025 -26 4,45 * 10 1 Kernzerfall und Radioaktivität Die Kerne instabiler Isotope zerfallen spontan zu einem anderen Kern mit einem niedrigeren und folglich stabileren Energieniveau. Bei ihrem Zerfall setzen sie Nuklearstrahlung frei; ein Phänomen, das sich Radioaktivität nennt. Die Welt auf der wir leben besteht fast nur aus stabilen Isotopen, d.h. aus Atomen, welche nicht zerfallen. Doch zu einem kleinen Bruchteil kommen instabile Isotope überall in der Natur vor, in Meeren, in Gesteinen, in der Atmosphäre und sogar in Pflanzen und Lebewesen. Selbst wir Menschen tragen radioaktive Isotope in uns, weshalb alles und jeder ständig einer sehr geringen Radioaktivität ausgesetzt ist. Atomkerne gelten als stabil, wenn die richtige Zahl an Protonen und Neutronen zusammenkommen. Die Neutronen nehmen die Funktion eines Puffers zwischen den sich durch gleiche Ladung abstoßenden Protonen ein. Je mehr Protonen sich im Kern befinden, umso mehr Neutronen werden benötigt, um die Protonen voneinander auf Abstand zu halten. Daher sind insbesondere bei schweren Elementen mit hoher Kernladungszahl überproportional viele Neutronen zur Stabilisierung der Kräfte im Kern nötig. Ist das Verhältnis zwischen Protonen und Neutronen nicht optimal, wandelt der Kern sich um bzw. er zerfällt, bis er ein stabiles Verhältnis erreicht hat. Dies kann auf verschiedene Weisen geschehen: Der Kern kann spontan von selbst in zwei neue Nuklide auseinanderbrechen, er kann einen sehr stabilen Heliumkern emittieren (Alphazerfall), einzelne Neutronen oder Protonen abstoßen oder ein Neutron in ein Proton oder umgekehrt umwandeln (Betazerfall). Nuklide welche zerfallen, werden auch Radionuklide genannt. Auf den Kern wirkt die starke Kernkraft (rote Pfeile) nach innen, während die elektrischen Abstoßungskräfte zwischen den Protonen nach außen wirken (grüne Pfeile). Je nach Zerfallsart verlässt ein Alphapartikel bzw. Heliumkern (oben rechts) oder ein Betapartikel bzw. Elektron den Kern. Bei jeder Zerfallsart wird auch Gammastrahlung freigesetzt (links).Neben Alpha-, Beta- und Gammastrahlung, kann der Kern auch in zwei neue Kerne auseinanderbrechen oder einzelne Neutronen oder Protonen emittieren, um stabil zu werden. 25 Alphazerfall auch α, Alphastrahlung Alphateilchen bestehen wie ein Heliumkern aus zwei Protonen und zwei Neutronen. Diese vier Nukleonen werden beim Zerfall eines Radionuklids wie beispielsweise Uran-238 vom Mutterkern emittiert. Durch den Verlust der Protonen und Neutronen wandelt sich das Uran-238 in Thorium-234 um. Alphazerfall wird durch folgende Kernreaktionsgleichung beschrieben: Der Alphazerfall tritt vor allem bei Nukliden mit besonders vielen Nukleonen auf. Damit der Alphazerfall überhaupt stattfinden kann, muss die starke Wechselwirkung überwunden werden, die die Nukleonen zusammenhält. Erst wenn diese überwunden ist und die elektrische Abstoßung der Protonen wirken kann, wird das Alphateilchen emittiert. Alleine kann das Alphateilchen diese Kraft nicht aufbringen. Da jedoch die Kräfte und Elementarteilchen im Atomkern stets miteinander wechselwirken, kann es in schweren Nukliden zwischen den subatomaren Partikeln zum "Ausleihen" von Kräften kommen. Beim Alphazerfall wirken kurzfristig so starke Kräfte auf das Alphateilchen ein, damit es die starke Wechselwirkung überwindet und den Kern verlässt. Alphazerfall ist nur bei Nukliden mit sehr vielen Nukleonen möglich. Insbesondere bei Nukliden mit einem übermäßig hohen Verhältnis von Protonen zu Neutronen wird der Kern instabiler. Je höher die Kernladungszahl ist, desto stärker wirken die elektromagnetischen Abstoßungskräfteder im Atomkern enthaltenen Protonen und machen ihn anfälliger für Alphazerfall. Alphateilchen werden mit einer Geschwindigkeit von 15.000 bis 20.000 Kilometern pro Sekunde emittiert. Nachdem sie durch Interaktionen mit umliegenden Atomen abgebremst wurden, ziehen sie Elektronen aus umliegenden Atomen an und werden so zu vollständigen 4 He-Atomen. Die umliegenden Atome werden dadurch in ihren chemischen Eigenschaften verändert. Aufgrund ihrer hohen Masse und ihrer starken Reaktionsfreudigkeit, kann Alphastrahlung leicht abgeschirmt werden. Trifft Alphastrahlung auf einen Menschen, ist es ihr kaum möglich die äußere Hautschicht zu durchdringen und ist somit relativ ungefährlich. Gefährlich werden Alphateilchen dann, wenn alphazerfallende Isotope durch Verschlucken oder Einatmen in den Körper gelangen. Betazerfall auch β, Betastrahlung Betateilchen sind Elektronen oder Positronen, die aus dem Atomkern emittiert werden. Diese Teilchen sind vor dem Betazerfall noch nicht existent und entstehen als Nebenprodukt aus der spontanen Umwandlung von Nukleonen. Der Vorgang der Umwandlung der Nukleonen von einem Neutron in ein Proton oder umgekehrt, wird durch subnukleare Prozesse verursacht, bei denen kräftevermittelnde Bosonen zwischen den Nukleonen interagieren, d.h. die schwache Kernkraft ist für die Umwandlung verantwortlich (siehe Schwache Kernkraft Seite 15 ff.).Als Resultat wandelt sich beim BetaMinus-Zerfall ein -⅓-Quark ei es Neutro s i ei +⅔-Quark um, welches die Ladung des Nukleons von ursprünglich Null (= Neutron) auf +1 (= Proton) verändert: Neutron u d d u d u Boson Proton Anti-Neutrino Elektron 26 Beim Beta-Minus-Zerfall verliert demnach das Atom ein Neutron, gewinnt aber dafür ein Proton hinzu. Der instabile Kern versucht somit seinen Überschuss an Neutronen durch Protonen zu ersetzen und in einen Stabileren Zustand zu gelangen. So wandelt sich beispielsweise das betastrahlende Cäsium-137 unter Aussenden eines Elektrons in Barium-137 um: Hat im Gegenzug ein Kern überproportional viele Protonen im Vergleich zu Neutronen, kann der Beta-Plus-Zerfall eintreten. Ein Proton wird dabei in ein Neutron umgewandelt. Proton u d u u d d Boson Neutron Neutrino Positron Beim Beta-Plus-Zerfall verringert sich die Kernladungszahl um eins, während sich die Massenzahl nicht verändert. Die Reaktionsgleichung für den Beta-Plus-Zerfall und ein Beispiel an der Umwandlung von Natrium-22 in Neon-22, sehen wie folgt aus: Die bei Betazerfällen entstehenden Neutrinos und Anti-Neutrinos besitzen aufgrund ihrer elektrischen Neutralität und geringen Masse ein sehr hohes Durchdringungsvermögen. Sie treten mit Materie kaum in Wechselwirkung und sind nur sehr schwer nachzuweisen. Bei Kernreaktionsgleichungen können sie daher vernachlässigt werden. Trifft ein Teilchen auf sein entsprechendes Anti-Teilchen, vernichten sich beide Partikel unter Abgabe von Energie restlos. Stoßen Positronen mit Elektronen oder Neutrinos mit Anti-Neutrinos zusammen, zerstrahlen beide Teilchen unter Freigabe von Gammastrahlung. Betateilchen können durch mehr Materie dringen als Alphapartikel, sind im Gegensatz zur Gammastrahlung jedoch relativ schwach. Ihre Reichweite durch Luft beträgt von ihrer Strahlungsquelle wenige Meter, bevor sie mit Materie reagiert. Auf nähere Entfernungen können sie von einem zwei Millimeter dicken Aluminiumblech vollständig abgeschirmt werden. Betapartikel verändern die chemischen Eigenschaften des getroffenen Atoms, indem sie entweder ein Elektron aus der Hülle schießen oder sich in der Hülle zusätzlich anlagern. Gammazerfall (auch γ, Gammastrahlung) Gammastrahlung ist von allen bei Nuklearreaktionen vorkommenden Strahlungsarten keine Teilchenstrahlung, sondern eine masselose elektromagnetische Strahlung, die energetischer als Röntgenstrahlung ist. Sie entsteht beim Übergang eines Nuklids von einem angeregten Zustand in einen energieärmeren und damit stabileren Zustand. Bei den meisten Teilchenstrahlungen wird zusätzlich auch Gammastrahlung freigesetzt. Wandelt sich ein Kern durch Alpha- oder Betazerfall, spontane Kernspaltung, Protonen- oder Neutronenemission um, kommt es infolge der Verschiebungen der 27 Ladungsverhältnisse im Kern auch zur Aussendung von Gammastrahlung. Im Gegensatz zu anderen Zerfallsarten, bleiben beim Gammazerfall die Massen- sowie Kernladungszahlen erhalten. Der Kern gibt per Gammazerfall lediglich überschüssige Energie ab, um in seinen energetischen Grundzustand zu gelangen. Ein Nukleus wird in seiner geometrischen Form immer den energetisch stabilsten Zustand einnehmen. Für gewöhnlich verspricht die Form einer Kugel den stabilsten Zustand eines Atomkerns. Verändert sich aufgrund eines Zerfalls der Kern, entsteht in der Kugel je nach Zerfallsart ein "Loch" oder eine "Ausbeulung". Wegen der starken Wechselwirkung, die die Nukleonen aneinander presst, wird die Verformung wieder ausgeglichen. Durch die Verschiebung der Nukleonen, und damit auch der Ladungsverhältnisse im Kern, wird Energie in Form von Gammastrahlung frei. Abbildung: Ein Uran-238-Kern unterliegt dem Alphazerfall. Durch die Emission des Alphateilchens wandelt sich das Uran-238 in Thorium-234 um. Das Thorium-234 befindet sich in angeregtem Zustand, da es nicht die energetisch stabilste Form einer Kugel einnimmt. Um in einen stabileren Zustand zu gelangen, geraten die Nukleonen in Bewegung, um das Loch zu kompensieren, das durch die Emission des Alphateilchens entstanden ist. Dabei wird Energie in Form von Gammastrahlung frei. Anders als die massereichen und elektrisch geladenen Alpha- und Betastrahlen, können Gammastrahlen nicht so leicht abgeschirmt werden. Je nach Strahlungsintensität ist entsprechend viel Materie zur hinreichenden Abschirmung nötig, wobei eine hundertprozentige Abschirmung kaum möglich ist. Ein einzelner Gammastrahl kann bereits nach wenigen Kontakten mit anderen Atomen absorbiert werden oder aber auch erst sehr viel Materie durchdringen, ehe er auf andere Atome trifft und abgeschwächt wird. Zur Abschirmung wird am besten dichtes, schweres Material verwendet. So besteht beispielsweise die Schutzhülle um Kernreaktoren aus über zwei Meter dickem Spezialbeton, der die Gammastrahlung weitestgehend absorbiert. Ein unumgänglicher, geringfügig erhöhter Strahlungswert ist rund um Kernanlagen dennoch festzustellen. Gammastrahlen sind so energetisch, dass sie beim Auftreffen auf andere Atome, deren Elektronen aus der Hülle schlagen können, wodurch sich die chemischen Eigenschaften des getroffenen Atoms verändern. Trifft hochenergetische Gammastrahlung auf einen Atomkern, kann dieser durch die enorme Energieaufnahme gespalten werden. Protonenemission Die Protonenemission, also das Abstoßen eines einzelnen Protons aus dem Atomkern, kommt im Vergleich zu anderen Zerfallsarten sehr selten vor. Sie tritt nur bei solchen Nukliden auf, die ein extrem hohes Verhältnis von Protonen zu Neutronen haben. Herrscht ein sehr starker Protonenüberschuss im Kern, können die Protonen kaum noch gebunden werden. Statt des Beta-Plus-Zerfalls, nach welchem sich ein Proton in ein Neutron umwandelt, wird ein Proton direkt emittiert. Ein freies Pro28 ton bzw. ein Wasserstoff-Ion wirkt wie eine starke Säure und kann ein Elektron aus einem umliegenden Atom an sich reißen. Die chemischen Eigenschaften des umliegenden Atoms werden dadurch verändert. Neutronenstrahlung (Freie Neutronen) Freie Neutronen stellen einen wesentlichen Faktor für künstlich erzeugte Reaktionen in Nuklearreaktoren und Kernwaffen dar. Je nach ihrer Geschwindigkeit können sich freie Neutronen an Atomkerne anlagern und eine Kernreaktion verursachen. Wird ein Neutron von einem Kern absorbiert, schichten sich die Ladungsverhältnisse des getroffenen Kerns um. Der Kern, der durch die Neutronenabsorption ein Neutron hinzugewonnen hat, kann zu einem Radionuklid werden oder sich spalten. Im Gegensatz zu den bisher angeführten Strahlungsarten interagiert die Neutronenstrahlung nicht mit der Elektronenhülle, sondern mit einem anderen Atomkern. Freie Neutronenkönnen aufgrund ihrer elektrischen Neutralität viel Masse durchdringen, bevor sie von einem Atomkern eingefangen werden. In ihrer Wirkung auf organisches Gewebe ist Neutronenstrahlung sehr schädlich. Neben der elastischen Kollisionswirkung an Wasser im Körper, die ein einzelnes Wasserstoff-Ion (starke Säure) und ein Hydroxyd-Ion (starke Base) generiert, können andere Nuklide durch den Neutroneneinfang radioaktiv werden. Ionisierende Wirkung Eine Ionisation beschreibt jeden Prozess, der ein Atom in seinen chemischen Eigenschaften verändert, d.h. meist die Entfernung, selten auch die Hinzufügung eines Elektrons in einem Atom bewirkt. Das ursprünglich elektrisch ausgeglichene Atom oder Molekül erlangt unter Verlust eines negativ geladenen Elektrons eine positive Ladung. Da dem getroffenen Atom nun ein negativ geladenes Elektron fehlt, um die positive Ladung der Protonen im Kern auszugleichen, geht es neue chemische Verbindungen ein, um wieder einen elektrisch neutralen Zustand zu erreichen. Die eintretende chemische Manipulation wirkt sich besonders auf komplexe organische Moleküle aus, die durch die Ionisation verändert oder gar zerstört werden können. In der Medizin wird unerwünschtes Gewebe, wie Krebszellen, ionisierenden Strahlen ausgesetzt, um es in seinen chemischen Eigenschaften soweit zu verändern, sodass es nicht mehr überlebensfähig ist und abstirbt. Abbildung einer typischen Gammainteraktion: Trifft Gammastrahlung (orange) auf ein Elektron, wird dieses durch die immense Energiezufuhr aus der Elektronenschale herausgeschossen. Die Energie des Gammastrahls wird auf das Elektron übertragen und überschüssige Energie in Form eines zweiten, energieärmeren elektromagnetischen Strahls abgegeben. Die Energie des Gammastrahls gleicht der Summe aus der Bindungsenergie und Geschwindigkeit des freigewordenen Elektrons und der Energie des energieärmeren Strahls. Das freigesetzte Elektron (BetaStrahlung) kann seinerseits Atome aus der Umgebung ionisieren. 29 Obwohl ionisierende Strahlung sehr gefährlich für Organismen ist, kann man sie nicht wahrnehmen. Lediglich aufgrund kleiner Besonderheiten lässt sie sich erahnen. So berichtete beispielsweise einer der Piloten der Enola Gay, dem Flugzeug von welchem aus die Atombombe auf Hiroshima abgeworfen worden war, kurze Zeit nach der Explosion der Bombe einen seltsam metallischen Geschmack im Mund gehabt zu haben. Dies kam infolgedessen, dass sich die bei der Explosion freiwerdende Strahlung auf seine Zahnfüllungen auswirkte. Halbwertszeit Der Kernzerfall vollzieht sich nicht chaotisch, sondern unterliegt einer gewissen Ordnung. Ein einzelnes Radionuklid kann man nicht daraufhin untersuchen, wann es zerfällt. Der Zerfall kann in der nächsten Sekunde oder aber erst in Tausenden Jahren eintreten. Bei einer großen Anzahl von Atomen des gleichen Radionuklids lässt sich allerdings eine Wahrscheinlichkeitsaussage über den zeitlichen Ablauf des Zerfalls treffen. Dieser Ablauf wird mit der Halbwertszeit beschrieben. Die Halbwertszeit ist die Zeit, nach welcher die Hälfte aller Radionuklide einer Substanz zerfallen. Jedes einzelne Radionuklid hat seine eigene charakteristische Halbwertszeit, die von Sekundenbruchteilen bis zu Jahrmilliarden reicht. Da die Dauer der Halbwertszeit in Proportion zur Strahlungsaktivität eines Stoffes steht, zieht eine kurze Halbwertszeit intensive Radioaktivität nach sich, während eine lange Halbwertszeit schwache Radioaktivität über einen langen Zeitraum impliziert. Abbildung: Zerfallskurve am Beispiel von Radium-227 mit einer Halbwertszeit von 42,2 Minuten. 30 In jeder Halbwertszeit wandelt sich stets die Hälfte der jeweils anfänglich vorhandenen Radionuklide um. Zunächst nimmt die Anzahl der radioaktiven Kerne sehr rasch ab, verlangsamt sich mit jeder Halbwertszeit immer mehr. Nach vier Halbwertszeiten ist das Radionuklid zu mehr als 90 % zerfallen, nach zehn Halbwertszeiten sogar zu mehr als 99 %.Bei einer angenommenen Ausgangsmenge von 32.000.000 Atomkernen des Radionuklids Radium-227 kann man den Zerfallsablauf verdeutlichen. Radium-227 hat eine Halbwertszeit von 42,2 Minuten. Die aufeinanderfolgenden Halbwertszeiten werden als Zahlen und Prozent in der folgenden Tabelle dargestellt: Zeit in Minuten 0 42,2 84,4 126,6 168,8 211 253,2 295,4 337,6 379,8 422 464,2 Anzahl der Halbwertszeiten 0 1 2 3 4 5 6 7 8 9 10 11 Anzahl der radioaktiven Kerne 32.000.000 (100 %) 16.000.000 (50 %) 8.000.000 (25 %) 4.000.000 (12,5 %) 2.000.000 (6,25 %) 1.000.000 (3,12 %) 500.000 (1,56 %) 250.000 (0,78 %) 125.000 (0,39 %) 62.500 (0,2 %) 31.250 (0,10 %) 15.625 (0,05 %) Anzahl der zerfallenen Tochterkerne 0 16.000.000 (50 %) 24.000.000 (75 %) 28.000.000 (87,5 %) 30.000.000 (93,75 %) 31.000.000 (96,88 %) 31.500.000 (98,44 %) 31.750.000 (99,22 %) 31.875.000 (99,61 %) 31.937.500 (99,80 %) 31.968.750 (99,90 %) 31.984.375 (99,95 %) Zerfallsreihe und Nuklidkarte Nachdem ein Radionuklid zerfallen ist, muss das entstandene Tochternuklid nicht zwingend stabil sein, sondern kann ebenfalls instabil sein. Zerfällt auch das Tochternuklid, wandelt sich der Kern in das sogenannte Enkelnuklid um. Ist dieses ebenfalls radioaktiv, folgt das Urenkelnuklid usw. bis schließlich nach mehreren radioaktiven Zerfällen ein stabiles Endnuklid erreicht wird. Je nach Radionuklid kann sich die Zerfallsreihe durch ein Dutzend oder mehr Zerfallsprodukte ziehen. 94 Zerfallsreihe von Uran-238 92 90 88 86 84 82 80 78 76 Pb-206 Po-210 Bi-211 Pb-210 Po-214 Bi-214 Pb-214 Po-218 Rn-222 Ra-226 Th-230 U-234 Pa-234 Th-234 U-238 31 Die Zerfallsreihe von Uran-238: Das Diagramm wird von oben rechts nach unten links gelesen. U-238 mit 92 Protonen und 146 Neutronen zerfällt zunächst unter Alphazerfall zu Th-234. Durch Betazerfall wird aus Th-234 Pa-234. Die Reihe setzt sich so lange fort, bis das stabile Nuklid Blei-206 erreicht wird. Die Zerfallsreihe eines bestimmten Nuklids lässt sich anhand der Nuklidkarte gut darstellen. Die Nuklidkarte ist ein Diagramm, das mit der entsprechenden Anzahl von Protonen und Neutronen die einzelnen Nuklide anzeigt. Jede Position entspricht einem eindeutigen Nuklid. Neben den einzelnen Nukliden zeigt es auch deren Stabilität und wahrscheinlichste Zerfallsart auf. Ganze Zerfallsreihen verschiedenster Nuklide lassen sich so auf einen Blick nachvollziehen. Je nach Zerfallsart rutscht das betroffene Nuklid auf der Nuklidkarte in eine bestimmte Richtung. D.h.: bei Alphazerfall zwei Felder nach links unten, bei Beta-Minus-Zerfall ein Feld nach links oben, bei einer Neutronenemission ein Feld nach links, bei einer Protonenemission ein Feld nach unten und bei einem Beta-Plus-Zerfall ein Feld nach rechts unten. Das Tochternuklid kann ebenfalls radioaktiv sein, weshalb sich dieser Prozess so lange fortsetzt, bis ein stabiles Nuklid erreicht ist. Die Nuklidkarte: Je nach farblicher Hinterlegung, ist eine bestimme Zerfallsart am wahrscheinlichsten. Eine detaillierte Darstellung der Nuklidkarte ist im Appendix ab Seite138 enthalten. 32 Stabilität und magische Zahlen in der Nuklidkarte Die Stabilität der einzelnen Nuklide ist abhängig vom Verhältnis an Protonen und Neutronen. Auffällig ist, dass bei leichteren Nukliden das Verhältnis zwischen diesen beiden Nukleonen etwa eins zu eins beträgt. Mit steigender Massenzahl ist bei stabilen Nukliden ein Überschuss an Neutronen im Vergleich zu den Protonen zu verzeichnen. Verfolgt man die Linie aus stabilen Nukliden von leichten Atomen zu schweren Atomen, steigt diese Linie in der Nuklidkarte zunächst um 45 Grad an. Bei schwereren Elementen verläuft diese Linie erheblich flacher. Verschiedene Faktoren bezüglich der Anzahl an Protonen und Neutronen wirken sich auf die Stabilität der Nuklide aus. Sind etwa Protonen und Neutronen beide von gerader Anzahl, sind die Nuklide allgemein eher besonders stabil. Nuklide, die eine gerade Anzahl von Protonen und eine ungerade Anzahl von Neutronen oder umgekehrt haben, sind eher im unteren Teil der Nuklidkarte stabil. Hat ein Nuklid eine ungerade Zahl sowohl an Protonen als auch an Neutronen, gilt es als nicht sehr stabil. Es gibt nur vier solcher Nuklide, die stabil sind. Neben dem Stabilitätskriterium der geraden oder ungeraden Anzahl von Protonen und Neutronen, spielen auch magische Zahlen eine Rolle. Magische Zahlen sind eine bestimmte Anzahl von Protonen oder Neutronen, bei denen das betreffende Nuklid besonders stabil ist. Die magischen Zahlen sind 2, 8, 20, 28, 50, 82 und 126. Bei magischer Protonenzahl existieren besonders viele stabile Isotope, bei magischer Neutronenzahl besonders viele stabile Isotone. Grund dafür ist der Aufbau des Atomkerns bzw. die Anordnung der Nukleonen. Es gibt nicht nur ein Schalenmodell für Elektronen, sondern auch für Nukleonen. Der Atomkern baut sich möglichst kugelsymmetrisch und damit stabil auf, wobei Protonen und Neutronen solche Positionen einnehmen, dass zwischen den Protonen die Neutronen als Abstandshalter stehen. Ist die äußerste Kernschale vollständig besetzt, ist der Atomkern in sich abgeschlossen. Jedes zusätzliche oder fehlende Proton oder Neutron würde sich auf die Kernstabilität auswirken. Nukleare Fisson (Kernspaltung) Kernspaltung ist in der Natur ein alltäglicher Vorgang und tritt sowohl in radioaktiven Elementen in der Erde, als auch durch kosmische Strahlung in der Atmosphäre auf. Grundsätzlich kann jedes beliebige Nuklid gespalten werden (außer selbstverständlich Wasserstoff-1). Schwere Atomkerne lassen sich dabei bedeutend einfacher spalten als Leichte. Außerdem wird bei der Spaltung schwerer Kerne mehr Energie freigesetzt als dafür aufgewendet werden muss (siehe Bindungsenergie und Massendefekt Seite 18 ff.). Ein Atomkern kann sich spontan selbst spalten oder durch Spallation oder Neutroneninduktion zur Fission gebracht werden. Spallation Spallation (aus dem Englischen: to spall = zersplittern/zertrümmern) beschreibt das Zerbersten eines Atomkerns in mehrere Bruchstücke und oftmals auch einzelne Neutronen unter Einwirkung kosmischer Strahlung. Hochenergetische Partikel aus der Sonne treffen nach ihrer Reise durch das Vakuum des Weltalls in der Erdatmosphäre ungebremst auf erste Materie (Luft). Die ungeheure Kraft dieser Partikel, kann die Energie eines ruhenden Atoms um das Hundertfache übertreffen. Trifft solch ein Partikel einen Atomkern, wird dieser regelrecht in seine Einzelteile zersplittert. Der Masseverlust eines solch zersplitterten Atomkerns wird durch die Abgabe von elektromagnetischer Strahlung aus- 33 Ende der Leseprobe von: Kernwaffen - Eine Einführung Stefan Erickson Hat Ihnen die Leseprobe gefallen? Das komplette Buch können Sie bestellen unter: http://epub.li/21jeUjJ