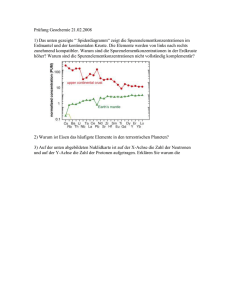
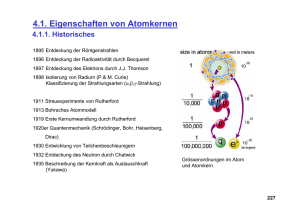
Die Deuterium-Tritium-Fusions-Reaktion wird als Quelle schneller
Werbung

Die Deuterium-Tritium-Fusions-Reaktion wird als Quelle schneller Neutronen genutzt und kann zur Energiegewinnung in einem Kernfusionsreaktor dienen. Kernfusion Wechseln zu: Navigation, Suche Die Deuterium-Tritium-Fusions-Reaktion wird als Quelle schneller Neutronen genutzt und kann zur Energiegewinnung in einem Kernfusionsreaktor dienen. vergrößern Die Deuterium-Tritium-Fusions-Reaktion wird als Quelle schneller Neutronen genutzt und kann zur Energiegewinnung in einem Kernfusionsreaktor dienen. Kernfusion bezeichnet eine Kernreaktion, bei der zwei Atomkerne zu einem schwereren Kern "verschmelzen". Grundsätzlich kann diese Reaktion exotherm oder endotherm sein; nennenswert große Wirkungsquerschnitte (Wahrscheinlichkeit, dass zwischen einem einfallenden Teilchen und einem anderen Teilchen eine bestimmte Wechselwirkung stattfindet) gibt es nur bei exothermen Fusionsreaktionen. Die Fusion setzt voraus, dass die Coulombsche Abstoßung der beiden Kerne (wegen der gleichartigen Ladung ihrer Protonen) überwunden wird. Dafür ist Energie notwendig (Bewegungsenergie der Kerne, welche sich in Druck äußert (siehe Luftdruck)). Die Kernfusion, als energetische Kettenreaktion zur Energiegewinnung in Fusionsreaktoren, kommt deshalb nur in einem Plasma mit hoher Temperatur und hohem Druck zu Stande (siehe Gastheorie). Wenn ein bestimmter Mindestabstand der Atomkerne unterschritten wird (10 − 15 m), bringt die anziehende starke Wechselwirkung durch den Tunneleffekt die Kerne zum Verschmelzen. Die freiwerdende Energie tritt als Bewegungsenergie der Reaktionsprodukte (s. Bild) auf, bei manchen Reaktionen zusätzlich auch in Form von Gammastrahlung. __ __ __ __ __ __ __ Energiebilanz Die Energietönung ist durch die Einsteinsche Masse-Energie-Äquivalenzformel E=m·c² angegeben. Sind die bei der Fusion entstandenen Kerne/Teilchen leichter als die Ausgangskerne, wird die Massendifferenz in Form von Energie frei. Solche exothermen Fusionsreaktionen sind nur im Gebiet der leichten Kerne möglich, weil die Bindungsenergie pro Nukleon mit steigender Massenzahl bis etwa 60 zunimmt. Ein starkes lokales Maximum hat sie beim Nuklid Helium-4. Die für die Fusionsenergiegewinnung günstigsten Reaktionen (siehe Kernfusionsreaktor) erzeugen daher He-4. Im Bild oben ist die am leichtesten einzuleitende dieser Reaktionen, D + T -> 4He + n, dargestellt. [Bearbeiten] Kernfusion in Gestirnen Die Kernfusion ist die Energiequelle der Sterne, etwa unserer Sonne. Die meisten Sterne fusionieren dabei beim so genannten Wasserstoffbrennen Wasserstoff über mehrere Zwischenschritte zu Helium, die dafür nötige Temperatur liegt bei ca. 10 Millionen Kelvin. Am Ende ihrer Lebenszeit, wenn der Wasserstoff aufgebraucht ist, kommt die Energie aus der Fusion von Helium oder noch schwereren Atomkernen. Diese Fusion liefert weniger Energie und benötigt eine höhere Fusionstemperatur. Größere Sterne können mit ihrer Masse auch einen stärkeren Gravitationsdruck erzeugen, wodurch diese am Ende auch schwerere Elemente fusionieren (bis zur Massenzahl 60). Elemente mit größeren Massenzahlen können hingegen nicht mehr auf diese Weise entstehen, da die Fusion der entsprechenden Kerne endotherm ist. Sie werden vielmehr durch Neutronen- (s- und r-Prozess) und Protonenanlagerung (p-Prozess) gebildet. Reaktionen (Auswahl): * D + T -> 4He + n + 17,588 MeV (größter Wirkungsquerschnitt) * D + D -> 3He + n + 3,268 MeV * D + D -> T + p + 4,03 MeV * 3He + D -> 4He + p + 18,34 MeV In der Sonne findet u.a. die Proton-Proton-Reaktion statt, eine Folge von Reaktionen, bei der ebenfalls Helium-4 mit entsprechendem Energiegewinn entsteht. Zudem findet in der Sonne ein Kohlenstoff-katalysierter Fusionszyklus statt, der Bethe-Weizsäcker-Zyklus, der etwa 1,6% der Energie des Sonnenhaushalts ausmacht. Die für die Fusion notwendige Temperatur hängt unter anderem vom Druck ab. Da ein ähnlich starker Druck wie der Gravitationsdruck in der Sonne auf der Erde nicht erzeugt werden kann, liegt hier die für die Wasserstofffusion nötige Temperatur bei etwa 100 Millionen Kelvin. _____________ Kernreaktion Eine Kernreaktion ist ein physikalischer Prozess, bei dem durch Zusammenstoß eines Atomkerns mit einem anderen Kern oder Teilchen mindestens ein Kern in ein anderes Nuklid und/oder in freie Nukleonen umgewandelt wird. __________________________ Nuklid Ein Nuklid ist in der Kernphysik ein Atomkern, der durch eine bestimmte Anzahl von Protonen und Neutronen gekennzeichnet ist und damit die Atomart bestimmt. Nuklid bedeutet also Kernsorte. Die verschiedenen Nuklide ein und desselben chemischen Elements, mit gleicher Zahl von Protonen aber unterschiedlichen Zahlen von Neutronen, werden als Isotope dieses Elements bezeichnet. Bis zur internationalen Einführung des Begriffs Nuklid (ca. 1950) wurde „Isotop“ auch (unkorrekt und verwirrend) in der allgemeinen Bedeutung Kernsorte gebraucht. Nuklide mit gleicher Massenzahl (Anzahl an Nukleonen), aber unterschiedlicher Ladung (Ordnungszahl), heißen Isobare (gleich schwer). Isotone sind Nuklide gleicher Neutronen- aber unterschiedlicher Protonenzahl. Kernisomere sind Atome desselben Nuklids, deren Kerne sich bei gleicher Ladung und gleicher Massenzahl in einem unterschiedlichen inneren Zustand befinden. Unstabile Nuklide sind radioaktiv und werden Radionuklide genannt. In der Natur existieren rund 270 stabile und etwa 70 radioaktive Nuklide. Weit über tausend wurden künstlich erzeugt. Die bekannten Nuklide werden in so genannten Nuklidkarten dargestellt. _____________ Nukleon Als Nukleonen (latein. nucleus - der Kern) bezeichnet man jene Teilchen, aus denen Atomkerne bestehen, also Protonen und Neutronen. Sie gehören zu den Hadronen, da sie aus Quarks zusammen gesetzt sind. Im erweiterten Sinne werden auch Antiprotonen und Antineutronen als Nukleonen bezeichnet; die Kerne exotischer Atome werden im Allgemeinen jedoch nicht mehr Nukleonen genannt. Jedes Atom, mit Ausnahme des Wasserstoffs und des Helium-3-Isotops (2 Protonen, 1 Neutron), hat in seinem Kern mindestens genauso viele Neutronen wie Protonen. Je schwerer ein Kern ist, desto größer ist das Verhältnis von Neutronen zu Protonen. Nukleonen sind im eigentlichen Sinne keine Elementarteilchen, da sie eine innere Struktur aufweisen: Jedes Nukleon besteht aus drei Quarks. Proton: 2 Up Quarks + 1 Down Quark Neutron: 1 Up Quark + 2 Down Quarks _______________ Atomkern Der Atomkern besteht aus Protonen und Neutronen, die zusammen auch Nukleonen genannt werden. Er befindet sich, anschaulich gesprochen, im Zentrum des Atoms und ist etwa 100.000-mal kleiner als die Elektronenhülle, konzentriert aber in sich mehr als 99,9 % der Masse des gesamten Atoms. Die Gesamtzahl der Nukleonen im Kern heißt deshalb auch Massenzahl. Mit steigender Massenzahl nimmt allgemein die Dichte des Materials zu. Beispielsweise "wiegt" Lithium (Massenzahl 6 und 7) 0,53 g/ml, Gold (Massenzahl 197) dagegen 19,3 g/ml. Sogenannte schwere Atomkerne gehören also zu auch umgangssprachlich/technisch schweren Elementen. Neutronen besitzen keine elektrische Ladung. Protonen sind jedoch positiv geladen. Infolgedessen ist der Atomkern elektrisch positiv geladen und kann über die Coulombkraft negativ geladene Elektronen an sich binden. Da die elektrische Ladung des Elektrons bis auf das Vorzeichen gleich der Ladung des Protons ist, muss ein nach außen hin elektrisch neutrales Atom ebenso viele Elektronen in der so genannten Elektronenhülle besitzen, wie Protonen im Kern. Atome mit einer unterschiedlichen Anzahl von Protonen und Elektronen sind nach außen hin elektrisch geladen und werden Ionen genannt. Eine Atomkernsorte (Nuklid) ist durch bestimmte Zahlen von Protonen und Neutronen bestimmt. Die Zahl der Protonen heißt Ordnungszahl oder Kernladungszahl. Sie bestimmt, zu welchem Element das Atom gehört. Nuklide gleicher Ordnungszahl werden als Isotope bezeichnet. Die Zahl der Neutronen hat nur geringeren Einfluss auf die chemischen Eigenschaften des Atoms, ist aber für die Stabilität oder Instabilität (Radioaktivität) des Kerns entscheidend. Nuklide mit gleich vielen Protonen und Neutronen, aber unterschiedlichem innerem Anregungszustand werden Isomere genannt. Bezeichnet werden Nuklide mit dem chemischen Elementsymbol und der Massenzahl, wie z.B. das häufigste Kohlenstoffisotop C-12 oder das häufigste Eisenisotop Fe-56 (bei Isomeren noch mit einem Zusatz wie "i"). Noch vollständiger ist die Schreibweise mit Massenzahl und Ordnungszahl, 126C oder 5626Fe. ___________ Helium3 + Helium3 ----> Helium4 + 2 Wasserstoff Bei der Umwandlung von Wasserstoff zu Helium geht 0,7% der Gesamtmasse verloren. Dies ist der Anteil, der in Energie umgewandelt wird. Bei der Fusion von 1kg Wassersroff zu Helium bedeutet das: 10 hoch 15 Joule Eine Verbrennung der gleichen Menge ergibt nur: 10 hoch 7 Joule Das bedeutet eine Fusion ist ungefähr 100.000.000 mal ertragreicher als die einfache Verbrennung. Um Kernfusion zu ermöglichen ist eine Temperatur notwendig von mindestens 10 Milliarden Grad Celsius notwendig. Bei.Temperaturen von über 15 Miliarden Grad Celsius setzt die Fusion von Kohlenstoff, Sauerstoff, Stickstoff und anderen Elementen ein. Alle Elemente, die schwerer als Eisen sind, erzeugen bei der Fusion weniger Energie, als sie benötigen. Diese Atome können nur bei Supernovae entstehen. ___________ Als Plasma bezeichnet man ionisiertes Gas. Dieses Gas besteht zumeist ganz oder zum großen Teil aus Wasserstoff (den beiden Wasserstoff-Isotopen Trilithium und Deuterium). Es ist der Ort der Kernfusion in Sternen und unserer Sonne. ____________