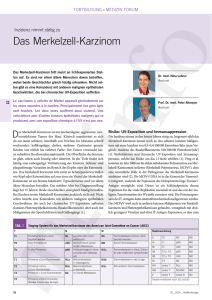
Ezrinexpression und Ezrinlokalisation in oralen
Werbung

Aus dem Zentrum für Zahn-, Mund- und Kieferheilkunde der Universität zu Köln Interdisziplinäre Poliklinik für Orale Chirurgie und Implantologie Direktor: Universitätsprofessor Dr. med. Dr. med. dent. J. E. Zöller Ezrinexpression und Ezrinlokalisation in oralen Plattenepithelkarzinomen Inaugural-Dissertation zur Erlangung der zahnärztlichen Doktorwürde der Hohen Medizinischen Fakultät der Universität zu Köln vorgelegt von Ali-Farid Safi aus Kabul/Afghanistan promoviert am 24. September 2014 Aus dem Zentrum für Zahn-, Mund- und Kieferheilkunde der Universität zu Köln Interdisziplinäre Poliklinik für Orale Chirurgie und Implantologie Direktor: Universitätsprofessor Dr. med. Dr. med. dent. J. E. Zöller Ezrinexpression und Ezrinlokalisation in oralen Plattenepithelkarzinomen Inaugural-Dissertation zur Erlangung der zahnärztlichen Doktorwürde der Hohen Medizinischen Fakultät der Universität zu Köln vorgelegt von Ali-Farid Safi aus Kabul/Afghanistan promoviert am 24. September 2014 Gedruckt mit Genehmigung der Medizinischen Fakultät der Universität zu Köln 2014 Dekan: Universitätsprofessor Dr. med. Dr. h. c. Th. Krieg 1. Berichterstatterin: Privatdozent Dr. med. Dr. med. dent. M. Kreppel 2. Berichterstatterin: Universitätsprofessor Dr. med. Dr. h.c. K.-B. Hüttenbrink Erklärung Ich erkläre hiermit, dass ich die vorliegende Dissertationsschrift ohne unzulässige Hilfe Dritter und ohne Benutzung anderer als der angegebenen Hilfsmittel angefertigt habe; die aus fremden Quellen direkt oder indirekt übernommenen Gedanken sind als solche kenntlich gemacht. Bei der Auswahl und Auswertung des Materials sowie bei der Herstellung des Manuskriptes habe ich Unterstützungsleistungen von folgenden Personen erhalten: Privatdozent Dr. med. Dr. med. dent. M. Kreppel Weitere Personen waren an der geistigen Herstellung der vorliegenden Arbeit nicht beteiligt. Insbesondere habe ich nicht die Hilfe einer Promotionsberaterin/eines Promotionsberaters in Anspruch genommen. Dritte haben von mir weder unmittelbar noch mittelbar geldwerte Leistungen für Arbeiten erhalten, die im Zusammenhang mit dem Inhalt der vorgelegten Dissertation stehen. Die Dissertationsschrift wurde von mir bisher weder im Inland noch im Ausland in gleicher oder ähnlicher Form einer anderen Prüfungsbehörde vorgelegt. Köln, den 20.03.2014 Ali-Farid Safi Die dieser Arbeit zugrunde liegenden onkologischen und funktionellen Befunde wurden ohne meine Mitarbeit im Rahmen der Tumorsprechstunde der Klinik und Poliklinik für Mund-, Kiefer- und Plastische Gesichtschirurgie der Universität zu Köln erhoben. Die Patientendaten wurden von mir persönlich erfasst und ausgewertet. Danksagung Herrn Privatdozent Dr. med. Dr. med. dent. Matthias Kreppel danke ich für die freundliche Überlasung des hochinteressanten Themas und die gute und lehrreiche Betreuung in allen Phasen der Erstellung dieser Doktorschrift. Ohne seinen kompetenten Rat, seine überaus hilfreiche Unterstützung sowie den vielen anregenden Diskussionen wäre die Erstellung dieser Dissertation nicht möglich gewesen. Den Ärzten und Schwestern der Tumorsprechstunde der Klinik und Poliklinik für Mund-, Kiefer- und Plastische Gesichtschirurgie und interdisziplinäre Poliklinik für Orale Chirurgie und Implantologie der Universität zu Köln danke ich für die akribische Dokumentation. Für meine Eltern Inhaltsverzeichnis Abkürzungsverzeichnis 1 1 Einleitung 3 1.1 Epidemiologie von oralen Plattenepithelkarzinomen 3 1.2 Ätiologie oraler Plattenepithelkarzinome 3 1.3 Präkanzeröse Läsionen 5 1.3.1 Squamous intraepithelial neoplasia (SIN) 7 1.4 Klinik der Mundhöhlenkarzinome 7 1.5 Diagnostik bei Mundhöhlenkarzinomen 8 1.6 TNM-Klassifikation und Staging 9 1.7 Karzinogenese 14 1.8 Metastasierung und molekulare Mechanismen der Metastasierung 15 1.9 Therapie des oralen Plattenepithelkarzinoms 18 1.10 Ezrin-Radixin-Moesin-Proteinfamilie 23 1.11 Zielstellung 26 2 Methodik 27 2.1 Patientenkollektiv 27 2.1.1 Auswahl des Patientenkollektivs 27 2.1.2 Auswertung und Erfassung der Daten 27 2.1.3 Erfassungsschema 28 2.1.4 Statistische Auswertung 29 2.2 Immunhistochemie 30 2.2.1 Geräte und Reagenzien 30 2.2.2 Anfertigung der Schnittpräparate 31 2.3 Semiquantitative Auswertung der Präparate 36 3 Ergebnisse 38 3.1 Epidemiologische Ergebnisse 38 3.1.1 Zusammensetzung/ Alterszusammensetzung des Patientenkollektivs 38 3.1.2 Risikofaktoren im Zusammenhang mit dem Auftreten von 40 Mundhöhlenkarzinomen 3.2 Lokalisation 41 3.3 Tumorausbreitung 42 3.3.1 T-Stadium - Ausbreitung des Tumors 42 3.3.2 N-Stadium 43 3.3.3 UICC-Stadium 45 3.4 Differenzierungsgrad 47 3.5 Resektionsränder 47 3.6 Lymphangiosis carcinomatosa 48 3.7 Ezrinexpression im Primärtumor 49 3.8 Ezrinlokalisation im Primärtumor 50 3.9 Assoziation der Ezrinexpression mit klinisch-pathologischen Parametern 51 3.10 Assoziation der Ezrinlokalisation mit klinisch-pathologischen Parametern 54 3.11 Onkologische Ergebnisse 56 3.11.1 Einfluss epidemiologischer Parameter auf das Überleben 56 3.11.2 Einfluss der Tumorausbreitung auf das Überleben 56 3.11.3 Einfluss des Tumordifferenzierungsgrades auf das Überleben 58 3.11.4 Einfluss der Lymphangiosis carcinomatosa auf das Überleben 59 3.11.5 Einfluss der Ezrinlokalisation auf das Überleben 59 3.11.6 Einfluss der Ezrinexpression auf das Überleben 60 3.11.7 Multivariate Analyse der prognostischen Faktoren 60 4 Diskussion 62 5 Zusammenfassung 69 6 Literaturverzeichnis 70 7 Anhang 82 7.1 Tabellenverzeichnis 82 7.2 Abbildungsverzeichnis 84 8 Lebenslauf 85 Abkürzungsverzeichnis: ABC- Methode - Avidin-Biotin-Enzym-Komplex-Methode AK - Antikörper AS - Aminosäure BSA - bovines Serumalbum CD - Cluster of Differentiation CT - Computertomographie DAB - 3,3’-Diaminobenzidin-Tetrahydrochlorid DNS - Desoxyribonukleinsäure DÖSAK - Deutsch-Österreichisch-Schweizerischer Arbeitskreis für Tumoren im Kiefer- und Gesichtsbereich ERM - Ezrin-Radixin-Moesin ERMAD - ERM-association-domain FERM - 4.1.-ERM GTP - Guanosin-Tri-Phosphat Gy - Gray HPV - Humanes Papillomavirus HRP - Horse-Radish-Peroxide ICAM - intracellular adhesion molecule ICD - Internationale statistische Klassifikation der Krankheiten und verwandter Gesundheitsprobleme ID-Nr. - Identifikationsnummer IgG - Immunglobulin G HIER - heat induced epitope retrieval MRT - Magnetresonanztomographie p- Wert - probability-Wert (Wahrscheinlichkeitswert) PBS - phosphate-buffered-saline PECAM1 - platelet endothelial cell adhesion PET - Positronenemissionstomographie PIP2 - Phosphatidylinositol-4,5-Bisphosphat RhoA - Ras homolog gene family member A RNS - Ribonukleinsäure 1 SIN - squamous intraepithelial neoplasia UICC - Union international contre le cancer VEGF - vascular endothelial growth factor WHO - World Health Organization 2 1 1.1 Einleitung Epidemiologie oraler Plattenepithelkarzinome Das Plattenepithelkarzinom der Mundhöhle ist der häufigste bösartige Tumor im Kopf-HalsBereich des Menschen. Die jährliche Inzidenz ist seit einigen Jahren steigend und liegt weltweit bei ungefähr 500.000 und in Deutschland bei circa 13.000 [24] [53] [149]. Die oralen Plattenepithelkarzinome stellen 5,6% aller bösartigen Tumoren dar und sind somit die sechsthäufigsten Malignome weltweit [53]. 90% der Kopf-Hals-Plattenepithelkarzinome befinden sich in der Mundhöhle und hier am häufigsten im Bereich von Zunge und Mundboden [142] [134]. 90% der Erkrankten sind über 45 Jahre alt. Männer sind etwa zwei- bis viermal häufiger als Frauen betroffen, wobei jedoch die Prävalenz bei Frauen steigend ist. Im Schnitt erkranken Männer mit 61 Jahren etwa fünf Jahre früher als Frauen [138]. Die 5-Jahres-Überlebensrate liegt bei Frauen mit 59% deutlich besser als bei den Männern mit 44%. Als Hauptgrund hierfür wird der statistisch höhere Tabak- und Alkoholkonsum der Männer gesehen [24] [134]. Die wachsende Zahl erkrankter Personen ohne Tabak-/Alkoholanamnese wird hauptsächlich durch die höhere Exposition dieser Bevölkerungsgruppe gegenüber onkogenen Humanen Papillomaviren (HPV) erklärt [89].Weltweit sterben etwa 200.000 Menschen pro Jahr an den Folgen des oralen Plattenepithelkarzinoms [149]. In Deutschland liegt die Mortalität bei knapp 5.000 pro Jahr [24]. Für alle Patienten liegt die durchschnittliche 5-Jahres-Überlebensrate bei unter 50% und ist damit geringer als beispielsweise für Kolorektal-, Zervix- oder Brustkarzinome [149]. Gründe für die geringe Überlebenswahrscheinlichkeit sind ein schlechtes Ansprechen einiger Patienten auf vorliegende Chemotherapeutika, eine späte Diagnose und ein Mangel an Tumormarkern, mit deren Hilfe die Erkrankung frühzeitig detektiert werden kann [88] [116]. 1.2 Ätiologie oraler Plattenepithelkarzinome Die Ätiologie oraler Plattenepithelkarzinome ist multifaktoriell [13]. Man unterscheidet grundsätzlich interne und externe Risikofaktoren. Die generell wichtigsten und zu der externen Gruppe gehörenden Risikofaktoren, sind der Tabak- und Alkoholkonsum. 90% der Betroffenen 3 weisen eine positive Raucheranamnese auf und es konnte nachgewiesen werden, dass Raucher gegenüber Nichtrauchern ein zwei- bis zwölffach erhöhtes Risiko haben an einem oralen Plattenepithelkarzinom zu erkranken [13-15]. Dabei ist das Risiko umso größer, je höher die Tabakmenge und die Anzahl an pack years ist [15]. Patienten, die zusätzlich zum Tabakabusus auch Alkohol konsumieren weisen aufgrund der synergistischen Effekte dieser beiden Noxen ein 15-fach erhöhtes Entartungsrisiko der Mundschleimhaut auf [24] [142] [54] [37]. Weitere bedeutende externe Risikofaktoren stellen Syphilis, physikalische Prozesse wie UV- und Röntgenstrahlen, sowie kanzerogene Chemikalien wie Formaldehyd oder beruflicher Kontakt zu Holzstäuben, insbesondere für Malignome des Nasopharynx, dar [24] [114] [15]. In Zentral- und Ostasien ist hauptsächlich neben den genannten Faktoren das Kauen der Betelnuss ein bedeutender externer Risikofaktor für die Entstehung von Plattenepithelkarzinomen im Bereich der Wangenschleimhaut [47] [117]. Als intrinsische Risikofaktoren werden Immunsuppression, der geringe Verzehr von Obst und Gemüse, eine unzureichende Mundhygiene sowie mechanische Irritationen, die zum Beispiel im Rahmen einer insuffizienten Prothese entstehen, aufgeführt [24]. Für Plattenepithelkarzinome der Lippe spielt insbesondere auch die Sonnenexposition eine wichtige Rolle [24]. 15% der oralen Plattenepithelkarzinome werden durch eine Infektion ausgelöst, insbesondere durch Humane Papillomaviren (HPV) vom Typ 16 und 18 [89]. HPV- Infektionen stellen die häufigste sexuell übertragbare Infektion dar, wobei vor allem junge Frauen und Männer betroffen sind [89]. Das Vorhandensein einer oralen HPV-Infektion erhöht das Risiko für die Entwicklung eines benignen oder malignen oropharyngealen Tumors um das 14-fache. Die Prävalenz von HPVpositiven Mundhöhlenkarzinomen liegt zwischen 19% und 72% [89] [49]. Statistisch sind Patienten mit Oropharynxkarzinomen und einem positiven HPV-Nachweis jünger, praktizieren häufiger oralen Sexualverkehr, haben mehr Lebenszeit-Sexualpartner und konsumieren vermehrt Marihuana [25], . Humane Papillomaviren bestehen aus etwa 8.000 Basenpaaren und sind 52-55 nm große, unbehüllte, doppelsträngige DNS-Viren. Sie gehören zur Familie der Papilomaviridae. Als epitheliotrope Viren können sie im Rahmen einer Infektion direkte Auslöser benigner sowie maligner Entartungen sein [85]. Klinisch manifestiert sich die HPV- Infektion je nach Genotyp und Lokalisation der Infektion unterschiedlich. Die bisher etwa 180 ermittelten HPV-Genotypen werden je nach onkogenem Potential in eine Niedrig- und eine Hochrisikogruppe eingeteilt. 4 Zur Niedrigrisikogruppe zählt man die HPV-Typen 6,11,40,42,43,44,54,61,70,72 und 81. Sie manifestieren sich vorwiegend als benigne Kondylome und Papillome [16] [85]. Zur Hochrisikogruppe gehören die Stämme HPV 16, 18, 31, 32, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68, 73 und 82. Sie führen am ehesten zu malignen Entartungen, so dass in 99,7% der Zervixkarzinome mindestens einer dieser HPV-Typen nachgewiesen werden konnte [16] [85]. In 20-90% der HPV-Infektionen konnte das zur Hochrisiko-Gruppe gehörende HPV-16 nachgewiesen werden. In Deutschland liegt die Inzidenz des HPV-16 geschätzt zwischen 20% und 30% [16] [85]. HPV-positive, oropharyngeale Plattenepithelkarzinome zeigen prognostisch trotz fortgeschrittener Tumorstadien und geringerer histologischer Tumordifferenzierung eine bessere Prognose als HPV-negative Tumore [21] [137]. Ein wichtiger Grund ist, dass HPVpositive, oropharyngeale Tumore besser durch Radiotherapie mit oder ohne Chemotherapie behandelt werden können, als HPV-negative Tumore gleicher Lokalisation [137] [156]. Demnach stellt das Vorhandensein einer HPV-Infektion, insbesondere durch HPV16, einen sehr starken und unabhängigen Faktor für die Entstehung eines Plattenepithelkarzinoms der Mundhöhle dar und ermöglicht eine bessere prognostische Abschätzung der individuellen Überlebensrate [156]. Das erhöhte Risiko einer HPV-Infektion bei Menschen mit Diabetes-Typ II, ausgeprägter Immunschwäche sowie einigen seltenen Vorerkrankungen, wird als Grund aufgeführt, wieso es bei dieser Personengruppe häufiger zur Entstehung von Malignomen der Mundhöhle kommt [24]. In 10% der Fälle ist die höhere Wahrscheinlichkeit der Entstehung von Plattenepithelkarzinomen genetisch prädisponiert, da die Ausstattung mit bestimmten Karzinogen-metabolisierenden Enzymen wie Glutathion-S-Transferase oder Cytochrom P-450 und bestimmten DNS-Reparatur-Enzymen, sowie mit dem p53-Antionkogen individuell unterschiedlich ist [134] [22] [59] [93]. Wenn ein Eltern- oder ein Geschwisterteil betroffen ist, erhöht sich das Risiko um das dreifache, an einem oralen Plattenepithelkarzinom zu erkranken [36]. 1.3 Präkanzeröse Läsionen Orale Plattenepithelkarzinome gehen in 60% der Fälle aus präkanzerösen Läsionen hervor. Diese sind umschriebene Mundschleimhautläsionen mit einem erhöhten Risiko zur Ausbildung eines Plattenepithelkarzinoms [148]. 5 Leukoplakie Die World Health Organization (WHO) definiert die Leukoplakie klinisch deskriptiv als eine weiße, nicht abwischbare Mukosaläsion, die klinisch und pathologisch keiner anderen Erkrankung zugeordnet werden kann. Orale Leukoplakien kommen vor allem in der bukkalen Mundschleimhaut, in der Mundbodenregion, an der Gingiva und im Bereich des Zungenrands vor. Man unterscheidet die homogene und inhomogene Form, wobei die inhomogene mit einem 30%-igen und die homogene Form mit einem 5%-igen Entartungsrisiko einhergeht [134] [148]. Proliferative verruköse Leukoplakie Diese stellt eine Sonderform der Leukoplakie dar, da sie als direkter Vorläufer des verrukösen Karzinoms und somit des oralen Plattenepithelkarzinoms gilt. Man unterscheidet bei der Pathogenese vier Stadien: Hyperkeratose ohne Entwicklung einer epithelialen Dysplasie, verruköse Hyperplasie, verruköses Karzinom und das orale Plattenepithelkarzinom [134] [148] [107]. Erythroleukoplakie Sie zählt zu den inhomogenen Leukoplakien, da sie sich durch ein Nebeneinander von weißlichen veränderten Läsionen und roten Schleimhautarealen auszeichnet [134] [148] [107]. Erythroplakie Bei der Erythroplakie liegt eine rötliche Mundschleimhautveränderung vor, die keiner anderen Erkrankung zugeordnet werden kann. Sie kommt vor allem im Bereich des Mundbodens, am Zungenrand, im retromolaren Feld und am weichen Gaumen vor. Die Erythroplakie kann durch ein Brennen des betroffenen klinischen Areals symptomatisch werden. Die Entartungsrate liegt zwischen 80-100% [134] [25] [148]. Lichen planus Beim Lichen planus handelt es sich um eine idiopathische, chronisch-entzündliche Erkrankung der Haut, Mund- und Genitalschleimaut, die über mehrere Wochen bis Jahre persistieren kann. Am bedeutendsten ist in Mitteleuropa der orale Lichen planus, welches mit einem unter 5%igen Entartungsrisiko einhergeht [134]. 6 Weitere Erkrankungen, die mit einer erhöhten Entartungstendenz zusammenhängen sind zum Beispiel die Eisenmangelanämie, orale submuköse Fibrose, Syphilis, Xeroderma pigmentosum, Epidermolysis bullosa dystrophicans oder der Lupus erythematodes [134]. 1.3.1 Squamous intraepithelial neoplasia (SIN) 2005 führte die WHO die Klassifikation der „intraepithelialen Plattenepithelneoplasie“ (squamous intraepithelial neoplasia (SIN)) zur besseren Abschätzung des Progressionsrisikos präkanzeröser Läsionen im Kopf-Hals-Bereich ein [75] [105]. Als Neoplasie ist hier die zweifelsfrei neoplastische, das heißt nicht reaktive Epithelveränderung definiert. Ausgehend von einer morphologischen Graduierung der Architekturstörung des Plattenepithels bei erhaltener Basalmembran, unterscheidet man die drei SIN-Stufen niedrig- mittel- und hochgradig. Niedriggradig bezieht sich auf das basale Drittel, mittelgradig auf die basalen Zweidrittel und hochgradig entspricht einem Carcinoma in situ [75] [105]. Die niedrig- und mittelgradige intraepitheliale Neoplasie (SIN I und SIN II) gehen mit einem Karzinomrisiko von 11% im nächsten Jahr einher und bedürfen einer regelmäßigen Kontrolle in Abständen von drei bis sechs Monaten [75] [105]. Die hochgradige intraepitheliale Neoplasie (SIN III) geht mit einem Karzinomrisiko von 90% im nächsten Jahr einher und erfordert als klinische Konsequenz die Entfernung der Läsion [75] [105]. Auf diese Weise kann man ein Malignitätsrisiko abschätzen und somit die weitere Diagnostik oder Therapie planen. Der wichtigste Unterschied zwischen der SIN-Einteilung und den bestehenden GradingSystemen präkanzeröser Läsionen ( Epitheldysplasie, Ljubljana-Klassifikation) ist, dass die SIN III dem Carcinoma in situ entspricht und somit eine Trennung zwischen diesen nicht mehr vorgenommen wird [75] [105]. 1.4 Klinik der Mundhöhlenkarzinome Der Zeitpunkt der Diagnosestellung des oralen Plattenepithelkarzinoms ist für die Prognose und den Erfolg einer möglichen Therapie von entscheidender Bedeutung [69]. Im Frühstadium ist das klinische Bild des Karzinoms jedoch eher unauffällig, so dass die Diagnose meistens erst spät gestellt wird, woraus folglich eine schlechtere Prognose resultiert [69] [90]. Meistens 7 werden die Mundschleimhautläsionen von dem betroffenen Patienten selbst bemerkt, doch vergehen im Schnitt bis zur endgültigen Diagnose etwa sechs Monate [91]. Durch Routineuntersuchungen und gezielte präventive Maßnahmen werden lediglich 10% der Tumore diagnostiziert [90]. Grundsätzlich bedürfen solitäre orale Schwellungen, Ulzerationen und präkanzeröse Läsionen, die länger als zwei Wochen anhalten, einer Inzisions- beziehungsweise Exzisionsbiopsie, die histopathologisch auf Malignität abgeklärt werden muss [90] . Weiterhin bedürfen nichtheilende Alveolen, nicht erklärbare Hyp-/Par-/Anästhesien und nicht-erklärbare Zahnverluste einer histopathologischen Untersuchung [90]. Karzinome werden meistens erst ab einer Größe von 2 cm symptomatisch. Häufigste Beschwerden sind Schmerzen, Schwellungen und Ulzerationen. Jedoch manifestieren sich orale Plattenepithelkarzinome je nach Lokalisation klinisch unterschiedlich. Je weiter posterior und kaudal der Tumor liegt, desto schlechter ist die Prognose [142] [134]. Bei Zungenkarzinomen sind die Schmerzen in 44% der Fälle das erste Symptom. Malignome im Bereich der Alveolarfortsätze können zu einer therapierefraktären Parodontitis oder einer nicht mehr passenden Prothese führen. Das erste Symptom eines oropharyngealen Karzinoms ist in 50% der Fälle ein Kratzgefühl im Hals [97]. In 6% der Fälle ist das erste Symptom von oralen Malignomen eine Schwellung der Halslymphknoten [124] [15]. 1.5 Diagnostik bei Mundhöhlenkarzinomen Die Anamnese und die klinische Untersuchung sind essentiell für die Diagnostik eines oralen Plattenepithelkarzinoms. Die Anamnese sollte vor allem die wichtigsten Risikofaktoren, also Tabak- und Alkoholkonsum berücksichtigen und die Nahrungsgewohnheiten erfassen. Systemische Erkrankungen spielen ebenfalls eine gesonderte Rolle. Eine körperliche Untersuchung mit Schwerpunkt auf die Inspektion, Palpation und Funktionsüberprüfung des Kopf-Hals-Bereiches sind notwendig und ermöglichen eine erste Einschätzung des Tumorgeschehens [44]. Bei Verdacht auf ein orales Plattenepithelkarzinom ist ein Staging notwendig. Für die Festlegung der lokalen Ausdehnung sollte ein CT oder MRT durchgeführt werden [56] [79] [95]. Ein PET-CT hat für die Primärdiagnostik der lokalen Ausdehnung eines bekannten oralen Plattenepithelkarzinoms keinen Stellenwert, da keine verbesserte Aussagekraft gegenüber 8 einem CT oder MRT ermittelt werden konnte [70] [135] [161]. Zur Feststellung der NKategorie wird die gesamte Region von der Schädelbasis bis zur oberen Thoraxapertur mittels CT oder MRT untersucht. Eine Ultraschall gestützte Feinnadelbiopsie sowie ein Fludeoxyglucose-PET-CT können die diagnostische Spezifität beziehungweise Sensitivität des Lymphknotenstagings steigern [1] [141]. Ein pulmonaler Tumorbefall bei Patienten mit oralem Plattenepithelkarzinom ab dem UICC-Stadium III wird durch ein Thorax-CT untersucht [3] [38] [122] [128]. Liegt der Verdacht auf ein Tumorrezidiv im Kopf-Hals-Bereich vor und konnte dieser nicht mit CT und/oder MRT bestätigt werden, so wird ein PET-CT durchgeführt [77] [82] [104]. Erst im Anschluss an die bildgebende Diagnostik, wird eine Biopsie und eine histopathologische Untersuchung durchgeführt. Auf diese Weise kann einerseits eine reaktive Lymphknotenschwellung, die zu einer fehlerhaften Einschätzung des Lymphknotenbefalls führen kann, verhindert und andererseits können Verfälschungen des Kontrastmittelverhaltens am Primärtumor vermieden werden [5] [35] [140] [154]. Üblicherweise wird eine Inzisionsbiopsie mit einem Resektionsabstand von 10 mm vom tastbaren Tumorrand durchgeführt. Bei der Biopsie wird eine repräsentative Probeentnahme aus der Progressionszone, also dem Randbereich des Tumors, entnommen [5] [35] [140] [154]. Ein positiver histologischer Tumornachweis ist Voraussetzung für das Einleiten einer tumorspezifischen Therapie [5] [35] [140] [154]. Im Rahmen einer präoperativen Diagnostik sollte auch eine zahnärztliche Untersuchung erfolgen und insbesondere vor dem Hintergrund der Prävention einer Osteoradionekrose des Kieferknochens eine zahnärztliche Sanierung stattfinden [41]. 1.6 TNM-Klassifikation und Staging Die TNM- Klassifikation wird von der Union International Contre le Cancer (UICC) herausgegeben und regelmäßig bezüglich ihrer prognostischen Relevanz und einfachen Anwendbarkeit überprüft und überarbeitet. Basierend auf der anatomischen Ausbreitung des Malignoms, wird dieses im TNM-System eingestuft. Die Klassifikation berücksichtigt die Tumorgröße (T), die Ausdehnung der regionären Lymphknotenmetastasierung (N) und das Vorliegen von Fernmetastasen (M). Die Daten dieser Dissertation basieren auf der 7. Auflage der TNM-Klassifikation der UICC vom Jahre 2010. 9 Übersicht über die ICD-Klassifikation der Mundhöhlenkarzinome Anatomische Bezirke und Unterbezirke der Mundhöhle. In Klammern sind die Bezeichnungen der Internationalen Klassifikation der Krankheiten und Todesursachen (ICD 10) enthalten [158]. 1. Mundschleimhaut - Schleimhaut der Ober- und Unterlippe (C00.3,4) - Wangenschleimhaut (C06.0) - Retromolargegend (C06.2) - Sulcus buccomandibularis und -maxillaris (C06.1) 2. Oberer Alveolarfortsatz und Gingiva (C03.0) 3. Unterer Alveolarfortsatz und Gingiva (C03.1) 4. Harter Gaumen (C05.0) 5. Zunge 6. - Zungenrücken und Vorderrand der Papillae vallatae (vordere 2/3) (C02.0,1) - Zungenunterseite (C02.2) Mundboden (C04) Abbildung 1 Abbildung 1: Anatomische Bezirke [158] 10 Tabelle 1 TNM-Klassifikation T Primärtumor Tx Primärtumor kann nicht beurteilt werden T0 Kein Anhalt für Primärtumor Tis Carcinoma in situ T1 Tumor 2 cm oder weniger in größter Ausdehnung T2 Tumor mehr als 2 cm, aber nicht mehr als 4 cm in größter Ausdehnung T3 Tumor mehr als 4 cm in größter Ausdehnung T4a Lippe: Tumor infiltriert durch kortikalen Knochen, den Nervus alveolaris inferior, in Mundhöhlenboden oder in die Haut (Kinn oder Gesichtshaut) Mundhöhle: Tumor infiltriert durch kortikalen Knochen in äußere Muskulatur der Zunge (Musculus genioglossus, Musculus hyoglossus, Musculus palatoglossus und Musculus styloglossus), Kieferhöhle oder Gesichtshaut T4b Lippe und Mundhöhle: Tumor infiltriert Spatium masticatorium, Processus pterygoideus oder Schädelbasis oder umschließt die Arteria carotis interna N Regionale Lymphknoten Nx Regionäre Lymphknoten können nicht beurteilt werden N0 Keine regionären Lymphknotenmetastasen N1 Metastase(n) in solitärem ipsilateralem Lymphknoten, 3 cm oder weniger in größter Ausdehnung N2a Metastase(n) in solitärem ipsilateralem Lymphknoten, mehr als 3 cm, aber nicht mehr als 6 cm in größter Ausdehnung N2b Metastasen in multiplen ipsilateralem Lymphknoten, keiner mehr als 6 cm in größter Ausdehnung N2c Metastasen in bilateralen oder kontralateralen Lymphknoten, keiner mehr als 6 cm in größter Ausdehnung N3 Metastase(n) in Lymphknoten, mehr als 6 cm in größter Ausdehnung M Fernmetastasen Mx Fermetastasen können nicht beurteilt werden M1 Keine Fernmetastasen M2 Fernmetastasen Tabelle 1: TNM-Klassifikation der siebten Auflage 11 Ein vorangestelltes „c“ besagt, dass es sich um eine prätherapeutische klinische TNMKlassifikation handelt und ein „p“ steht für eine postoperative, histopathologische TNMKlassifikation [158]. Ausgehend von der cTNM-Klassifikation kann man die Tumore einem entsprechenden Stadium zuordnen, so dass die Wahl und Beurteilung von Therapiemethoden erleichtert wird. Mithilfe des postoperativ bestimmten pTNM-Stagings lässt sich eine genauere Prognose treffen und beurteilen, inwiefern eine adjuvante Radio- und/oder Chemotherapie notwendig ist [158]. Die TNM-Klassifikation wird aus Gründen der besseren und einfacheren Übersicht in eine UICC- Stadiengruppierung eingeteilt. Man unterscheidet UICC I, II, III, IV A, B und C. Tabelle 2 Stadiengruppierung für Karzinome der Lippen und Mundhöhle Stadium 0 Tis N0 M0 Stadium I T1 N0 M0 Stadium II T2 N0 M0 Stadium III T1, T2 N1 M0 T3 N0 M0 Stadium IVA T1,T2,T3 N2 M0 T4a Stadium IVB Jedes T T4b Stadium IVC Jedes T N0,N1,N2 M0 N3 M0 Jedes N M0 Jedes N M1 Tabelle 2: Stadiengruppierung für Karzinome der Lippen und Mundhöhle der siebten Auflage Weitere wichtige Staging-Prozeduren, die eine bessere Prognose ermöglichen, sind das Grading und die Residualtumor-Klassifikation [158]. 12 Tabelle 3 Histopathologisches Grading Gx Differenzierungsgrad kann nicht bestimmt werden G1 Gut differenziert G2 Mäßig differenziert G3 Schlecht differenziert G4 Undifferenziert Tabelle 3: Histopathologisches Grading der siebten Auflage Das histopathologische Grading bezieht sich auf histologische und zytologische Kriterien, zu denen Kernatypien, Mitosezahl pro 10 definierte Gesichtsfelder und der Differenzierungsgrad gehören . Tabelle 4 Definitionen des C-Faktors C1 klinische Untersuchung C2 Zuhilfenahme spezieller diagnostischer Mittel C3 Chirurgische Exploration unter Einbeziehung von Biopsie und Zytologie C4 Nach erfolgter chirurgischer Behandlung einschließlich der vollständigen histopathologischen Untersuchung des Resektionspräparates C5 Autopsie Tabelle 4: Definitionen des C-Faktors der siebten Auflage Residualtumor-(R)-Klassifikation Das Vorliegen oder Fehlen von Residualtumoren nach der Therapie ist wesentlich für das weitere therapeutische Vorgehen und ermöglicht eine zuverlässigere Aussage bezüglich der Prognose . 13 Tabelle 5 Definitionen der R-Klassifikation RX Vorhandensein von Residualtumor kann nicht beurteilt werden R0 Kein Residualtumor R1 Mikroskopischer Residualtumor R2 Makrospischer Residualtumor Tabelle 5: Definitionen der R-Klassifikation der siebten Auflage 1.7 Karzinogenese Es wird vermutet, dass entweder transformierte Stammzellen des Stratum basale oder transformierte Zellen, welche die Fähigkeit der unkontrollierten Zellteilung erlangt haben, Ausgangspunkt für die Entstehung von oralen Plattenepithelkarzinomen sind [102]. Die DNS der betroffenen Zellen mutiert entweder spontan oder unter Einfluß bestimmter exogener kanzerogener Faktoren, die chemischer, physikalischer oder mikrobieller Art sind [134]. Das Zusammenspiel der im Folgenden beschriebenen Eigenschaften führt dann zur Transfomation einer normalen Zelle in eine maligne Tumorzelle. Die Tumorzellen erlangen Autonomie gegenüber exogenen wachstumsfördernden und wachstumshemmenden Signalen, indem sie ihr Wachstum autonom regulieren und sich somit ungehemmt proliferieren können [63]. Durch Produktion eigener Wachstumsfaktoren werden die Tumorzellen unabhängig von wachstumsfördernden Signalen. Wachstumshemmende Faktoren werden inaktiviert, indem es zur Überexpression von Cyclin D, Mutation von CDK4 oder Verlust der Tumorsuppressorgene p16 oder p53 (Angriffspunkt für Tabak, HPV 16 und 18) kommt. Auf diese Weise umgehen Tumorzellen auch die Apoptose [134] [63]. Mittels verstärkter Aktivierung der Telomerase findet die Immortalisierung der Tumorzellen statt [143]. Sie produzieren spezifische Faktoren, wie VEGF (vascular endothelial growth factor), welche die normalerweise ruhenden Endothelzellen aktivieren können und eine verstärkte Angiogenese induzieren, um den erhöhten Nährstoff- und Sauerstoffbedarf zu kompensieren [43]. Durch Verlust von zum Beispiel E-Cadherin wird die Zell-Zell-Kopplung aufgelöst und die Tumorzellen können ihre Motilität erhöhen. Weiterhin erlangen sie die Fähigkeit zum Durchdringen der Basalmembran, so dass sie metastasieren können [43]. Neuere Studien belegen das Vorhandensein von sogenannten Tumorstammzellen, die zwar eine relativ kleine Subpopulation von Zellen innerhalb von Malignomen darstellen, aber notwendig 14 für die Tumorentstehung sind [102]. Es wird vermutet, dass ihr Überleben während einer Chemo- und Radiotherapie, trotz der Beseitigung des Großteils des Tumors, der wesentliche Grund für das Weiterbestehen des Tumors ist [102]. 1.8 Metastasierung und molekulare Mechanismen der Metastasierung 90% der Patienten, die an einem Malignom erkrankt sind, sterben an den Folgen der Metastasierung [139]. Von einer Metastase spricht man in der Onkologie, wenn sich ein Tumorgewebsverband in einem vom Primärtumor entfernten Organ ausgebildet hat [150] Orale Plattenepithelkarzinome metastasiseren in erster Linie lymphogen [134]. Die Prävalenz regionärer Lymphknotenmetastasen wird beim oralen Plattenepithelkarzinom mit 52% bis 82% angegeben [25] [71] [26]. Der Zugang zum Blutgefäßsystem kann entweder primär durch direkten Einbruch der Tumorzellen in ein Blutgefäß oder durch Verschleppung über den Ductus thoracicus oder den rechten Lymphgang in das venöse System stattfinden. In diesem Falle spricht man von Fernmetastasen [150]. In Tumoren und auch Präkanzerosen ist die Menge an angiogen wirksamen Molekülen, wie zum Beispiel VEGF (vascular endothelial growth factor) signifikant erhöht, so dass die Wahrscheinlichkeit der Invasion von Tumorzellen in das Blutgefäßsystem erhöht wird [33]. Abhängig von der Tumorgröße und Lokalisation metastasieren orale Malignome in unterschiedliche Lymphknotengruppen [123]. Mundbodenkarzinome metastasieren meistens in die submandibulären, in die oberen und mittleren jugulären und seltener in die submentalen Lymphknoten. Anteriore Mundbodenkarzinome metastasieren häufig zusätzlich kontralateral, da die Lymphgefäße im Bereich des anterioren Mundbodens kreuzen. Karzinome der Zungenspitze metastasieren ebenfalls oft in kontralaterale submentale und juguläre Lymphknoten. Malignome, die sich im Bereich der Zungenmitte befinden, metastasieren in die unteren jugulären Lymphknoten. Zungengrundtumore metastasieren meistens in submandibuläre und obere juguläre Lymphknoten. Karzinome der Wangenschleimhaut metastasieren in die parotidealen, submandibulären sowie oberen und mittleren jugulären Lymphknoten [123]. Am häufigsten sind Hypopharynx, Epipharynx, Tonsille, Zungengrund, Zunge, Unterkiefer, Mundboden, Wange, weicher Gaumen, Oberkiefer, Nasennebenhöhlen und die Lippen betroffen. Generell konnte nachgewiesen werden, dass Karzinome aus anterioren Regionen der mastikatorischen Schleimhaut seltener metastasieren als Karzinome aus posterioren Regionen der auskleidenden Mundschleimhaut [126] [127]. 15 Das Committee for Neck Dissection Classification der American Head and Neck Society verfasste eine überarbeitete Version der Halslymphknoteneinteilung [121]. Abbildung 2 Abbildung 2: Einteilung der Lymphknotengruppen [126] Level Ia Submentale Lymphknotengruppe Level Ib Submandibuläre Lymphknotengruppe Level IIa und IIb Tiefe kraniojuguläre Lymphknotengruppe Level III Tiefe mediojuguläre Lymphknotengruppe Level IV Tiefe kaudojuguläre Lymphknotengruppe Level V Lymphknotengruppe des posterioren Halsdreiecks Level VI Lymknotengruppe des anterioren Kompartiments (prätracheale, perithyroidale und präcricoidale Lymphknotengruppe) [126] 16 In dieser Einteilung sind jedoch nicht die retroaurikulären, die subokzipitalen, die parotidealen und die oropharyngealen Lymphknoten berücksichtigt. Fernmetastasen werden bei etwa 10-20% der Patienten diagnostiziert. Sie befinden sich am häufigsten in der Lunge, in den mediastinalen Lymphknoten, der Leber und im Knochenmark [106]. Fernmetastasen gehen mit einer schlechten Überlebensprognose einher [123] [130]. Bei 10% der Patienten mit oralen Plattenepithelkarzinomen liegen schon zum Zeitpunkt der Erstdiagnose Fernmetastasen vor. Weitere 10% entwickeln im weiteren Verlauf ihrer Erkrankung Fernmetastasen [159]. An einem zweiten malignen Tumor leiden 10-15% der Patienten mit Mundhöhlenkarzinomen. Diese kommen meistens in der Mundhöhle, im Pharynx und in der Lunge vor [68] [17] [55]. Hierbei ist es für die weitere Therapie von essentieller Bedeutung den Zweittumor mithilfe einer Biopsie und anschließender pathohistologischer Untersuchung von einer Metastase zu unterscheiden. Das Zweitkarzinom muss auch von gesunder Schleimhaut umgeben sein [71] [46]. Die Zweittumoren werden zeitlich in die simultanen (gleichzeitige Diagnose beider Malignome), synchronen (Diagnose des Zweittumors 6 Monate nach Diagnose des Ersttumors) und metachronen Tumoren (Diagnose mehr als 6 Monate nach der Diagnose des Ersttumors) eingeteilt. Zweittumoren des oberen Aerodigestivtraktes haben eine bessere Prognose als Zweittumoren anderer Regionen [71] [46]. Molekulare Mechanismen der lymphatischen Metastasierung Orale Plattenepithelkarzinome metastasieren häufiger lymphogen als hämatogen [134]. Ein wesentlicher Grund ist, dass der Einbruch in Lymphkapillaren, welche ein offenes System darstellen, für die Tumorzellen keine Barriere darstellt [150]. Nach dem Einbruch gelangen die Tumorzellen zu den Lymphknoten. Dies erfolgt, da es einerseits einen gerichteten Flüssigkeitsstrom zu diesen gibt und andererseits, weil die Tumorzellen auf chemotaktische Signale reagieren, welche für dendritische Zellen bestimmt sind, die als antigenpräsentierende Zellen zu den T-Helfer-Zellen der Lymphknoten gelangen müssen [150]. Es konnte nachgewiesen werden, dass die Mobilisierung der dendritischen Zellen aus dem interstitiellen Gewebe in die Lymphgefäße durch den Chemokin-Rezeptor CCR7 reguliert wird. Hierfür bilden die Lymphendothelien die CCR7-Liganden CCL19 und CCL21 [18]. Auch bei Plattenepithelkarzinomen der Kopf-Hals-Region konnte eine verstärkte CCR7-Expression nachgewiesen werden. Hingegen war CCR6 herunterreguliert [18] [29]. Verstärkte CCR7- und 17 CCL21- Expressionen konnten auch auf malignen Melanomzellen, beim Plattenepithelkarzinom des Ösophagus und beim Adenokarzinom des Magens nachgewiesen werden. Diese metastasieren alle vorwiegend lymphogen [23] [92] [157]. Weiterhin konnte nachgewiesen werden, dass Tumorzellen die Lymphangiogenese stimulieren können und so die Wahrscheinlichkeit der lymphatischen Metastasierung erhöhen [18]. Dabei müssen die Tumorzellen sich an den Strömungsdruck innerhalb der Blutbahn anpassen, um sich anschließend an das Gefäßendothel zu adaptieren. Erfolgt dann eine Extravasation sowie Einnistung und Wachstum in ein fremdes Organsystem spricht man von einer Metastase, da sich ein Tumorgewebsverband in einem vom Primärtumor entfernten Organ ausgebildet hat [150] [151]. Abbildung 3 Abbildung 3: Mechanismen der lymphatischen Metastasierung [150] 1.9 Therapie des oralen Plattenepithelkarzinoms Die Therapie des oralen Plattenepithelkarzinoms fußt auf drei Säulen. Hierzu gehören die chirurgische Therapie, die Strahlentherapie und die Chemotherapie. Man kann jede Säule einzeln als Therapiemöglichkeit in Betracht ziehen oder die einzelnen drei Methoden kombinieren [136]. Sekundär basiert die Therapie auf präventiven Strategien, zu denen die Änderung des Lebensstils sowie eine Chemoprävention gehören [136]. Die Therapieentscheidung ist abhängig vom Tumortyp, Staging, Grading, dreidimensionale Ausdehnung, Allgemeinzustand des Patienten, Alter, Befall von Lymphknoten und Fernmetastasen [133]. Eine kombiniert, multimodale Therapie hat sich statistisch ab der Tumorgröße T2 als effektiv erwiesen [18] [39] [40] [45] [120] [132] [133] [72]. Vor einer Kopf-Hals-Bestrahlungstherapie 18 sollte immer eine Gebisssanierung erfolgen, da auf diese Weise das erhöhte Risiko einer Osteoradionekrose präventiv reduziert werden kann [100]. Chirurgische Therapie Von den drei Säulen der Behandlung des oralen Plattenepithelkarzinoms stellt die chirurgische Resektion immer noch die wichtigste Behandlungsmöglichkeit dar [96] [111] [124]. Sie zielt auf eine komplette en-bloc Resektion des Tumors mit allen Ausläufern und einem dreidimensionalen Sicherheitsabstand von 1 bis 1,5 cm und die radikale Entfernung der regionären Lymphknoten ab [119] [52]. Die Art des chirurgischen Vorgehens ist abhängig von tumorbezogenen (Tumorlokalisation, Tumorgröße, Infiltrationstiefe, Nähe zum Knochen, Vorbehandlungen, histologische Kriterien), patientenbezogenen (psychischer und physischer Zustand, Lebensstil) und behandlerbezogenen Faktoren (infrastrukturelle Möglichkeit interdisziplinärer Therapie, ärztliche Kompetenz etc.) [136]. Die Neck Dissection bezeichnet die operative Entfernung der Halslymphknoten mit dem Ziel der Beseitigung von klinisch apparenten und okkulten Metastasen [136]. Man unterscheidet verschiedene Formen der Neck Dissection, wobei heutzutage eher die modifizierte radikale und die selektive Form anstatt der radikalen Neck Dissection empfohlen und durchgeführt werden [136]. Die Wahl ist aber abhängig von der Lokalisation des Primärtumors sowie von der Anzahl, Größe und Lokalisation der Lymphknotenmetastasen [32]. Bei der radikalen Neck Dissection werden die Lymphknoten der Level I-V vollständig entfernt. Zusätzlich werden der Musculus sternocleidomastoideus, die Vena jugularis interna und/oder der Nervus accessorius entfernt [52]. Ein wesentlicher Nachteil der radikalen Neck Dissection ist, dass durch die Entfernung des Nervus accessorius das sogenannte „shoulder syndrom“ auftreten kann, welches mit generalisierten Schmerzen im Schultergürtel und Lähmungen des Musculus trapezius einhergeht [103]. Die modifizierte radikale (= konservative oder funktionelle) Neck Dissection beinhaltet die Entfernung der Level I-V Lymphknoten, jedoch unter Erhalt des Nervus accessorius, der Vena jugularis interna und des Musculus sternocleidomastoideus. Bei der selektiven Neck Dissection bleibt einer der Lymphknotengruppen der Level I-V erhalten. Man unterteilt die selektive Neck Dissection in eine supraomohyoidale (Level I-III), anterolaterale (Level VI), posterolaterale (Level II-V) und laterale Form (Level II-VI). Bei der elektiven Neck Dissection werden nur die Lymphknotengruppen entfernt, entlang denen der typische Metastasierungsweg des Malignoms verläuft. Bei der erweiterten Neck Dissection 19 werden zusätzlich zu den Lymphknoten der Level I-V noch weitere Lymphknoten entfernt, wie zum Beispiel retropharyngeale, postaurikuläre oder subokzipitale oder es werden weitere nichtlymphatische Strukturen, wie die Arteria carotis externa, der Nervus hypoglossus oder der Nervus vagus entfernt [119] [52] [160] [67]. Nach Robbins wird die Ausräumung der Level 1-3 als Mittel der Wahl bei oralen Karzinomen empfohlen [121]. Multimodale Therapie Eine monomodale chirurgische Resektion ist nur im Stadium T1 indiziert [133]. In fortgeschrittenen Tumorstadien ist die Wahrscheinlichkeit sehr groß, dass im Rahmen eines lokoregionären Therapieversagens restliches Tumorgewebe in situ verbleibt, welches dann weiter invasiv wachsen kann. Daher ist die multimodale Therapie ab dem Stadium T2 angezeigt [18] [39] [40] [45] [120] [132]Sie stellt eine interdisziplinäre Therapie dar, zu der die chirurgische Resektion sowie die Radio- und Chemotherapie gehören. Dabei können durch eine Radiatio insbesondere die gut durchbluteten peripheren Tumorausläufer zerstört werden, welche im Rahmen der chirurgischen Resektion in einigen Fällen nicht mit Sicherheit entfernt werden können [123]. Mithilfe der Chemotherapie konnten Bourhis und Pignon zeigen, dass die Überlebensrate der Patienten sich verlängert [7]. Eine alleinige chirurgische Resektion beziehungsweise Radiatio liefert nur eine lokale Kontrolle von weniger als 30% [7]. Eine alleinige Radiotherapie kann den Tumor nur bei weniger als 20% der Patienten vollständig zerstören [123]. Die Radiatio kann in Form einer definitiven Radiatio als alleinige Therapie, zum Beispiel im Rahmen palliativmedizinischer Behandlungen, angewendet werden oder erfolgt neoadjuvant beziehungsweise adjuvant als Teil einer multimodalen Therapie, zu der zusätzlich die chirurgische Resektion und Chemotherapie gehören. Eine alleinige Chemotherapie wird ebenfalls meistens nur in palliativen Situationen durchgeführt . Die Frage, ob zusätzlich zur chirurgischen Therapie eine neoadjuvante oder eine adjuvante Radiochemotherapie durchgeführt werden soll, wird in der Literatur kontrovers diskutiert. Die neoadjuvante Therapie ist aggressiver und nebenwirkungsreicher, so dass sie für den Patienten belastender ist. Andererseits geht sie mit einer höheren Überlebensrate einher. Gründe hierfür sind, dass die maligne entartete Region vor der chirurgischen Therapie besser durchblutet ist, wodurch die Radiotherapie besser wirken kann. Es werden mehr Tumorzellen zerstört und dadurch das Tumorzellvolumen verkleinert. Auf diese Weise ist die Wahrscheinlichkeit höher, intraoperativ das gesamte Tumorgewebe zu entfernen [25] [26] [112]. Weiterhin werden durch 20 die neoadjuvante Radiochemotherapie vitale Tumorzellen zerstört, so dass das Risiko von intraoperativen Implantationsmetastasen verringert wird. Mithilfe der neoadjuvanten Radiochemotherapie kann die Rezidivgefahr gesenkt werden [62]. Die adjuvante Radiatio geht mit weniger perioperativen Komplikationen und einer geringeren postoperativen Morbidität einher. Weiterhin ist ein genaueres Staging möglich, da intraoperativ im nicht vorbestrahlten Gewebe die Tumorausdehnung durch eine Schnellschnittdiagnostik bestimmt werden kann. Noch ein Vorteil ist, dass postoperativ durch die Bestrahlung restliches Tumorgewebe zerstört werden kann. Diesbezüglich ist jedoch zu erwähnen, dass sich im Rahmen der postoperativen Entstehung von Narbengewebe und der Minderdurchblutung des betroffenen Gewebes, eine lokale Strahlenresistenz ausbilden kann und das Risiko einer Osteoradionekrose erhöht wird [155] [162]. Der DÖSAK hat im Rahmen zweier prospektiver, multizentrischer Studien gezeigt, dass bei Patienten mit oralen und oropharyngealen T2-T4, N0-N3, M0 Plattenepithelkarzinomen die neoadjuvante multimodale Therapie im Vergleich zur monomodal chirurgischen Therapie, mit einer signifikant höheren Überlebensrate einhergeht. Daher wird in Deutschland bei Patienten mit den genannten Tumorstadien, angelehnt an das „Essener Konzept“, eine neoadjuvante, multimodale Therapie durchgeführt [100]. Kreppel et al konnten zeigen, dass eine postoperative Radiochemotherapie prognostisch günstiger ist als eine reine Radiotherapie [25] [72]. Kölner Konzept Entsprechend den Ergebnissen der genannten DÖSAK-Studien werden Mund-, Kiefer- und Plastische Gesichtschirurgie der in der Klinik für Universität zu Köln Plattenepithelkarzinome der Mundhöhle im Stadium T2-T4, N0-N3, M0 multimodal mit einer kombiniert präoperativen Radiochemotherapie behandelt. Eine postoperative Nachbestrahlung erfolgt wenn eine unvollständige Tumorresektion, ein Lymphknoten-Kapseldurchbruch, eine Lymphangiosis carcinomatosa oder eine ausgedehnte Lymphknotenmetastasierung vorliegen [27] [48]. Das Patientenkollektiv dieser Studie war primär operiert und die Bestrahlungstherapie erfolgte demnach adjuvant. Die Gesamtdosis von 60-65 Gy wurde in einer Dauer von fünf Wochen an der Klinik für Strahlentherapie der Universität zu Köln verabreicht. 21 Gleichzeitig zur Radiatio wurde Carboplatin AUC-5 als Chemotherapeutikum in der ersten und fünften Woche mit einer Tagesdosis von 70mg/m² Körperoberfläche eingesetzt, da es gegenüber Cisplatin nebenwirkungsärmer ist [27] [48]. Die chirurgische Therapie erfolgte in der Klinik für Mund-, Kiefer- und Plastische Gesichtschirurgie der Universität zu Köln. Rekonstruktion Bei kleineren Weichteildefekten erfolgen lokale Lappenplastiken wie Platysma- oder Nasolabiallappen [136]. Bei ausgedehnten Defekten erfolgt die Weichteilrekonstruktion durch beispielsweise fasziokutane mikrovaskulär anastomosierte Radialislappen. Großvolumige, tief gehende Defekte werden eher mit einem myokutanen, mikrovaskulär anastomosierten Latissimus-dorsi-Lappen oder anterolateralen Oberschenkel-Lappen gedeckt [136]. Knöcherne Defekte können zum Beispiel mit einem avaskulären freien Beckenkamm- oder Skapulatransplantat ersetzt werden [136]. Größere Defekte und schlechte Bedingungen im Bereich des Transplantatlagers sowie Teilresektionen der Mandibula erfordern ein freies mikrovaskulär anastomosiertes Knochentransplantat, zum Beispiel ein Fibulatransplantat [136]. Nachsorge Ein engmaschiger Tumor-Recall ist notwendig, da ca. 75% der Lokalrezidive beziehungsweise Metastasen in den ersten beiden Jahren nach der Primärtherapie auftreten [98]. 22 1.10 Ezrin-Radixin-Moesin Proteinfamilie Als ERM-Proteine werden Ezrin, Radixin und Moesin zusammengefasst, da sie eine hohe Übereinstimmung in ihrer Sequenz aufzeigen [34]. Sie gehören zur Superfamilie der Band 4.1 Proteine [10]. ERM-Proteine haben 2 wesentliche Funktionen. Einerseits die Verlinkung von Proteinen der Plasmamembran mit F-Aktinfilamenten des Zytoskeletts und andererseits als Bestandteil verschiedener Signaltransduktionswege [10]. ERM-Proteine sind durch diese Funktionen beteiligt an Zell-Zell-, sowie an Zell-Matrix-Interaktionen, an der Zellform, der Zelladhäsion, der Zellmotilität, der Zytokinese und der Phagozytose sowie an der Apoptose, der Karzinogenese und an der Metastasierung [6] [84]. Ezrin ist im Bereich des Zellkortex lokalisiert und wird vor allem physiologisch in intestinalen, epithelialen Mikrovilli und Parietalzellen des Magens exprimiert [16] [21] [123]. Radixin befindet sich vor allem im Bereich adhärenter Kontaktstellen und wird insbesondere in Mikrovilli von biliären Canaliculi produziert und stellt das Haupt ERM-Protein der Leber dar [10] [34] [145]. Moesin kommt vorwiegend in Endothelzellen vor und bindet das Glykosaminoglykan Heparin [85]. Strukturell bestehen ERM-Proteine aus einer N-terminalen Region, einer zentralen Alphahelikalen-Domäne und einer C-terminalen Region [34]. Die N-terminale Region wird auch als FERM-Domäne bezeichnet wird, da sie denen der Band 4.1 Proteine homolog ist. Die FERMDomäne besteht aus etwa 300 Aminosäuren und hat 3 Untereinheiten, die in einer KleeblattForm angeordnet sind. Die Subdomäne A zeigt eine Ubiquitin-Faltung. Die Subdomäne B hat die Struktur einer Co-A-Bindeprotein-Bindestelle. Die Subdomäne C ist charakterisiert durch eine Pleckstrin-Homologie [34]. Die zentrale Alpha-helikale-Domäne besteht aus etwa 200 Aminosäuren [34]. Die C-terminale Region, ca. 100 AS lang, besteht aus einem Beta-Strang und 6 helikalen Bereichen, die an die FERM-Domäne binden und diese größtenteils bedecken [34]. 23 Abbildung 4 Abbildung 4: Sequenzanalyse der ERM-Proteine [108] ERM-Proteine liegen durch intra- beziehungsweise intermolekularen Interaktionen zwischen dem N-terminalen und dem C-terminalen Ende als Homo- beziehungsweise Heterodimere im Zytoplasma, in einem inaktiven Zustand vor [10]. Vom inaktiven Zustand spricht man, wenn durch die Aneinanderlagerung der N-terminalen und C-terminalen Region, Proteinbindungsstellen für F-Aktin beziehungsweise für Membranproteine verdeckt werden [10]. Die Bindungsstellen zwischen dem N- und dem C-terminalen Ende werden auch als Nbeziehungsweise C-ERMAD (ERM association domain) bezeichnet [10]. Die Aktivierung der ERM-Proteine basiert auf 2 Schritten. Erstens auf der Bindung von Phosphatidyl-Inositol (4,5)-Bisphosphat und zweitens auf der Phosphorylierung von Threonin [34]. PIP2 bindet an die FERM-Domäne, genauer an die Lysinreste K63, K64, K253, K254, K262 und K263 [10]. Die Phosphorylierung findet bei Ezrin an Threonin 567, bei Radixin an Threonin 564 und bei Moesin an Threonin 558 statt [34]. Die Phosphorylierung führt zu einer Minderung der Affinität von C-ERMAD zu N-ERMAD, so dass die aktive Form des ERMProteins stabilisiert wird [10]. Für die Phosphorylierung sind 3 Kinasen bekannt, und zwar die Rho-Kinase, die Protein-Kinase-Alpha und die Protein-Kinase-Theta [6]. Proteine mit nur einer Transmembrandomäne (zum Beispiel CD43/44/95, ICAM-1/2/3, Syndecan-2) binden direkt an das ERM-Protein. Proteine mit multiplen TransmembranDomänen (Na+/H+ Antiporter, CFTR) hingegen werden per Adapterproteine an die ERMProteine verlinkt [6]. Zu diesen Adapterproteinen zählen EBP50/NHE-RF und E3KARP, welche 2 PDZ-Domänen für die Bindung an das Membranprotein haben und eine C-terminale Region für die Bindung an die FERM-Domäne der ERM-Proteine [10]. 24 Abbildung 5 Abbildung 5: Aktivierungs- und Funktionsmodell der ERM-Proteine [10] Neben der Verlinkungsfunktion zwischen Membranproteinen und dem Zytoskelett sind ERMProteine auch assoziiert mit zytoplasmatischen Signalmolekülen [10]. ERM-Proteine stimulieren im Rahmen eines autoregulatorischen positiven Feedback-Mechanismuses die RhoAktivität [10]. Rho-Proteine stellen eine Familie innerhalb der kleinen G-Proteine dar. Als GTPasen kommen sie in einem inaktiven, GDP-gebundenen Zustand und in einem aktiven, GTP-gebundenen Zustand vor [30]. Im aktiven Zustand des ERM-Proteins führt die Bindung von RhoGDI, einem Inhibitor der Rho-GTP-ase, an die FERM-Domäne zur Dissoziation des Rho von GDI. Damit kann Rho nun GTP binden und die Rho-Kinase aktivieren. Die RhoKinase wiederum kann dann den Threoninrest 558 eines anderen ERM-Proteins phosphorylieren, so dass das ERM-Protein wieder in einen aktiven Zustand übertreten kann [10]. Rolle des Ezrins bei der Metastasierung 2004 konnten Hunter et al zeigen, dass eine Überexpression von Ezrin für die Metastasierung von Osteosarkomen und Rhabdomyosarkomen notwendig ist [49]. Zur verstärkten Expression von Ezrin kann es zum Beispiel durch Stimulation des 25 oben genannten Hyaluronsäure- Rezeptors CD44 kommen. Daraus resultiert eine zunehmende Zellmotilität, so dass die Metastasierung erleichtert wird [87]. Die Zellmotilität wird auch dadurch verbessert, dass bei einer Ezrin-Überexpression weniger E-Cadherin produziert wird, welches ein struktureller Bestandteil von Zell-Zell-Kontakten ist [118]. Auch die Expression von Integrinen, als Bestandteile der Zell-Matrix-Kontakte, sinkt, wenn vermehrt Ezrin exprimiert wird. Da Integrine die Apoptose stimulieren, führt die erhöhte Ezrin-Expression indirekt zur Hemmung der Apoptose. Dies ist eine weitere Voraussetzung zur erfolgreichen Metastasierung eines Tumors [49]. Wie schon beschrieben hat eine verstärkte Aktivität von ERM-Proteinen einen positiven regulatorischen Feedback-Mechanismus auf die Rho-Aktivität [98]. Bei malignen Melanomen und Gallenblasenkarzinomen konnte gezeigt werden, dass eine verstärkte RhoAktivität ebenfalls mit einer erhöhten Metastasierungsrate einhergeht [49]. 1.11 Zielstellung Das Ziel der Dissertation ist die immunhistologische Untersuchung der Ezrinexpression und -lokalisation in oralen Plattenepithelkarzinomen, um einerseits zu analysieren inwiefern Korrelationen zu klinisch-pathologischen Parametern vorliegen und andererseits, um die Relevanz für die Prognose und zervikale Metastasierung zu bestimmen. 26 2 Methodik 2.1 Patientenkollektiv 2.1.1 Auswahl des Patientenkollektivs Für die retrospektive Fallstudie wurde das Untersuchungsmaterial von 80 Patienten verwendet, bei denen erstmalig ein orales Plattenepithelkarzinom im Stadium I-IV diagnostiziert wurde. Die Patienten wurden in der Klinik für Mund-, Kiefer- und Plastische Gesichtschirurgie der Universität zu Köln in der Zeit zwischen Juni 2002 bis Oktober 2005 behandelt. Patienten mit oropharyngealen Karzinomen wurden ausgeschlossen. Als Inklusionkriterien wurden die folgenden Parameter festgelegt: • Histologisch gesichertes primäres orales Plattenepithelkarzinom • pT1-pT4b • pN0-pN3 • Keine Fernmetastasen (cM0) • Kurativ operabler Tumor Als Ausschlusskriterien wurden folgende Faktoren berücksichtigt: • Metastasen von anderen Tumoren im Bereich der Mundhöhle • Rezidive von früher diagnostizierten und behandelten oralen Plattenepithelkarzinomen. • Patienten, bei denen ein palliativer Therapieansatz gewählt wurde • Als Ersttherapie durchgeführte neoadjuvante Radiochemotherapie Untersucht wurden Tumorlokalisation die und so lokale ermittelten Patienten Ausdehnung, im Bezug auf Metastasierungsverhalten, Patientendaten, onkologische Langzeitergebnisse, Ezrinexpression und -lokalisation. 2.1.2 Auswertung und Erfassung der Daten Die gesammelten Daten wurden mithilfe der in der Klinik vorliegenden Operationsbücher, Patientenkarteien, Krankenakten und archivierten histopathologischen Befunden, die auf prä27 und postoperativen Tumorbiopsien basierten, erfasst. Somit lagen die Anamnesebögen, Arztbriefe, radiologische sowie sonographische und histopathologische Befunde und die Operationsberichte der Patienten vor. Bei Patienten, die über eine längere Zeit nicht mehr zur Nachsorge erschienen, wurde das Einwohnermeldeamt kontaktiert, um bezüglich eines eventuelles Versterbens nachzufragen und somit den Nachbeobachtungszeitraum zu verlängern. Das Follow-up der Patienten lag im Durschnitt bei 42,9 Monaten. Alle Daten wurden gemäß des Datenschutzes mithilfe des PC-Programms SPSS (Version 21.0) anonymisiert erfasst. Die statistische Auswertung und die Erstellung der Grafiken wurde ebenfalls mit dem Programm SPSS (Version 21.0) vorgenommen. Die Datentabellen wurden mit Microsoft Excel (Version XP) erstellt. 2.1.3 Erfassungsschema Folgendes Schema diente der Erfassung der Patientendaten: 1. Patientennummer (ID-Nr.) 2. Geschlecht 3. Geburtsdatum 4. Datum der Erstdiagnose 5. Datum des Beginns und des Endes der Radiochemotherapie 6. Datum der Operation 7. Letzter Beobachtungszeitpunkt 8. Tod (ja/nein) 9. Todesursache 10. Ezrinexpression im Operationsresektat 11. Ezrinlokalisation im Operationsresektat 12. Lokalisation des Primärtumors 13. Lokalisation von Metastasen 14. Datum der Diagnose der Metastasen 15. Histopathologisches T-Stadium (lokale Tumorausbreitung, pT) 16. Histopathologisches N-Stadium (regionäre Metastasierung in die Lymphknoten, pN) 17. pUICC-Stadium 28 18. Histopathologischer Differenzierungsgrad des Tumors (G-Kategorie) 19. Anzahl der entfernten Lymphknoten 20. Anzahl der vom Tumor befallenen Lymphknoten 21. Anzahl der Lymphknoten mit Kapseldurchbruch des Tumors 22. Status der Tumorresektionsränder (R0, R1 oder R2) 23. Lymphangiosis carcinomatosa (ja/ nein) 24. Rezidiv (ja/nein) 25. Art des Rezidivs (Lokalrezidiv/ Lymphknotenrezidiv) 26. Datum des Rezidivs Die Patientennummer (Identifikationsnummer) diente der anonymisierten Darstellung der Patientendaten. Als Datum der Erstdiagnose diente die pathohistologische Diagnose eines oralen Plattenepithelkarzinoms. Der letzte Beobachtungszeitpunkt war entweder der Tod des Patienten, die letzte Kontrolluntersuchung oder eine entsprechende Information aus dem zuständigen Einwohnermeldeamt. Die Ezrinexpression wurde histologisch im Operationsresektat bestimmt. Das Staging erfolgte mittels klinischer Untersuchung, bildgebender Verfahren sowie pathohistologischer Untersuchung der Gewebeproben. 2.1.4 Statistische Auswertung In der statistischen Analyse wurde der Einfluss der Ezrinexpression und -lokalisation auf klinisch-pathologische Parameter untersucht. Kontinuierliche Variablen wurden dabei mithilfe des Wilcoxon-Rangsummentest ermittelt und kategoriale Variablen mittels des χ² -Tests nach Pearson und des exakten Tests nach Fischer berechnet. Die onkologischen Ergebnisse basierten auf den Parametern „Gesamtüberleben“ und „lokoregionäre Kontrolle“. Das Gesamtüberleben (englisch: overall survival) gibt den Zeitraum zwischen Beginn der Primärtherapie und dem Tod des Patienen in Monaten an. Alle Patienten, die bis zum Ende des Beobachtungszeitraums nicht gestorben waren beziehungsweise bei denen es unklar war, ob sie lebten, wurden für die Studie nicht berücksichtigt. Die lokoregionäre Kontrolle (englisch: locoregional control) bezieht sich auf den monatlichen Zeitraum zwischen dem Beginn der Primärtherapie und dem Auftreten eines Lokalrezidivs oder Metastasenrezidivs in den Halslymphknoten. Patienten, die im Beobachtungszeitraum tumorfrei gestorben waren, wurden zum Zeitpunkt des Todes zensiert. 29 Die Gesamtüberlebenszeit und die lokoregionäre Kontrolle wurden mithilfe der Kaplan-MeierMethode berechnet [57]. Dabei wurden die kumulierten Überlebensraten aufgeteilt nach Therapieregime, lokaler Tumorausbreitung, regionärem Lymphknotenbefall, UICC-Stadium, G-Kategorie des Tumors, Status der Tumorresektionsränder, Kapseldurchbruch bei Lymphknotenmetastasen, Lymphangiosis carcinomatosa, Ezrinexpression und -lokalisation. Patienten, die nicht bis zum letzten Beobachtungszeitpunkt verstorben waren, wurden zum letzten Beobachtungszeitpunkt zensiert. Die univariate Analyse wurde anhand des Log-Rank-Tests für wichtige Faktoren des Gesamtüberlebens und der lokoregionären Kontrolle durchgeführt. Das Signifikanzniveau wurde auf 5% festgelegt. Dabei wurden Alter, Geschlecht, lokale Tumorausbreitung (T- Stadium), regionäre Lymphknotenmetastasierung (N-Stadium), UICC-Stadium, Lymphangiosis carcinomatosa, Kapseldurchbruch bei Lymphknotenmetastasen, Rezidivverhalten, histopathologische Tumordifferenzierung (G-Kategorie), sowie Tabak- und Alkoholabusus berücksichtigt. Variablen, die sich in der univariaten Analyse als signifikant herausstellten, wurden in einer multivariaten Analyse durch die Regressionsanalyse nach Cox bezüglich ihres prognostischen Einflusses auf die Überlebenswahrscheinlichkeit, analysiert [20]. Stets wurde eine zweiseitige Signifikanzrechnung vorgenommen. Untersucht wurden die Parameter Alter, Geschlecht, lokale Tumorausbreitung (T-Stadium), regionäre Lymphknotenmetastasierung (NStadium), UICC-Stadium, Lymphangiosis Lymphknotenmetastasen, Rezidivverhalten, Immunhistochemie 2.2.1 Geräte und Reagenzien Kapseldurchbruch bei histopathologische Tumordifferenzierung (G- Kategorie), sowie Tabak- und Alkoholabusus. 2.2 carcinomatosa, - feuchte Kammer, Aufbewahrungsbox - Kunststoffküvette für die Mikrowelle - Kühlschrank/ Gefriertruhe - Lichtmikroskop - Mikrowelle - Schlittenmikrotom 30 - Objektträger - TechMate 500 - Wärmeschrank - ABC-System: TP-015-HD, Labvision, Fremont, CA, USA - Alkohol - Antibody-Diluent - Aqua destillata - 1%-iges BSA/PBS - Citrat- Puffer pH 6,0 - DAB - Eukit - Hämatoxylin - Mayers- Hämalaun - Normalserum (Horse) - PBS-Puffer pH 7,2 - Perhydrollösung 0,3% - Roti-Histol - Xylol - Primärer Antikörper (Katalognummer: MS-661-P0) - Sekundärer Antikörper (TP-015-HD; Labvision, Fremont, CA, USA) 2.2.2 Anfertigung der Schnittpräparate Fixierung Biopsien müssen fixiert werden, da es ansonsten zur Gewebsnekrose kommt. Mittel der Wahl ist die Fixierung in 8%-igem Formaldehyd. Die Gewebeprobe sollte innerhalb von 30 min in eine Formaldehydlösung eingebracht werden und 6-24h fixiert werden. Die Gewebeproben aus der peripheren Invasionsfront des Tumors, wurden im Institut für Pathologie der Universität zu Köln fixiert und eingebettet. Einbettungsprozess Die Einbettung dient dazu, dass das Formalin aus dem Einbettungsmedium durch Paraffin ersetzt wird und somit schneidbar gemacht wird. 31 Daher werden die fixierten Gewebeproben in einer aufsteigenden Alkoholreihenfolge (50%60%-70%-95%-100% Ethanol) entwässert. Als Intermedium zwischen hydrophoben Paraffin und 100% Ethanol dient das Xylol. Anschließend kann in einem Paraffinbad das Paraffin das Gewebe infiltrieren. Mikrotomie Mithilfe des Rotationsmikrotoms wurden aus den gekühlten eingebetteten Gewebeblöcken 3-4 µm dünne Paraffinschnitte hergestellt. Die Schnitte wurden anschließend auf die Objektträger gezogen und bei etwa 60°C über Nacht in einem Wärmeschrank angebacken, so dass das Paraffin sich verflüssigen und das Wasser abdampfen konnte. Entparaffinisierung Voraussetzung für die Färbung war, dass eine Entparaffinisierung stattfinden konnte und die Proben in ein wässriges Medium gebracht wurden. Die getrockneten Objektträger wurden daher aus dem 56-60°C warmen Brutschrank sofort für fünf Minuten in eine Xylol-Lösung gebracht und gleichmäßig bewegt. Übriggebliebenes Paraffin führt ansonsten grundsätzlich zu optischen Störflecken im Präparat. Rehydriert wurde anschließend in einer absteigenden Alkoholreihe bis zu destilliertem Wasser. Dabei wurden die Schnitte für zweimal drei Minuten in 100% Alkohol, eine Minute in 95% Alkohol, eine Minute in 70% Alkohol und anschließend für fünf Minuten in Aqua destillata gefüllte Küvetten gelegt. Generell ist das Abspülen in PBS-Tween 20 für zweimal zwei Minuten wichtig, da die später hinzugegeben Antikörper als Proteine vom pH-Wert und der Salzkonzentration abhängig sind und man daher ein optimales Reaktionsmilieu schaffen möchte. Antigen-Demaskierung Sowohl die Membranen als auch die im Rahmen der Fixierung entstandenen MolekülVernetzungen maskieren die Antigene. Damit diese jedoch für die Antikörper erreichbar gemacht werden, findet eine Antigen-Demaskierung statt. Mithilfe der HIER (heat induced epitop retrieval)- Methode kommt es durch Einwirkung von feuchter Hitze im Bereich um 100°C bei pH-Werten von 2-10 zu einer erhöhten Permeabilität des fixierten Gewebes, so dass Epitope freigelegt werden und Antikörper an diese binden 32 können. Daher wurde auf einer Heizplatte die 10 mM (Natrium-)Citrat-Pufferlösung (pH 6.0) zum Kochen gebracht und die Schnitte hierin für 20 Minuten abgedampft. Nach der Inkubation wurden die Schnitte langsam für 45 Minuten abgekühlt. Endogene Enzymaktivität Das Chromogen soll nur vom zugeführten Enzym umgesetzt werden, und so zur Farbstoffentwicklung führen. Liegt jedoch eine endogene Enzymaktivität vor, so kann es zu „falsch-positiven“ Reaktionen kommen und die Aussagekraft der Färbung stark einschränken. Daher wurde die endogene Peroxidaseaktivität durch eine Inkubation der Schnitte in 3%-igem Wasserstoffperoxid, blockiert. Immunhistochemische Färbung von Ezrin Antigene verfügen über mehrere Epitope (antigene Determinantien), die sich membranständig, nukleär oder im Zytoplasma befinden können. Ein Epitop weist eine bestimmte Aminosäuresequenz auf und hat eine typische dreidimensionale Struktur. Bei den Antikörpern der immunhistologischen Technik handelt es sich vorwiegend um solche aus der Gruppe der Gamma-Immunglobuline (IgG). Sie haben einen Fc-Teil, der zum Beispiel für die Opsonierung wichtig ist und einen variablen Fab-Teil, der für die Antigenbindung notwendig ist. Weiterhin haben Antikörper auch selber antigene Eigenschaften, so dass sie von artfremden Antikörpern als Antigene erkannt und gebunden werden können. Man unterscheidet daher den primären Antikörper, der direkt das Antigen bindet und den sekundären Antikörper, der gegen den Primärantikörper gerichtet ist und aus einer anderen Spezies stammt. Mehrere polyklonale Sekundärantikörper können an einen Primärantikörper binden und zur Verstärkung des Signals führen. Die in dieser Arbeit verwendete Methode war die des Avidin-BiotinPeroxidase-Komplexes (ABC). Das ABC-System wird vorab zusammengemischt und besteht aus Vernetzungen von Streptavidin, Biotin und konjugiertem Enzym. Biotin (Vitamin H) dient der Markierung von Antikörpern. Es hat eine hohe Affinität zu Avidin, welches ein aus dem Hühnereiweiß gewonnenes Glykoprotein ist. Das Streptavidin ist bakteriellen Ursprungs und hat eine höhere Spezifität zu Biotin als Avidin und kann mit Enzymen oder Fluorochromen markiert werden. Als konjugiertes Enzym wird die Meerrettichperoxidase (horseradish peroxidase, HRP) benutzt. Als Chromogen wird DAB (Diaminobenzidin) verwendet. Generell kann diese makromolekulare Struktur dann an den mehrfach biotinylierten Sekundärantikörper binden. Auf diese Weise kann die starke Affinität zwischen Biotin und Avidin beziehungsweise 33 Streptavidin ausgenutzt werden und eine sehr hohe Anzahl an Markern an den Ort des Antigens gebracht werden, so dass die Sensitivität der ABC-Methode prinzipiell höher ist als bei den Techniken mit unkonjugierten-AK-Methoden. Bevor die Inkubation der Gewebeschnitte mit dem primären Antikörper stattfinden konnte, mussten unspezifische Epitope blockiert werden. Dies erfolgte mithilfe von 10%-igem Pferdeserum, welches auf die Schnitte gegeben wurde und für 30 Minuten wirken konnte. Die monoklonalen primären Antikörper (MS-661-P0), 1:100.000 in PBS verdünnt, wurden hiernach auf die Schnitte geträufelt und es fand eine Inkubation über Nacht statt. Am nächsten Tag wurden die Schnitte für zweimal fünf Minuten abgespült, damit anschließend die Inkubation mit dem biotinyliertem sekundären Antikörper (TP-015-HD, Labvision, Fremont, CA, USA) für 15 Minuten stattfinden konnte. Die Detektion erfolgte mit dem Streptavidin-BiotinPeroxidase Komplex (TP-015-HD, Labvision, Fremont, CA, USA), indem dieses für 10 Minuten auf den Gewebeschnitten einwirken konnte. Das Chromogen DAB wird unter der katalytischen Wirkung von Peroxidase in eine farbige Substanz umgesetzt. Dabei ergibt DAB ein braunes Farbprodukt. Daher wurde DAB-Lösung auf die Schnitte gegeben und eine Einwirkungszeit von drei Minuten eingehalten. Vor der anschließenden Gegenfärbung wurden die Schnitte mit PBS für zweimal zwei Minuten gespült. Hiernach wurden die Schnitte für fünf Minuten in eine Küvette, gefüllt mit MayerHämatoxylin (Dako-Cytomation) gegeben, damit die Kerne in einer zum Chromogen kontrastierenden Farbe dargestellt werden konnten. Es erfolgte die anschließende Abspülung in destilliertem Wasser und das Dehydrieren in einer aufsteigenden Alkoholreihenfolge. Hierfür wurden die Schnitte für zwei Minuten jeweils in 70% und 95% Ethanol gegeben und anschließend für zweimal drei Minuten in 100% Ethanol getaucht. Das Dehydrieren ist prinzipiell notwendig, damit überschüssiger Farbstoff entfernt wird. Hiernach fand die Klärung in Xylol für zweimal fünf Minuten statt, damit das hydrophobe Xylol-lösliche Einschlussmittel auf dem Objektträger wirken konnte. Abschließend wurde das Deckglas manuell aufgebracht. Färbeprotokoll 1. Formalin-Fixierung und Herstellung der Paraffinschnitte. 2. Deparaffinisation in Xylol, zweimal fünf Minuten. 34 3. Rehydrieren in absteigender Alkohol-Reihenfolge. 100% Ethanol, zweimal drei Minuten. In 95% Ethanol, eine Minute. 70% Ethanol, eine Minute. 4. Spülen in Aqua destillata. 5. Abspülen in PBS-Tween 20 für zweimal zwei Minuten. 6. Zur Antigendemaskierung dampft man in 10 mM (Natrium-)Citrat-Puffer (pH 6.0) für 20 Minuten ab. Anschließend kühlt man für 45 Minuten ab. 7. Inkubation in 3%-igem Wasserstoffperoxid für 10 Minuten. 8. Inkubation in 10%-igem Pferdeserum für 30 Minuten bei Raumtemperatur. 9. Inkubation über Nacht mit monoklonalem primären Antikörper, welche 1:10000 in PBS verdünnt wurden (MS-661-P0). 10. Abspülen mit PBS (zweimal fünf Minuten) 11. Inkubation mit biotyniliertem sekundärem Antikörper (15 min) (TP-015-HD; Labvision, Fremont, CA, USA). 12. Detektion mit Strepavidin-Biotin-Peroxidase-Komplex (10 min) (TP-015-HD; Labvision, Fremont, CA, USA). 13. Präparate in DAB-Lösung für drei Minuten inkubieren. 14. Mit PBS zweimal zwei Minuten spülen. 15. Gegenfärbung mit Mayer- Hämatoxylin (Dako-Cytomation) für drei bis fünf Minuten. 16. Abspülen in Aqua destillata 17. Dehydrieren in aufsteigender Alkoholreiheinfolge. 70% Ethanol für zwei Minuten , 95% Ethanol für zwei Minuten, 100% Ethanol für zweimal drei Minuten. 18. Reinigung in Xylol zweimal fünf Minuten. 19. Deckglas aufbringen. Negativ- und Positivkontrollen Die Validität der Ergebnisse von immunhistochemischen Färbungen wird mittels Negativ- und Positivkontrollen nachgewiesen. Negativkontrollen sollen falsch-positive Ergebnisse ausschließen und Positivkontrollen falsch-negative Ergebnisse. In dieser Arbeit wurden bei allen Färbungen Negativkontrollen mitgeführt. Dafür wurde der primäre Antikörper durch Normalserum ersetzt, so dass bei einer positiven Färbereaktion es sich um eine unspezifische Reaktion im Rahmen einer fehlerhaften Probenvorbereitung oder der Verwendung fehlerhafter Reagenzien gehandelt hätte. 35 Positivkontrollen auf Schnitten, die das gesuchte Antigen sicher enthielten, bestätigten die Sensitivität der Antikörper und ordnungsgemäße Behandlung der Proben. 2.3 Semiquantitative Auswertung der Präparate Die Farbintensität und die Anzahl positiv gefärbter Zellen wurde mittels eines semiquantitativen Scores in Zusammenarbeit mit zwei Fachärzten für Pathologie (PD Dr. Uta Drebber, Dr. Inga Grünewald), die keine Kenntnis über klinischen Daten der Patienten hatten, bewertet. Hierbei fand eine Einstufung der beiden genannten Parameter zwischen null und drei statt (null=kein Ezrin, eins=schwache Expression, zwei=moderate Expression, drei=hohe Expression) [73]. Das Gesamtergebnis wurde errechnet, indem die Punkte für die Farbintensität und die Punkte für die Anzahl positiv gefärbter Zahlen addiert und anschließend die Summe durch zwei dividiert wurde. Wenn das Ergebnis keine glatte Zahl war, wurde abgerundet, so dass zum Beispiel 1,5 als schwache Expression eingestuft wurde. 36 Abbildung 6 Abbildung 6: Semiquantitative Auswertung der Präparate 37 3 Ergebnisse 3.1 Epidemiologische Ergebnisse Das Untersuchungsmaterial dieser retrospektiven Studie stammt von 80 Patienten, bei denen in der Klinik für Mund-, Kiefer- und Plastische Gesichtschirurgie der Universität zu Köln zwischen Oktober 2002 und Juni 2005 ein Plattenepithelkarzinom der Mundhöhle diagnostiziert wurde. 3.1.1 Zusammensetzung/ Alterszusammensetzung des Patientenkollektivs 51 (64%) der 80 Patienten waren männlich und 29 (36%) waren weiblich. Die Patienten waren im Durchschnitt 61,56 Jahre alt. Das mediane Alter lag bei 61,82 Jahren und die Standardabweichung hierzu betrug 12,036 Jahre. Insgesamt erstreckte sich die Altersspanne des Gesamtkollektivs von 30 bis 91 Jahren. Je nach Alter wurden die Patienten in sechs Gruppen eingeteilt. Mit 30% war diejenige der 51-60 Jährigen, die Gruppe mit den am meisten Erkrankten. 29% der Patienten waren zwischen 61 und 70 Jahren alt. Die Gruppe der 71-80 Jährigen machte 18% aus. 11% der Patienten waren 41-50 Jahre alt und 8% waren über 80 Jahre alt. Die verhältnismäßig kleinste Gruppe stellte diejenige der 30-40 Jährigen mit einem Anteil von 5% dar. Der Nachbeobachtungszeitraum der Patienten betrug im Durchschnitt 42,9 Monate. Tabelle 6 Altersgruppierung Alter der Patienten Häufigkeit Prozent 30 - 40 Jahre 4 5% 41 - 50 Jahre 9 11% 51 - 60 Jahre 24 30% 61 - 70 Jahre 23 29% 71 - 80 Jahre 14 18% > 80 Jahre 6 8% Tabelle 6: Altersverteilung des gesamten Patientenkollektivs (80 Patienten) bei Diagnosestellung 38 Abbildung 7 30 25 Anzahl 20 15 10 5 0 30-40 Jahre 41-50 Jahre 51-60 Jahre 61-70 Jahre 71-80 Jahre >80 Jahre Altersgruppe Abbildung 7: Altersverteilung des gesamten Patientenkollektivs (80 Patienten) bei Diagnosestellung Tabelle 7 Alter bei Erstdiagnose Durchschnittsalter 61,56 Medianes Alter 61,82 Standardabweichung 12,036 Minimum 30 Maximum 91 Tabelle 7: Statistische Altersangaben des gesamten Patientenkollektivs (80 Patienten) bei Erstdiagnose 39 3.1.2 Risikofaktoren im Zusammenhang mit dem Auftreten von Mundhöhlenkarzinomen Tabakabusus gaben 63 (79%) der erkrankten Patienten an. Alkohol konsumierten 53 (66%). Tabelle 8 Tabakabusus Häufigkeit Prozent nein 17 21% ja 63 79% Häufigkeit Prozent nein 27 34% ja 53 66% Alkoholabusus Tabelle 8: Prozentuale Verteilung der Risikofaktoren im Gesamtkollektiv Abbildung 8 Tabakabusus 21% nein ja 79% Abbildung 8: Tabakabusus des Gesamtkollektivs 40 Abbildung 9 Alkoholabusus nein 49% 51% ja Abbildung 9: Alkoholabusus des Gesamtkollektivs 3.2 Lokalisation Am häufigsten, und zwar bei 35 (44%) der Patienten, befand sich das orale Plattenepithelkarzinom im Bereich des Mundbodens. 18 (23%) Patienten waren am Plattenepithelkarzinom der Zunge erkrankt. In der Unterkieferregion lag bei 14 (18%) Patienten eine maligne Entartung vor und die Wange war bei acht (10%) Patienten betroffen. Am seltensten, und zwar bei fünf (6%) Patienten wurde das Plattenepithelkarzinom im Bereich des Oberkiefers beziehungsweise des harten Gaumens diagnostiziert. Tabelle 9 Lokalisation Häufigkeit Prozent Mundboden 35 44% Zunge 18 23% Unterkiefer 14 18% Oberkiefer/harter Gaumen 5 6% Wange 8 10% Tabelle 9: Lokalisation des Primärtumors 41 Plattenepithelkarzinome der Lippen wurden in dieser Studie nicht berücksichtigt, da sie eine signifikant bessere Prognose aufweisen und daher einer eigenen Tumorentität zugerechnet werden. Prozent Abbildung 10 50 45 40 35 30 25 20 15 10 5 0 Mundboden Zunge Unterkiefer Oberkiefer/harter Gaumen Wange Lokalisation Abbildung 10: Lokalisation des Primärtumors des Gesamtkollektivs 3.3 Tumorausbreitung 3.3.1 T-Stadium - Ausbreitung des Primärtumors Am häufigsten fand sich ein Primärtumor der Kategorie T2 (27%). Bei 30 (24%) Patienten wurde die Tumorgröße in die T1-Gruppe eingestuft. Ähnlich viele Malignome gehörten zur Gruppe T4, wobei 15 (19%) als T4a und acht (10%) als T4b klassifiziert wurden. Sechs (8%) Patienten wiesen einen Tumor im T3-Stadium auf. 42 Tabelle 10 T-Klassifikation Häufigkeit Prozent T1 24 30% T2 27 34% T3 6 8% T4a 15 19% T4b 8 10% Tabelle 10: T-Stadium des Primärtumors Abbildung 11 T-­‐Klassi(ikation 10% T1 30% T2 19% T3 T4a 8% T4b 33% Abbildung 11: Prozentuale Verteilung des T-Stadiums im Gesamtkollektiv 3.3.2 N-Stadium Bei 49 (61%) Patienten wurden keine regionären Lymphknotenmetastasen (N0) nachgewiesen. Bei 22 (28%) Patienten lag die Lymphknotenmetastasierung im N2- Stadium und bei neun (11%) Patienten im N1-Stadium vor. 43 Tabelle 11 N-Klassifikation Häufigkeit Prozent N0 49 61% N1 9 11% N2 22 28% Tabelle 11: N-Stadium des Primärtumors Abbildung 12 70 60 Prozent 50 40 30 20 10 0 N0 N1 N2 N-Klassifikation Abbildung 12: Prozentuale Verteilung des N-Stadiums am Gesamtkollektiv Ein Durchbruch der Lymphknotenkapsel konnte in 84% der Fälle nachgewiesen werden. Bei 16% der Patienten lag kein Durchbruch vor. 44 Tabelle 12 Kapseldurchbruch Häufigkeit Prozent nein 67 84% ja 13 16% Häufigkeit Prozent 0 67 84% 1 9 11% 2 3 4% 3 1 1% Anzahl der Kapseldurchbrüche Tabelle 12: Anzahl der Kapseldurchbrüche des Tumors Abbildung 13 Anzahl der Kapseldurchbrüche 4% 1% 1 11% 2 3 84% 4 Abbildung 13: Prozentuale Verteilung der Anzahl der Kapseldurchbrüche im Gesamtkollektiv 3.3.3 UICC-Stadium In der UICC-Klassifikation wurden die meisten Tumoren, und zwar 36 (45%) ins Stadium IV eingestuft, gefolgt vom Stadium I, mit 23 (28,7%). Im Stadium II lagen 13 (16,5%) Tumoren vor und ins Stadium III wurden acht (10%) Tumore eingestuft. 45 Tabelle 13 UICC-Stadium Häufigkeit Prozent I 23 28,7% II 13 16,3% III 8 10% IV 36 45% Tabelle 13: Häufigkeits- und prozentuale Verteilung des UICC-Stadiums Abbildung 14 UICC-­‐Stadium 29% I 45% II III IV 16% 10% Abbildung 14: Prozentuale Verteilung des UICC-Stadiums am Gesamtkollektiv 46 3.4 Differenzierungsgrad Das histopathologische Grading ergab bei 78% der Patienten eine mäßige (G2), bei 16% eine schlechte (G3) und bei 6% eine hohe Differenzierung (G1) des Tumors. Tabelle 14 G-Kategorie Häufigkeit Prozent G1 5 6% G2 62 78% G3 13 16% Tabelle 14: Häufigkeits- und prozentuale Verteilung der Differenzierungsgrade der Tumoren des Gesamtkollektivs Abbildung 15 90 80 70 Prozent 60 50 40 30 20 10 0 G1 G2 G3 Differenzierungsgrad Abbildung 15: Prozentuale Verteliung des Differenzierungsgrades im Gesamtkollektiv 3.5 Resektionsränder In 81% der Fälle konnte die chirurgische Tumorbehandlung im Gesunden durchgeführt werden. In 19% der Fälle ergab der histopathologische Befund, dass ein mikroskopischer Resttumor in situ vorlag. 47 Tabelle 15 Resektionsränder Häufigkeit Prozent R0 65 81% R1 15 19% Tabelle 15: Tumorresektionsränder des Gesamtkollektivs Abbildung 16 Resektionsränder 19% R0 R1 81% Abbildung 16: Prozentuale Verteilung der Tumorresektionsränder im Gesamtkollektiv 3.6 Lymphangiosis carcinomatosa Eine Lymphangiosis carcinomatosa konnte in 15% der Fälle nachgewiesen werden. Bei den restlichen 85% konnte kein Durchbruch in die Lymphgefäße diagnostiziert werden. Tabelle 16 Lymphangiosis Häufigkeit Prozent nein 68 85% ja 12 15% carcinomatosa Tabelle 16: Vorkommen von Lymphangiosis carcinomatosa 48 Abbildung 17 Lymphangiosis carcinomatosa 15% nein ja 85% Abbildung 17: Prozentuale Verteilung des Vorhandenseins der Lymphangiosis carcinomatosa im Gesamtkollektiv 3.7 Ezrinexpression im Primärtumor Histologisch war die Ezrinexpression im Primärtumor bei 28 (35%) Patienten stark. Nahezu genauso viele Patienten, und zwar 27 (34%), zeigten eine moderate Ezrinexpression im Tumor. 21 (26%) Biopsien wiesen eine schwache und nur vier (5%) eine negative Ezrinexpression auf. Tabelle 17 Ezrinexpression Häufigkeit Prozent negativ 4 5% schwach 21 26% moderate 28 35% stark 27 34% Tabelle 17: Ezrinexpression im Primärtumor 49 Abbildung 18 Ezrinexpression im Primärtumor 5% 34% negativ 26% schwach moderate stark 35% Abbildung 18: Prozentuale Verteilung der Ezrinexpression des Primärtumors im Gesamtkollektiv 3.8 Ezrinlokalisation im Primärtumor In 34% der Fälle konnte Ezrin sowohl membranär als auch zytoplasmatisch nachgewiesen werden. In 31% lag Ezrin ausschließlich zytoplasmatisch und in 30% nur membranär vor. In lediglich 5% der Proben konnte keine Ezrinexpression histologisch ermittelt werden. Tabelle 18 Ezrinlokalisation Häufigkeit Prozent negativ 4 5% membranär 24 30% gemischt 27 34% zytoplasmatisch 25 31% Tabelle 18: Ezrinlokalisation im Primärtumor 50 Abbildung 19 Ezrinlokalisation im Primärtumor 5% 31% negativ 30% membranär gemischt zytoplasmatisch 34% Abbildung 19: Prozentuale Verteilung der Ezrinlokalisation des Primärtumors im Gesamtkollektiv 3.9 Assoziation der Ezrinexpression mit klinisch-pathologischen Parametern Im χ²-Test konnte eine signifikante Korrelation zwischen der Ezrinexpression und der NKlassifikation (p= 0,009) gezeigt werden. Je stärker die Ezrinexpression war, desto eher konnten regionäre Lymphknotenmetastasen festgestellt werden. Während bei starkem Expressionsmuster 17 Tumore mit N+ korrelierten, waren es bei schwacher Expression nur fünf Tumore, die mit N+ einhergingen. Bei der signifikanten Korrelation zwischen der Ezrinexpression und der UICC-Klassifikation (p=0,01) zeigte sich, dass eine verstärkte Expression mit einem höheren UICC-Grad assoziiert war. Für die UICC-Stadien III-IVb wurde in 21 Fällen eine starke Expression nachgewiesen, während die UICC-Stadien I und II nur in sechs Fällen mit einer starken Expression korrelierten. Auch für die Lymphangiosis carcinomatosa wurde eine signifikante Korrelation zur Ezrinexpression (p=0,001) ermittelt. Es zeigte sich, dass je stärker die Expression war, desto eher ein Durchbruch in die Lymphgefäße stattgefunden hatte. Bei starker Expression wurde in zehn Fällen eine Lymphangiosis carcinomatosa nachgewiesen und bei schwacher Expression carcinomatosa bei keinem Patienten ermittelt werden. 51 konnte eine Lymphangiosis Zum Alter (p= 0,54), Geschlecht (p= 0,795), ECS (p= 0,525), Rezidivverhalten (p= 0,215), Tabakabusus (p= 0,362), Alkoholabusus (p= 0,786) sowie zur T-Klassifikation (p= 0,122) und G-Kategorie (p= 0,332) bestand keine signifikante Korrelation.mit der Ezrinexpression. 52 Tabelle 19 Ezrinexpression Kein Ezrin Schwache Moderate Starke Expression Expression Expression Alter (Jahre) p-Wert 0,54 ≤ 61,82 Jahre (unterer Median) 1 12 14 11 > 61,82 Jahre (älterer Median) 3 9 14 16 Geschlecht 0,795 Männlich 2 12 19 18 Weiblich 2 9 9 9 T-Klassifikation 0,122 T1-T2 3 17 19 13 T3-T4b 1 4 9 14 N-Klassifikation 0,009 N0 4 16 19 10 N+ 0 5 9 17 UICC-Klassifikation 0,01 I-II 3 14 14 6 III-IVb 1 7 14 21 Lymphangiosis 0,001 Nein 4 21 26 17 Ja 0 0 2 10 ECS 0,525 nein 4 19 23 21 ja 0 2 5 6 Rezidiv 0,215 nein 2 17 22 16 ja 2 4 6 11 G-Kategorie 0,332 G1&G2 4 19 24 20 G3 0 2 4 7 Tabakabusus 0,362 nein 4 19 24 20 ja 0 2 4 7 Alkoholabusus 0,786 nein 1 7 8 11 ja 3 14 20 16 Tabelle 19: Assoziationen der Ezrinexpression und Patientencharakterisitika 53 3.10 Assoziation der Ezrinlokalisation mit klinisch-pathologischen Parametern Im χ² -Test wurde eine signifikante Assoziation zwischen der Ezrinlokalisation und der NKlassifikation gezeigt (p=0,003). Bei Tumoren mit einer zytoplasmatischen Ezrinexpression wurde in 16 Fällen eine regionäre Lymphknotenmetastasierung festgestellt, während bei membranärer Ezrinexpression nur in vier Fällen ein N+ Status ermittelt werden konnte. Demnach ging ein zytoplasmatisches Ezrinexpressionmuster eher mit einer regionären Lymphknotenmetastasierung einher als eine membranäre Ezrinexpression. Die signifikante Assoziation der Lymphangiosis carcinomatosa zur Ezrinlokalisation (p=0,036) ergab, dass nur bei einer zytoplasmatischen Ezrinexpression ein Durchbruch in die Lymphgefäße erfolgte. Bei membranärer Ezrinexpression konnte keine Lymphangiosis carcinomatosa festgestellt werden. Bei zytoplasmatischer Expression lagen sieben Fälle beziehungsweise bei kombiniert membranär-zytoplasmatischer Expression fünf Fälle einer Lymphangiosis carcinomatosa vor. Die signifikante Korrelation der Ezrinlokalisation zum Tabakabusus (p=0,031) ergab, dass die Expression von Ezrin bei positiver Tabakanamnese sowohl zytoplasmatisch als auch membranär erhöht war. Im Bezug auf das Alter (p= 0,710), Geschlecht (p= 0,799), ECS (0,112), Rezidivverhalten (p= 0,18), die T-Klassifikation (p= 0,139), UICC-Klassifikation (0,01), G-Kategorie (p= 0,63) und Alkoholabusus (p= 0,777) bestand keine signifkante Korrelation zur Ezrinlokalisation. 54 Tabelle 20 Ezrinlokalisation Kein Ezrin membranäre gemischte zytoplasmatische Expression Expression Expression Alter (Jahre) p-Wert 0,719 ≤ 61,82 Jahre (unterer Median) 1 13 12 12 > 61,82 Jahre (älterer Median) 3 11 15 13 Geschlecht 0,799 Männlich 1 7 8 11 Weiblich 3 14 20 16 T-Klassifikation 0,139 T1-T2 3 19 18 12 T3-T4b 1 5 9 13 N-Klassifikation 0,003 N0 4 20 16 9 N+ 0 4 11 16 UICC-Klassifikation 0,01 I-II 3 17 10 7 III-IVb 1 7 17 18 Lymphangiosis 0,036 Nein 4 24 22 18 Ja 0 0 5 7 ECS 0,112 nein 4 23 22 18 ja 0 1 5 7 Rezidiv 0,18 nein 2 21 18 16 ja 2 3 9 9 G-Kategorie 0,63 G1&G2 4 21 21 21 G3 0 3 6 4 Tabakabusus 0,031 nein 2 6 1 8 ja 2 18 26 17 Alkoholabusus 0,777 nein 1 8 11 7 ja 3 16 16 18 Tabelle 20: Ezrinlokalisation und Patientencharakteristika 55 3.11 Onkologische Ergebnisse 3.11.1 Einfluss epidemiologischer Parameter auf das Überleben Das Alter (p= 0,232), Geschlecht (0,273) sowie der Tabak- (p= 0,248) und Alkoholabusus (p= 0,277) hatten keinen signifikanten Einfluss auf die 5-Jahres-Überlebensrate. Tabelle 21 Alle Patienten 5-Jahres OS p-Wert Alter 0,232 Jüngere Hälfte Median 79% Ältere Hälfte Median 60% Alle Patienten 5-Jahres OS p-Wert Geschlecht 0,273 männlich 68% weiblich 70% Alle Patienten 5-Jahres OS p-Wert Tabak 0,248 nein 52% Ja 73% Alle Patienten 5-Jahres OS p-Wert Alkohol 0,277 Nein 82% Ja 62% Tabelle 21: Einfluss epidemiologischer Parameter auf das Überleben 3.11.2 Einfluss der Tumorausbreitung auf das Überleben Die T-Klassifikation beeinflusste die 5-Jahres-Überlebensrate signifikant (p= 0,001). Je weiter sich der Primätumor ausdehnte, desto geringer war die 5-Jahres-Überlebensrate. Während T1 mit einer 87%-igen 5-Jahres- Überlebensrate einherging, lag sie bei T4b nur bei 25%. 56 Auch bei der N-Klassifikation zeigte sich ein signifikanter Zusammenhang (p= 0,017) zur 5Jahres- Überlebensrate . N0 ging mit einer 80%-igen, N1 mit einer 44%-igen und N2 mit einer 57%-igen 5-Jahres- Überlebensrate einher. Tabelle 22 Alle Patienten 5-Jahres OS T-Klassifikation p-Wert <0,001 T1 87% T2 77% T3 63% T4a 52% T4b 25% Tabelle 22: Einfluss der T-Klassifikation auf das Überleben Tabelle 23 Alle Patienten 5-Jahres OS p-Wert N-Klassifikation 0,017 N0 80% N1 44% N2 57% Tabelle 23: Einfluss der N-Klassifikation auf das Überleben Die UICC-Klassifikation beeinflusste ebenfalls signifikant (p=0,001) die 5-Jahres- Überlebensrate. Während die Prognosen insbesondere in den Stadien I, II und III ähnlich waren, zeigte sich von Stadium III auf Stadium IVa ein deutlicher Abfall von 88% auf 54% und auf Stadium IVa auf 25%. 57 Tabelle 24 Alle Patienten 5-Jahres OS p-Wert UICC-Klassifikation <0,001 I 86% II 83% III 88% IVa 54% IVb 25% Tabelle 24: Einfluss der UICC-Klassifikation auf das Überleben Auch ein Durchbruch der Tumorzellen aus den Lymphknotenkapseln heraus beeinflusste (p= 0,045) die 5-Jahres-Überlebensrate signifikant (p= 0,045). Dabei sank die 5-Jahres- Überlebensrate von 72% auf 54%, wenn ein Kapseldurchbruch vorlag. Tabelle 25 Alle Patienten 5-Jahres OS ECS p-Wert 0,045 nein 72% ja 54% Tabelle 25: Einfluss des ECS auf das Überleben 3.11.3 Einfluss des Tumordifferenzierungsgrades auf das Überleben Die G-Kategorie des Tumors beeinflusste die 5-Jahres-Überlebensrate nicht signifikant (p= 0,21). Tabelle 26 Alle Patienten 5-Jahres OS G-Kategorie p-Wert 0,21 G1 100% G2 67% G3 66% Tabelle 26: Einfluss des Differenzierungsgrades auf das Überleben 58 3.11.4 Einfluss der Lymphangiosis carcinomatosa auf das Überleben Der Einfluss der Lymphangiosis carcinomatosa auf die 5-Jahres-Überlebensrate war signifikant (p= 0,001). Brachen die Tumorzellen in die Lymphgefäße ein, so zeigte sich eine schlechtere Prognose für die 5-Jahres-Überlebensrate (46%) als beim einem Nicht-Durchbruch (73%). Tabelle 27 Alle Patienten 5-Jahres OS Lymphangiosis carcinomatosa p-Wert 0,001 nein 73% ja 46% Tabelle 27: Einfluss der Lymphangiosis carcinomatosa auf das Überleben 3.11.5 Einfluss der Ezrinlokalisation auf das Überleben Die Ezrinlokalisation zeigte einen signifikante Einfluss (p= 0,001) auf die 5-JahresÜberlebensrate . Dabei lag die 5-Jahres-Überlebensrate bei 100%, wenn Ezrin histologisch nicht nachgewiesen werden konnte. Eine membranäre Ezrinexpression ging mit einer 92%-igen 5-Jahres-Überlebensrate einher, während die gemischte mit einer 77%-igen einherging. Eine zytoplasmatische Ezrinexpression zeigte mit einer 37%-igen 5-Jahres-Überlebensrate die geringste Überlebenswahrscheinlichkeit auf. Tabelle 28 Alle Patienten 5-Jahres OS Ezrinlokalisation p-Wert <0,001 Negativ 100% Membranäre Expression 92% Gemischte Expression 77% Zytoplasmatische Expression 37% Tabelle 28: Einfluss der Ezrinlokalisation auf das Überleben 59 3.11.6 Einfluss der Ezrinexpression auf das Überleben Die Ezrinexpression beeinflusste die 5-Jahres-Überlebensrate signifikant (p<0,001). Je stärker die Ezrinexpresssion war, desto niedriger war die 5-Jahres-Überlebensrate. Bei einer schwachen Ezrinexpression lag die 5-Jahres-Überlebensrate bei 95%, bei einer moderaten bei 66% und bei einer starken Expression bei 47%. Eine negative Ezrinexpression ging mit einer 5Jahres-Überlebensrate von 100% einher. Tabelle 29 Alle Patienten 5-Jahres OS Ezrinexpression p-Wert <0,001 Negativ 100% Schwach 95% Moderat 66% Stark 47% Tabelle 29: Einfluss der Ezrinexpression auf das Überleben 3.11.7 Multivariate Analyse der prognostischen Faktoren Tabelle 30 Multivariate Analyse Gesamtüberleben Parameter RR (95% KI) p-Wert Alter (jüngere vs. ältere Hälfte) 0,541 (0,26-1,14) 0,107 Geschlecht (männlich vs. weiblich 1,171 (0,48-2,85) 0,728 Ezrinexpression (0&1 vs. 2&3) 0,235 (0,07-0,72) 0,011 T-Klassifikation (T1&T2 vs. T3&T4) 0,421 (0,20-0,90) 0,026 N-Klassifikation (N0 vs. N+) 0,770 (0,33-1,82) 0,551 Lymphangiosis carcinomatosa (nein vs. ja) 0,645 (0,27-1,57) 0,333 Tabelle 30: Multivariate Analyse der prognostischen Faktoren auf Gesamtüberleben; RR = Hazard Ratio (Relatives Risiko), KI = Konfidenzintervall 60 das Tabelle 31 Multivariate Analyse Gesamtüberleben Parameter RR (95% KI) p-Wert Alter (jüngere vs. ältere Hälfte) 0,593 (0,28-1,24) 0,166 Geschlecht (männlich vs. weiblich 1,316 (0,56-3,10) 0,530 Ezrinexpression (0&1 vs. 2&3) 0,230 (0,07-0,700) 0,010 UICC-Klassifikation (I&II vs. III&IV) 0,468 (0,19-1,15) 0,098 Lymphangiosis carcinomatosa (nein vs. ja) 0,693 (0,29-1,65) 0,409 Tabelle 31: Multivariate Analyse der prognostischen Faktoren auf das Gesamtüberleben (T- & N-Klassifikation wurden durch die UICC-Klassifikation ersetzt); RR = Hazard Ratio (Relatives Risiko), KI = Konfidenzintervall Auch aus der multivariaten Analyse wird ersichtlich, dass die Ezrinexpression einen signifikanten Einfluss auf das Gesamtüberleben hatte und mit einem p-Wert von 0,011 beziehungsweise 0,010 als ein hochgradig signifikanter Prognosefaktor zu bewerten ist. Weiterhin zeigte die T-Klassifikation mit einem p-Wert von 0,026 einen starken Einfluss auf das Gesamtüberleben. 61 4 Diskussion Das Protein Ezrin gehört zu den ERM-Proteinen, welche zur Superfamilie der Band 4.1 Proteine gehören [10]. Ezrin hat zwei wesentliche physiologische Funktionen, und zwar einerseits die Verlinkung von Proteinen der Plasmamembran mit F-Aktinfilamenten des Zytoskeletts und andererseits als ein Bestandteil verschiedener Signaltransduktionswege [10]. Somit ist Ezrin beteiligt an der Zell-Zell- und Zell-Matrix-Interaktion, an der Zellform, Zelladhäsion, Zellmotilität, Zellpolarität, Zytokinese, Phagozytose, Apoptose, Oberflächenstruktur und an der Integration von Membrantransportern [88] [84] [58] [83]. Dadurch ist Ezrin an einigen wesentlichen Zellfunktionen, die auch eine bedeutende Rolle im Rahmen der Karzinogenese und Metastasierung spielen, beteiligt und kann diese modifizieren, so dass in verschiedenen Studien nachgewiesen werden konnte, dass Ezrin im Rahmen der Tumorgenese, Tumorinvasion, Tumorprogession und Metastasierung durch die Regulation von Adhäsionsmolekülen und der Beeinflussung von Zellsignaltransduktionswegen eine sehr wichtige Rolle spielt [19] [86] [101] [115]. Diese molekularbiologischen Funktionen, insbesondere die essentielle Rolle von Ezrin bei der Regulation der Zellmigration und Zelladhäsion, welche im Rahmen der Metastasierung und Karzinogenese entscheidend sind, können auch zur Interpretation unserer Ergebnisse aus der univariaten Analyse herangezogen werden. Hierin wurde errechnet, dass die Ezrinexpression signifikant mit dem pN-Stadium (p=0,009), der pUICC-Klassifikation (p=0,01) und der Lymphangiosis carcinomatosa (p=0,001) korreliert. Da diese Parameter auf eine erfolgreiche Metastasierung eines Malignoms hinweisen, deutet dies auf einen statistischen Zusammenhang einer erhöhten Ezrinexpression und einer höheren Metastasierungswahrscheinlichkeit eines oralen Plattenepithelkarzinoms hin. Vergangene Studien konnten ebenfalls belegen, dass Ezrin eine essentielle Rolle bei der Metastasierung von Tumoren spielt, so zum Beispiel bei Osteosarkomen, Brustkarzinomen, Nasopharynxkarzinomen, Pankreaskarzinomen und Prostatakarzinomen [58] [78] [83] [101] [115]. Da die Metastasierung wiederum der häufigste Grund für das Versterben von Patienten ist, die an einem malignen Tumor erkranken, kann man somit auch unser Ergebnis aus der univariaten und multivariaten Analyse erklären, und zwar, dass eine vermehrte Expression von Ezrin mit einer signifikant niedrigeren 5-Jahres-Überlebensrate für das Gesamtüberleben einhergeht [139]. Diese Beobachtung deckt sich mit den Ergebnissen mehrerer vergangener Studien, die ebenfalls eine signifikante Korrelation zwischen der Ezrinexpression und einer 62 geringeren Überlebenswahrscheinlichkeit nachweisen konnten, so zum Beispiel bei Brustkarzinomen, Endometriumskarzinomen, Ovarialkarzinomen, kutanen und uvealen Melanomen und Weichgewebssarkomen [9] [11] [28] [51] [65] [81] [110] [152]. 2004 kamen Hunter et al zu dem Schluss, dass eine Überexpression von Ezrin notwendig für die Metastasierung ist und demnach zu einer geringeren Überlebenswahrscheinlichkeit führt [49]. Diese These konnte jedoch durch andere Studien nur eingeschränkt bestätigt werden, da bei Untersuchungen der Ezrinexpression an verschiedenen Malignomen, diese zu dem Ergebnis kamen, dass sowohl eine Überexpression als auch eine verringerte Expression von Ezrin im signifikanten Zusammenhang zur Ausbildung von Metastasen steht. So konnte an Mäusen, welche an einem Osteosarkom erkrankt waren, gezeigt werden, dass die Rate an Lungenmetastasen signifikant niedriger war, wenn die Ezrinexpression supprimiert wurde [94]. Weiterhin konnte auch gezeigt werden, dass eine signifikante Assoziation zwischen der Ezrinexpression und einer früheren Entwicklung von Metastasen bei Kaninchen mit einem Osteosarkom vorlag [60]. Hingegen konnte bei serösen Ovarialkarzinomen und Adenokarzinomen der Lunge gezeigt werden, dass eine nicht vorhandene oder schwache Ezrinexpression mit einer schlechteren Prognose einherging [101] [28] 51] [144]. Daher gibt es bezüglich der Rolle des Ezrins bei der Tumorprogression zwei verschiedene Ansichten. Einerseits konnte in Studien gezeigt werden, dass Ezrin als Suppressor der malignen Progression einiger Tumorarten dient, da eine Inhibition der Ezrinexpression zu einer verringerten Zell-Zell-Adhäsion führte und somit die Zellmotilität und folglich die Möglichkeit zur Invasion des Tumors in benachbartes Gewebe erhöht wurde. Andererseits konnte in Studien nachgewiesen werden, dass eine erhöhte Ezrinexpression zu einer verstärkten Tumorprogression führen konnte [125]. Diese Beobachtung legt nahe, dass die molekularbiologischen Funktionen von Ezrin in unterschiedlichen Zelltypen verschieden sind und die intrazellulären Signale je nach extrazellulärer Umgebung variieren [101]. Dies konnte zum Beispiel im Rahmen der modulatorischen Eigenschaften von Ezrin auf die Apoptose gezeigt werden, da Ezrin gleichzeitig auf Lymphozyten einen pro-apoptotischen Effekt und auf tubuläre Nierenepithelzellen einen anti-apoptotischen Effekt hatte [101]. Eine weitere Erklärungsmöglichkeit für den unterschiedlichen Einfluss der Ezrinexpression auf die Prognose von verschiedenen Malignomen ist es, dass eventuell mehrere Isoformen von Ezrin vorliegen, die abhängig vom entsprechenden Gewebe unterschiedlich stark ausgeprägt sind und diese unterschiedlich stark beeinflussen [108] . Darüber hinaus ist es auch möglich, dass Ezrin abhängig vom Ursprungsgewebe der verschiedenen Tumoren, unterschiedliche 63 Funktionen erfüllt. Weiterhin konnte in der univariaten Analyse gezeigt werden, dass die Ezrinlokalisation signifikant mit der N-Klassifikation (p=0,003), der Lymphangiosis carcinomatosa (p=0,036) und Tabakabusus (p=0,031) korreliert. Es konnte auch ermittelt werden, dass die Ezrinlokalisation einen signifikanten Einfluss auf die 5-Jahres-Überlebensrate der betroffenen Patienten hatte (p=<0,001). Man konnte feststellen, dass eine nicht vorhandene Ezrinexpression mit einer 100%-igen 5-Jahres-Überlebensrate einherging. Lag jedoch Ezrin membranär vor, dann sank die 5-Jahres-Überlebensrate auf 92%, wenn sie membranär und zytoplasmatisch lag auf 77% und, wenn sie nur zytoplasmatisch nachgewiesen wurde, auf 37%. Diese Beobachtung deckt sich mit Ergebnissen vorangegangener Studien, da diese ebenfalls eine signifikante Korrelation zwischen einer erhöhten zytoplasmatischen Ezrinexpression und einer geringeren Überlebenswahrscheinlichkeit der betroffenen Patienten zeigen konnten [9] [11] [28] [51] [65] [81] [110] [152]. Mehrere Studien, die dies nachweisen konnten, konnten durch RNS-Analysen belegen, dass eine erhöhte zytoplasmatische Ezrinexpression von Kopf-Hals-Karzinomen zu einem invasiveren Charakter der Tumore führte und diese demnach aggressiver waren und mit einer niedrigeren Überlebenswahrscheinlichkeit als Malignome mit einer membranären Ezrinexpression einhergingen [28] [29] [81] [99]. In nicht proliferierender, normaler Schleimhaut befindet sich Ezrin eher membranär. Aktives Ezrin befindet sich physiologisch eher submembranär in den basalen und parabasalen Zellschichten des Epithels, welche die Invasionsfront eines Tumors darstellen [113]. Kobayashi et al konnten zeigen, dass in proliferierenden Schleimhautzellen eine Translokation des Ezrins von membranär ins Zytoplasma stattfindet [64]. Tumorzellen, die eine verstärkte zytoplasmatische Ezrinexpression aufweisen, zeigen auch einen verstärkten Verlust an Zell-Zell-Kontakten, so dass die Fähigkeit zur Metastasierung verbessert wird [8]. Auch im Rahmen der malignen Transformation kommt es zu einer Translokation des Ezrins ins Zytoplasma, so dass Kobayashi et al. davon ausgehen, dass die Lokalisation von ERM-Proteinen mit dem biologischen Verhalten korreliert [64]. Eine vermehrte zytoplasmatische Ezrinexpression konnte in kolorektalen Karzinomen sowie Brustkarzinomen nachgewiesen werden [115] [42]. Eine vermehrte membranäre Expression kommt zum Beispiel in Adenokarzinomen des Endometriums und Gallenblasenkarzinomen vor [113]. Schlecht et. al konnten nachweisen, dass die hohe zytoplasmatische Ezrinexpression mit einer erhöhten Expression von Genen einherging, welche die Zellmigration und Invasion förderten (SERPINE2, EFNB2, ETS1, NET1, ITGB1) 64 [131]. Andererseits konnten sie zeigen, dass diejenigen Gene, die für die epidermale Entwicklung (zum Beispiel tight junctions) wichtig sind, herunterreguliert waren. Weiterhin konnte bei den Tumoren, in denen eine hohe zytoplasmatische Ezrinexpression vorlag, ermittelt werden, dass anti-apoptotische Gene (BIRC2, CCDC50, TGM2) verstärkt exprimiert und pro-apoptotische Gene (EDARADD) weniger exprimiert wurden [131]. In Studien von Zeng et al sowie Fazioli et al konnte nachgewiesen werden, dass die Translokation des Ezrins aus der Membran ins Zytoplasma mit einer erhöhten Tumorinvasivität einherging [31] [163]. Gunn-Moore et al haben gezeigt, dass der HippoSignalweg durch Ezrin blockiert werden kann. Der Hippo-Signalweg führt durch eine Kinase-Kaskade zu einer Deaktivierung durch Phosphorylierung des Transkriptionsfaktors YAP, so dass es zu einer Apoptose der Zelle kommt. Ezrin hingegen führt dazu, dass YAP nicht phosphoryliert wird, so dass Gene exprimiert werden, welche die Zellproliferation fördern und die Apoptose modulieren können [4]. Ein Grund für die vermehrte zytoplasmatische Ezrinexpression in einigen Malignomen könnte sein, dass sich das Gleichgewicht zwischen der membranären und zytoplasmatischen Expression zugunsten der zytoplasmatischen verändert, weil es zu einer Verminderung aktivierender Signale und einem gleichzeitigen Anstieg inaktivierender Signale für die Ezrinexpression kommt. Ezrin spielt somit eine Rolle im Bezug auf das Wachstum und das Metastasierungspotential von malignen Tumorzellen [65]. Demnach können die Ezrinexpression und -lokalisation, wie durch unsere uni- und multivariate Analyse bestätigt, als bedeutende Risikofaktoren für die Prognose der Überlebenswahrscheinlichkeit von Patienten mit oralen Plattenepithelkarzinomen dienen, so wie es für andere Malignome in vorhergehenden Studien ebenfalls nachgewiesen werden konnte [60]. Gegenwärtig wird zur Ermittlung der anatomischen Ausbreitung des Tumors das TNMStaging durchgeführt. Diese basiert auf einer eingehenden körperlichen Untersuchung, der bildgebenden Darstellung und der histopathologischen Beurteilung [134]. Man unterscheidet bei der TNM-Klassifikation eine prätherapeutische, klinische (cTNM) und eine posttherapeutische, pathohistologische (pTNM) Stadieneinteilung. Nachteilig ist, dass die cTNM-Klassifikation abhängig von diagnostischen Mitteln ist, so dass je nach technischer Ausstattung unterschiedliche Voraussetzungen und folglich Möglichkeiten für eine genaue Diagnose vorliegen. Demnach liegt eine eingeschränkte Objektivierbarkeit von Ergebnissen der cTNM-Klassifikation vor. Koch et al wiesen nach, dass mithilfe der pTNM-Klassifikation eine genauere prognostische Abschätzung der Überlebenswahrscheinlichkeit getroffen 65 werden kann [66]. Jedoch besteht bei der pTNM-Klassifikation das Problem, dass es nur an Patienten angewendet werden kann, bei denen keine neoadjuvante Radiochemotherapie stattgefunden hat. Ansonsten würde es nämlich zu verfälschten Ergebnissen im Rahmen der pathohistologischen Untersuchung kommen. Das TNM-System basiert auf dem Konzept des zeitlichen Modells, da es von einer anatomischen Ausbreitung des Tumors ausgeht, bei der sich dieser kontinuierlich von lokal über regional in die Ferne ausdehnt. In Anlehnung an dieses Konzept, geht man davon aus, dass die Prognose des Patienten umso schlechter wird, je weiter sich der Tumor anatomisch ausbreitet [109]. Ein wesentlicher Nachteil dieses Modells liegt jedoch darin, dass weitere Parameter, welche die Prognose signifikant beeinflussen, nicht berücksichtigt werden. So können zum Beispiel eine mögliche neoadjuvante Therapie, eine antihormonelle Therapie, eine Chemotherapie oder eine zielgerichtete Therapie mit monoklonalen Antikörpern in das System nicht integriert werden, so dass eine individuelle Abschätzung mithilfe der TNMKlassifikation nicht möglich ist [12] [76]. Weiterhin werden auch molekulare Charakteristika der Tumorprogression im TNM-System nicht berücksichtigt, obwohl sie entscheidend für das Tumorverhalten sind und abschätzen lassen können, wie aggressiv das Ausbreitungsverhalten des Tumors und entsprechend wie hoch die Überlebenswahrscheinlichkeit des Patienten ist [12] [2]. Demnach sind für eine genauere Prognose und Therapieplanung prognostische Biomarker notwendig, die auch die molekulare Tumorbiologie berücksichtigen [2]. Auf diese Weise lässt sich das zeitabhängige TNM-Klassifikationsmodell mithilfe von Biomarkern wie Ezrin erweitern, so dass ein biologisches Modell entsteht, in der die Karzinogenese nicht stadienabhängig ist, sondern auf den molekularen Eigenschaften des Tumors basiert [76]. Wenn jedoch weitere patienten- und tumorbezogene Parameter, wie zum Beispiel molekulare Biomarker in die TNM-Klassifikation integriert werden, dann steigt die Anzahl der möglichen Kombinationen exponentiell [12]. Die TNM-Klassifikation der 7. Ausgabe lässt 5 x 6 x 2, also 60 Kombinationen (5 T-Stadien, 6 N-Stadien, 2 M-Stadien) zu, die in 6 UICC-Stadien zusammengefasst werden. Würde man nun die Intensität der Ezrinexpression in keine, schwach, moderat und stark einstufen und diese in das TNM-System einfügen, so hätte man 5 x 6 x 2 x 4, also 240 Kombinationen. Hieran erkennt man, dass auf diese Weise das Stagingsystem unhandlich gemacht wird und ein Vergleich zwischen den verschiedenen Gruppen sich erschwert [12] [74]. Abhilfe schaffen bei dieser Problematik Nomogramme, welche eine individuelle Risikobestimmung der Patienten unter Berücksichtigung unterschiedlich gewichteter Prognosefaktoren ermöglichen und als Entscheidungshilfe zur 66 Auswahl einer adjuvanten Therapie dienen können [153] [80]. Liao & Kreppel haben 2013 ein computerbasiertes kontinuierlich aktualisierbares Nomogramm für Patienten mit Mundhöhlenkarzinomen mit Lymphknotenbefall und extrakapsulärem Tumorwachstum entwickelt [80]. Durch Eingabe entsprechender klinisch-pathologischer Parameter ist eine genauere Vorhersage des Gesamtüberlebens möglich als durch die TNM-Klassifikation. In den letzten Jahren wurden viele weitere molekulare Biomarker entdeckt, die einen Einfluss auf die prognostische Abschätzung von Patienten mit oralen Plattenepithelkarzinomen haben [12]. Ein ebenfalls vielversprechender Biomarker ist das Protein Podoplanin. Kreppel et al konnten zeigen, dass die Expression des Proteins Podoplanin einen signifikanten Einfluss auf die Gesamtüberlebensrate von Patienten mit oralen Plattenepithelkarzinomen hat [76]. Podoplanin wird vor allem bei Patienten mit zervikalen Lymphknotenmetastasen exprimiert, da es als transmembranes Glycoprotein des Muzintyps in erster Linie in lymphatischen endothelialen Zellen, aber nicht in endothelialen Zellen des Blutes exprimiert wird [129]. Podoplanin interagiert über ERM-Proteine mit Aktinfilamenten. Eine erhöhte Expression von Podoplanin führt zu einer Phosphorylierung von Ezrin, welches Podoplanin mit Aktin verbindet und so zu einer Veränderung der Tumorzellmotilität führen kann. Podoplanin stimuliert auch GTPasen der Rho-Familie, insbesondere RhoA, welche ebenfalls die Tumorzellmotilität fördern [76]. In einer Studie von Kreppel et al lag die 5-Jahres-Überlebensrate von Patienten mit schwacher Podoplaninexpression bei 92,9%, bei Patienten mit moderater Expression bei 29,4% und bei starker Podoplaninexpression bei 15,0% [73]. Demnach konnte gezeigt werden, dass die Podoplaninexpression in oralen Plattenepithelkarzinomen einen starken Einfluss auf das Gesamtüberleben hat. Weiterhin konnten Kreppel et al auch nachweisen, dass Podoplanin einen signifikanten Einfluss auf die lymphogene Metastasierung, sowie Tumorprogression und Tumorinvasion hat [73]. In Studien über das ERM-Protein Moesin wurde herausgefunden, dass auch dieses Protein als ein potentieller Biomarker für die Abschätzung der Tumorprogression dienen kann [86] [14] [50]. Moesin ist in erster Linie in Filopodien sowie anderen membranären Ausstülpungen zu finden und fungiert wie die anderen ERM-Proteine vor allem im Bezug auf die Regulation von Zell-Zellkontakten, der Signaltransduktion und der Zellmotilität [86]. Im Unterschied zu Ezrin, gibt es jedoch für Moesin wenige Studien, die sich mit der Bedeutung von Moesin für das molekulare Verhalten von Tumoren befasst haben. So konnten Carmeci et al an Östrogenrezeptor-negativen Mammakarzinomzelllinien eine starke Moesinexpression 67 zeigen während in Östrogenrezeptor-positiven Mammakarzinomzelllinien keine erhöhte Moesinexpression nachgewiesen werden konnte [14]. Ichikawa et al untersuchten 1998 in ihrer Studie die Moesinexpression bei verschiedenen epithelialen Hauttumoren. Während bei Basalzellkarzinomen, Morbus Bowen und dem extramammären Morbus Paget die Moesinexpression negativ beziehungsweise sehr gering war, konnte beim invasiven Plattenepithelkarzinom der Haut eine erhöhte Moesinexpression nachgewiesen werden [50]. Kobayashi et al kamen 2003 zu dem Ergebnis, dass Moesin in normaler Mundschleimhaut, bei einfachen oralen Schleimhautdysplasien und beim oralen verrukösen Karzinom Moesin eher membranär exprimiert wird und bei oralen Plattenepithelkarzinomen es zu einer Translokation ins Zytoplasma der Tumorzellen kommt [64]. Demnach kamen sie zum Schluss, dass Moesin als ein unabhängiger prognostischer Biomarker dienen kann, da eine erhöhte Expression zytoplasmatischen Moesins mit einer signifikant höheren zervikalen Metastasierungsrate und signifikant geringerer Überlebenswahrscheinlichkeit einherging. Diese Beobachtungen konnten auch für Ezrin gemacht werden, so dass man davon ausgehen kann, dass wahrscheinlich die Lokalisation von ERM-Proteinen allgemein ein wichtiger Faktor für das Tumorverhalten ist [50]. Radixin als Haupt-ERM-Protein der Leber kommt auch in den Stereozilien der Cochlea vor. Kitajiri et al konnten 2004 an Mäusen zeigen, dass das Fehlen von Radixin zur Taubheit führt, aber das Vestibularsystem nicht beeinträchtigt [61]. 2012 erst belegten Valderrama et al , dass Radixin die Zellform, Zellmigration und Zell-Zell-Adhäsion reguliert. Dementsprechend ist es sehr wahrscheinlich, dass auch Radixin eine wichtige Rolle in der Karzinogenese spielt, so wie es in der Studie von Valastyan et al von 2010 im Bezug auf Mammakarzinome nachgewiesen wurde [146] [147]. Ein weiteres Protein, welches zur Familie der ERM-Proteine gehört, ist das Moesin-EzrinRadixin-like-Protein (Merlin), welches von dem Tumorsuppressorgen Neurofibromatosis 2 (NF2) codiert wird und auch als Schwannomin bekannt ist. Merlin hat viele überlappende Funktionen mit den ERM-Proteinen, ist jedoch als einziges von ihnen ein Tumorsuppressor [94]. 68 5 Zusammenfassung Das orale Plattenepithelkarzinom geht mit einer 5-Jahres-Überlebensrate von unter 50% einher. Als Gründe hierfür werden das schlechte Ansprechen einiger Patienten auf vorliegende Chemotherapeutika, eine späte Diagnose sowie ein Mangel an Tumormarkern angegeben, mit deren Hilfe die Erkrankung frühzeitig detektiert werden kann und eine genaue Einschätzung der weiteren Tumorprogression und Behandlung getroffen werden kann. In mehreren Studien konnte bisher die entscheidende Rolle des ERM-Proteins Ezrin im Bezug auf das molekularbiologische Verhalten von Tumoren nachgewiesen werden. Für das orale Plattenepithelkarzinom lagen jedoch bisher kaum Daten vor, so dass im Rahmen dieser Dissertation die Korrelation zwischen der Ezrinexpression/-lokalisation und klinischpathologischen Parametern sowie die Aussagekraft der Ezrinexpression/-lokalisation für die Prognose und zervikale Metastasierung untersucht wurden. Für die retrospektive Studie lag das Untersuchungsmaterial von 80 Patienten aus dem Zeitraum Juni 2002 bis Oktober 2005 vor, bei denen erstmalig ein orales Plattenepithelkarzinom im Stadium I-IVb diagnostiziert wurde. Die statistische Analyse ergab, dass die Ezrinexpression signifikant mit dem N-Stadium (p=0,009), der UICC-Klassifikation (p=0,01) und der Lymphangiosis carcinomatosa (p=0,001) korrelierte. In der univariaten Analyse konnte weiterhin ein signifikantes Verhältnis zwischen der Ezrinlokalisation und der N-Klassifikation (p=0,003), der Lymphangiosis carcinomatosa (p=0,036) und Tabakabusus (p=0,031) ermittelt werden. Darüber hinaus konnte in der univariaten Analyse ein signifikanter Einfluss der Ezrinlokalisation (p<0,001) und -expression (p=0,001) auf die 5-Jahres-Überlebensrate nachgewiesen werden. Dabei wurde ermittelt, dass eine zytoplasmatische und eine verstärkte Ezrinexpression mit einer geringeren 5-Jahres-Überlebensrate einhergingen. Die multivariate Analyse bestätigte den signifikanten Einfluss der vermehrten Ezrinexpression auf das Gesamtüberleben (p=0,011). Dementsprechend kann man schlussfolgern, dass Ezrin auch in oralen Plattenepithelkarzinomen Tumorprogression und das eine entscheidende Metastasierungpotential Rolle spielt. im Bezug Demnach auf die können die Ezrinexpression und –lokalisation als bedeutende Risikofaktoren für die Prognose der Überlebenswahrscheinlichkeit von Patienten mit oralen Plattenepithelkarzinomen dienen. 69 6 Literatur [6, 10, 20, 30, 32, 34, 43, 49, 53, 57, 63, 69, 76, 84, 87, 88, 91, 102, 109, 116-118, 121, 134, 136, 142, 143, 145, 149] 6.1 Literaturverzeichnis 1. Adams, S., R.P. Baum, T. Stuckensen, et al., Prospective comparison of 18F-FDG PET with conventional imaging modalities (CT, MRI, US) in lymph node staging of head and neck cancer. Eur J Nucl Med, 1998. 25(9): p. 1255-60. Altman, D.G., L.M. McShane, W. Sauerbrei, et al., Reporting Recommendations for Tumor Marker Prognostic Studies (REMARK): explanation and elaboration. PLoS Med, 2012. 9(5): p. e1001216. Andrle, J., V.H. Schartinger, I. Schwentner, et al., Initial staging examinations for head and neck squamous cell carcinoma: are they appropriate? J Laryngol Otol, 2009. 123(8): p. 885-8. Angus, L., S. Moleirinho, L. Herron, et al., Willin/FRMD6 expression activates the Hippo signaling pathway kinases in mammals and antagonizes oncogenic YAP. Oncogene, 2012. 31(2): p. 238-50. Bailey, J.S., R.H. Blanchaert, Jr., and R.A. Ord, Management of oral squamous cell carcinoma treated with inadequate excisional biopsy. J Oral Maxillofac Surg, 2001. 59(9): p. 1007-10; discussion 1011. Bonilha, V.L., Focus on molecules: ezrin. Exp Eye Res, 2007. 84(4): p. 613-4. Bourhis, J. and J.P. Pignon, Meta-analyses in head and neck squamous cell carcinoma. What is the role of chemotherapy? Hematol Oncol Clin North Am, 1999. 13(4): p. 769-75, vii. Brambilla, D. and S. Fais, The Janus-faced role of ezrin in "linking" cells to either normal or metastatic phenotype. Int J Cancer, 2009. 125(10): p. 2239-45. Bretscher, A., Regulation of cortical structure by the ezrin-radixin-moesin protein family. Curr Opin Cell Biol, 1999. 11(1): p. 109-16. Bretscher, A., K. Edwards, and R.G. Fehon, ERM proteins and merlin: integrators at the cell cortex. Nat Rev Mol Cell Biol, 2002. 3(8): p. 586-99. Bruce, B., G. Khanna, L. Ren, et al., Expression of the cytoskeleton linker protein ezrin in human cancers. Clin Exp Metastasis, 2007. 24(2): p. 69-78. Burke, H.B., Outcome prediction and the future of the TNM staging system. J Natl Cancer Inst, 2004. 96(19): p. 1408-9. Campo-Trapero J, C.-S.n.J., Palacios-Sa'nchez B, Sa'nchez-Gutierrez J, Gonza'lezMoles M, Bascones-Marti'nez A, Update on Molecular Pathology in Oral Cancer and Precancer. Anticancer Res, 2008: p. 1197-206. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 70 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. Carmeci, C., D.A. Thompson, W.W. Kuang, et al., Moesin expression is associated with the estrogen receptor-negative breast cancer phenotype. Surgery, 1998. 124(2): p. 211-7. Casiglia, J. and S.B. Woo, A comprehensive review of oral cancer. Gen Dent, 2001. 49(1): p. 72-82. Chaturvedi, A.K., Epidemiology and clinical aspects of HPV in head and neck cancers. Head Neck Pathol, 2012. 6 Suppl 1: p. S16-24. Cianfriglia, F., D.A. Di Gregorio, and A. Manieri, Multiple primary tumours in patients with oral squamous cell carcinoma. Oral Oncol, 1999. 35(2): p. 157-63. Cooper, J.S., T.F. Pajak, A.A. Forastiere, et al., Postoperative concurrent radiotherapy and chemotherapy for high-risk squamous-cell carcinoma of the head and neck. N Engl J Med, 2004. 350(19): p. 1937-44. Curto, M. and A.I. McClatchey, Ezrin...a metastatic detERMinant? Cancer Cell, 2004. 5(2): p. 113-4. D, C., Regression modell and life-tables. J R Stat Soc, 1972: p. 34:187-220. Dalla Torre, D.S., E.; Burtscher, D.; Widschwendter, A.; Steger, C.; Puelacher, W., Die orale Bürstenabstrichmethode zur Bestimmung von humanen Papillomavirus (HPV)-Infektionen. Stomatologie, 2012. 109: p. 35 - 39. Das, B.R. and J.K. Nagpal, Understanding the biology of oral cancer. Med Sci Monit, 2002. 8(11): p. RA258-67. Ding, Y., Y. Shimada, M. Maeda, et al., Association of CC chemokine receptor 7 with lymph node metastasis of esophageal squamous cell carcinoma. Clin Cancer Res, 2003. 9(9): p. 3406-12. e.V., R.-K.-I.u.d.G.d.e.K.i.D., Cancer in Germany 2007/2008. Incidence and Trends. . 2010(8. Ausgabe). Eckardt, A., G. Wegener, and J.H. Karstens, [Preoperative radiochemotherapy of advanced resectable cancer of the oral cavity with cisplatin vs paclitaxel/carboplatin. Analysis of two multimodality treatment concepts]. Mund Kiefer Gesichtschir, 2006. 10(1): p. 30-6. Eich, H.T., M. Loschcke, M. Scheer, et al., Neoadjuvant radiochemotherapy and radical resection for advanced squamous cell carcinoma of the oral cavity. Outcome of 134 patients. Strahlenther Onkol, 2008. 184(1): p. 23-9. Eisenberger, M., J. Hornedo, H. Silva, et al., Carboplatin (NSC-241-240): an active platinum analog for the treatment of squamous-cell carcinoma of the head and neck. J Clin Oncol, 1986. 4(10): p. 1506-9. Elliott, B.E., J.A. Meens, S.K. SenGupta, et al., The membrane cytoskeletal crosslinker ezrin is required for metastasis of breast carcinoma cells. Breast Cancer Res, 2005. 7(3): p. R365-73. 71 29. 30. 31. 32. 33. 34. 35. 36. 37. 38. 39. 40. 41. 42. Elzagheid, A., E. Korkeila, R. Bendardaf, et al., Intense cytoplasmic ezrin immunoreactivity predicts poor survival in colorectal cancer. Hum Pathol, 2008. 39(12): p. 1737-43. Fang, X., M. Ueno, T. Yamashita, et al., RhoA activation and effect of Rho-kinase inhibitor in the development of retinal neovascularization in a mouse model of oxygen-induced retinopathy. Curr Eye Res, 2011. 36(11): p. 1028-36. Fazioli, F., W.T. Wong, S.J. Ullrich, et al., The ezrin-like family of tyrosine kinase substrates: receptor-specific pattern of tyrosine phosphorylation and relationship to malignant transformation. Oncogene, 1993. 8(5): p. 1335-45. Ferlito, A., K.T. Robbins, C.E. Silver, et al., Classification of neck dissections: an evolving system. Auris Nasus Larynx, 2009. 36(2): p. 127-34. Ferrara, N., From the discovery of vascular endothelial growth factor to the introduction of avastin in clinical trials - an interview with Napoleone Ferrara by Domenico Ribatti. Int J Dev Biol, 2011. 55(4-5): p. 383-8. Fievet, B., D. Louvard, and M. Arpin, ERM proteins in epithelial cell organization and functions. Biochim Biophys Acta, 2007. 1773(5): p. 653-60. Fortin, A., C. Couture, R. Doucet, et al., Does histologic grade have a role in the management of head and neck cancers? J Clin Oncol, 2001. 19(21): p. 4107-16. Foulkes, W.D., J.S. Brunet, L.P. Kowalski, et al., Family history of cancer is a risk factor for squamous cell carcinoma of the head and neck in Brazil: a case-control study. Int J Cancer, 1995. 63(6): p. 769-73. Gellrich N, Z.C., Mund-, kiefer- und gesichtschirurgische Aspekte des Mundhöhlenkarzinoms. Strahlentherapie im Kopf-Hals Bereich, 2004. 1 ed(Schlütersche Verlagsgesellschaft): p. 11-26. Ghosh, S.K., N.J. Roland, A. Kumar, et al., Detection of synchronous lung tumors in patients presenting with squamous cell carcinoma of the head and neck. Head Neck, 2009. 31(12): p. 1563-70. Giralt, J.L., J. Gonzalez, J.M. del Campo, et al., Preoperative induction chemotherapy followed by concurrent chemoradiotherapy in advanced carcinoma of the oral cavity and oropharynx. Cancer, 2000. 89(5): p. 939-45. Grau, J.J., J. Domingo, J.L. Blanch, et al., Multidisciplinary approach in advanced cancer of the oral cavity: outcome with neoadjuvant chemotherapy according to intention-to-treat local therapy. A phase II study. Oncology, 2002. 63(4): p. 338-45. Grotz, K.A., [Dental care for patients with antineoplastic radiotherapy of the head and neck]. Strahlenther Onkol, 2003. 179(4): p. 275-8. Gschwantler-Kaulich, D., C. Natter, S. Steurer, et al., Increase in ezrin expression from benign to malignant breast tumours. Cell Oncol (Dordr), 2013. 72 43. 44. 45. 46. 47. 48. 49. 50. 51. 52. 53. 54. 55. 56. 57. 58. 59. Ha, P.K., S.S. Chang, C.A. Glazer, et al., Molecular techniques and genetic alterations in head and neck cancer. Oral Oncol, 2009. 45(4-5): p. 335-9. HH, H., Mund-Kiefer-Gesichtschirurgie. 2007. 4. Aufl. (Urban & Fischer, München). Howaldt HP, V.H., Blecher J, Reicherts M, Kainz M, Ergebnisse aus dem DÖSAKTumorregister. 2000(Mund Kiefer GesichtsChir): p. 4:216-25. Hsu, Y.B., S.Y. Chang, M.C. Lan, et al., Second primary malignancies in squamous cell carcinomas of the tongue and larynx: an analysis of incidence, pattern, and outcome. J Chin Med Assoc, 2008. 71(2): p. 86-91. Huang, C.H., S.T. Chu, L.P. Ger, et al., Clinicopathologic evaluation of prognostic factors for squamous cell carcinoma of the buccal mucosa. J Chin Med Assoc, 2007. 70(4): p. 164-70. Hughes, R.S. and E.P. Frenkel, The role of chemotherapy in head and neck cancer. Am J Clin Oncol, 1997. 20(5): p. 449-61. Hunter, K.W., Ezrin, a key component in tumor metastasis. Trends Mol Med, 2004. 10(5): p. 201-4. Ichikawa, T., J. Masumoto, M. Kaneko, et al., Expression of moesin and its associated molecule CD44 in epithelial skin tumors. J Cutan Pathol, 1998. 25(5): p. 237-43. Ilmonen, S., A. Vaheri, S. Asko-Seljavaara, et al., Ezrin in primary cutaneous melanoma. Mod Pathol, 2005. 18(4): p. 503-10. JE, H., Tumor surgery. Mund Kiefer GesichtsChir, 2004: p. 142-154. Jemal, A., R. Siegel, E. Ward, et al., Cancer statistics, 2009. CA Cancer J Clin, 2009. 59(4): p. 225-49. Johnson, N., Tobacco use and oral cancer: a global perspective. J Dent Educ, 2001. 65(4): p. 328-39. Jovanovic, A., I.G. van der Tol, P.J. Kostense, et al., Second respiratory and upper digestive tract cancer following oral squamous cell carcinoma. Eur J Cancer B Oral Oncol, 1994. 30B(4): p. 225-9. Kaanders, J.H., G.J. Hordijk, H. Dutch Cooperative, et al., Carcinoma of the larynx: the Dutch national guideline for diagnostics, treatment, supportive care and rehabilitation. Radiother Oncol, 2002. 63(3): p. 299-307. Kaplan EL, M.P., Non-parametric estimation from incomplete observations. J Am Stat Assoc, 1958: p. 53:457-81. Kapoor, S., Ezrin and its emerging role in tumor progression in systemic malignancies. Cryobiology, 2013. 66(2): p. 93. Katoh, T., S. Kaneko, S. Takasawa, et al., Human glutathione S-transferase P1 polymorphism and susceptibility to smoking related epithelial cancer; oral, lung, gastric, colorectal and urothelial cancer. Pharmacogenetics, 1999. 9(2): p. 165-9. 73 60. 61. 62. 63. 64. 65. 66. 67. 68. 69. 70. 71. 72. Khanna, C., X. Wan, S. Bose, et al., The membrane-cytoskeleton linker ezrin is necessary for osteosarcoma metastasis. Nat Med, 2004. 10(2): p. 182-6. Kitajiri, S., K. Fukumoto, M. Hata, et al., Radixin deficiency causes deafness associated with progressive degeneration of cochlear stereocilia. J Cell Biol, 2004. 166(4): p. 559-70. Klug, C., A. Wutzl, C. Kermer, et al., Preoperative radiochemotherapy and radical resection for stages II-IV oral and oropharyngeal cancer: outcome of 222 patients. Int J Oral Maxillofac Surg, 2005. 34(2): p. 143-8. Knoblich, J.A., Mechanisms of asymmetric stem cell division. Cell, 2008. 132(4): p. 583-97. Kobayashi, H., J. Sagara, J. Masumoto, et al., Shifts in cellular localization of moesin in normal oral epithelium, oral epithelial dysplasia, verrucous carcinoma and oral squamous cell carcinoma. J Oral Pathol Med, 2003. 32(6): p. 344-9. Kobel, M., E. Gradhand, K. Zeng, et al., Ezrin promotes ovarian carcinoma cell invasion and its retained expression predicts poor prognosis in ovarian carcinoma. Int J Gynecol Pathol, 2006. 25(2): p. 121-30. Koch, W.M., J.A. Ridge, A. Forastiere, et al., Comparison of clinical and pathological staging in head and neck squamous cell carcinoma: results from Intergroup Study ECOG 4393/RTOG 9614. Arch Otolaryngol Head Neck Surg, 2009. 135(9): p. 851-8. Kokemuller, H., P. Brachvogel, A. Eckardt, et al., [Effectiveness of neck dissection in metastasizing mouth carcinoma. Uni- and multivariate analysis of factors of influence]. Mund Kiefer Gesichtschir, 2002. 6(2): p. 91-7. Koo, B.S., Y.C. Lim, J.S. Lee, et al., Management of contralateral N0 neck in oral cavity squamous cell carcinoma. Head Neck, 2006. 28(10): p. 896-901. Kowalski, L.P. and A.L. Carvalho, Influence of time delay and clinical upstaging in the prognosis of head and neck cancer. Oral Oncol, 2001. 37(1): p. 94-8. Krabbe, C.A., P.U. Dijkstra, J. Pruim, et al., FDG PET in oral and oropharyngeal cancer. Value for confirmation of N0 neck and detection of occult metastases. Oral Oncol, 2008. 44(1): p. 31-6. Kreppel, M., Vergleichende retrospektive Untersuchung der neoadjuvanten Radiochemotherapie und der primär operativen Therapie bei Patienten mit Plattenepithelkarzinomen der Mundhöhle aus der Klinik für Mund-, Kiefer- und plastische Gesichtschirurgie der Universität zu Köln. Ref Type: Thesis/Dissertation, 2011. Kreppel, M., U. Drebber, H.T. Eich, et al., Combined-modality treatment in advanced oral squamous cell carcinoma: Primary surgery followed by adjuvant concomitant radiochemotherapy. Strahlenther Onkol, 2011. 187(9): p. 555-60. 74 73. 74. 75. 76. 77. 78. 79. 80. 81. 82. 83. 84. 85. Kreppel, M., U. Drebber, I. Wedemeyer, et al., Podoplanin expression predicts prognosis in patients with oral squamous cell carcinoma treated with neoadjuvant radiochemotherapy. Oral Oncol, 2011. 47(9): p. 873-8. Kreppel, M., H.T. Eich, A. Kubler, et al., Prognostic value of the sixth edition of the UICC's TNM classification and stage grouping for oral cancer. J Surg Oncol, 2010. 102(5): p. 443-9. Kreppel M, K.B., Scheer M, Drebber U, Zöller J. , Epitheliale Vorläuferläsionen - Die orale Leukoplakie. Oralchirurgie Journal, 2011: p. 6-13. Kreppel, M., M. Scheer, U. Drebber, et al., Impact of podoplanin expression in oral squamous cell carcinoma: clinical and histopathologic correlations. Virchows Arch, 2010. 456(5): p. 473-82. Kyzas, P.A., E. Evangelou, D. Denaxa-Kyza, et al., 18F-fluorodeoxyglucose positron emission tomography to evaluate cervical node metastases in patients with head and neck squamous cell carcinoma: a meta-analysis. J Natl Cancer Inst, 2008. 100(10): p. 712-20. Lee, H.W., E.H. Kim, and M.H. Oh, Clinicopathologic implication of ezrin expression in non-small cell lung cancer. Korean J Pathol, 2012. 46(5): p. 470-7. Leslie, A., E. Fyfe, P. Guest, et al., Staging of squamous cell carcinoma of the oral cavity and oropharynx: a comparison of MRI and CT in T- and N-staging. J Comput Assist Tomogr, 1999. 23(1): p. 43-9. Liao CT, K.M., Prognostic Nomograms for 5-year Outcome in Patients with Oral cavity Cancer and Extracapsular Spread. Eingereicht zur Publikation in J Clin Oncol. 2013. Ling, Z.Q., K. Mukaisho, H. Yamamoto, et al., Initiation of malignancy by duodenal contents reflux and the role of ezrin in developing esophageal squamous cell carcinoma. Cancer Sci, 2010. 101(3): p. 624-30. Lonneux, M., G. Lawson, C. Ide, et al., Positron emission tomography with fluorodeoxyglucose for suspected head and neck tumor recurrence in the symptomatic patient. Laryngoscope, 2000. 110(9): p. 1493-7. Ma, L., Y.P. Liu, X.H. Zhang, et al., Relationship of RhoA signaling activity with ezrin expression and its significance in the prognosis for breast cancer patients. Chin Med J (Engl), 2013. 126(2): p. 242-7. Madan, R., M. Brandwein-Gensler, N.F. Schlecht, et al., Differential tissue and subcellular expressionof ERM proteins in normal and malignant tissues: cytoplasmic ezrin expression has prognostic signficance for head and neck squamous cell carcinoma. Head Neck, 2006. 28(11): p. 1018-27. Maier, M., Kraft K, Humane Papillomavirusinfektionen bei Plattenepithelkarzinomen des Kopf- und Halsbereichs. HNO, 2013: p. 593-601. 75 86. 87. 88. 89. 90. 91. 92. 93. 94. 95. 96. 97. 98. 99. 100. Mangeat, P., C. Roy, and M. Martin, ERM proteins in cell adhesion and membrane dynamics. Trends Cell Biol, 1999. 9(5): p. 187-92. Martin, T.A., G. Harrison, R.E. Mansel, et al., The role of the CD44/ezrin complex in cancer metastasis. Crit Rev Oncol Hematol, 2003. 46(2): p. 165-86. Martin-Villar, E., F.G. Scholl, C. Gamallo, et al., Characterization of human PA2.26 antigen (T1alpha-2, podoplanin), a small membrane mucin induced in oral squamous cell carcinomas. Int J Cancer, 2005. 113(6): p. 899-910. Marur, S., G. D'Souza, W.H. Westra, et al., HPV-associated head and neck cancer: a virus-related cancer epidemic. Lancet Oncol, 2010. 11(8): p. 781-9. Mashberg A, S.A., Early diagnosis of asymptomatic oral and oropharyngeal squamous cancers. CA Cancer J Clin, 1995: p. 328-51. Mashberg, A. and A. Samit, Early diagnosis of asymptomatic oral and oropharyngeal squamous cancers. CA Cancer J Clin, 1995. 45(6): p. 328-51. Mashino, K., N. Sadanaga, H. Yamaguchi, et al., Expression of chemokine receptor CCR7 is associated with lymph node metastasis of gastric carcinoma. Cancer Res, 2002. 62(10): p. 2937-41. Matthias, C., V. Jahnke, A.A. Fryer, et al., [First results on the influence of polymorphisms at glutathione S-transferase, cytochrome P450, and tumor necrosis factor gene loci on the development of multiple head and neck cancer]. Laryngorhinootologie, 2003. 82(1): p. 25-30. McClatchey, A.I., Merlin and ERM proteins: unappreciated roles in cancer development? Nat Rev Cancer, 2003. 3(11): p. 877-83. McGurk, M., Effective head and neck cancer management: a consensus document. Clin Otolaryngol Allied Sci, 1999. 24(3): p. 163. Metelmann, H.R., [Chemotherapy and radiochemotherapy in tumors of the head-neck area]. Mund Kiefer Gesichtschir, 2000. 4 Suppl 1: p. S155-9. Metelmann HR, K.W., Tumoren im Kopf-Hals-Bereich. Mund- KieferGesichtschirurgie, 2007. 4th ed(Elsevier): p. 670-753. Metz A, P.R., Schmeling C, Mohr C, Mundschleimhautkarzinom. Onkologie, 2012. 7(Springer Verlag): p. 46-53. Mhawech-Fauceglia, P., P. Dulguerov, A. Beck, et al., Value of ezrin, maspin and nm23-H1 protein expressions in predicting outcome of patients with head and neck squamous-cell carcinoma treated with radical radiotherapy. J Clin Pathol, 2007. 60(2): p. 185-9. Mohr, C., W. Bohndorf, H. Gremmel, et al., Preoperative radiochemotherapy and radical surgery of advanced head and neck cancers--results of a prospective, multicenter DOSAK study. Recent Results Cancer Res, 1994. 134: p. 155-63. 76 101. 102. 103. 104. 105. 106. 107. 108. 109. 110. 111. 112. 113. 114. 115. 116. 117. Moilanen, J., H. Lassus, A. Leminen, et al., Ezrin immunoreactivity in relation to survival in serous ovarian carcinoma patients. Gynecol Oncol, 2003. 90(2): p. 273-81. Molinolo, A.A., P. Amornphimoltham, C.H. Squarize, et al., Dysregulated molecular networks in head and neck carcinogenesis. Oral Oncol, 2009. 45(4-5): p. 324-34. Nahum, A.M., W. Mullally, and L. Marmor, A syndrome resulting from radical neck dissection. Arch Otolaryngol, 1961. 74: p. 424-8. Nakamoto, Y., K. Tamai, T. Saga, et al., Clinical value of image fusion from MR and PET in patients with head and neck cancer. Mol Imaging Biol, 2009. 11(1): p. 46-53. Neid M, T.A., Intraepitheliale Plattenepithelneoplasie (WHO 2005). HNO 2009: p. 181-8. Nemeth, Z., N. Velich, S. Bogdan, et al., The prognostic role of clinical, morphological and molecular markers in oral squamous cell tumors. Neoplasma, 2005. 52(2): p. 95-102. Neville, B.W. and T.A. Day, Oral cancer and precancerous lesions. CA Cancer J Clin, 2002. 52(4): p. 195-215. Niggli, V. and J. Rossy, Ezrin/radixin/moesin: versatile controllers of signaling molecules and of the cortical cytoskeleton. Int J Biochem Cell Biol, 2008. 40(3): p. 344-9. O'Sullivan, B. and J. Shah, New TNM staging criteria for head and neck tumors. Semin Surg Oncol, 2003. 21(1): p. 30-42. Ohtani, K., H. Sakamoto, T. Rutherford, et al., Ezrin, a membrane-cytoskeletal linking protein, is involved in the process of invasion of endometrial cancer cells. Cancer Lett, 1999. 147(1-2): p. 31-8. Ord, R.A. and R.H. Blanchaert, Jr., Current management of oral cancer. A multidisciplinary approach. J Am Dent Assoc, 2001. 132 Suppl: p. 19S-23S. Panje, W.R., A.J. Namon, E. Vokes, et al., Surgical management of the head and neck cancer patient following concomitant multimodality therapy. Laryngoscope, 1995. 105(1): p. 97-101. Park, H.R., S.K. Min, K. Min, et al., Differential expression of ezrin in epithelial skin tumors: cytoplasmic ezrin immunoreactivity in squamous cell carcinoma. Int J Dermatol, 2010. 49(1): p. 48-52. Partanen, T., Formaldehyde exposure and respiratory cancer--a meta-analysis of the epidemiologic evidence. Scand J Work Environ Health, 1993. 19(1): p. 8-15. Patara, M., E.M. Santos, A. Coudry Rde, et al., Ezrin expression as a prognostic marker in colorectal adenocarcinoma. Pathol Oncol Res, 2011. 17(4): p. 827-33. Patel, V., C. Leethanakul, and J.S. Gutkind, New approaches to the understanding of the molecular basis of oral cancer. Crit Rev Oral Biol Med, 2001. 12(1): p. 55-63. Petti, S., Lifestyle risk factors for oral cancer. Oral Oncol, 2009. 45(4-5): p. 340-50. 77 118. 119. 120. 121. 122. 123. 124. 125. 126. 127. 128. 129. Pujuguet, P., L. Del Maestro, A. Gautreau, et al., Ezrin regulates E-cadherindependent adherens junction assembly through Rac1 activation. Mol Biol Cell, 2003. 14(5): p. 2181-91. Reuther, T., N.K. Posselt, J. Rabbels, et al., [Oral squamous cell carcinoma Retrospective analysis of therapy results and prognosis by neoadjuvant, preoperative radio-chemotherapy]. Mund Kiefer Gesichtschir, 2006. 10(1): p. 18-29. Robbins, K.T., P. Kumar, J. Harris, et al., Supradose intra-arterial cisplatin and concurrent radiation therapy for the treatment of stage IV head and neck squamous cell carcinoma is feasible and efficacious in a multi-institutional setting: results of Radiation Therapy Oncology Group Trial 9615. J Clin Oncol, 2005. 23(7): p. 144754. Robbins, K.T., A.R. Shaha, J.E. Medina, et al., Consensus statement on the classification and terminology of neck dissection. Arch Otolaryngol Head Neck Surg, 2008. 134(5): p. 536-8. Roh, J.L., N.K. Yeo, J.S. Kim, et al., Utility of 2-[18F] fluoro-2-deoxy-D-glucose positron emission tomography and positron emission tomography/computed tomography imaging in the preoperative staging of head and neck squamous cell carcinoma. Oral Oncol, 2007. 43(9): p. 887-93. Rudert H. Maligne Tumoren der Lippen, d.M.h.u.d.O., Maligne Tumoren der Lippen, der Mundhöhle und des Oropharynx. Oto-Rhino-Laryngologie in Klinik und Praxis, 1992. 1.Ausgabe(Stuttgart: Thieme Verlag): p. S.648-669. Rudert H. Naumann H, H.J., Herberhold C, Kastenbauer E. , Maligne Tumoren der Lippen, der Mundhöhle und des Oropharynx. Oto-Rhino-Laryngologie in Klinik und Praxis, 1992. 1st ed(Thieme Verlag): p. 648-69. Saito, S., H. Yamamoto, K. Mukaisho, et al., Mechanisms underlying cancer progression caused by ezrin overexpression in tongue squamous cell carcinoma. PLoS One, 2013. 8(1): p. e54881. Schantz, S.P. and J.S. Ostroff, Novel approaches to the prevention of head and neck cancer. Proc Soc Exp Biol Med, 1997. 216(2): p. 275-82. Schantz, S.P. and G.P. Yu, Head and neck cancer incidence trends in young Americans, 1973-1997, with a special analysis for tongue cancer. Arch Otolaryngol Head Neck Surg, 2002. 128(3): p. 268-74. Schartinger, V.H., L. Kacani, J. Andrle, et al., Pharmacodiagnostic value of the HER family in head and neck squamous cell carcinoma. ORL J Otorhinolaryngol Relat Spec, 2004. 66(1): p. 21-6. Scheer, M., A.C. Kubler, N.N. Manawi, et al., [Endosonographic imaging of tumor thickness in oral squamous cell cancer and its effect on the incidence of lymph node metastases]. Mund Kiefer Gesichtschir, 2005. 9(5): p. 282-9. 78 130. 131. 132. 133. 134. 135. 136. 137. 138. 139. 140. 141. 142. Schimming, R., [Tumor angiogenesis--value and significance in squamous epithelial carcinoma of the mouth cavity]. Mund Kiefer Gesichtschir, 2002. 6(4): p. 217-30. Schlecht, N.F., M. Brandwein-Gensler, R.V. Smith, et al., Cytoplasmic ezrin and moesin correlate with poor survival in head and neck squamous cell carcinoma. Head Neck Pathol, 2012. 6(2): p. 232-43. Schuller, D.E., E. Ozer, A. Agrawal, et al., Multimodal intensification regimens for advanced, resectable, previously untreated squamous cell cancer of the oral cavity, oropharynx, or hypopharynx: a 12-year experience. Arch Otolaryngol Head Neck Surg, 2007. 133(4): p. 320-6. Schultze J, S.l.H., Roldan JC, Wiltfang J, Kimmig B, Die präoperative RadioChemo-Therapie beim fortgeschrittenen Mundhöhlenkarzinom. Die Kieler DÖSAKErfahrungen bezüglich Kurabilität und Lebensqualität. Mund Kiefer GesichtsChir 2006. 10(4): p. 249-257. Scully, C. and J. Bagan, Oral squamous cell carcinoma overview. Oral Oncol, 2009. 45(4-5): p. 301-8. Seitz, O., N. Chambron-Pinho, M. Middendorp, et al., 18F-FluorodeoxyglucosePET/CT to evaluate tumor, nodal disease, and gross tumor volume of oropharyngeal and oral cavity cancer: comparison with MR imaging and validation with surgical specimen. Neuroradiology, 2009. 51(10): p. 677-86. Shah, J.P. and Z. Gil, Current concepts in management of oral cancer--surgery. Oral Oncol, 2009. 45(4-5): p. 394-401. Shi, W., H. Kato, B. Perez-Ordonez, et al., Comparative prognostic value of HPV16 E6 mRNA compared with in situ hybridization for human oropharyngeal squamous carcinoma. J Clin Oncol, 2009. 27(36): p. 6213-21. Silverman, S., Jr., Demographics and occurrence of oral and pharyngeal cancers. The outcomes, the trends, the challenge. J Am Dent Assoc, 2001. 132 Suppl: p. 7S-11S. Spano, D., C. Heck, P. De Antonellis, et al., Molecular networks that regulate cancer metastasis. Semin Cancer Biol, 2012. 22(3): p. 234-49. Spiro, R.H., O. Guillamondegui, Jr., A.F. Paulino, et al., Pattern of invasion and margin assessment in patients with oral tongue cancer. Head Neck, 1999. 21(5): p. 408-13. Stokkel, M.P., F.W. ten Broek, and P.P. van Rijk, Preoperative assessment of cervical lymph nodes in head and neck cancer with fluorine-18 fluorodeoxyglucose using a dual-head coincidence camera: a pilot study. Eur J Nucl Med, 1999. 26(5): p. 499503. Tanaka, T. and R. Ishigamori, Understanding carcinogenesis for fighting oral cancer. J Oncol, 2011. 2011: p. 603740. 79 143. 144. 145. 146. 147. 148. 149. 150. 151. 152. 153. 154. 155. 156. 157. Todd, R., P.W. Hinds, K. Munger, et al., Cell cycle dysregulation in oral cancer. Crit Rev Oral Biol Med, 2002. 13(1): p. 51-61. Tokunou, M., T. Niki, Y. Saitoh, et al., Altered expression of the ERM proteins in lung adenocarcinoma. Lab Invest, 2000. 80(11): p. 1643-50. Tsukita, S., Y. Hieda, and S. Tsukita, A new 82-kD barbed end-capping protein (radixin) localized in the cell-to-cell adherens junction: purification and characterization. J Cell Biol, 1989. 108(6): p. 2369-82. Valastyan, S., A. Chang, N. Benaich, et al., Concurrent suppression of integrin alpha5, radixin, and RhoA phenocopies the effects of miR-31 on metastasis. Cancer Res, 2010. 70(12): p. 5147-54. Valderrama, F., S. Thevapala, and A.J. Ridley, Radixin regulates cell migration and cell-cell adhesion through Rac1. J Cell Sci, 2012. 125(Pt 14): p. 3310-9. van der Waal, I., Potentially malignant disorders of the oral and oropharyngeal mucosa; present concepts of management. Oral Oncol, 2010. 46(6): p. 423-5. Vormittag, L., D. Thurnher, S. Geleff, et al., Co-expression of Bmi-1 and podoplanin predicts overall survival in patients with squamous cell carcinoma of the head and neck treated with radio(chemo)therapy. Int J Radiat Oncol Biol Phys, 2009. 73(3): p. 913-8. Wagener A, M.l.O., Molekulare Onkologie. 2010. 3. Aufl: p. 351. Wang, J., L. Xi, J.L. Hunt, et al., Expression pattern of chemokine receptor 6 (CCR6) and CCR7 in squamous cell carcinoma of the head and neck identifies a novel metastatic phenotype. Cancer Res, 2004. 64(5): p. 1861-6. Wang, L., G.N. Lin, X.L. Jiang, et al., Expression of ezrin correlates with poor prognosis of nasopharyngeal carcinoma. Tumour Biol, 2011. 32(4): p. 707-12. Wang, S.J., S.G. Patel, J.P. Shah, et al., An oral cavity carcinoma nomogram to predict benefit of adjuvant radiotherapy. JAMA Otolaryngol Head Neck Surg, 2013. 139(6): p. 554-9. Weijers, M., G.B. Snow, D.P. Bezemer, et al., The status of the deep surgical margins in tongue and floor of mouth squamous cell carcinoma and risk of local recurrence; an analysis of 68 patients. Int J Oral Maxillofac Surg, 2004. 33(2): p. 146-9. Wennerberg, J. and U. Mercke, Growth potential of acoustic neuromas. Am J Otol, 1989. 10(4): p. 293-6. Wentzensen N, v.K.D.M., Virale Kanzerogenese von Kopf-Hals- Tumoren. Der Pathologe, 2004: p. 21-30. Wiley, H.E., E.B. Gonzalez, W. Maki, et al., Expression of CC chemokine receptor-7 and regional lymph node metastasis of B16 murine melanoma. J Natl Cancer Inst, 2001. 93(21): p. 1638-43. 80 158. 159. 160. 161. 162. 163. Wittekindt C, M.H., Bootz F, Kopf-Hals- Tumoren, TNM-Klasifikation maligner Tumoren, 6 ed. Berlin: Springer,. 2003: p. 19-53. Woolgar, J.A., S.N. Rogers, D. Lowe, et al., Cervical lymph node metastasis in oral cancer: the importance of even microscopic extracapsular spread. Oral Oncol, 2003. 39(2): p. 130-7. Yao, M., J.B. Epstein, B.J. Modi, et al., Current surgical treatment of squamous cell carcinoma of the head and neck. Oral Oncol, 2007. 43(3): p. 213-23. Yen, T.C., J.T. Chang, S.H. Ng, et al., Staging of untreated squamous cell carcinoma of buccal mucosa with 18F-FDG PET: comparison with head and neck CT/MRI and histopathology. J Nucl Med, 2005. 46(5): p. 775-81. Zackrisson, B., C. Mercke, H. Strander, et al., A systematic overview of radiation therapy effects in head and neck cancer. Acta Oncol, 2003. 42(5-6): p. 443-61. Zeng, H., L. Xu, D. Xiao, et al., Altered expression of ezrin in esophageal squamous cell carcinoma. J Histochem Cytochem, 2006. 54(8): p. 889-96. 81 7 Anhang 7.1 Tabellenverzeichnis Tabelle 1: Klinische TNM-Klassifikation der siebten Auflage 11 Tabelle 2: Stadiengruppierung für Karzinome der Lippen und Mundhöhle der 12 siebten Auflage Tabelle 3: Histopathologisches Grading der siebten Auflage 12 Tabelle 4: Definitionen des C-Faktors der siebten Auflage 13 Tabelle 5: Definitionen der R-Klassifikation der siebten Auflage 14 Tabelle 6: Altersverteilung des gesamten Patientenkollektivs bei Diagnosestellung 38 Tabelle 7: Statistische Altersangaben des gesamten Patientenkollektivs (80 Patienten) 40 bei Erstdiagnose Tabelle 8: Prozentuale Verteilung der Risikofaktoren im Gesamtkollektiv 40 Tabelle 9: Lokalisation des Primärtumors 41 Tabelle 10: T-Stadium des Primärumors 43 Tabelle 11: N-Stadium des Primärtumors 44 Tabelle 12: Anzahl der Kapseldurchbrüche des Tumors 45 Tabelle 13: Häufigkeits- und prozentuale Verteilung des UICC-Stadiums 46 Tabelle 14: Häufigkeits- und prozentuale Verteilung der Differenzierungsgrade der 47 Tumoren des Gesamtkollektivs Tabelle 15: Tumorresektionsränder des Gesamtkollektivs 48 Tabelle 16: Vorkommen von Lymphangiosis carcinomatosa 48 Tabelle 17: Ezrinexpression im Primärtumor 49 Tabelle 18: Ezrinlokalisation im Primärtumor 50 Tabelle 19: Assoziationen der Ezrinexpression und Patientencharakterisitika 53 Tabelle 20: Ezrinlokalisation und Patientencharakteristika 55 Tabelle 21: Einfluss epidemiologischer Parameter auf das Überleben 56 Tabelle 22: Einfluss der T-Klassifikation auf das Überleben 57 Tabelle 23: Einfluss der N-Klassifikation auf das Überleben 57 Tabelle 24: Einfluss der UICC-Klassifikation auf das Überleben 58 Tabelle 25: Einfluss des ECS auf das Überleben 58 Tabelle 26: Einfluss des Differenzierunggrades auf das Überleben 58 82 Tabelle 27: Einfluss der Lymphangiosis carcinomatosa auf das Überleben 59 Tabelle 28: Einfluss der Ezrinlokalisation auf das Überleben 59 Tabelle 29: Einfluss der Ezrinexpression auf das Überleben 60 Tabelle 30: Multivariate Analyse der prognostischen Faktoren auf das Gesamtüberleben 60 Tabelle 31: Multivariate Analyse der prognostischen Faktoren auf das Gesamtüberleben 61 83 7.2 Abbildungsverzeichnis Abbildung 1: Anatomische Bezirke [158] 10 Abbildung 2: Einteilung der Lymphknotengruppen [74] 16 Abbildung 3: Mechanismen der lymphatischen Metastasierung [69] 18 Abbildung 4: Sequenzanalyse der ERM-Proteine [108] 24 Abbildung 5: Aktivierungs- und Funktionsmodell der ERM-Proteine [10] 25 Abbildung 6: Semiquantitative Auswertung der Präparate 37 Abbildung 7: Altersverteilung des gesamten Patientenkollektivs (80 Patienten) 39 bei Diagnosestellung Abbildung 8: Tabakabusus des Gesamtkollektivs 40 Abbildung 9: Alkoholabusus des Gesamtkollektivs 41 Abbildung 10: Lokalisation des Primärtumors des Gesamtkollektivs 42 Abbildung 11: Prozentuale Verteilung des T-Stadiums im Gesamtkollektiv 43 Abbildung 12: Prozentuale Verteilung des N-Stadiums am Gesamtkollektiv 44 Abbildung 13: Prozentuale Verteilung der Anzahl der Kapseldurchbrüche 45 im Gesamtkollektiv Abbildung 14: Prozentuale Verteilung des UICC-Stadiums am Gesamtkollektiv 46 Abbildung 15: Prozentuale Verteliung des Differenzierungsgrades im Gesamtkollektiv 47 Abbildung 16: Prozentuale Verteilung der Tumorresektionsränder im Gesamtkollektiv 48 Abbildung 17: Prozentuale Verteilung des Vorhandenseins der 49 Lymphangiosis carcinomatosa im Gesamtkollektiv Abbildung 18: Prozentuale Verteilung der Ezrinexpression des Primärtumors 50 im Gesamtkollektiv Abbildung 19: Prozentuale Verteilung der Ezrinlokalisation des Primärtumors im Gesamtkollektiv 84 51 8 Lebenslauf Mein Lebenslauf wird aus Gründen des Datenschutzes in der elektronischen Fassung meiner Arbeit nicht veröffentlicht. 85 Gedruckt durch: Copy Shop Mensa Nassestraße 1 53113 Bonn 86