pdf-file, 2.8 MB
Werbung

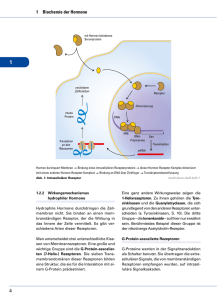
Block 3 Physiologie Intrazelluläre Signalübertragung I 1 Objectives • Nenne die wichtigsten intrazellulären Signalübertragungswege • Beschreibe die Funktionsweise von G-protein gekoppelten Rezeptoren • Beschreibe Auslösung und Folge von Ca++ Signalen • Beschreibe Auslösung und Folge von cAMP Signalen • Beschreibe Auslösung und Folge von Signalen über Rezeptor Tyrosin Kinasen 2 1 Inhalte • – – – • • • • • Allgemeine Prinzipien der Zellkommunikation Signaltransduktion Botenstoffe Rezeptortypen Mechanismen der Signaltransduktion Signalübertragung durch Rezeptor-Tyrosin-Kinasen Signalübertragung durch G-Protein gekoppelte Rezeptoren Konzept der second messenger Botenstoffe Transport in den Zellkern 3 Kombinationen von Signalmolekülen bestimmen das Zellverhalten 4 2 Signalübertragung über Botenstoffe 1. 2. 3. 4. 5. 6. Synthese des Botenstoffes: lipophile meist im Cytoplasma, Peptidhormone und hydrophile Botenstoffe meist im ER Freisetzung (Sekretion): lipophile durch Diffusion durch die Cytoplasma-Membran, hydrophile durch sekretorische Granula Transport zur Zielzelle: a) über den Blutkreislauf b) durch Diffusion Bindung an spezifische Rezeptoren: a) an der Zelloberfläche b) intrazellulär (z.B. Transkriptionsfaktoren) Aktivierung eines intrazellulären Signals: oft über Adapterproteine, sekundäre Botenstoffe, Signalkaskaden Ausschalten des Signals (und Entfernung des Botenstoffes): a) Endozytose und Abbau von Rezeptor und/oder Ligand b) Enzymatische Inaktivierung des Botenstoffs oder Deaktivierung von Signalmolekülen (z.B. Dephosphorylierung, Spaltung von GTP bei GProteinen...) 5 Formen der Signalübertragung • • endokrin: Der Signalstoff wird von endokrinen Organen (z.B. Drüsen) freigesetzt, die nicht direkt neben den Zielzellen liegen (Übertragung meist über den Blutkreislauf) Blutgefäß endokrine Drüse Zielzellen parakrin: Der Signalstoff wirkt auf benachbarte Zellen (Übertragung meist über Diffusion) sezernierende Zelle • • autokrin: Der Signalstoff wirkt auf die Zelle, die ihn sezerniert hat. benachbarte Zielzelle Zielorte auf der gleichen Zelle direkter Zellkontakt: Der Signalstoff ist membrangebunden und bindet an einen Rezeptor einer anderen Zelle (z.B. immunologische Synapse). signalisierende Zelle empfangende Zelle 6 3 Unterschiede endokriner und synaptischer Signalübertragung 7 8 4 Signalmolekülklassen – Proteine - Wachstumsfaktoren (EGF, FGF, VEGF, PDGF), Cytokine (Interleukine, TNF, TGF, Interferone) – Peptide - Insulin, Glucagon, Gastrin – Aminosäuren, -derivate - Histamin, Adrenalin, Neurotransmitter – Eicosanoide - Prostaglandine, Thromboxane, Leukotriene – Second messenger - Ca2+, cAMP, cGMP, IP3, DAG, NO, CO 9 Hormone I • lipophile Hormone: z.B. Steroide wie Progesteron (durchdringen die Zellmembran durch Diffusion und binden an intrazelluläre „Rezeptoren“ z.B. Transkriptionsfaktoren) Progesteron • Retinsäure hydrophile Peptid-Hormone: können nicht durch die Membran diffundieren und binden an Zelloberflächen-Rezeptoren: z.B. Insulin, Glucagon, Wachstumsfaktoren: werden oft aus einer inaktiven Proform gebildet 10 5 Hormone II • kleine hydrophile Hormone: z.B. Adrenalin, Serotonin, Histamin Serotonin (5-Hydroxytryptamin) • Histamin lipophile Hormone mit zelloberflächen-Rezeptoren: z.B. Prostaglandine, Thromboxane und Leukotriene. 11 Überblick über Rezeptoren • G-Protein gekoppelte Rezeptoren (z.B. Adrenalin- oder SerotoninRezeptoren) • Ionenkanalrezeptoren (z.B. Acetylcholinrezeptor) • Tyrosin-Kinase gekoppelte Rezeptoren (z.B. Interferon-Rezeptoren): aktivieren intrazelluläre Tyrosin-Kinasen • Rezeptoren mit eigener Enzymaktivität: z.B. Rezeptor-Tyrosinkinasen Rezeptor G-Protein 12 6 Sekundäre Botenstoffe (Second Messenger) werden meist intrazellulär gebildet oder freigesetzt, wenn bestimmte Botenstoffe entsprechende Rezeptoren und Signalwege aktivieren. Übertragen oder verstärken das Signal intrazellulär: • • • • • cAMP: cyclisches Adenosin-3‘,5‘ monophosphat cGMP: cyclisches Guanosin-3‘,5‘ monophosphat DAG: 1,2-Diacylglycerin IP3: Inositol-1,4,5-triphosphat Ca2+ .... 13 „ Molekulare Schalter“ Phosphorylation/Dephosphorylation Tyrosin-Proteinkinasen Serin/Threonin-Proteinkinasen Phosphatasen GTPasen Ubiquitin/SUMO 14 7 GTPasen als „Schaltproteine“ 1. trimere G-Proteine binden an G-Protein gekoppelte Rezeptoren und übertragen das Signal an Effektorproteine (z.B. Adenylatzyklasen) 2. Kleine GTPasen (Ras-ähnlich) 6 Familien: Ras, Rho, Rab, Ran, ARF und RGK: aktive Form: GTP-gebunden, inaktive: GDP GEF: guanine nucleotide exchange factors: tauschen GDP gegen GTP GAP: GTPase Aktivierende Proteine blau: α cyan: β grün: γ gelb: GDP 15 16 8 Adapterproteine ... haben keine eigene Enzymaktivität, können aber an Rezeptoren oder Signalenzyme (z.B. Kinasen) binden und dadurch das Signal weiterleiten oder regulieren. ... haben meist Interaktionsdomänen: z.B.: SH2-oder PTB-Domänen (binden an phosphorylierte Tyrosinreste), SH3- und WWDomänen (binden an prolinreiche Sequenzen), PH-Domänen binden an Phosphoinoside.... Die Kombination von Adapterdomänen mit Enzymaktivitäten (z.B. Kinasedomänen) bietet eine sehr hohe Flexibilität der Signalübertragung. SH2-Domäne von Grb-2 P-Tyrosin-Peptid Prolin-reiche Sequenz SH3-Domäne 17 Rezeptor-Tyrosinkinasen ... dimerisieren nach Bindung des Liganden (z.B. einem Wachstumshormon), wodurch es zur gegenseitigen Phosphorylierung von Tyrosinresten auf der cytoplasmatischen Domäne kommt und zur Bindung von Adapterproteinen an die P-TyrReste über SH2-Domänen (Grb2 – Sos). Dadurch werden weitere Signalmoleküle aktiviert (GTPase Ras) und das Signal wird an weitere Signalwege weitergeleitet (MAPK-Kaskade) 18 9 Enzyme linked Receptor 19 20 10 Enzyme linked Receptor Unterfamilien der Rezeptor-Tyrosin-Kinasen 21 Ras Aktiverung Ras funktioniert als molekularer Schalter 22 11 Signalübertragung von der Zellmembran in den Zellkern II: RTK-Ras-MAPK-Weg ... aktivierte MAP-Kinasen wandern als Dimere in den Kern und aktivieren dort durch Phosphorylierung verschiedene Transkriptionsfaktoren (Jun, Fos, ATF-2, TCF, SRF...) Aktivierung von MAP Kinasen 23 24 12 Block 3 Physiologie Intrazelluläre Signalübertragung II 25 Objectives • Nenne wichtige Signaltransduktionswege welche über Zytokinrezeptoren vermittelt werden • Beschreibe die Mechanismen der Aktivierung des Nuclear Faktor-kappa B (NF-κB) • Erkläre die Bedeutung des Transportes von Proteinen in den bzw. aus dem Zellkern. • Erkläre die Freisetzung und Wirkung von NO 26 13 LDL IL-1 IL-6 IL-8 ELAM VACM ICAM RANTES TF O- Radicals Amyloid AGE beta RAGE TNF IL-1 LPS TNF-R Il-1-R CD14 Apoptosis IkB IAPs P Ubiquitin NFkB iNOS NO Sap COX-2 Gene Transcription CRE Ankyrin repeats Proliferation G1 cyclins E GC IRF-1 IL-8 GRE AP-1 E-Selectin HMG-1 +1 NF/IL6 NF-κB ATF-2 p65/cR EL NFκB PAI-1 NF-κB p65/p50/HMG-1 p65/p50 NF-κB IRF-1 p65/p50 SP-1 +1 +1 VCAM-1 NF-κB NF/IL6 P91/p91 p65/cREL +1 ICAM-1 NF-κB TF β-IFN p65/cREL AP-1 ATF-2 IRF-1 +1 SP-1 NF-κB p65/p50 +1 28 14 Scheme of the NF-κB signaling pathway TNFα TNFα TNFR1 TNFR1 FADD TNFR2 TRAF2 apoptosis TNFR... FADD... TRADD ... TRAF... NIK... MEKK1... IKK... NEMO... NF-κB... IκB... TRAF2 TRADD Procaspase 8 MEKK1 Tumor necrosis factor receptor Fas associated death domain protein TNFR associated death domain protein TNFR associated factor NF-κB inducing kinase MAPK/ERK kinase kinase 1 IκB kinase NF-κB essential modulator Nuclear transcription factor κB Inhibitor of NF-κB MEKK1 TRAF1 NIK P TNFR2 NIK P IKKγ (ΝΕΜΟ) IKK1 IKK2 IκB p50 p65 Ubiquitinylation Degradation in proteasomes NF-κB Transcription p50 p65 29 Johannes A. Schmid Kernporenkomplex 30 15 Ran-Lokalisation Modell für Kernimport 31 32 16 Modell für Kernexport 33 NO (Stickstoffmonoxid) und cGMP als sekundäre Botenstoffe Acetylcholine führt in Endothelzellen über Ca/Calmodulin zur Bildung von NO (aus Arginin). Dieses diffundiert zu benachbarten glatten Muskelzellen des Blutgefäßes, wo es an der Membran eine Guanylatzyklase aktiviert. Der Anstieg des cGMP in den Zellen führt zu einer Muskelrelaxation und Erweiterung der Blutgefäße. Guanylatzyklase: NO bindet an die Hämgruppe und aktiviert das Enzym 34 17 Bildung von NO durch unterschiedliche NO-Synthasen • eNOS - endotheliale NOS • nNOS -neuronal NOS • iNOS - inducible NOS – – – – Activation by shear stress, Acetylcholine, Kinins Maintainance of relaxed state of vasculature Inhibition of platelet and white cell adhesion Suppression of smooth muscle cell proliferation – Activation by Glutamate, NO-Release from Neurons – Regulation of local blood flow in the brain – Neuronal induced vasodilation in the urogenital tracts – Released from Monocytes and endothelial cells – Host defence against protozoa, bacteria, fungi, virus – Increased levels in septic shock, inflammation, arthritis, asthma, brain traum 35 PKA Src Ca++ α β PI4P PI3 K SOS PLCγ IP 3 Integrins FGF EGF cAMP PLC PI3, 4P ILK FAK Src PDK2 cas pax Tyrosine Ras-GTP 14-3-3 substrates PKCε cPLA TNFR1 CBP/p3oo CREB 12 HETE RAF Ö MEK 4/7 ERK-1/2 8 Cycl D p50 p65 NF-κB P NAK--1 NAK P P IKK1 IKK2 TAB¾ TAK JNK MEK 3/6 P3 Nab--2 Nab Gene transcription Ö ¾ Antiapoptotic genes Inflammatory mediators Gene transcription TRAF2 TRAF1 NI PKC K NI K PKR NEM O p PAK XIAP P TFs,, Myc TFs NFAT Procaspase 8 TNFR2 TRADD TRAF2 Cdc42/RAC PPARγγ PPAR EGR--1 EGR FAD D apoptosis MEKK1 Akt 2 Calcineurin lipoxygenase MEK-1/2 NFAT LTbR TNFα RTK VEGF GCK Gαs Lox-1 Gαq GCK Ox PL IkB p50 p65 ubiquitination NF-κB degradation in proteasomes p50 p65 NF-κB ELAM VCAM Rantes IL-1, IL-6, IL-8 iNOS COX-2 PAI-1 36 Tissue factor 18 Bei Unklarheiten und Fragen hinsichtlich des Prüfungsstoffes: Prof. B. Binder Tel. 4277-62502 mail: [email protected] andere Fragen: Johannes Schmid Tel. 4277-62555 mail: [email protected] 37 G-Protein gekoppelte Rezeptoren (GPCR) Membranproteine mit 7 TransmembranRegionen. Liganden: meist kleine hydrophile Botenstoffe (binden zwischen den Helices). Intrazelluläre Bindungspartner: trimere G-Proteine (binden an C3, C2-Schleifen und CTerminus). Funktionen: GlucoseMetabolismus (durch Adrenalin etc. geregelt), schnelle Signalübertragungen (Muskelkontraktion, Herzfrequenz.. 38 19 G-Protein gekoppelter Rezeptor • Adenylatcyclase – Alpha-s und alpha-i • Phospholipase C – Alpha-q • Phosphodiesterase – Alpha-t • Rho-Aktivierung – Alpha-12 • K-Kanäle – Beta/gamma 39 Signalübertragung über G-Proteine Gγ G β Gsα 5. das Hormon dissoziiert vom Rezeptor, durch GTP-Hydrolyse löst sich Gsα vom Effektorenzym und bindet wieder an Gβγ 1. Hormonbindung induziert eine Konformationsänderung des Rezeptors 4. Gsα bindet an das Effektorenzym (Adenylatzyklase) und aktiviert es (zur cAMPSynthese) 15_5 GPCR.mov 2. G-Protein bindet über Gsα an den Rezeptor 3. durch die Bindung an den Rezeptor ändert sich die Struktur des Gsα und GDP wird durch GTP ersetzt, Gsα dissoziiert von Gβγ ab. 40 20 Signalübertragung über G-Proteine II Oft sind Effektorenzyme (z.B. Adenylatzyklase) ebenso wie G-Protein gekoppelte Rezeptoren Membranproteine mit mehreren Transmembranregionen. Da die G-Proteine selbst über Lipidketten in der Membran verankert sind, sind die Diffusionsstrecken zwischen GPCR und dem Effektorenzym gering. Durch die enzymatische Aktivität und die Bildung vieler sekundärer Botenstoffe (cAMP-Moleküle) kommt es zu einer deutlichen Signalverstärkung Schematische Darstellung der Adenylatzyklase 41 Es gibt stimulatorische und inhibitorische G-Proteine (Gs und Gi) 42 21 GPCR und Cholera 43 Verstärkungskaskade 44 22 45 Effekte sekundärer Botenstoffe: cAMP Aktivierung cAMPabhängiger Kinasen (PKA, Protein Kinase A): im Ruhezustand als Tetramer inaktiv (2 regulatorische, 2 katalytische Einheiten), Bindung von cAMP (kooperativ) an die regulatorischen Einheiten führt zur Dissoziation und Aktivierung der katalytischen Einheiten 46 23 Signalübertragung von der Zellmembran in den Zellkern: PKA/CREB-Weg ... die katalytischen Einheiten der aktivierten PKA wandern in den Kern und phosphorylieren, bzw. aktivieren den Transkriptionsfaktor CREB (cAMPresponsive element binding protein), der gemeinsam mit einem Kofaktor (CBP, CREB binding protein) and Promoterelemente bindet (CRE, cAMP responsive elements) und die Transkription bestimmter Gene induziert. 47 48 24 GPCR Desensibilisierung 49 Rezeptordesensibilisierung 50 25 Sekundäre Botenstoffe: Phosphatidylinosit-Derivate cytosol. Seite der ZytoplasmaMembran Diacylglycerin (DAG) Membranständige PI-Kinasen bilden die PI-Derivate PIP und PIP2, Spaltung von PIP2 durch das Signalenzym Phopholipase C (PLC) führt zur Bildung der second 51 messenger IP3 (Inositol 1,4,5-Triphosphat) und DAG (Diacylgyzerin) Wirkung von IP3 auf den Calcium-Spiegel Rekrutierung von PKC an die Zellmembran PLC kann durch HormonBindung an GPCR über trimere G-Proteine aktiviert werden. Dies führt zur Freisetzung von IP3 ins Cytosol und Bindung von IP3 an Calciumkanäle des ER, die dadurch geöffnet werden. Das ausströmende Calcium fördert wiederum das Öffnen von Calciumkanälen an der Zelloberfläche (Verstärkungseffekt). Die Erhöhung der intrazellulären Calcium-Konzentration führt zur Fixierung Ca-abhängiger Proteinkinase C-Formen (PKC) an die Zellmembran, wo es durch DAG aktiviert wird und Rezeptoren oder andere Substrate phosphoryliert. 52 26 Inositol-Phospholipid vermittelte Signaltransduktion 15_6 IP3.mov 53 Calcium/Calmodulin Calmodulin ist ein kleines Ca-bindendes Protein (16.7 kD) mit 4 Bindungstellen für Calcium. Wenn alle Bindungsstellen besetzt sind nimmt es eine gestreckte helikale Konformation ein, bei niedrigeren Konzentrationen oder gebunden an andere Proteine, kann es eine globuläre Form einnehmen. Calmodulin bei voller CalciumBeladung Calmodulin gebunden an eine Peptidhelix 54 27 Calciumsignale Calciumwelle/Calmodulin 55 Calciumfreisetzung und Entfernung aus dem Cytosol 56 28