Die Grätzel – Zelle
Werbung

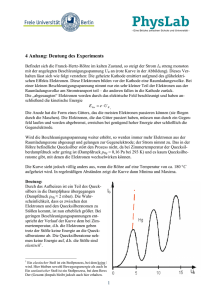
1 Pflanzenphysiologische Übungen WS 07 Die Grätzel – Zelle Ein Weg zur integrativen Gestaltung des Biologieunterrichts Verfasst von Dr. Robert Kartusch Unter Mitwirkung von Assmann Daniela Beguin Andreas Fürnkranz Michael 2 Die Grätzel – Zelle Konventionelle photovoltaische Zellen beruhen auf den halbleitenden Eigenschaften bestimmter Elemente, wo durch Licht Elektronen angeregt werden und gleichzeitig Ladungstrennung an n- und p- Stellen stattfinden kann. Dafür sind Materialien von besonderer Reinheit notwendig, was die Fertigung von photovoltaischen Anlagen sehr kostenintensiv macht – ein wesentlicher Grund, daß Anlagen dieser Art keine breitere Verwendung finden. Nanokristalline Solar-Zellen, die von der Arbeitsgruppe um Michael Grätzel in Lausanne entwickelt wurden, arbeiten nach einem anderen Prinzip. Lichtabsorption und Ladungstrennung sind hier getrennt. Lichtabsorption wird zunächst von Farbstoffmolekülen übernommen, die an Titandioxid-Partikel adsorbiert sind. Die durch Licht angeregten Elektonen werden in ein Leitungsband des Titandioxids eingespeist und können von dort in ein leitendes Trägermaterial gelangen, zweckmäßiger Weise ein mit Metalloxid beschichtetes leitfähiges Glas. Die in den Farbstoffmolekülen entstehenden positiven Ladungen werden über einen Vermittler ausgeglichen, der wiederum Elektronen von einer Gegenelektrode übernehmen kann. Neben ihrer praktischen Bedeutung liegt der Wert dieser einfach zu bauenden photovoltaischen Elemente in der Möglichkeit, damit naturwissenschaftliche Grundlagen aus Physik, Chemie und Biologie integrativ im Unterricht anschaulich vermittelbar zu machen. 1. Halbleiter Halbleiter sind Stoffe, bei denen das sog. „Valenzband“ vollständig aufgefüllt ist und die zusätzlich noch freie“Leitungsbänder“, in denen sich Elektronen frei bewegen können, besitzen. Im Gegesatz zu einem Isolator ist die Energiedifferenz zwischen Valenz- und Leitungsband nicht sehr groß, so daß einzelne Elektronen in das Leitungsband gelangen können. An Stellen mit e-Defizit (p) und e-Überschuss (n) baut sich ein elektrisches Feld auf (p-n junktion), das den Ladungsausgleich verhindert und bei Anregungsvorgängen Elektronen dazu zwingt, das Leitungsband zu bevölkern. Nähere Angaben zu Halbleitern unter www.science-forum.de (Bau und Funktionsweise einer Grätzel-Zelle, Sekundarstufe I). Titandioxid ist ein Halbleiter, dessen Eigenschaften in Bezug auf Photokatalyse und Photokonversion seit längerer Zeit Gegenstand intensiver Forschung sind. Für sich allein sind die Anwendungsmöglichkeiten beschränkt. Die Energiedifferenz (band gap) zwischen Valenz- und Leitunsbahn ist relativ hoch (3.2 eV), so daß nur 5% der im Sonnenlicht enthaltenen Photonen diese Energie aufbringen (z. B. ist eV/Photon zw. 420 und 490 nm etwa 2.7), zum anderen ist die interne Rekombinationsgeschwindigkeit der Ladungsträger groß, so daß die Effizienz der Ladungstrennung gering ist. Durch Sensibilisierung , i.e., Adsorption von Farbstoffen an Nanopartikel von TiO2, können diese Schwierigkeiten umgangen werden, da die durch Licht angeregten Elektronen der Farbstoffmoleküle in das Leitungsband des TiO2 eingespeist werden können. Anregungsvorgang und Ladungstrennung werden dadurch räumlich getrennt. ausgenutzt werden können der bei der Grätzel-Zelle in nanokristalliner Form auf eine Trägerschicht aus leitfähigem Glas aufgebracht wird. 2. Licht Es ist im Bewußtsein der Öffentlichkeit viel zu wenig verankert, daß es eine Wertigkeit der Energieformen gibt. Strahlungs- bzw. Lichtenergie nimmt dabei den obersten Rang ein, und Licht ist der eigentliche Motor des Lebens auf der Erde. Die Geschichte des Lebens begann damit, als es gelang, mit Hilfe geeigneter Moleküle Licht in andere Energieformen, primär in elektrische Energie, umzuwandeln. 3. Wechselwirkung von Materie mit Licht Für die Wechselwirkung mit Licht sind vor allem leicht delokalisierbare Elektronen Vorrausetzung. Bei organischen Molekülen findet sich diese Möglichkeit bei Elektronen, die an Doppelbindungen teilnehmen, speziell bei sog. konjugierter Anordnung (mehrere durch jeweils eine Einfachbindung getrennte Doppelbindungen), wodurch zusätzlich eine Möglichkeit zur Resonanzstabilisierung des angeregten Zustands geschaffen wird. Anzahl und Anordnung der Doppelbindungen und das Vorhandensein zusätzlicher Substituenten bestimmen, in welchen Spektralbereich Licht absorbiert wird und wie stark die Wechselwirkung mit Licht ist. 4. Photochemische Reaktionsmechanismen Absorbtion von Licht führt zur Entstehung sog. Anregungszuständen, d. h., Zuständen, wo sich ein Valenzelektron auf einer eigenen, energiereichen Bahn bewegt. Moleküle in einem solchen Zustand sind im Prinzip Radikale und daher sehr reaktionsfähig. Es gibt verschiedene Möglichkeiten, diesen angeregten Zustand wieder zu verlassen, entweder durch physikalische Abgabe der Anregungsenergie (Fluoreszenz, Phosphoreszenz) oder durch diverse chemische Reaktionsmechanismen, u. a. durch Übertragung des angeregten Elektrons auf einen Akzeptor. 5. Biologisch wichtige lichtabsorbierende Farbstoffe Hier bietet sich die Möglichkeit, Bau und Chemismus der Farbstoffe mit ihrer Funktion zu verknüpfen. 3 Bau einer Grätzelzelle im Experiment Herstellung der Titandioxid-Suspension Etwa 12 g Titanoxid (Degussa P 25) werden in einer Reibschale mit verdünnter Säure (2 ml konz. Essigsäure und 3 ml a.d.) mit 12 – 15 ml a.d. zu einem homogenen Brei verrührt. Wichtig ist eine portionsweise Zugabe (1 – 2 ml) des Wassers. Die Säure ist wichtig für die Stabilisierung der kolloidalen Suspension. Der Brei kann in eine Injektionsspritze gefüllt werden. Dadurch erleichtert sich einerseits die Handhabung, anderseits kann die Suspension leichter aufbewahrt werden. Aufbringen der Titanodixid-Schicht TOC („tin oxid coated“) – Glas kann im Prinzip im Bauhandel (Isolierglas) bezogen werden. Meist ist aber nur schwer verarbeitbares Material mit etwa 5 mm Dicke erhältlich. Glas mit 2.5 mm Dicke konnte aus den U.S.A. bezogen werden (Hartford Glass, Hartford, CT, U.S.A.). Widerstand der leitfähigen Schicht sollte etwa 25 – 30 Ohm/cm betragen. Das Glas wird in rechteckige Stücke von ca. 2 x 3 cm geschnitten. Zur Beschichtung wird ein Stück mit den längeren Seiten zwischen zwei größeren Glasplatten gleicher Dicke fixiert. Die Schichtdicke wird durch Klebeband (Scotch) definiert, das an den anliegenden Rändern der Glasplatten angebracht wird und das gleichzeitig für die Fixierung sorgt. Ein schmales Ende der zu beschichtenden Platte wird in etwa 5 mm Breite ebenfalls durch Klebeband freigehalten. Die Titanoxidsuspension wird auf die Glasplatte aufgebracht und mit Hilfe eines Glasstabes gleichmäßig verstrichen. Die Titanoxidschicht wird anschließend in einem Muffelofen bei 450 °C ( 10 min) gesintert. Sensibilisieren der Schicht Zur Sensibilisierung von Titandioxid durch Naturstoffe eignen sich Farbstoffe von Blüten, Blättern oder Früchten, Anthocyane oder der grüne Blattfarbstoff Chlorophyll. Die Gewinnung der Anthocyane ist einfach ( z.B. Heißwasserextrakte von Büten, Tees, Rotkraut oder dergl.). Der Farbstoff adsorbiert sich rasch und in hoher Konzentration an das Titanoxid, wobei oft ein Farbumschlag des Farbstoffs an der Schicht zu beobachten ist (rot nach blau, Hinweis auf die basische Natur des Titanoxids). Die Herstellung der Chlorophyllösung ist aufwendiger, aber didaktisch wertvoll, da eine unmittelbare Beziehung zur Photosynthese besteht. Die Blattfarbstoffe werden mit Aceton am einfachsten aus Spinatblättern (frisch oder tiefgekühlt) extrahiert und anschließend in einer Benzinphase angereichert (zur Vorgangsweise siehe gängige Praktikumsliteratur). Der Benzinextrakt bietet die Möglichkeit zur chromatographischen Trennung der Blattfarbstoffe (Xanthophylle, Chlorophyll a und b, Carotin) und zur präparativen Reindarstellung. Aus dem Aceton- bzw. Benzinextrakt adsorbiert sich das Chloropyll kaum an das Titanoxid, da es durch die Veresterung mit dem Phytolalkohol noch stark lipohil ist und kaum Bindungsstellen besitzt. Durch Verseifung wird der lipophile Phytolrest abgespalten, gleichzeitig wird am Porphyrinring eine Carboxylgruppe frei. Zur Verseifung werden in einem Reagensglas einige ml Benzinextrakt mit 5 – 8 Tropfen konz. methanolischer KOH versetzt. Die Lösung verfärbt sich zunächst bräunlich, nach einiger Zeit setzt sich das jetzt wasserlösliche Chlorophyllin am Boden der Eprouvette ab. Der gelbe Überstand kann leicht abdekantiert werden, der Niederschlag wird mit etwas Benzin nachgewaschen. Es empfiehlt sich, gleich mehrere Reagensgläser vorzubereiten. Zur Sensibilisierung der Titanoxidschicht löst man den Niederschlag in 4 – 5 ml reinem Ethylalkohol und bringt die beschichtete Glasplatte in diese Lösung ein. Der grüne Farbstoff adsorbiert sich jetzt leicht an das Titanoxid. Nach der Sensibilisierung werden die Plättchen im Luftstrom eines Föns getrocknet. 4 Der Elektrolyt Der Elektrolyt besteht aus einer Jod-Jodkalilösung (0.5 M KJ plus 0.05 M Jod; in wässriger (Lugol) oder in nichtwässriger (Ethylenglycol o.a.) Lösung). Er übernimmt die Rolle der Elektronenübermittlung zwischen dem oxydiertem Farbstoff und der Gegenelektrode nach dem Schema Gegenelektrode J3- + 2e- zu 3 JFarbstoff-Elektrode 3 J- zu J3- + 2eFox + 2 e- zu Fred Dem Elektrolyten kommt insofern eine wichtige Rolle zu, da die Spannungsdiferenz, die von der Zelle erzeugt werden kann, letzlich von der Potentialdifferenz zwischen der Leitungsbahn im Titandioxid und dem Jodid/J2 abhängig ist, und diese wiederum vom Zustand des Titanoxids und dem für den Elektrolyten verwendeten Lösungsmittel. Um den Stromfluß zwischen den Elektroden mit einer zufriedenstellender Rate zu ermöglichen, wird die Gegenelektrode durch Graphitisierung vorbereitet. Der Kohlenstoff katalysiert die Elektronenübertragung von der leitenden Schicht des Glases zum Elektrolyten. Am besten eignet sich dafür ein weicher Bleistift, optimal erwiesen sich Bleistifte der Marke FABER-CASTELL 9000 HB. Auf die beschichtete Platte werden mit einer Pipette einige Tropfen Elektrolytlösung aufgebracht und die Gegenelektrode luftblasenfrei überlappend aufgelegt. Die beiden Platten werden mit Klammern fixiert. An den freien Schmalseiten kann die Zelle über Krokodilklemmen mit dem Meßinstrument verbunden werden. Ergebnisse Bei Belichtung kann nun ein Strom gemessen werden. Bei Kunstlicht konnten Spannungen um die 400 mV gemessen werden. Die beiden Farbstoffe verhielten sich im wesentlichen gleich. Auffallend war, daß der Spannung nicht linear mit der Lichtintesität zunahm, der Anstieg verflachte sich bei hohen Lichtintensitäten Bei Serienschaltung von drei einzelnen Zellen waren Spannungen bis 1.5 V zu erzielen. Bei mit Chlorophyll sensibilisierten Zellen konnten bei vollem Sonnenlicht Spannungen um 600 mV und ein Strom von 0.7 mA gemessen werden, allerdings nur kurzfristig, die Zelle verlor ziemlich rasch an Leistung. Gleichzeitig war eine Entfärbung (Abnahme der braunen Jodfarbe) des Elektrolyten zu beobachten, was auf Nebenreaktionen, ev. mit dem Lösungsmittel (hier : Glycerin) hindeutet. Mit Hilfe von farbigen Folien als Filter läßt sich bei mit Chlorophyll sensibilisierten Zellen die Abhängigkeit der Spannung von der Lichtfarbe demonstrieren, die dem Absorptionsspektrum des Chlorophylls folgt Grätzel - Zelle, mit Anthocyan (Rotkraut) sensibilisiert Strom - Spannungscharakteristik 350 0.5 300 0.4 250 Strom (mA) Spannung ( mV ) Grätzel - Zelle, mit Anthcyan (Rotkraut) sensibilisiert Abhängigkeit der Spannung von der Lichtintensität 200 0.3 0.2 150 0.1 100 0.0 50 0 50 100 150 200 250 300 -2 Lichtintensität ( W m ) Wellenlängenabhängigkeit der erzeugten Spannung 350 0 50 100 150 200 Spannung (mV) 250 300 350 5 Literatur Woyke, Andreas, Die Grätzel-Zelle: Aufbau, Funktionsweise und Bau. Science Forum : www.science-forum.de. Smestad, Greg P., 1998, Education and solar conversion : Demonstrating electron transfer. Solar Energy Materials and solar cells 55: 157 – 178 Dank Der Praktikumsleiter Dr. Robert Kartusch dankt der Fa. Degussa , insbesonders Frau Sandra Lasser, für die großzügige Bereitstellung des Titandioxids.