Lasix ® 250 mg/500 mg
Werbung

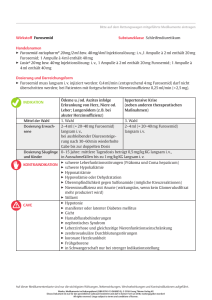
Fachinformation des Arzneimittel-Kompendium der Schweiz® Lasix® 250 mg/500 mg Sanofi-Aventis (Suisse) SA AMZV Zusammensetzung Tabletten Wirkstoff: Furosemidum. Hilfsstoffe: Maisstärke, Lactose-Monohydrat, mikrokristalline Cellulose, Natriumstärkeglykolat (Typ C), Talkum, kolloidales Siliciumdioxid wasserfrei, Magnesiumstearat, Farbstoff: E 104 (Chinolingelb). Ampullen Wirkstoff: Furosemidum ut Furosemidum natricum. Hilfsstoffe: pro 25 ml (pH-Wert um 9) Mannitolum, Aqua ad iniectabilia. Galenische Form und Wirkstoffmenge pro Einheit Tabletten à 500 mg. Ampullen à 250 mg. Indikationen/Anwendungsmöglichkeiten Die hochdosierten Formen von Lasix sind zur Diuresesteigerung ausschliesslich für Patienten mit stark verminderter Glomerulumfiltration (GFR <20 ml/min) angezeigt. Drohende und bereits eingetretene akute Niereninsuffizienz, zur Aufrechterhaltung der Diurese und zur Erleichterung der parenteralen Ernährung, solange noch eine Restfiltration vorhanden ist. Chronische Niereninsuffizienz im prädialytischen Stadium mit Flüssigkeitsretention und Hochdruck. Terminale Niereninsuffizienz zur Aufrechterhaltung einer Restdiurese. Nephrotisches Syndrom bei Patienten, die auf eine orale Dosis von Lasix bis 120 mg/Tag nicht ansprechen. Beim nephrotischen Syndrom steht die Therapie der Grunderkrankung im Vordergrund. Dosierung/Anwendung Im Allgemeinen soll die Dosierung so gering wie möglich gehalten werden, um den gewünschten Effekt zu gewährleisten. Bei i.v. Therapie wird empfohlen, so bald als möglich auf orale Therapie umzustellen. Für eine optimale Wirksamkeit und um eine Gegenregulation zu unterdrücken wird generell eine Dauerinfusion gegenüber wiederholten Bolusinjektionen bevorzugt. Für Kinder und Säuglinge sollen niedrig dosierte Furosemid-Präparate verwendet werden (Lasix Tabletten à 40 mg und Kapseln à 30 mg). Lasix 250 mg (Infusionslösung) Akutes Nierenversagen: Bei Patienten mit Schock sind vor Beginn der Behandlung durch geeignete Massnahmen die Hypovolämie und die Hypotonie zu beseitigen. Ebenso ist eine deutlich ausgeprägte Störung der Serumelektrolyte und des Säure-Basen-Gleichgewichts zu korrigieren. Führt eine Tagesdosis von 40 mg Furosemid, langsam intravenös injiziert, nicht zur vermehrten Diurese, so kann die Behandlung mit Lasix 250 mg begonnen werden. Mittels eines Perfusors können über den Tag pro Stunde 50-100 mg Furosemid appliziert werden. Die Tagesdosis richtet sich nach einer ausreichenden Diurese, wobei die Maximaldosis nicht höher als 1'500 mg/Tag sein sollte. Chronische Niereninsuffizienz im prädialytischen Stadium mit Flüssigkeitsretention und Hochdruck, nephrotisches Syndrom: Da die natriuretische Antwort von zahlreichen Variabeln abhängt, z.B. Grad der Niereninsuffizienz, Natriumbilanz usw., und daher prinzipiell im Einzelfall nicht präzise vorhergesagt werden kann, sollte die korrekte Dosis am besten durch stufenweise Erhöhung der Dosis ermittelt werden. Wegen des raschen Wirkungseintritts kann die Dosis in ½ bis stündlichen Abstand gesteigert werden. Die empfohlene Anfangsdosis sollte 0,1 mg/min als Infusion betragen. Da bei den chronisch niereninsuffizienten Patienten die Ausschwemmung langsam erfolgen sollte, ist die Dosis so zu wählen, dass der Patient in der Bilanz pro Tag etwa 2 kg Gewicht (280 mmol Na+) verliert. Lasix 500 mg (Tabletten) Chronische Niereninsuffizienz im prädialytischen Stadium mit Flüssigkeitsretention und Hochdruck: Bei ungenügendem Ansprechen auf eine orale Dosis von 120 mg (3 Tabletten Lasix zu 40 mg) pro Tag kann auf Lasix 500 mg Tabletten übergegangen werden. Dabei kann die Tagesdosis von 250 mg (½ Tablette Lasix 500 mg) bis zu 1'500 mg (3 Tabletten) in Ausnahmefällen bis zu 2'000 mg (4 Tabletten) gesteigert werden. Bei Dialyse-Patienten richtet sich die Dosis nach der Restdiurese und dem Körpergewicht. Die Tagesdosis liegt im Allgemeinen zwischen 250 mg und 1'500 mg (½-3 Tabletten Lasix 500 mg). Nephrotisches Syndrom: Bei ungenügendem Ansprechen auf eine orale Dosis von 120 mg (3 Tabletten Lasix 40 mg) pro Tag kann auf Lasix 500 mg Tabletten übergegangen werden. Im Allgemeinen beträgt die Tagesdosis 250-500 mg (½-1 Tablette Lasix 500 mg). Bei drohendem und bereits eingetretenem akutem Nierenversagen: Um eine bedarfsgerechte Dosierung sicherstellen zu können, sollte Lasix zunächst intravenös verabreicht werden. Ist eine länger dauernde Gabe von Lasix notwendig und zeigt es sich im klinischen Verlauf, dass eine Umstellung auf die Tablettenform möglich ist, so sollte sich die Dosierung auch bei oraler Gabe am notwendigen Effekt orientieren. Es wird empfohlen, 1'500 mg Lasix als Höchstdosis in 24 Stunden nicht zu überschreiten. Anwendungshinweise (siehe «Sonstige Hinweise», Inkompatibilitäten). Lasix 250 mg Infusionslösung ist in aller Regel über einen Perfusor zu applizieren. Bei Bedarf kann die Lasix Infusionslösung mit isotonischer Natriumchloridlösung verdünnt werden. Die Infusionsgeschwindigkeit von Furosemid darf 4 mg pro Minute nicht überschreiten. Bei Patienten mit fortgeschrittener Niereninsuffizienz (Serumkreatinin >5 mg/dl) sollte die Infusionsrate von 2,5 mg/min nicht überschritten werden. Die Einnahme der Lasix 500 mg Tabletten sollte unzerkaut, nüchtern mit reichlich Flüssigkeit erfolgen. Die Teilung der Tabletten wird durch drei Bruchkerben erleichtert. Über die Dauer der Behandlung entscheidet der Arzt bzw. die Ärztin. Sie richtet sich nach Art und Schwere der Erkrankung. Kontraindikationen Bei Patienten mit normaler Nierenleistung dürfen Lasix 250 mg Infusionslösung bzw. 500 mg Tabletten nicht angewendet werden, da in diesen Fällen die Gefahr eines zu starken Flüssigkeits- und Elektrolytverlustes besteht. Nierenversagen mit fehlender Harnproduktion (Anurie); Coma und Präcoma hepaticum; schwere Hypokaliämie, schwere Hyponatriämie, Hypovolämie sowie Dehydratation mit oder ohne begleitende Hypotonie; Überempfindlichkeit gegen Furosemid, Sulfonamide oder einen der Hilfsstoffe; Stillzeit. Warnhinweise und Vorsichtsmassnahmen Während der Therapie ist eine sorgfältige Überwachung der Elektrolyte und Flüssigkeitsbilanz generell zu empfehlen. Kreatinin und Harnstoff im Blut sowie Plasmaelektrolyte, insbesondere Kalium, Kalzium, Chlorid und Bikarbonat sind regelmässig zu kontrollieren. Besondere Überwachung ist bei Patienten mit hohem Risiko von Elektrolytstörungen notwendig sowie im Fall von zusätzlichem Flüssigkeitsverlust durch z.B. Schwitzen, Durchfall oder Erbrechen. Der Kohlenhydratstoffwechsel ist zu überwachen. Eine besonders sorgfältige Überwachung ist erforderlich bei: erniedrigtem Blutdruck; besonders sorgfältige Überwachung ist bei Patienten angezeigt, die durch einen bedeutenden Blutdruckabfall besonders gefährdet wären (z.B. Patienten mit signifikanten cerebrovaskulären oder koronaren Stenosen); latentem oder manifestem Diabetes mellitus (regelmässige Blutzuckerkontrolle); Gicht (regelmässige Harnsäurekontrolle); Behinderung des Harnabflusses (z.B. bei Prostatahypertrophie, Ureterstenose, Hydronephrose), Harnabfluss muss gewährleistet sein; gleichzeitigem Vorliegen von Leberzirrhose und Nierenfunktionseinschränkung (hepatorenalem Syndrom); Hypoproteinämie (z.B. bei nephrotischem Syndrom), vorsichtige Dosistitration ist erforderlich; Seite 1 Fachinformation des Arzneimittel-Kompendium der Schweiz® Frühgeborenen (Möglichkeit der Entwicklung von Nephrolithiasis und Nephrokalzinose; Kontrolle der Nierenfunktion und Nierensonographie). Wird Furosemid bei Patienten mit leichter Hypokaliämie oder Hyponatriämie eingesetzt, so sollte gleichzeitig eine entsprechende Elektrolytsubstitution erfolgen. Eine Hypovolämie oder Dehydratation muss ausgeglichen werden, ebenso signifikante Elektrolytstörungen und Störungen des Säure-BaseHaushalts. Bei Patienten mit einer Teilobstruktion des Urin-Stream (z.B. Patienten mit einer Störung der Blasenentleerung, Prostata-Hyperplasie oder Verengung der Harnröhre), kann die Erhöhung der Urinproduktion die Schmerzen verursachen oder verschlimmern. Deshalb benötigen diese Patienten eine besondere Überwachung. Gleichzeitige Anwendung von Risperidon In placebokontrollierten Studien mit Risperidon wurde bei älteren Patienten mit Demenz, die mit Furosemid plus Risperidon behandelt wurden, eine höhere Mortalitätsrate (7,3%; mittleres Alter 89 Jahre, Altersspanne 75-97 Jahre) im Vergleich zu Patienten, die Risperidon allein (3,1%; mittleres Alter 84 Jahre, Altersspanne 70-96 Jahre) oder Furosemid allein (4,1%; mittleres Alter 80 Jahre, Altersspanne 67-90 Jahre) erhalten hatten, beobachtet. Die Erhöhung der Mortalitätsrate bei Patienten, die mit Furosemid plus Risperidon behandelt wurden, wurde in zwei von vier klinischen Studien beobachtet. Die gleichzeitige Anwendung von Risperidon und anderen Diuretika (hauptsächlich Thiazid-Diuretika in niedriger Dosierung) zeigte solche Befunde nicht. Es konnte kein pathophysiologischer Mechanismus zur Erklärung dieser Beobachtung identifiziert und kein einheitliches Muster der Todesursachen festgestellt werden. Dennoch ist Vorsicht angezeigt und sind Risiken und Nutzen dieser Kombination oder der gleichzeitigen Behandlung mit anderen potenten Diuretika vor Therapieentscheidung abzuwägen. Bei Patienten, die andere Diuretika als begleitende Behandlung zu Risperidon einnahmen, wurde keine erhöhte Mortalitätsrate gefunden. Unabhängig von der Behandlung war Dehydratation ein allgemeiner Risikofaktor für Mortalität und muss daher bei älteren Patienten mit Demenz vermieden werden (siehe «Kontraindikationen»). Bei Patienten, die mit Furosemid behandelt werden, kann Lupus erythematodes aktiviert werden oder ein vorbestehender Lupus erythematodes kann sich verschlimmern. Interaktionen Nicht empfohlene Kombinationen Die Ototoxizität von Aminoglykosid-Antibiotika (z.B. Kanamycin, Gentamycin, Tobramycin) und anderen ototoxischen Substanzen kann sich bei gleichzeitiger Anwendung von Furosemid erhöhen. Dabei auftretende Hörstörungen können irreversibel sein. Deshalb sollte die gleichzeitige Anwendung vitalen Indikationen vorbehalten bleiben. In einzelnen Fällen kann es nach intravenöser Gabe von Furosemid innerhalb von 24 Stunden nach Einnahme von Chloralhydrat zu Hitzegefühl, Schweissausbruch, Unruhe, Übelkeit, Blutdruckanstieg und Tachykardie kommen. Deshalb wird die gleichzeitige Anwendung von Furosemid und Chloralhydrat nicht empfohlen. Kombinationen unter Vorsichtsmassnahmen oder besonderer Aufmerksamkeit Manche Elektrolytstörungen (z.B. Hypokaliämie, Hypomagnesiämie) können die Toxizität von bestimmten anderen Substanzen (z.B. Digitalispräparate und Medikamente, welche das QT-Intervallverlängerungssyndrom induzieren können) erhöhen. Bei gleichzeitiger Anwendung von Glukokortikoiden, Laxantien (über längere Zeit) oder Carbenoxolon ist zu berücksichtigen, dass es zu einem verstärkten Kaliumverlust kommen kann. Lakritze wirkt in dieser Hinsicht wie Carbenoxolon. Furosemid kann die toxischen Effekte nephrotoxischer Arzneimittel (z.B. Aminoglykoside, Cephalosporine, Polymyxine) verstärken. Bei Patienten mit antibiotikainduzierter Nierenschädigung sollte Furosemid daher mit Vorsicht eingesetzt werden. Bei gleichzeitiger Anwendung von Furosemid und Cisplatin ist mit der Möglichkeit eines Hörschadens zu rechnen. Wird bei einer Cisplatinbehandlung eine forcierte Diurese mit Furosemid angestrebt, so darf Furosemid nur in niedriger Dosis (z.B. 40 mg bei normaler Nierenfunktion) und bei positiver Flüssigkeitsbilanz eingesetzt werden. Andernfalls kann es zu einer Verstärkung der Nephrotoxizität von Cisplatin kommen. Furosemid kann die Wirkung anderer Medikamente abschwächen (z.B. den Effekt von Antidiabetika und von blutdruckerhöhenden Sympathomimetika (z.B. Epinephrin, Norepinephrin) oder verstärken (z.B. Theophyllin, Lithium [durch verminderte Lithiumausscheidung erhöhte kardio- und neurotoxische Wirkung] und kurareartigen Muskelrelaxanzien). Der Lithiumspiegel muss in Kombination mit Furosemid sorgfältig überwacht werden. Die Toxizität hochdosierter Salicylate kann durch Furosemid verstärkt werden. Die Wirkung von Antihypertensiva, Diuretika oder anderen blutdrucksenkenden Medikamenten kann durch Furosemid verstärkt werden. Insbesondere in Kombination mit ACE-Hemmern wurden starke Blutdruckabfälle bis hin zum Schock beobachtet. Patienten unter Diuretika können eine schwere Hypotonie und Verschlechterung der Nierenfunktion einschliesslich Nierenversagen erleiden, wenn ein ACE-Hemmer oder Angiotensin-II-Rezeptor-Antagonist zum erstenmal oder in einer höheren Dosis verabreicht wird. Die Lasix-Verabreichung soll vorübergehend unterbrochen oder in seiner Dosierung für 3 Tage reduziert werden, bevor ein ACE-Hemmer oder Angiotensin-II-Rezeptor-Antagonist gegeben oder deren Dosis gesteigert wird. Nichtsteroidale Antiphlogistika (z.B. Indometacin, Acetylsalicylsäure) können die Wirkung von Furosemid abschwächen und bei bestehender Hypovolämie oder Dehydratation zu akuten Nierenversagen führen. Phenytoin kann die Wirkung von Furosemid ebenfalls abschwächen. Probenecid, Methotrexat und andere Substanzen, die wie Furosemid einer signifikanten renal tubulären Sekretion unterliegen, können die Wirkung von Furosemid beeinträchtigen. Anderseits kann Furosemid die renale Ausscheidung dieser Substanzen verhindern. Bei hoher Dosierung von solchen Substanzen und von Furosemid kann dies zu einem erhöhten Serumspiegel führen und die Nebenwirkungen von Furosemid oder der gleichzeitigen Medikation verstärken. Sucralfat kann die Resorption von Furosemid beeinträchtigen. Die Einnahme muss 2 h voneinander getrennt erfolgen. Bei gleichzeitiger Behandlung mit Furosemid und bestimmten Cephalosporinen (z.B. Cephaloridine, Cephalotin) in hoher Dosierung kann die Nierenfunktion beeinträchtigt werden. Wegen der Furosemid induzierten Hyperurikämie und der durch Ciclosporin verursachten Verschlechterung der renalen Harnsäureausscheidung ist das Risiko einer Gichtarthritis unter gleichzeitiger Behandlung mit Ciclosporin und Furosemid erhöht. Patienten mit einem erhöhten Risiko für eine Röntgenkontrastmittel bedingte Nephropathie hatten nach Behandlung mit Furosemid ohne vorherige intravenöse Hydrierung eine erhöhte Inzidenz von Nierenfunktionsstörungen im Vergleich zu Patienten, die vor der Röntgenkontrastmittelapplikation intravenös hydriert wurden. Es wird empfohlen, dass mit Furosemid behandelte Patienten zur Senkung des Risikos für eine Röntgenkontrastmittel-bedingte Nephropathie vorgängig und anschliessend der Verabreichung von Kontrastprodukten mit physiologischer Kochsalzlösung hydriert werden. Risperidon: Vorsicht walten lassen und Risiken und Nutzen einer Kombination oder gleichzeitigen Behandlung mit Furosemid oder anderen potenten Diuretika vor Therapieentscheidung sorgfältig abwägen. Siehe «Warnhinweise und Vorsichtsmassnahmen» zur erhöhten Mortalität bei älteren Patienten mit Demenz, die gleichzeitig Risperidon eingenommen hatten. Levothyroxin: Hohe Dosen von Furosemid können die Bindung von Schilddrüsenhormonen an Transportproteinen inhibieren und führen dadurch anfänglich zu einem vorübergehenden Anstieg an freien Schilddrüsenhormonen und folglich zu einer allgemeinen Reduktion des gesamten Schilddrüsenhormonspiegels. Der Schilddrüsenhormonspiegel ist zu überwachen. Schwangerschaft/Stillzeit Furosemid passiert die Placenta und erreicht im Nabelschnurblut 100% der maternalen Serumkonzentration. Bisher sind keine Fehlbildungen beim Menschen bekannt geworden, die mit einer Furosemid-Exposition in Zusammenhang stehen könnten. Es liegen jedoch zur abschliessenden Beurteilung einer eventuellen schädigenden Wirkung auf den Embryo/Fötus keine ausreichenden Erfahrungen vor. Im Fötus kann dessen Urinproduktion in utero stimuliert werden. Es existieren keine kontrollierte Humanstudien. Tierstudien haben unerwünschte Effekte auf den Fötus gezeigt (Embryotoxizität, pharmakologisch bedingt durch die Elektrolytverarmung). Lasix sollte während der Schwangerschaft nicht angewendet werden, es sei denn es ist klar notwendig. Eine Behandlung muss kurzfristig und unter besonders strenger Indikationsstellung erfolgen. Eine Behandlung während der Schwangerschaft erfordert die Überwachung des Foetuswachstums. Furosemid geht in die Muttermilch über und hemmt die Laktation. Deshalb wird von der Anwendung von Lasix in der Stillzeit abgesehen; wenn eine zwingende Indikation für Furosemid vorliegt und keine risikoärmere Alternative, wird das Abstillen empfohlen. Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von Maschinen Sowohl durch eine Senkung des Blutdrucks als auch durch andere der untengenannten Nebenwirkungen kann die Fähigkeit zur aktiven Teilnahme am Strassenverkehr oder zum Bedienen von Maschinen beeinträchtigt werden. Dies gilt in verstärktem Masse bei Behandlungsbeginn und Präparatewechsel sowie im Zusammenwirken mit Alkohol. Unerwünschte Wirkungen Die Häufigkeitsangaben sind Veröffentlichungen zu Studien entnommen, in denen insgesamt 1'387 Patienten Furosemid inmit unterschiedlichen Dosierungen und Indikationen erhalten haben. Wenn eine Nebenwirkung dabei in unterschiedlicher Häufigkeit beobachtet wurde, wird hier die höchste beobachtete Seite 2 Fachinformation des Arzneimittel-Kompendium der Schweiz® Häufigkeitskategorie angegeben. Je nach Bedarf werden folgende Häufigkeitsangaben gemäss CIOMS-Einteilung verwendet: Sehr häufig: ≥10%; Häufig: ≥1 und <10%; Gelegentlich: ≥0,1 und <1%; Selten: ≥0,01 und <0,1%; Sehr selten: <0,01%; Nicht bekannt: (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar) Erkrankungen des Blutes und des Lymphsystems Häufig: Hämokonzentration mit Thromboseneigung, vor allem bei älteren Menschen. Gelegentlich: Thrombozytopenie mit potenziell verstärkter Blutungsneigung. Selten: Leukopenie, Eosinophilie. Sehr selten: Agranulozytose mit erhöhter Infektionsneigung; hämolytische oder aplastische Anämie. Erkrankungen des Immunsystems Gelegentlich können allergische Reaktionen auftreten. Grundsätzlich können sich diese allergischen Reaktionen als Haut- und Schleimhautreaktionen (z.B. Pruritus, Urtikaria und andere Hautausschläge, bullöses Pemphigoid, Erythema multiforme, Dermatitis exfoliativa, Purpura) äussern, aber auch in Form fieberhafter Zustände. Selten: anaphylaktische und anaphylaktoide Reaktionen, die potenziell lebensbedrohlich werden können (z.B. durch Herzversagen), wurden nur nach intravenöser Gabe beschrieben.* Nicht bekannt: Verschlimmerung oder Aktivierung des systemischen Lupus erythematodes. Stoffwechsel- und Ernährungsstörungen Sehr häufig: Störungen des Elektrolythaushalts (einschliesslich symptomatischer Störungen); erhöhtes Serumkreatinin; erhöhter Triglyceridspiegel im Blut. Nach einer Diurese kann es vor allem bei älteren Patienten und Kindern zu Hypovolämie oder Dehydratation kommen; häufig begleitet von Symptomen wie Kopfschmerzen, Schwindel, Schwäche, Apathie, Verwirrung, Schläfrigkeit oder Sehstörungen. Häufig: Hyponatriämie, Hypochlorämie, Hypokaliämie, erhöhter Cholesterinspiegel im Blut, erhöhter Harnsäurespiegel im Blut, dadurch potenziell Gichtanfälle bei entsprechend prädisponierten Patienten. Gelegentlich: Die Behandlung mit Furosemid kann zur Verminderung der Glukosetoleranz führen. Bei Diabetikern kann dies in eine reine Verschlechterung der Stoffwechsellage resultierenzur Folge haben. In seltenen Fällen kann es dazu kommen, dass ein latenter Diabetes mellitus sich manifestiert. Nicht bekannt: Hypokalzämie, Hypomagnesiämie, erhöhter Harnstoffspiegel im Blut, potenzielle Verschlechterung einer vorbestehenden metabolischen Alkalose (z.B. bei dekompensierter Leberzirrhose) unter Furosemid. Pseudo-Bartter-Syndrom bei Furosemid-Abusus und/oder Langzeitbehandlung mit Furosemid. Erkrankungen des Nervensystems Häufig: hepatische Enzephalopathie bei Patienten mit Leberinsuffizienz. Selten: Parästhesie. Häufigkeit unbekannt: Es wurde über Fälle von Schwindel, Ohnmacht oder Bewusstlosigkeit und Kopfschmrezen berichtet. Erkrankungen des Ohrs und des Labyrinths Gelegentlich: reversible Hörstörungen. Mit dieser Möglichkeit muss vor allem bei zu schneller intravenöser Injektion gerechnet werden, insbesondere bei niereninsuffizienten Patienten. Es wurden Fälle von Schwerhörigkeit beschrieben, die gelegentlich nicht reversibel waren. Selten: Tinnitus aurium. Herzerkrankungen Ein Kaliummangel kann sich in kardialer Symptomatik, z.B. Reizbildungs- und Reizleitungsstörungen äussern. Bei erhöhten renalen Magnesiumverlusten wurden als Folge einer Hypomagnesiämie in seltenen Fällen Herzrhythmusstörungen beobachtet. Gefässerkrankungen Sehr häufig (bei intravenöser Injektion): Hypotonie einschliesslich orthostatischer Hypotonie. Selten: Vaskulitis. Nicht bekannt: Thrombose. Infolge Diurese kann es vor allem bei älteren Patienten und Kindern zu Hypovolämie oder Dehydratation mit Anzeichen und Symptomen wie z.B. Kreislaufbeschwerden, Hypotonie und orthostatischen Kreislaufregulationsstörungen kommen. Schwere Kaliumverluste können zu Bewusstseinsstörungen bis hin zum Koma führen. Erkrankungen des Gastrointestinaltrakts Gelegentlich: Übelkeit. Selten: Erbrechen, Durchfall. Sehr selten: In Einzelfällen kann akute Pankreatitis auftreten. Erbrechen, Verstopfung und Meteorismus können durch Kaliummangel bedingt sein. Appetitlosigkeit und Erbrechen können durch eine Hyponatriämie verursacht werden. Schwere Kaliumverluste können zu paralytischem Ileus führen. Infolge Diurese kann es vor allem bei älteren Patienten und Kindern zu Hypovolämie oder Dehydratation mit Anzeichen von Mundtrockenheit kommen. Affektionen der Leber und Gallenblase Sehr selten: Eine Erhöhung der Lebertransaminasewerte oder eine intrahepatische Cholestase können auftreten. Erkrankungen der Haut und des Unterhautzellgewebes (siehe auch «Erkrankungen des Immunsystems») Gelegentlich: Eine Lichtüberempfindlichkeit der Haut kann auftreten, ausserdem Pruritus/Juckreiz, Urtikaria, Exanthem, bullöse Dermatitis, Erythema multiforme, Pemphigoid, exfoliative Dermatitis, Purpura, Lichtempfindlichkeit. Unbekannte Häufigkeit: Stevens-Johnson-Syndrom, toxische epidermale Nekrolyse, AGEP (akute generalisierte exanthematische Pustulose) und DRESS (Hautausschlag mit Eosinophilie und systemischen Symptomen). Skelettmuskulatur- und Bindegewebs-Erkrankungen Ein Kaliummangel kann sich in neuromuskulärer Symptomatik, z.B. Muskelschwäche sowie in unvollständigen oder vollständigen Lähmungen äussern. Eine Hyponatriämie kann sich in Wadenkrämpfe äussern. Bei erhöhten renalen Magnesiumverlusten wurden als Folge einer Hypomagnesiämie in seltenen Fällen eine Tetanie beobachtet. Erhöhte renale Kalziumverluste können zu Hypokalzämie führen. Diese kann einen Zustand neuromuskulärer Übererregbarkeit, in seltenen Fällen mit Tetanie, auslösen. Häufigkeit unbekannt: Fälle von Rhabdomyolyse wurden berichtet, oftmals im Zusammenhang mit schwerer Hypokaliämie (siehe «Warnhinweise und Vorsichtsmassnahmen»). Erkrankungen der Nieren und Harnwege Häufig: erhöhtes Urinvolumen. Selten: tubulointerstitielle Nephritis. Nicht bekannt: Bei Frühgeborenen können Nephrolithiasis und Nephrokalzinose auftreten. Ein Kaliummangel kann sich in renaler Symptomatik, z.B. Polyurie und Polydipsie äussern. Bei Patienten mit Harnflussbehinderungen, kann eine akute Harnverhaltung auftreten. Schwangerschaft, Wochenbett und perinatale Erkrankungen Unbekannt: Erhöhtes Risiko eines persistierenden Ductus arteriosus bei Frühgeborenen mit Atemnotsyndrom bei einer diuretische Behandlung mit Furosemid in den ersten Lebenswochen. Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Seite 3 Fachinformation des Arzneimittel-Kompendium der Schweiz® Selten: Fieber. Unbekannt: Es können lokale Reaktionen mit Schmerz nach einer i.m. Injektion auftreten. Untersuchungen Als Folge der vermehrten Wasser- und Elektrolytausscheidung werden häufig Störungen im Flüssigkeits- und Elektrolythaushalt beobachtet. Hypokaliämie (bis zu 89% nach hohen parenteralen Dosen bei schweren Herzinsuffizienz-Patienten mit eingeschränkter Nierenfunktion), Hyponatriämie (in ca. 20%), Hypokalzämie (ca. 20%), Hypomagnesiämie (bis ca. 50%) bei magnesiumarmer Diät, Hypovolämie (ca. 15%) und metabolische Alkalose. Insbesondere bei gleichzeitig verminderter Kaliumzufuhr und/oder erhöhten extrarenalen Kaliumverlusten (z.B. durch Erbrechen oder chronischen Durchfall) kann als Folge erhöhter renaler Kaliumverluste eine Hypokaliämie auftreten. Ausserdem disponieren Erkrankungen wie z.B. Leberzirrhose zu Kaliummangelzuständen. Entsprechende Überwachung und Substitution sind daher erforderlich. Infolge erhöhter Natriumverluste über die Nieren kann es - insbesondere bei eingeschränkter Zufuhr von Kochsalz - zu einer Hyponatriämie kommen. Vorübergehend können Kreatinin und Harnstoff im Serum ansteigen. Ein Anstieg von Cholesterin und Triglyceriden im Blut kann unter Furosemid auftreten. * Therapie des Schocks Im Allgemeinen werden folgende Sofortmassnahmen empfohlen: Bei den ersten Anzeichen (Schweissausbruch, Übelkeit, Zyanose) Injektion unterbrechen, die Kanüle in der Vene belassen respektive einen venösen Zugang schaffen. Neben anderen gebräuchlichen Notfallmassnahmen Kopf-Oberkörper-Tieflage, Atemwege freihalten! Medikamentöse Sofortmassnahmen Sofort Epinephrin (Adrenalin) i.v.: Nach Verdünnen von 1 ml der handelsüblichen Epinephrin-Lösung 1:1'000 auf 10 ml wird zunächst davon 1 ml (= 0,1 mg Epinephrin) unter Puls- und Blutdruckkontrolle langsam injiziert (cave Herzrhythmusstörungen!). Die Gabe von Epinephrin kann wiederholt werden. Danach Glukokortikoide i.v.: z.B. 250-1'000 mg Prednisolon (oder die äquivalente Menge eines Derivates). Die Glukokortikoid-Gabe kann wiederholt werden (Gebrauchsinformation des Glukokortikoids beachten!). Anschliessend Volumensubstitution i.v.: z.B. Plasmaexpander, Humanalbumin, Vollelektrolytlösung. Weitere Therapiemassnahmen: künstliche Beatmung, Sauerstoffinhalation, Kalzium, Antihistaminika. Überdosierung Bei Einnahme von Überdosen besteht die Gefahr einer akuten Hypotonie infolge der Exsikkation (begleitet von deliranten Zustandsbildern) und Elektrolytdepletion durch exzessive Diurese. Die Behandlung besteht in Flüssigkeits- und Elektrolytsubstitution in Abhängigkeit vom Ausmass der Diurese (ggf. Kontrolle von Stoffwechselfunktionen). Bei Patienten mit Miktionsstörungen ist der Harnabfluss sicherzustellen. Bei Prostatikern gilt es zu beachten, dass durch eine plötzlich eintretende Harnflut eine Harnsperre mit akuter Überdehnung der Blase auftreten kann. Eigenschaften/Wirkungen ATC-Code: C03CA01 Wirkungsmechanismus/Pharmakodynamik Lasix ist ein stark, kurz und schnell wirkendes Schleifendiuretikum; es führt zu einer ausreichend vermehrten Diurese, auch bei beträchtlich eingeschränkter Glomerulumfiltration, Hypoalbuminämie und azidotischer Stoffwechsellage. Voraussetzung für die saluretische Wirksamkeit von Furosemid ist allerdings, dass die Substanz über einen Anionentransportmechanismus in das Tubuluslumen gelangt und hier mit dem in der luminalen Zellmembran vorhandenen Cotransportsystem, dem Na+2Cl- K+-Carrier, reagieren kann. Furosemid führt bei Herzinsuffizienz akut zu einer Senkung der Vorlast des Herzens durch Erweiterung der venösen Kapazitätsgefässe. Dieser frühe vaskuläre Effekt scheint durch Prostaglandine vermittelt zu sein und setzt eine ausreichende Nierenfunktion mit Aktivierung des Renin-Angiotensin-Systems und eine intakte Prostaglandinsynthese voraus. Darüber hinaus vermindert Furosemid durch seinen kochsalzausschwemmenden Effekt die beim Hypertoniker erhöhte Gefässreagibilität gegenüber Katecholaminen. Klinische Wirksamkeit Lasix führt dosisabhängig in Fällen z.B. bei beträchtlich eingeschränkter Glomerulumfiltration, Hypoalbuminämie und azidotischer Stoffwechsellage, bei denen auf andere Weise keine Diuresesteigerung zu erreichen ist, meist eine ausreichend vermehrte Natrium- und Wasserausscheidung herbei. Nach oraler Anwendung setzt der diuretische Effekt im Allgemeinen innerhalb der ersten Stunde ein. Die Wirkungsdauer beträgt 4-8 Stunden. Bei intravenöser Infusion beginnt die Mehrausscheidung bereits während der Applikation. Die Wirkungsdauer hängt von der Infusionszeit ab. Pharmakokinetik Absorption Lasix wird nach oraler Applikation zu ca. 65% absorbiert, dies entspricht auch der Bioverfügbarkeit. Bei Niereninsuffizienz wird die Absorption auf 43-46% reduziert. Maximale Serumkonzentrationen werden nach oraler Applikation von Lasix nach 60-120 Minuten erreicht. Distribution Das Verteilungsvolumen beträgt 10,0 ± 2,1 l. Lasix wird zu etwa 98% an Plasmaproteine gebunden. Furosemid passiert die Plazentarschranke und geht auch in die Muttermilch über. Der Bereich der optimalen Wirkkonzentration im Plasma richtet sich nach dem gewünschten diuretischen Effekt. Nach i.v. Infusion von 1'000 mg Lasix innerhalb von 4 Stunden (4 mg/min) bei Niereninsuffizienz (GFR <10 ml/min) wurden maximale Serumkonzentrationen von durchschnittlich 29 µg/ml berechnet. Metabolismus Im Stoffwechselprozess entstehen keine aktiven Metaboliten. Im Urin werden ca. 14% der verabreichten Substanz als Furosemidglukuronid wiedergefunden. Elimination Die Serumeliminationshalbwertszeit liegt bei ca. 1 h. Furosemid wird zu ca. 50-70% renal ausgeschieden, davon ca. 14% als Glukuronid. 24 h nach p.o. oder i.v. Applikation sind 95% bzw. 99% der verabreichten Dosis ausgeschieden. Bereich von optimalen Wirkkonzentrationen im Plasma Der Bereich der optimalen Wirkkonzentrationen richtet sich nach dem gewünschten diuretischen Effekt. Kinetik spezieller Patientengruppen Die Eliminationsrate von Furosemid wird durch eine 50%ige Reduktion der Nierenfunktion nicht verändert. Mit zunehmender Niereninsuffizienz kommen extrarenale Eliminationswege zur Wirkung (der biliäre Anteil kann mehr als 60% betragen). Bei chronische Niereninsuffizienz (GFR <10 ml/min.) betrug die terminale Halbwertszeit aus dem Serum 13,5 h. Dabei wurde eine Gesamtelimination von 56% der zugeführten Dosis in 24 h errechnet. Bei kombinierter hepatorenaler Insuffizienz wurde eine Halbwertszeit bis zu 20 Stunden bestimmt. Präklinische Daten Mutagenese/Karzinogenese Es liegen sowohl positive als auch negative Testergebnisse an Bakterien und Säugerzellen in-vitro vor. Eine Induktion von Gen- und Chromosomenmutationen wurde erst im zytotoxischen Konzentrationsbereich beobachtet. Langzeituntersuchungen an Ratte und Maus ergaben keine Hinweise auf ein tumorerzeugendes Potential. Reproduktionstoxizität Furosemid erzeugte keine Beeinträchtigung der Fertilität in Studien an männlichen und weiblichen Ratten. In Reproduktionsstudien an Ratten, Mäusen und Kaninchen kam es zu ungeklärten Aborte und Todesfälle der Muttertiere und der Föten. Bei Studien an Kaninchen und Ratten wurden bei den Föten eine erhöhte Anzahl von Hydronephrose beobachtet. Untersuchungen an Neugeborenen von Ratten haben eine verminderte Zahl von differenzierten Glomeruli gezeigt. Sonstige Hinweise Inkompatibilitäten Seite 4 Fachinformation des Arzneimittel-Kompendium der Schweiz® Die Lösung zur parenteralen Applikation enthält das Natriumsalz der Karbonsäure ohne Lösungsvermittler, sie zeigt eine pH-Wert um 9 und besitzt keine Pufferwirkung. Im pH-Bereich unter 7 kann somit der Wirkstoff ausfallen.Saure Lösungen dürfen daher mit Lasix nicht gemischt werden, besonders solche mit grosser Pufferkapazität, wie z.B. Vitamin C und B, Adrenalin oder Noradrenalin. Salze organischer Basen können durch Mischen mit Lasix aus ihrer Lösung gefällt werden, z.B. Lokalanästhetika, Alkaloide, Narkotika, Antihistaminika. Lasix darf nicht mit anderen Medikamenten in der Mischspritze verwendet werden. Besondere Lagerungshinweise Bei Raumtemperatur (15-25 °C) und vor Licht geschützt aufbewahren. Bei zu starker Lichteinwirkung kann es zu Verfärbungen der Tabletten (und Ampullen) kommen, wodurch die Wirksamkeit jedoch nicht beeinträchtigt wird. Das Arzneimittel darf nur bis zu dem auf der Packung mit «EXP» bezeichneten Datum verwendet werden. Falls der pH-Wert der gebrauchsfertigen Lösung im schwach alkalischen bis neutralen Bereich liegt, sind die Mischungen bis 24 Stunden haltbar. Arzneimittel für Kinder unzugänglich aufzubewahren! Hinweise für die Handhabung Alkalische, neutrale oder schwach saure Lösungen mit sehr geringer Pufferkapazität können mit Lasix im Allgemeinen gemischt werden, z.B. isotonische NaCl- und Ringer-Lösungen, Strophantin- und neutrale Glukose-Lösungen (cave: Glukose-Lösungen des Handels reagieren vielfach deutlich sauer). Die chemische und physikalische Stabilität der gebrauchsfertigen Zubereitung mit isotonischer Natriumchloridlösung wurde für 24 Stunden bei Raumtemperatur (15-25 °C) nachgewiesen. Aus mikrobiologischer Sicht sollte die gebrauchsfertige Zubereitung sofort verwendet werden, es sei denn, die Methode des Verdünnens schliesst das Risiko einer mikrobiellen Kontamination aus. Zulassungsnummer 36442, 36443 (Swissmedic). Zulassungsinhaberin sanofi-aventis (schweiz) ag, 1214 Vernier/GE. Stand der Information Oktober 2016. Packungen Menge CHF LASIX Inf Lös 250 mg/25ml i.v. 6 Ampullen 25 ml LASIX Tabl 500 mg 20 Stk Abgabekat. Rückerstattungskat. B 39.20 B SL Publiziert am 21.11.2016 Seite 5