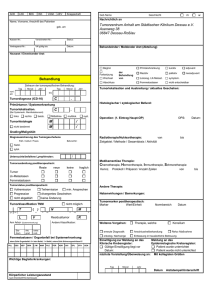
Untersuchung zu hochdifferenzierten \(G1\) Weichteiltumoren an
Werbung

Aus der Abteilung für Chirurgie des Israelitischen Krankenhauses in Hamburg Direktor: Professor Dr. med. Carsten Zornig Hochdifferenzierte Weichteilsarkome an Extremitäten und Rumpf Dissertation zur Erlangung des Grades eines Doktors der Medizin dem Fachbereich Medizin der Universität Hamburg vorgelegt von Gabriela Popovich aus Hildesheim Hamburg 2003 Angenommen vom dem Fachbereich Medizin der Universität Hamburg am: 8.1.2004 Veröffentlicht mit Genehmigung des Fachbereichs Medizin der Universität Hamburg Prüfungsausschuß, der Vorsitzende: Professor Dr. C. Zornig Prüfungsausschuß: 2. Gutachter: Professor Dr. S. Schröder Prüfungsausschuß: 3. Gutachter: Professor Dr. J. Bruns 1 1 EINLEITUNG............................................................................................................ 3 1.1 ÄTIOLOGIE ............................................................................................................... 3 1.2 GENETISCHE FAKTOREN ......................................................................................... 6 1.3 HISTOLOGISCHE SUBTYPEN .................................................................................... 6 1.4 STADIENEINTEILUNG ............................................................................................. 10 1.5 WACHSTUMSVERHALTEN ...................................................................................... 13 1.6 PROGNOSEFAKTOREN............................................................................................ 15 1.7 THERAPIE ............................................................................................................... 18 1.7.1 Operative Therapie .......................................................................................... 18 1.7.2 Strahlentherapie ............................................................................................... 19 1.7.3 Chemotherapie................................................................................................. 20 1.8 FRAGESTELLUNG ................................................................................................... 22 2 MATERIAL UND METHODEN........................................................................... 23 3 ERGEBNISSE.......................................................................................................... 25 3.1 ALTER UND GESCHLECHT ..................................................................................... 25 3.2 KLINISCHE PRÄSENTATION ................................................................................... 25 3.3 HISTOPATHOLOGISCHE ERGEBNISSE ................................................................... 26 3.4 OPERATIVE THERAPIE .......................................................................................... 27 3.4.1 Operative Therapie bei Primärmanifestation................................................... 28 3.4.2 Operative Therapie von Lokalrezidiven .......................................................... 28 3.4.3 Operative Therapie von Fernmetastasen ......................................................... 30 3.5 ENTDIFFERENZIERUNG IM VERLAUF .................................................................... 32 3.5.1 Lokalrezidive und Entdifferenzierung............................................................. 32 3.5.2 Fernmetastasen und Entdifferenzierung .......................................................... 34 3.6 METASTASENENTSTEHUNG IN ABHÄNGIGKEIT VON LOKALREZIDIV UND GRADING IM LOKALREZIDIV .............................................................................................. 35 3.6.1 Metastasenenstehung in Abhängigkeit von Lokalrezidiv................................ 35 3.6.2 Metastasenentstehung in Abhängigkeit von Entdifferenzierung im vorausgehenden Lokalrezdiv .......................................................................................... 35 3.7 CHEMOTHERAPIE .................................................................................................. 36 3.8 RADIOTHERAPIE .................................................................................................... 37 3.9 FOLLOW-UP ........................................................................................................... 38 3.9.1 Patienten ohne zweite Tumormanifestation .................................................... 39 3.9.2 Patienten mit zweiter Tumormanifestation...................................................... 39 3.10 SPEZIELLE EINZELFÄLLE ...................................................................................... 40 3.10.1 Tumortod ohne zweite Tumormanifestation ................................................... 40 3.10.2 Fernmetastasierung mit Entdifferenzierung ohne vorrangehendes Lokalrezidiv ......................................................................................................................... 40 3.10.3 Auftreten eines späten Lokalrezidives mit Entdifferenzierung ....................... 41 3.10.4 Entdiffernzierung im Lokalrezidiv und nachfogender Fernmetastase ............ 42 3.11 PROGNOSEFAKTOREN............................................................................................ 43 4 DISKUSSION .......................................................................................................... 51 5 ZUSAMMENFASSUNG......................................................................................... 59 6 LITERATURVERZEICHNIS ............................................................................... 61 7 DANKSAGUNGEN................................................................................................. 71 2 8 LEBENSLAUF ........................................................................................................ 72 3 1 Einleitung Bei Weichteiltumoren handelt es sich entsprechend der WHO-Klassifikation (Enzinger FM und Weiss SW, 1994) um Neoplasien des mesenchymalen Gewebes. Sie sind nichtepithelialen, extraskelettalen Ursprungs und entstehen im Binde-, Fett-, Muskel- und Nervenhüllgewebe. Obgleich der Mensch zu mehr als 80 % aus mesenchymalem Gewebe besteht, sind Weichteiltumoren mit einer Inzidenz von 1-2 / 100.000 Einwohner pro Jahr in der Bevölkerung ausgesprochen selten. Sie machen nur etwa 1 % aller malignen Erkrankungen des Erwachsenenalters und 15 % des Kindesalters aus (Hoos et al., 2000, Enzinger FM und Weiss SW, 1994). Dabei ist die Entstehung in allen Körperregionen möglich, am häufigsten jedoch entwickeln sie sich an den Extremitäten (50 %), visceral (16,4 %), retroperitoneal (15,1 %) und am Körperstamm (10,7 %). An anderen Körperstellen manifestieren sie sich in 12,1 % (Hoos et al., 2000). 1.1 Ätiologie Für die Mehrzahl aller Patienten mit Weichteiltumoren lässt sich kein spezifischer ätiologischer Faktor erkennen, jedoch wurden einige prädisponierende Faktoren identifiziert (Tabelle 1). Genetische Syndrome wie Neurofibromatose (Sorensen et al., 1986, Barken et al., 1987), familiäre Polypose und das Li-Fraumeni-Syndrom (Li und Fraumeni, 1969, Strong et al., 1992) konnten mit der Entstehung von Weichteilsarkomen in Verbindung gebracht werden. Ionisierende Strahlen (Brady et al., 1992, Smith, 1987, Coia et al., 1980), und chronisches Lymphödem (Lymphangiosarkom Stewart-Treves) (Chung et al., 2000) sind als ätiologische Faktoren ebenfalls anerkannt, werden jedoch selten beobachtet. Der Zusammenhang mit einem traumatischen Ereignis als kausaler Faktor ist unbestimmt. Chemische Karzinogene wurden häufig als Kausalfaktoren impliziert, jedoch sind die Daten, die für eine Assoziation bestimmter Substanzen mit der 4 Entstehung von Sarkomen sprechen, nicht eindeutig (Fingerhut et al., 1991, Hoar et al., 1986, Wingren et al., 1990). So soll die Exposition gegenüber Dioxin-enthaltenden Herbiziden bei Waldarbeitern und Landwirten zu einer erhöhten Prävalenz von Sarkomen geführt haben (Hardell und Sandstrom, 1979). Ein weiteres Beispiel in diesem Zusammenhang ist auch die Exposition von US-Soldaten mit dem Entlaubungsmittel Agent-Orange im Verlaufe des Vietnam-Krieges (Kang et al., 1987, Kramarova et al., 1998). Zusätzlich werden Medikamente mit dem Auftreten von Sarkomen in Verbindung gebracht. Beispielsweise konnte bei Kindern nach Therapie mit Melaphan, Procarbazin, Chlorambucil und anderen Chemotherapeutika das vermehrte Auftreten von Osteosarkomen beobachtet werden. Auch Viren können an der Entstehung von Weichteilsarkomen beteiligt sein. Dies ist insbesondere für das Humane Herpesvirus 8 bei der Entstehung des Kaposi-Sarkoms im Zuge einer HIV-Infektion belegt worden (Hengge et al., 2002). Tabelle 1 Sarkome: Prädisponierende Faktoren (Hoos et al., 2000) Prädisponierende Faktoren Molekularer Defekt Genetische Prädisposition Neurofibromatose ( von Recklinghausen) Neurofibromin-Inaktivierung Li-Fraumeni-Syndrom p53 Deletion Retinoblastom Rb1 Deletion Gardner-Syndrom Ionisierende Strahlen n.a. Lymphödem n.a. Chemische Substanzen n.a. Trauma n.a. n.a. nicht anwendbar 5 Tabelle 2 Genetische Anomalien in Sarkomen (Lewis und Brennan, 1996) Histologie Zytogenetische Anomalie Synoviales Sarkom t(X ; 18) (p11.2 ; q11.2) Myxoides Liposarkom t(12 ; 16) (q13 ; p11) Ewing-Sarkom t(11;22) (q21-24; q11-14) Alveoläres Rhabdomyosarkom t(2;13) (q35-37; q14) Extraskeletales, myxoides Chondrosarkom t(9 ;22) (q22 ; q11-12) Histologie Molekulare Veränderung Leiomyosarkom RB1 Punktmutationen oder Deletionen Malignes fibröses Histiocytom Maligner peripherer Nervenscheidentumor Malignes fibröses Histiocytom Leiomyosarkom Liposarkom Rhabdomyosarkom p53 Punktmutationen oder Deletionen 6 1.2 Genetische Faktoren Genetische Determinanten von malignen Weichteiltumoren konnten in jüngerer Zeit charakterisiert werden (Tabelle 2). Tatsächlich wurden bei bestimmten histologischen Subtypen charakteristische chromosomale Translokationen gefunden (Fletcher, 1991, Sreekantaiah et al., 1992, Sreekantaiah, 1998). Daher können cytogenetische Untersuchungen essentielle Bedeutung für die pathologische Diagnostik haben. Hierbei muss jedoch auch beachtet werden, dass verschiedene Translokationen auch bei benignen Weichgewebstumoren gefunden werden können. Neben großen strukturellen Chromosomenveränderungen konnten weitere, molekulare Alterationen im Sinne von Punktmutationen oder Deletionen in definierten Genorten in Assoziation mit bestimmten Sarkomen gefunden werden (Tabelle 2). Hierbei sind die am besten untersuchten molekularen Genloci die Tumorsuppressorgene p53 und RB1 (Mulligan et al., 1990). Die Inaktivierung beider Gene ist an der Kanzerogenese verschiedener Sarkome beteiligt (Cance et al., 1990, Sreekantaiah, 1998). 1.3 Histologische Subtypen Die Weichteiltumoren werden anhand ihres Ursprungsgewebes klassifiziert, gleichwohl diese Herkunft nicht immer völlig eindeutig ist. Für die Typisierung werden herkömmliche Mikroskopie, immunhistochemische Techniken sowie Elektonenmikroskopie angewandt. Die häufigsten histologischen Subtypen sind Liposarkome, maligne fibröse Histiocytome (MFH) und Leiomyosarkome (Hoos et al., 2000) (Tabelle 3, Abbildung 1). Hierbei weisen verschiedene histopathologische Typen eine gewisse Abhängigkeit von der anatomischen Lokalisation auf. So sind die häufigsten Subtypen bei Extremitätentumoren Liposarkome und MFH, während retroperitoneale oder viszerale Tumoren beinah ausschließlich von Liposarkomen und Leiomyosarkomen repräsentiert werden (Lewis und Brennan, 1996, Mann et al., 1999). 7 Tabelle 3 Verteilung der histologischen Typen bei 3968 Patienten des Memorial SloanKettering Cancer Center anhand der Endhistologie (Hoos et al., 2000) Histologischer Typ Häufigkeita Liposarkom 19,5 % Leiomyosarkom 18,1 % Malignes fibröses Histiozytom 17,9 % Fibrosarkom 10,4 % Synovialsarkom 7,1 % maligner peripherer Nervenscheidentumor 3,5 % Andere 23,5 % a Diese Daten umfassen Sarkome der Extremitäten, des Körperstamms, des Bauchraums und des Retroperitoneums Abbildung 1: Hämatoxilin-Eosin-gefärbte Präparate der häufigsten histologischen Sarkomtypen. (A) Hochdifferenziertes Fibrosarkom, (B) hochdifferenziertes, lipomartiges Liposarkom, (C) MPNST, Maligner peripherer Nervenscheidentumor, (D) hochdifferenziertes myxoides malignes fibröses Histiozytom (MFH). 8 Auch finden sich bestimmte histopathologische Subtypen in Abhängigkeit vom Erkrankungsalter des Patienten. Dabei sind im Kindesalter am häufigsten embryonale Rhabdomyosarkome. Synoviale Sarkome treten gehäuft bei jungen Erwachsenen (< 35 Jahre) auf, während Liposarkome und MFH bei älteren Patienten den Hauptteil ausmachen (Abbildung 2). Jahre Abbildung 2: Altersabhängige Verteilung der häufigen histologischen Typen von Sarkomen (nach (Enzinger FM und Weiss SW, 1994)). MPNST, Maligner peripherer Nervenscheidentumor; MFH, Malignes fibröses Histiozytom Neben der Klassifikation auf dem Boden des Ursprungsgewebes erfolgt eine weitere Einteilung anhand des Differenzierungsgrades (Grading). Dieses basiert auf mitotischem Index, Cellularität, Nekrosen und dem Grad von nukleären Anaplasien (Hajdu, 1986) und führt zur Zuordnung des jeweiligen Tumors in einen von drei Differenzierungsgraden: G1, G2 oder G3 für hoch, mittelgradig und schlecht differenziert (siehe Kapitel 1.4) 9 Einige histologische Typen können in ihrem klinischen Verhalten in allen Differenzierungsgraden vorkommen, andere sind per Definitionem einem festen Grading zugeordnet, so ist das Dermatofibrosarkom protuberans immer hochdifferenziert, das Rhabdomyosarkom hingegen immer niedrigdifferenziert (Tabelle 4). Tabelle 4 Grading einzelner histologischer Typen in Kenntnis des klinischen Verhaltens (Enzinger und Weiss, 1994) Hisologischer Typ Histologisches Grading I II Fibrosarkom Dermatofibrosarcoma protuberans MFHa Liposarkom Leiomyosarkom Rhabdomyosarkom Angiosarkom Malignes Hämangiopericytom Synovialsarkom MPNSTb Extraskelettales Chondrosarkom a MFH, Malignes fibröses Histiozytom; bMPNST, Maligner peripherer Nervenscheidentumor III 10 1.4 Stadieneinteilung Für die prognostische Beurteilung und Stadieneinteilung der Weichteilsarkome wird zum einen das TNM-System sowie der Differenzierungsgrad und die Residualtumorklassifikation angegeben (Hermanek et al., 1987). Im aktuellen TNMSystem (Tabelle 5) werden Tumoren mit einem Durchmesser von größer oder kleiner 5 cm unterschieden. Der Lymphknotenstatus kennt nur einen regionalen Lymphknotenbefall oder tumorfreie Lymphknoten. Ebenso verhält es sich mit Fernmetastasen, deren Vorhandensein oder Fehlen beurteilt wird. Mit den Daten des TNM-Systems und dem histologischen Grading (Tabelle 6) wird das Tumorstadium entsprechend dem StagingSystem des American Joint Commitee on Cancer (AJCC), welches mit dem der Union International Contre le Cancer (UICC) übereinstimmt, für Weichteilsarkome festgelegt (Tabelle 7). Das GTNM-System der UICC hat kürzlich eine entscheidende Modifikation erfahren. Insbesondere die Lokalisation des Tumors hinsichtlich der Muskelkompartimente (oberflächlich versus tief) wird bei dieser Einteilung zusätzlich berücksichtigt. Oberflächlich bedeutet, der Tumor liegt subcutan außerhalb der äußersten Muskelfaszie, während die tiefen von einer Muskelfaszie umgeben sind (Tabelle 7). Die Stadieneinteilung erlaubt, eine Aussage über die Prognose der Erkrankten zu machen. So nehmen die Überlebenschancen mit zunehmendem Tumorstadium ab (5- Jahresüberlebensraten für Stadium 1, 99 %; Stadium 2, 82 %; Stadium 3, 52 % und Stadium 4, 22 %). (Geer et al., 1992). Neben der häufig verwendeten GTNM-Einteilung nach AJCC / UICC gibt es weitere Einteilungen, z. B. in low–grade und high-grade Tumoren oder aber in drei Differenzierungsgrade (Saddegh et al., 1992, Heise et al., 1986, Enneking, 1988). Die Verwendung verschiedener Stadieneinteilungen stiftet zunehmende Verwirrung und macht einen sinnvollen Vergleich der publizierten Studien äußerst schwierig. 11 Tabelle 5 Staging von Sarkomen nach dem TNM-System (Hermanek et al., 1987, Beahrs et al., 1992) T Primärtumor TX Primärtumor kann nicht untersucht werden T0 Kein Hinweis auf den Primärtumor T1 Tumor < 5 cm in seiner größten Ausdehnung T1a oberflächlicher Tumor T1b tiefer Tumor T2 Tumor > 5 cm in seiner größten Ausdehnung T2a oberflächlicher Tumor T2b tiefer Tumor N Regionäre Lymphknoten NX Regionäre Lymphknoten können nicht untersucht werden N0 Keine regionären Lymphknotenmetastasen N1 Regionäre Lymphknotenmetastasen M G Fernmetastasen MX Keine Beurteilung möglich M1 Keine Fernmetastasen M2 Fernmetastasen GX Differenzierungsgrad kann nicht beurteilt werden G1 Hochdifferenzierter Tumor G2 Mäßig differenzierter Tumor G3 – 4 Schlecht differenzierter / entdifferenzierter Tumor 12 Tabelle 6 Histopathologisches Grading von Sarkomen (Coindre et al., 1986) Tumordifferenzierung Score 1 Sarkom ist dem gesunden Gewebe ähnlich Score 2 Sarkomen, deren histologische Typisierung sicher möglich ist Score 3 Embryonale Sarkome, undifferenzierte Sarkome, eindeutig zu typisierende Sarkome Anzahl der Mitosen Tumornekrose Score 1: 0 – 9/10 Feldern1 Score 0: keine Nekrosen Score 2: 10 – 19/10 Feldern Score 1: weniger als 50 % Nekrosen Score 3: ≥ 20/10 Feldern Score 2: mehr als 50 % Nekrosen Endgültiges Grading2 Grade 1: Score 2 – 3 Grade 2: Score 4 – 5 Grade 3: Score 6 – 8 1 ein Feld entspricht 0,1734 mm 2 zur Ermittlung des Grades werden die Scores der drei Kategorien addiert nicht 13 Tabelle 7 Staging Gruppen nach AJCC1 (Coindre et al., 1986) Stage G2 T2 N2 M2 Stage IA G1, 2 T1a N0 M0 G1, 2 T1b N0 M0 Stage IB G1, 2 T2a N0 M0 Stage IIA G1, 2 T2b N0 M0 Stage IIB G3, 4 T1a N0 M0 Stage IIIA G3 – 4 T1 N0 M0 Stage IIIB G3 – 4 T2 N0 M0 Stage IVA G1 – G4 T1 – T2 N1 M0 Stage IVB G1 – G4 T1 – T2 N0 / N1 M1 1 2 American Joint Committee on Cancer siehe Tabelle 5 für Definition 1.5 Wachstumsverhalten Hochdifferenzierte Sarkome zeichnen sich durch langsames Wachstum aus. Im Gegensatz dazu ist eine Tumorverdopplung bei G3 Tumoren in ein bis zwei Monaten möglich (Rougraff, 1999). Sarkome imponieren in 50 % der Fälle makroskopisch kapselbegrenzt. Nur bei einem Teil dieser Tumoren kann dann aber mikroskopisch eine rundum intakte Pseudokapsel nachgewiesen werden (Abbildung 3A). Die übrigen Sarkome wachsen infiltrativ oder weisen Satellitenknoten auf (Abbildung 3B). Dieses Wachstumsverhalten begründet unter 14 anderem bei inadäquater chirurgischer Therapie die hohe Lokalrezidivrate (Enzinger und Weiss, 1994, Zornig, 1997). Das Rezidiv- und Metastasierungsverhalten von Weichteilsarkomen ist abhängig vom Grading. Es wird jedoch auch entscheidend vom Residualstatus nach chirurgischer Therapie beeinflusst. Dies macht deutlich, dass der R-Status die entscheidende, direkt beeinflussbare Determinante für die Prognose (siehe Kapitel 1.6) darstellt. Lokale Rezidive treten bei hochdifferenzierten Sarkome in 16 – 36 % der Fälle auf (Gaynor et al., 1992, Potter et al., 1985, Saddegh et al., 1992, Singer et al., 1994, Lewis et al., 1997, Peiper et al., 1995). Im Gegensatz dazu wird die Lokalrezidivrate bei mässigdifferenzierten Weichteilsarkomen mit über 33 % angegeben (Peiper et al., 1995). Bei den G3–klassifizierten Tumoren liegt die Lokalrezidivrate bei 22% (Peiper et al., 1995). Diese niedrigere Lokalrezidivrate resultiert aus dem durch Fernmetastasierung meist kurzen Krankheitsverlauf mit raschem Tumortod. Metastasen entwickeln sich bei hochdifferenzierten Sarkomen nur selten. Die Häufigkeit wird in der Literatur mit unter 15 % angegeben (Lewis et al., 1999, Trovik et al., 2000), wobei diese Studien G1 und G2 Weichteilsarkome zu den low-grade Sarkomen zusammengefasst haben. Daher dürfte die eigentliche Metastasierungsrate bei den hochdifferenzierten Weichteilsarkomen deutlich unter 15 % liegen. Im Gegensatz dazu treten Metastasen bei niedrigerem Differenzierungsgrad bei über 50 % der Fälle auf (Lewis und Brennan, 1996). Hierbei neigen die niedrigdifferenzierten Sarkome direkt, das heißt auch ohne vorheriges Rezidiv, zur Fernmetastasenbildung. Hochdifferenzierte Weichteiltumoren können im Zuge eines lokalen Rezidives entdifferenzieren und dabei die Charakteristika der schlechter differenzierten Tumoren, also auch eine vermehrte Neigung zur Fernmetastasierung, annehmen. Es muß aber betont werden, daß bei diesen Tumoren 15 Fernmetastasen auch ohne vorheriges Rezidiv und ohne Entdifferenzierung auftreten können (Billingsley et al., 1999, Lewis et al., 1999, Coindre et al., 2001). Fernmetastasen entwickeln sich in 80 % innerhalb der ersten zwei Jahren nach Diagnosestellung (Coindre et al., 2001, Lewis und Brennan, 1996, Zornig, 1997). Der häufigste Metastasierungsort peripherer Weichteilsarkome ist mit etwa 80 % die Lunge, als weitere Manifestationsorte finden sich Leber und Haut. Lymphknotenmetastasen werden in der Literatur mit weniger als 3 % angegeben (Fong et al., 1993). Für die retroperitonealen Sarkome stehen Leber und Lunge als Manifestastionsorte der Metastasenbildung im Vordergrund, gefolgt von peritonealen Absiedlungen. Abbildung 3: Hämatoxilin-Eosin-gefärbte Präparate von Weichteilsarkomen mit unterschiedlichen Wachstumsarten. (A) Peripherie eines kapselartig begrenzten, hochdifferenzierten malignen peripheren Nervenscheidentumors, (B) Randbereich eines hochdifferenzierten, myxoiden Liposarkoms mit satellitenartigem Invasionsverhalten. 1.6 Prognosefaktoren In vielen Studien ist versucht worden, Prognosefaktoren für die Entstehung von Lokalrezidiven und Metastasen, das Erkrankungs-spezifische Überleben und das Überleben nach Metastasenentstehung zu bestimmen. Bei der Betrachtung der publizierten 16 Daten muß dabei unbedingt beachtet werden, daß sie durch Untersuchung gemischter Paatientenkollektive, also Patienten mit G1 – G4 Weichteilsarkomen erhoben wurden. Daher ist nicht klar, ob die ermittelten Prognosefaktoren auch zwanglos für hochdifferenzierte Weichteilsarkome gelten können. Der histologische Typ läßt kaum Aussagen über die Prognose zu, vielmehr ist das Grading und als einzige beinflußbare Determinante der Residualstatus nach Operation von Bedeutung (Tabelle 8) (Markhede et al., 1982, Rooser et al., 1988, Stotter et al., 1990). In einer Studie zu prognostischen Determinanten (Pisters et al., 1996b) wurden die Daten von 1041 Patienten mit Sarkomen der unteren Extremität durch uni- und multivariate Analysen untersucht. Endpunkte waren Lokalrezidiv, das Auftreten von Fernmetastasen, Erkrankungs-spezifisches Überleben und Überleben nach dem Auftreten von Fernmetastasen (Tabelle 8). Wichtig ist es, anzumerken, dass die erarbeiteten Aussagen streng genommen nur für Patienten mit Sarkomen an der genannten Lokalisation gelten können. Als Determinanten einer ungünstigen Prognose für das Auftreten eines Lokalrezidives waren ein Lebensalter von über 50 Jahren bei Diagnose, Rezidive in der Vorgeschichte, mikroskopisch Tumor-positive Resektionsränder sowie der Nachweis eines Fibrosarkoms oder MPNST. Für das Auftreten von Fernmetastasen konnte ein großer Primärtumor, tiefe Tumorlokalisation und der Nachweis eines Leiomyosarkoms als Risikofaktoren gefunden werden. Ähnliche Risikofaktoren für die Fernmetastasierung wurden auch in anderen Studien nachgewiesen (Enzinger und Weiss, 1994, Trovik und Bauer, 1999, Billingsley et al., 1999, Coindre et al., 2001, Tomita et al., 1994, Choong et al., 1995a, Lewis et al., 1997). Eine unterschiedliche Gewichtung der Risikofaktoren besteht darin, dass für das Auftreten einer frühen Fernmetastase (< 2 Jahre) insbesondere das Grading von Bedeutung ist, während für späte Fernmetastasen (>5 Jahre) vor allem die Größe des Primärtumors 17 sowie die Resektionsqualität Einfluss besitzt (Lewis und Brennan, 1996). Für das Erkrankungs-spezifische Überleben stellen ein Tumor von größer 5 cm, geringe Differenzierung, eine tiefe Tumorlokalisation, Lokalrezidive in der Vorgeschichte und mikroskopisch Tumor-positive Resektionsränder prognostisch ungünstige Faktoren dar (Pisters et al., 1996b). Ein Tumor größer als 10 cm wurde als einziger prognostisch ungünstiger Marker für das Überleben nach dem Auftreten von Fernmetastasen gefunden (Singer et al., 1994). Tabelle 8 Ungünstige Prognosefaktoren für den Verlauf von Weichteilsarkomen der Extremitäten a (Gaynor et al., 1992, Pisters et al., 1996b) Auftreten eines Zustand nach Lokalrezidiv Lokalrezidives Makroskopisch oder mikroskopisch Tumorpositive Resektionsränder Auftreten einer Niedriger Differenzierungsgrad Fernmetastase Tiefe Tumorlokalisation Tumorgröße > 5 cm Erkrankungs-spezifisches Niedriger Differenzierungsgrad Überleben Tiefe Tumorlokalisation Tumorgröße > 5 cm Lokalrezidiv positive Resektionsränder Überleben nach dem Alter > 60 Auftreten von Metastasen Metastasierung nicht in die Lunge Zeitraum zwischen Erkrankungsmanifestation und dem Auftreten von Metastasen a Prognosefaktoren wurden durch Untersuchung gemischter Kollektive (G1 – G4) erhoben. 18 1.7 Therapie Die klassische Therapie der Weichgewebssarkome besteht aus Chirurgie, Strahlentherapie und Chemotherapie. Zusätzlich gibt es weitere Therapiemöglichkeiten wie die isolierte hypertherme Extremitätenperfusion mit Tumor-Nekrose-Faktor-α (TNFα) und Melphalan (Lienard et al., 1992) und die regionale Hyperthermie. 1.7.1 Operative Therapie Die wichtigste Therapiemaßnahme ist zur Zeit die komplette chirurgische Entfernung des Primärtumors. Gleiches gilt aber auch für das Lokalrezidiv oder Fernmetastasen. Daher hängt die Prognose jedes einzelnen Patienten zu einem erheblichen Anteil auch vom RStatus ab (Tabelle 8). Nach Enneking werden operative Maßnahmen anhand der zurückbleibenden Resektionsränder eingeteilt (Enneking, 1984). (i) Intrakapsuläre Resektion: Der Tumor wird innerhalb seiner Pseudokapsel entfernt. Hierbei liegt das Risiko eines Lokalrezidivs bei 100 %. (ii) Marginale Exzision: Der Tumor wird inklusive seiner Pseudokapsel, aber innerhalb der reaktiven Zone des Tumor-umgebenden Gewebes exzediert. Die Lokalrezidivraten liegen bei dieser Operations-Strategie bei 60 – 80 %. (iii) Weite Exzision: en bloc Resektion des Tumors innerhalb des gesunden Gewebes unter Berücksichtigung eines Sicherheitsabstandes von 2 – 5 cm. Der Tumor wird bei dieser Operationsform für den Operateur nie sichtbar. Die Lokalrezidivrate liegt bei etwa 30 %. (iv) Radikale Exzision: Es erfolgt die komplette Resektion des Tumors unter Mitnahme des gesamten intakten Kompartments. Bei dieser Operationsform können die niedrigsten Lokalrezidivraten erzielt werden. Eine Sonderform der radikalen Exzision stellt die Amputation bei Tumoren der Extremitäten dar (Enzinger und Weiss, 1994, Kettelhack et al., 1998). Ergänzend zur chirurgischen Therapie stehen hauptsächlich die Bestrahlung und Chemotherapie zur Verfügung. 19 1.7.2 Strahlentherapie Die Strahlentherapie wird häufig als lokale Maßnahme vor allem bei R1-Situationen (Tumor reicht mikroskopisch bis an Resektionsrand) zur Absicherung des operativen Ergebnisses angewandt, da bei mikroskopisch befallenem Resektionsrand ein deutlich erhöhtes Risiko für ein lokales Tumorrezidiv besteht. Bei Einsatz der postoperativen Bestrahlung liegen die erzielten lokalen Tumorkontrollraten in einem Nachbeobachtungszeitraum von 5 Jahren bei 82 - 91 % (Cheng et al., 1996, Herbert et al., 1993, Suit et al., 1988). Die erforderliche Strahlendosis beträgt 60-66 Gy. Prinzipiell muß hierbei das gesamte Operationsgebiet mit einem Sicherheitssaum bestrahlt werden. Die postoperative Strahlentherapie ist darüber hinaus bei vielen Sarkomen mit einem Durchmesser >10 cm auch nach weiter Resektion indiziert, da deren erhöhtes Lokalrezidivrisiko dadurch erheblich gesenkt werden konnte (Mundt et al., 1995, Pisters et al., 1996a). Außerdem kommt die Strahlentherapie bei Patienten zum Einsatz, die keiner chirurgischen Therapie zugeführt werden können. Als besondere Form der Strahlentherapie kann eine Brachytherapie durchgeführt werden. Ihr Vorteil liegt in der rascheren Beendigung der Strahlenapplikation, technisch ist sie jedoch anspruchsvoller als die externe Strahlentherapie, da im Afterloading-Verfahren über intraoperativ eingelegte Katheter eine gezielte Bestrahlung des Wundbettes durchgeführt wird. Ein zu beachtendes Problem der postoperativen Brachytherapie ist eine erhöhte Wundkomplikationsrate (Brennan et al., 1991). Neben der klassischen postoperativen Bestrahlung werden zunehmend im Rahmen multimodaler Therapiekonzepte auch die präoperative und intraoperative Radiotherapie angewandt. Ziel der präoperativen Bestrahlung ist die Devitalisierung des Tumors. Auch wenn die makroskopische Tumorrückbildung meist nur gering ist, kann zum Teil eine deutliche Regression vitaler Tumorzellen erreicht werden. Von einer kanadischen Arbeitsgruppe wurden bei 35 % der Tumoren histologisch ein Nekroseanteil von über 20 80 % festgestellt (Hew et al., 1994, Willet et al., 1987). Ein Nachteil der präoperativen Bestrahlung ist die deutlich gesteigerte Rate postoperativer Wundheilungsstörung ( 2537 %). (Bujko et al., 1993, Cheng et al., 1996). Die intraoperative Strahlentherapie lässt eine gezielte Applikation einer hohen Strahlendosis auf einen intraoperativen verbleibenden Tumorrest bei gleichzeitig nur relativ geringer Belastung des umliegenden Gewebes zu. Vor allem bei retroperitonealen Tumoren mit knappen Resektionsgrenzen konnte durch die intraoperative Strahlentherapie eine Verbesserung der lokalen Tumorkontrolle erzielt werden (Sindelar et al., 1993). Den Vorteil einer kombinierten intra- und postoperativen Strahlentherapie zeigt eine Heidelberger Untersuchung bei Patienten mit fortgeschrittenen Extremitätensarkomen. Hierbei trat bei 30 Patienten, welche intraoperativ (7 Patienten, mittlere Dosis 15 Gy) und postoperativ (23 Patienten, mittlere Dosis 43 GY) bestrahlt wurden, nach einer Nachbeobachtungszeit von 24 Monaten bisher nur ein Rezidiv auf (Schwarzbach et al., 1996). Das wesentliche Problem der intraoperativen Strahlentherapie bleibt jedoch der große apparative Aufwand, so daß die Verfügbarkeit auch auf absehbare Zeit limitiert bleiben wird. 1.7.3 Chemotherapie Generell gilt, daß die Weichteilsarkome einen nur mässigen chemosensitiven Tumortyp repräsentieren, wobei jedoch je nach histologischem Subtyp unterschiedliche Ansprechraten gefunden werden. Daher ist die Chemotherapie insgesamt als adjuvante Therapieform von Weichteilsarkomen bei Erwachsenen umstritten, da letztlich bislang eindeutige Belege fehlen, dass sie zu einer Verlängerung des Lebens der jeweiligen Patienten führt. Zur Wertigkeit der adjuvanten systemischen Chemotherapie nach Resektion von Weichteilsarkomen gibt es eine Reihe von prospektiv randomisierten Studien. Nur in 2 von 12 Studien konnte eine Verbesserung des krankheitsfreien- und 21 Gesamtüberlebens durch die Chemotherapie nachgewiesen werden (Gortzak und van Coevorden, 1995). Eine Metaanalyse der durchgeführten Studien konnte allerdings einen signifiankten Vorteil für die therapierten Patienten bezüglich des Gesamtüberlebens feststellen (Zalupski et al., 1993). Problematisch bei einer derartigen retrospektiven Analyse ist die möglicherweise ungleiche Verteilung prognostisch wichtiger Tumorcharakteristika (z.B. G1 versus G3) in den einzelnen Arbeiten. Dies kann in einer erheblichen Verzerrung der Ergebnisse resultieren (Tierney et al., 1995). Eine Chemotherapie wird im Allgemeinen als neoadjuvantes oder aber palliatives Therapiekonzept genutzt. Die neoadjuvante Chemotherapie wird überwiegend bei großen Extremitätensarkomen angewandt. Ziel ist zum einen die Devitalisierung und Verkleinerung des Tumors, um die spätere Resektion zu erleichtern oder aber erst zu ermöglichen. Gleichzeitig soll aber auch die Überlebenszeit durch Abtötung eventueller vorhandener Mikrometastasen verbessert werden. Die Angaben über klinische oder histologisch gesicherte Tumorrückbildung sind sehr uneinheitlich und schwanken zwischen 3 % und 40 % (Casper et al., 1994, Pezzi et al., 1990). Randomisierte Studien konnten bisher keinen eindeutigen Vorteil des neoadjuvanten Therapieansatzes zeigen. Als palliative Therapieform bei Vorliegen von Fernmetastasen fanden sich im Gegensatz dazu Ansprechraten von etwa 30 % (Enzinger und Weiss, 1994). 22 1.8 Fragestellung Bislang gelten hochdifferenzierte Weichteilsarkome als lokal rezidivierende Tumorform, jedoch quod vitam eher als ungefährlich. So liest man als Anmerkung für den klinisch tätigen Arzt in histopathologischen Beurteilungen oftmals, dass bei knapper Resektion Lokalrezidiv-, aber keine Fernmetastasierungsgefahr besteht. Dieses entsprach in den letzten Jahren nicht unseren eigenen klinischen Erfahrungen. Vielmehr haben wir in Einzelfällen Fernmetastasen bei stets hochdifferenzierten Weichteilsarkomen beobachtet. Zusätzlich fanden wir bei Lokalrezidiven von hochdifferenzierten Sarkomen eine Entdifferenzierung, resultierend in einer erhöhten Fernmetastasierungswahrscheinlichkeit entsprechend primär niedrig differenzierten Sarkomen. Unter Rückgriff auf eine bis 1970 zurückreichende Datenbank sollten daher die klinischen Verläufe von Patienten mit hochdifferenzierten Weichteilsarkomen bezüglich folgender Fragen untersucht werden: • Wieviele Patienten mit hochdifferenziertem Weichteilsarkom (lokales Tumorwachstum immer G1) erleben eine Fernmetastasierung? • Wieviele Patienten mit hochdifferenziertem Weichteilsarkom entwickeln eine Entdifferenzierung im Zuge des lokalen Rezidivierns? • Wieviele Patienten entwickeln Fernmetastasen nach Entdifferenzierung des lokalen Tumors? • Wieviele Patienten mit hochdifferenzierten Sarkom versterben ? • Wie ist die Überlebensrate der Patienten, die im Zuge von Lokalrezidiven entdifferenziert sind? 23 2 Material und Methoden In diese Studie wurden 116 Patienten aufgenommen. Von 1970 bis 1998 wurden 67 Patienten mit einem hochdifferenzierten Weichteiltumor an Extremitäten und Rumpf in der Abteilung für Allgemeinchirurgie des Universitätsklinikums Hamburg-Eppendorf sowie von 1998 – 2000 5 Patienten im Israeltischen Krankenhaus Hamburg operiert. Weitere 44 Patienten erhielten ihre Primäroperation auswärtig und sind erst im Zuge der Nachresektion im Rahmen der Primärtherapie oder bezüglich eines Lokalrezidives in den oben genannten Krankenhäusern vorstellig geworden. Einschlußkriterien waren ein hochdifferenziertes Tumorwachstum (G1) bei der Primäroperation, Tumorlokalisation an den Extremitäten oder am Rumpf sowie ein Nachbeobachtungszeitraum von mindestens 12 Monaten nach der Erstoperation. Zunächst wurden 129 Patienten in die Studie eingeschlossen. Die histologischen Schnittpräparate dieser Patienten wurden unter Zuhilfenahme immunhistologischer Methoden entsprechend den WHO-Kriterien reklassifiziert und das Grading in Anlehnung an die Klassifikation von Enzinger und Weiss (Enzinger FM und Weiss SW, 1994) von einem auf diesem Gebiet erfahrenen Pathologen festgelegt. Dieses gilt für die histologischen Schnittpräparate der Primärmanifestation, zusätzlich wurde auch die erneute histologische Begutachtung sämtlicher Lokalrezidive und Fernmetastasen angestrebt. Das Staging erfolgte durch das System der UICC (TNM und Stadieneinteilung Ι- ΙV; Tabelle 6 und 7). In sieben Fällen wurde nach histologischer Begutachtung die Eingangshistologie nach den WHO-Kriterien korrigiert. Durch die Reklassifizierung der Primärtumoren mußten 13 Patienten wegen eines nicht hochdifferenzierten Gradings aus der Studie ausgeschlossen werden, so dass schließlich 116 Patienten in die Studie aufgenommen wurden. 24 Zur Auswertung erfasst wurden die Patientendaten wie Alter, Geschlecht, behandelnder Hausarzt und Onkologe, die Symptomdauer, prädisponierende Faktoren (genetische Prädisposition, ionisierende Strahlen, Lymphödem, chemische Substanzen, Trauma), Art der Operation (z. B. wide excison, Kompartmentresektion), die Charakteristika des Primärtumors (Lokalisation, Tumorgröße, Tumortiefe, Tumorrand, Histologie mit Eingangshistologie und Endhistologie nach Reklassifizierung, Grading, Staging nach der UICC) und der Residualtumorstatus (R-Klassifikation). Weiterhin wurde zur operativen Therapie auch die Chemotherapie und Strahlentherapie miterfasst. Hierbei wurde die Art der Therapie sowie der Zeitraum in die Auswertung mit aufgenommen. Ebenso wurde bei allen Therapieformen der behandelnde Arzt erfasst. Bei Lokalrezidiven und Fernmetastasen wurde der Zeitpunkt des Auftretens, die jeweilige Therapie (Operation, Bestrahlung und Chemotherapie) und das histologische Grading registriert. Bei chirurgischer Therapie von Lokalrezidiven beziehungsweise von Fernmetastasen wurde ebenfalls die R-Klassifikation erfaßt. Die Beurteilung der Resektionsqualität erfolgte nach der R-Klassifikation (R0, kein Residualtumor; R1, mikroskopischer Residualtumor; R2, makroskopischer Residualtumor) (Hermanek et al., 1987). In diese Beurteilung gingen der Operationsbericht und vor allem der pathologische Befund ein. Bei allen Patienten erfolgte eine Aktualisierung ihres Krankheitsverlaufes. Dies erfolgte durch persönliche Kontaktaufnahme mit den Patienten oder zu Angehörigen. Letzlich konnte der Krankheitsverlauf aller 116 Patienten geklärt werden. Die Überlebensraten wurden nach Kaplan / Meier (Kaplan et al., 1958) und die Prognosefaktoren in einer Multivarianzanalyse nach dem Coxschen Regressionsmodell (Cox, 1972) berechnet. Daneben erfolgte die Berechnung der prognostischen Signifikanz univariat mittels Logrank- und Wilcoxon-Test und multivariat mittels des Propotional- 25 Hazard-Modells Für die Auswertung der Daten wurde die SPSS-Software (Version 10.0) verwendet. 3 3.1 Ergebnisse Alter und Geschlecht Den Einschlusskriterien entsprachen 116 Patienten. Es handelte sich dabei um 70 Männer und 46 Frauen (Ratio 1,5 : 1) mit einem Durchschnittsalter von 48 (15 - 86) Jahren. 3.2 Klinische Präsentation Die Symptomdauer lag im Mittel bei 12 (0-120) Monaten. Nahezu alle Patienten stellten sich mit einem schmerzlosen Tumor vor. Bei 17 Patienten lagen Faktoren vor, die man als prädisponierend für die Entstehung des Weichteilsarkoms einschätzen kann. In drei Fällen (2,6 %) war ein vorangegangenes Trauma an der Lokalisation des Sarkoms dokumentiert worden. Acht Patienten (7,0 %) waren in gleicher Lokalisation an einem als vorher benigne eingeschätzten Tumor operiert worden. Bei weiteren vier Patienten (3,4 %) lag das Weichteilsarkom im Strahlenfeld einer aufgrund eines Weichteilsarkom-unabhängigen Tumorleidens 3-23 Jahre zuvor durchgeführten Strahlentherapie (1x Hämangion im Kindesalter, 1 x Mammacarcinom, 2 x Hämangiopericytom). Die Weichteilsarkome dieser Patienten wurden in zwei Fällen als Hämangiosarkom und den beiden anderen als Fibrosarkom klassifiziert. Zwei Patienten (1,7 %) entwickelten einen malignen peripheren Nervenscheidentumor im Rahmen eines Morbus von Recklinghausen. Bei 99 Patienten (85,3 %) fand sich keiner der bekannten prädisponierenden Faktoren (siehe Tabelle 1, Seite 4). Bei 63 Patienten (54,3 %) war das Sarkom an der unteren Extremität lokalisiert (2 x Leiste, 5 x gluteal, 40 x Oberschenkel, 3 x Knie, 12 x Unterschenkel, 1 x Fuß). In 29 Fällen 26 (25 %) war der Tumor an der oberen Extremität (1 x Achsel, 2 x Ellenbogen, 2 x Hand, 7 x Oberarm, 11 x Schulter, 6 x Unterarm) und in 24 Fällen (20,4 %) am Rumpf lokalisiert (Tabelle 9). Tabelle 9 Übersicht über die Tumorlokalisation im untersuchten Kollektiv (n=116) Lokalisation Anzahl (%) Untere Extremität 63 (54,3 %) Obere Extremität 29 (25 %) Rumpf 24 (20,7 %) 3.3 Histopathologische Ergebnisse Die häufigsten histologischen Typen (Tabelle 10) stellten das Liposarkom (44,8 %), das Fibrosarkom (14,7 %), das MPNST (10,3 %), das MFH (9,5 %) und das Leiomyosarkom (8,6 %) dar. 69 Tumoren (59,5 %) waren größer (T2), 47 Tumoren (40,5 %) waren kleiner (T1) als 5 cm. Die Tumorgröße lag im Mittel bei 7,6 (0,5-23) cm. 58 der Weichteiltumoren entwickelten sich subkutan, die übrigen 58 subfaszial. 47,4 % wiesen eine Kapselbegrenzung auf, hingegen zeigten 45,7 % mikroskopisch ein infiltratives Wachstum. Bei einem Patienten fanden sich histologisch Satellitenknoten. Bei 7 Patienten konnte das Wachstumsverhalten nicht eindeutig beurteilt werden. 27 Tabelle 10 Verteilung der histologischen Typen in der untersuchten Gruppe (n = 116) anhand der Endhistologie Histologischer Typ 3.4 Häufigkeit (%) Liposarkom 52 (44,8 %) Fibrosarkom 17 (14,7 %) maligner peripherer Nervenscheidentumor 12 (10,3 %) Malignes fibröses Histiozytom 11 (9,5 %) Leiomyosarkom 10 (8,6 %) Chondrosarkom 6 (5,2 %) Dermatofibrosarkom 3 (2,6 %) Hämangiosarkom 3 (2,6 %) Synovialsarkom 1 (0,9 %) Unklassifizierte Sarkome 1 (0,9 %) Operative Therapie Bei den 116 Patienten wurden 340 Operationen durchgeführt. Hierbei betrafen 168 Operationen die Primärmanifestation des Tumors, eingeschlossen der Nachresektionen bei inadäquater Primäroperation (45 Nachresektionen bei ungenügender, auswärtiger Primäroperartion, 3 Nachresektionen bei ungenügender Primäroperation im Universitätsklinikum Hamburg-Eppendorf sowie fünf zweite Nachresektionen). Im Verlauf wurden 152 Eingriffe aufgrund von Lokalrezidiven vorgenommen (1-14 pro Patient). Bei 12 Patienten wurden wegen Auftretens von Metastasen 20 Operationen durchgeführt (einmalige Metastasenchirurgie, 7 Patienten; zweimalige Metastasenchirurgie, 4 Patienten; fünfmalige Metastasenchirurgie, ein Patient). 28 3.4.1 Operative Therapie bei Primärmanifestation Beim Primäreingriff (inklusive eventueller Nachresektion) wurde bei 67 Patienten (57,8 %) eine R0- Resektion erzielt. In 50 Fällen (74,6 %) gelang dies durch weite Exzision, in 15 Fällen (22,4 %) durch eine Kompartmentresektion und in zwei Fällen (3 %) durch Amputation (einmal Oberschenkelamputation, einmal Oberschenkelexartikulation). Eine R1-Resektion erfolgte bei 45 Patienten (38,8 %). Bei diesen Patienten war vorwiegend eine weite Exzision geplant, jedoch zeigte das pathologische Ergebnis nicht allseits freie Resektionsränder. In vier Fällen (3,4 %) gelang nur eine R2-Resektion. 3.4.2 Operative Therapie von Lokalrezidiven Im Verlauf der Erkrankung entwickelten 52 Patienten (44,82 %) ein Lokalrezidiv (Tabelle 11). In diesem Zusammenhang ist allerdings die Selektionierung dieses Krankengutes insofern zu beachten, als daß 41 Patienten, die ihre Primäroperation in einem auswärtigen Krankenhaus hatten, erst aufgrund eines Lokalrezidives in das Universitätsklinikum Hamburg-Eppendorf oder das Israelitische Krankenhaus kamen. Die rezidivfreie Zeit betrug im Mittel 38,6 (3-160) Monate (Abbildung 4), wobei ein deutlicher Unterschied der Lokalrezidiv-freien Zeit in Abhängigkeit von dem Krankenhaus bestand, in dem die Primäroperation stattfand. Das erste Lokalrezidiv manifestierte sich bei 14 Patienten (26,92 %) innerhalb eines Jahres, bei weiteren 9 Patienten (17,6 %) wurde innerhalb von zwei Jahren die Diagnose eines Lokalrezidives gestellt und bei 29 Patienten (56,6 %) nach mehr als zwei Jahren. Lokalrezidive führten insgesamt zu 152 Operationen (pro Patient 114 Rezidivoperationen, inklusive Nachresektion). Von 72 Patienten, die primär im Universitätsklinikum Hamburg-Eppendorf beziehungsweise im Israelitischen Krankenhaus operiert worden waren, bekamen 11 Patienten (15,3 %) ein Lokalrezidiv. Die 41 weiteren Patienten mit Rezidiv waren zunächst außerhalb der oben genannten Kliniken einer chirurgischen Therapie unterzogen worden. 29 Bei 40 der 52 Patienten (76,9 %) mit Lokalrezidiv war initial eine R1-Resektion des Primärtumors erfolgt, in 12 Fällen (23,5 %) %) wurde die Erstoperation als R0-Resektion eingeschätzt. Bei 30 Patienten (57,7 %) konnte anlässlich der Operation des ersten Lokalrezidives eine R0-Resektion erzielt werden (in 7 Fällen gelang dies durch eine Amputation). In 19 Fällen (36,5 %)gelang eine R1-, in 3 Fällen (5,7 %) eine R2-Resektion. Die endgültige Amputationsrate (Primär- und Rezidivoperationen zusammengefaßt) betrug 11,8 % (11 Überlebenswahrscheinlickeit für rezidivfreie Zeit von 93 Patienten, die ein Sarkom an den Extremitäten aufwiesen). 100 80 60 40 Primäroperation auswärts 20 UKE und IK 0 0 10 20 30 Zeit in Jahren Abbildung 4: Geschätzte Überlebenswahrscheinlichkeit für die rezidivfreie Zeit von 116 Patienten mit hochdifferenzierten Weichteilsarkomen an Extremitäten und Rumpf in Abhängigkeit von dem Krankenhaus, in welchem die Primäroperation stattfand. 30 Tabelle 11 Übersicht über die Art der Tumorzweitmanifestation bei 60 von 116 Patienten Tumorzweitmanifestation Patienten (n=60) Lokalrezidiv 33 (55 %) Lokalrezidiv und Metastase 19 (31,6 %) Metastase 8 (13,3 %) 3.4.3 27 Operative Therapie von Fernmetastasen Patienten entwickelten im Verlauf Fernmetastasen (Tabelle 11). Erster Manifestationsort der Fernmetastasierung war in 63 % (17 von 27) die Lunge. Bei jeweils zwei Patienten traten die ersten Fernmetastasen in Leber, Haut, Knochen und Lymphknoten, je einmal in Peritoneum und Weichteile auf. Das freie Intervall bis zur Entwicklung von Fernmetastasen betrug im Durchschnitt 79 (3-329) Monate (Abbildung 5). Synchrone Metastasen fanden sich bei keinem der 116 Patienten. Acht Patienten entwickelten Fernmetastasen ohne vorheriges Lokalrezidiv (Tabelle 11). In 19 von 27 Fällen (70,4 %) gingen der Entstehung von Fernmetastasen ein oder mehrere Lokalrezidive voraus (Tabelle 11). Bei 8 von diesen blieb das Grading im Lokalrezidiv unverändert (Tabelle 12). Somit kam es bei 16 von 27 Patienten (59,3 %) zu einer Metastasierung ohne vorherige Entdifferenzierung im Lokalrezidiv. Eine Entdifferenzierung im Lokalrezidiv vor Entstehung von Metastasen konnte insgesamt bei 8 Patienten nachgewiesen werden, bei 5 zu G2 beziehungsweise bei 3 zu G3 (Tabelle 12). Überlebenswahrscheinlichkeit für metastasenfreie Zeit 31 100 80 60 40 20 Überlebensfunktion 0 0 10 20 30 Zeit in Jahren Abbildung 5: Geschätzte Überlebenswahrscheinlichkeit für die metastasenfreie Zeit von 116 Patienten mit hochdifferenzierten Weichteilsarkomen an Extremitäten und Rumpf. Betrachtet man die Abhängigkeit der Fernmetastasierung vom Grading des Primärtumors oder seines Lokalrezidives, so ergibt sich, dass 16 von 92 (17,40 %) hochdifferenzierten Sarkomen metastasierten. Im Gegensatz dazu fand sich eine Metastasierung bei 8 von 18 (44,4%) Patienten mit Entdifferenzierung des Lokalrezidives, nämlich bei 5 von 9 der zu G2 und 3 von 9 der zu G3 entdifferenzierten Sarkome. Bei den 6 Patienten, deren histologisches Grading des Lokalrezidives nicht vorlag, entwickelten 3 Patienten Metastasen. Bei 12 Patienten wurden 20 Operationen aufgrund von Fernmetastasen vorgenommen. Sieben Patienten erhielten eine einmalige chirurgische Therapie aufgrund von Fernmetastasen. Bei 2 von diesen 7 Patienten konnte durch die Metastasenchirurgie Tumorfreiheit erzielt werden. In einem Fall konnte eine Lungenmetastase R0 reseziert werden, in dem anderen Fall ist durch Wedgeresektion einer Lebermetastase Tumorfreiheit erzielt worden. 32 Bei den übrigen 5 Patienten konnte nur eine R1-Situation im Rahmen der Metastastenentfernung erzielt werden. Drei Patienten wurden aufgrund von Lungenmetastasen einer chirurgischen Therapie unterzogen, die beiden übrigen an peritonealen Fernmetastasen beziehungsweise an Lymphknotenmetasasen. Vier Patienten wurden zweimal aufgrund von Fernmetastasen einer chirurgischen Therapie unterzogen. Bei zwei Patienten sind zweimalig Lungenmetastasen reseziert worden. Die beiden anderen erhielten eine chirurgische Therapie aufgrund von Weichteilmetastasen im Bereich des Nackens beziehungsweise scrotale und Hautmetastasen. Ein Patient wurde fünfmal aufgrund von Fernmetastasen operiert. Zweimal war die Lunge Manifestastionsort, die übrigen drei Operationen wurden aufgrund von Fernmetastasen im Bereich der Thorax- und Bauchwand und der Wange vorgenommen. 3.5 Entdifferenzierung im Verlauf Von 116 Patienten haben 56 Patienten in ihrem bisherigen Verlauf bei adäquater Therapie ihrer Primärmanifestation bisher keine Zweitmanifestation erlebt. Die Problematik der Entdifferenzierung bezieht sich daher auf 60 Patienten, die eine zweite Tumormanifestation entwickelt haben (Tabelle 11). Von diesen haben 52 Patienten in ihrem Verlauf ein oder mehrere Lokalrezidive entwickelt, davon entwickelten 19 zusätzlich Fernmetastasen. Acht Patienten haben als zweite Tumormanifestation ohne vorheriges lokoregionäres Rezidiv eine Fernmetastase entwickelt. 3.5.1 Lokalrezidive und Entdifferenzierung Betrachtet man zunächst die 52 Patienten mit einem oder mehreren lokoregionären Rezidiven in ihrem Verlauf und das Verhalten des lokalen Tumorwachstums, zeigt sich, daß 18 Patienten (34,6 %) im Zuge ihres lokalen Tumorwachstums eine Entdifferenzierung 33 erlebt haben (9 Patienten: Übergang in mässigdifferenziertes Grading; 9 Patienten: Übergang in niedrigdifferenziertes Grading; Tabelle 12). Bei sieben von neun Patienten mit einer Entdifferenzierung zu G3 entwicklte sich die Entdifferenzierung direkt. Nur 2 Patienten sind zunächst von G1 zu G2 schließlich zu G3 entdifferenziert. Bei sechs Patienten blieb das Grading im Rezidiv unklar, diese sind aus den in Kapitel 3.10 genannten statistischen Berechnungen ausgeschlossen worden. Die Zahl von Lokalrezidiven schwankt in diesem Patientengut von ein bis 14 Rezidivereignissen. 25 von 52 (48,1 %) Patienten haben in ihrem bisherigen Verlauf nur ein lokales Tumorrezidiv entwickelt. Davon sind 8 Patienten schon im Zuge ihres ersten Lokalrezidives entdifferenziert (4 zu G2, 4 zu G3). 7 Patienten entwickelten in ihrem Verlauf 2 Lokalrezidive (3 x G1, 2 x unklares Grading). Ein Patient ist dabei schon im ersten Lokalrezidiv zu einem mässiggradigen lokalen Tumorwachstum entdifferenziert. Ein weiterer Patient ist erst im Zuge seines 2. Lokalrezidives zu G3 entdifferenziert. Vier Patienten haben 3 Lokalrezidive entwickelt, davon zeigte das lokale Tumorwachstum bei einem Patienten im ersten und zweiten Lokalrezidiv ein mässigdifferenziertes Grading und im dritten Lokalrezidiv kam es zu einer weiteren Entdifferenzierung zu G3. Vier Lokalrezidive entwickelten sechs Patienten, hierbei kam es bei 2 Patienten zu einer Entdifferenzierung zu G2 und bei zwei weiteren zu G3. Die Entdifferenzierung fand jeweils im ersten beziehungsweise im zweiten Loklarezidiv statt. Bei sieben Patienten kam es während des bisherigen Verlaufes zu einer Entwicklung von 5 Lokalrezidiven. Eine Entdifferenzierung konnte in drei Fällen histologisch nachgewiesen werden. Dabei kam es in zwei Fällen erst im 4. beziehungsweise im 5. Lokalrezidiv zu einer Entdifferenzierung. Drei Patienten entwickelten zwischen acht und 14 lokale Rezidive. Bei keinem kam es trotz der häufigen lokalen Rezidive zu keiner Entdifferenzierung. 34 Tabelle 12 Übersicht über die histologisch gesicherte Entdifferenzierung bei Patienten mit Tumorzweitmanifestation (n=24) Tumorzweitmanifestation Entdifferenzierung Gesamt G2 G3 nur Lokalrezidiv (n=33) 9a 4 5 Lokalrezidiv und Metastase (n=19) 12 Entdifferenzierung in Lokalrezidiv und Metastase 9b 5c 4d Entdifferenzierung nur in Metastase 3e 2 1 3f 2 1 Metastase (n=8) a 3 Patienten mit unklarem Grading im Lokalrezidiv sind nicht aufgeführt. 3 Patienten mit unklarem Grading im Lokalrezidiv sind nicht aufgeführt. c Bei 2 / 5 Patienten konnte ein identische Grading in Lokalrezidiv und Metastase histologisch gesichert werden, bei 3 / 5 ist augfrund nicht durchgeführter Metastasenchirurgie keine Aussage möglich. d Bei 2 / 4 Patienten konnte ein identische Grading in Lokalrezidiv und Metastase histologisch gesichert werden, bei 2 / 4 ist augfrund nicht durchgeführter Metastasenchirurgie keine Aussage möglich. e 2 Patienten mit unklarem Grading der Metastase bei nicht durchgeführter Metastasenchirurgie sind nicht aufgeführt. f 5 Patienten mit unklarem Grading der Metastase bei nicht durchgeführter Metastasenchirurgie sind nicht aufgeführt. b 3.5.2 Fernmetastasen und Entdifferenzierung Von 116 Patienten haben 27 (23,3 %) Patienten in ihrem bisherigen Verlauf Fernmetastasen ausgebildet. Bei 19 Patienten kam es im voraus zum Auftreten von Lokalrezidiven, acht Patienten entwickelten ohne vorheriges Lokalrezidiv Fernmetastasen (Tabelle 12). 12 Patienten wurden aufgrund ihrer Fernmetastasierung einer chirurgischen Therapie unterzogen. Bei sechs Patienten fand eine Entdifferenzierung erst im Rahmen der Fernmetastasierung statt (4 x G2, 2 x G3). Drei von diesen sechs Patienten haben ohne vorheriges Lokalrezidiv eine Fernmetastasierung erlebt. Zwei Patienten haben ihr Grading 35 sowohl im Lokalrezidiv als auch während der Fernmetastasierung beibehalten und blieben somit hochdifferenziert. Bei vier Patienten konnte eine Entdifferenzierung in den vorangehenden Lokalrezidiven histologisch gesichert werden, die jeweiligen Fernmetastasen entsprachen dem Grading des zuletzt aufgetreten lokoregionären Rezidiv. 3.6 3.6.1 Metastasenentstehung in Abhängigkeit von Lokalrezidiv und Grading im Lokalrezidiv Metastasenentstehung in Abhängigkeit von Lokalrezidiv Von 52 Patienten mit Lokalrezidiv haben 19 Patienten (36,53 %) Fernmetastasen entwickelt. Im Vergleich dazu entwickelten von 64 Patienten ohne Lokalrezidiv, also guter lokaler Tumorsanierung, 8 Patienten Fernmetastasen (12,5 %). Das Risiko, Fernmetastasen auszubilden, steigt in statitisch signifikanter Form mit dem Auftreten lokaler Rezidive an (p=0,004; Exakter Test nach Fisher). 3.6.2 Metastasenentstehung in Abhängigkeit von Entdifferenzierung im vorausgehenden Lokalrezidiv Es stellte sich die Frage, in welcher Weise eine Entdifferenzierung im Lokalrezidiv Einfluß auf die Entwicklung von Fernmetastasen nimmt. 28 Patienten haben ein hochdifferenziertes Grading im Lokalrezidiv beibehalten. 28,6 % (8 von 28) haben trotz des hochdifferenzierten Gradings eine Fernmetastase entwickelt. 9 Patienten sind im Zuge des lokalen Rezidivierens zu G2 entdifferenziert, davon haben 5 (55,5 %) Patienten im weiteren Verlauf Fernmetastasen entwickelt. Von 9 Patienten, die im Zuge von Lokalrezidiven ein entdifferenziertes Grading angenommen haben, entwickelten 3 Patienten (37,5%) Fernmetastasen. Bei sechs Patienten konnte das Grading im Lokalrezidiv nicht eruiert werden, von diesen haben 3 Patienten Fernmetasatsen entwickelt. Diese sechs Patienten wurden aus den statistischen Berechnungen 36 ausgeschlossen. Zusammenfassend bedeutet dies, dass von 18 Patienten, die im Zuge des Lokalrezidives eine Entdifferenzierung erlebten, 44,4 % (8 von 18) Fernmetastasen entwickeln. Im Vergleich dazu entwickeln 28,6 % (8 von 28) der Patienten mit stets hochdifferenzierten Lokalrezidiven Fernmetastasen. 3.7 Chemotherapie Bei 21 Patienten wurde eine Chemotherapie durchgeführt. In den frühen Jahren wurde nach dem CYVADIC–Schema, später mit Adriamycin (60 mg/m2 am Tag 1), kombiniert mit DTIC (400 mg/m2 am 1. und 2. Tag), therapiert. In jüngerer Zeit wurde Adriamycin (30 mg/m2 am 1. und 2. Tag) in Kombination mit Ifosfamid (2,5g/m2 pro Tag, kombiniert mit Mesna an Tag 1 bis 4 Tag) verwendet. Eine adjuvante Chemotherapie wurde bei sieben von den 21 Patienten durchgeführt. 4 von den sieben erhielten die Chemotherapie nach der Operation des Primärtumors. Ein Patient lebt seitdem tumorfrei (12 Jahre Nachbeobachtung, kein Rezidiv, keine Metastasen). Eine Patientin hat 7 Jahre nach der adjuvanten Chemotherapie für den Primärtumor ein Lokalrezidiv entwickelt, welches R1 reseziert werden konnte. Dieses wurde adjuvant mit Photonen mit einer Gesamtdosis von 50,4 Gy nachbestrahlt. Seither ist sie seit zwei Jahren tumorfrei. Ein weiterer Patient ist 17 Jahre später tumorfrei verstorben. Die vierte Patientin entwickelte vier Jahren nach der adjuvanten Chemotherapie für den Primärtumor fünf Lokalrezidive (alle G1) und letztendlich Lungenmetastasen (G3) nach 18 Jahren. Zwei Jahre darauf ist sie am Tumorleiden verstorben. 3 Patienten erhielten eine adjuvante Chemotherapie nach Metastasenchirurgie beziehungsweise nach Resektion eines Lokalrezidivs. Ein Patient hat eine adjuvante Chemotherapie für eine R0 resezierte Lungenmetastase (G1) erhalten. Er lebt seitdem drei Jahre tumorfrei. Die beiden übrigen Patienten haben eine adjuvante Chemotherapie für Hautmetastase beziehungsweise für das 37 2. Lokalrezidiv erhalten. Beide Patienten verstarben an einer tumorunabhängigen Todesursache. Zusammenfassend leben aus dieser Gruppe 4 von 7 Patienten tumorfrei, 2 sind Tumor-unabhägig verstorben und eine Patientin erlag dem Tumorleiden. Bei 14 von den 21 Patienten ist eine Chemotherapie unter palliativen Gesichtspunkten angewandt worden. In 10 Fällen war die Indikation aufgrund von Lungenmetastasen gestellt worden, die alle operativ nicht angegangen werden konnten. In drei Fällen wurde die Chemotherapie wegen anderen Metastasen durchgeführt (2 x Haut, 1 x Knochen), bei einem Patienten aufgrund eines R2- resezierten Primärtumors. Insgesamt erlagen die 14 Patienten im Durchschnitt 14 (3 - 41) Monate nach der palliativen Therapie dem Tumorleiden. 3.8 Radiotherapie Eine Strahlentherapie wurde bei 53 der 116 Patienten postoperativ durchgeführt. Zum Einsatz kam eine Neutronenbestrahlung mit einer Dosis von 13,6 - 19,6 Gy, vorwiegend bei R0 resezierten Primärtumoren und nach Lokalrezidiven. Bei allen R1- oder R2resezierten Primärtumoren oder Lokalrezidiven sowie in einem Fall von Lungenmetastasen wurden Photonen und oder Elektronen mit einer Dosis zwischen 50- 72 Gy eingesetzt. Bei 31 von 53 Patienten wurde die Strahlentherapie postoperativ nach der Primäroperation eingesetzt. Bei den restlichen 22 Patienten erfolgte die Radiotherapie nach operativer Therapie eines Lokalrezidives (ein Patient wurde palliativ aufgrund von Lungenmetastasen bestrahlt). Nach weiter Exzision (R0) erhielten 24 Patienten eine Strahlentherapie. Drei von ihnen entwickelten im Verlauf Lokalrezidive. Zwei konnten im Rezidiv R0 reseziert werden und sind seitdem tumorfrei. 4 von 24 entwickelten im Verlauf Fernmetastasen (drei mit Rezidiv, ein Patient ohne vorheriges Rezidiv). Im Gegensatz zu den R0-resezierten Patienten entwickelten von den 24 R1-resezierten und nachbestrahlten Patienten 13 im 38 weiteren Verlauf Lokalrezidive und 11 Patienten Fernmetastasen. Drei R2 resezierte Patienten (2 x Primärtumor, 1 x Lokalrezidiv) verstarben trotz Nachbestrahlung am Tumorleiden. 3.9 Follow-up Alle Patienten wiesen zum Zeitpunkt der Nachuntersuchung einen Mindestverlauf von 12 Monaten auf. Die Nachbeobachtungszeit betrug im Durchschnitt 107 (12-360) Monate. Die Nachbeobachtungsrate lag bei 100 %. Am Studienende waren 77 Patienten (66,4 %) tumorfrei (no evidence of disease). Fünf Patienten (4,3 %) leben mit Tumor (4 Patienten mit Metastasen, ein Patient mit Lokalrezidiv). 21 Patienten (18,1 %) sind aufgrund des Sarkomleidens verstorben. An einer Tumor-unabhängigen Erkrankung verstarben 13 Patienten (11,2 %). Die mediane Überlebensdauer betrug 107 Monate, die 5- Überlebenswahrscheinlichkeit Jahresüberlebensrate 90,7 % und die 10-Jahresüberlebensrate 83 % (Abbildung 6). 100 80 60 40 20 Überlebensfunktion 0 0 10 20 30 Zeit in Jahren Abbildung 6: Geschätze Überlebenswahrscheinlichkeit von 116 Patienten mit hochdifferenzierten Weichteilsarkomen an Extremitäten und Rumpf nach Kaplan-Meier. 39 3.9.1 Patienten ohne zweite Tumormanifestation 56 von 116 Patienten (48,3 %) hatten nach Therapie des Primärtumors keine weitere Tumormanifestation. Nur ein Patient dieser Gruppe verstarb an seinem Sarkomleiden. Er litt unter einem großen Primärtumor, welcher nur R2 reseziert und nachfolgend bestrahlt wurde. Es leben 87,5 % (49 von 56) der Patienten tumorfrei. Sechs Patienten (10,7%) sind an einer sakomunabhängigen Erkrankung verstorben. 3.9.2 Patienten mit zweiter Tumormanifestation 60 von 116 Patienten (51,7 %) entwickelten mindestens eine zweite Tumormanifestation. Bei 33 Patienten handelte es sich um lokale Rezidive. Ein Patient verstarb als Folge des Lokalrezidivs. Ein Patient (3 %) lebt mit Tumor. 78,8 % (26 von 33) der Patienten leben tumorfrei. Fünf Patienten (15,2 %) sind an einer sarkomunabhängigen Erkrankung verstorben. Von den 27 Patienten mit Fernmetastasen (23,3 %) sind 19 Patienten (70,4 %) der Sarkomerkrankung erlegen. 14,8 % (4 /27) leben mit Tumor. Zwei Patienten leben nach erfolgter R0 Resektion der Fernmetastasen tumorfrei und zwei Patienten sind an einer anderen Erkrankung verstorben. Von 21 Patienten, die der Sarkomerkrankung erlegen sind, haben 19 Patienten in ihrem Verlauf eine Fernmetastasierung erlebt. Zwei Patienten verstarben in der Folge lokaler Sarkommanifestationen ohne die Entstehung von Fernmetastasen. Während der eine Patient nur eine Primärmanifestation erlitt, entdifferenzierte der andere im Lokalrezidiv zu G2. Betrachtet man die 19 am Tumorleiden verstorbenen Patienten mit Fernmetastasen, so war bei 5 Patienten nur eine Fernmetastasierung aufgetreten. Von diesen blieb das Grading der Metastase bei nicht durchgeführter Metastasenchirurgie unklar, in einem Fall konnte eine Entdifferenzierung zu G2 dokumentiert werden. Bei 14 Patienten kam es im voraus zum Auftreten von einem oder mehreren Lokalrezidiven. Bei 5 von diesen 14 Patienten mit 40 Lokalrezidiv und Fernmetastasierung lag im Lokalrezidiv ein hochdifferenziertes Grading vor. Sechs Patienten sind im Zuge des lokoregionären Rezidivieren entdifferenziert. Bei 3 Patienten konnte das Grading des Rezidives nicht eruiert werden. 10 von 21 (47,62 %) der an der Sarkomerkrankung Verstorbenen waren im Tumorgrading zum Zeitpunkt des Todes hochdifferenziert. 38,1 % (8 von 21) sind vor Eintreten des sarkombedingten Todes im Rahmen des Lokalrezidives oder der Fernmetastasierung entdifferenziert. 3.10 Spezielle Einzelfälle In diesem Kapitel sollen besondere Einzelfälle, welche durch einen ungewöhnlichen Verlauf charakterisiert waren, detaillierter beschrieben werden. 3.10.1 Tumortod ohne zweite Tumormanifestation Ein 22-jähriger, männlicher Patient stellte sich 8 Monate nach Beginn der Symptomatik mit einem 12 cm durchmessenden, subfaszial gelegenen, myxoiden Liposarkom am Oberschenkel vor. 1977 gelang nur eine R2-Resektion. Das Wachstumsverhalten war in den histologischen Schnittpräparaten als infiltrativ beurteilt worden. Da keine R0Resektion erzielt werden konnte, erfolgte eine postoperative Nachbestrahlung mit Elektronen mit einer Dosis von 66 Gy. Der Patient verstarb 17 Monate nach der Operation am Tumorleiden, ohne dass sich eine Fernmetastase ausgebildet hatte. Dieser Fall zeigt, daß in seltenen Einzelfällen auch hochdifferenzierte Weichteilsarkome ohne Fernmetastasierung zum Tumortod führen können. 3.10.2 Fernmetastasierung mit Entdifferenzierung ohne vorrangehendes Lokalrezidiv Ein 38-jähriger, männlicher Patient stellte sich 17 Monate nach Symptombeginn mit einem 15 cm großen, gekapselten Liposarkom in subfaszialer Lokalisation am Oberschenkel vor. Trotz eines R0-Resektionsstatus wurde zur sicheren lokalen Tumorkontrolle eine 41 adjuvante, postoperative Strahlentherapie mit Neutronen vorgenommen. Vier Jahre nach Primärmanifestation entwickelte sich eine 20 cm durchmessende peritoneale Fernmetastase. Diese konnte im Rahmen einer Darmresektion mit einer zweiten, kleineren Tumormanifestation reseziert werden. Die histologische Begutachtung zeigte eine Entdifferenzierung zu G3. Ein Jahr nach operativer Therapie dieser Fernmetastasen lebt der Patient tumorfrei. Exemplarisch zeigt dieser Fall, daß hochdifferenzierte Weichteilsarkome auch direkt, daß heißt ohne vorheriges Lokalrezidiv, Fernmetastasen entwickeln können. 3.10.3 Auftreten eines späten Lokalrezidives mit Entdifferenzierung Ein 33-jähriger, männlicher Patient wurde mit einem 6 cm durchmessenden, gekapselten Liposarkom vom Mischtyp in subfaszialer Lokalisation am Unterschenkel vorstellig. Trotz R0-Resektion in der Primäroperation entwickelte er 10 Jahre später ein Lokalrezidiv. Dieses wurde nicht operativ angegangen, sondern mittels Neutronenbestrahlung (19,6 Gy) therapiert. Weitere 12 Jahre später stellte sich der Patient mit einem zweiten Lokalrezidiv vor, die Symptomdauer betrug hierbei 8 Monate. Die histologische Untersuchung zeigte eine Entdifferenzierung zu G3. Durch eine Unterschenkelamputation konnte bei dem sehr ausgedehnten Befund (Abbildung 7) Tumorfreiheit erzielt werden. Typischerweise treten Lokalrezidive von Weichteilsarkomen zwei Jahre nach Primärmanifestation auf. Der hier geschilderte Fall zeigt, daß diese jedoch in seltenen Fällen auch deutlich außerhalb dieses Zeitfensters manifest werden können. 42 Abbildung 7: Makroskopischer Befund des Lokalrezidives am rechten Unterschenkel bei dem unter 3.10.3 beschriebenen Patienten. Dieser massive Befund hat sich über einen Zeitraum von 8 Monaten entwickelt. 3.10.4 Entdiffernzierung im Lokalrezidiv und nachfolgender Fernmetastase In diesem Fall entwickelte eine 47-jährige Patientin mit einem hochdifferenzierten, subkutan gelegenen Dermatofibrosarkom am Oberarm mit infiltrativem Tumorwachstum und einer Tumorgröße von 4 cm (Symptomdauer 10 Monate) 6 Monate nach Primäroperation ein mässigdifferenziertes Lokalrezidiv. Dieses wurde R1–reseziert. Eine Nachbestrahlung erfolgte nicht. 11 Monate nach Primärmanifestation und somit 5 Monate nach Therapie des ersten Lokalrezidives kam es zur Entstehung von mässigdifferenzierten Lungen und Hautmetastasen. Trotz Erzielung einer R0-Situation im Rahmen der Metastasenchirurgie wurde eine anschliessende, adjuvante Chemotherapie vorgenommen (Adriamycin / Holoxan). 18 Monate nach dieser Therapie erlag die Patientin dem Rezidiv ihrer Lungenmetastasierung. Beispielhaft demonstriert dieser Fall, daß eine Entdifferenzierung bereits im ersten Lokalrezidiv stattfinden kann und sich hierdurch die Prognose des Patienten dramatisch verschlechtert. 43 3.11 Prognosefaktoren In der univariaten Analyse stellte sich die Entdifferenzierung im Verlauf (p<0,0030) wie auch das Auftreten von Fernmetastasen (p<0,000) als signifikant das Überleben determinierende Variablen dar (Tabelle 13, Abbildung 8, 9). Des weiteren ist eine Tumorgröße > 5cm ein prognostisch ungünstiger Marker, wenn auch nicht statistisch signifikant (p<0,055). Andere Variablen wie Alter, Geschlecht, histologischer Typ, Tumortiefe, R-Status und Lokalrezidiv waren nicht mit einer signifikanten Verkürzung der Überlebenszeit korreliert (Tabelle 13). In der multivariaten Analyse konnten die Entstehung von Fernmetastasen (p<0,000) als auch eine Entdifferenzierung im vorangehenden Lokalrezidiv (p=0,042) als signifikante Einflussfaktoren auf das Überleben gefunden werden (Tabelle 14). Bei Fernmetastasenentstehung sowie einer Entdifferenzierung im Lokalrezidiv ist das Risiko, am Tumortod zu versterben, ungefähr Überlebenswahrscheinlichkeit 30- beziehungsweise 6-fach erhöht (Tabelle 14). 100 80 60 40 Metastasen ja 20 nein 0 0 10 20 30 Zeit in Jahren Abbildung 8: Geschätzte Überlebenswahrscheinlichkeit von 116 Patienten mit hochdifferenzierten Weichteilsarkomen in Abhängigkeit von der Entwicklung von Metastasen (p<0,000). Überlebenswahrscheinlichkeit 44 100 80 60 Entdifferenzierung Entdifferenzierung 40 G2 und G3 im Verlauf 20 keine Änderung weiterhin G1 0 0 10 20 30 Zeit in Jahren Abbildung 9: Geschätzte Überlebenswahrscheinlichkeit von 116 Patienten mit hochdifferenzierten Weichteilsarkomen in Abhängigkeit von der Entdifferenzierung im Verlauf (p<0,0030). 45 Tabelle 13 Univariate Analyse nach dem Log Rank Test zur Ermittlung von Einflussfaktoren auf das Überleben im untersuchten Kollektiv a Kennzeichen Patientenzahl Tumortod (%) p-Wert Alter < 50 Jahre ≥ 50 Jahre 59 57 11 (18,65%) 10 (17,24 %) 0,5729 Geschlecht Männlich Weiblich 70 46 11 (15,71 %) 10 (21,74 %) 0,5100 Symptomdauer ≤ 5 Monate > 5 Monate 49 c 54 9 (18,37 %) 12 (22,22 %) 0,5471 Grading im Verlauf G1 G2/ G3 92a 18 10 (10,87 %) 8 (44,44 %) 0,0030 Resektabilität R0 R1 / R2 67 49 7 (10,45 %) 14 (28, 57 %) 0,3910 Metastase Ja Nein 27 89 19 (70,37 %) 2 (2,25 %) 0,000 Lokalrezidiv Ja Nein 52 64 15 (28,85 %) 6 (9,4 %) 0,2075 Tumorgröße < 5 cm ≥ 5 cm 47 69 4 (8,51 %) 17 (24, 64 %) 0,055 Wachtumsverhalten Gekapselt Infiltrativ 55 53 5 (9,10 %) 16 (30,20 %) 0,1797 Tumortiefe Subcutan Subfaszial 58 58 8 (13,79 %) 13 (22,41 %) 0,346 Die Gesamtzahl liegt in dieser Kategorie unterhalb der Gesamtzahl der untersuchten Patienten, da das Grading von 6 Patienten im Lokalrezidiv unklar blieb und diese daher in die statistische Berechnung nicht mit eingingen. b 8 Patienten mit Satellitenknoten beziehungsweise unklarem Wachstumsverhalten wurden aus der Berechnung ausgeschlossen. c 13 Patienten sind bei fehlender Angabe zur Symptomdauer aus der Berechnung ausgeschlossen worden. 46 Tabelle 14 Multivariate Analyse nach dem stufenweisen Coxschen Regressionsmodell zur Ermittlung von Einflussfaktoren auf das Überleben im untersuchten Kollektiv Kennzeichen Patientenzahl Tumortod (%) p-Wert Relatives Risiko Alter < 50 Jahre ≥ 50 Jahre 59 57 11 (18,65%) 10 (17,24 %) 0,609 1,010 Geschlecht Männlich Weiblich 70 46 11 (15,71 %) 10 (21,74 %) 0,979 1,018 Grading im Verlauf G1 G2 / G3 92 a 18 10 (10,87 %) 8 (44,44 %) 0,042 6,083 Resektabilität R0 R1 / R2 67 49 7 (10,45 %) 14 (28, 57 %) 0,562 0,693 Metastase Ja Nein 27 89 19 (70,37 %) 2 (2,25 %) 0,000 29,792 Lokalrezidiv Ja Nein 52 64 15 (28,85 %) 6 (9,4 %) 0,226 0,410 Tumorgröße < 5 cm ≥ 5 cm 47 69 4 (8,51 %) 17 (24, 64 %) 0,366 2,093 Tumortiefe Subcutan Subfaszial 58 58 8 (13,79 %) 13 (22,41 %) 0,212 2,501 a Die Gesamtzahl liegt in dieser Kategorie unterhalb der Gesamtzahl der untersuchten Patienten, da das Grading von 6 Patienten im Lokalrezidiv unklar blieb und diese daher in die statistische Berechnung nicht mit eingingen. 47 Für das Auftreten von Lokalrezidiven konnte in der univariaten Analyse die Resektabilität (R0 vs. R1/R2) als statistisch signifikanter (p<0,000) Risikofaktor ermittelt werden (Abbildung 10). Ebenso hat die Wachstumsform (infiltrativ vs. Pseudokapsel) statistisch signifikanten (p<0,0136) Einfluss auf die Loklarezidiventstehung (Tabelle 15). Für andere Marker konnte kein Einfluss gefunden werden (Tabelle 15). In der multivariaten Analyse waren die Resektabilität (p<0,00), die Entdifferenzierung (p<0,001) und die Tumortiefe (p<0,01) signifikant prognostisch ungünstige Variablen für die rezidivfreie Zeit. Das Risiko, ein Lokalrezidiv zu entwickeln, war für einen Patienten, der eine R1-Resektion seines Primärtumors erhalten hatte, um den Faktor 5,6 höher als für einen R0-resezierten Patienten. Abbildung 10: Geschätzte rezidivfreie Überlebenswahrscheinlichkeit in Jahren in Abhängigkeit von der Resektabilität des Primärtumors. 48 Tabelle 15 Ermittlung von Prognosefaktoren für das Auftreten von Rezidiven in der univariaten Analyse unter Verwendung des Log Rank Tests a Kennzeichen Patientenzahl Rezidive (%) p-Wert Alter < 50 Jahre ≥ 50 Jahre 59 57 25 (42,37 %) 27 (47,37 %) 0,0816 Geschlecht Männlich Weiblich 70 46 32 (45,71 %) 20 (43,48 %) 0,6134 Symptomdauer ≤ 5 Monate > 5 Monate 49 c 54 19 (38,80 %) 26 (48,15 %) 0,1477 Grading im Verlauf G1 G2 / G3 92 a 18 28 (30,43 %) 18 (100 %) 0,000 Resektabilität R0 R1 67 49 12 (17,91 %) 40 (81,63 %) 0,000 Wachtumsverhalten Gekapselt Infiltrativ 55b 53 17 (30,91 %) 31 (58,49 %) 0,0136 Tumorgröße < 5 cm ≥ 5 cm 47 69 18 (38,30 %) 34 (49,28 %) 0,2601 Tumortiefe 0,3262 29 (50 %) 58 Subcutan 23 (39,66 %) 58 Subfaszial Die Gesamtzahl liegt in dieser Kategorie unterhalb der Gesamtzahl der untersuchten Patienten, da das Grading von 6 Patienten im Lokalrezidiv unklar blieb und diese daher in die statistische Berechnung nicht mit eingingen. b 8 Patienten mit Satellitenknoten beziehungsweise unklarem Wachstumsverhalten wurden aus der Berechnung ausgeschlossen. c 13 Patienten sind bei fehlender Angabe zur Symptomdauer aus der Berechnung ausgeschlossen worden. 49 Die univariate Analyse zeigte, dass die Entdifferenzierung ein signifikanter (p=0,0089) Risikofaktor für die Entstehung von Fernmetastasen ist (Tabelle 16). Das Risiko eines Patienten mit einem G2-Tumor im Lokalrezidiv, eine Fernmetastase zu entwickeln, ist im Vergleich zu einem Patienten mit einem G1-Lokalrezidiv um den Faktor 11 erhöht. Eine subfasziale Tumorlokalisation ist ebenfalls ein signifikanter (p=0,0285) Risikofaktor für die Entstehung einer Fernmetastase. Eine Tumorgröße über 5 cm ist prognostisch ebenfalls, wenn auch nicht statistisch signifikant (p=0,0748), ungünstig. Der Einfluss weiterer Variablen auf die Fernmetastasenentstehung konnten nicht gefunden werden (Tabelle 16). Eine multivariate Analyse der Risikofaktoren für die Fernmetastasenentstehung war aufgrund der kleinen Fallzahl nicht möglich. 50 Tabelle 16 Ermittlung von Prognosefaktoren für die Entstehung von Fernmetastasen in der univariaten Analyse unter Verwendung des Log Rank Tests Kennzeichen Patientenzahl Metastase (%) p-Wert Alter < 50 Jahre ≥ 50 Jahre 59 57 14 (23,73 %) 13 (22,81 %) 0,4341 Geschlecht Männlich Weiblich 70 46 15 (21,43 %) 12 (26,10 %) 0,6771 Symptomdauer ≤ 5 Monate > 5 Monate 49 c 54 10 (20,40 %) 15 (27,78 %) 0,3936 Grading im Verlauf G1 G2 / G3 92 a 18 15 (16,3 %) 9 (50 %) 0,0089 Resektabilität R0 R1 / R2 67 49 8 (11,94 %) 19 (38,78 %) 0,1490 Lokalrezidiv Ja Nein 52 64 19 (36,54 %) 8 (12,5 %) 0,2063 Wachtumsverhalten Gekapselt Infiltrativ 55b 53 9 (16 %) 16 (30,2 %) 0,7166 Tumorgröße < 5 cm ≥ 5 cm 47 69 6 (12,77 %) 21 (30,43 %) 0,0748 Tumortiefe Subcutan 58 9 (15,52 %) 0,0285 Subfaszial 58 19 (32,76 %) a Die Gesamtzahl liegt in dieser Kategorie unterhalb der Gesamtzahl der untersuchten Patienten, da das Grading von 6 Patienten im Lokalrezidiv unklar blieb und diese daher in die statistische Berechnung nicht mit eingingen. b 8 Patienten mit Satellitenknoten beziehungsweise unklarem Wachstumsverhalten wurden aus der Berechnung ausgeschlossen. c 13 Patienten sind bei fehlender Angabe zur Symptomdauer aus der Berechnung ausgeschlossen worden. 51 4 Diskussion Weichteilsarkome sind eine seltene Gruppe von Tumoren, die etwa 1 % aller malignen Erkrankungen des Erwachsenenalters und 15 % des Kindesalters ausmachen. Sie können in allen Körperregionen entstehen, entwickeln sich jedoch in bis zu 50 % in den Extremitäten. Sie können in jedem Lebensalter auftreten, eine Prädominanz für ein Geschlecht liegt nicht vor. In der hier vorgelegten Untersuchung wurden 116 Patienten mit ausschließlich hochdifferenzierten (G1) Weichteilsarkomen an Extremitäten und Rumpf aufgenommen. Ein grundsätzliches Problem, welches die Vergleichbarkeit mit bislang publizierten Studien erschwert, ist die weltweit zum Teil uneinheitliche Klassifizierung der Weichteilsarkome. So wird zum Teil die Einteilung in low-grade versus high-grade Sarkome gewählt. Gerade bei dieser Einteilung herrschen für die Beurteilung der Ergebnisse entscheidende Unstimmigkeiten: so fasst Trovik G1 und G2 Sarkome zu den low grade Sarkomen zusammen (Trovik und Bauer, 1994), hingegen wählt die Arbeitsgruppe von Choong eine Einteilung, in der die low-grade Sarkome aus G1-G3 bestehen und in der high-grade Gruppe nur die G4 Sarkome enthalten sind (Choong et al., 1995a). Daher wurde für diese Untersuchung die zur Zeit gebräuchliche Einteilung der UICC, welche mit der der AJCC übereinstimmt, gewählt. Um falsche Klassifikationen hinsichtlich des Gradings und damit einer Verfälschung der Datenauswertung zu vermeiden, wurden alle histologischen Präparate von einem auf diesem Gebiet erfahrenen Pathologen reklassifiziert. Ein weiterer wesentlicher Unterschied zu bislang publizierten Untersuchungen ist die Fokussierung auf Patienten mit G1 Weichteilsarkomen. Frühere Studien betrachten häufig ein gemischtes Kollektiv aller drei Gradingeinteilungen, wobei die niedrigdifferenzierten Sarkome den Hauptteil des Krankengutes ausmachten (Coindre et al., 1996, Tomita et al., 52 1994, Coindre et al., 2001, Pisters et al., 1996b, Billingsley et al., 1999). Gründe, aus denen diese Ungleichgewichtung resultiert, sind das häufigere Vorkommen von G3 im Vergleich zu G1 Sarkomen (Tomita et al., 1994, Coindre et al., 2001, Singer et al., 1994). Zudem lenkt die deutlich höhere Malignität dieser Tumoren das Hauptinteresse auf diese Gruppe von Weichteilsarkomen. G3 Sarkome entwickeln in bis zu 50 % Metastasen, die 5-Jahres-Überlebensrate beträgt 38 % (Myhre-Jensen et al., 1983). Hingegen wird die Metastasierungswahrscheinlichkeit bei den hochdifferenzierten Sarkomen in der Literatur mit unter 15 % angegeben (Lewis et al., 1999). Wahrscheinlich liegt sie jedoch sogar deutlich niedriger, da die publizierten Zahlen auf Studien beruhen, die G1 und G2 Sarkome zu low-grade Sarkomen zusammengefasst haben. Hochdifferenzierte Weichteilsarkome werden daher häufig in ihrer Gefährlichkeit unterbewertet. Dies äußert sich in der Annahme, dass hochdifferenzierte Weichteilsarkome vorwiegend zu Lokalrezidiven neigen und nur im Einzelfall fernmetastasieren. Auf die Problematik der möglichen Entdifferenzierung im Zuge von lokoregionären Rezidiven und dem damit verbundenen aggressiveren biologischen Verhalten wird in den meisten Studien nicht gezielt eingegangen. Es sollte daher an diesem großen Patientenkollektiv primärer G1 Weichteilsarkome die Entstehung sowie das Grading von Lokalrezidiven wie auch Determinanten der Fernmetastasierung untersucht werden. Die anamnestischen Daten unserer Patienten mit hochdifferenzierten Weichteilsarkomen an Extremitäten und Rumpf entsprachen weitgehend denen der Literatur (Billingsley et al., 1999, Tomita et al., 1994, Singer et al., 1994, Lewis et al., 1999). Die Tumoren traten in jedem Lebensalter auf, wobei der Altersdurchschnitt in unserem Patientengut bei 48 (15 86) Jahren lag. Ähnliche Angaben finden sich in der Literatur (Coindre et al., 2001, Peiper et al., 1995, Trovik und Bauer, 1999). 53 Am häufigsten stellten sich die Patienten mit einem schmerzlosen Tumor vor. Da die Beschwerden eher unspezifisch waren, lag die Dauer bis zur Diagnosesicherung im Mittel bei 12 (0-120) Monaten. Dies entspricht ebenfalls den Daten anderer Kollektive Literatur (Coindre et al., 2001, Peiper et al., 1995, Trovik und Bauer, 1999). Bei 99 (85,3 %) der Patienten fanden sich keine bekannten prädisponierenden Faktoren für ein Sarkomleiden. Bei vier Patienten (3,4 %) war die Lokalisation der späteren Sarkommanifestation zuvor aufgrund einer anderen Erkrankung bestrahlt worden. Zwei Patienten (1,7 %) entwickelten einen malignen peripheren Nervenscheidentumor im Rahmen eines Morbus von Recklinghausen. Des weiteren fand sich an prädisponierenden Faktoren in 2,6 % ein vorangegangenes Trauma und in 7 % ein benigner Tumor (4 x Lipom,2 x benignes Histiocytom,1 x Fibrom,1 x mesenchymaler Mischtumor) im späteren Operationsgebiet. Solch ein Übergang eines primär benignen Weichteiltumors in ein malignes Weichteilsarkom ist gut bekannt (Zornig und Schröder, 1992). Sarkome treten typischerweise an den Extremitäten auf (Lewis und Brennan, 1996, Peiper et al., 1997, Choong et al., 1995b). In der hier untersuchten Population manifestierte sich das Sarkom am häufigsten mit 54,3 % an der unteren Extremität, gefolgt von der oberen Extremität in 25 % und dem Rumpf in 20,7 % der Fälle. Diese anatomische Verteilung entspricht im wesentlichen der aller G1 – G3 Weichteilsarkome (n=629), die im selben Beobachtungszeitraum erfasst wurden (obere Extremität, 16,22 %; untere Extremität, 41,49 %; Rumpf, 14,15 %; andere Lokalisation, 28,14 %; Popovich, Zornig, unveröffentlichte Daten). Das Liposarkom (44,8%), das Fibrosarkom (14,7 %), der MPNST (10,3 %), das MFH (9,5 %) und das Leiomyosarkom mit 8,6 % waren die häufigsten klassifizierten histologischen Typen, wobei diese Verteilung im wesentlichen der anderer 54 Untersuchungen entspricht (Lewis und Brennan, 1996, Rougraff, 1999, Zornig et al., 1992, Trovik und Bauer, 1999). Insgesamt wurden 52 Patienten aufgrund von Lokalrezidiven behandelt. Auffälliges Charakteristikum von 40 dieser Patienten war, daß sie einen R1 Resektionsstatus aufwiesen. Tatsächlich konnte eine R1 Resektion in der univariaten Analyse als statistisch signifikanter Risikofaktor für das Auftreten eines Lokalrezidivs ermittelt werden. Von großer Bedeutung ist allerdings in diesem Zusammenhang, daß die Mehrzahl der primär nicht R0 resezierten Tumoren (insgesamt 49 / 116) nicht in einem mit der operativen Therapie von Weichteilsarkomen vertrauten Haus behandelt wurden (35 / 44 solcher Patienten gegenüber 14 / 72 aus dem UKE / Israelitisches Krankenhaus). Die häufigere R0 Resektion des Primärtumors in diesen Zentren spiegelt sich auch in einer mit 15,3 % niedrigen Lokalrezidivrate wieder. Andere Studien ermittelten Lokalrezidivraten von 18 % - 47 % (Heise et al., 1986, Markhede et al., 1982, Stotter et al., 1990, Peiper et al., 1995). Es zeigt sich damit, dass der Ort der Tumorersttherapie einen erheblichen Einfluß auf den weiteren Verlauf der Sarkomerkrankung hat (Kettelhack et al., 1998, Lehnert et al., 2000, Hoos et al., 2000, Gustafson et al., 1994). Neben einem R1-Resektionstatus war auch ein infiltratives Wachstum des Tumors ein signifikanter Risikofaktor für die Entstehung eines Lokalrezidivs. Bei den 52 Patienten mit Lokalrezidiv als zweiter Tumormanifestation konnte in 18 Fällen (34,61 %) eine Entdifferenzierung histologisch gesichert werden. Hierbei fand die Entdifferenzierung bei 11 dieser Patienten (61,1 %) im Zuge des ersten Lokalrezidives statt. Es ist zwar bekannt, dass Weichteilsarkome im Zuge des häufigen lokalen Rezidivierens einen Entdifferenzierungsprozeß durchlaufen können, allerdings wird in den großen Studien mit gemischten Patientenkollektiven auf diese Fragestellung nicht eingegangen. Die hier präsentierten Zahlen zeigen deutlich, daß bei mehr als 50 % der 55 Fälle eines Lokalrezidivs bereits im ersten Lokalrezidiv mit einer Entdifferenzierung und damit dem Übergang in ein aggressiveres Tumorwachstum, insbesondere mit Fernmetastasenentstehung, gerechnet werden muß. Die Bedeutung von Lokalrezidiven für ein erhöhtes Risiko einer Fernmetastasenentwicklung konnte in verschiedenen Studien belegt werden (Trovik und Bauer, 1994, Gustafson et al., 1993, Choong et al., 1995a, Stotter et al., 1990, Singer et al., 1994). In unserem Patientenkollektiv zeigte sich, dass in 36,53 % der Fernmetastasenentstehung ein oder mehrere Lokalrezidive vorrangingen (19 Patienten von 52 mit Lokalrezidiven). Weiterhin fanden wir, dass die Entdifferenzierung im vorangehenden Lokalrezidiv einen Einfluss auf die Fernmetastasenentstehung hat. 28,6 % der im Lokalrezidiv weiterhin hochdifferenzierten Weichteilsarkome entwickelten Fernmetastasen (8/28), hingegen entwickelten 55,5 % (5/9) der im Lokalrezidiv zu G2 und 37,5% (3/9) der im Lokalrezidiv zu G3 entdifferenzierten Weichteilsarkome Fernmetastasen. In der univariaten Analyse war die Entdifferenzierung im Verlauf und eine subfasziale Lokalisation des Primärtumors signifikant beeinflussend auf die Fernmetastasenentstehung. Entsprechend den Angaben anderer Studien konnte die Tumorgrösse auch in unserem Patientenkollektiv als ein ungünstiger Marker determiniert werden (Billingsley et al., 1999, Pisters et al., 1996b, Hashimoto et al., 1992, Coindre et al., 2001). Es ist jedoch von großer Bedeutung, daß eine Fernmetastasierung auch bei 8 von 64 (12,5 %) der Patienten ohne das Auftreten von Lokalrezidiven und damit auch ohne Entdifferenzierung auftrat. Um daher die Bedeutung einer Entdifferenzierung im Lokalrezidiv für die Entstehung einer Fernmetastase differenzierter zu beurteilen, ist eine isolierte Betrachtung der 27 Patienten mit Fernmetastasen notwendig. Von diesen wiesen 19 Patienten in der Vorgeschichte ein oder mehrere Lokalrezidive auf, welche bei 8 Patienten (42,11 %) entdifferenziert waren. Diese Zahlen machen deutlich, dass die ursprünglich hochdifferenzierten Weichteilsarkome im Rahmen einer Entdifferenzierung das biologisch aggressivere Verhalten und somit die Fernmetastasierunghäufigkeit eines 56 primär schlechter differenzierten Weichteilsarkoms annehmen. Jedoch muß darauf hingewiesen werden, daß auch 8 Patienten ohne vorherige Entdifferenzierung des Lokalrezidivs Fernmetastasen entwickelten. Außerdem kam es auch bei 8 Patienten, also 29,62 % aller Patienten mit einer Fernmetastase ohne vorheriges Lokalrezidiv zur Entstehung von Fernmetastasen. Zusammengefasst zeigen diese Daten erstmals, daß ein Großteil (59,26 %) aller Patienten mit Fernmetastasen keine Entdifferenzierung ihres lokalen Tumorwachtums erlebten. Die Prognose von hochdifferenzierten Weichteilsarkomen ist, verglichen mit anderen neoplastischen Erkrankungen, als gut zu beurteilen (Pisters et al., 1996b, Lewis und Brennan, 1996, Hashimoto et al., 1992, Markhede et al., 1982). So betrug die 5Jahresüberlebensrate auch in dem hier vorgestellten Patientenkollektiv 90,7 % und die 10Jahresüberlebensrate 83 %. Doch die hier vorgelegte Untersuchung zeigt auch, daß eine Bagatellisierung dieser Tumorerkrankung nicht angemessen ist. Denn 21 / 116 Patienten, also 18, 1 %, verstarben direkt an der Sarkomerkrankung, wobei immerhin 33,33 % dieser Patienten im Verlauf ihrer Erkrankung nicht entdifferenzierten. 5 Patienten (4,3 %) leben mit Tumor. Auffällig bei den an der Sarkomerkrankung verstorbenen Patienten war, daß 20 von ihnen eine Tumorzweitmanifestation im Sinne von Lokalrezidiv und / oder Fernmetastasen aufwiesen, wobei 19 dieser 20 Patienten Fernmetastasen entwickelt hatten. Tatsächlich zeigte sich in der univariaten wie auch multivariaten Analyse eine statistisch signifikante Prognoseverschlechterung bei Auftreten von Fernmetastasen. Das Risiko, am Weichteilsarkom zu versterben, ist bei Fernmetastasenentstehung um den Faktor 30 erhöht. Als weiterer sich statistisch sigifikant ungünstig auf das Überleben auswirkender Faktor ließ sich die Entdifferenzierung definieren (Risiko für Tumortod 11-fach erhöht), eine 57 Tumorgröße über 5 cm stellte sich als ungünstiger Marker ohne statistische Signifikanz dar (p = 0,055). Demnach müssen im Hinblick auf eine weitere Verbesserung der Prognose therapeutische Maßnahmen gefordert werden, die insbesondere die Entstehung von Fernmetastasen verhindern. Aus den genannten Daten wird ersichtlich, daß vor allem die Erzielung einer R0 Resektion des Primärtumores hierzu in der Lage ist. Der Resektionsstatus nimmt direkt statistisch signifikant Einfluß auf die Häufigkeit von Lokalrezidiven (Peiper et al., 1995, Barr et al., 1991, Gustafson und Rydholm, 1992, Gustafson et al., 1994, Singer et al., 1994, Lewis et al., 1997). Lokalrezidive sind ein statistisch signifikanter Risikofaktor für eine Fernmetastasenentstehung (Trovik et al., 2000, Gustafson et al., 1993, Barr et al., 1991). In dem hier vorgestellten Patientenkollektiv fand sich bei 19 / 27 Patienten mit Fernmetastasen ein vorangehendes Lokalrezidiv, so dass dessen Verhinderung auch die Entstehung von Fernmetastasen beeinflussen kann. Allerdings entwickelten auch 8 / 27 Patienten mit Fernmetastasen diese ohne vorheriges Lokalrezidiv. Diese Patienten waren jedoch durch große Primärtumoren (> 5 cm) und eine lange Symptomdauer vor Therapie gekennzeichnet. Daher erscheint es möglich, daß die rasche Diagnosesicherung und frühzeitige operative Therapie ebenfalls die Prognose von hochdifferenzierten Weichteilsarkomen beeinflussen kann. Als weitere therapeutische Optionen stehen die Strahlen- und Chemotherapie zur Verfügung (Lewis und Brennan, 1996, Hoos et al., 2000). In unserem Kollektiv wurde die Strahlentherapie vorwiegend bei R1-resezierten Primärtumoren oder nach Lokalrezidiven eingesetzt. Die Chemotherapie wurde vorwiegend als palliative Therapieform bei nicht resektablen Fernmetastasen genutzt. Beide Therapieformen erzielten in unserem Patientenkollektiv keine überzeugenden Ergebnisse hinsichtlich der Lokalrezidiv- und 58 Fernmetastasenrate. Jedoch kann nicht ausgeschlossen werden, daß die Prognose bei bestimmten Patienten günstig beeinflusst wird. Die Möglichkeit der Entstehung von Lokalrezidiven, welche wiederum Grundlage für eine Entdifferenzierung und damit den Übergang in einen prognostisch ungünstigeren Verlauf darstellt, macht es notwendig, daß Patienten mit hochdifferenzierten Weichteilsarkomen einer regelmäßigen Tumornachsorge unterzogen werden. Diese sollte in den ersten beiden Jahren nach Auftreten der Primärmanifestation eine lokale Tumorkontrolle im Sinne einer MRT-Untersuchung und eine Thoraxübersichtsaufnahme in dreimonatigen Abständen beinhalten (Lewis und Brennan, 1996, Rougraff, 1999). Für die darauffolgenden drei Jahre ist ein Nachsorgezeitraum von sechs Monaten ausreichend. Die hier vorgelegte Untersuchung macht deutlich, daß hochdifferenzierte Weichteilsarkome durch Entdiffernzierung im Lokalrezidiv und Fernmetastasenbildung eine ernstzunehmende maligne Erkrankung darstellen. Die weitere, gezielte Untersuchung dieser Patienten wird helfen, in Zukunft durch Verbesserung von Diagnostik und suffizienter Therapie die Prognose zu verbessern. 59 5 Zusammenfassung Weichteilsarkome können in allen Differenzierungsgraden vorkommen, wobei die hochdifferenzierten Tumoren als ungefährlicher gelten als niedrig differenzierte Sarkome. Bisher wurde angenommen, daß hochdifferenzierte Weichteilsarkome vorwiegend nur zu lokalen Rezidiven neigen und nur in sehr seltenen Fällen fernmetastasieren und zum Tod führen. Auf eine mögliche Entdifferenzierung bei lokalen Rezidiven und der damit verbundenen erhöhten Malignität dieser Weichteilsarkome wird in der Literatur nicht eingegangen. Die hier vorgelegte Untersuchung eines großen, aus 116 Patienten bestehenden Kollektivs mit ausschließlich hochdifferenzierten Weichteilsarkomen an Extremitäten und Rumpf zeigt, daß hochdifferenzierte Weichteilsarkome in relevantem Umfang Fernmetastasen entwickeln (23,3 %). Wichtigster Risikofaktor für ihre Entstehung ist eine Entdifferenzierung im Lokalrezidiv, die bei 35 % der Patienten mit Lokalrezidiv gefunden werden konnte. Die Entdifferenzierung ist mit einem 11-fach erhöhten Risiko für die Entstehung einer Fernmetastase verbunden. Allerdings zeigte sich ebenfalls, daß Weichteilsarkome auch ohne Entdifferenzierung oder sogar primär, das heißt auch ohne vorheriges Lokalrezidiv, Fernmetastasen entwickeln können (16 / 27 Patienten mit Fernmetastasen). Fernmetastasen waren der entscheidende, statistisch signifikante Marker eines prognostisch ungünstigen Verlaufs und mit einem 30-fach erhöhten Risiko, an der Sakomerkrankung zu versterben, assoziiert. Weiterhin zeigte sich, dass auch die Entdifferenzierung im Lokalrezidiv ein signifikanter Faktor für die Verkürzung der Überlebenszeit darstellt. Als Konsequenz ergibt sich, daß das Ziel aller diagnostischen wie auch therapeutischen Maßnahmen die Verhinderung eines Lokalrezidives (und damit einer möglichen Entdifferenzierung) sowie der Entstehung von Fernmetastasen sein muß. Dies kann durch eine rasche Diagnose sowie die frühzeitige, optimale operative Therapie in 60 einem Zentrum ermöglicht werden. Es ist wahrscheinlich, daß hierdurch die Prognose von Patienten mit hochdifferenzierten Weichteilsarkomen weiter verbessert werden kann. 61 6 Literaturverzeichnis 1. Barken D, Wright E und Nguyen K. 1987. Gene for von Recklinghausen neurofibromatosis is in the pericentromeric region of chromosome 17. Science 236:1100-1102. 2. Barr, L. C., A. T. Stotter und R. P. A'Hern. 1991. Influence of local recurrence on survival: a controversy reviewed from the perspective of soft tissue sarcoma. Br. J. Surg. 78:648-650. 3. Beahrs OH, Henson DE, Hutter RVP und Myers MH. 1992. AJCC (American Joint Comittee on Cancer): manual for staging of cancer In Beahrs OH, Henson DE, Hutter RVP, and Myers MH (ed.), 4 ed. Lippincott, Philadelphia. 4. Billingsley, K. G., J. J. Lewis, D. H. Leung, E. S. Casper, J. M. Woodruff und M. F. Brennan. 1999. Multifactorial analysis of the survival of patients with distant metastasis arising from primary extremity sarcoma. Cancer 85:389-395. 5. Brady, M. S., J. J. Gaynor und M. F. Brennan. 1992. Radiation-associated sarcoma of bone and soft tissue. Arch. Surg. 127:1379-1385. 6. Brennan, M. F., E. S. Casper, L. B. Harrison, M. H. Shiu, J. Gaynor und S. I. Hajdu. 1991. The role of multimodality therapy in soft-tissue sarcoma. Ann. Surg. 214: 328-336. 7. Bujko, K., H. D. Suit, D. S. Springfield und K. Convery. 1993. Wound healing after preoperative radiation for sarcoma of soft tissues. Surg. Gynecol. Obstet. 176:124-134. 8. Cance, W. G., M. F. Brennan, M. E. Dudas, C. M. Huang und C. CordonCardo. 1990. Altered expression of the retinoblastoma gene product in human sarcomas. N. Engl. J. Med. 323:1457-1462. 62 9. Casper, E. S., J. J. Gaynor, L. B. Harrison, D. M. Panicek, S. I. Hajdu und M. F. Brennan. 1994. Preoperative and postoperative adjuvant combination chemotherapy for adults with high grade soft tissue sarcoma. Cancer 73:1644-1651. 10. Cheng, E. Y., K. E. Dusenbery, M. R. Winters und R. C. Thompson. 1996. Soft tissue sarcomas: preoperative versus postoperative radiotherapy. J. Surg. Oncol. 61:90-99. 11. Choong, P. F., P. Gustafson und A. Rydholm. 1995a. Size and timing of local recurrence predicts metastasis in soft tissue sarcoma. Growth rate index retrospectively analyzed in 134 patients. Acta Orthop. Scand. 66:147-152. 12. Choong, P. F., A. Rydholm und P. Gustafson. 1995b. Patients with soft-tissue sarcomas. Ann. Surg. 221:203-205. 13. Chung, K. C., H. J. Kim und L. L. Jeffers. 2000. Lymphangiosarcoma (StewartTreves syndrome) in postmastectomy patients. J. Hand Surg. [Am. ] 25:1163-1168. 14. Coia, L. R., J. T. Fazekas und S. Kramer. 1980. Postirradiation sarcoma of the head and neck: a report of three late sarcomas following therapeutic irradiation for primary malignancies of the paranasal sinus, nasal cavity, and larynx. Cancer 46:1982-1985. 15. Coindre, J. M., P. Terrier, N. B. Bui, F. Bonichon, F. Collin, D. Le, V, A. M. Mandard, M. O. Vilain, J. Jacquemier, H. Duplay, X. Sastre, C. Barlier, M. Henry-Amar, J. Mace-Lesech und G. Contesso. 1996. Prognostic factors in adult patients with locally controlled soft tissue sarcoma. A study of 546 patients from the French Federation of Cancer Centers Sarcoma Group. J. Clin. Oncol. 14:869877. 16. Coindre, J. M., P. Terrier, L. Guillou, D. Le, V, F. Collin, D. Ranchere, X. Sastre, M. O. Vilain, F. Bonichon und B. B. N'Guyen. 2001. Predictive value of grade for metastasis development in the main histologic types of adult soft tissue 63 sarcomas: a study of 1240 patients from the French Federation of Cancer Centers Sarcoma Group. Cancer 91:1914-1926. 17. Coindre, J. M., M. Trojani, G. Contesso, M. David, J. Rouesse, N. B. Bui, A. Bodaert, M. de, I, A. De Mascarel und J. F. Goussot. 1986. Reproducibility of a histopathologic grading system for adult soft tissue sarcoma. Cancer 58:306-309. 18. Cox DR. 1972. Regression models and life tables (with discussion). Journal of the royal Statistical Society of Britan 34:187-220. 19. Enneking WF. 1984. Staging of musculoskeletal neoplasms In Current concepts of diagnosis and treatment of bone and soft tissue tumors Springer, Heidelberg. 20. Enneking, W. F. 1988. A system of staging musculoskeletal neoplasms. Instr. Course Lect. 37:3-10. 21. Enzinger FM und Weiss SW. 1994. Soft tissue tumors 3 ed. Mosby, St. Louis. 22. Fingerhut, M. A., W. E. Halperin, D. A. Marlow, L. A. Piacitelli, P. A. Honchar, M. H. Sweeney, A. L. Greife, P. A. Dill, K. Steenland und A. J. Suruda. 1991. Cancer mortality in workers exposed to 2,3,7,8-tetrachlorodibenzop-dioxin. N. Engl. J. Med. 324:212-218. 23. Fletcher, J. A. 1991. Laboratory investigation, genetics, and experimental models in sarcomas. Curr. Opin. Oncol. 3:665-670. 24. Fong, Y., D. G. Coit, J. M. Woodruff und M. F. Brennan. 1993. Lymph node metastasis from soft tissue sarcoma in adults. Analysis of data from a prospective database of 1772 sarcoma patients. Ann. Surg. 217:72-77. 25. Gaynor, J. J., C. C. Tan, E. S. Casper, C. F. Collin, C. Friedrich, M. Shiu, S. I. Hajdu und M. F. Brennan. 1992. Refinement of clinicopathologic staging for localized soft tissue sarcoma of the extremity: a study of 423 adults. J. Clin. Oncol. 10:1317-1329. 64 26. Geer, R. J., J. Woodruff, E. S. Casper und M. F. Brennan. 1992. Management of small soft-tissue sarcoma of the extremity in adults. Arch. Surg. 127:1285-1289. 27. Gortzak, E. und F. van Coevorden. 1995. Soft tissue sarcoma--messages from completed randomized trials. Eur. J. Surg. Oncol. 21:469-471. 28. Gustafson, P., K. E. Dreinhofer und A. Rydholm. 1993. Metastasis-free survival after local recurrence of soft-tissue sarcoma. J. Bone Joint Surg. Br. 75:658-660. 29. Gustafson, P., K. E. Dreinhofer und A. Rydholm. 1994. Soft tissue sarcoma should be treated at a tumor center. A comparison of quality of surgery in 375 patients. Acta Orthop. Scand. 65:47-50. 30. Gustafson, P. und A. Rydholm. 1992. Selection bias in treatment of soft-tissue sarcoma. J. Bone Joint Surg. Br. 74:501-503. 31. Hajdu SI. 1986. Differential diagnosis of soft tissue and bone tumors, 1st ed. Lea & Febiger, Philadelphia. 32. Hardell, L. und A. Sandstrom. 1979. Case-control study: soft-tissue sarcomas and exposure to phenoxyacetic acids or chlorophenols. Br. J. Cancer 39:711-717. 33. Hashimoto, H., Y. Daimaru, S. Takeshita, M. Tsuneyoshi und M. Enjoji. 1992. Prognostic significance of histologic parameters of soft tissue sarcomas. Cancer 70:2816-2822. 34. Heise, H. W., M. H. Myers, W. O. Russell, H. D. Suit, F. M. Enzinger, J. H. Edmonson, J. Cohen, R. G. Martin, W. T. Miller und S. I. Hajdu. 1986. Recurrence-free survival time for surgically treated soft tissue sarcoma patients. Multivariate analysis of five prognostic factors. Cancer 57:172-177. 35. Hengge, U. R., T. Ruzicka, S. K. Tyring, M. Stuschke, M. Roggendorf, R. A. Schwartz und S. Seeber. 2002. Update on Kaposi's sarcoma and other HHV8 associated diseases. Part 1: epidemiology, environmental predispositions, clinical manifestations, and therapy. Lancet Infect. Dis. 2:281-292. 65 36. Herbert, S. H., B. W. Corn, L. J. Solin, R. M. Lanciano, D. J. Schultz, W. G. McKenna und L. R. Coia. 1993. Limb-preserving treatment for soft tissue sarcomas of the extremities. The significance of surgical margins. Cancer 72:12301238. 37. Hermanek P, Spiessel B, und Wagner G. 1987. TNM-Klassifikation maligner Tumoren (IUCC), pp. 156-179. 4 ed. Springer, Berlin-Heidelberg-New YorkTokyo. 38. Hew L, Kandel R, Davis A und O´Sullivan B. 1994. Histological necrosis in soft tissue sarcoma following preoperative radiation. J. Surg. Oncol. 57:111-117. 39. Hoar, S. K., A. Blair, F. F. Holmes, C. D. Boysen, R. J. Robel, R. Hoover und J. F. Fraumeni, Jr. 1986. Agricultural herbicide use and risk of lymphoma and soft-tissue sarcoma. JAMA 256:1141-1147. 40. Hoos, A., J. J. Lewis und M. F. Brennan. 2000. [Soft tissue sarcoma: prognostic factors and multimodal treatment]. Chirurg 71:787-794. 41. Kang, H., F. M. Enzinger, P. Breslin, M. Feil, Y. Lee, B. Shepard und F. Enziger. 1987. Soft tissue sarcoma and military service in Vietnam: a case-control study. J. Natl. Cancer Inst. 79:693-699. 42. Kaplan EL und Meier P. 1958. Nonparametric estimation from incomplete observation. Journal of the American Statistical Association 53:457-481. 43. Kettelhack Ch, Tunn U und Schlag PM. 1998. Strategie multimodaler Therapie bei Weichgewebssarkomen des Stammes und der Extremitäten. Chirurg393-401. 44. Kramarova, E., M. Kogevinas, C. T. Anh, H. D. Cau, L. C. Dai, S. D. Stellman und D. M. Parkin. 1998. Exposure to Agent Orange and occurrence of soft-tissue sarcomas or non-Hodgkin lymphomas: an ongoing study in Vietnam. Environ. Health Perspect. 106 Suppl 2:671-678. 66 45. Lehnert, T., M. Schwarzbach, F. Willeke, M. Treiber, U. Hinz, M. M. Wannenmacher und C. Herfarth. 2000. Intraoperative radiotherapy for primary and locally recurrent soft tissue sarcoma: morbidity and long-term prognosis. Eur. J. Surg. Oncol. 26 Suppl A:S21-S24. 46. Lewis, J. J. und M. F. Brennan. 1996. Soft tissue sarcomas. Curr. Probl. Surg. 33:817-872. 47. Lewis, J. J., D. Leung, E. S. Casper, J. Woodruff, S. I. Hajdu und M. F. Brennan. 1999. Multifactorial analysis of long-term follow-up (more than 5 years) of primary extremity sarcoma. Arch. Surg. 134:190-194. 48. Lewis, J. J., D. Leung, M. Heslin, J. M. Woodruff und M. F. Brennan. 1997. Association of local recurrence with subsequent survival in extremity soft tissue sarcoma. J. Clin. Oncol. 15:646-652. 49. Li F P und Fraumeni J F Jr. 1969. Soft-tissue sarcomas, breast cancer, and other neoplasms: a familial syndrom? Annals of Internal Medicine 71:747-752. 50. Lienard, D., P. Ewalenko, J. J. Delmotte, N. Renard und F. J. Lejeune. 1992. High-dose recombinant tumor necrosis factor alpha in combination with interferon gamma and melphalan in isolation perfusion of the limbs for melanoma and sarcoma. J. Clin. Oncol. 10:52-60. 51. Mann, G. B., J. J. Lewis und M. F. Brennan. 1999. Adult soft tissue sarcoma. Aust. N. Z. J. Surg. 69:336-343. 52. Markhede, G., L. Angervall und B. Stener. 1982. A multivariate analysis of the prognosis after surgical treatment of malignant soft-tissue tumors. Cancer 49:17211733. 53. Mulligan, L. M., G. J. Matlashewski, H. J. Scrable und W. K. Cavenee. 1990. Mechanisms of p53 loss in human sarcomas. Proc. Natl. Acad. Sci. U. S. A 87:5863-5867. 67 54. Mundt, A. J., A. Awan, G. S. Sibley, M. Simon, S. J. Rubin, B. Samuels, W. Wong, M. Beckett, S. Vijayakumar und R. R. Weichselbaum. 1995. Conservative surgery and adjuvant radiation therapy in the management of adult soft tissue sarcoma of the extremities: clinical and radiobiological results. Int. J. Radiat. Oncol. Biol. Phys. 32:977-985. 55. Myhre-Jensen, O., S. Kaae, E. H. Madsen und O. Sneppen. 1983. Histopathological grading in soft-tissue tumours. Relation to survival in 261 surgically treated patients. Acta Pathol. Microbiol. Immunol. Scand. [A] 91:145150. 56. Peiper, M., D. Zurakowski und C. Zornig. 1995. [Local recurrence of soft tissue sarcoma of the extremities and trunk]. Langenbecks Arch. Chir 380:333-339. 57. Peiper, M., D. Zurakowski und C. Zornig. 1997. Survival in primary soft tissue sarcoma of the extremities and trunk. Langenbecks Arch. Chir 382:203-208. 58. Pezzi, C. M., R. E. Pollock, H. L. Evans, J. G. Lorigan, T. A. Pezzi, R. S. Benjamin und M. M. Romsdahl. 1990. Preoperative chemotherapy for soft-tissue sarcomas of the extremities. Ann. Surg. 211:476-481. 59. Pisters, P. W., L. B. Harrison, D. H. Leung, J. M. Woodruff, E. S. Casper und M. F. Brennan. 1996a. Long-term results of a prospective randomized trial of adjuvant brachytherapy in soft tissue sarcoma. J. Clin. Oncol. 14:859-868. 60. Pisters, P. W., D. H. Leung, J. Woodruff, W. Shi und M. F. Brennan. 1996b. Analysis of prognostic factors in 1,041 patients with localized soft tissue sarcomas of the extremities. J. Clin. Oncol. 14:1679-1689. 61. Potter, D. A., J. Glenn, T. Kinsella, E. Glatstein, E. E. Lack, C. Restrepo, D. E. White, C. A. Seipp, R. Wesley und S. A. Rosenberg. 1985. Patterns of recurrence in patients with high-grade soft-tissue sarcomas. J. Clin. Oncol. 3:353-366. 68 62. Rooser, B., R. Attewell, N. O. Berg und A. Rydholm. 1988. Prognostication in soft tissue sarcoma. A model with four risk factors. Cancer 61:817-823. 63. Rougraff B. 1999. The Diagnosis and Management of Soft Tissue Sarcomas of the Extremities in the Adult. Current Problems in Cancer 64. Saddegh, M. K., J. Lindholm, A. Lundberg, U. Nilsonne und A. Kreicbergs. 1992. Staging of soft-tissue sarcomas. Prognostic analysis of clinical and pathological features. J. Bone Joint Surg. Br. 74:495-500. 65. Schwarzbach, M., F. Willeke, M. Eble, T. Lehnert, V. Ewerbeck, M. Wannenmacher und C. Herfarth. 1996. [Intraoperative radiotherapy in advanced soft tissue sarcoma of the extremities]. Langenbecks Arch. Chir Suppl Kongressbd. 113:214-217. 66. Sindelar, W. F., T. J. Kinsella, P. W. Chen, T. F. DeLaney, J. E. Tepper, S. A. Rosenberg und E. Glatstein. 1993. Intraoperative radiotherapy in retroperitoneal sarcomas. Final results of a prospective, randomized, clinical trial. Arch. Surg. 128:402-410. 67. Singer, S., J. M. Corson, R. Gonin, B. Labow und T. J. Eberlein. 1994. Prognostic factors predictive of survival and local recurrence for extremity soft tissue sarcoma. Ann. Surg. 219:165-173. 68. Smith, J. 1987. Postradiation sarcoma of bone in Hodgkin disease. Skeletal Radiol. 16:524-532. 69. Sorensen SA, Mulvihill JJ und Nielsen A. 1986. Long-term follow-up of von Recklinghausen neurofibromatosis: survival and malignant neoplasms. New England Journal of Medicin 314:1010-1015. 70. Sreekantaiah, C. 1998. The cytogenetic and molecular characterization of benign and malignant soft tissue tumors. Cytogenet. Cell Genet. 82:13-29. 69 71. Sreekantaiah, C., C. P. Karakousis, S. P. Leong und A. A. Sandberg. 1992. Cytogenetic findings in liposarcoma correlate with histopathologic subtypes. Cancer 69:2484-2495. 72. Stotter, A. T., R. P. A'Hern, C. Fisher, A. F. Mott, M. E. Fallowfield und G. Westbury. 1990. The influence of local recurrence of extremity soft tissue sarcoma on metastasis and survival. Cancer 65:1119-1129. 73. Strong, L. C., W. R. Williams und M. A. Tainsky. 1992. The Li-Fraumeni syndrome: from clinical epidemiology to molecular genetics. Am. J. Epidemiol. 135:190-199. 74. Suit, H. D., H. J. Mankin, W. C. Wood, M. C. Gebhardt, D. C. Harmon, A. Rosenberg, J. E. Tepper und D. Rosenthal. 1988. Treatment of the patient with stage M0 soft tissue sarcoma. J. Clin. Oncol. 6:854-862. 75. Tierney, J. F., V. Mosseri, L. A. Stewart, R. L. Souhami und M. K. Parmar. 1995. Adjuvant chemotherapy for soft-tissue sarcoma: review and meta-analysis of the published results of randomised clinical trials. Br. J. Cancer 72:469-475. 76. Tomita, Y., S. Kuratsu, N. Naka, A. Uchida, K. Ono, M. Ohsawa und K. Aozasa. 1994. A staging system for soft-tissue sarcoma and its evaluation in relation to treatment. Int. J. Cancer 58:168-173. 77. Trovik, C. S. und H. C. Bauer. 1994. Local recurrence of soft tissue sarcoma a risk factor for late metastases. 379 patients followed for 0.5-20 years. Acta Orthop. Scand. 65:553-558. 78. Trovik, C. S. und H. C. Bauer. 1999. Local recurrence after surgery for soft tissue sarcoma. The Scandinavian Sarcoma Group experience. Acta Orthop. Scand. Suppl 285:45-46. 79. Trovik, C. S., H. C. Bauer, T. A. Alvegard, H. Anderson, C. Blomqvist, O. Berlin, P. Gustafson, G. Saeter und A. Walloe. 2000. Surgical margins, local 70 recurrence and metastasis in soft tissue sarcomas: 559 surgically-treated patients from the Scandinavian Sarcoma Group Register. Eur. J. Cancer 36:710-716. 80. Willet CG, Schiller AL, Suit HD, Mankin HJ und Rosenberg A. 1987. The histologic response of soft tissue sarcoma to radiation therapy. Cancer 60:15001505. 81. Wingren, G., M. Fredrikson, H. N. Brage, B. Nordenskjold und O. Axelson. 1990. Soft tissue sarcoma and occupational exposures. Cancer 66:806-811. 82. Zalupski MM, Ryan JA und Hussein ME. 1993. Defining the role adjuvant chemotherapy for patients with soft tissue sarcoma of the extremities, pp. 385-394. In Salmon SE (ed.), Adjuvant therapy of cancer VII Lippincott, Philadelphia. 83. Zornig C. 1997. Weichteiltumoren, pp. 742-747. In Häring R und Zilch H (ed.), Chirurgie De Gruyter, Berlin New York. 84. Zornig, C. und S. Schröder. 1992. Does malignant transformation of benign softtissue tumours occur? A clinicomorphological study of ten initially misdiagnosed soft-tissue sarcomas. J. Cancer Res. Clin. Oncol. 118:166-169. 85. Zornig, C., H. J. Weh, A. Krull, R. Schwarz, R. E. Hilgert und S. Schroder. 1992. Soft tissue sarcomas of the extremities and trunk in the adult. Report of 124 cases. Langenbecks Arch. Chir 377:28-33. 71 7 Danksagungen Herrn Professor Dr. med. C. Zornig möchte ich für die Überlassung des Themas und die exzellente Betreuung danken. Weiterhin danke ich Herrn Professor Dr. med. S. Schröder für seine stete Kooperationsbereitschaft, die kompetente Begutachtung der immnunhistologischen Präparate und für die Beantwortung aller histologischen Fragen. Desweiterten gilt mein Dank den niedergelassenen Kollegen und Pathologen, die mir fehlende Befunde haben zukommen lassen. Ein besonderer Dank gilt den Patienten und ihren Angehörigen, die mir alle Fragen bezüglich ihrer Erkrankung beantwortet haben, ohne sie wäre eine Aktualisierung des Patientenkollektives nicht möglich gewesen. Weiterhin gilt mein Dank dem Institut für Biomathematik des Universitätsklinikums Hamburg-Eppendorf für die Überlassung und Nutzung der SPSS-Software, sowie die Hilfestellung und Beratung statistischer Probleme durch Herrn Brose, Herrn Schoder und insbesondere Herrn Supplieth. Abschließend sei der Werner Otto-Stiftung für die finanzielle Unterstüztung gedankt, ohne die diese Arbeit nicht möglich gewesen wäre. 72 8 Lebenslauf Name: Gabriela Popovich Wohnort: Ellenbogen 2 20144 Hamburg Geburtstag: 23.04.1972 Geburtsort: Hildesheim Familienstand: ledig Nationalität: italienisch Schulbildung 1978 - 1982 Grundschule Sorsum 1982 - 1991 Marienschule Hildesheim 29.05.1991 Abitur Studium Oktober 1991 - August 1994 Vorklinisches Studium / Universität Hamburg Frühjahr 1996 1. Staatsexamen Frühjahr 1998 2. Staatsexamen Oktober 1998 Beginn des Praktischen Jahres 11.11.1999 3. Staatsexamen, Erteilung der Teilapprobation 01.07.2001 Erteilung der Vollapprobation Berufliche Tätigkeiten 01.01.2000 – 30.06.2001 Ärztin im Praktikum in der allgemeinchirurgischen Abteilung des Israelitischen Krankenhaus / Hamburg (Prof. Dr. C. Zornig) seit 01.07.2001 Assistenzärztin in der allgemeinchirurgischen Abteilung des Israelitischen Krankenhaus / Hamburg (Prof. Dr. C. Zornig) 73 Erklärung Ich versichere ausdrücklich, daß ich die Arbeit selbständig und ohne fremde Hilfe verfasst, andere als die von mir angegebenen Quellen oder Hilfsmittel nicht benutzt und die aus den benutzten Werken wörtlich oder inhaltlich entnommenen Stellen einzeln nach Ausgabe (Auflage und Jahr des Erscheinens), Band und Seite des benutzten Werkes kenntlich gemacht habe, und daß ich die Dissertation nicht einem Fachvertreter an einer anderen Hochschule zur Überprüfung vorgelegt oder mich anderweitig um Zulassung zur Promotion beworben habe. Gabriela Popovich