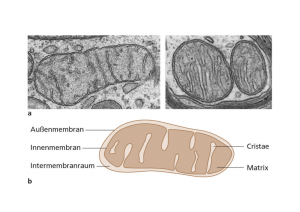
Der Malat
Werbung

Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: ► 1. Pyruvat ► 2. Malat ► 3. Aspartat ► 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: ► 1. Wasserstoffatomen > ► 2. Acetyl- CoA > ► 3. Acyl- CoA > ► 4. Oxalacetat > ► 5. ATP > Adenylat- Translocator Die innere Mitochondrienmebran ist durchlässig für: ► 1. Pyruvat ► 2. Malat ► 3. Aspartat ► 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: ► 1. Wasserstoffatomen > ( Oxalacetat) Malatshuttle ► 2. Acetyl- CoA > Citratshuttle ► 3. Acyl- CoA > Carnithin-shuttle ► 4. Oxalacetat > (Oxalacetat-) MalatShuttle ► 5. ATP > Adenylat- Translocator a Malat x Zytosol MALAT-ASPARTAT-SHUTTLE Malat Mito a Malat Oxalacetat x Zytosol MALAT-ASPARTAT-SHUTTLE Malat Oxalacetat Mito a Malat dehydro genase Malat NAD Malat MALAT-ASPARTAT-SHUTTLE NAD Malatdehydrogenase NADH2 Oxalacetat x Zytosol NADH2 Oxalacetat Mito a Malat dehydro genase Malat Malat MALAT-ASPARTAT-SHUTTLE NAD NAD Malatdehydrogenase NADH2 NADH2 Oxalacetat Oxalacetat GOT GOT x Zytosol Aspartat Aspartat Mito Aminosäuren & Ketosäuren Transaminasen: 1. Glutamat + Oxalacetat a-Ketoglutarat + Aspartat GOT = ASAT = Glutamat– Oxalactat– Transaminase 2. Glutamat + Pyruvat a-Ketoglutarat + Alanin GPT = ALAT = GLUTAMAT- PYRUVAT- TRANSAMINASE a Malat dehydro genase Malat Malat MALAT-ASPARTAT-SHUTTLE NAD NAD Malatdehydrogenase NADH2 Oxalacetat NADH2 Glutamat Glutamat GOT GOT a-Ketoglutarat x Zytosol Aspartat Oxalacetat Aspartat a-Ketoglutarat Mito Glycerin-3-P-Shuttle Glycerin-3-P Glycerin-3-P Dihydroxy aceton-P Dihydroxy a aceton-P Beachte Beziehung zur Glykolyse! MALAT-ASPARTAT-SHUTTLE x Zytosol Mito KOHLENHYDRATE Glucose Hexokinase 2+ Mg Kostet 1ATP Glucose-6-P Phospho Hexo isomerase Fructose-6-P ENDOPLASM.-RETIC. Fructose-1.6-Bisphosphat ALDOLASE Glycerinaldehyd-3-P (Aldose) 3-Phospho Glycerinaldehyd dehydrogenase Dihydroxyaceton-P (Ketose) Substratketten phosphorylierung 1,3-Bisphosphoglycerat ADP Pyruvat 3-Phospho glyceratkinase ATP 3-Phosohoglycerinsäure Mohammed Jaber ATP Phospho glycratmutase 2-Phospho glycerinsäure Pyruvatkinase ADP Enolase H2O geht ab Phosphoenolpyruvat NAD Glycerin-3-P 2H NADH2 Glycerin-3-P FAD 2H Dihydroxy aceton-P Dihydroxy a aceton-P FADH2 MALAT-ASPARTAT-SHUTTLE x Zytosol Mito NADH2 Dihydroxy aceton-P a-Glycerophosphat dehydrogenase 2H a-Glycerophosphat dehydrogenase NAD Glycerin-3-P Glycerin-3-P FAD 2H FADH2 Dihydroxy a aceton-P MALAT-ASPARTAT-SHUTTLE x Zytosol Mito NADH2 Malat dehydro genase Dihydroxy aceton-P Malat a-Glycerophosphat dehydrogenase 2H a-Glycerophosphat dehydrogenase NAD Glycerin-3-P Glycerin-3-P FAD 2H FADH2 Dihydroxy a aceton-P Malat MALAT-ASPARTAT-SHUTTLE NAD NAD Malatdehydrogenase NADH2 Oxalacetat NADH2 Glutamat Glutamat GOT GOT a-Ketoglutarat x Zytosol Aspartat Oxalacetat Aspartat a-Ketoglutarat Mito Atmungskette Was ist falsch? a) In den Mitochondrien findet die Oxidation des Substratwasserstoffs zu H2O statt b) Am Wasserstoff-bzw. Elektronentransport in der Atmungskette ist das FAD beteiligt c) Die innere Mito.-Membran ist für Malat durchlässig d) Der Glycerin-3-P-Shuttle gibt die Reduktionsäquivalente von NADH2 an den Komplex I e) Die Selbstregulation der Atmungskette (Atmungskontrolle) erfolgt durch den ATP/ADP-Quotienten Atmungskette Was ist falsch? a) In den Mitochondrien findet die Oxidation des Substratwasserstoffs zu H2O statt b) Am Wasserstoff-bzw. Elektronentransport in der Atmungskette ist das FAD beteiligt c) Die innere Mito.-Membran ist für Malat durchlässig d) Der Glycerin-3-P-Shuttle gibt die Reduktionsäquivalente von NADH2 an den Komplex I e) Die Selbstregulation der Atmungskette (Atmungskontrolle) erfolgt durch den ATP/ADP-Quotienten d) Die Atmungskette Atmungskette Isoliert man ein Mitochondrium und stellt ihm die notwendigen Substrate zu Verfügung, so ist es durchaus imstande, über die Atmungskette Energie bereit zustellen um so ATP aus ADP zu bilden. Das Zauberwort: OXIDATIVE PHOSPHORYLIERUNG Der Elektronenfluß vom Substrat zum Sauerstoff unter ATP-Bildung. - Die Atmungskette läuft in der inneren Mitochondrienmembran ab. - Im Durchschnitt besitzt eine eukaryontische Zelle 2000 Mitochondrien. Atmungskette Die oxidative Phosphorylierung nutzt die Energie, die bei der Übertragung von Protonen und Elektronen zwischen den Redoxsystemen der Atmungskette entsteht. Atmungskette ENERGIE NADH2 FADH2 ATP Der Elektronenfluß vom Substrat zum Sauerstoff unter ATP-Bildung. Diese Energie treibt außerdem noch eine Protonenpumpe an, die dann Hs aus dem Matrixraum des Mitochondriums in den Zwischenraum der inneren und der äußeren Membran pumpt. Atmungskette Die Hs werden schrittweise übertragen (Oxidation = Elektronenabgabe) auf die einzelnen mitochondrialen Multienzymkomplexe der Atumungskette. Zuletzt werden sie auf Sauerstoff übertragen. Bei diesem gesamten Ablauf wird Energie frei. H2 + ½ 02 H2O Stark exergone Knallgasreaktion! “Ganz einfach: H geht zum O und gibt Energie ab…“ Atmungskette Energie kann weder erzeugt noch vernichtet werden. Sie kann lediglich von einer Form in die andere Überführt werden. Atmungskette H2 + ½ 02 H2O Dies ist eine stark exergone Knallgasreaktion, bei der Energie frei wird. 57 kcal/Mol. Damit das Mito bei dieser Reaktion net auseinanderfliecht, hat es sich 4 kleine Helfer zugelegt… Die Multienzymkomplexe I-IV, deren Aufgabe es ist, die freiwerdende Energie schrittweise abzugeben. Atmungskette Welche Aussage über die Atmungskette und oxidativer Phosphorylierung ist falsch? a) b) c) d) e) Eine oxidative Phosphorylierung ist nur an intakten Membranvesikel möglich. Bei der Oxidation von einem Molekül NADH wird ein Elektron auf ein Atmungskettenenzym übertragen. Mit dem Elektronenentransport in der Atmungskette ist die Entstehung eines Protonengradienten an der inneren Mito.Membran gekoppelt. Elektronen werden von Redoxpaaren mit negativem Potential auf Redoxpaare mit positiverem potential übertragen. Das Elek. Transportierende System besteht aus wasserunlöslichen Komplexen, aus Ubichinon und Cyt. C. Atmungskette Welche Aussage über die Atmungskette und oxidativer Phosphorylierung ist falsch? a) b) c) d) e) Eine oxidative Phosphorylierung ist nur an intakten Membranvesikel möglich. Bei der Oxidation von einem Molekül NADH wird ein Elektron auf ein Atmungskettenenzym übertragen. Mit dem Elektronenentransport in der Atmungskette ist die Entstehung eines Protonengradienten an der inneren Mito.Membran gekoppelt. Elektronen werden von Redoxpaaren mit negativem Potential auf Redoxpaare mit positiverem potential übertragen. Das Elek. Transportierende System besteht aus wasserunlöslichen Komplexen, aus Ubichinon und Cyt. C. b Atmungskette - Als erstes braucht die Atmungskette Hs, die geliefert werden von NAD bzw. FAD. - Komplex I oxidieren seinerseits diese Substrate Atmungskette NADH2 FMN 2H+2e- FMNH2+2eUbichinon - Ubihydrochinon NAD I Atmungskette - Als erstes braucht die Atmungskette Hs, die geliefert werden von NAD bzw. FAD. - Komplex I oxidieren seinerseits diese Substrate und überträgt die Hs weiter auf das Ubichinon. Atmungskette NADH2 FMN 2H+2e- FMNH2+2e- NAD I Ubichinon 2H Ubihydrochinon +2eCytochrom b+c III Atmungskette - Als erstes braucht die Atmungskette Hs, die geliefert werden von NAD bzw. FAD. - Komplex I oxidieren seinerseits diese Substrate und überträgt die Hs weiter auf das Ubichinon…Übertragung der Hs auf O2 - Komplex III reoxidiert das Ubihydrochinonab jetzt werden nur noch e- und keine Hs mehr übertragen - III überträgt seine e auf Cytochrom c Atmungskette NADH2 FMN 2H+2e- NAD FMNH2+2e- I Ubichinon 2H Ubihydrochinon +2eCytochrom b+c +2e- III Cytochrom C+2e- 2H Atmungskette - Als erstes braucht die Atmungskette Hs, die geliefert werden von NAD bzw. FAD. - Diese oxidieren ihrerseits Komplex I… Komplex I reduziert die Hs weiter auf das Ubichinon…Übertragung der Hs auf O2 - Komplex III reoxidiert das Ubihydrochinonab jetzt werden nur noch e und keine Hs übertragen - III überträgt seine e auf Cytochrom c, das durch IV oxidiert wird. Atmungskette NADH2 FMN 2H+2e- NAD FMNH2+2e- I Ubichinon 2H Ubihydrochinon +2eCytochrom b+c +2e- III ½O Cytochrom C+2eCytochrom a1+a3 +2e- 2- O IV 2H H2O Atmungskette Die Succinatdehydrogenase, die im Citratcyklus das Succinat zum Fumarat dehydrirert, ist zur gleichen Zeit Bestandteil des Komplex II. Die Hs, die auf dieser Höhe der Atmungskette eingeschleust werden, liefern nur 2ATP!! Das liegt daran, daß das FADH2 ein nicht so negatives Redoxpotential hat wie das NADH2 (und nicht weil es erst bei II anfängt!!!). Atmungskette Redoxpotential: …als Maß für die Oxidations-bzw. Reduktionskraft eines Redoxsystems. Es ist Proportional der freien Energie in einem System. Die Elektronen fließen vom Redoxsystem mit negativerem Potential zu dem mit positiveren Potential. Das Redoxsystem mit negativerem Potential wird oxidiert, das mit dem positiveren reduziert. Atmungskette NADH2 FMN 2H+2e- NAD FMNH2+2e- I Succinat H2 Ubichinon 2H Citratcyklus Succinat dehydrogenase FADH2 2H + 2e- Ubihydrochinon +2e- FAD Fumarat Cytochrom b+c +2e- III ½O Cytochrom C+2eCytochrom a1+a3 IV 2H +2e- 2- O H2O II Atmungskette Kommen wir nun zum Wesentlichen…der Energie ZUR ATP-SYNTHESE!!! Atmungskette NADH2 Oxidation 1 ATP NAD C-Raum I FADH2 2H+2e II Ubichinon 2H+2e 2H+2e Ubichhydrochinon 1 ATP Oxidation III FAD 2e Ubichinon Cytochrom 1 ATP äußere Mito.-Membran innere Mito.-Membran Oxidation Cytochrom IV Atmungskette 1 ATP – bei Oxidation von NAD(P)H2 durch Komplex I 1 ATP – bei Oxidation des Ubihydrochinon durch Komplex III 1 ATP – bei Oxidation des Cytochrom c durch Komplex IV 3 ATP Ausgehend von FADH2, sind es nur 2 ATP!!! (Redoxpotential!) Atmungskette Die oxidative Phosphorylierung nutzt die *Energie, die bei der Übertragung von Protonen und Elektronen zwischen den Redoxsystemen der Atmungskette entsteht. Atmungskette ENERGIE NADH2 FADH2 ATP Der Elektronenfluß vom Substrat zum Sauerstoff unter ATP-Bildung. Diese *Energie treibt außerdem noch eine Protonenpumpe an, die dann Hs aus dem Matrixraum des Mitochondriums, in den Zwischenraum der inneren und der äußeren Membran pumpt. Atmungskette Das heißt letzendlich, daß die Energie des Elektronentransport zusätzlich von einem Protonenfluß durch die innere Mito-Membran aus der Matrix, in den Intramembranraum begleitet wird. Atmungskette Warum wird diese Wasserstoffkonzentration überhaupt aufgebaut?? Wozu dieser elektrochemische Gradient?? Atmungskette Die Mengenmäßig wichtigere Möglichkeit ATP zu synthetisieren ist über die ATP-Synthase(!) (Komplex V). Als integraler Proteinkomplex der inneren Mito.-Membran, fließen die Hs aus dem C-Raum, wo die H-Konzentration ja hoch ist, durch den Komplex V (da ja die Mito-Membran nicht durchlässig ist für die Protonen). Atmungskette Die mengenmäßig wichtigere Möglichkeit ATP zu synthetisieren ist über die ATP-Synthase(!) (Komplex V). Als integraler Proteinkomplex der inneren Mito.-Membran, fließen die Hs aus dem C-Raum, wo die H-Konzentration ja hoch ist, durch den Komplex V. Diese Protein besteht aus 2 Untereinheiten. P0 und P1. P0 als der H-durchlässige Kanal. Erreichen die Hs nach der P0 die P1-Untereinheit, so kommt es zu einer Konformationsänderung innerhalb dieser. Dies ermöglicht letzendlich die ATP-Synthese=ENERGIE!!! Atmungskette Dieser elektrochemischer Konzentrationsgradient dient außerdem dem Antrieb des - P/H-Symport - ADP/ATP-Antiporter Atmungskette Die Konzentration an ADP limitiert die ATP-Synthese. Atmungskette Die Konzentration an ADP limitiert die ATP-Synthese. d.h. : ADP ATP-Synthese Das Selbe gilt für das NADH2! NADH2 ATP-Synthese Atmungskette Und wie wird die Atmumgskette gehemmt?? Atmungskette Es gibt hemmende Stoffe, die die Komplexe I-IV angreifen, und solche, die den Komplex V hemmen. Was bedeutet das für den Sauerstoff?? Atmungskette Abhängig vom Angriffsort wird der O2-Verbrauch an sich gehemmt oder die ATP-Bildung. Hemmung Komplexe I-IV Hemmung Komplex V O2-Verbrauch ATP-Bildung