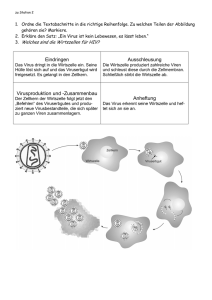
HIV
Werbung

HIV Dr. med. Stefan Esser Universitäts-Hautklinik Essen HIV-Übertragung • Die statistische Wahrscheinlichkeit einer HIV-Übertragung liegt für die unterschiedlichen Übertragungswege zwischen 1 Infektion pro 100 Kontakten und 1 Infektion pro 1000 Kontakten oder Expositionen. • Übertragungen sind möglich vor allem durch Blut, Sperma und Vaginalsekret, Liquor, Gewebe, Kulturmaterial. • Geschätztes Übertragungsrisiko nach Exposition mit HIV-infiziertem Blut: - Perkutane Stich- oder Schnittverletzung 0,3 % - Schleimhautkontakt 0,03 % • Grundsätzlich gilt, je länger die Verweildauer infektiöser Flüssigkeiten auf Wunden, geschädigter Haut oder auf Schleimhäuten und je höher die HIViruslast der Indexperson ist, desto höher wird die Wahrscheinlichkeit einer Übertragung. Universitätshautklinik Essen Akzidentelle HIV Exposition Vorgehen 1 • Fremdmaterial entfernen, Blutung anregen Dauer 1-2 Minuten • Hilfsperson zuziehen, Desinfektion mit alkoholischen Desinfektionsmitteln, bei Stichkanal spreizen. Dauer 2-4 Minuten. EFFEKTIVE DESINFEKTION SCHMERZT !!! • Bei Schleimhautkontakt mehrere Minuten spülen • Abschätzen der Infektionsgefahr: Patientenanamnese? Material? Menge? Verletzungsart? Universitätshautklinik Essen Akzidentelle HIV Exposition Vorgehen 2 • Einleiten einer medikamentösen Postexpositionsprophylaxe (PEP) innerhalb von 2 Stunden nach dem Unfall • HIV-Test beim Verunfallten am Tag des Ereignisses (Nachweis neg. Antikörper- Status) • Nachfolgend nach 1, 2, 3 und 6 Monaten Universitätshautklinik Essen Akzidentelle HIV Exposition Vorgehen 3 - PEP • PEP ist eine antiretrovirale Therapie die i.d.R. aus 3 Wirkstoffen besteht • Zusammensetzung der PEP richtet sich nach möglicher Therapie der Indexperson • Standard-PEP: 2 NRTI´s + PI/r oder INI für 4 Wochen • Schwangerschaft muß ausgeschlossen sein • Keine Daten über Langzeittoxizität vorhanden Universitätshautklinik Essen Maßnahmen zur Verhinderung einer HIVÜbertragung bei beruflicher Exposition • Kein wirksamer Impfstoff gegen HIV steht bisher zur Verfügung! • Eine HIV-Postexpositionsprophylaxe (PEP) nach Kontamination mit HIV-haltigen (Körper-) Flüssigkeiten mit einer antiretroviralen Kombinations-Therapie kann das Risiko einer Infektion senken (keine Erfolgsgarantie). • Die prophylaktische Behandlung sollte so schnell wie möglich (< 24 Std.) nach der Kontamination begonnen im Regelfall über 28 Tage durchgeführt werden. • In Zweifelsfällen kann notfallmäßig mit der PEP begonnen werden. Ein Abbruch der Prophylaxe, falls bei näherer Kenntnis des Unfallhergangs eine solche unnötig erscheint, ist zu jedem Zeitpunkt möglich. • Da die zur PEP eingesetzten Medikamente für diese Indikation nicht zugelassen sind, bedarf die Durchführung einer HIV-PEP der ausdrücklichen Zustimmung und ausführlichen Aufklärung des Betroffenen. Universitätshautklinik Essen Voraussetzungen für eine PEP • Voraussetzung für die ärztliche Empfehlung einer HIV-PEP ist grundsätzlich ein Kontakt mit relevantem Übertragungsrisiko zwischen einer HIV-negativen und einer HIV-infizierten Person (Indexperson). • Bei unbekanntem HIV-Serostatus, bzw. wenn die klinische Diagnose einer HIV-Infektion nicht wahrscheinlich ist, sollten die Empfehlungen zurückhaltend gehandhabt werden. • Nachteile einer HIV-PEP betreffen akute Nebenwirkungen der ART während der ersten Wochen der Einnahme (meist gastrointestinale Nebenwirkungen, Übelkeit), die jedoch in der Regel abklingen oder nach Beendigung der Therapie reversibel sind. • Zur Beurteilung des HIV-Expositionsrisikos und zur Abwägung des Nutzens und der Risiken einer HIV-PEP sollte ein in der HIV-Therapie erfahrener Arzt hinzugezogen werden. Dies kann auch nach einer vorläufigen, notfallmäßigen Einleitung einer HIV-PEP geschehen. Universitätshautklinik Essen Durchführung der PEP • Sofern bei der Indexperson die Behandlungsanamnese oder bestehende Medikamenten­Resistenzen bekannt sind, sollte die zur PEP verwendete Medikamentenkombination entsprechend angepasst werden. • Deshalb ist bei behandelten HIV-Patienten dringend Rücksprache mit dem betreuenden HIV-Schwerpunktzentrum zu empfehlen! • In allen anderen Fällen kann eine der in der nachfolgenden Tabelle aufgeführten Standard-Kombinationen verwendet werden: – Kombination PI/r oder INI mit zwei NRTI`s Universitätshautklinik Essen Nebenwirkungen der PEP • Antiretrovirale Therapie Kopfschmerzen, Übelkeit, Erbrechen, Abgeschlagenheit, Müdigkeit • Reverse Transkriptase Inhibitoren (NRTI) • Proteaseinhibitoren (PI) Glucoseintoleranz, Fettstoffwechselstörungen, Lipodystrophie Diarrhoe Lipodystrophiesyndrom Hepatische Steatose Lactatazidose Neutropenie, Anämie, Myopathie • Integraseinhibitoren (INI) Nierenfunktionsstörungen Hypophosphatämie Ein erheblicher Anteil bricht die PEP aufgrund von Nebenwirkungen ab! Universitätshautklinik Essen Was bedeutet HIV/AIDS? Universitätshautklinik Essen Die Prä-HAART-Ära Anfang der 80-ziger Entdeckung des HI-Virus als Ursache für eine Immunschwäche die zu AIDS-definierenden Erkrankungen und letztlich zum Tode führt Vor 1996 lag die durchschnittliche Lebenserwartung nach der Diagnose AIDS-Vollbild bei zwei Jahren (Prä-HAART-Ära) l HIV/AIDS führt regional in bestimmten Altersgruppen zu einer erheblichen Mortalität und Morbidität: *von 1982-1996 ca. 20000 AIDS-Patienten *von denen bis Ende 1996 etwa 75 % verstorben sind Universitätshautklinik Essen Virale Replikation HIV 1 und 2 = RNS-Viren = Retroviren HIV gp41 gp120 virale RNA Reverse Transkriptase provirale DNA Protease Integrase virale Proteine Nukleus CD4-T-Lymphozyt zelluläre DNA mRNA Universitätshautklinik Essen Klinischer Verlauf der HIV-Infektion: Surrogatmarker: CD4, HIViruslast Akutes HIV-Syndrom: Dissemination des Virus, Lymphknotenbefall 1100 1000 210.000 190.000 Opportunistische Erkrankungen 900 CD4 230.000 Tod Primär Infektion 1200 170.000 800 150.000 700 130.000 600 110.000 500 90.000 VL Klinische Latenz 400 70.000 300 50.000 200 30.000 100 10.000 0 0 0 3 6 9 Wochen 12 1 2 3 4 5 Jahre 6 7 8 9 10 11 Universitätshautklinik Essen Die CDC – Klassifikation AIDS ist eine klinische Diagnose! Labor CD4-Zellzahl Klinische Kategorien AIDS ≥ 500 /µl A1 B1 C1 200-499 /µl A2 B2 C2 < 200 /µl A3 B3 C3 Erwachsene und Kinder: HIV-Neuinfektionen 2008 North America and Western/Central Europe 81,000 Total: 2.0 million Caribbean 20,000 Total: 230,000 Latin America 140,000 Total: 1.7 million Eastern Europe and Central Asia 110,000 Total: 1.5 million North Africa and Middle East 40,000 Total: 380,000 Sub-Saharan Africa 1.9 million Total: 22 million UNAIDS, 2008. Available at: http://www.unaids.org. Asia 380,000 Total: 4.2 million Oceania 13,000 Total: 74,000 HIV-Infektion und AIDS Epidemiologie 2012: Deutschland • 78 000 HIV-Infizierte (davon etwa 200 Kinder) • 3400 Neuinfektionen 2012 • 1100 neue AIDS-Erkrankungen 2012 • 550 HIV/ AIDS Todesfälle 2012 • Seit Beginn der Epidemie starben 27 000 Menschen an den Folge von AIDS. • Geschätzte nicht diagnostizierte HIV-Infektionen 14 000 • Antiretroviral behandelte HIV-Infizierte 50 000 Epidemiologisches Bulletin Nr. 47 RKI 2008 Audit von 397 Todesfällen in UK 2005: Szenarien die zu AIDS-assoziierter Mortalität führen Szenario % der AIDS-Todesfälle Zu spät für eine effektive Therapie diagnostiziert 40 Unter medizinischer Betreuung, aber unbehandelbare Komplikationen 29 Ineffektive Behandlung wegen mangelhafter 12 Therapietreue Behandlung verweigert 8 Bekannter HIV-Infekt, dennoch ohne 6 medizinische Betreuung: Anbindung zu spät Multiresistentes HIV ohne antiretrovirale Salvageoptionen 5 A. Phillips 15th CROI 2008 Boston USA #8; BHIVA Audit-Johnson et al. 2005 Universitätshautklinik Essen Hautveränderungen als Marker des HIV-bedingten Immundefektes Klinische CDC WHO Klassifikation A Mononukleose-artiges Exanthem B Psoriasisexazerbation Papulöse Dermatitis / Follikulitiden Xerosis cutis Seborrhoisches Dermatitis Condylomata acuminata Scabies Herpes rezidivans Universitätshautklinik Essen C Oropharyngeale Candidose Vulvovaginale Candidose Rezidivierender Zoster Haarleukoplakie Bazilläre Anggiomatose chronische Herpes- simplex-Ulcera Candida-Paronychie Nekrotisierende Pyodermien Mollusca contagiosa Kaposi-Sarkome Zytomegalievirus-Ulcera Soorösophagitis Stadien-definierende Hautmanifestationen bei HIV und AIDS Kategorie A • Akute, symptomatische (primäre) HIVInfektion (auch in der Anamnese): HIV-Exanthem Universitätshautklinik Essen Stadien-definierende Hautmanifestationen bei HIV und AIDS Kategorie B: • Oropharyngeale Candida-Infektionen • Vulvovaginale CandidaInfektionen • Herpes zoster bei Befall mehrerer Dermatome oder nach Rezidiven in einem Dermatom • Orale Haarleukoplakie • Zervikale Dysplasien oder Carcinoma in situ • Idiopathische thrombozytopenische Purpura • Bazilläre Angiomatose Universitätshautklinik Essen Stadien-definierende Hautmanifestationen bei HIV und AIDS Kategorie C • Ösophageale CandidaInfektion oder Befall von Bronchien, Trachea oder Lungen oder Sepsis • Chronische Herpes simplex-Ulzera (> 1 Mo.) o. Herpes-Bronchitis, Pneumonie oder – Ösophagitis • CMV-Infektion der Haut sowie der Schleimhäute • Tuberkulose • Atypische Mykobakteriose Infektionen mit Mykobakterium avium complex oder M.kansasii, disseminiert oder extrapulmonal • Extrapulmonale kutane Kryptokokkeninfektionen Universitätshautklinik Essen Kategorie C, AIDS-definierende Neoplasien • Kaposi-Sarkom (HHV-8) • Non-Hodgin Lymphome (EBV, HHV-6, HHV-8) (Burkitt’s, immunoblastisches oder primäres zerebrales Lymphom) • Invasives Zervix-Karzinom (HPV) Universitätshautklinik Essen HPV, Analkarzinom und HIV • Studie an homosexuellen Männern in San Francisco (1992): – Abstrichuntersuchung auf eine anale HPV-Infektion mittels PCR • Nachweis bei 93% der HIV-positiven Patienten und • Nachweis bei 63% der HIV-negativen Probanten • Die Inzidenz der AIN bei homosexuellen Männern ist mit einer Rate von 35/100.000 im Vergleich zur Normalbevölkerung deutlich erhöht. • Inzidenz (Relative Rate adjustiert: RRadj) gegenüber Normalbevölkerung (SEER) bei HIV (HOPS) signifikant erhöht (CI 95%): – – – – • Anorektal 10,13; Hodgin Lymphom 4,58; Melanom 2,99; Lunge 2,13 Multivarianz-Analyse (HIV-P. Chicago/Krebs-Register): Signifikant höhere Inzidenz (RRadj) bei HIV: – – – – – Hodgin Lymphom 77,43; HNO 9,96; Anorektal 5,03; Melanom 4,10; Lunge 3,63 11th CROI 2004 #81 P. Patel et al. Universitätshautklinik Essen Entwicklung der antiretroviralen Therapie = ART 1987: Zidovudin (Retrovir TM, AZT) wird als erstes antiretroviral wirksames Medikament gegen HIV eingesetzt. Seither Entwicklung neuer Wirkstoffe und Substanzklassen: Reverse Transkriptase Inhibitoren (RTI): Nukleosidale RTI (NsRTI): Nicht NRTI (NNRTI): Nukleotidische RTI (NtRTI) Protease Inhibitoren (PI): Fusionsinhibitoren (FI): CCR5-Chemokinrezeptorantagonisten Integrase Inhibitoren 1987 1998 2002 1996 2002 2008 2008 Universitätshautklinik Essen Entwicklung der antiretroviralen Therapie = ART Überlegenheit der (Dreifach-) Kombinationstherapie = High active ART = HAART (1996: Divergente Regime: 2 NRTI`s + PI) Dramatische Verbesserungen der Mortalität und Morbidität, die seit 1996 jeweils um 75 % gesenkt wurden. Therapieindikation 1996: Hit hard and early Universitätshautklinik Essen EuroSIDA November 2000 Deaths AIDS Patients on HAART (%) Calendar period Patients on HAART (%) Incidence (per 100 pt-years) Klinische Effektivität der HAART Incidence von AIDS und Death (1994–2000) Universitätshautklinik Essen Geschätzte HIV/AIDS Inzidenz, Prävalenz und Todesfälle in Deutschland (Modell) 8000 50000 7000 45000 40000 6000 HIV prevalence (r) AIDS prevalence (r) HIV incidence (l) AIDS incidence (l) HIV/AIDS deaths (l) 5000 4000 3000 35000 30000 25000 20000 15000 2000 10000 1000 5000 0 0 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 99 00 01 Jahr Entwicklung unter ART gegen HIV Langlebige, chronisch HIV-infizierte Zelllinien verhindern die HIV-Eradikation unter ART. Absetzen der ART führt erneut zu explosionsartiger Vermehrung von HIV Lebenslange Therapie erforderlich Neben den akuten Nebenwirkungen treten z.T. schwere LangzeitNebenwirkungen unter der Dauer-Kombinationstherapie auf: - Liopodystrophiesyndrom - Metabolisches Syndrom - Periphere Insulinresistenz - Mitochondriale Toxizität Universitätshautklinik Essen HIV-Therapie heißt lebenslänglich Patienten werden älter Therapiedauer wird länger mehr andere Erkrankungen Langzeit NW werden sichtbar HIV-Arsenal muss länger halten mehr andere Medikamente Interaktionen Langzeit NW Resistenz Universitätshautklinik Essen % der Patienten mit vollständiger Suppression HAART “verzeiht” Einnahmefehler nur selten p<0,0001 Adherence / Compliance in % p < 0,00001 Universitätshautklinik Essen DL Paterson et al. 6th CROI, Chicago (1999) DL Paterson et al. Ann Intern Med 133, (2000), 21-30 Sterberaten bei Patienten mit sofortigem vs. verzögertem Therapiebeginn in Abhängigkeit von der CD4-Zellzahl 60 56,4 50 40 30 unverzüglicher Therapiebeginn verzögerter Therapiebeginn 20 10 16,5 15,4 10,7 0 6,7 5,6 Gruppe 1 Gruppe 2 Gruppe 3 201 – 350 CD4-Zellen/µl 351 – 500 CD4-Zellen/µl 501 – 750 CD4-Zellen/µl Palella et al., Ann Int Med 2003; 158,8:620-27 Universitätshautklinik Essen Therapieempfehlungen 2011 für die Einleitung der antiretroviralen Therapie (ART) AIDS Symptomatische HIV-Infektion Ja Nein CD4-Zellzahl/µl = Behandlung empfehlen <350 350-500* *Zusatzkriterien = abwarten und regelmäßige Kontrolle der Laborwerte Leitlinien DAIG 2011 -HBV, HCV, -Verlauf, -Alter > 50, -Kardiovaskuläres Risiko -Reduktion Infektiösität -Schwangerschaft >500* ? HIV-RNA (Kopien/ml) >100.000 Ziele der antiretroviralen HIV-Therapie Unmittelbares Therapieziel: Viruslast unter der Nachweisgrenze Langfristiges Therapieziel: Stabilisierung des Immunsystems, Verbesserung der Lebenserwartung Verbesserung der Lebensqualität l Zukunft: HIV – eine chronische Erkrankung, die obwohl sie unheilbar ist, unter konsequenter Therapie nicht mehr zum Tode führt? Universitätshautklinik Essen Virale Replikation und HAART Vor 2007 zugelassene Substanzklassen HIV gp41 gp120 virale RNA EntryInhibitoren: -Fusionsinhibitoren (FI) -CCR5Chemokinrezeptor-Antagonisten Reverse Transkriptase/ Ribonuklease H provirale DNA Protease Integrase virale Proteine Nukleus Reverse CD4-T-Lymphozyt Transkriptase Inhibitoren (RTI): zelluläre -nukleosidale (NRTI) DNA mRNA -Nicht nukleosidale (NNRTI) Protease Inhibitoren (PI) Universitätshautklinik Essen Deutsch-Österreichische Leitlinien 2011 zur antiretroviralen Therapie von Erwachsenen: Regimewahl Efavirenz** NNRTI Nevirapin*** „Backbone“ Atazanavir/r Tenofovir + Emtricitabin Abacavir + Lamivudin* Tenofovir + Lamivudin Darunavir/r + Lopinavir/r PI/r Fosamprenavir/r Saquinavir/r Raltegravir empfohlen *nur für HLA-B*5701-Negative; Cave: evtl. erhöhtes kardiovaskuläres Risiko, virologisch leicht unterlegen S. Esser Universitätshautklinik Essen INI Alternative **nicht bei Schwangerschaft und Frauen mit Kinderwunsch ***Cave: Hepatotoxizität erhöht bei Frauen mit CD4+-Zellen >400/Männern mit >250/µL Kriterien für die Auswahl der Substanzen für eines Regimes • Anamnese, Vortherapien • Bekannte Resistenzen aus vorherigen Resistenztests • Interaktionen • Nebenwirkungen • Begleiterkrankungen Universitätshautklinik Essen Immunrekonstitutionssyndrom (IRS) • Definition: Atypische inflammatorische Erkrankungen verbunden mit der Immunrekonstitution nach Einleitung einer effektiven antiretroviralen Therapie (ART) IRS: Pathogenese • Rapide Inhibition der HIV-Replikation durch die ART • Anstieg der zirkulierenden CD4 Zellen • Qualitative und quantitative Erholung der pathogenspezif. Immunantworten – Rekonstitution der spezifischen zellulären Immunantworten gegenüber Mitogenen und Pathogenen und der humoralen Immunität meistens innerhalb der ersten 3 Monate nach ART-Einleitung – Veränderungen im Zytokinnetzwerk #J R Deayton et al. AIDS 2002, 16:2129-2135 #M A French et al. AIDS 2004, 18:1615-27 IRS: Risikofaktoren • Immundysregulation: – CD4 T-Zellen < 200/µl – z. B: Imbalance zwischen Effektor (Th1, Th 17) und regulatorischen (IL-10+) T-ZellAntworten • Hohe initiale HIViruslast vor ARTEinleitung • Infektions- oder Autoimmunerkrankungen • Latente, maskierte, subklinische Infektionsoder Autoimmunerkrankungen • Disseminierte Infektion mit hoher Pathogenbeladung • Kurze Zeit antherapierte Infektionen Entwicklung der HAART gegen HIV Therapieversagen in HIV-ART-Studien: 20 % der Therapieabbrüche, infolge virologischem Versagen 80 % der Therapieabbrüche durch Unverträglichkeiten, Toxizitäten komplizierte Einnahmevorschriften und Complianceprobleme Wechselwirkungen zwischen verschiedenen Medikamenten: Nutzung günstiger Interaktionen z. B. Wirkverstärkung von Proteaseinhibitoren durch die Boosterung mit Ritonavir (RTV, /r)! Nebenwirkungen: Entwicklung weniger toxischer Substanzen; späterer Therapiebeginn Z. T. Komplizierte Einnahmebedingungen (mehrmals täglich, nüchtern) von zahlreichen verschiedenen Tabletten mit schlechter Verträglichkeit führen zu Complianceproblemen: ART wird einfacher und verträglicher! Resistenzen gegen antiretrovirale Substanzen werden zunehmend beobachtet, selbst bei therapienaiven Patienten, und führen zum Therapieversagen: Neue Substanzen ohne Kreuzresistenzen mit neuen Wirkmechismen! Was ist Boosterung? • Ritonavir (RTV) ist ein potenter Inhibitor des Isoenzyms 3A4, einer Untereinheit des Cytochrom P450Enzymsystems in der Leber und im GI-Trakt. • Die Spiegel fast aller Proteaseinhibitoren werden durch die gleichzeitige Gabe von geringen (100-400 mg/Tag), nicht antiretroviral wirksamen (Baby-)Dosen Ritonavir (rtv) deutlich gesteigert. • Diese rtv-Boosterung ermöglicht eine Pillenreduktion, reduziert die Häufigkeit der Einnahme und macht die Resorption teilweise unabhängig von der Nahrungsaufnahme . Universitätshautklinik Essen Antiretrovirale Therapie (ART) wirkt! • Patienten unter ART mit erfolgreicher HIViruskontrolle erreichen eine relativ normale Lebenserwartung. • Ein 20-jähriger, der eine HAART beginnt, erreicht eine durchschnittl. Lebenserwartung von weiteren 43 Jahren; ein 35jähriger 32 weitere Jahre. • Mortalitätsraten werden nach 6 Jahren Follow-up vergleichbar mit der Normalbevölkerung bei Patienten, die 500 CD4Zellen/mm3 und mehr erreichen. ATTC Lancet 2008; 372:293-299 Lewden C, et al. JAIDS. 2007;46:72-77. Universitätshautklinik Essen Versagen der antiretroviralen Therapie Universitätshautklinik Essen Was bedeutet Therapieversagen und Resistenzentwicklung? • Therapieversagen: – Viraler “Rebound” durch Verlust der Viruskontrolle • Resistenz: – Verlust der Empfindlichkeit gegenüber der antiviralen Aktivität eines Wirkstoffes in Abhängigkeit vom Medikamentenspiegel • Durch Kreuzresistenzen Wirkverlust ganzer Substanzklassen und bei suboptimalem Einsatz verschiedener Substanzklassen Multiresistenz gegen mehrere Substanzklassen Antivirale Aktivität Selektionsdruck Auftreten von Resistenzen Therapieversagen Vermehrung Mutationsrate Verlust der Kontrolle über HIV Virale Fitness, Replikative Kapazität • Replikative Kapazität (RC) – Möglichkeit der Vermehrung unter idealen Bedingungen • Fitness – Möglichkeit der Vermehrung unter definierten Bedingungen • M-Typ und RC – „bezahlt“ Selektionsvorteil durch die Entwicklung von Resistenzen unter einer ART häufig mit einem Verlust an replikativer Kapazität gegenüber dem HIV-Wildtyp. – Primärmutationen verändern die Bindungsfähigkeit einer Substanz an sein Zielenzym, so daß immer höhere Konzentrationen notwendig wären, um die Enzymwirkung weiterhin zu hemmen. – Sekundärmutationen erhöhen die Fitness (Replikative Kapazität) eines Virusstammes, der bereits Primärmutationen hat. Universitätshautklinik Essen Konsequenzen von Resistenzen • Jede Resistenz wird im Erbgut archviert und ist damit irreversibel vorhanden, so dass sie bei entsprechendem Selektionsdruck lebenslang abgerufen werden kann. • Reduktion zukünftiger Therapieoptionen • HIV-Patienten mit vielen Resistenzen erkranken häufiger und sterben früher, • Übertragung resistenter HIV und Superinfektionen • Jede neue Resistenzmutation gefährdet sowohl den Einzelnen als auch die Gesamtpopulation der HIV-Patienten. Johnson et al. XV int. HIV Drug Resistance Workshop, 2006, #69 Palmer et al. PNAS 103 (no. 18) 2006, 7094-7099 Zweite HAART-Welle 2008: Zugelassene Antiretrovirale Medikamente in der EU/US Zwischen ’87 und ’95 wurden 4 Antiretrovirale Medikamente zugelassen. Seit ’95 wurden 27 neue Produkte eingeführt. emea.europa.eu website (EU Zulassung) Celsentri Kivexa Combivir Hivid Retrovir Videx Epivir Rescriptor* Isentress Viread Truvada Ziagen Emtriva Viramune Atripla* Sustiva Trizivir Zerit ’87 ’88 ’89 ’90 ’91 ’92 ’93 ’94 ’95 ’96 ’97 ’98 ’99 ‘00 ’01 ‘02 ‘03 ‘04 ‘05 ‘06 ‘07 ‘08 NRTI NNRTI PI FI CCR5I INI Invirase Viracept? Kaletra Prezista Reyataz Fortovase Agenerase Fuzeon Telzir Norvir Crixivan Kaletra Tablette Invirase500 Aptivus Virologisches Therapieversagen: Konsequenzen: • Wenn 2 oder mehr neue und aktive Substanzen/Klassen verfügbar sind: – Wahl des maximal aktiven Regimes – Fortführung von Substanzen gegen die keine Resistenzen vorliegen mögl. • Ziel: – Maximale und dauerhafte Suppression der HIVirusreplikation möglichst unter die Nachweisgrenze Universitätshautklinik Essen Die zweite HAART-Welle: Neue Klassen HIV gp41 gp120 provirale DNA virale RNA Reverse Transkriptase/ Ribonuklease H EntryInhibitoren: -Attachment -CCR5: *Maraviroc *Vicriviroc Maturations (Reifungs) Inhibitoren Integrase Inhibitoren: *Raltegravir *Elvitegravir Integrase Protease -CXCR4 -Fusionsi. virale Proteine Nukleus Reverse Transkriptase Inhibitoren: CD4-T-Lymphozyt -NRTI -NNRTI: Etravirine zelluläre DNA mRNA Protease Inhibitoren: -Darunavir -Tipranavir Universitätshautklinik Essen Eintrittsinhibitoren CD4Bindung CD4-BindungsInhibitoren KorezeptorBindung Verankerung der Fusionspeptide CCR5 VerankerungsAntagonisten Inhibitoren # F. Kirchhoff et al, 15th CROI 2008, Boston USA, Plenary Session 19 Virus-ZellFusion FusionsInhibitoren Was ist eine ‘optimized background therapy (OBT)’? Eine ART-Kombination ausgewählt nach der maximal zu erwartenden antiretroviralen Aktivität unter den möglichen Optionen in Verbindung mit mindestens einer weiteren neuen Substanz/Klasse. Available options Drug A Drug B Drug C Optimized background New agents SELECTED FOR MAXIMUM ACTIVITY Drug A Drug C Drug D Was ist eine aktive Substanz? Drug E Drug F ? Zusammenfassung • Klinische Zeichen der HIV-Infektion werden häufig nicht oder zu spät erkannt: – Hauptursache für AIDS und HIV-assoziierte Todesfälle in westlichen Industrieländern • Ein umfangreiches diagnostisches Instrumentarium steht bei HIV zur Verfügung: – Surrogatmarker (CD4-Lymphozyten, HIViruslast) – Geno-/phänotypische Resistenzbestimmung – Medikamentenspiegelmessung • Ein umfangreiches therapeutisches Arsenal steht für die Behandlung der HIVInfektion zur Verfügung: NRTI, NNRTI, PI, FI, CCR5 I, INI • ART sollte die HIVirusreplikation maximal (unter die Nachweisgrenze) suppremieren. • Patienten unter ART mit erfolgreicher HIViruskontrolle erreichen eine relativ normale Lebenserwartung. • Je besser die Substanzen werden, desto mehr kommt es auf die Erfahrung des Arztes und die Compliance des Patienten an. Universitätshautklinik Essen