1.Klasse_3.1-3.4_Einige_Stoffe_der_Natur
Werbung

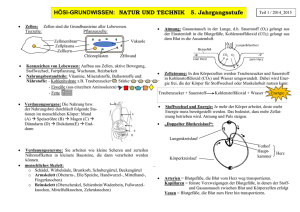
3 Einige Stoffe der Natur Themenbereich: Stoffe und Stoffumwandlungen Vier Sphären Unser Planet kann grob in vier Sphären eingeteilt werden: - Feuer (Energie) - Luft (Atmosphäre) - Wasser (Hydrosphäre) - Erde (Lithosphäre) Übersicht: • 3.1 Feuer (Energie) • 3.2 Luft (Atmosphäre) • 3.3 Wasser (Hydrosphäre) • 3.4 Erde (Lithosphäre) 3.1 Feuer (Energie) Stoffe wandeln sich in der Natur um. Jede Reaktion ist mit einem Energieumsatz verbunden. Der Energieumsatz erfolgt in Form von Wärme, Licht, Strom, Bewegung oder Schall. Energieumsatz in der Natur Waldbrand Blitze/Strom Donner Energieumsatz in der Natur Sonnenlicht Vulkanausbruch 3.2 Luft Luft ist ein Gasgemisch und besteht hauptsächlich aus folgenden Bestandteilen: - 78 % 21 % 1% 0.04 % Stickstoff Sauerstoff Argon Kohlenstoffdioxid Zusammensetzung Luft Photosynthese Der Sauerstoff in unserer Atmosphäre stammt aus einem chemischen Prozess, der Photosynthese. Photosynthese: Pflanzen sind in der Lage mit Hilfe von Sonnenlicht folgende Reaktion durchzuführen: Zellatmung Der Mensch und alle Tiere brauchen Sauerstoff zum Leben. Der Grund dafür ist, dass im Körper damit eine chemische Reaktion durchgeführt wird: die Zellatmung. Die Zellatmung ist die umgekehrte Reaktion der Photosynthese. Bei der Zellatmung wird Wärme frei. Sie ist der Grund für unsere Körpertemperatur von 37 °C. Nachweis von Kohlenstoffdioxid Wird in eine gesättigte Caliumhydroxid-Lösung hineingeblasen, wird die zuvor durchsichtige Lösung trübe: Durch eine Reaktion mit Kohlenstoffdioxid entsteht Kalk. Kohlenstoffdioxid und Treibhauseffekt Kohlenstoffdioxid ist ein so genanntes Treibhausgas. Treibhausgase absorbieren die Wärmeenergie der Erde und sind verantwortlich für das Klima auf unserer Erde. Grosse Mengen Treibhausgase in der Luft erwärmen die Erde stark: Es kommt zur Erderwärmung. Kohlenstoffdioxid und Treibhauseffekt Woher kommt das Kohlenstoffdioxid? • 1) Kohlenstoffdioxid (g) ist ein Produkt bei der Zellatmung. • 2) Kohlenstoffdioxid (g) entsteht bei der Verbrennung Kohlenstoffhaltiger Verbindungen. Kohlenstoffhaltige Verbindungen: - Öl, Benzin, Plastik, Kohle, Holz, Erdgas Sauerstoff Entsteht als „Abfallprodukt“ der Photosynthese, ist aber für das Leben auf der Erde (Zellatmung) essentiell. Ohne Sauerstoff kann der Mensch nicht überleben. Auch Fische atmen Sauerstoff ein. Sie benutzen dazu Kiemen mit denen sie Wasser aufsaugen und den darin gelösten Sauerstoff verwerten. Sauerstoff und Verbrennungen Definition: Eine Reaktion mit Sauerstoff nennt man eine Verbrennung. Produkte von Verbrennungen nennt man Oxide. Metalloxide sind salzartige Stoffe (fest). Nichtmetalloxide sind flüchtige Stoffe (oft gasförmig). Experiment: Verbrennung Eine Kerze wird angezündet. Man stülpt ein Glasbecher darüber. Was passiert? Ergebnis Die Kerze wird ausgelöscht. Grund: Der ganze Sauerstoff unter dem Glasbecher ist bei der Verbrennung verbraucht worden. Sobald kein Sauerstoff mehr vorhanden ist, löscht die Kerze aus. Stickstoff Stickstoff ist nicht in der Lage eine Verbrennung zu unterhalten: Reiner Stickstoff löscht eine Flamme. Übung Gib die Reaktionsgleichung und das Teilchenmodell für: – die Verbrennung von Kohle an – die Verbrennung von Eisen an – die Analyse von Zinkoxid an. 3.3 Wasser (Hydrosphäre) Geht bitte das Arbeitsblatt durch. 3.4 Erde (Lithosphäre) Geht bitte das Arbeitsblatt durch Quellen Seite 5: www.naturpark-suedheide.12see.de http://www.allmystery.de/themen/uh85958-17 Seite 6: http://www.regioonline.ch/magazin/zitate---humor/zitate/zitate-freude.php http://www.vulkane.net/vulkanismus/vulkanausbruch-eruption-vulkanasche.html Seite 8: http://www.uni-duesseldorf.de/MathNat/Biologie/Didaktik/Atmung/start/ voraus/voraus2.html Seite 13: http://www.bs-wiki.de/mediawiki/index.php?title=Treibhauseffekt Seite 15 http://www.kinder-hd-uni.de/luft/luft17.html