Posaconazol – ein neues Azolantimykotikum Einleitung
Werbung

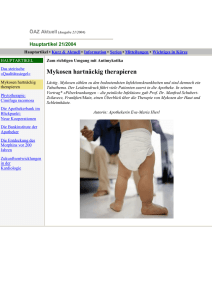
1. Jahrgang, Mai 2007, 32-38 - - - Rubrik Neue Arzneimittel - - Posaconazol – ein neues Azolantimykotikum Bedeutung für die Behandlung von invasiven Mykosen Einleitung Klinische Wirksamkeit Wirkungsmechanismus Sicherheit In-vitro und in-vivo Studien Verträglichkeit Pharmakokinetik Fazit Posaconazol – ein neues Azol-Antimykotikum - 33 - Posaconazol (Noxafil®) Ein neues Azol-Antimykotikum Marc Oppermann Apotheker Institut für Pharmakologie und klinische Pharmakologie Universitätsklinikum, Heinrich-Heine-Universität Moorenstr. 5, 40225 Düsseldorf [email protected] Den Fortbildungsfragebogen zur Erlangung eines Fortbildungspunktes zum Fortbildungstelegramm Pharmazie finden Sie hier*: http://www.uni-duesseldorf.de/kojda-pharmalehrbuch/Fortbildungstelegramm%20Pharmazie/index.html Es handelt sich um einen Rubrik-Fortbildungsfragebogen, d.h. dass dieser Fragenbogen Fragen zu mehreren Beiträgen im FORTE-PHARM enthält Titelbild : Universitätsbibliothek New York , Urheber : Photoprof , Lizenz : Fotolia Fortbildungstelegramm Pharmazie 2007;1:32-38 Posaconazol – ein neues Azol-Antimykotikum Abstract Posaconazole, a new azole antifungal drug, was approved for the treatment of refractory invasive fungal infections in October, 2005 in Germany. It is available as a suspension under the name Noxafil®. The suspension it is orally applied twice or four times daily, with a dose of 800 mg / day. Similar to all azole antifungal drugs, it inhibits the synthesis of ergosterole, a steroid essential for cell membrane function in fungi, resulting in a fungistatic effect. Invitro experiments show a broadspectrum antifungal activity against Candida species, Aspergillus species, Fusarium species, zygomycetes and species resistant against other antifungal drugs, including azoles. Posaconazole has shown a promising clinical efficacy against life-threatening invasive fungal infections refractory to current therapy. Frequent (1-10%) adverse events are gastrointestinal, dermal and neurological symptoms and are quite similar to other conazoles, but posaconazol is less toxic that amphotericin B which is still viewed as the drug of choice in systemic mycosis. Interactions may occur due to the fact that posaconazole inhibits CYP3A4 enzyme. Abstrakt Posaconazol, ein neues Antimykotikum aus der Gruppe der Azole, ist zur Behandlung von invasiven Mykosen als Reservetherapie zugelassen und seit Oktober 2005 als Suspension zum Einnehmen unter dem Namen Noxafil® im Handel. Wie alle Azolantimykotika bewirkt es eine Hemmung der Ergosterolsynthese und besitzt dadurch eine fungistatische Wirkung. In-vitroExperimente zeigten ein breites Wirkspektrum von Posaconazol gegenüber Candida-, Aspergillus- und Fusarium-Spezies sowie Zygomyceten, auch gegenüber Spezies, die gegen andere (Azol-)Antimykotika resistent gewesen sind. Der Wirkstoff wird zu 800 mg täglich, aufgeteilt in zwei oder vier Dosen, verabreicht. Erste klinische Studien weisen auf eine vielversprechende Wirksamkeit von Posaconazol in der Therapie von lebensbedrohlichen systemischen - 34 - Mykosen hin. Häufig (1-10%) auftretende Nebenwirkungen sind gastrointestinale, dermale und neurologische Symptome. Sie sind vergleichbar denen der anderen Azole, jedoch ist Posaconazol weniger toxisch als Amphotericin B, welches immer noch als Mittel der Wahl bei systemischer Mykose gilt. Da Posaconazol ein CYP3A4Hemmer ist, können Wechselwirkungen mit anderen Arzneistoffen auftreten. Einleitung Die in den letzten Jahren steigende Anzahl von immunsupprimierten Patienten, z.B. durch HIV-Infektion, Zytostatikatherapie und iatrogene Immunsuppression (Transplantationen, Rheuma, Arthrose, Asthma, Morbus Crohn etc.), führt dazu, dass die Häufigkeit systemischer Mykosen zunimmt. Auch eine Antibiotikatherapie kann Mykosen verursachen, denn die bakterizide/bakteriostatische Wirkung begünstigt wegen der Schädigung konkurrierender bakterieller Keime das Wachstum vieler potentiell humanpathogener Pilzarten. Neben den bekannten Candida- und AspergillusInfektionen werden auch vermehrt Infektionen mit eher ungewöhnlichen Erregern, z.B. Fusariose und Zygomykose, beobachtet (1). Systemische Mykosen sind stets schwerwiegende Erkrankungen und eine nicht zu unterschätzende Gefahr für die meist ohnehin durch ihre Grunderkrankung stark beeinträchtigten Patienten, die zu hohem Fieber und Funktionsbeeinträchtigung von Organen wie Lunge und Niere führen und letal enden können (2). Die Diagnose einer systemischen Mykose erfordert eine Kultur aus einer sterilen Gewebeprobe oder eine entsprechend charakteristische Histopathologie. Jedoch zeigen beide Methoden eine nur limitierte Sensitivität, so dass der behandelnde Arzt sich oft am klinischen Bild und den vorliegenden Risikofaktoren (z.B. Verweildauer auf einer Intensivstation) orientieren und eine empirische therapeutische Entscheidung treffen muss (3). Bislang sind vier Antimykotika-Gruppen zur Therapie systemischer Mykosen zugelassen: Amphotericin B, die Azole (Ketoconazol, Itraconazol, Fluconazol Fortbildungstelegramm Pharmazie 2007;1:32-38 Posaconazol – ein neues Azol-Antimykotikum Ravuconazol und Voriconazol, siehe auch Abb. 1), Flucytosin und das Echinocandin Caspofungin. Die Verwendung dieser Stoffe ist jedoch aufgrund starker Neben- und Wechselwirkungen sowie Resistenzen limitert (4). Posaconazol (Abb. 1A) wurde im Oktober 2005 als weiteres systemisch verfügbares AzolAntimykotikum zugelassen. Wirkmechanismus Der Wirkmechanismus von Posaconazol unterscheidet sich nicht von dem der anderen Azole. Das Enzym Lanosterol14α-Demethylase (CYP51A) wird gehemmt, indem der Azolring (s. farbliche Hervorhebung in Abb. 1) des Moleküls mit dem Eisenatom des HämRinges interagiert (5). Dieses Enzym katalysiert die Abspaltung einer Methylgruppe des Lanosterols, einer Vorstufe des für die Zellmembran essenziellen Ergosterols. Durch die Hemmung kommt es zu einem Ergosterolmangel (6) (Abb. 2), infolgedessen zu Schäden der Zellmembran und zur Lyse der Zelle. - 35 - Daraus resultiert eine fungistatische Wirkung; in in-vitro-Experimenten wurde für einige Pilzspezies auch eine fungizide Wirkung von Posaconazol beobachtet (1). Die lange lipophile Seitenkette führt zu einer stärkeren Bindung von Posaconazol zu CYP51A im Vergleich zu Fluconazol und Voriconazol, welche diesen Substituenten nicht tragen, indem ein zusätzlicher Hohlraum in der Nähe der Bindungsstelle ausgefüllt wird. Posaconazol wird dadurch weniger empfindlich für Mutationen des Enzyms im Bereich der Häm-Gruppe. Itraconazol kann mit einer ähnlichen Seitenkette den Hohlraum ebenfalls ausfüllen, ist jedoch aufgrund anderer sterischer Bedingungen anfälliger für Veränderungen in der Nähe des Häms als Posaconazol. Diese Beobachtungen werden von in-vitro-bestimmten minimalen Hemmkonzentrationen (MHK) unterstützt (5). Ein möglicher Resistenzmechanismus ist neben den Mutationen (v.a. im Bereich des erwähnten Hohlraumes) auch die E Azol-Antimykotika Ergosterol Episterol Reduktasen Isomerase 14α-Demethylase Lanosterol Squalenepoxid SqualenEpoxidase Zellmembran Abbildung: A-D: Strukturformeln von A) Posaconazol, B) Itraconazol, C) Voriconazol und D) Fluconazol. Die für die Wirkung essentielle Triazol-Gruppe ist jeweils farblich hervorgehoben (modifiziert nach (5)). E: Wirkungsweise der Azol-Antimykotika. Die Ergosterolsynthese wird durch Hemmung des Enzyms Lanosterol-14α-Demethylase gestört. Das für die Funktion der Zellwand essentielle Ergosterol wird nicht mehr synthetisiert und es resultiert eine fungistatische Wirkung (modifiziert nach (2)). Fortbildungstelegramm Pharmazie 2007;1:32-38 Posaconazol – ein neues Azol-Antimykotikum - 36 - erhöhte Expression von Effluxpumpen, die in einer verminderten intrazellulären Konzentration des Arzneistoffes resultiert (1) sind v.a. Glukuronid-Konjugate (17%) (10). In-vitro- und in-vivo-Studien Die Indikationsgebiete sind laut Fachinformation invasive Mykosen wie Aspergillosen, Fusariosen, Chromoblasomykosem und Myzetom sowie Kokzidioidomykosen bei Patienten, die gegenüber Amphotericin B, Itraconazol oder Fluconazol therapieresistent sind oder Unverträglichkeit gegen diese Arzneimittel aufweisen. Therapieresistenz ist dabei definiert als „Progression der Infektion oder Ausbleiben der Besserung nach mindestens 7 Tagen unter einer wirksamen antimykotischen Therapie in therapeutischer Dosierung“. Zusätzlich wird empfohlen, die Therapie nur von einem Arzt mit Erfahrung in der Behandlung invasiver Pilzinfektionen einzuleiten (11). In zahlreichen in-vitro-Untersuchungen wurden für verschiedene Pilzgattungen und -arten die MHK von Posaconazol im Vergleich zu anderen Antimykotika bestimmt. Dabei zeigte der Wirkstoff v.a. für Schimmelpilze (Aspergillus, Fusarium, Pseudallescheria) eine höhere Aktivität als Voriconazol, Itraconazol, Ravuconazol und Amphotericin B (7). Posaconazol hemmt dabei auch Aspergillus-Stämme, die gegen Itraconazol, Voriconazol oder Amphotericin B resistent sind (8), sowie Itraconazol-, Fluconazolund Voriconazol-resistente Candida-Arten (7). Die Aktivität gegen Zygomyceten ist zwar geringer als die von Amphotericin B, jedoch größer als die Aktivitäten von Voriconazol, Fluconazol und Itraconazol (7). Auch gegen Candida-Arten konnte eine gegenüber anderen Antimykotika erhöhte Aktivität gefunden werden. In Tierexperimenten verbesserte Posaconazol das Überleben und/oder reduzierte die Organbelastung in z.T. immunsupprimierten Tieren, die mit verschiedenen Pilzen infiziert worden waren (4). Pharmakokinetik Posaconazol ist als Suspension zu 40 mg/ml im Handel und wird oral verabreicht. Die Dosis beträgt zweimal täglich 400 mg zu den Mahlzeiten bzw. viermal täglich 200 mg, falls der Patient nicht zur Nahrungsaufnahme fähig ist. Die flüssige Darreichungsform ist ebenso wie fettige Nahrung geeignet, die systemische Verfügbarkeit im Gegensatz zu einer festen Formulierung bzw. Nüchterneinnahme zu erhöhen (9). Eine höhere Dosis als 800 mg pro Tag führt zu keinem höheren Plasmaspiegel. Das Verteilungsvolumen ist hoch (1774 Liter), und Posaconazol liegt in hohem Maß an Protein gebunden vor (> 98%). Es wird mit einer mittleren Halbwertszeit von 35 Stunden eliminiert, wobei der Großteil unverändert im Urin oder im Faeces ausgeschieden wird. Metabolite Klinische Wirksamkeit Die Zulassung basiert auf einer offenen, multizentrischen Phase-III-Studie mit 330 Patienten, die resistent oder intolerant gegenüber einer vorherigen Therapie (hauptsächlich Amphotericin B oder Itraconazol) waren und eine sichere oder wahrscheinliche (siehe Absatz 2, Einleitung) invasive Pilzinfektion aufwiesen. Als Kontrollgruppe dient eine retrospektive Studie mit 279 Patienten aus dem selben Zeitraum. Die Studien wurden verblindet und von einem externen Komitee ausgewertet (1,8). 800 mg Posaconazol pro Tag zeigte in dieser Studie eine klinisch relevante Aktivität gegenüber einem großen Spektrum invasiver Mykosen, bei denen Therapieresistenz vorlag oder Unverträglichkeiten aufgetreten waren. So sprachen 42,1% der Patienten mit invasiver Aspergillose auf Posaconazol an, jedoch nur 25,6% in der Kontrollstudie. Die Wirksamkeit gegen Fusariose, Chromoblastomykose, Myzetom und Kokzidoidomykosen konnte in dieser Studie ebenfalls nachgewiesen werden, wenn auch nicht in jedem Falle mit höherer Ansprechrate als bei der Kontrollgruppe. Um positive Aussagen für die Behandlung der Zygomkose, Kryptokokkose und Candidiasis sowie für die Behandlung von Kindern zu treffen, reichte die Datenlage nicht aus. Ebenso Fortbildungstelegramm Pharmazie 2007;1:32-38 Posaconazol – ein neues Azol-Antimykotikum gibt es weder einen direkten Vergleich mit Voriconazol oder Caspofungin, noch eine Evaluation von Posaconazol bei Patienten, die nicht auf eine Therapie mit diesen Medikamenten angesprochen haben oder Unverträglichkeit zeigen (8). Es gibt jedoch neuere Studien, die gerade für die Behandlung der Zygomykose Hinweise auf gute Wirksamkeit von Posaconazol geben (12). Therapie der Wahl ist hier nach wie vor das nebenwirkungsreiche Amphotericin B in hoher Dosierung. Sicherheit und Verträglichkeit Posaconazol zeigt insgesamt eine vergleichbare Verträglichkeit zu anderen Conazol-Antimykotika bei der Langzeittherapie invasiver Mykosen. Häufig (1-10%) auftretende Nebenwirkungen sind gastrointestinale, dermale und neurologische Symptome. Dazu zählen insbesondere Bauchschmerzen, Diarrhoe, Übelkeit, Erbrechen und Anorexie; Hautreaktionen wie Trockenheit, Pruritus und Ausschlag; sowie Schwindel, Kopfschmerz, Parästhesien, Schlaflosigkeit und Somnolenz (13). - 37 - gleichzeitiger Rifabutin-Gabe (ein CYP3A4-Induktor) erhöht sich die Posaconazol-Clearance. Eine Therapie mit beiden Stoffen wird daher nicht empfohlen, genauso wie eine gleichzeitige Gabe von Phenytoin oder Cimetidin (4). Fazit Posaconazol ist ein Beispiel für einen Arzneistoff, der zwar keinen neuen Wirkmechanismus aufweist, anderen Azolen jedoch in Bezug auf Wirksamkeit (Wirkspektrum) und Amphotericin B hinsichtlich Verträglichkeit überlegen ist und insgesamt daher kein „Me-Too“Präparat darstellt. Die Erweiterung der Zulassung für Indikationen wie Zygomykose, die Behandlung von Kindern, den prophylaktischen Einsatz und Primär- oder Kombinationstherapien wäre wünschenswert. Hierfür sind jedoch weitere Studien notwendig. Posaconazol ist somit weniger toxisch als Amphotericin B, welches derzeit als Mittel der Wahl zur systemischen Behandlung lebensbedrohlicher Pilzinfektionen gilt, aber schwere, zum Teil lebensbedrohliche Nebenwirkungen aufweist (4,14). Hier ist vor allem die Nephrotoxizität zu nennen, hinzu kommen häufig Fieber, Kopfschmerzen, gastrointestinale Störungen und Anämie (15). Da die Wirkung von Posaconazol auf einer Hemmung von CYP450-Enzymen beruht, können Interaktionen mit Arzneistoffen, die über diese Enzyme metabolisiert werden, nicht ausgeschlossen werden. Tatsächlich ist Posaconazol in therapeutischer Konzentration ein CYP3A4-Hemmer. Ritonavir- und Indinavir-Dosierungen müssen daher angepasst werden, wenn diese Stoffe gleichzeitig mit Posaconazol gegeben werden. Es wird auch empfohlen, ein Monitoring bei gleichzeitiger Ciclosporinoder Tacrolimus-Gabe durchzuführen und die Dosis eventuell zu verringern. Bei Fortbildungstelegramm Pharmazie 2007;1:32-38 Posaconazol – ein neues Azol-Antimykotikum - 38 - Literatur 1. Keating GM. Posaconazole. Drugs 2005;65;11:1553-1567. 2. Kojda G, Hafner D, Behne M, Wilhelm M. Pharmakologie Toxikologie Systematisch. 2 ed. Bremen, London, Boston, UNI-MED AG, 2002. 3. Ostrosky-Zeichner L, Pappas PG. Invasive candidiasis in the intensive care unit. Crit Care Med 2006;34;3:857-863. 4. Torres HA, Hachem RY, Chemaly RF, Kontoyiannis DP, Raad II. Posaconazole: a broad-spectrum triazole antifungal. Lancet Infect Dis 2005;5;12:775-785. 5. Xiao L, Madison V, Chau AS, Loebenberg D, Palermo RE, McNicholas PM. Three-dimensional models of wild-type and mutated forms of cytochrome P450 14alpha-sterol demethylases from Aspergillus fumigatus and Candida albicans provide insights into posaconazole binding. Antimicrob Agents Chemother 2004;48;2:568-574. 6. Munayyer HK, Mann PA, Chau AS, Yarosh-Tomaine T, Greene JR, Hare RS, Heimark L, Palermo RE, Loebenberg D, McNicholas PM. Posaconazole is a potent inhibitor of sterol 14alpha-demethylation in yeasts and molds. Antimicrob Agents Chemother 2004;48;10:3690-3696. 7. Sabatelli F, Patel R, Mann PA, Mendrick CA, Norris CC, Hare R, Loebenberg D, Black TA, McNicholas PM. In vitro activities of posaconazole, fluconazole, itraconazole, voriconazole, and amphotericin B against a large collection of clinically important molds and yeasts. Antimicrob Agents Chemother 2006;50;6:2009-2015. 8. EMEA. Noxafil Zulassungsdossier. www emea eu int/humandocs/Humans/EPAR/noxafil/noxafil htm 2005. 9. Courtney R, Wexler D, Radwanski E, Lim J, Laughlin M. Effect of food on the relative bioavailability of two oral formulations of posaconazole in healthy adults. Br J Clin Pharmacol 2004;57;2:218-222. 10. Courtney R, Pai S, Laughlin M, Lim J, Batra V. Pharmacokinetics, safety, and tolerability of oral posaconazole administered in single and multiple doses in healthy adults. Antimicrob Agents Chemother 2003;47;9:2788-2795. 11. Essex Pharma. Noxafil 40 mg/ml Suspension zum Einnehmen. Fachinformation 2005. 12. Greenberg RN, Mullane K, van Burik JA, Raad I, Abzug MJ, Anstead G, Herbrecht R, Langston A, Marr KA, Schiller G, Schuster M, Wingard JR, Gonzalez CE, Revankar SG, Corcoran G, Kryscio RJ, Hare R. Posaconazole as salvage therapy for zygomycosis. Antimicrob Agents Chemother 2006;50;1:126-133. 13. Raad II, Graybill JR, Bustamante AB, Cornely OA, Gaona-Flores V, Afif C, Graham DR, Greenberg RN, Hadley S, Langston A, Negroni R, Perfect JR, Pitisuttithum P, Restrepo A, Schiller G, Pedicone L, Ullmann AJ. Safety of longterm oral posaconazole use in the treatment of refractory invasive fungal infections. Clin Infect Dis 2006;42;12:17261734. 14. arznei-telegramm. atd Arzneimitteldatenbank. www arznei-telegramm de 2006. 15. Bristol-Myers Squibb. Amphotericin B. Fachinformation 2005. Der Autor Herr Marc Oppermann, geboren 1978 in Bochum, Schulabschluss 1998 in Menden, Pharmaziestudium 1999-2004, Praktisches Jahr im Institut für Pharmakologie in Düsseldorf und in der Apotheke Dr. Herrmann, Düsseldorf, Approbation als Apotheker Juni 2005, Seit 2005 Promotion unter der Leitung von Prof. Dr. G. Kojda, Institut für Pharmakologie und klinische Pharmakologie in Düsseldorf, Seit Juni 2005 Weiterbildung zum Fachapotheker für Arzneimittelinformation Fortbildungstelegramm Pharmazie 2007;1:32-38