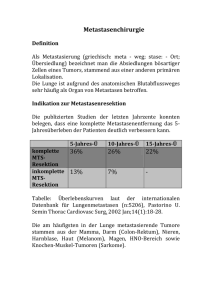
Langzeitüberleben von Patienten nach Laserablation pulmonaler
Werbung

Aus dem Institut für Diagnostische Radiologie und Neuroradiologie der Medizinischen Fakultät der Ernst-Moritz-Arndt-Universität Greifswald Direktor: Univ.-Prof. Dr. med. Norbert Hosten Langzeitüberleben von Patienten nach Laserablation pulmonaler Metastasen INAUGURAL-DISSERTATION zur Erlangung des akademischen Grades Doktor der Medizin (Dr. med.) der MEDIZINISCHEN FAKULTÄT der Ernst-Moritz-Arndt-Universität Greifswald (2010) vorgelegt von KAREN BOCK geb. am: 29.03.1980 in Berlin Dekan: Prof. Dr. rer. nat. Heyo Klaus Kroemer 1. Gutachter: Prof. Dr. N. Hosten (Greifswald) 2. Gutachter: Prof. Dr. C. Stroszczynski Tag der Disputation: 20. September 2010 2 Inhaltsverzeichnis 1. Grundlagen und Problemabgrenzung ……………………………………………… 06 1.1 Epidemiologie ………………………………………………………………….……..06 1.2 Therapeutische Optionen bei Lungenmetastasen …………………………….……… 10 1.2.1 Die chirurgische Therapie ………………………………………….……….10 1.2.2 Die Chemotherapie ………………………………………………………… 13 1.2.3 Die Strahlentherapie …………………………………………………...….. 15 1.2.4 Minimalinvasive Behandlungsmethoden ……………………………….…..17 1.3 Die Laserablation als minimalinvasive Behandlungsmethode von Lungenmetastasen 24 1.3.1 Entstehungsgeschichte der Laserablation …………….………………...… 24 1.3.2 Technische Grundlagen ……………………………………………………. 25 1.3.3 Bisherige klinische Erfahrungen ……………………………………………27 1.3.4 Komplikationen ……………………………………………………..…...… 30 1.3.5 Vorteile der Laserablation …………………………………………...…….. 31 1.4 Zielsetzung ……………………………………………………………………...…… 32 2. Material und Methoden …………………………………………….………………. 33 2.1 Patientenkollektiv ……………………………………………………………………. 33 2.1.1 Geschlechterverteilung ……………………………………………………. 33 2.1.2 Altersverteilung …………………………………………………………… 33 2.1.3 Art des Primärtumors ……………………………………………………… 34 2.1.4 Lokalisation der Metastasen …………………………………….…………. 35 2.1.5 Anzahl der Metastasen …………………………………………………….. 35 2.1.6 Größe der behandelten Metastasen ………………………………………… 36 2.2 Einschlusskriterien …………………………………………………………………... 37 2.3 Technische Durchführung …………………………………………………………… 38 2.3.1 Applikatorsystem …………………………………………………………... 38 2.3.2 Planung/ Platzierung ……………………………………………………….. 39 2.3.3 Verfahrensweise ……………………………………………………...…… 40 2.3.4 Behandlungsevaluation und Follow-up ………………….………………… 41 3 2.4 Erhebung und Auswertung ………………………………………………….…...….. 44 2.4.1 Datengrundlage …………………………………………………………….. 44 2.4.2 Statistische Methoden ……………………………………………………... 45 3. Ergebnisse …………………………………………………………………………… 46 3.1 Applikationen ……………………………………………………………….……….. 46 3.2 Technischer Erfolg der Metastasenbehandlung ……………………………………....46 3.3 Progression / Rezidiv …………………………………………………………..…….. 48 3.4 Technischer Erfolg der Gesamtbehandlung ………………………………….……… 50 3.5 Überlebenszeitanalyse ……………………………………………………………….. 51 3.5.1 Allgemeines zum Langzeitüberleben und Zahlen zum technischen Gesamtbehandlungserfolg …………………………………………………. 51 3.5.2 Gesamtüberleben ………………………………………………….……….. 52 3.5.3 Komplette vs. zytoreduktive Gesamtbehandlung …………………..……… 52 3.5.4 Gesamtüberleben nach Primärtumorentitäten ……………………..….…….54 3.4 Progressionsfreies Überleben ………………………………………………..………. 60 3.4.1 Allgemeines progressionsfreies Überleben ………………………………... 60 3.4.2 Lokale Tumorprogression/ -rezidiv ………………………………………... 61 3.4.3 Intrapulmonale Progression ……………………………………….….……. 64 3.4.4 Systemische Progression ……………………………………….….………. 65 3.5 Komplikationen ………………………………………………………….…………... 66 4. Diskussion ……………………………………………………………………………. 67 4.1 Langzeitergebnisse ……………………… ……………...…………………………... 67 4.2 Komplikationen ……………………… ……………...…………………………….... 77 4.3 Kritische Anmerkungen ……………………… ……………...……………………....80 4.4 Schlussfolgerungen ……………………… ……………...…………………………...81 5. Zusammenfassung ………………………………………………………………….... 83 6. Literaturverzeichnis …………………………………………………………………. 85 4 7. Abbildungsverzeichnis ………………………………………………………………. . 98 8. Tabellenverzeichnis ……………………..…………………………………….……... 100 9. Abkürzungsverzeichnis ………………………………………………….……….…. 101 10. Eidesstattliche Erklärung ………...…………………………………………….…. 103 11. Lebenslauf ……………………………………………………………….…….…… 104 12. Danksagung ……………………………………………………………….…….….. 105 5 1 GRUNDLAGEN UND PROBLEMABGRENZUNG 1.1 Epidemiologie Unter Krebs insgesamt werden alle bösartigen Neubildungen einschließlich der nicht organgebundenen Neubildungen des blutbildenden Systems verstanden. Für das Jahr 2004 schätzt das Robert-Koch-Institut die Zahl der jährlichen Neuerkrankungen an Krebs in Deutschland auf etwa 436.500 Fälle (ca. 230.500 Männer und ca. 206.000 Frauen). Die häufigste Krebserkrankung der Männer ist mit 25 % der Prostatakrebs, bei Frauen mit einem Anteil von fast 28 % der Brustkrebs (vgl. Abb. 1). Das mittlere Erkrankungsalter liegt für beide Geschlechter bei 69 Jahren [67]. Männer Frauen Prostata Darm Lunge 25,4 27,8 16,2 17,5 14,3 6,4 Harnblase 9,3 5,7 Magen Niere Mundhöhle u. Rachen Non-Hodgkin-Lymphome 4,9 4,7 4,7 4,1 3,3 3,8 2,9 3,6 Malignes Melanom Bauchspeicheldrüse 2,8 3,2 2,7 3,2 Leukämien 2,1 3,0 Hoden 2,1 Speiseröhre 1,7 Kehlkopf 1,3 30 25 20 15 10 5 2,9 2,1 Brustdrüse Darm Lunge Gebärmutterkörper Eierstöcke Malignes Melanom Magen Harnblase Bauchspeicheldrüse Niere Gebärmutterhals Non-Hodgkin-Lymphome Leukämien 1,7 Schilddrüse 00 5 10 15 20 25 30 Abb. 1 Prozentualer Anteil ausgewählter Tumorlokalisationen an allen Krebsneuerkrankungen in Deutschland 2004 [Quelle: Schätzung der Dachdokumentation Krebs im Robert Koch Institut] Bei den Todesursachen im Jahre 2004 liegen in Deutschland bösartige Tumorerkrankungen mit 25 % an zweiter Stelle hinter Erkrankungen des Kreislaufsystems (45 %). Von den ca. 208.824 krebsbedingten Todesfällen/Jahr bei Männern sind mit 26 % bösartige Neubildungen der Lunge die häufigste Todesursache. Mit 17,9 % der ca. 110.745 Todesfälle/Jahr bei Frauen ist es der Brustkrebs. Darmkrebs ist bei beiden Geschlechtern die zweithäufigste krebsbedingte Todesursache (vgl. Abb. 2, Seite 7). Die alterstandardisierte Krebsmortalität ist bei Männern seit Mitte der 1980er Jahre rückläufig, bei Frauen bereits seit 1970. Das mittlere Sterbealter an Krebs liegt bei Männern bei 71 und bei Frauen bei 75 Jahren [67]. 6 Männer Frauen Lunge Darm Prostata 26,0 17,9 12,4 14,3 10,1 Bauchspeicheldrüse Magen Niere Leukämien Harnblase 25 20 15 5,7 5,6 Eierstöcke 3,7 5,3 3,4 3,2 3,4 2,7 Magen Leukämien Non-Hodgkin-Lymphome Speiseröhre 3,1 2,7 3,1 2,6 Non-Hodgkin-Lymphome 2,4 2,0 5 Bauchspeicheldrüse 6,7 Mundhöhle u. Rachen 10 Lunge 11,2 5,8 Kehlkopf 1,2 Malignes Melanom 1,1 Schilddrüse 0,2 30 Brustdrüse Darm Harnblase Gebärmutterkörper Niere 1,7 Gebärmutterhals 1 Speiseröhre 1 Malignes Melanom 00 5 10 15 20 25 30 Abb. 2 Prozentualer Anteil ausgewählter Tumorlokalisationen an allen Krebssterbefällen in Deutschland 2004 [Quelle: Amtliche Todesursachenstatistik, Statistisches Bundesamt, Wiesbaden] Die 5-Jahres-Überlebensraten umfassen für Patienten mit malignen Neubildungen einen breiten Bereich von prognostisch sehr günstigen Raten für das Lippenkarzinom und den Hodenkrebs, bis hin zu sehr ungünstigen Raten bei Tumoren der Bauchspeicheldrüse, der Lunge und der Speiseröhre (vgl. Tab. 1). Insgesamt zeigt sich seit den 1970er Jahren eine Verbesserung der Überlebensraten, dazu haben u.a. der Rückgang des Magenkarzinoms mit schlechteren und die Zunahme von Darmkrebs mit besseren Überlebensraten beigetragen. Der deutliche Anstieg der Überlebenswahrscheinlichkeit ist ebenfalls auf die besseren und häufigeren Früherkennungsuntersuchungen beispielsweise von Prostata, Darm und Brust und den damit verbundenen verbesserten Therapiemöglichkeiten zurückzuführen [67]. Tumorlokalisation Primärtumor kumuliert Speiseröhre Mundhöhle u. Rachen Mundhöhle u. Rachen Magen Darm Bauchspeicheldrüse Kehlkopf Lunge Malignes Melanom Brustdrüse Gebärmutterhals Gebärmutterkörper Eierstöcke Prostata Hoden Niere Ösophaguskarzinom Lippenkarzinom Pharynxkarzinom Magenkarzinom kolorektales Karzinom Pankreaskarzinom Larynxkarzinom Bronchialkarzinom Malignes Melanom Mammakarzinom Zervix-Karzinom Endometriumkarzinom Ovarialkarzinom Prostatakarzinom Keimzellkarzinom Nierenzellkarzinom 20 – 22 %[67] 90 % [67] 30 – 40 % [67] 31 – 35 % [67] 60 % [67] 6,4 - 7,6 % [67] 61 – 62 % [67] 15 -18 % [67] 84 – 88 % [67] 81 - 87,7 % [69] 61 % [67] 82 % [67] 47 % [67] 87 - 99,3 % [69] 98 - 100 % [67] 66 – 67 %[67] 5-Jahres-Überlebensrate lokales Stadium regionales Stadium 34 - 38 % [11] 89,9 % [69] 20-25 % [8, 36] 19 % [11] 67,3 % [69] 50 % [67] 90 % [31] 97,5 % [69] 80 - 95 % [20] 16,1 % [69] 30 % [31] 80,4 % [69] 38–66 %[20] 70 % [50] 100 % [69] 98 % [67] 80–90 % [67] Tab. 1 Geschätzte 5-Jahres-Überlebensraten ausgewählter Primärtumore 7 Fernmetastasen 3 % [113] 19 % [58] 15 % [134] 10 % [11] 5-15 % [69] < 1 % [36] 5 % [67] < 1 % [31] 25,5 % [69] 10 % [20] 10 % [50] 34–40 % [7, 69] 70 % [67] 10 % [67] Für alle Krebslokalisationen unterscheiden sich die Überlebensraten deutlich nach der Histologie und dem Stadium der Erkrankung. Bei der Prognose sind langsam voranschreitend wachsende Tumore von aggressiven, metastasierenden Verlaufsformen zu unterscheiden. Während beim Keimzellkarzinom des Hodens als wenig aggressiver Tumor die 5-JahresÜberlebensrate über alle Stadien über 98 % und im metastasierenden Stadium noch bei 70 % liegt, beträgt die 5-Jahres-Überlebensrate beim Malignen Melanom im lokalen Stadium ca. 90 %, bei Vorhandensein von Fernmetastasen hingegen weniger als 1 %. Für das kolorektale Karzinom liegt die durchschnittliche relative 5-Jahres-Überlebensrate bei 60 %, bei bereits eingetretener Metastasierung aber nur zwischen 5-15 %. Aus klinischen Studien ist bekannt, dass bei Früherkennung des Mammakarzinoms 97,5 % der Patientinnen die ersten fünf Jahre nach der Diagnose überleben, bei bereits eingetretener Metastasierung sind es aber nur noch 25 % [67]. Gleiches gilt bei der Prostatakrebserkrankung. Beschränkt sich der Tumor auf die Prostata, leben fünf Jahre nach Diagnosestellung noch bis zu 90 % der Betroffenen. Bei Bildung von Metastasen sind es noch 40 %. Ohne Behandlung liegt die Lebenserwartung bei einem 60-jährigen Mann mit einem lokalen Prostatakrebs zwischen 10 bis 15 Jahren [7]. Vor allem die Lunge bietet mit ihrem ausgedehnten Blut- und Lymphgefäßsystem ein zentrales Zielorgan für eine Metastasierung und stellt bei allen histologischen Tumortypen neben der Leber das größte Auffangbecken für Malignome aller Art und Herkunft dar. Ein Drittel aller Patienten mit Karzinomen und Sarkomen entwickeln im Laufe ihrer Erkrankung Tumorabsiedlungen in die Lunge [115]. Laut Sektionsstatistik werden in 20-54 % aller durchgeführten Autopsien bei Tumorpatienten Lungenmetastasen gefunden [150]. Die geschätzte jährliche Inzidenz von Lungenmetastasen in den USA, EU und Japan (Autopsie) beträgt 700.000 [138]. Dabei erfolgt die Absiedlung in die Lunge meist hämatogen, eine Streuung via Lymphbahnen sowie per continuitatem sind seltenere Geschehen. In 15-25 % der Fälle findet sich eine auf die Lunge beschränkte Metastasierung [15, 150]. Pharynxkarzinome und Mammakarzinome haben eine hohe Rate der Metastasierung in die Lunge. In ca. 25 % aller neu diagnostizierten Fälle liegt ein metastasiertes Stadium vor, dabei treten in 70 % Lungenmetastasen auf [104, 139, 152]. Bei Osteosarkomen und Weichteilsarkomen ist die Lunge häufig das einzige von Metastasen befallene Organ [65, 115]. Metastasen des Nierenzellkarzinoms finden sich in über 30 % in der Lunge [7, 104]. Das Prostatakarzinom metastasiert bei 40 % der Patienten in die Lunge [40]. Ca. 15-26 % der Patienten mit kolorektalen Karzinom entwickeln pulmonale Metastasen [63]. Dabei besteht 8 eine erhöhte Inzidenz, wenn es sich um ein Rektum- bzw. ein linksseitig lokalisiertes Kolonkarzinom handelt [138]. Solitäre Lungenmetastasen werden beim kolorektalen Karzinom in 10% der Fälle festgestellt [104]. Das Risiko der Fernmetastasierung beim Malignen Melanom (Größe <1 mm) liegt innerhalb der ersten 5 Jahre unter 10 %, bei sehr weit fortgeschrittenen Tumoren (>4 mm Dicke) steigt es auf bis zu 70 % an. Maligne Melanome mit Fernmetastasierung sind in aller Regel mit einer schlechten Prognose korreliert. Die mediane Überlebenszeit beträgt in diesem Fall 5-8 Monate [31]. Bei 70 % der Patienten entstehen im Krankheitsverlauf Lungenmetastasen, jedoch ist die Lunge nur bei 10 % als einziges Organ betroffen. Solitäre Lungenmetastasen findet man bei 20 % der Melanom-Patienten [10, 18]. Tumorlokalisation Speiseröhre Hals-, Nasen-, Ohren-Tumore Magen Darm Bauchspeicheldrüse Leber Lunge Malignes Melanom der Haut Brustdrüse Prostata Niere Weich- und Stützgewebe Primärtumor Auftreten von Metastasierungen Ösophaguskarzinom Pharynx- u. Larynxkarzinom Magenkarzinom kolorektales Karzinom Pankreaskarzinom Hepatozelluläres Karzinom Bronchialkarzinom Malignes Melanom Mammakarzinom Prostatakarzinom Nierenzellkarzinom Osteosarkom 10 – 25 % [40, 152] 10 – 24 % [5, 40] 3 % [104] 20-25 % [40, 104] Auftreten von Metastasen in der Lunge 21 % [11] 40-70 % [51,152] 28 % [11] 15-26 % [63] 10 % [11] 30 – 50 % [11] 17 - 40 % [17,51] 60-80 % [10, 51, 86] 60-68 % [ 51, 139] 40 % [40] 10-40 % [40, 68, 104] 20-40 % [104] 75% - 80 % [40, 51, 113] Tab. 2 Prozentuales Auftreten von Metastasen in der Lunge ausgewählter Primärtumore Typischerweise treten Lungenmetastasen peripher und multipel auf und können bei einer Größe > 1 cm als flaue Rundherde bereits auf einer konventionellen Röntgenaufnahme erkannt werden. Metastasen < 1 cm werden mit der CT besser erfasst. Mit deren Diagnosestellung ist oft eine infauste Prognose mit kurzer Überlebenszeit zu erwarten [55]. Die zunehmende Bedeutung der Therapie von Lungenmetastasen wird anhand der vorstehenden Daten hinsichtlich der Häufigkeit der Metastasierung in die Lunge und der damit verbundenen teils erheblich niedrigeren 5-Jahres-Überlebensraten deutlich. Berücksichtigt man, dass häufig eine kurative Therapie des Primärtumors möglich ist und die Patienten infolge der Metastasierung versterben, wird die Dringlichkeit einer adäquaten Therapie der sekundären Lungentumore deutlich. Die Art der Therapie hängt von der Prognose des Primärtumors, der Anzahl der Metastasen und des tumorfreien Intervalls von Behandlung des Primärtumors bis zur Fernmetastase ab. Sie ist in einer engen interdisziplinären Zusammenarbeit zwischen Chirurgen, Onkologen, Pathologen, Radiologen und Strahlentherapeuten zu entwickeln [115]. 9 1.2 Therapeutische Optionen bei Lungenmetastasen 1.2.1 Die chirurgische Therapie Eine komplette chirurgische Entfernung der Lungenmetastasen unter Einhaltung eines Sicherheitsabstandes im gesunden Gewebe bietet gegenwärtig die besten Chancen Lungenmetastasen kurativ zu behandeln. Daher gilt die operative Resektion derzeit als Goldstandard bei der Therapie pulmonaler Metastasen, zumal niedrige Morbiditäts- und Mortalitätsraten bestehen [55, 104, 115, 124, 140]. Erstmals wurden Mitte der 60er Jahre Metastasenresektionen durchgeführt [127]. Sie zeigten überraschend gute Ergebnisse, woraufhin führende Thoraxzentren Ende der 70er Jahre mit der planmäßigen Resektion von Lungenmetastasen begannen. Zu diesem Zeitpunkt galten allerdings sehr eingeschränkte Indikationskriterien. Es wurden nur Patienten mit Solitärmetastasen operiert, die zusätzlich ein möglichst langes Intervall zur Primäroperation aufwiesen. Heute werden auch Patienten mit multiplen und synchronen Metastasen operiert. Auch werden heute Patienten operativ therapiert, die Rezidivmetastasen entwickeln oder bei denen vorausgegangene komplette Resektionen von Metastasen anderer Organe durchgeführt wurden, insbesondere wenn kein Ansprechen auf Chemotherapie zu verzeichnen ist oder anfängliche Remissionen im weiteren Verlauf ausbleiben [64, 82]. Trotz der großen Fortschritte auf dem Gebiet der Lungenmetastasenresektion gilt bis heute die Bedingung, dass der Primärtumor komplett entfernt sein sollte (R0-Resektion) und andere extrapulmonale Herde in dem vorgeschalteten Tumor-Staging von Abdomen, Schädel- und Skelettsystem ausgeschlossen sind [55]. Weitere Voraussetzung ist die funktionelle Reserve im Hinblick auf den zu erwartenden Parenchymverlust. Im thoraxchirurgischen Patientenkollektiv sind diese Bedingungen am häufigsten bei Patienten mit Metastasen des kolorektalen Karzinoms und des Nierenzellkarzinoms gegeben. Davon unabhängig ist in Einzelfällen die Operation unter palliativem Aspekt oder aus diagnostischen Gründen indiziert [16]. Als Resektionsverfahren haben sich in der Lungenmetastasenchirurgie klassische parenchymsparende Operationstechniken wie Keil-, Subsegment- oder Segmentresektion und die videoassistierte Thoraxchirurgie (VATS) bewährt [70, 140]. Die operationsassoziierte Mortalität liegt zwischen 1 % und 4 % [1, 43, 61, 66, 99, 115], Schirren et al. beschreiben bei 10 849 Patienten mit operierten Lungenmetastasen eine 30-Tage-Letalität von 2,2 % [115]. Die Morbiditätsrate wird je nach Studie zwischen 6,3 % und 30 % angegeben, wobei Keilresektionen weniger postoperative Komplikationen verursachen als Lob- und Pneumonektomien [1, 43, 61, 66]. Die 5-Jahres-Überlebensrate nach pulmonaler Metastasenresektion wird unabhängig vom Primärtumor in aktuellen Studien mit 30-50 % angegeben [76, 87, 104, 124]. In der bislang größten Analyse zu Langzeitergebnissen mit 5206 untersuchten Fällen („The International Registry of Lung Metastases“) werden 5-, 10- und 15-Jahres-Überlebensraten von 36 %, 26 % und 22 % angegeben [27]. Aufgeschlüsselt nach den Primärtumoren werden in Tabelle 3 die 5-Jahres-Überlebensraten aus verschiedenen Studien dargestellt. Autor Cheuk-Kin Lo [13] Rotolo [112] Lee [73] Goya [35] Ogata [92] Pfannschmidt [100] Hatz [43] Jahr 2007 2007 2006 2006 2005 2003 n PT 80 23 59 62 76 167 CRC CRC CRC CRC CRC CRC R0 med. Follow-up (Mon) Überlebensraten (in %) 1 3 4 61 (5-121) 34,7 10 35,5 74 50,3 42 32 32,4 + + 5 42,5 med. ÜLZ (Mon) 58,6 22 24 40,2 2002 69 Rektum 49,9 29,3 17,4 33,8 46 Colon 47,4 26,8 11,6 7,1 De Giacomo [14] 1998 24 CRC 50 Schirren [115] 1998 91 CRC 42,1 50,2 Meimarakis [84] 2007 180 RCC + 58 45 31 43 Hofmann[52] 2005 64 RCC 33,4 39,2 Piltz [101] 2003 105 RCC 40 33 Hatz [43] 2002 128 RCC 55,2 40,5 29,9 42,4 Schirren [115] 1998 95 RCC 43,2 44 Hatz [43] 2002 33 MM 31,2 14,2 5,3 15 Leo [75] 2000 282 MM + 22 16 Schirren [115] 1998 18 MM 13 21,4 Harpole [42] 1992 98 MM + 20 22 Gorenstein [34] 1991 56 MM + 25 18 Friedel [26] 2002 467 Mamma + 38 22 Hatz [43] 2002 47 Mamma 49,6 36,3 22 35 Schirren [115] 1998 50 Mamma 46,2 53,6 Hatz [43] 2002 710 various 45 (0-275) 45 32 22 30 576 various + 51 38 26 38 Abecasis [1] 1999 85 various 22 (1-146) 29,2 n=Anzahl der Patienten; PT=Primärtumor; R0 – Komplette Resektion; med.=median; Mon=Monate; ÜLZ=Überlebenszeit Tab. 3 Überlebensraten nach Resektion der Lungenmetastasen verschiedener Primärtumore Bei Patienten mit Keimzelltumoren ist die 5-Jahres-Überlebensrate nach Metastasenresektion mit über 70 % am besten [43], die niedrigsten zeigen Patienten mit resezierten Lungenmetastasen eines malignen Melanoms. Bei einer hohen pulmonalen Metastasierungsrate dieses Primärtumors können nur wenige Patienten aufgrund des oft 11 disseminierten Organbefalls einer chirurgischen Therapie zugeführt werden. Die 5-JahresÜberlebensraten werden zwischen 14 % und 25 % angegeben, die mediane Überlebenszeit zwischen 15 und 29 Monaten [34, 42, 43, 75, 115]. Die Resektion pulmonaler Metastasen stellt das Verfahren der 1. Wahl bei Nierenzellkarzinomen und kolorektalen Karzinomen dar. Die 5-Jahres-Überlebensraten werden mit bis zu 50 % angegeben und sind damit signifikant höher im Vergleich zu unbehandelten Patienten [43, 52, 73, 84, 92, 100, 101, 115]. Beim Mammakarzinom sind die Voraussetzungen zur potentiell kurativen Operation ungünstig. Nur in 22 % metastasierender Mammakarzinome liegt ein isoliert pulmonaler Befall vor und die oftmals diffuse Lymphangiose um die Herde stellt eine Kontraindikation zur Resektion dar. Die 5-Jahres-Überlebensrate wird mit 36 % - 46 % angegeben [26, 43, 115]. Auch die Anzahl der Metastasen hat einen signifikanten Einfluss auf das Langzeitüberleben nach der Resektion. Pfannschmidt et al. berichten von 5-Jahresüberlebensraten von 45 % nach der Resektion solitärer Lungenmetastasen eines kolorektalen Karzinoms und von 19,8 % bei Patienten mit multiplen Befall [100]. Lediglich 10-30 % der Tumorpatienten mit einer pulmonalen Metastasierung kommen für eine operative Therapie in Frage, da der Metastasenresektion operationstechnische Grenzen gesetzt sind [115]. Obwohl Lungenmetastasen in der Regel lange lokal wachsen und deshalb mit einem geringem Sicherheitsabstand entfernt werden können, ist die Anzahl konventioneller Klemmen- oder Stapler-Keilresektionen derzeit auf etwa drei bis fünf pro Lungenseite begrenzt. Darüber hinaus erfordert die zentrale oder hiläre Lage einer Metastase durchschnittlich in 20-25 % die Resektion eines ganzen Lappens, so dass nur Patienten mit einer guten Lungenfunktion in Frage kommen. Vor allem im Falle von Rezidivmetastasen ist die pulmonale Reserve oftmals eingeschränkt. Zwar sind erneute chirurgische Interventionen nach einem Rezidiv auch mehrmals erfolgreich durchführbar, jedoch wird mit jeder weiteren Operation die verbleibende pulmonale Reserve zunehmend verkleinert, so dass die pulmonale Metastasektomie an die Grenze der Operabilität stößt [27, 38, 57]. Auch ein multifokales Auftreten von Metastasen, der Befall beider Lungenlappen und die Größe können eine chirurgische Resektion unmöglich machen [19, 55]. Weitere Ursachen für eine Inoperabilität können neben den operationstechnischen Grenzen auch in einem schlechten Allgemeinzustand, einer Multimorbidität oder einer ablehnenden Haltung der Patienten gegenüber einer Operation liegen. 12 1.2.2 Die Chemotherapie Ist eine operative Entfernung der Lungenmetastasen nicht möglich, sollte primär eine medikamentöse Behandlung begonnen werden [116]. Bei Absiedlungen nichtseminomatöser Keimzelltumoren, des Mammakarzinoms und Osteosarkoms wird die Chemotherapie sogar der operativen Therapie vorgezogen, da Metastasen dieser Tumore eine gute Ansprechrate zeigen. In diesen Fällen hat die Chirurgie lediglich die Aufgabe, noch verbliebene Herde zu eliminieren. [16, 26, 43, 83, 141]. Die Standardbehandlung ist die systemische Chemotherapie. Bei dieser Therapieform werden Zytostatika durch eine venöse Infusion über das Blutsystem im gesamten Körper verteilt. In der Regel läuft die Infusion durch eine Vene am Arm oder über ein Portsystem unter der Haut im Brustbereich, das zuvor operativ mit einer Verbindung zu einer zentralen Körpervene angelegt wurde. Auch die Chemotherapie in oraler Form, bei der die Wirkstoffe über das Verdauungssystem in die Blutbahn gelangen, ist eine systemische Behandlungsmöglichkeit. Bei der überwiegenden Anzahl der Patienten wird die systemische Chemotherapie zur Behandlung von Lungenmetastasen in palliativer Intention durchgeführt. Ziel der Behandlung ist es das Tumorwachstum eine zeitlang aufzuhalten oder zu verlangsamen und so die Überlebenszeit der Patienten mit einer Verbesserung des Allgemeinzustands und einem Rückgang von tumorbedingten Beschwerden und Schmerzen zu verlängern. Echte Langzeitemissionen sind jedoch noch immer selten [19, 111]. Bei gutem Ansprechen der Therapie kann aber ein sekundär operabler Befund entstehen, so dass bei der Behandlung von initial als inoperabel geltenden Tumoren stets die Möglichkeit einer Operation geprüft werden sollte. In der bislang größten Studie zu Langzeitergebnissen lag bei Patienten mit primär als nicht resektabel eingestuften Lungenmetastasen nach Chemotherapie „im neoadjuvanten Sinne“ die Rate der Resektion bei 22 % [27]. Problematisch ist vor allem das oft ungenügende Ansprechen der Metastasen auf die Zytostatika. So wird in der Literatur bei alleiniger systemischer Chemotherapie pulmonaler Metastasen von Ansprechraten von maximal 20 % bis 30 % berichtet, ohne jedoch die Überlebensprognose wesentlich zu verbessern [37, 48, 71, 81, 96, 102]. Einige Autoren berichten nach der Behandlung von Patienten mit pulmonal metastasierten kolorektalen 13 Karzinom von Prognoseverbesserungen und Ansprechraten von bis zu 30 bis 50 % [111, 120]. Langzeitergebnisse stehen noch aus. Ein Grund für die geringen Ansprechraten liegt in der Schwierigkeit, eine genügend hohe Zytostatikakonzentration in der Lunge zu erzielen. Die applizierbare Dosis wird dabei durch die systemische Toxizität der Zytostatika begrenzt, ohne dass eine antineoplastische Gewebekonzentration erreicht wird [3]. Eine Möglichkeit, die wirksame Konzentration im Zielorgan zu erhöhen, bietet sich durch die Anwendung der isolierten Lungenperfusion. Da die spezifische Toxizitätsschwelle des einzelnen Organs oft wesentlich höher liegt als die systemische, können durch dieses Verfahren, bei dem ausschließlich das betroffene Zielorgan perfundiert wird, weit höhere Zytostatikakonzentrationen im Tumorgewebe erreicht werden. Zudem wird eine systemisch-toxische Reaktion vermieden, da das Medikament nicht in den systemischen Kreislauf gelangt. Der Nachteil dieser Methode besteht allerdings in der begrenzten einmaligen Applikation des Zytostatikums und dem erheblichen operativen Aufwand, da der Patient thorakotomiert werden muss [3, 133]. Eine wesentliche Limitation der systemischen Chemotherapie ist durch die patientenabhängigen erheblichen unerwünschten Nebenwirkungen des Körpers auf diese Behandlung determiniert. Denn einerseits hemmen die Zytostatika das Zellwachstum von sich häufig teilenden Zellen und sind somit ein wirksames Mittel gegen die sich häufig teilenden und ausbreitenden Tumorzellen, andererseits wirkt diese Therapie an mehreren Organen und Körperbereichen, so dass auch gesunde, sich oft erneuernde Körperzellen wie Knochenmark, Schleimhaut- und Haarzellen von angegriffen werden. Dies kann zu Entzündungen, Anämie, Infektionsanfälligkeit, kleinen Geschwüren, Haarausfall, Appetitlosigkeit, Durchfall, Übelkeit, Erbrechen, verlängerte Blutungsdauer, stärkeres Nasen- und Zahnfleischbluten, Müdigkeit, Erschöpfung und Leistungsschwäche führen. Trotz ständiger Weiterentwicklung potenter Chemotherapeutika und neuer Kombinationstherapien sind die meisten Patienten durch eine Chemotherapie allein nicht heilbar. Daher wird die komplette chirurgische Resektion weiterhin als einzig potentiell kurative Behandlungsoption angesehen [115]. 14 1.2.3 Die Strahlentherapie Die Strahlentherapie, auch Radiotherapie genannt, ist die dritte Säule in der Behandlung von Krebserkrankungen. Bei der Behandlung von Lungenmetastasen spielt sie im Sinne einer Ganzlungenbestrahlung aber aufgrund der ausgeprägten Dosis-Volumen-Beziehung nur eine untergeordnete Rolle, da durch die flächenhafte Bestrahlung auch gesunder Lungenareale ein erheblicher Fibroseschaden zu erwarten ist. Dieser würde zu einer deutlichen Einschränkung der Lebensqualität des Patienten führen [103]. Wegen bestehender Indikationen wie fehlender Resektabilität und Nichtansprechen auf eine systemische Chemotherapie sollte die Möglichkeit einer Durchführung dennoch überprüft werden [16, 76]. Üblicherweise erfolgt die Strahlentherapie von Lungenmetastasen als adjuvante Ergänzung einer Chemo- oder chirurgischen Therapie, als kurative Therapie hat sie bislang keine Bedeutung [3]. Mit der Strahlenbehandlung ist die Zerstörung von Tumorgewebe durch ionisierende Strahlen möglich. Ionisierende Strahlung führt zu Veränderungen im Erbgut der Zellen, die von normalen, gesunden Zellen in der Regel wieder repariert werden. Tumorzellen haben hingegen ein weniger gut funktionierendes Reparatursystem, so dass die durch die Bestrahlung verursachten Einwirkungen nicht behoben werden können. Ziel ist es, im zu bestrahlenden Gebiet eine möglichst hohe Strahlendosis zu erreichen und dabei gleichzeitig das umgebende gesunde Gewebe so weit wie möglich zu schonen. Der Erfolg der Strahlentherapie hängt entscheidend davon ab, welche Strahlendosis die Metastase erreicht. Auf das umgebende gesunde Gewebe sollte möglichst wenig Strahlung fallen, damit es so wenig wie möglich in Mitleidenschaft gezogen wird. Je genauer also die Tumorabsiedlung von der Strahlung erfasst wird, desto höher kann die eingesetzte Strahlendosis sein, ohne dass folgenschwere Schäden im angrenzenden Gewebe entstehen. Doch bei Lungenmetastasen ist die punktgenaue und hochdosierte Bestrahlung besonders schwierig, da sich der Tumor mit dem Ein- und Ausatmen bewegt und deshalb während der Bestrahlung ständig die Position verändert. Daher wurden in der jüngeren Vergangenheit spezielle Formen der Strahlentherapie entwickelt, bei der die Strahlenquelle innerhalb oder in unmittelbarer Nähe des Zielgebietes im Körper des Patienten platziert werden kann. Eine spezielle Form der Bestrahlung von Metastasen ist die stereotaktische Strahlentherapie. Hierbei handelt es sich um eine hochpräzise Bestrahlungstechnik mit Atemsynchronisation, bei der die definierte Dosis an Röntgenstrahlen punktgenau in ein zuvor definiertes Zielgebiet 15 eingebracht wird [79]. Dabei wird die genaue Position der Tumorabsiedlung mit Hilfe von Aufnahmen eines Computertomographen erfasst, nachdem diese zuvor mit einer speziellen Goldspirale markiert wurde. Auf diese Weise kann die Bestrahlung genau gesteuert werden: Strahlung wird nur dann abgegeben, wenn sich der Tumor im Zielbereich befindet. Dadurch kann die Strahlenbelastung für das angrenzende gesunde Gewebe gering gehalten werden, umgekehrt ist die Strahlenkonzentration in der Metastase besonders hoch. Die Bestrahlung ist so präzise, dass eine im Vergleich zu herkömmlichen Verfahren mehrfach erhöhte Strahlendosis verabreicht werden kann. Damit erhöht sich die Wirksamkeit der Bestrahlung und die Chancen steigen, dass die Metastase sich verkleinert bzw. ganz zerstört werden kann. Auch Rezidive können mit diesem Verfahren wirksam bestrahlt werden. Ein weiteres Bestrahlungsverfahren zur Tumortherapie von Lungenmetastasen ist die noch experimentelle interstitielle Brachytherapie. Bei dieser Therapieform wird unter CTMonitoring der Tumorherd punktiert und eine 192 Iridium-Strahlenquelle eingeführt. Dadurch kann am Zielort eine relativ hohe Einzeldosis von bis zu 20 Gray appliziert werden. Die Möglichkeit der hohen Einzeldosisgabe besteht, da im Vergleich zum Tumorgewebe die Toleranzdosis des Lungenparenchyms sehr hoch ist. In ersten Studienergebnissen konnte eine hohe therapeutische Effizienz aufgezeigt werden, allerdings muss dieser Therapieansatz noch in weiteren prospektiven Studien evaluiert werden [29, 98, 105]. Wie die Operation und Chemotherapie ist auch die Strahlenbehandlung ein Verfahren, das mit Belastungen für den Patienten einhergeht. Wie ausgeprägt die Nebenwirkungen sind, hängt von der verabreichten Strahlendosis ab, von der Empfindlichkeit der bestrahlten Gewebeart und von der individuellen Reaktion des Patienten. Frühreaktionen wie Hautreizungen im Bestrahlungsfeld, Übelkeit und Durchfall sowie Spätreaktionen aufgrund von Fibrosierung und Gefäßverengung können auftreten. Dazu zählen Verfärbungen der Haut, Verhärtungen im Unterhautfettgewebe und Lungenfibrose. Die Spätfolgen werden in Schweregrade 0-5 der LENT-SOMA-Klassifizierung eingeordnet. Nach dieser Klassifizierung traten in der Gruppe von Okunieff et al. [94] bei 35 % aller Patienten Toxizitäten 1.Grades, bei 6,1 % aller Patienten Toxizitäten 2.Grades und bei 2 % der Patienten Toxizitäten 3.Grades auf. In einer weiteren Studiengruppe wurden aufgrund der stereotaktischen Bestrahlung bei einem Patienten toxische Reaktionen 4. Grades beobachtet [10]. Als Risiken der Brachytherapie sind am ehesten Komplikationen hinsichtlich eines Pneumothorax, einer Parenchymblutung, dermatologische Folgen und die Gefahr einer Pneumonie zu nennen [29, 98, 106]. 16 1.2.4 Minimalinvasive Behandlungsmethoden Da sich die Chemo- und Strahlentherapie oftmals nicht als effiziente Behandlungsmethode beim Vorliegen einer Metastasierung der Lunge erwiesen hat, standen für inoperable Patienten in früherer Zeit keine anderen adäquaten Therapiemethoden zur Verfügung, die eine zur Resektion vergleichbare Effektivität bieten konnten. Dies hat in den letzten Jahren zu einem verstärkten wissenschaftlichen Interesse an der Entwicklung alternativer Therapieverfahren geführt, die statt oder ergänzend zur Operation, Bestrahlung oder Chemotherapie, das Ziel haben, mit möglichst geringer Invasivität, hoher lokaler Erfolgsrate und potentieller Wiederholbarkeit sowohl die Überlebenszeit als auch die Lebensqualität der Tumorpatienten zu verbessern [19, 108]. Neben Kombinationstherapien wie der Radio-Chemotherapie wurden im Rahmen der interdisziplinären Tumorbehandlung neue Verfahrensansätze erprobt, bei denen spezielle Sonden oder Nadeln direkt in das zu behandelnde Tumorgewebe geführt werden. Es entstanden radiologisch-interventionelle Behandlungsmethoden. Gemeinsames Kennzeichen der Methoden ist der minimalinvasive Zugangsweg, der entweder perkutan oder transpulmonal unter örtlicher Betäubung erfolgen kann. Eine Narkose ist in der Regel nicht erforderlich. Verfahren zur Bewertung von minimalinvase Therapieverfahren Verfahren zur Bewertung von Wirkungen Wirkungen Ablationsverfahren Eindimensionale Eindimensionale chemische statische Verfahren dynamische thermische Verfahren Verfahren Verfahren • Äthanolablation Kostenvergleichsrechnun • Kapitalwertmethod Radiofrequenzablation vaskuläre Verfahren Mehrdimensionale Mehrdimensionale • Nutzwertanalys regionale Kurzzeitchemotherapie • Argumentenbilan transpulmonale • endotumorale Chemotherapie • Annuitätenmethod Gewinnvergleichsrechnun Laserablation • Sensitivitätsanalys Chemoembolisation • Rentabilitätsrechnun • Interne Mikrowellenablation • Nutzeneffektkette • stat. • dyn. Ultraschallablation • Kryoablation Abb. 3 Minimalinvasive Behandlungsmöglichkeiten 17 Die minimalinvasiven Methoden werden unterteilt in die vaskulären Verfahren und die Ablationsverfahren. Letztere werden wiederum in die chemischen Ablationsverfahren, zu denen die Äthanolablation gehört, und in die thermischen Ablationsverfahren unterteilt. Bei den gegenwärtig klinisch eingesetzten thermischen Ablationsverfahren wird zwischen hyperthermen Techniken (z.B. Laser- oder Radiofrequenzablation), die den Tumor durch Hitze zerstören, und hypotherme Technik wie der Kryoablation, die die Gewebedestruktion durch Kälte herbeiführt, unterschieden. Die Wahl des jeweiligen Verfahrens richtet sich nach der Größe, Anzahl, Lage und Beschaffenheit des entsprechenden Tumors. Der zerstörte Tumor wird in der Zeit nach dem Eingriff vom Körper abgebaut und das behandelte Gewebe vernarbt. Die Therapiekontrolle erfolgt durch bildgebende Verfahren wie die Magnetresonanz- oder Computertomographie sowie in Einzelfällen durch die Angiographie [19, 32]. Wenn ein Ablationsverfahren zum Einsatz kommt, kann es je nach Größe und Lage der Tumoren notwendig sein, mehrere Sonden gleichzeitig zu verwenden und die Eingriffe zu wiederholen. Ein Vorteil dieser Behandlungstechniken ist, dass sie meist beliebig oft eingesetzt werden können. Sie sind parenchymsparend und im Gegensatz zur Strahlen- oder Chemotherapie treten keine systemischen Nebenwirkungen auf. Ihre Wirksamkeit und Anwendbarkeit ist jedoch überwiegend in Fallserien und kleinen Kohortenstudien untersucht worden, so dass der Stellenwert dieser lokalablativen Verfahren im gesamten onkologischen Behandlungskonzept noch unklar ist [116]. Das älteste noch gebräuchliche Verfahren zur perkutanen Tumorbehandlung ist die Äthanolablation. Bei diesem erstmals 1983 beschriebenen Verfahren zur lokalen Tumordestruktion wird das zu behandelnde Tumorgewebe durch eine Direktinjektion von hochprozentigem Alkohol verödet. Die Injektion des Äthanols führt zu einer Dehydrierung der Zellen, Ausfällen von Eiweiß und Thrombose kleinster Gefäße. Die Folge ist eine Koagulationsnekrose, die anschließend vom Körper abgebaut wird und vernarbt. Je nach Gewebebeschaffenheit, Lokalisation und Tumortyp variiert die Menge des Alkohols. Bei größeren Tumoren kann die mehrfache Behandlung erforderlich werden [79]. Die Tumorbehandlung mittels perkutaner Äthanolablation eignet sich nicht für alle Patienten. Da sich Flüssigkeiten im Gewebe unvorhersehbar verteilen, hat sich die Technik nur bei 18 kapselbildenden Tumoren wie z.B. Metastasen des hepatozellulären Karzinoms (HCC) bewährt. Der zerstörende Alkohol verteilt sich homogen innerhalb des Tumors, gelangt aber nicht in das gesunde Gewebe. Zur Therapie von Metastasen anderer Tumoren hat sich diese Technik bisher nicht bewährt [79]. Die transpulmonale Chemoembolisation (TPCE) ist eine minimalinvasive Therapieform, bei der die Gabe von Chemotherapeutikum und die Embolisation kombiniert werden. Dieses Therapiekonzept ermöglicht die lokale Behandlung direkt an der Metastase, also eine selektive Applikation des Chemotherapeutikums. Dazu wird die Chemotherapie mittels interventioneller Angiographie über eine pulmonale Arterie mit Hilfe eines endovaskulären Ballonkatheters direkt an der Metastase platziert. Das Chemoembolisat besteht aus einem Chemotherapeutikum, einer Mediatorsubstanz zur Verbesserung der Substanzaufnahme sowie einem abbauverzögerndem Mittel. Ein kleiner Ballon an der Katheterspitze verhindert den Weiterfluss des Chemotherapeutikums in die weiterführenden Arterien bzw. in das venöse Abflusssystem [133]. Die transpulmonale Chemoembolisation ermöglicht die Applikation eines hoch dosierten Zytostatikums direkt in die tumorbefallene Lunge, wobei eine systemische Belastung durch die gleichzeitige Embolisation von Gefäßen und damit der Weitertransport des Medikamentes in den Körper weitgehend vermieden werden kann. Schneider et al. verglichen im Jahre 2002 anhand eines Rattenmodells die Wirksamkeit von systemischer Chemotherapie, isolierter Lungenperfusion und Chemoembolisation der Lunge. Dabei erwies sich die Chemoembolisation der intravenösen Chemotherapie als überlegen, die Effizienz von Chemoembolisation und isolierter Lungenperfusion waren vergleichbar [117, 118]. Der Vorteil der Chemoembolisation gegenüber der isolierten Lungenperfusion besteht darin, dass sie perkutan durchgeführt werden kann und somit eine Thorakotomie, wie bei der isolierten Lungenperfusion, nicht nötig ist. Erstmals wurde 2005 eine Studie zur Evaluation der transpulmonalen Chemoembolisation bei Lungenmetastasen in vivo vorgestellt. Von 23 behandelten Patienten konnte bei 26 % ein Wachstumsstop und bei 35 % eine Volumenreduktion der Metastasen beobachtet werden [133]. In der weiterführenden Studie 2008 konnte bei 52 Patienten ein medianes Überleben von 17 Monaten erzielt werden. Besonders gut spricht die TPCE bei Lungenmetastasen von soliden Tumoren wie Schilddrüsen- und Nierenzellkarzinomen an [129]. 19 Der Vorteil dieses Verfahrens besteht in einer geringen Patientenbelastung hinsichtlich der Nebenwirkungen, da eine niedrigere Dosis an Chemotherapeutika ausreicht als bei einer systemischen, intravenösen Therapie. Als unerwünschte Komplikationen können sich Schmerzen, Übelkeit und Fieber nach der Behandlung einstellen. Diese lassen sich aber in der Regel problemlos mit oraler Medikation behandeln. In die Gruppe der selteneren Komplikationen sind der Lungeninfarkt mit sekundärer Pneumonie, der Pleuraerguss, die Atelektase sowie Vergiftungserscheinungen und allergische Reaktionen zu nennen [76]. Weitere Therapieansätze zur perkutanen Tumorbehandlung sind die hyperthermen Verfahren wie Laser-, Radiofrequenz-, Mikrowellen- und Ultraschallablation, die auf der Destruktion durch gezielte Wärmeentwicklung basieren. Eine Zellzerstörung ist bereits bei Temperaturen von 45 – 48 °C möglich, allerdings nur bei Einwirkungszeiten von über einer Stunde. Temperaturen von 50 – 52 °C wirken bereits innerhalb von wenigen Minuten zytotoxisch. Bei 60 °C und mehr tritt die zelltötende Wirkung unmittelbar ein. Diesen Effekt macht sich auch die Radiofrequenzablation (RFA) zu Nutze. Unter CT- oder MRT-Führung werden mittels eines Applikatorsystems eine oder mehrere Elektroden im Zentrum des Tumors positioniert, durch die ein hochfrequenter Wechselstrom (375 – 460 Hz) geleitet wird. Dies führt zu einem starken Temperaturanstieg im Gewebe auf 90 °C bis 120 °C und somit zu einer „Verkochung“ des Tumors [19]. Erstmals beschrieben wurde die Radiofrequenzablation an hepatischen Tumoren 1990 [80, 110]. Drei Jahre später gab es die ersten klinischen Anwendungen [109]. Mittlerweile finden zur Behandlung vor allem von Lebertumoren jährlich deutschlandweit mehrere tausend Interventionen statt [6]. Die erste Radiofrequenzablation pulmonaler Tumoren wurde im Jahre 2000 von der Arbeitsgruppe um Dupuy beschrieben [18]. Seitdem wurden weitere Studien (siehe Tab. 4, Seite 21) veröffentlicht, welche die Durchführbarkeit und Sicherheit des Verfahrens bei der Therapie primärer und sekundärer Lungentumore zeigen. Einheitliche Indikationen sind momentan nicht definiert [45]. Die neusten Publikationen über die Radiofrequenzablation pulmonaler Metastasen präsentieren in kleinen Patientenpopulationen 3-Jahres-Überlebensraten von bis zu 46 %. Die besten Ergebnisse wurden hier in homogenen Patientengruppen mit pulmonalen Metastasen 20 des kolorektalen Karzinoms oder des Nierenzellkarzinoms, die einen Durchmesser unter 3 cm aufwiesen, erzielt [46, 121, 122, 147, 148]. Autor Jahr N M PT Lencioni [74] Gillams [30] 2008 2007 53 37 72 CRC var. 13 (6-48) Yamakado [147] Simon [121] 2007 71 155 CRC 19 (4-42) 2007 189 Okuma [93] 2007 153 18 49 Hiraki [46] Yan [148] Ambrogi [4] Thanos [126] 2007 2006 2006 2006 27 55 54 22 49 var. CRC var.* (24/25) CRC CRC var* var.* (14/8) Lee [72] Vogl [132] 2004 2004 100 64 med. Follow-up (Mon.) 20,1 24 (6-40) 23,7 (6-50) Überlebensraten (in %) 1 2 3 89 66 84 46 70 87 54 78 44 57 96 85 54 64 48 46 med. ÜLZ (Mon) 31 33 33 28,9 Progress Tumore <= 3,5cm: 28% Tumore > 3,5cm: 100% Tumore < 3cm: 11% Tumore 3-6cm: 50% 66 % (local: 38 %) med. Progr. Freies Intervall: 29,2 Monate 30 39 var.* 20 32 var. 3,9 (1-7) 10 CRC Akeboshi [2] 2004 31 54 var. Yasui [149] 2004 35 99 var.* (3/96) 7,1 (1-17) Steinke [122] 2004 23 52 CRC 14,3 (6-28) Morris [85] 2002 20 38 CRC 6,7 (1-13) n= Anzahl der Patienten; M= Anzahl der Metastasen, PT= Primärtumor; * - primäre und sekundäre Lungentumore (Bronchialkarzinom/ Metastasen), med.= median; Mon.= Monate; ÜLZ= Überlebenszeit Tab. 4 Überlebensraten nach Radiofrequenztherapie von Lungenmetastasen Die Komplikationsrate schwankt je nach Studie und wird mit bis zu 76 % angegeben [46, 72, 85, 121, 122, 123, 132, 147, 148, 149]. Typische Komplikationen sind Pneumothorax, Fieber, Hämoptysen, Pleuraerguss, Empyem und Hämatothorax. Als Vorteile der Radiofrequenzablation der Lunge gelten die einfache Handhabung sowie die Möglichkeit der Direktpunktion der Läsion innerhalb der Lunge mit vereinfachter Manipulation. Ein wesentlicher Nachteil ist die Impedanzproblematik und die kleinen Ablationsvolumen mit den derzeit zur Verfügung stehenden Systemen [132]. Die perkutane Mikrowellenablation (PMA), auch Mikrowellenkoagulationstherapie genannt, ist ebenfalls ein Verfahren, dessen Wirkungsmechanismus auf einer Koagulation mit lokaler Hitzeerzeugung beruht. Die Therapie erfolgt in der Regel in einer Frequenz von 900 bis 2.450 MHz, bei einer Zeitdauer von 60 Sekunden und befindet sich in einer frühen klinischen Phase [95]. Bisher wird die Mikrowellenablation vornehmlich zur Behandlung kleiner HCC eingesetzt [78, 119]. 21 Für die Anwendung bei Lungenmetastasen liegen derzeit nur kleine Kohortenstudien vor. Die chinesische Arbeitsgruppe um Wen He veröffentlichte 2006 Daten über eine Behandlungsserie von 12 Patienten. In einem Nachbeobachtungszeitraum von 6 – 40 Monaten (Median: 20 Monate) überlebten 7 Patienten ohne schwere Komplikationen, 5 Patienten starben an der Metastasierung. In allen Fällen konnte eine Größenreduktion erzielt werden [44]. Wolf et al. [143] publizierten 2008 eine Studie über 50 Patienten mit insgesamt 82 Lungenmetastasen. Bei einem medianen Follow-up von 10 Monaten wurde von 1-, 2- und 3-JahresÜberlebensraten von 65 %, 55 % und 45 % berichtet. Gegenüber der Radiofrequenzablation bietet die Ablation mit Mikrowellen den Vorteil, dass sie eine Behandlung mit höheren Temperaturen erlaubt und weniger abhängig vom Kühleffekt ist, den Gefäße in der behandelten Region ausüben. Allerdings erreicht dieses Verfahren nur kleine Abtragungsvolumen, so dass bei Tumoren > 2 cm multiple Applikationen notwendig sind. Weiterhin sind Mikrowellenablationssysteme bisher nicht kommerziell erhältlich und die bisherigen Studien wurden mit Prototypen durchgeführt. Hoch intensiver fokussierter Ultraschall (HIFU) ist eine weitere minimalinvasive Methode zur Thermoablation von Geweben. Durch MRT-gesteuerte Fokussierung des eingestrahlten Ultraschalls auf ein kleines Zielvolumen kann im Gewebe innerhalb weniger Sekunden eine Temperatur von 55–90 °C erreicht werden. Diese lokale Hitzeeinwirkung führt im Zielvolumen zur Denaturierung von Proteinen und irreversibler Zellschädigung, ohne das umgebende Gewebe zu schädigen. Trotz ermutigender Ergebnisse bei Mammakarzinomen, HCC und Osteosarkomen befindet sich der fokussierte Ultraschall noch im experimentellen Stadium und wird bisher nicht bei primären oder sekundären Lungentumoren angewendet [144, 145]. Im Gegensatz zu den hyperthermen Therapiekonzepten, bei denen die Gewebedestruktion durch Hitze herbeigeführt wird, erfolgt bei hypothermen Verfahren wie der Kryoablation die Gewebezerstörung durch schnelle Abkühlung des Gewebes. Die Bildung von intra- und extrazellulären Eiskristallen bei Temperaturen zwischen -50 °C und -150 °C bewirkt eine hyperosmolare Umgebung und führt zu einer Dehydrierung der Zellen, Denaturierung von Enzymen und verschiedenen Zelldysfunktionen. Es kommt dadurch zu einer irreversiblen Austrocknung und Zerstörung der Zellen sowie zum Verschluss kleinster Arterien und Venen [142]. 22 Erste klinische Ergebnisse der Kryoablation sind vielversprechend. Kawamura et al. [60] berichten von einer Behandlungsserie an 20 Patienten, bei der in 22 Sitzungen 35 pulmonale Metastasen mittels Kryoablation therapiert wurden. Die 1-Jahres-Überlebensrate dieser Gruppe betrug 89,4 %. In einem medianen Follow-up von 21 Monaten wurde bei 35 % der Patienten ein lokales Rezidiv beobachtet. Der Vorteil dieser Therapie liegt in der fast völligen Schmerzfreiheit, da die Kälte eine schmerzstillende Wirkung hat und eine zusätzliche Schmerzbekämpfung nicht erforderlich ist. Die Ausdehnung der Kälte bzw. des gefrorenen Tumors kann durch die Magnetresonanztomographie sehr gut dargestellt werden und somit ist eine hohe Präzision der Gewebezerstörung während der Behandlung möglich. Die Nachteile des Verfahrens sind gegenüber den hyperthermen Therapiekonzepten die höheren Nebenwirkungsraten. Als Komplikation wird das sogenannte „Ice-cracking“ beschrieben, bei dem es durch unterschiedliche Ausdehnung und Spannung oder durch Bewegung der Kryosonden zum Bruch des Eisballes mit Einblutungen kommen kann [97]. Weiterhin werden auch hier vor allem Pneumothorax und Hämoptysen genannt [60]. Ausreichende Langzeitergebnisse für eine differenziertere Aussage über den Stellenwert der Kryoablation in der Behandlung pulmonaler Metastasen stehen noch aus. 23 1.3 Die Laserablation als minimalinvasive Behandlungsmethode von Lungenmetastasen 1.3.1 Entstehungsgeschichte der Laserablation Die Laserablation, auch laserinduzierte Thermotherapie (Laser-induced thermotherapy, LITT) genannt, ist eine minimalinvasive Behandlungsmethode zur lokalen Tumordestruktion. Dieses phototermische Verfahren wurde 1983 erstmals als neue Behandlung von benignen und malignen Tumoren alternativ zur chirurgischen Intervention von Stephen G. Bown in seinem Artikel „Phototherapy of tumors“ beschrieben und 1993 nach umfangreichen präklinischen Studien erstmalig am Menschen zur Behandlung von malignen Lebertumoren eingesetzt [9, 19, 131, 153]. Ergebnisse der jüngsten Vergangenheit haben gezeigt, dass sich dieses Therapieverfahren sehr gut für die Behandlung primärer und sekundärer Lebertumore eignet [19, 75, 153]. Aber auch in der Therapie von Tumormanifestationen an der Niere, in der Kopf-Hals-Region und an Lymphknoten hat sich die Laserablation in den letzten Jahren bewährt und wird nun auch in der Therapie von Lungenmetastasen eingesetzt [132, 153]. Erstmals 1996 veröffentlichten Fielding et al., aus der Arbeitsgruppe um S.G. Bown, eine tierexperimentelle Studie zur Laserablation an der Lunge. Es wurden Ergebnisse von perkutan durchgeführten Thermotherapien an gesunden Ratten publiziert [22]. 1998 erschien eine ähnliche Studie [23] und 2001 wurde über Versuche an Schweinelungen berichtet [24]. In allen Studien konnte eine technische Durchführbarkeit der Laserablation an Lungengewebe gezeigt werden [22, 23, 24, 25]. Die erste Behandlungsserie an Patienten wurde von unserer Gruppe im Universitätsklinikum der Ernst-Moritz-Arndt-Universität erfolgreich durchgeführt und die Ergebnisse 2003 veröffentlicht [54]. 24 1.3.2 Technische Grundlagen Der Laserablation liegt das gleiche Wirkprinzip wie allen hyperthermen Verfahren zu Grunde. Durch eine lokale Gewebeerhitzung kommt es zur Ausbildung von Koagulationsnekrosen. Die lokale Gewebeerhitzung wird bei der Laserablation über Laserlicht erzeugt, das über einen interstitiell im Tumor platzierten Applikator direkt in das zu therapierende Tumorgewebe eingebracht wird. Dort kommt es durch Absorption der Photonen zur Erwärmung des Gewebes und damit zur letalen Zellschädigung. Das Verfahren kann meist ohne Operation in Lokalanästhesie und Sedierung durchgeführt werden und stellt so eine schonende Behandlung dar. Vor allem für Patienten mit kardinalen, pulmonalen, hepatischen oder renalen Begleiterkrankungen, für die nur eingeschränkte Behandlungsalternativen existieren, ist die Laserablation eine interessante Erweiterung der Therapieoptionen. Abb. 4 Aufbau eines gekühlten Applikators und Wirkungsprinzip der Laserablation Grundlage der Laserablation ist die klassische Hyperthermie. Die Wirkung des Laserlichts ist gewebeabhängig und wird beeinflusst durch die Absorption und Wärmeleitfähigkeit in unterschiedlichen Gewebeschichten (Atemluft, Blutfluss, gesundes Lungengewebe, solider Tumor). Gesundes und neoplastisches Gewebe weisen eine unterschiedliche Wärmetoleranz 25 auf. Im Vergleich zu normalen Zellen haben maligne Zellen aufgrund ihres veränderten Stoffwechsels hypoxiebedingt eine höhere Temperaturempfindlichkeit und eine geringere Fähigkeit zur Reparatur von Zellschäden. Temperaturen von mindestens 42°C führen zu einer Wachstumsverzögerung der Tumorzellen und lösen einen zytotoxischen Effekt aus. Die temperaturabhängigen Gewebewirkungen des Laserlichts führen zu einer Enzyminduktion, Ödemausbildung und Membranauflockerung in einem Temperaturbereich von 42 °C bis 45 °C. Ab 60 °C resultiert infolge der Hitzeeinwirkung eine Proteindenaturierung, die zu letalen Zellschädigungen führt. Die letalen Zellschädigungen lösen eine Koagulation der Tumorzellen aus und bilden letztendlich eine Nekrose. Ab 80 °C erfolgt eine Kollagendenaturierung bis hin zur Karbonisation bei 150 °C. Entscheidend für den Erfolg der Laserablation ist ein ausreichender Koagulationseffekt über die gesamte zu behandelnde Metastase [130]. Um die vollständige Koagulation einer dreidimensionalen Tumorgeometrie zu erzielen, muss ein annährend sphärisches Gewebevolumen gleichmäßig erhitzt werden. Aus diesem Grunde sind Applikationssysteme entwickelt worden, die eine gleichmäßige zirkumferente Abstrahlung ermöglichen [130]. Als Energiequelle dienen am häufigsten Neodym dotierte Yttrium-Aluminium-Grant-Laser (Nd:YAG-Laser). Diese Laser haben den Vorteil, dass sie aufgrund ihrer Wellenlängen von 1064 bzw. von 900 nm, die nahe dem infraroten Bereich liegen, eine besonders gute Tiefenwirkung in biologischen Geweben und gute Koagulationseigenschaften aufweisen [19, 130, 153]. Die Therapieplanung der Laserablation ist aufwendig, da die zu erwartende Schädigungszone von verschiedenen Parametern in komplexer Weise abhängt. Einflussfaktoren sind dabei die Laserleistung, Kühlrate an der Applikatorspitze, Bestrahlungszeit, Applikatorgeometrie, optische und thermische Gewebeparameter wie Gewebeperfusion und Blutfluss durch größere Gefäße sowie der Ventilationsgrad des zu therapierenden Lungenareals. Durch mehrfache technische Verbesserungen der Interventionskatheter und der Laserapplikatoren gelang es in den letzten Jahren, die laserinduzierte Gewebenekrose stetig zu präzisieren und zu vergrößern. Je nach Größe und Anzahl der zu therapierenden Tumoren muss unter Umständen das Volumen der Nekrosen gesteigert werden. Dazu kommen Multi-Applikator-Anwendungen 26 zum Einsatz, mit denen bis zu vier Laserapplikatoren simultan in einer großen Metastase oder mehreren kleinen Metastasen eingesetzt werden können [130]. Durch die zahlreicheren Punktionen bringt diese Technik jedoch auch eine erhöhte Belastung und ein vermehrtes Risiko für den Patienten mit sich, so dass die Applikatorzahl generell so gering wie möglich gehalten werden sollte [19]. Der maximale Durchmesser einer Nekrose, der durch eine Behandlung erreicht werden kann, ist jedoch durch den Blutfluss limitiert, der einen Teil der Wärme abführt [153]. Die Computertomographie stellt aktuell das Goldstandardverfahren im klinischen Einsatz zum Monitoring der Applikatorplatzierung dar. Sie bietet eine sehr schnelle und gute Bilderstellung zur Kontrolle der Behandlung und der Erkennung von möglichen Komplikationen sowie zur Beurteilung des Therapieerfolges. Vor allem bei der Erkennung und Beherrschung eines therapieinduzierten Pneumothorax ist sie der Magnetresonanztomographie bisher überlegen. Des Weiteren bietet sie beim Follow up eine sehr gute Vergleichbarkeit. Zukünftig scheint eine Nutzung der Magnetresonanztomographie und ihrer vorteilhaften Thermometrie zur noch exakteren Kontrolle der Ablationszone durch die Weiterentwicklung der Geräte und Programme sowie der MRT-geeigneten Applikatorsysteme nahe, was das Problem einer möglicherweise hohen Strahlenbelastung bei Langzeitpatienten deutlich reduzieren würde. Dies wäre gerade bei Patienten in jüngerem Alter wünschenswert. Limitierend wirkt bei der MRT allerdings die Tatsache, dass sich keine Metallgegenstände im Körper befinden dürfen, die sich erwärmen oder zu einer Magnetfeldabweichung führen können. In solchem Falle muss auf andere Verfahren der Bilderzeugung zurückgegriffen werden [21]. 27 1.3.3 Bisherige klinische Erfahrungen Erstmals publizierten Hosten et al. [54] im Jahre 2003 eine erste Serie von 10 Patienten, deren Lungenmetastasen unter Anwendung der Laserablation therapiert wurden. Mittels eines eigens entwickelten Punktionssystems und dem Einsatz eines Nd:YAG-Lasers konnten maximal zwei pulmonale Absiedlungen pro Patient behandelt werden, im Mittel wurde eine Leistung von 12 W über 20 Minuten appliziert. Als Zeichen der vollständigen Ablation und somit der erfolgreichen Behandlung wurde eine fehlende Kontrastmittelanreicherung der Metastase in der CT-Bildgebung gewertet. Aufgrund zu kurzer Verlaufsbeobachtungen waren aber die Angaben zum Behandlungserfolg noch ungenau. Schwerwiegende Komplikationen traten während den Behandlungssitzungen nicht auf. Die technische Machbarkeit der Therapie für Patienten mit Lungenmetastasen war nachgewiesen und musste nun in künftigen Behandlungsserien weiter evaluiert werden. Erste fortführende Ergebnisse wurden 2004 von Weigel et al. [136] aus derselben Arbeitsgruppe veröffentlicht. Anhand von 30 Patienten mit 42 behandelten pulmonalen Metastasen konnte die klinische Durchführbarkeit des Verfahrens weiter belegt werden. In dieser Studie wurde festgestellt, dass zentral lokalisierte Metastasen im Gegensatz zur videoassistierten Thorakoskopie (VATS) besser als periphere Metastasen behandelt werden können. Aussagen über langfristige Behandlungserfolge, die mit dem Verfahren zu erzielen sind, konnten aber aufgrund zu kurzer Nachbeobachtungszeiträume noch nicht getroffen werden. Ebenfalls im Jahre 2004 publizierten Vogl et al. [128] eine Behandlungsserie, in der bei 24 Patienten 38 Lungenmetastasen unterschiedlicher Primärtumore und 6 Patienten mit einem Bronchialkarzinom behandelt wurden. Eine vollständige Ablation gelang bei den Patienten mit Lungenmetastasen in 74 % (28/38) aller Fälle, bei den Patienten mit Bronchialkarzinom zu 100 % (6/6). Die 3-Monats-Verlaufskontrolle mittels CT/MRT zeigte eine Tumorkontrollrate von 80 %. Ein Größenprogress wurde bei 9 (21 %) und eine Regression bei 3 Tumoren (7 %) beobachtet. In 4 Fällen (9 %) wurde ein Rezidiv der schon behandelten Läsionen festgestellt. Neue Lungenherde unabhängig von den therapierten Tumoren traten bei 7 Patienten (16 %) auf. Auch in dieser Publikation konnten aufgrund des zu kurzen Nachbeobachtungszeitraums noch keine validen Daten zum Langzeitüberleben angegeben 28 werden. Es wurden aber erstmals Indikationenstellungen für die Laserablation von Lungentumoren beschrieben: • Inoperabilität der Patienten aufgrund schlechter Lungenfunktion, fortgeschrittener Tumorerkrankung oder kardiopulmonaler Begleiterkrankungen • fehlendes Ansprechen auf konventionelle Therapieverfahren • max. Anzahl der Herde pro Lunge: 3 • max. Größe der Herde: 3 cm • Distanz der Herde zu vitalen Gefäß- und Bronchialstrukturen mindestens 1 cm • Pro Sitzung sollte nur eine Lungenhälfte behandelt und die kontralaterale Seite erst nach vollständigem Abklingen eines möglicherweise induzierten Pneumothorax oder Pleuraergusses angegangen werden. Noch im gleichen Jahr setzten Vogl et al. [132] in einer weiteren Publikation die maximale Obergrenze der Metastasengröße auf 5 cm hoch. Auch Weigel et al. [137] veröffentlichten 2006 weitere Erfahrungen mit dem Einsatz der Laserablation und berichteten von einem Tumorprogress bei 20 % (13/64) aller behandelten Lungenmetastasen. Der Stellenwert der Laserablation zur Behandlung von Lungenmetastasen ist im Vergleich zu den jeweiligen Standardtherapien weiterhin unklar, so dass diese Therapieform derzeit noch als experimentelles Verfahren innerhalb von Studien angesehen werden muss. Dementsprechend wurde die Laserablation vom Untersuchungsausschuss „Ärztliche Behandlung“ des Gemeinsamen Bundesausschusses der Anlage B (nicht anerkannte Untersuchungs- und Behandlungsmethoden) der BUB-Richtlinien zugewiesen. Der vom Bundesministerium für Gesundheit und Soziale Sicherung nicht beanstandete Beschluss ist seit dem 13.01.2006 in Kraft [153]. 29 1.3.4 Komplikationen Wie bei jedem medizinischen Eingriff sind auch bei der Laserablation bestimmte unerwünschte Komplikationen nicht auszuschließen. Dabei sind vor allem die Punktionsrisiken zu nennen. Die häufigste Komplikation im Zusammenhang mit der perkutanen Lungenpunktion ist der Pneumothorax. Weiterhin können während des Eingriffs Blutungen und Hämatome aufgrund von Gefäßverletzungen entlang des Stichkanals entstehen. Auch benachbarte Organe oder Nerven können beschädigt werden [107, 108, 125, 128, 132, 136, 137, 138]. Eine zusätzliche mögliche Komplikation ist die Infektion. Selbst bei sorgfältiger und korrekter Durchführung des Eingriffs kann es nicht ausgeschlossen werden, dass es in seltenen Fällen zu einer Infektion der Haut, des Zugangsweges durch die Brustwand oder der Lunge selbst kommt. Eine Antibiotika-Therapie kann in diesen Fällen notwendig werden. Seltener treten eine Fistelbildung oder ein Abszess aufgrund einer Infektion am Ort des abgetöteten Tumors, allergische Reaktionen und/ oder Störungen des Herz-Kreislauf-Systems auf. Nicht unerwähnt bleiben darf die sehr seltene Verschleppung von Tumorzellen entlang des Punktionskanals (Stichkanalmetastasensetzung). Eine ebenfalls sehr seltene, schwerwiegende Komplikation, die nicht ganz ausgeschlossen werden kann, ist die Embolie. Bei der Embolie bildet sich ein Blutgerinnsel in einem Lungengefäß in der Nähe der zu behandelnden Metastase. Diese Embolie kann mit dem Blutstrom fortgeschwemmt werden, zu einem Ausfall von anderen Organen oder in schwerwiegenden Fällen zu einem Herz- oder Hirninfarkt führen. Neben den Punktionsrisiken gibt es auch thermische Gefahren. So können durch die Erwärmung des Gewebes mittels Lasertechnik thermische Schäden in der Haut und im gesunden Gewebe der Lunge sowie in anliegenden Organen verursacht werden [21, 77]. 30 1.3.5 Vorteile der Laserablation Der Vorteil der Laserablation liegt in der zielgenauen Erzeugung einer Koagulationsnekrose bei größtmöglicher Schonung der umliegenden Strukturen. Der zu behandelnde primäre oder sekundäre Tumor kann zerstört werden, während das umgebende Organgewebe aber weitgehend erhalten bleibt. Besonders bei bereits an der Lunge voroperierten Patienten bietet die Laserablation somit eine Alternative zur chirurgischen Therapie, da die verbliebene Lungenfunktion einen limitierenden Faktor für eine weitere Organresektion darstellt. Ein weiterer Vorteil beruht auf der perkutanen Platzierung des Laserapplikators unter Lokalanästhesie. Durch den schonenden Eingriff können auch Patienten therapiert werden, die aufgrund ihrer Gesamtsituation (Herz-Kreislauf-Erkrankungen, Multimorbidität) für eine Vollnarkose und Operation nicht infrage kommen. Das Verfahren ist auch beim Auftreten mehrerer Metastasen und Rezidive sehr geeignet. Da es nahezu beliebig oft wiederholbar ist, können diese hintereinander oder in einigen Fällen auch zeitgleich lokal therapiert werden. Desweiteren sind die geringen Komplikationsraten und auch die dadurch bedingten niedrigen Hospitalisierungzeiten sowie die geringeren Kosten im Vergleich zur Lungenteilresektion zu den Vorteilen zu zählen [130]. 31 1.4 Zielsetzung Auch wenn zur Laserablation zuverlässige Zahlen zum technischen Erfolg vorliegen, existieren klinische Langzeitergebnisse vor allem über den Einfluss auf die Überlebenszeiten der Patienten derzeit nur in unzureichendem Maße. Da Patienten häufig nicht an ihrem Primärtumor, sondern an den Folgen der Lungenmetastasierung sterben, ist es von großer Bedeutung die Frage zu klären, inwieweit die Lasertherapie die Überlebenszeit eines nicht operablen oder anderweitig therapierbaren Patienten verlängern kann und dieser somit von der Behandlung profitiert. In der vorliegenden Arbeit werden die folgenden Fragen näher untersucht. 1.) Welche Überlebenszeiten und Rezidivraten können in einer Patientengruppe mit der Laserablationstherapie erreicht werden? Profitiert ein Patient von dieser Therapie und ist dies abhängig von dem Primärtumor? 2.) Wie viele der abladierten Läsionen konnten erfolgreich behandelt werden? 3.) Wie hoch ist die Rezidiv-/ Progressrate in Abhängigkeit von der Größe und Anzahl sowie der Primärtumorentität? 4.) Wie häufig sind das Auftreten von Komplikationen und die Notwendigkeit einer Folgetherapie? 32 2 MATERIAL UND METHODEN 2.1 Patientenkollektiv 2.1.1 Geschlechterverteilung Insgesamt wurden 64 Patienten zwischen Februar 2001 und März 2007 aufgrund einer Lungenmetastasierung mit der perkutanen Laserablation in der Radiologischen Abteilung des Universitätsklinikums Greifswald therapiert. Es waren 36 Patienten männlichen (56 %) und 28 weiblichen (44 %) Geschlechts. Das Geschlechterverhältnis betrug somit 1,3 : 1. 2.1.2 Altersverteilung Das Alter der Patienten lag zum Zeitpunkt des Therapiebeginns zwischen 19 und 82 Jahren, das mediane Alter der Gesamtgruppe (n=64) betrug 66 Jahre. Zur Veranschaulichung der Alterstruktur wurde eine Aufteilung in einzelne Altersklassen vorgenommen. Die Abbildung 5 gibt die Verteilung auf die einzelnen Altersklassen und das jeweilige Geschlecht im untersuchten Patientengut wieder. 25 gesamt 20 männlich 20 weiblich 17 15 12 11 12 10 10 8 5 8 9 6 4 5 2 3 1 0 <50 50-59 60-69 70-79 Alter in Jahren Abb. 5 Altersstruktur und Geschlechtsverteilung (Die Ziffern auf den Säulen entsprechen der Anzahl der Patienten) 33 >=80 2.1.3 Art des Primärtumors Im Patientenkollektiv fanden sich Lungenmetastasen unterschiedlicher Primärtumorentitäten. Mit 20 Fällen (31 %) war das kolorektale Karzinom als Primärtumor am häufigsten vertreten, gefolgt von pulmonalen Metastasen des Nierenzellkarzinoms mit 16 % (n=0), von HalsNasen-Ohren-Tumoren mit 11 % (n=7), des Melanoms mit 9 % (n=6) und des Mammakarzinoms mit 6 % (n=4). Aufgrund zu geringer Fallzahlen wurden die übrigen Primärtumore (Anzahl <= 3) unter der Angabe „sonstige Karzinome“ zusammengefasst. In dieser Gruppe waren Patienten mit einer pulmonalen Metastasierung gynäkologischer Karzinome (n=3), des NSCLC (n=3), des Sarkoms (n=3), des Schwanoms (n=2), des Hepatozellulären Karzinoms (n=1), des Schilddrüsenkarzinoms (n=1), des Neuroendokrinen Karzinoms (n=1), des Oesophaguskarzinoms (n=1) sowie des Blasenkarzinoms (n=2) enthalten. sonstige Tumore; 27% Colon-Ca.; 31% Malignes Melanom; 9% Mamma-Ca.; 6% Nierenzell-Ca.; 16% HNO-Tumore; 11% Abb. 6 Prozentuale Verteilung der Primärtumore Alle Patienten erhielten vor der Lasertherapie eine onkologische Behandlung ihrer Primärtumorerkrankungen in Form einer chirurgischen Resektion, einer Chemo- und/oder einer Strahlentherapie. 34 2.1.4 Lokalisation der Metastasen Bei 24 der insgesamt 64 Patienten (38 %) bestand vor Beginn der Lasertherapie eine extrapulmonale Metastasierung. Die intrapulmonalen Metastasen wurden zur Planung des Zugangsweges in eine zentrale, periphere, apikale oder basale Lokalisation in der Lunge differenziert. 2.1.5 Anzahl der Metastasen 36 % der Patienten (n=23) zeigten eine solitäre Metastase. 41 der 64 Patienten (64 %) wiesen einen multiplen Befall auf. Davon hatten 27 % der Patienten zwei oder drei Metastasen und 37 % mehr als drei Metastasen. Die mittlere Anzahl pro Patient betrug 2,0 (Bereich: 1 bis 33). Abbildung 7 fasst die Metastasenbelastung im Patientenkollektiv zusammen. 30 Patientenanzahl 25 24 23 20 17 15 10 5 0 1 2-3 Anzahl der Metastasen >3 Abb. 7 Absolute Metastasenhäufigkeit im Patientenkollektiv Im gesamten Patientenkollektiv wurden 108 Lungenmetastasen behandelt. Bei 69 % der Patienten (n=44) wurde eine, bei 20 % der Patienten (n=13) zwei bzw. drei und bei 11 % der Patienten (n=7) mehr als drei pulmonale Metastasen therapiert. 35 Abbildung 8 fasst die Anzahl der behandelten Lungenmetastasen im Patientengut zusammen. 50 45 44 Patientenanzahl 40 35 30 25 20 15 11 10 2 5 3 2 1 0 1 7 8 0 1 2 3 4 5 6 Anzahl behandelter pulmonaler Metasten Abb. 8 Anzahl behandelter pulmonaler Metastasen 2.1.6 Größe der behandelten Metastasen Der Durchmesser der behandelten Läsionen betrug zwischen 0,4 und 8,5 cm (Median 2,0 cm). Dabei waren 69 Lungenherde (64 %) kleiner als 3 cm, 33 (30 %) zwischen 3 und 5 cm und 6 Lungenherde (6 %) größer als 5 cm. > 5cm: 6(6%) 3-5 cm: 33 (30%) <3 cm 69(64%) Abb. 9 Prozentuale Verteilung nach Tumorgröße 36 2.2 Einschlusskriterien Eingeschlossen in das Studienprotokoll wurden Patienten, bei denen eine operative Behandlung der Lungenmetastasen nicht möglich war, oder die eine chirurgische Metastasenresektion abgelehnt hatten. Dabei mussten folgende Kriterien zutreffen: • Nachgewiesene Metastasierung der Lunge (Entweder bioptisch gesichert oder Auftreten eines metastasentypischen Lungenherdes bei bekanntermaßen in die Lunge metastasierenden Primärtumor, wobei der Herd in CT-Voruntersuchungen nicht abzugrenzen war.) • Fehlen von verfassungsbedingten oder medizinisch-induzierten Koagulopathien • Thrombozyten-Anzahl > 50.000/ µl • PTT < 50 sek • Quickwert > 50 % • Karnofsky-Index > 60 % • Mindestalter 18 Jahre • Unterschriebene Einverständniserklärung Die Diagnose eines Lungenemphysems stellte kein Ausschlusskriterium dar. Alle Patienten unterzeichneten vor der ersten Behandlung nach einem ausführlichen Aufklärungsgespräch eine von der Ethikkommission des Universitätsklinikums Greifswald bestätigte Einwilligungserklärung. Die Patienteninformation beinhaltete ausführliche Informationen über die Risiken und Nebenwirkungen der Laserablation und die Aufklärung über den experimentellen Therapiecharakter als Positionierung des Verfahrens in der Krebstherapie. 37 2.3 Technische Durchführung 2.3.1 Applikatorsystem Bei der Laserablation wurde ein miniaturisiertes, intern gekühltes Applikatorsystem verwendet (Monocath, Trumpf Medizinesysteme, Umkirch Germany). Es besteht aus einer 5,5 French Teflon-Kanüle, mit darin enthaltenem Titanmandrin für die Platzierung der Kanüle. Das Titanmandrin wird nach Erreichen der richtigen Position in der Metastase durch einen Hüllkatheter mit der optischen Laserfaser ersetzt. Die Teflonkanüle und der Hüllkatheter verhindern während der Laserung einen direkten Kontakt von Gewebe und Laserfaser, so dass im Falle eines Schadens an der Faser diese vollständig mit dem Hüllkatheter entfernt und die Sitzung mit einer neu eingeführten Faser beendet werden kann. Diese spezielle Lichtleitfaser, mit einer Gesamtlänge von 12 m, dient zur symmetrischen Bestrahlung von Volumengewebe mit Laserlicht. Hierzu besitzt die Faser an ihrem distalen Ende einen Streuapplikator, der über die Applikatorlänge die Laserlichtleistung gleichmäßig radial und axial abstrahlt. Diese sogenannte Diffusor-Spitze steht in verschiedenen Längenausführungen zur Verfügung (1, 2, 2,5 und 3 cm). Um die Metastasen möglichst optimal zu erreichen ist die Kanüle ebenfalls in unterschiedlichen Längen verfügbar (12, 14, 16 und 18 cm). Als verwendete Energiequelle diente ein Neodym dotierter YttriumAluminium-Grand-Laser (Nd:YAG-Laser) mit einer Wellenlänge von 1064 nm. Aufgrund dieser Wellenlänge, die nahe dem infraroten Bereich liegt, werden eine besonders gute Tiefenwirkung in biologischen Geweben und gute Koagulationseigenschaften erreicht [19, 130]. Betrieben wurde der Laser von einem Nd:YAG Lasergenerator (Dornier, Wessling). a b Abb. 10 Applikatorsystem. a: Titanmandrin (oben) und Teflonkanüle mit eingeführtem Hüllkatheter und Laserfaser (unten). b: Teflonkanüle (oben) und Hüllkatheter mit Laserfaser (unten) 38 2.3.2 Planung/ Platzierung Alle Ablationssitzungen wurden CT-gestützt durchgeführt. Während der Therapie wurden zum Monitoring der sichtbaren Gewebseffekte CT-Scans mit einer Schichtdicke von 2,5 mm, 120 kV und 60 mA durchgeführt. Diese dienten ebenfalls zur Kontrolle möglicher Komplikationen. Je nach Größe und Lage der zu therapierenden Metastase wurden entweder ein Applikator verwendet, eine Doppelapplikation durchgeführt oder drei Applikatoren eingebracht, wodurch eine simultane Mehrfachlaserung ermöglicht wurde. a b c d Abb. 11 Platzierung des Applikators. Metastasen bis 2 cm werden durch Einfachapplikation „aufgespießt“ (a), sehr kleine Metastasen werden von zwei Applikatoren flankiert (b). Bei Metastasen > 2 cm wird eine parallele Doppelapplikation (c) oder eine Mehrfachapplikation (d) notwendig. 39 Bei einer Tumorgröße bis 2 cm wurde ein Applikator benutzt, der in der Mitte der Metastase platziert wurde und zwei sich gegenüberliegende Ränder perforierte. War eine Metastase zu klein um eine Perforation zu ermöglichen, wurden 2 Applikatoren verwendet, die die Läsion an den Rändern flankierten. Ab einer Tumorgröße von mehr als 2 cm wurde mit 2 Applikatoren parallel oder sich in der Läsion kreuzend therapiert. Wenn mehrere Applikatoren simultan zum Einsatz kamen, überlappte sich die ellipsoide Wirkungszone mit der Länge der aktiven Spitze und einem veranschlagtem Maximum von 2,5 cm. Diese Therapieparameter waren standardisiert und stimmten mit den Erkenntnissen aus frühen exvivo und in-vivo Experimenten überein [54, 62]. Nach regelrechter Platzierung des Applikators und Einführung der Laserfaser wurde die applizierte Wattleistung in Schritten von 2 W/min gesteigert. Nach ca. 15 Minuten wurde unter Berücksichtigung des Wärmeabtransportes durch die Belüftungs- und Durchblutungssituation der Lunge eine maximale Energie von ca. 14 W am Zielort erreicht. Der totale Energiebetrag, der pro Ziel appliziert wurde, lag zwischen 7,4 und 68 W (Mittel 20 W). 2.3.3 Verfahrensweise Die perkutane Laserablation wurde bei allen Patienten unter sterilen Bedingungen, Lokalanästhesie (Lidocain 1 %) und Analgosedierung (10 ml Haloperidol, 20 mg Metoclopramide und 100 mg Pethidin als langsame Infusion in 500 ml NaCl-Lösung), durchgeführt. Über den gesamten Zeitraum der Sitzung wurde der Patient mittels EKGMonitoring überwacht. Bei Notwendigkeit war eine Sauerstoffgabe jederzeit möglich. Die Lagerung des Patienten auf dem CT-Tisch erfolgte je nach Planung des optimalen Zugangsweges anhand der CT-Voruntersuchungen in Rücken-, Seit- oder Bauchlage. Die Kriterien des optimalen Zugangsweges beruhten dabei auf der Lage der Läsion in der Nähe zur Pleura und in der Beziehung zu den großen Gefäßen, wie Pulmonalarterien und –venen, sowie zum Bronchialsystem. Dabei wurde ein breitflächiger Kontakt des Laserapplikators zum Tumorvolumen erreicht, um einen größtmöglichen Effekt zu erzielen. Nach Hautdesinfektion und sterilem Abdecken wurde die Lokalanästhesie im Zugangsgebiet durch Infiltration der Subkutis, des Rippenperiostes und der parietalen Pleura durchgeführt. 40 Darauf folgend begann die Positionierung des Teflonkatheters mittels des darin enthaltenden Titanmandrins. Wurde die gewünschte Position erreicht und durch CT-Monitoring bestätigt, wurde der Mandrin entfernt und der Hüllkatheter mit der flexiblen Laserfaser eingeführt. Nach erneuter Ortskontrolle und Erreichen der angestrebten Lage in der Metastase erfolgte der Anschluss an den Nd:YAG Laser und die Applikation der entsprechenden WattLeistungen. Nach Beendigung der Lasersitzung wurden alle eingeführten Fremdkörper entfernt. Um einen relevanten Pneumothorax und Blutungen ausschließen zu können, wurde ein abschließender CT-Scan durchgeführt. Toleriert wurden kleine und lokal auftretende pleurale Lufteinschlüsse, nur ein größerer oder instabiler Pneumothorax wurde mittels 14F-Drainage (Pneumocath) behandelt. Alle Patienten erhielten 4 Stunden nach der Therapie eine RöntgenThorax-Kontrolle sowie regelmäßige Herz-Kreislauf-Kontrollen auf einer Krankenstation. Jeder Patient wurde mindestens 48 Stunden nach Therapieende stationär überwacht. 2.3.4 Behandlungsevaluation und Follow-up Die postinterventionelle Untersuchung wurde durchgeführt mittels eines Spiral-CT-Scanners in Einfach- oder Multischichtspiraltechnik (8-Zeilen LightSpeed, 1-Zeilen HiSpeed vor 2005, beide GE Medical Systems, Solingen, Deutschland; 16-Zeilen Sensation, Siemens, Erlangen, Deutschland) unter Verwendung eines standardisierten intravenösen Kontrastmittelinjektionsprotokolls (Röhrenspannung 120 kVp, 5 mm großen, überlappenden Schichten, Stromstärke der Röhre 80-120 mA, 27-35 g Jod, Accupaque 350 oder Visipaque 270, injiziert mit einer Flussrate von 0,9 – 1,3 mg Jod/ sek, injiziert mit einem Delay von 25 Sekunden). Die Behandlungen sowie Vor- und Nachuntersuchungen wurden unverblindet und im Konsens von drei erfahrenen interventionellen begutachtet. Zur Beurteilung des Behandlungserfolges wurde ein kontrastmittelverstärktes CT, das am ersten Tag nach der Behandlung erstellt wurde, begutachtet. Die technisch erfolgreiche Ablation wurde definiert durch Nachweis einer Koagulationszone, die aus einer dünnen hyperämischen Linie, Milchglasoptik oder einem Kavernen-Defekt besteht. Diese Koagulationszone muss die behandelte Läsion vollständig mit einem Sicherheitsabstand von idealerweise 5 mm einschließen. Das regulär in allen drei Dimensionen verformte Gewebe 41 einerseits und das Nichtvorhandensein von Kontrastmittelanreicherungen innerhalb des behandelten Tumors andererseits wurde als technischer Erfolg gewertet. In einigen Fällen von primär oder sekundär sehr dichten Zielläsionen wurde die Ablation ebenfalls als technischer Erfolg gewertet, wenn früher gezeigte Kontrastmittelanreicherungen der Läsionen in der Kontrolluntersuchung fehlten. a b c d Abb. 12 CT-gesteuerte Laserablation einer Lungenmetastase. 77jährige Patientin mit pulmonaler Metastase eines Nierenzellkarzinoms. a: während Thermotherapie. b: postinterventionelle Untersuchung. c: Verlaufskontrolle nach 3 Monaten. d: Verlaufskontrolle nach 6 Monaten Die klinische Nachbeobachtung der 64 Patienten erfolgte über einen Zeitraum von 0,0 – 63,9 Monaten (Median 8,9 Monate). 6 Wochen nach der initialen Behandlung wurde die erste Follow-Up-Untersuchung durchgeführt, weitere folgten 3, 6, 9 und 12 Monaten nach der 42 Ablation. Anschließend fanden Verlaufskontrollen im Abstand von 6 Monaten statt. Eine neuauftretende Kontrastmittelanreicherung in der behandelten Läsion, im Residuum oder in der Koagulationszone (frühestens 3 Monate nach der Behandlung) wurde als lokaler Tumorprogress bzw. als Rezidiv gewertet. Eine Vergrößerung des Residuums im Vergleich zum initialen Kontroll-CT wurde ebenfalls als lokaler Tumorprogress interpretiert mit Ausnahme von einer entzündlich bedingten Veränderung. Üblicherweise wurde bei Patienten mit einem lokalen Tumorprogress/- rezidiv eine erneute Ablation in Betracht gezogen. In Absprache mit dem Patienten und unter Beachtung eines medizinischen Erreichens der lokalen Tumorkontrolle wurden dann der Allgemeinzustand des Patienten und der Erkrankungsstand neu evaluiert. 43 2.4 Erhebung und Auswertung 2.4.1 Datengrundlage Grundlage der vorliegenden retrospektiven Untersuchung sind die klinischen Daten von 64 Patienten. Unter anderem wurden technische Daten, der initiale technische Erfolg, behandlungsrelevante Komplikationen und der lokale Tumorprogress im Verlauf tabellarisch nach Studienprotokoll erfasst. Die Intervalle bis zum Eintritt eines definierten Ereignisses wurden in Tagen gezählt und später zum besseren Verständnis in Monaten angegeben, wobei 30 Tage als ein Monat festgelegt wurden. Die Terminologie und die Beurteilungskriterien orientierten sich an den WHO-Richtlinien und Festlegungen sowie Empfehlungen der Arbeitsgruppe Goldberg [32]. Die Verlaufsanalyse erfolgte anhand der Auswertung des institutionellen RadiologieInformationssystems (RIS) und erhobener Daten des Tumorzentrums Greifswald. Einzelne Daten, insbesondere zum Krankheitsverlauf nach der Erstdiagnose und der Primärtherapie sowie zum Zeitpunkt und zur Ursache des Todes, wurden durch telefonische und schriftliche Anfragen beim betreuenden Fach- oder Hausarzt sowie bei Familienangehörigen in Erfahrung gebracht. Dies sicherte bei allen Patienten die Aufzeichnung jener Parameter, die in dieser retrospektiven Untersuchung Berücksichtigung finden. Es gab keinen Fall, in dem Nachsorgedaten nicht erhoben werden konnten. Bei allen Patienten konnten folgende Parameter festgehalten werden: • Patientenkollektiv o Name, Alter und Geschlecht der Patienten o Angaben zur Inoperabilität und zu Comorbiditäten • Daten zum Primärtumor o Art des Primärtumors o Synchroner/metachroner Verlauf der Metastasierung o Fernmetastasierung • Daten zu den Metastasen o Gesamtanzahl o Behandelte Metastasen (Anzahl, Lokalisation, Größe) 44 • Laserablation o Zeitpunkt der Therapie o Anzahl der Applikatoren o Applikationsleistung und –zeit o Technischer Erfolg o Komplikationen und notwendige Behandlungen • Follow-up o Zeitpunkte der Nachsorgeuntersuchungen o Lokaler, pulmonaler und/oder systemischer Progress/Rezidiv mit Zeitangaben zum freien Intervall o Zeitpunkt des letzten Kontakts o Todeszeitpunkt und –ursache Die Daten wurden in einer Microsoft Excel-Datenbank erfasst. Die Patientennamen wurden durch eine fortlaufende Nummer ersetzt, so dass anonym ausgewertet werden konnte. 2.4.2 Statistische Methoden Die Berechnungen der Überlebenszeiten wie auch alle anderen Analysen wurden computergestützt durchgeführt. Zur Auswertung der ermittelten Daten kamen das StatistikProgramm SPSS für Windows Version 16.0 („Statistical Package for the Social Sciences“, SPSS GmbH, an IBM Company, München) und Microsoft Excel zur Anwendung. Ebenso wurden auch sämtliche Tabellen, Diagramme und Graphiken mit diesen Programmen erstellt. Zur Ermittlung der Überlebenszeiten wurde die Methode nach Kaplan und Meier, Sterbetafeln und zur Signifikanzanalyse der Überlebenszeiten der log-rank-Test bzw. der Mann-WhitneyU-Test verwendet. Als statistisch signifikant wurden jeweils Aussagen bewertet, deren Signifikanzniveau p < 0,05 war. Zur Berechnung wurde die überlebte Zeit in Tagen vom Zeitpunkt des Therapiebeginns bis zum Tag des Todes herangezogen. Die Kaplan-Meier-Überlebenskurve berücksichtigt jedoch auch Patienten, die nicht an der Tumorerkrankung verstorben sind, die noch leben oder die die Studie verlassen haben. Diese werden graphisch in Form eines Kreuzes als so genannte zensierte Fälle markiert. 45 3 ERGEBNISSE 3.1 Applikationen Bei den 64 Patienten wurden insgesamt 108 Lungenmetastasen in 129 Thermositzungen behandelt. In 6 Fällen wurden zwei separate Metastasen in ein und derselben Sitzung abladiert. Damit stieg die Gesamtzahl der behandelten Ziele auf 135. Von diesen 135 Zielen handelt es sich in 27 Fällen um eine wiederholte Behandlung. In 21 Fällen gab es eine zweite und in 6 Fällen eine dritte Therapie. 72/135 Behandlungen wurden mit einem Applikator durchgeführt, 52/135 mit Doppelapplikationen und 11 Behandlungen mit 3 Applikatoren pro Läsion. Bei allen Patienten konnte das Applikationssystem während der Behandlung erfolgreich positioniert werden. 3.2 Technischer Erfolg der Metastasenbehandlung Ein technischer Behandlungserfolg konnte in Einzelfällen mehrere im Voraus geplante Ablationssitzungen erfordern und bezog eine wie beschrieben technisch erfolgreiche Ablation und einen therapeutischen Einfluss auf die Metastase(n) (gemäß Studienprotokoll) ein. 81/108 Metastasen wurden in der Erstbehandlung technisch erfolgreich behandelt. 4 weitere Ziele konnten aufgrund einer zeitnahen Zweitsitzung mit eingeschlossen werden. Somit konnten 85 der 108 Ziele gemäß den beschriebenen Kriterien vollständig abladiert werden. Das entspricht einer primären Effektivitätsrate von 78 %. 13/85 der initial in der ersten Sitzung erfolgreich behandelten Läsionen erhielten im Laufe des Follow-ups aufgrund eines lokalen Tumorprogresses/-rezidivs eine Re-Ablation, davon konnten 10 erneut technisch erfolgreich behandelt werden. Daraus resultiert eine sekundäre Erfolgsrate von 76 % (82/108). 46 Unter Anwendung der Laserablation konnten 61/69 (88 %) Ziele, die einen Durchmesser kleiner 3 cm aufwiesen und 23/33 (70 %) Metastasen mit einer Größe zwischen 3 und 5 cm technisch erfolgreich behandelt werden. Im Gegensatz dazu konnten nur 17 % der Ziele (1/6) mit einem Durchmesser größer 5 cm komplett abladiert werden. Der Einfluss der Größe auf eine technisch erfolgreiche Behandlung war in unserer Studie signifikant (p=0,0004). Anzahl der Metastasen 80 70 nicht erfolgreich 8 60 erfolgreich Progress 50 40 61 30 10 20 23 10 5 1 0 <3cm 3-5 cm >5 Größe der Metastasen Abb. 13 Technisch komplette Ablation in Bezug zur Größe der Metastasen. Die höchste Erfolgsrate (88 %) wurde bei einer Metastasengröße < 3 cm erreicht. 35/37 (95 %) der pulmonalen Absiedlungen kolorektaler Karzinome, 11/18 (61 %) des Nierenzellkarzinoms, 5/6 (83 %) des Malignen Melanoms, 5/8 (63 %) des Mammakarzioms, 11/15 (73 %) von Hals-, Nasen- und Ohrentumoren und 18/24 (75 %) der sonstigen Karziome konnten technisch komplett abladiert werden. Anzahl der Metastasen 40 35 2 nicht erfolgreich 30 erfolgreich Progress 25 20 15 6 35 7 4 10 5 11 1 5 NierenzellCa. Malignes Melanom 0 Kolorektales Ca. 3 5 Mamma-Ca 18 11 HNOTumore Sonstige Tumore Art des Primärtumors Abb. 14 Technisch komplette Ablation in Bezug zur Primärtumorentität. 95 % aller Lungenmetastasen des kolorektalen Karzinoms konnten technisch komplett abladiert werden. 47 32/44 (73 %) der Patienten mit nur einer behandelten Metastase, 8/13 (62 %) der Patienten mit zwei oder drei therapierten Metastasen und 6/7 (86 %) der Patienten mit mehr als 3 behandelten Metastasen konnten komplett abladiert werden. 3.3 Progression / Rezidiv Bis zum Ende der Studie (Stichtag: 28.03.2007) wurde bei 44/64 der Patienten im Laufe der Nachbeobachtung ein lokaler, pulmonaler und/oder systemischer Progress/Rezidiv diagnostiziert. Unter Berücksichtigung der festgelegten Kriterien entwickelten 30 % aller behandelten Patienten (n=19) einen lokalen Tumorprogress/-rezidiv, 39 % (n=25) einen intrapulmonalen und 50 % (n=32) einen systemischen Progress. Abb. 15 Diagnose von Progressen auf Patientenbasis Bezogen auf alle 108 Läsionen lag die lokale Tumorprogressionsrate bei 30 % (n=32). Von den 85 technisch erfolgreich abladierten Zielen trat bei 24 ein lokaler Tumorprogress auf. Dies entspricht einem Anteil von 28 %. Bei der Analyse der lokalen Progresse/Rezidive fällt auf, dass vor allem pulmonale Absiedlungen von Karzinomen des Hals-, Nasen-, Ohrenbereiches betroffen waren. Über die Hälfte (53 %) wies eine lokale Progression auf. Eine ebenfalls hohe Progressionsrate zeigten die Absiedlungen des Malignen Melanoms, von denen 33 % eine lokale Progression zeigten. Die Absiedlungen des kolorektalen Karzinoms und des Mammakarzinoms wiesen mit 27 % bzw. 25 % ein etwa gleich großes prozentuales Auftreten auf. Die geringste Progressionsrate 48 mit 17 % wiesen die Patienten mit Nierenzellkarzinom auf. Die Progression der einzelnen Metastasen nach Primärtumorentitäten ist in Abbildung 16 (Seite 49) dargestellt. Anzahl der Metastasen 40 35 kein Progress 30 Progress 25 27 20 17 15 7 15 10 10 5 4 2 NierenzellCa. Malignes Melanom 0 Kolorektales Ca. 6 3 8 7 HNOTumore Sonstige Tumore 2 Mamma-Ca Primärtumor Abb. 16 Lokale Progression nach Primärtumorentität. Die niedrigste Progressionsrate zeigten Patienten mit Nierenzellkarzinom als Primärtumor. Bei der Analyse eines möglichen Zusammenhangs zwischen Metastasengröße bei Erstdiagnose und einer lokalen Progression fällt auf, dass von den 69 Metastasen, deren Maximaldurchmesser unter 3 cm lag, nur 17 eine Progression zeigten (25 %). Von den 33 Tumoren mit einem Maximaldurchmesser zwischen 3 und 5 cm waren 12 progredient (36 %) und von den restlichen 6 Tumorabsiedlungen, die größer 5 cm waren, zeigten 3 (50 %) eine lokale Progression. Der Unterschied zwischen den Gruppen war mit p=0,124 nicht signifikant. Anzahl der Metastasen 80 70 kein keinProgress Progress Progress Progress 60 50 40 52 30 21 20 10 17 12 3 3 3-5 cm >5cm 0 <3cm Größe der Metastasen Abb. 17 Lokale Progression in Bezug zur Größe des Tumors Die geringste Progressionsrate zeigten Metastasen kleiner 3 cm. 49 3.4 Technischer Erfolg der Gesamtbehandlung Der technische Erfolg einer einzelnen Metastasenbehandlung ist nicht notwendigerweise gleichzusetzen mit dem technischen Erfolg der Gesamtbehandlung des Patienten. Die Ausnahme bildete der Patient mit einer solitären Metastase, deren technisch erfolgreiche Ablation gleich zu setzen war mit dem technischen Erfolg der Gesamtbehandlung. Es wurden auch Patienten mit einer Vielzahl von Metastasen eingeschlossen. Therapeutische Zielsetzung war immer die komplette Ablation aller Lungenmetastasen. Im Falle eines Progresses vor Abschluss der Erstbehandlung aller Metastasen galt diese als nicht komplett und der Patient wurde in die Zytoreduktions-Gruppe eingeschlossen. Die Gruppen waren nicht randomisiert. Nach diesen Kriterien konnten 31/64 Patienten insgesamt vollständig therapiert werden. Die 15 männlichen und 16 weiblichen Patienten wiesen ein medianes Alter von 67 Jahren auf. Die mediane Metastasenanzahl betrug 2,0 und die mediane Tumorgröße 2,1 cm. 33/64 Patienten konnten nicht komplett therapiert werden. In dieser zytoreduktiv-behandelten Gruppe betrug das Geschlechterverhältnis 2:1 (22 Männer/11 Frauen). Das mediane Alter der Patienten betrug 58 Jahre. Die mediane Tumoranzahl lag bei 10,1 und die mediane Metastasengröße bei 3,7 cm. Der Einfluss der Metastasenanzahl und Metastasengröße auf den technischen Erfolg der Gesamtbehandlung war mit jeweils p=0,0004 signifikant. Das Ergebnis bezogen auf die Primärtumorentitäten stellt Abbildung 18 genauer dar. Anzahl der Patienten 25 cytoreduktiv 20 komplett Progress 8 15 12 10 5 13 0 Kolorektales Ca. 7 2 1 3 3 4 NierenzellCa. Malignes Melanom Mamma-Ca 4 3 HNOTumore 5 Sonstige Tumore Art des Primärtumors Abb. 18 Technischer Erfolg der Gesamtbehandlung bezogen auf Primärtumorentität Patienten mit Mamma-Ca., gefolgt von Kolorektalem Ca. und Malignem Melanom, konnten am häufigsten komplett therapiert werden. 50 3.5 Überlebenszeitanalysen 3.5.1 Allgemeines zum Langzeitüberleben und Zahlen zum technischen Gesamtbehandlungserfolg Als Überlebenswahrscheinlichkeit der Patienten wurde die Zeit vom Therapiebeginn bis zum Tag des Endereignisses, dem Tod des Patienten, berechnet. Bei 30/64 Patienten trat bis zum Ende der Studie (Stichtag: 28.03.2007) das Ereignis ein, 34 der 64 Patienten haben den Beobachtungszeitraum überlebt bzw. sind durch ein konkurrierendes Ereignis aus der Studie ausgeschieden. Bei diesen Patienten ist nur die untere Grenze bekannt, also der Zeitpunkt, bei dem das Endereignis nicht eingetreten ist. In Abbildung 19 wird der Anteil dieser zensierten Fälle dem der „echten“ Fälle gegenübergestellt. zensierte Fälle; 53% n=34 echte Fälle; 47% n=30 Abb. 19 Verteilung der echten und zensierten Fälle (Gesamtüberleben) Da zensierte Daten vorliegen, kann die mittlere Überlebenszeit nicht bestimmt werden. Stattdessen wird die mediane Überlebenszeit angegeben, die die Zeitspanne quantifiziert, die von der Hälfte der Patienten überlebt wird. Zeitangaben mit Konfidenzintervall sind nach Kaplan-Meier berechnet. Konnte aufgrund zu geringer unzensierter Fallzahlen diese Methode nicht angewendet werden, basieren die Berechnungen auf Sterbetafeln. 51 3.5.2 Gesamtüberleben Das mediane Gesamtüberleben von allen 64 Patienten lag bei 23,1 Monaten (95 % Konfidenzintervall, 11,8 – 34,5 Monate). Die Kaplan-Meier-Überlebenskurve in Abbildung kumulatives Überleben 20 zeigt den prognostischen Verlauf im Hinblick auf das Gesamtkollektiv der Patienten. Zeit (in Monaten) Abb. 20 Überlebensfunktion des Gesamtpatientenkollektivs Das 5-Jahres-Überleben bezogen auf alle Patienten lag bei 18 %. Die Überlebenswahrscheinlichkeit lag nach einem Jahr bei 69 %, nach 2 Jahren bei 48 %, nach 3 und 4 Jahren bei 30 % und nach 5 Jahren bei 18 %. 3.5.3 Komplette vs. zytoreduktive Gesamtbehandlung Das Überleben in der Gruppe der komplett erfolgreich behandelten Patienten betrug im Median 32,4 Monate (95 % Konfidenzintervall, 17,5 – 47,3 Monate) mit 1-, 2-, 3-, 4- und 5Jahres-Überlebensraten von 81 %, 59 %, 44 %, 44 % und 27 %. In der Gruppe der zytoreduktiv behandelten Patienten betrug die mediane Überlebenszeit 12,2 Monate (95 % Konfidenzintervall, 0,8 – 23,6 Monate) mit 1-, 2- und 3-JahresÜberlebensraten von 57 %, 37 % und 7 %. 52 Die Kaplan-Meier-Kurven in Abbildung 21 stellen das Überleben des Gesamtkollektivs in Abhängigkeit des Therapieerfolgs der Gesamtbehandlung dar. kumulatives Überleben - komplett - cytoreduktiv Zeit (in Monaten) Abb. 21 Gesamtüberleben komplett erfolgreiche vs. zytoreduktive Therapie Das Gesamtüberleben der komplett behandelten Patienten lag signifikant höher. Die Unterschiede zwischen beiden Gruppen in den Überlebensraten waren signifikant (p=0,008). Die Patienten mit kompletter Ablation aller Metastasen wiesen im Vergleich zu Patienten mit zytoreduktiver Therapie eine signifikant bessere Überlebensrate auf. 53 3.5.4 Gesamtüberleben nach Primärtumorentitäten Die Art des Primärtumors zeigte in unserer Studie keinen signifikanten Einfluss auf die Überlebenszeiten. 20/64 Patienten des gesamten Patientenkollektivs wiesen pulmonale Metastasen des kolorektalen Karzinoms auf. Das mediane Überleben dieser Gruppe lag bei 23,1 Monaten (95 % Konfidenzintervall, 12,3 – 33,9 Monate), das mediane Überleben nach Sterbetafel betrug 23,6 Monaten. Abbildung 22 stellt das Überleben nach Kaplan-Meier dar. Die kumulativen 1-, 2-, 3-, 4- und 5-Jahres-Überlebensraten betrugen 76 %, 49 %, 27 %, 27 % kumulatives Überleben und 0 %. Zeit (in Monaten) Abb. 22 Gesamtüberleben (CRC) Die kumulative 5-Jahres-Überlebensrate für CRC-Patienten betrug 0 %. 13/20 Patienten aus dem Kollektiv der Patienten, die pulmonale Absiedlungen des kolorektalen Karzinoms aufwiesen, konnten komplett technisch erfolgreich behandelt werden. In dieser Patientenpopullation lag das mediane Gesamtüberleben bei 33,2 Monaten. Die 1-, 2-, 3-, 4- und 5-Jahres-Überlebensraten betrugen kumulativ 80 %, 64 %, 46 %, 46 % und 0 %. Das mediane Überleben der 7 zytoreduktiv behandelten Patienten lag bei 17,8 Monaten. In diesem Kollektiv betrugen die kumulativen 1- und 2-Jahres-Überlebensraten 69 % und 30 %. 54 Der Verlauf des kumulativen Überlebens der Patienten mit kolorektalen Karzinom in Abhängigkeit des Therapieerfolgs der Gesamtbehandlung wird in Abbildung 23 dargestellt. kumulatives Überleben - komplett - cytoreduktiv - zensiert - zensiert Zeit (in Monaten) Abb. 23 Gesamtüberleben (CRC) komplett erfolgreiche vs. zytoreduktive Therapie. Eine Steigerung der kumulativen 1- und 2-JÜR um 11 % bzw. 31 % konnte nach komplett erfolgreicher Therapie beobachtet werden. Bei Patienten mit einem Nierenzellkarzinom (n=10) als Primärtumor betrug das mediane kumulatives Überleben Überleben 24,0 Monate bei 1-, 2- und 3-Jahres-Überlebensraten von jeweils 56 %. Zeit (in Monaten) Abb. 24 Gesamtüberleben (RCC) Die 1-, 2- und 3-Jahres-Überlebensraten betrugen 56 %. 55 Drei der zehn Patienten mit pulmonal metastasiertem Nierenzellkarzinom konnten technisch erfolgreich behandelt werden. Die mediane Überlebenszeit in dieser Patientegruppe betrug wie in der gesamten RCC-Population ebenfalls 24,0 Monaten mit kumulativen Überlebensraten in den ersten drei Jahren von jeweils 67 %. Sieben der insgesamt zehn Patienten wurden in die Zytoreduktionsgruppe eingeschlossen. Die kumulativen 1- und 2Jahres-Überlebensraten betrugen jeweils 50 %. Das mediane Überleben in dieser Patientenpopulation betrug 12,0 Monate. kumulatives Überleben - komplett - cytoreduktiv - zensiert - zensiert Zeit (in Monaten) Abb. 25 Gesamtüberleben (RCC) komplett erfolgreiche vs. zytoreduktive Therapie Die 1- und 2-Jahres-Überlebensrate der komplett therapierten Patienten stieg um 17 %. Die mediane Überlebenszeit der insgesamt sechs Patienten mit Lungenmetastasen der Primärtumorerkrankung Malignem Melanom betrug 12,2 Monate (95 % Konfidenzintervall, 0,0 – 24,6 Monate). Die mediane Überlebenszeit nach Sterbetafel, welche die statistische altersbedingte Sterblichkeit in der Gesamtbevölkerung einbezieht, betrug in dieser Patientenpopulation 16,0 Monate. 56 kumulatives Überleben Die kumulativen 1- und 2-Jahres-Überlebensraten betrugen 60 % und 30 %. Zeit (in Monaten) Abb. 26 Gesamtüberleben (Malignes Melanom) Die kumulativen 1- und 2-Jahres-Überlebensraten betrugen 60 % und 30 %, das mediane Gesamtüberleben lag bei 12 Monaten. Die technisch erfolgreich behandelten Patienten aus dieser Gruppe (n=4) wiesen ein medianes Überleben von 19,2 Monaten auf, bei kumulativen 1- und 2-Jahres-Überlebensraten von 71 % und 36 %. kumulatives Überleben - komplett - cytoreduktiv - zensiert - zensiert Zeit (in Monaten) Abb. 27 Gesamtüberleben (MM) komplett erfolgreiche vs. zytoreduktive Therapie. 57 Die mediane Überlebenszeit nach Kaplan-Meier betrug bei Patienten mit Mammakarzinom (n=4) und Hals-, Nasen-, Ohrentumoren (n=7) jeweils 9 Monate. Die 1- und 2-JahresÜberlebensraten lagen bei Patienten mit Mammakarzinom bei 67 % und 0 %. Die 5-Jahres- kumulatives Überleben Überlebensraten betrug bei Patienten mit HNO-Tumor über den gesamten Zeitraum 54 %. Zeit (in Monaten) Abb. 28 Gesamtüberleben (Mamma-Ca.) kumulatives Überleben Die 1- und 2-Jahres-Überlebensraten lagen bei 67 % und 0 %. Zeit (in Monaten) Abb. 29 Gesamtüberleben (HNO-Tumore) Die 5-Jahres-Überlebensrate betrug 54 %. 58 Während bei den Patienten mit technisch erfolgreich behandelten pulmonalen Metastasen der HNO-Tumore eine mediane Überlebenszeit von 48 Monaten mit kumulativen 1-, 2- und 3Jahres-Überlebensraten von jeweils 100 % aufwiesen, haben die zytoreduktiv behandelten Patienten eine mediane Überlebenszeit von 8 Monaten und 1- und 2-Jahres-Überlebensraten von jeweils nur 25 %. Patienten mit Mammakarzinom stieg die mediane Überlebenszeit auf 14 Monate mit kumulativen 1- und 2-Jahres-Überlebensraten von 60 % und 0 %. kumulatives Überleben - komplett - cytoreduktiv - zensiert - zensiert Zeit (in Monaten) Abb. 30 Gesamtüberleben (Mamma-Ca.) komplett erfolgreiche vs. zytoreduktive Therapie. Die mediane Überlebenszeit verlängerte sich bei kompletter Therapie um 3 Monate. kumulatives Überleben - komplett - komplett - cytoreduktiv - cytoreduktiv - zensiert - zensiert - zensiert - zensiert Zeit (in Monaten) Abb. 31 Gesamtüberleben (HNO) komplett erfolgreiche vs. zytoreduktive Therapie. Die 5-Jahres-Überlebensrate betrug bei erfolgreicher Therapie 100 %. 59 3.6 Progressionsfreies Überleben 3.6.1 Allgemeines progressionfreies Überleben Bisher wurde nur auf die allgemeine Überlebenszeit der Patienten eingegangen. In diesem Abschnitt wird nun das progressionsfreie Überleben untersucht. Dazu wurde für jeden Patienten das progressionsfreie Intervall, also die Zeit vom Tag des Therapiebeginns bis zum Zeitpunkt der Diagnose eines Progresses berechnet. Da bei einigen Patienten bis zum letzten Follow-up-Termin kein Progress festgestellt wurde bzw. sie durch ein konkurrierendes Ereignis aus der Studie ausgeschieden sind, werden diese Fälle als zensierte Fälle betrachtet. Aufgrund des Vorhandenseins von zensierten Daten wird analog der Berechnung der Gesamtüberlebenszeit das mediane progressionsfreie Überleben, also die Zeitspanne in der bei der Hälfte der Patienten kein Tumorprogress beobachtet wurde, angegeben. Zeitangaben mit Konfidenzintervall sind nach Kaplan-Meier berechnet. Bis zum Ende der Studie wurde bei 44/64 der Patienten im Laufe der Nachuntersuchung ein lokaler, pulmonaler und/oder systemischer Progress diagnostiziert. Das generelle progressionsfreie Intervall im gesamten Patientenkollektiv lag im Median bei 5,8 Monaten (95 % Konfidenzintervall, 1,5 – 8,6 Monate). Abbildung 32 veranschaulicht das Überleben kumulatives Überleben hinsichtlich des Auftretens eines Progress unabhängig von der Lokalisation. Zeit (in Monaten) Abb. 32 Progressionsfreies Intervall des Gesamtpatientenkollektivs Das progressionsfreie Intervall aller Patienten betrug 5,8 Monate. 60 3.6.2 Lokale Tumorprogression/ -rezidiv Unter Berücksichtigung der festgelegten Rezidivkriterien entwickelten 30 % der behandelten Patienten (n=19) einen lokalen Tumorprogress/ Rezidiv. Bei den übrigen 45 Patienten (70 %) wurde bis zum letzten Follow-up-Termin kein lokaler Tumorprogress innerhalb der Ablationszone festgestellt. Das mediane progressionsfreie Intervall der Gesamtpatientenpopulation (n=64) bezogen auf einen lokalen Tumorprogress/Rezidiv lag bei kumulatives Überleben kumulatives Überleben 24,5 Monaten. Zeit (in Monaten) Zeit (in Monaten) Abb. 33 Lokalprogressionsfreies Überleben (Gesamtpatientenkollektiv) Das mediane progressionsfreie Überleben aller Patienten betrug 24,5 Monate. Abb. 34 Progressionsfreies Überleben bei Auftreten eines lokalen Tumorprogresses Das med. progressionsfreie Intervall der Patienten mit Progress betrug 6,4 Monate. Betrachtet man nur die 19 Patienten, bei denen ein lokaler Tumorprogress/Rezidiv auftrat, lag das mediane progressionsfreie Intervall innerhalb dieser Gruppe bei 6,4 Monaten (95 % Konfidenzintervall, 3,8 – 9,0 Monate). Von den technisch erfolgreich behandelten Patienten trat bei 6/31 (19,4 %) ein lokaler Tumorprogress auf. In der Gruppe der zytoreduktiv behandelten Patienten wurde bei 13/33 (39,4 %) Patienten eine lokale Größenprogression beobachtet. Bezogen auf die Gesamtpatientenpopulation betrug der Mittelwert für die Gruppe der komplett erfolgreich behandelten Patienten 23,6 Monate. Das mediane progressionsfreie Intervall in der Gruppe der zytoreduktiv behandelten Patienten betrug 13,7 Monate (95 % Konfidenzintervall, 8,5 – 61 18,9 Monate). Der Unterschied zwischen den beiden Gruppen war mit p= 0,039 signifikant. Die Überlebenskurven nach Kaplan-Meier sind in den Abbildungen 35 und 36 dargestellt. - cytoreduktiv - komplett kumulatives Überleben kumulatives Überleben - cytoreduktiv - komplett - zensiert - zensiert Zeit (in Monaten) Zeit (in Monaten) Abb. 35 Lokalprogressionsfreies Überleben Gesamtpatientenkollektiv (zytoreduktiv vs. komplett) Das progressfreie Intervall bei kompletter Therapie betrug 23,6 Monate. Abb. 36 Progressionsfreies Überleben bei Auftreten eines lokalen Tumorprogresses (zytoreduktiv vs. komplett) Das progressionsfreie Intervall der Patienten Mit Kompletttherapie und einem lokalen Progress betrug 2,8 Monate. Das mediane rezidivfreie Intervall der sechs technisch erfolgreich behandelten Patienten mit lokalem Tumorrezidiv betrug nach Kaplan-Meier 2,8 Monate (95 % Konfidenzintervall, 2,3 – 3,2 Monate). Bei den 13 zytoreduktiv-behandelten Patienten, die einen lokalen Tumorprogress aufwiesen, betrug das mediane progressionsfreie Intervall 7,5 Monate (95 % Konfidenzintervall, 3,1 – 11,9 Monate). Die Datenauswertung des lokalen Tumorprogresses hinsichtlich der unterschiedlichen Metastasengrößen zeigt, dass von den insgesamt 69 Metastasen mit einer Größe kleiner 3 cm in 17 Fällen (24,6 %) eine Größenprogredienz auftrat. Es zeigte sich ein mittleres progressfreies Intervall von 31,4 Monaten. Dagegen waren Tumore mit einer Größe zwischen 3 und 5 cm zu 36,4 % (12/33) lokal größenprogredient mit einem kürzeren medianen Intervall von 14,1 Monaten (95 % Konfidenzintervall, 5,0 – 25,5). Bei den Metastasen, die größer waren als 5 cm, fand sich in 3/6 Fällen (50 %) eine lokale Größenzunahme. Das mediane lokalprogressionsfreie Intervall betrug hier 4,5 Monaten. Der Einfluss der Größe auf ein Lokalrezidiv war in unserer Studie mit >0,05 nicht signifikant. Die Überlebenskurven nach 62 Kaplan-Meier eingeteilt in drei verschiedene Größengruppen sind in Abb. 37 bis 39 kumulatives Überleben kumulatives Überleben dargestellt. Zeit (in Monaten) Zeit (in Monaten) Abb. 37 Lokalprogressionsfreies Überleben (Größe der Metastasen < 3cm) Abb. 38 Lokalprogressionsfreies Überleben (Größe der Metastasen 3-5 cm) kumulatives Überleben . kumulatives Überleben - zytoreduktiv - komplett - zensiert - zensiert Zeit (in Monaten) Zeit (in Monaten) Abb. 39 Lokalprogressionsfreies Überleben (Größe der Metastasen >5 cm) Abb. 40 Lokalprogressionsfreies Überleben bezogen auf technischen Erfolg (Metastasen < 3cm) Betrachtet man die Gruppe der Metastasen mit einer Größe unter 3 cm, die technisch erfolgreich behandelt wurden, zeigt sich in 14/61 Fällen ein lokales Rezidiv mit einem mittleren rezidivfreien Intervall von 31 Monaten, während die zytoreduktiv behandelten Läsionen in 37,5 % (3/8) lokal progredient waren und ein kürzeres mittleres rezidivfreies Intervall von 21 Monaten aufwiesen. Die Kaplan-Meier-Kurven in Abbildung 40 stellen das lokalprogressionsfreie Überleben in Abhängigkeit des Therapieerfolgs dar. 63 3.6.3 Intrapulmonale Progression Ein intrapulmonaler Progress wurde bei 39 % aller behandelten Patienten (n=25) innerhalb von 0,5 – 24,5 Monaten diagnostiziert. Das progressionsfreie Intervall lag bei diesen 25 kumulatives Überleben kumulatives Überleben Patienten im Median bei 2,8 Monaten (95 % Konfidenzintervall, 1,9 – 3,8 Monate). Zeit (in Monaten) Zeit (in Monaten) Abb. 41 Intrapulmonal-progressionsfreies Überleben (Gesamtpatientenkollektiv) Das progressfreie Intervall aller Pat. Betrug 15,2 Monate. Abb.42 Progressionsfreies Überleben bei Auftreten eines intrapulmonalen Tumorprogresses Das progressfreie Intervall der 25 Pat. mit Progress betrug 2,8 Monate. Bei 61 % aller Patienten (n=39) wurde kein intrapulmonaler Tumorprogress diagnostiziert. Das mediane progressionsfreie Intervall der Gesamtpatientenpopulation (n=64) bezogen auf einen intrapulmonalen Tumorprogress lag bei 15,2 Monaten (95 % Konfidenzintervall, 10,6 – 19,9 Monate) und ist in Abbildung 42 graphisch dargestellt. 64 3.6.4 Systemische Progression Ein Progress einer extrapulmonalen/systemischen Metastasierung wurde bei der Hälfte aller Patienten (32/64) beobachtet. Das mediane progressionsfreie Intervall dieser 32 Patienten mit einer systemischen Erkrankungszunahme betrug 4,4 Monate (95 % Konfidenzintervall, 3,3 – 5,6 Monate). Der späteste Zeitpunkt zu dem ein Progress beobachtet wurde, lag bei 52,9 Monaten. Das mediane progressionsfreie Intervall bezogen auf die Gesamtpatientenpopulation betrug 13,9 Monate (95 % Konfidenzintervall, 6,8 – 21,0 Monate). Abbildung 43 veranschaulicht das Überleben des gesamten Patientenkollektivs bis zum Auftreten des kumulatives Überleben kumulatives Überleben systemischen Progresses. Zeit (in Monaten) Zeit (in Monaten) Abb. 43 Extrapulmonal-progressionsfreies Überleben (Gesamtpatientenkollektiv) Das progressionsfreie Intervall für alle Patienten betrug 13,9 Monate. 65 Abb. 44 Progressionsfreies Überleben bei Auftreten eines systemischen Tumorprogresse Das progressionsfreie Intervall der 32 Pat. mit Progress betrug 4,4 Monate. 3.7 Komplikationen Alle Patienten tolerierten die Laserablation gut in Lokalanästhesie, Sedierung und unter systemischer Applikation niedrig dosierter Analgetika. Die therapiebedingte Mortalitätsrate lag bei 0 %. In Tabelle 5 sind die Nebenwirkungs- und Komplikationsraten dokumentiert. Komplikation Leichte Komplikationen Pneumothorax asymptomatisch behandlungsbedürftig mit Drainagenanlage Parenchymeinblutung Hämoptysen Dyspnoe Pneumonie Nebenwirkungen Pleuraerguss starke Schmerzen postablative Syndrome Weichteilemphysem Schwere Komplikationen kombinierte Blutung und Dyspnoe (ohne Intensivüberwachung) Empyem (mit Notaufnahme) Anzahl Rate 49 42 7 17 9 3 2 38 % 33 % 5% 13 % 7% 2% 2% 24 6 6 5 19 % 5% 5% 4% 2 2% 1 1% Tab. 5 Häufigkeit der aufgetretenen Komplikationen bei 129 ablativen Verfahren Das Auftreten eines Pneumothorax war die häufigste Komplikation während der Laserablation. Insgesamt trat er in 49/129 Ablationssitzungen auf. Das entspricht einer Quote von 38 % aller Behandlungen. Dabei handelte es sich in 5 % der Fälle (7/129) um einen behandlungsbedürftigen Pneumothorax, der während der Intervention mittels PneumocathDrainage therapiert werden musste. Parenchymblutungen kamen in 17/129 Behandlungen (13 %) vor, diese waren in allen Fällen selbstlimitierend und führten in 9/129 Fällen (7 %) zu temporären Hämoptysen. Kleine reaktive Pleuraergüsse traten in 24/129 Fällen (19 %) auf. Diese waren nicht therapiebedürftig. Es traten drei schwere Komplikationen auf, die zu einer verlängerten Hospitalisierung, unerwartetem gesteigerten Behandlungsaufwand oder zu einer Wiederaufnahme führten. Zwei dieser Patienten wurden nach zeitgleich auftretenden Parenchymblutungen und Dyspnoe über Nacht stationär überwacht. In einem Fall führte sechs Wochen nach der Behandlung eine spätauftretende Pneumonie zur Wiederaufnahme, mit der Diagnose eines Empyems. Dieser Patient wurde mittels Abszessdrainage behandelt und zwei Nächte auf der Intensivstation überwacht. 66 4 DISKUSSION 4.1 Langzeitergebnisse Die chirurgische Resektion gilt nach wie vor als therapeutischer Goldstandard der Behandlung pulmonaler Metastasen, da keine andere Therapieform derzeit auch nur annähernd vergleichbare Ergebnisse liefert. In aktuellen Studien kann in 88 % aller Fälle eine komplette Resektion erzielt werden, die 3- und 5-Jahres-Überlebensraten werden nach vollständiger Resektion unabhängig vom Primärtumor mit 45 % bzw. 30 % und mehr angegeben [13, 27, 43, 76, 87, 100, 104, 124, 135, 140]. In der bislang größten Analyse zu Langzeitergebnissen mit 5206 Patienten geben Friedel et al. [27] 5-, 10- und 15-JahresÜberlebensraten von 36 %, 26 % und 22 % an. Die Morbidität der Lungenresektion liegt zwischen 6,3 % und 30 %, die Operationsletalität bei 2,2 % [1, 43, 61, 66, 115]. Beide Faktoren korrelieren direkt mit dem Ausmaß der Resektion. Auch wenn eine spezielle Nachsorge nach kurativer Resektion einer Lungenmetastase in den Leitlinien nicht vorgesehen ist, ist eine solche essentiell, da die Rezidivhäufigkeit mit bis zu 70 % sehr hoch ist [12, 14, 89, 90, 92, 103, 151]. Aufgrund operationstechnischer Grenzen ist weiterhin eine Lungenteilresektion mit kurativer Intention für mehr als 70 % aller Patienten mit Lungenmetastasen nicht möglich [115]. Für die meisten dieser inoperablen Patienten kommt erschwerend hinzu, dass eine adäquate Chemotherapie nicht zur Verfügung steht. Die Chemotherapie bei Patienten mit Lungenmetastasen ist größtenteils nicht signifikant lebensverlängernd und sollte aufgrund eventueller Nebenwirkungen und der damit einhergehenden Beeinträchtigung der Lebensqualität der Patienten nur in Studien erfolgen [37, 48, 59, 71, 81, 91, 96, 102]. Da auch die Strahlentherapie bei der Behandlung von Lungenmetastasen in kurativer Intention nur eine untergeordnete Bedeutung hat, standen für inoperable Patienten in früherer Zeit keine anderen adäquaten Therapiemethoden zur Verfügung. Für die Entwicklung alternativer Behandlungsverfahren von Lungenmetastasen lassen sich aus den limitierenden Faktoren der chirurgischen Therapie wesentliche Kriterien ableiten. So ergibt sich aufgrund der direkten Korrelation von Resektionsausmaß und Komplikationsrate bei der Lungenteilresektion die Forderung nach einem möglichst parenchymsparenden und komplikationsarmen Therapieverfahren. Weiterhin belegt die hohe Rezidivrate nach initial kurativer Resektion die Notwendigkeit der potentiellen Wiederholbarkeit der Therapieform. 67 Vor diesem Hintergrund erlangen die erst vor wenigen Jahren eingeführten minimalinvasiven Therapieverfahren immer mehr an Bedeutung. Diese Therapieformen werden den erwähnten Anforderungen gerecht. Die Laserablation, als eine dieser neuen minimimalinvasiven Techniken, wird seit einigen Jahren erfolgreich zur Behandlung primärer und sekundärer Lebertumore eingesetzt [11, 19, 75, 130, 131, 153]. Aufgrund der vielversprechenden Ergebnisse wird das Verfahren nun auch zur lokalen Tumordestruktion an anderen Organen angewendet. Seit 2003 wurden Studien zur Laserablation pulmonaler Absiedlungen veröffentlicht, deren Ergebnisse eine sichere Durchführbarkeit des Verfahrens an der Lunge belegen [54, 128, 132, 136, 137]. Im Gegensatz zu den großen chirurgischen Kollektiven konnten Aussagen über langfristige Erfolge aber aufgrund zu geringer Patientenzahlen und kurzer Nachbeobachtungszeiträume nicht getroffen werden. Untersucht werden konnten bisher nur die technische Machbarkeit, die lokale Tumorkontrollrate und die Komplikationsrate. In der vorliegenden Arbeit werden die Ergebnisse von 64 Patienten hinsichtlich ihres Langzeitüberlebens untersucht, deren insgesamt 108 Lungenmetastasen in 129 Sitzungen mittels Laserablation behandelt wurden. Die klinische Nachbeobachtung erfolgte über einen Zeitraum von bis zu 63,9 Monaten (Median 8,9 Monate). Zielgröße für eine sinnvolle Therapie pulmonaler Metastasen ist die zu erreichende Überlebenszeit. Die 3- und 5-Jahres-Überlebensraten in dem untersuchten Gesamtpatientenkollektiv betrugen 30 % und 18 % bei einer medianen Überlebenszeit von 23,1 Monaten und liegen damit unter den Ergebnissen, die nach radikaler pulmonaler Metastasenchirurgie berichtet werden (5-JÜR 36 % / mediane Überlebenszeit 35 Monate) [27]. Diese Ergebnisse werden aber nach R0-Resektion erzielt, für inkomplette chirurgische Resektionen wird eine 5-Jahres-Überlebensrate von lediglich 7 % angegeben. Der technisch vollständige Behandlungserfolg hat somit einen Einfluss auf die Überlebensraten. Die technische Erfolgsrate der Erstbehandlung in unserer Studie lag bei 78 %. Aufgrund eines lokalen Tumorrezidivs im Laufe des Follow-ups mussten 15 % der Metastasen erneut behandelt werden. In der Zweitbehandlung konnten 77 % der pulmonalen Tumore erneut vollständig abladiert werden, so dass eine sekundäre Erfolgsrate von 76 % resultiert. Die Ergebnisse unserer Studie liegen im Bereich derer, die in einer anderen Studie zur 68 Laserablation von Vogl et al. mit 74 % erzielt wurden [128]. Im Vergleich zur Radiofrequenztherapie wird in der Literatur allgemein von „diskret erhöhten Raten an kompletten Tumorablationen“ nach Laserablation gesprochen ohne konkrete Zahlenangaben zu nennen [132]. In einer Publikation von Lee et al. [72] wird sogar nur eine Rate von 38 % nach Radiofrequenzablation angegeben, eine Vergleichbarkeit ist aber aufgrund unterschiedlicher Einschluss- und Auswertungskriterien nicht sinnvoll. Ein Vergleich mit anderen minimalinvasiven Therapien kann nicht erfolgen, da zum Zeitpunkt der vorliegenden Arbeit keine vergleichbaren Veröffentlichungen zu technisch komplett erfolgreichen Ablationen bekannt sind. Die Ergebnisse in unserer Studie zeigen in der Gruppe der technisch komplett erfolgreich behandelten Patienten 3- und 5-Jahres-Überlebensraten von 44 % und 27 %. Der Einfluss war signifikant (p=0,008). Die mediane Überlebenszeit betrug 32,4 Monate und nähert sich den berichteten Überlebenszeiten nach Metastasenresektion an. Die Bedeutung der technisch erfolgreichen Behandlung zeigt sich auch bei der Betrachtung der homogeneren, wenn auch sehr kleinen Primärtumorgruppen, wobei der Einfluss auf die Überlebenszeit, vielleicht auch wegen der geringen Patientenzahlen, nicht signifikant war. Es konnte allerdings auch hier eine Steigerung der Überlebensraten nach technisch kompletter Lasertherapie beobachtet werden. Während von einem medianen Überleben von 19 Monaten bei unbehandelten Patienten mit metastasiertem Nierenzell-Karzinom berichtet wird [88], wiesen die Patienten in unserem Kollektiv ein medianes Überleben von 24 Monaten auf. Dieses von uns erzielte mediane Überleben liegt deutlich unter dem nach Metastasenresektion von 42 Monaten [31]. Bei Patienten mit Malignem Melanom als Primärtumor konnte das Überleben bei unbehandelten Patienten von 10 Monate [43] auf 19,2 Monate nach Laserablation gesteigert werden, dieses Ergebnis liegt innerhalb des Bereiches der erzielten medianen Überlebenszeiten nach Operation von 15-22 Monaten [34, 42, 43, 115]. Patienten mit HNO-Tumoren profitierten in unserer Studie am meisten von der Behandlung mittels Laserablation. Hier ließ sich eine 5-Jahres-Überlebensrate von 54 % erreichen, Patienten im fernmetastasierten Stadium (70 % Lunge [104, 139, 152]) zeigten hingegen nur eine Überlebensrate von unter 19 % [58, 134]. Auch Patienten mit pulmonalen Metastasen des kolorektalen Karzinoms zeigten mit einem medianen Gesamtüberleben von 33,2 Monaten und kumulativen 1-, 2- und 3-Jahres-Überlebensraten von 80, 64 und 46 % gute Überlebensraten. Die Ergebnisse liegen innerhalb des Bereiches der Überlebenszeiten bei operativ therapierten 69 Patienten mit pulmonalen Metastasen des Kolorektalen Karzinoms, die mit 7-40 Monaten angegeben werden [35, 43, 100]. Nur bei Patienten mit pulmonalen Absiedlungen des Mamma-Karzinoms blieb das mediane Überleben in unserer Studie gegenüber unbehandelten Patienten mit 9 Monaten unverändert [86]. Mammakarzinom-Patienten mit Metastasenresektion zeigten ein medianes Gesamtüberleben von 35-54 Monaten [43, 115], allerdings kommen generell nur sehr wenige Brustkrebspatienten für eine Operation überhaupt in Frage, da in den meisten Fällen ein Metastasenbefall mehrerer Organe vorliegt [115]. Die Art des Primärtumors hatte in unserer Studie keinen signifikanten Einfluss auf die Überlebenszeiten. Somit kann hier aufgrund zu geringer Fallzahlen nur eine Tendenz aufgezeigt werden und diese muss in fortführenden Studien mit größeren Fallzahlen weiter evaluiert werden. Einen signifikanten Einfluss auf die Möglichkeit der Durchführung einer technisch kompletten Therapie und somit die Chance einer Verbesserung der Überlebensraten, hatte in unserer Studie (p=0,0004) die Anzahl der zu behandelnden Metastasen. Prinzipiell sollte die Gesamtzahl der Lungenmetastasen möglichst gering sein. Mehrere Studien analysierten den Einfluss der Metastasenanzahl auf das Langzeitüberleben nach operativer Therapie. Ist die Anzahl der Metastasen < 4 kann eine mittlere Überlebenszeit von bis zu 45 Monaten erzielt werden, mit einer Metastasenanzahl > 4 sinken die Überlebensdaten auf 21 Monate [27]. Die 5-Jahres-Überlebensraten betrugen bei Patienten mit einer solitären Metastasen 45% - 62 %, bei Patienten mit vier oder mehr Metastasen 0 % [100, 114]. In unserer Studie zeigt sich das die maximale Anzahl an Lungenmetastasen nicht mehr als 2 betragen sollte, in Zusammenschau mit anderen Studien sollte die maximale Anzahl der Herde pro Lungenseite aus heutigen Erfahrungen nicht mehr als 3 betragen, um in einem möglichst kurzen Zeitrahmen die technisch komplette Behandlung aller Metastasen eines Patienten zu erreichen [32]. Ein Vergleich der Überlebenszeiten nach Laserablation mit denen anderer minimalinvasiver Therapieverfahren ist aufgrund der geringen Nachbeobachtungszeiten nur bedingt möglich. In aktuellen Studien zur Radiofrequenzablation beschränken sich die Nachbeobachtungszeiten auf maximal 48 Monate. Die mediane Überlebenszeit nach Radiofrequenzablation pulmonaler Metastasen wird mit bis zu 33 Monaten angegeben, die Überlebensraten schwanken je nach Studie zwischen 70 % - 96 % (1-JÜR), 54 % - 66 % (2-JÜR) und 44 % - 48 % (3-JÜR) [4, 30, 46, 85, 122, 132, 147, 148, 149]. In der bisher größten Studie mit 153 Patienten wurden 1-, 270 und 3-Jahres-Überlebensraten von 70 %, 54 % und 44 % erzielt [121]. Damit liegen die Ergebnisse im Bereich unserer Resultate nach technisch erfolgreicher Laserablationsbehandlung (1-, 2-, 3-JÜR: 81 %, 59 %, 44 %, med. ÜLZ: 32,4 Monate). Publikationen über die perkutane Mikrowellenablation von pulmonalen Metastasen berichten bei einem medianen Follow-up von 10 Monaten von 1-, 2- und 3-Jahres-Überlebensraten von 65 %, 55 % und 45 % [143]. Für die Anwendung der Kryo- und Äthanolablation liegen derzeit nur kleine Kohortenstudien vor, die eine 1-Jahres-Überlebensrate von 89,4 % [60] und 64,2 % aufweisen [39]. In einer Studie zur Evaluation der transpulmonalen Chemoembolisation bei Lungenmetastasen konnte bei 52 Patienten ein medianes Überleben von 17 Monaten erzielt werden [129]. Autor Jahr n Lencioni [74] Yamakado [147] Simon [121] 2008 2007 2007 Hiraki [46] Yan [148] Wolf [143] He [44] 2007 2006 2008 2008 53 71 153 18 27 55 50 12 M 155 189 49 82 16 PT CRC CRC var. CRC CRC CRC var. var.* Med. Follow-up (Mon) 19 (4-42) 20,1 24(6-40) 10 20 (6-40) Überlebensraten (in %) 1 2 3 89 66 84 46 70 54 44 87 78 57 96 54 48 85 64 46 65 55 45 med. ÜLZ (Mon) 31 Therapieart Radiofrequenzablation 33 33 Mikrowellenablation Kawamura [60] 2006 20 35 var. 21 (9-28) 89,4 Kryoablation Laserablation Weigel [137] 2006 42 64 var* 7,6 (6-39) Vogl [128] 2004 24 34 var. Vogl [129] 2008 52 116 var. 6 – 27 17 TPCE n= Anzahl der Patienten; M = Anzahl der Metastasen, PT= Primärtumor; med.= median; Mon= Monate; ÜLZ= Überlebenszeit, * - beinhaltet primäre und sekundäre Lungentumore, TPCE = Transpulmonale Chemoembolisation Tab. 6 Überlebensraten minimalinvasiver Behandlungsmethoden primärer und sekundärer Lungentumore Ähnliche Ergebnisse werden in der Literatur nach stereotaktischer Bestrahlung angegeben. Wulf et al. [146] berichten von insgesamt 41 Patienten mit 51 pulmonalen Metastasen, die mittels stereotaktischer Bestrahlung behandelt wurden. Die lokale Kontrollrate lag bei 80 %, das kumulative 1- und 2-Jahres-Überleben bei 85 % und 33 %. Die lokale Kontrollrate im Patientenkollektiv von Fritz et al. [28] lag bei 87 %. In dieser Studie wurden bei 25 Patienten 31 Lungenmetastasen mittels stereotaktischer Bestrahlung mit einer Einzeldosis von bis zu 30 Gray behandelt. Die kumulativen 1-, 2- und 3-Jahres-Überlebensraten betrugen 97 %, 73 % und 42 %. Eine ähnlich hohe lokale Tumorkontrollrate (83 %) erreichten Okunieff et al. [94]. Die mediane Überlebenszeit der kurativ behandelten Patienten betrug nach der stereotaktischen Bestrahlung 23,4 Monate. Ricke et al. berichten seit 2004 über die Therapie von Patienten mit primären und sekundären Lungentumoren mittels Brachytherapie, bisher allerdings ohne Angaben zu Langzeitüberlebensraten [98, 105, 106]. 71 Autor Jahr n M PT Med. Überlebensraten med. ÜLZ Therapieart Follow-up (in %) (Mon) (Mon) 1 2 3 Brown [10] 2008 35 69 var. 18 (2-41) stereotaktische Strahlentherapie Hof [49] 2007 61 71 var. 14 78, 4 65,1 47, 8 Fritz [28] 2006 25 31 var. 22 97 73 42 26 Okunieff [94] 2006 50 125 var. 18, 7 23,4 Wulf [146] 2004 41 51 var. 9 (2-37) 85 33 Peters [98] 2007 30 83 var.* 9 (1-21) Brachytherapie Ricke [106] 2005 15 30 (2/28) var.* 5 n= Anzahl der Patienten; M = Anzahl der Metastasen, PT= Primärtumor; med.= median; Mon= Monate; ÜLZ= Überlebenszeit, * - beinhaltet primäre und sekundäre Lungentumore Tab. 7 Überlebensraten nach stereotaktischer Strahlen- und Brachytherapie von Lungentumoren Die Resultate der technisch erfolgreich behandelten Patienten in unserer Studie liegen über denen der Radiofrequenz-, Mikrowellen- und Äthanolablation, in etwa in dem Bereich der Strahlentherapie und leicht unter denen der Kryoablation. Die mediane Überlebenszeit der technisch erfolgreich behandelten Patienten unserer Studie liegt mit 32,4 Monaten im Bereich des erzielten medianen Überlebens von 31 – 33 Monaten nach Radiofrequenzablation [46, 147, 148] und über denen der stereotaktischen Bestrahlung mit 23,4 – 26 Monaten [28, 94] sowie denen der transpulmonalen Chemoembolisation mit 17 Monaten [129]. Ausbleiben muss ein Vergleich der Überlebenszeiten nach Brachytherapie, da zu diesem sehr jungen Verfahren bisher keine Langzeitergebnisse veröffentlicht wurden. Auch wurden bisher keine Daten zu den 5-Jahres-Überlebensraten nach Radiofrequenzablation, stereotaktischer Bestrahlung, transpulmonaler Chemoembolisation, Kryoablation, Äthanolablation oder Mikrowellenablation publiziert. Mit Ausnahme der Radiofrequenzablation wurden bisher nur wenige Studien mit nur sehr kleinen Behandlungsserien veröffentlicht. Erschwerend kommt hinzu, dass die publizierten Daten aufgrund sehr unterschiedlicher Einschluss- und Auswertungskriterien nur grenzwertig vergleichbar sind. Ein limitierender Faktor der Therapie pulmonaler Metastasen bei onkologischen Patienten stellt ein Progress der Tumorkrankung in Form lokaler Rezidive, neuer pulmonaler Metastasen oder Fernmetastasen anderer Organe dar. Derzeitige Studien lassen annehmen, dass hier ein Verbleiben vitaler Tumorzellen innerhalb des Zielvolumens zur Entwicklung eines interläsionären Rezidivs oder Progresses führt. Beim Vorliegen von Tumorzellen außerhalb des Koagulationsvolumens kommt es gewöhnlich zur Entstehung eines extraläsionären Rezidivs. [33, 132]. Ein Lokalrezidiv trat in unserer Studie bei 30 % der Patienten auf, das mediane progressionsfreie Intervall der Gesamtpopulation lag bei 24,5 Monaten. Die Rezidiv- bzw. Progressraten wiesen in den Gruppen der technisch erfolgreich und den zytoreduktiv 72 behandelten Patienten einen deutlichen Unterschied auf und waren signifikant. In der zytoreduktiv behandelten Gruppe wurde bei 39,4 % der Patienten ein Progress/ Rezidiv beobachtet, in dem Patientenkollektiv mit technisch kompletter Gesamtbehandlung dagegen nur bei 19,4 %. Ebenso zeigt das rezidivfreie Intervall mit 23,7 Monaten in der Gruppe der technisch erfolgreich behandelten Patienten gegenüber der zytoreduktiven Gruppe mit 13,7 Monaten eine deutliche Steigerung. Die Patienten mit Lokalrezidiv aus dem technisch komplett behandelten Patientenkollektiv wiesen ein medianes rezidivfreies Intervall von 2,7 Monaten auf, was die Bedeutung des Follow-ups – insbesondere der Kontrolluntersuchung nach 3 Monaten – deutlich macht, um eine frühzeitige Re-Laserablation zu ermöglichen und damit einen sekundären technischen Behandlungserfolg zu erzielen. Studien von Patienten, die eine chirurgische Resektion des kolorektalen Karzinoms erhalten haben, zeigten ein pulmonales Rezidiv in 50-79 % der Fälle [12, 92]. In unserer Studie traten ein pulmonales bzw. systemisches Rezidiv nach der Laserablation bei 39 % bzw. 50 % aller Patienten auf. Unter Beachtung, dass bei einigen Patienten mit frühen und schnellprogressiver extrapulmonaler Metastasierung eine Bestätigung eines intrapulmonalen Progresses fehlt, sollte aber die geschätzte intrapulmonale Rezidivrate innerhalb des Bereichs liegen, die nach chirurgischer Resektion in der Literatur berichtet wird. Auch die lokale Rezidivrate in unserer Studie lag mit 30 % bei allen 64 Patienten relativ niedrig im Vergleich zu den Daten aus der Literatur. Hier zeigt sich ein limitierender Faktor der chirurgischen Therapie, denn Rezidive können auf Grund des oft hohen Parenchymverlustes und der hohen Invasivität des Eingriffes nicht beliebig oft reseziert werden, während einer Wiederholung der Lasertherapie nichts entgegensteht. Unabhängig von der Art des Progresses zeigte sich nach Radiofrequenzablation eine Rate von 66 % [148], in unserer Studie eine nur geringfügig höhere mit 68,8 %. Das kumulativ progressionsfreie Intervall hinsichtlich eines allgemeinen Progresses lag nach stereotaktischer Bestrahlung bei 25 % - 35 % nach 12 Monaten und 16 % nach 24 Monaten [94, 146], in unserer Studie wurden gleiche bis etwas höhere Ergebnisse von 32 % und 22 % erzielt. Ein lokaler Progress nach Laserablation zeigte sich bei 30 % der von uns behandelten Patienten, nach transpulmonaler Chemoembolisation trat bei 48 % der Patienten ein Progress auf [129]. Nach Kryotherapie wurde eine lokale Rezidivrate von 35 % nach einem medianen Follow-up von 21 Monaten verzeichnet [60], in unserer Studie betrug die Rezidivrate nach 21 Monaten 46,6 %, allerdings lassen sich hier beide Ergebnisse auf Grund der unterschiedlichen 73 Auswertung Follow-up/ Kaplan-Meier nicht sicher vergleichen. Nach Radiofrequenzablation zeigt sich eine lokale Rezidivrate von 38 % [148] und liegt damit leicht über den von uns erzielten Resultaten. Die Ergebnisse unserer Studie zeigen, dass die Rezidivrate mit der Größe der Läsionen korreliert. Bei zunehmender Metastasengröße stieg die Rezidivrate und das rezidivfreie Intervall sank. Während bei Metastasen kleiner 3 cm Rezidivraten von 24,6 % und bei Metastasen 3-5 cm von 36,4 % beobachtet wurden, stieg die Rate auf 50 % bei Metastasen größer 5 cm. Analog zu den steigenden Rezidivraten sank das rezidivfreie Intervall bei zunehmender Größe (31,4 Mon., 14,1 Mon., 4,5 Mon.). Auch wenn sich hier ein signifikanter Einfluss nicht nachweisen ließ, zeigt sich doch eine gewisse Tendenz. Ähnlicher Ergebnisse werden auch nach Radiofrequenzablation berichtet. Bei Tumoren unter 3 cm werden Progressraten von 11 % und bei Tumoren über 3 cm von 50 % nach RFA erreicht [147]. In einer Studie von Gilliams [30] über die Radiofrequenzablation bei 72 Lungenmetastasen (Follow-up > 6 Monate, mittleres Follow-up: 13 Monate) zeigte sich eine Progressionsrate von 28 % bei Läsionen < 3,5 cm und von 100 % bei Läsionen > 3,5 cm. Eine Abhängigkeit der Größe der Läsion war auch zum technischen Behandlungserfolg zu beobachten. Hinsichtlich der Metastasengröße nahmen die erzielten technisch kompletten Ablationen mit zunehmender Größe der behandelten Metastasen drastisch ab. Während 88 % aller Metastasen kleiner 3 cm und noch 77 % aller Metastasen zwischen 3 und 5 cm technisch erfolgreich behandelt werden konnten, lag die Erfolgsrate bei Metastasen größer 5 cm nur noch bei 17 %. Der Einfluss der Metastasengröße auf den technischen Behandlungserfolg war in unserer Studie signifikant und sollte eine Größe von 2,1 cm nicht überschreiten. Ein Grund für die sinkenden technischen Erfolgsraten und steigenden Rezidivraten bei zunehmender Metastasengröße liegt in einer Diskrepanz zwischen der Geometrie der Läsion und der Geometrie der durch die Laserablation induzierten Nekrose. Es ist von essentieller Bedeutung eine ausreichend große Ablationszone zu erzielen, innerhalb der sämtliche Zellen letal geschädigt werden. Rezidiventstehungen bei thermischen Ablationsverfahren treten insbesondere in der Übergangszone der Ablation auf. Wird keine ausreichende Überlappung des Thermoläsionsvolumens über die ursprüngliche Tumorgröße hinaus erzielt, steigt die Wahrscheinlichkeit für das Auftreten eines Rezidivs [33, 132]. Aufgrund der diffusen Tumorinfiltration bei Metastasen wird daher allgemein ein thermischer Sicherheitsabstand 74 von mindestens 5 mm gefordert. Methodenbedingt sinkt bei größeren Läsionen wegen der Abhängigkeit von der Wärmeleitfähigkeit im Gewebe der Effekt der Laserablation mit Ausbildung einer Totalnekrose deutlich. Aus den Daten unserer Studie ergibt sich der Schluss, dass pulmonale Metastasen bis 3 cm Durchmesser mit hoher Erfolgsrate behandelt werden können. Metastasen mit einem Durchmesser größer 5 cm sind derzeit für eine Behandlung mittels initialer Lasertherapie ungeeignet. In diesen Fällen sind MehrfachApplikationen und möglicherweise wiederholte Eingriffe erforderlich. Dabei hängt der Erfolg der Laserablation von der Verteilung der Laserapplikatoren im Tumor ab. Begrenzt ist der Einsatz von Mehrfach-Applikatoren durch erhöhte Punktionsrisiken, durch anatomische Gegebenheiten und durch eine erhöhte Wärmeabfuhr infolge erhöhter Blutungsneigung. Problematisch erweist Temperaturverteilung sich im bei der Zielvolumen. Laserablation Diese vor entsteht allem durch die die inhomogene unterschiedliche Wärmeleitfähigkeit der verschiedenen Gewebearten in Tumor und Lungengewebe sowie der in der Lunge enthaltenen Luft. Darüber hinaus bilden sich in den Bereichen mit geringster Wärmeleitfähigkeit „Hotspots“, die zu einer lokalen Karbonisierung führen können. Die außergewöhnlich Inhomogenität geringe der Wärmeleitfähigkeit Temperaturverteilung karbonisierten aufgrund der Gewebes Bildung von verstärkt die sogenannten Wärmeschatten. Dies führt zu einer unregelmäßigen Nekrosezone und zu einem Anstieg der Wahrscheinlichkeit, dass Tumorzellen auch innerhalb des Koagulationsvolumens vital bleiben. Abb. 45 Entstehung der Inhomogenität der Temperaturverteilung im Tumorgewebe 75 Damit hat die Laserablation ähnliche Inhomogenitäts-Probleme wie die Radiofrequenzablation. Eine wesentliche Limitation des Einsatzes der Radiofrequenztherapie stellt die sichere Induktion einer Thermoläsion ohne die Gefahr von unkontrollierten elektrischen Energieflüssen dar. Bei der Radiofrequenzablation werden durch unkontrollierte Strompfade Hitzeentwicklungen an ungewollten Orten, insbesondere in der Randzone des Tumorübergangs zum Lungenparenchym, beobachtet. Dieses Problem tritt bei der Laserablation nicht auf. Das Problem beider thermischen Ablationsverfahren besteht somit in der Kontrolle der gezielten Hitzeentwicklung. Hierbei ist die Laserablation durch die Möglichkeit der Induktion größerer Ablationsvolumina der Radiofrequenzablation im Vorteil [132]. Außerdem ist die bildgebende Beobachtung der Ausbreitung der Thermonekrose bei der Radiofrequenzablation schwierig. In der Computertomographie ist sie nicht ausreichend sichtbar, und eine MRT-gesteuerte Überwachung ist aufgrund der Entstehung von Bildartefakten durch den Wechselstrom problematisch [19]. Bei der Laserablation ist die Nutzung der Magnetresonanztomographie und ihrer vorteilhaften Thermometrie zur noch exakteren Kontrolle der Ablationszone grundsätzlich möglich. Allerdings ist die MRTBildgebung der Lunge mit derzeitigen MR-Techniken noch schwierig und bleibt bisher Ausnahmefällen vorbehalten. Durch neuentwickelte Geräte und Programme mit schnellerer Sequenzerstellung und MRT-geeigneten Applikatorsystemen soll dieses Problem in der Zukunft gelöst werden. 76 4.2 Komplikationen Wie bei jedem invasiven Eingriff sind bei der perkutanen Laserablation unerwünschte Nebenwirkungen nicht auszuschließen. So sind vor allem Punktionsrisiken wie Pneumothorax (teilweise drainagepflichtig), Lungenparenchymblutungen und Hämoptysen zu nennen. Die Komplikationsrate nach Laserablation der Lunge ist gering und zeigt kein signifikant höheres Auftreten von interventionell bedingten Komplikationen und Nebeneffekten im Vergleich mit der täglichen Routine diagnostischer Lungenbiopsien [136]. Häufigste Komplikation in unserer Studie war das Auftreten eines Pneumothorax. Die Pneumothoraxrate lag bei 38 % und damit insgesamt in dem Bereich, der bei anderen perkutan bildgesteuerten Thermoablationsverfahren beobachtet werden kann. So wird in der Literatur nach Radiofrequenzablation von Pneumothoraxraten von 29 % - 52 % berichtet [46, 47, 72, 85, 121, 122, 148], nach Mikrowellenablation von 39 % [143] und nach Kryoablation von 50 % [60]. Im Vergleich zu anderen Gruppen war jedoch mit 5 % die Anzahl der Drainagenanlagen zur Behandlung eines Pneumothorax in unserer Patientenpopulation gering. Andere Autoren berichteten über eine Drainagenanlage in bis zu 40 % der Behandlungen [46, 47, 72, 85, 121, 122, 148]. In einer Multicenter-Studie zu Ergebnissen der Radiofrequenzablation von pulmonalen Metastasen mit insgesamt 493 Fällen trat ein Pneumothorax in bis zu 30% aller Fälle auf, 10 % waren drainagepflichtig [123]. Auch Hiraki et al. [47] untersuchten die Risiken der Radiofrequenzablation primärer und sekundärer Lungentumore. In einer retrospektiven Studie wurden 224 Ablationsbehandlungen für 392 Tumore bei 142 Patienten untersucht. In 52 % aller Behandlungen trat ein Pneumothorax auf, 7 % waren behandlungsbedürftig und wurden durch eine Drainage versorgt. Parenchymblutungen traten in unserer Studie in 13 % aller Behandlungen auf und liegen damit im Bereich der Ergebnisse nach Radiofrequenz- und Kryoablation [60, 148]. Die Blutungen waren in allen Fällen selbstlimitierend und führten in 7 % zu temporären Hämoptysen. Ähnliche Hämoptysenraten werden auch nach perkutaner Mikrowellenablation (6 %) beobachtet [143]. Die Daten nach Radiofrequenzablation pulmonaler Metastasen schwanken je nach Studie zwischen 2,7 % und 20 % [72, 121, 122, 147], ein hohes Auftreten 77 von Hämoptysen berichten Peters et al. [98] nach der Brachytherapie und Kawamura et al. [60] nach Kryoablation. In beiden Studien betrug die Rate bei 36 %. Kleine, nicht therapiebedürftige Pleuraergüsse traten in unserer Studie bei 19 % aller Behandlungen auf. Gleiche Ergebnisse werden auch von Hiraki et. al. [47] nach Radiofrequenzablation berichtet. Autor Jahr Pneumothorax / Drainage Hämoptysen Yamakado [147] 2007 37 % / 20 % 20 % Simon [121] Hiraki [46] Yan [148] 2007 2007 2006 28,4 % / 9,8 % 49 % / 3 % 29 % / 16 % 2,7 % Lee [72] Steinke [122] Morris [85] Wolf [143] 2004 2004 2002 2008 36 % / k.A. 43 % / 7 % 50 % / 40 % 39 % / k.A. 3,3 % 9% Kawamura [60] 2006 50 % / k.A. 36 % Weigel [137] Vogl [128] 2006 2004 35 % / 7% 9,8 % / 7 %. 10,5 % Pleuraerguss Infektion Sonstige Therapieart 20 % mild, 1% stark 2,2 % Empyem: 1,5 % Radiofrequenzablation 15 % 7% Parenchymblutung: 9 % 5% 10 % 6% Hautbrennen: 8% Parenchymblutung: 12 % 23 % 1% Mikrowellenablation Kryoablation Laserablation Tab. 8 Komplikationsraten minimalinvasiver Behandlungsmethoden primärer und sekundärer Lungentumore Weigel et al. [127] berichteten 2006 von einer Pneumothoraxrate von 35 %, insgesamt waren 7 % behandlungsbedürftig und wurden durch eine Drainage versorgt. In 23 % der Fälle wurde ein Pleuraerguss, in 12 % Parenchymblutungen und in 10,5 % Hämoptysen beobachtet. Eine Infektion trat in 1 % aller Fälle auf. Auch eine Behandlungsserie von Vogl et al. [128] verlief ohne klinisch schwerwiegende Komplikationen. 86 % der Patienten (n=26) tolerierten die Therapiesitzungen ohne wesentliche Nebenwirkungen oder Einschränkungen. Bezogen auf die Anzahl der Sitzungen (n=41) betrug die Pneumothoraxrate 9,8 %, bei zwei Patienten (7 %) musste eine Thoraxdrainage gelegt werden. Ein Patient hatte postinterventionell schwere Schmerzen, die mittels intravenöser Analgetika und oraler Medikation beherrscht werden konnten und ein weiterer Patient mit Bronchialkarzinom erlitt 10 Stunden nach der Therapie eine Blutung, die eine Thorakotomie mit Lungenresektion erforderlich machte. Die Mortalität der Eingriffe lag in unserer Studie bei 0 %, während in der Literatur eine operationsassoziierte Mortalität zwischen 1 % und 4 % angegeben wird [1, 43, 61, 66, 99, 78 115]. Eine verfahrensbedingte Mortalitätsrate von 2,6 % nach Radiofrequenzablation wird bei Simon et. al. berichtet, nachdem 4 von 153 Patienten therapiebedingt verstarben [121]. Im Vergleich zur chirurgischen Resektion führt der Einsatz perkutaner Ablationsverfahren zu einer deutlich verkürzten Hospitalisierung. Wird die mittlere Hospitalisierungsdauer nach einem operativen Eingriff mit 6-12 Tagen [41, 97] und nach Brachytherapie mit 3-5 Tagen [29] angegeben, können nach Behandlung mittels thermischer Ablationsverfahren die Patienten das Krankenhaus in der Regel schon einen Tag nach dem Eingriff verlassen. Die mittlere Hospitalisierungsdauer nach Laserablation in unserer Studie betrug 2 Tage, ähnliche Zeiten werden auch nach einer Radiofrequenzablation mit ebenfalls 2 Tagen (Range 1-13 Tage) [85, 122, 148] und nach Kryoablation mit 2,6 Tagen [60] berichtet. In einer Studie über die transpulmonale Chemoembolisation pulmonaler Metastasen konnte die Mehrheit der Patienten (94,2 %) das Krankenhaus noch am gleichen Tag verlassen [129]. 79 4.3 Kritische Anmerkungen Verschiedene Punkte müssen bei der Betrachtung der Studie kritisch hinterfragt werden. Die Studie basiert auf einem ungleichen Patientenkollektiv mit teilweise geringen, unzensierten krankheitsbezogenen Falldaten. Die Resultate konnten nicht mit dem Alter, der Co-Morbidität und der Art einer früheren Chemotherapie in Beziehung gesetzt werden. Weiterhin wurden die Überlebensdaten nicht mit prospektiven, randomisierten Studiengruppen verglichen. Wenn neudiagnostizierte Lungenknötchen bei Patienten auftraten, die einen malignen Primärtumor mit bevorzugter Lungenmetastasierung aufwiesen, konnte im Einzelfall die Diagnose von pulmonalen Metastasen auch ohne histologischen Nachweis erfolgen. Demzufolge wurden vor der eigentlichen Therapie nicht alle Patienten biopsiert. In einigen Fällen wurden eingelesene externe CT’s und Informationen durch Telefonate mit Patienten und behandelten Ärzten in die Datensammlung mit einbezogen. Nur 12,5 % der in der Studie einbezogenen Patienten wiesen synchrone Metastasen auf. Die Mehrzahl der Patienten hatten metachron auftretende Metastasen. Da die meisten der Patienten eine vorherige und/ oder in geringen Fällen zeitgleiche adjuvante Chemotherapie erhielten, kann der alleinige Effekt der Laserablation nicht zuverlässig bestimmt werden. Das Vorenthalten einer Chemotherapie wäre bei Patienten mit systemischer Metastasierung ethisch bedenklich. Daher favorisieren und empfehlen wir für alle unsere Patienten eine begleitende systemische Therapie, auch hinsichtlich einer Vermeidung eines Rezidivs. Wie auch aus anderen Gruppen mit vergleichbaren Patientenkollektiven berichtet, könnte es einen synergetischen Effekt von Laserablation und Chemotherapie geben. So berichtet eine multimodale Therapiestudie von 3-Jahres-Überlebensraten von 33,3 % mit alleiniger Chemotherapie und 87,5 % bei der Kombination von Chemotherapie und Radiofrequenzablation bei Patienten mit pulmonalen Metastasen des kolorektalen Karzinoms [56]. Multizentrische Studien, idealerweise in homogenen Patientenpopulationen, sind für eine weitere Validerung der hier präsentierten Resultate entscheidend. Inwieweit die Laserablation bei primär resektablen Metastasen Operation ersetzen können, ist weiterhin fraglich und muss noch in prospektiv randomisierten Studien geklärt werden. 80 4.4 Schlussfolgerungen Die erzielten Ergebnisse dieser Studie zeigen, dass mittels Laserablation pulmonale Metastasen komplikationsarm und minimalinvasiv in situ zerstört werden können und eine Steigerung der Überlebenszeit für Patienten möglich ist. Es konnten Aussagen zum Einfluss des Verfahrens auf die Überlebenszeit getroffen werden, so dass dieser neue Therapieansatz zur Behandlung primärer und sekundärer Lungentumore in prospektiven Studien weiter evaluiert werden sollte. Die Laserablation kann sich ähnlich erfolgreich im klinischen Alltag etablieren wie die bereits heute weit verbreitete Laserablation von Lebermetastasen [138]. Da bislang noch keine evidenzbasierten Daten aus großen Studienreihen vorliegen, wird sie derzeit nur zur palliativen Behandlung eingesetzt und kann nicht als ein konkurrierendes Verfahren zur thoraxchirurgischen Therapie eingeschätzt werden [108]. Im Gegensatz zu unserer Studie wurden die Ergebnisse nach Operation in sehr homogenen Patientengruppen mit harten Einschlusskriterien erzielt. Somit ist zu erwarten, dass die Überlebensraten nach Laserablation in weiterführenden Studien mit härteren Einschlusskriterien und homogeneren Patientengruppen noch bessere Ergebnisse zeigen würden. Ein entscheidender Einflussfaktor auf die Überlebenszeiten und die Rezidivraten ist der technische Gesamtbehandlungserfolg, welcher in unserer Studie maßgeblich von der Anzahl der Lungenmetastasen (nicht mehr als 2) und der Tumorgröße (nicht mehr als 2,1 cm) abhängt. Um eine erfolgreiche Behandlung zu erreichen, muss eine 100 %ige Abtragung der zu behandelnden Läsionen erzielt werden. Eine teilweise Tumorablation kann kein zufriedenstellendes Therapieergebnis darstellen und muss eine weitere Intervention bis zur kompletten Ablation zur Folge haben. Mit dem jetzigen Stand der Technik ist die Wärmeentwicklung durch das Strahlungsfeld des Lasers nicht mit Sicherheit über das gesamte Volumen des Tumors steuerbar, wodurch auch mit dieser Methode bei komplexen Tumorformen eine komplette Ablation nicht immer sicher erreicht werden kann. Dennoch ist im Vergleich zur Radiofrequenztherapie eine gezieltere Ablation möglich. Für inoperable Tumorpatienten, für die sich weder Chemo- noch Strahlentherapie als alternative Therapieformen erwiesen haben, bietet das Verfahren schon jetzt eine therapeutische Möglichkeit, die Überlebenszeit bei verbesserter Lebensqualität zu verlängern. 81 Die unzureichende Vergleichbarkeit der minimalinvasiven Verfahren führt dazu, dass sich die Anerkennung und Validierung der thermoinduzierten Lasertherapie verzögert. Einen Ansatz zur Vergleichbarkeit machen Goldberg et al. durch eine Standardisierung der Definitionen und Terminologien zur Auswertung lokalablativer Verfahren als auch in der Festlegung von Einschlusskriterien [32]. Erst durch die Verwendung einheitlicher Begriffe und Kriterien wird eine vergleichende Bewertung der unterschiedlichen Therapiekonzepte möglich. Somit muss eine tiefgreifende Bewertung innerhalb der verschiedenen minimalinvasiven Verfahren auf einen späteren Zeitpunkt fallen. 82 5 ZUSAMMENFASSUNG Bei vielen onkologischen Krankheitsbildern stellt das Vorhandensein und Ausmaß eines Lungenbefalls den das Überleben limitierenden Faktor dar. Die chirurgische Resektion der Lungenmetastasen ist derzeit die einzige potentiell kurative Behandlung. Da bei vielen Patienten aufgrund von Komorbiditäten eine Resektion nicht möglich ist, wurden in den letzten Jahren alternative lokalablative Behandlungsmethoden wie die Laserablation entwickelt, die parenchymsparend, komplikationsarm und potentiell wiederholbar sind und zu einer Steigerung der Überlebenszeit und Verbesserung der Lebensqualität für inoperable Patienten führen können. Aussagen über Langzeiterfolge konnten aufgrund zu kleiner Patientenzahlen und zu geringer Nachbeobachtungszeiträume bisher nicht getroffen werden. Ziel dieser retrospektiven Untersuchung ist die Beurteilung des therapeutischen Potentials der Laserablation bei Patienten mit pulmonalen Metastasen unterschiedlicher Primärtumore anhand von Langzeitergebnissen. Die Studie basiert auf 64 Patienten mit insgesamt 108 behandelten Lungenmetastasen, die im Universitätsklinikum Greifswald in 129 Therapiesitzungen mittels Laserablation therapiert wurden. Für die Behandlungen wurden ein Nd-YAG-Laser (1064 nm) und spezielle Power-Laser-Applikationssysteme perkutan eingesetzt. Alle 64 Patienten tolerierten die Therapie unter Lokalanästhesie und Analgosedierung gut. Die Mortalitätsrate betrug 0 %. Das Auftreten eines Pneumothorax war die häufigste Komplikation während der Laserablation. Insgesamt trat er in 49/129 Ablationssitzungen auf (38 %). In 5 % der Fälle (7/129) handelte es sich um einen behandlungsbedürftigen Pneumothorax, der während der Intervention mittels Drainagenanlage therapiert wurde. Paremchymblutungen kamen in 13 % der Therapiesitzungen vor und waren in allen Fällen selbstlimitierend, in 7 % führten sie zu temporären Hämoptysen. Kleine reaktive Pleuraergüsse traten in 24/129 Fällen (19 %) auf. Diese waren nicht therapiebedürftig. Klinisch relevante Komplikationen, die zu einer verlängerter Hospitalisierung, unerwartetem gesteigerten Behandlungsaufwand oder zu einer stationären Wiederaufnahme führten traten in nur 3 Fällen (2 %) auf. In der Erstbehandlung konnten 78 % aller Metastasen komplett technisch erfolgreich behandelt werden. Das mediane Gesamtüberleben aller Patienten betrug 23,1 Monate (95 % 83 Konfidenzintervall, 11,8 – 34,5 Monate) mit 1-, 3- und 5-Jahres-Überlebensraten von 69 %, 30 % und 18 %. In der Gruppe der komplett erfolgreich behandelten Patienten betrug die mediane Überlebenszeit 32,4 Monate (95 % KI, 17,5 – 47,3 Monate) mit 1-, 2- und 5-JahresÜberlebensraten von 81 %, 44 % und 27 %. Die Ergebnisse der vorliegenden Studie zeigen einen signifikanten Einfluss der Metastasenanzahl (Median 2) und der Metastasengröße (Median 2,1 cm) auf den technischen Behandlungserfolg. Die Erfolgsrate lag bei pulmonalen Metastasen < 3 cm bei 88 %, bei Metastasen zwischen 3 und 5 cm bei 77 % und bei Metastasen > 5 cm bei 17 %. Mit zunehmender Metastasengröße stieg die Rezidivrate und das rezidivfreie Intervall sank. Die Rezidivrate bei Metastasen < 3 cm betrug 24,6 %, bei Metastasen 3-5 cm 36,4 % und 50 % bei Metastasen > 5 cm. Mit zunehmender Größe der Metastasen sank das rezidivfreie Intervall (31,4 Mon., 14,1 Mon., 4,5 Mon.). Unterschiedliche Primärtumore zeigen unterschiedliche Tendenzen hinsichtlich der Verbesserung der Überlebenszeiten nach Laserablation. So scheinen pulmonale Metastasen mit einem Primärtumor der HNO-Region in unserer Studie am meisten von der Lasertherapie zu profitieren. Allerdings war der Einfluss des Primärtumors auf die Überlebenszeiten in unserer Studie bei geringen Patientenzahlen nicht signifikant und muss in folgenden Studien weiter evaluiert werden. Die Ergebnisse nach 5 Jahren Erfahrung in unserer Studie lassen den Schluss zu, dass die perkutane Laserablation ein effektives Verfahren zur technisch erfolgreichen Behandlung von Lungenmetastasen mit einer Anzahl nicht mehr als 2 und einer Tumorgröße von nicht mehr als 2,1 cm darstellt. Bei einer technisch erfolgreichen Gesamtbehandlung kann eine deutliche Erhöhung der Überlebenszeiten und Senkung der Rezidivraten bei gleichzeitig schonendem und auch beliebig oft zu wiederholendem Therapieerfahren für inoperable Patienten erzielt werden. 84 6 LITERATURVERZEICHNIS [1] Abecasis N, Cortez F, Bettencourt A, Costa CS, Orvalho F, de Almeida. Surgical treatment of lung metastases: prognostic factors for long-term survival. J Surg Oncol 1999 Dec; 72(4):193-8 [2] Akeboshi M, Yamakado K, Nakatsuka A, Hataji O, Taguchi O, Takao M, Takeda K. Percutaneous radiofrequency ablation of lung neoplasms: initial therapeutic response. J Vasc Interv Radiol. 2004 May; 15(5): 463-470 [3] Albert M. Einfluss der Cisplatin-Konzentration auf die Lungenfunktionsparameter im Rahmen der isolierten Lungenperfusion. Dissertation an der Medizinischen Fakultät der Friedrich-Schiller-Universität Jena [4] Ambrogi MC, Lucchi M, Dini P, Melfi F, Fontanini G, Faviana P, Fanucchi O, Mussi A. Percutaneous radiofrequency ablation of lung tumors: results in the mid-term. Eur J Cardiothorac Surg 2006; 30: 177-183 [5] Bechstein WO, Gog C, Wullstein . Therapie des synchron metastasierten Rektumkarzinoms. Viszeralchirurgie 2006; 41: 338-341 [6] Birth M, Hildebrand P, Dahmen G, Ziegler A, Broring DC, Hillert C, Bruch HP. Aktueller Stand der Radiofrequenzablationen von Lebertumoren – eine deutschlandweite Umfrage. Chirurg 2004, 75(4): 417-423 [7] Börgermann C, Luboldt HJ, Schröder FH, Fornara P: Prostatakrebs - Screening und Früherkennung. In: Rübben H(Hrsg.): Uroonkologie. Springer Verlag: Berlin, New York 2007, 4. Auflage: 407 [8] Böttger T, Engelmann R, Seifert JK, Löw R, Junginger T. Preoperative diagnostics in pancreatic carcinoma: would less be better? Langenbeck’s Arch Surg 1998; 383: 243-248 [9] Bown SG. Phototherapy of tumors. World J Surg. 1983 Nov; 7(6): 700-709 [10] Brown W, Xiadong W, Fowler JF, Garcia S, Fayad F, Amendola BE, de la Zerda A, Schwade JG. Lung Metastases Treated by CyberKnife Image-Guided Robotic Stereotactic Radiosurgery at 41 Months. Southern Medical Journal 2008; 101(4): 376-382 [11] Bumm R. Klinikmanual Chirurgie. Chirurgische Klinik der TU München (im Web: http://h568612.serverkompetenz.net/kman/content/index_ger.html (Stand 5.8.2009)) [12] Casali C, Stefani A, Storelli E, Morandi U. Prognostic factors and survival after resection of lung metastases from epithelial tumors. Interact Cardiovasc Thorac Surg. 2006. Jun; 5(3): 317-321 85 [13] Cheuk-Kin Lo, Colin SH Chu, Tong Zhu, Chan-Chung Ma, Kai-Ming Ko, Kwok-Keung Ho. Pulmonary resection for metastases from colorectal cancer. Surgical Practice 2007; 11(4): 147-153 [14] De Giacomo T, Rendina EA, Venuta F, Ciccone AM, Coloni GF. Thoracoscopic resection of solitary lung metastases from colorectal cancer is a viable therapeutic option. Chest 1999; 115: 1441-1443 [15] Dienemann H. Lungenmetastasen, in: Siewert JR, Harder F, Rothmund M (Hrsg): Praxis der Viszeralchirurgie, Siewert JR (Bandhrsg.) Onkologische Chirurgie. Berlin, Heidelberg, New York: Springer Verlag 2001 [16] Dienemann H, Hof H, Debus J, Drings P. Lungenmetastasen. Der Onkologe 2004; 10(5): 458–473 [17] Drings P, Vogt-Moykopf I (Hrsg). Die Chemotherapie des Bronchialkarzinoms – Thoraxtumoren Diagnostik . Staging – Therapiekonzept. Springer, Berlin, Heidelberg, New York. 1991: 219-230 [18] Dupuy DE, Zagoria RJ, Akerley W et al.: Percutaneus radiofrequency ablation of malignancies in the Lung. Am J Roentgen 2000; 174:57-59 [19] Eckert UC. Charakteristik von Koagulationsnekrosen nach laserinduzierter Thermotherapie (LITT) und deren Einfluss auf den Therapieerfolg. Dissertation an der Klinik für Strahlenheilkunde der Medizinischen Fakultät der Charite-Universitätsmedizin Berlin und der Abteilung für Diagnostische und Interventionelle Radiologie der Medizinischen Fakultät der Ernst-Moritz-Arndt-Universität Greifswald, 12/2005 [20] Einzmann T: Ätiologie und Diagnostik prämaligner und maligner Erkrankungen der Zervix und der Vulva. Vortrag am 2.11.2007 [21] Ernst S. Ergebnisse der Laserinduzierten Thermotherapie (LITT) in der Behandlung von Lebertumoren, Dissertation an der Klinik für Strahlenheilkunde der Medizinischen Fakultät der Charite, Berlin 02/2003 [22] Fielding DI, Buonaccorsi G, Hanby A, Hetzel MR., Bown SG. Preclinical Studies on the use of Interstitial Laser Photocoagulation in the Lung parenchyma, in: Altshuler GB, Chieso F, Geschwind HJ, Hibst R, Klasner N, Latifette F, Maira G, Neumann R, Pini R, Reidenbach HD, Roggan A. Montserrat S.I.M. (Hrsg.) Proceedings in Laser Applications in Medicine and Dentistry. Bellingham: SPIE Press 1996 [23] Fielding DI, Buonaccorsi G. Hanby A, Hetzel MR, Bown SG: Interstitial laser photocoagulation of normal lung parenchyma in rats, Thorax 1998; 53: 692-697 86 [24] Fielding DI, Buonaccorsi G, Cowley G, Johnston AM, Hughes G, Hetzel MR, Bown SG. Interstitial Laser Photocoagulation of Normal Lung Parenchyma in the Pig. Lasers Med Sci 2001; 16: 26-33 [25] Fielding DI, Buonaccorsi GA, MacRobert AJ, Hanby AM, Hetzel MR, Bown SG. FineNeedle Interstitial Photodynamic Therapy of the Lung Parenchyma, Chest 1999; 115:502-510 [26] Friedel G, Kyriss T, Zoller J, Pastorino U, Johnston M, Pass H, Putnam JB, Toomes H, Ergebnisse der Lungenmetastasenresektion beim Mammakarzinom: Prognosekriterien basierend auf 467 Fällen des International Registry of Lung Metastases. Onkologie 2003; 26: 41 [27] Friedel G , Pastorino U, Buyse M, Ginsberg RJ, Girard P, Goldstraw P, Johnston M, McCormack P, Pass H, Putnam JB. Long-term result of lung metastasectomy: Prognostic Analyses based on 5206 cases. The International Registry of Lung Metastases. J. Thorac Cardiovasc Surg 1997; 113: 37-49 [28] Fritz P, Kraus HJ, Mühlnickel W, Hammer U, Dölken W, Engel-Riedel W, Chemaissani A, Stoelben E. Stereotactic, single-dose irradiation of stage I non-small cell lung cancer and lung metastases. Radiat. Oncol. 2006 Aug 20; 1: 30 [29] Gebauer B, Denecke T. CT-gesteuerte interstitielle Brachytherapie. Im Web: http://radiologie.charite.de/index.action/cat4_open.cat_oid/427924.page/1.html;jsessionid=a9 uS-GXFwjt6 (Stand: 10.1.2009) [30] Gillams AR, Lees WR. Radiofrequency ablation of lung metastases: factors influencing success. Eur Radiol. 2008 Apr; 18(4): 672-677 [31] Göhl J., Meyer Th. Therapie-Handbuch: Malignes Melanom der Haut. (im Web: www1.us.elsevierhealth.com/THB/chapter_L015.php#section|15009 (Stand: 5.1.2009)) [32] Goldberg SN, Charboneau JW, Dodd GD 3rd, Dupuy DE, Gervais DA, Gillams AR, Kane RA, Lee FT Jr, Livraghi T, McGahan JP, Rhim H, Silverman SG, Solbiati L, Vogl TJ, Wood BJ. Image-guided Tumor Ablation: Proposal for Standardization of Terminology and Reporting Criteria. Radiology 2003; 228:335-345 [33] Goldberg S, Gazelle G, Sompton C. Radiofrequency tissue ablation in the rabbit lung: Efficacy and complications. Acad Radiol 1995; 2: 776-784 [34] Gorenstein LA, Putnam JB, Natarajan G, Balch CA, Roth JA. Improved survival after resection of pulmonary metastases from malignant melanoma. Ann Thorac Surg 1991; 52: 204-210 87 [35] Goya T, Miyazawa N, Kondo H, Tsuchiya R, Naruke T, Suemasu K: Surgical resection of pulmonary metastases from colorectal cancer. 10-year follow up. Cancer Vol.64(7)2006:1418-1421 [36] Graggen K, Biral R, Thüring C, Gwerder C, Furrer T: Das Pankreaskarzinom – Aktuelle Epidemiologie, Diagnostik, Therapie. Der Onkologe 2006; 4: 14-22 [37] Greenall MJ, Magill GB, DeCosse JJ, Brennan MF. Chemotherapy for soft tissue sarcoma. Surg Gynecol Obstet.1986; 162: 193-198 [38] Groeger AM, Kandioler D, Müller MR, End A, Eckersberger F, Wolner E. Survival after surgical treatment of recurrent pulmonary metastases. Eur J Cardiothorac Surg. 1997; 12: 703-705 [39] Gu YK, Fan WJ, Huang JH, Zhang L, Gao F. Efficacy of CT-guided intra-tumoral dehydrated ethanol injection on lung metastasis from liver cancer. Ai Zheng. 2007; 10: 11121115 [40] Gütz S. Pulmonale Metastasen – transthorakale Feinnadelbiopsie. Klinische Zytologie in der Pneumologie – 6. Hallesches Seminar 2007 [41] Hamy A, Baron O, Bennouna J, Roussel JC, Paineau J, Douillard JY: Recection of Hepatic and Pulmonary Metastases in Patients with Colorectal Cancer. American Journal of Clinical Oncology. 24(6):607-609, Dezember 2001 [42] Harpole DH, Johnson CM, Wolfe WG, George SL, Seigler HF. Analysis of 945 cases of pulmonary metastatic melanoma. J Thorac Cardiovasc Surg 1992; 103 (4): 743-750 [43] Hatz RA, Rüttinger D, Strauss T, Graeb C: Chirurgische Intervention bei Lungenmetastasen. Einblicke 2005; 2 [44] He W, Hu X, Wu D, Guo L, Zhang L, Xiang D, Ning B. Ultrasonography-guided percutaneous microwave ablation of peripheral lung cancer. Clinical Imaging 2006 July; 30(4): 234-241 [45] Hechelhammer L, Pfiffner R, Marincek B, Pfammatter T. Perkutane Radiofrequenzablation bei Leber-, Nieren- und Lungentumoren. Schweiz Med Forum 2008; 8(38): 710-712 [46] Hiraki T, Gobara H, Iishi T, Sano Y, Iguchi T, Fujiwara H, Tajiri N, Sakurai J, Date H, Mimura H. Percutaneous Radiofrequency Ablation for Pulmonary Metastases from Colorectal Cancer: Midterm Results in 27 Patients. Journal of Vascular and Interventional Radiology 2007; 18(10): 1264-1269 [47] Hiraki T, Tajiri N, Mimura H, Yasui K, Gobara H, Mukai T, Hase S, Fujiwara H, Iguchi T, Sano Y, Shimizu N, Kanazawa S. Pneumothorax, pleural effusion, and chest tube 88 placement after radiofrequency ablation of lung tumors: incidence and risk factors. Radiology 2006; 241:275-283 [48] Hochster H, Strawderman MH, Harris JE, Atkins MB, Oken M, Skeel RT, Jubelirer SJ, Parkinson D. Conventional dose melphalan is inactive in metastatic melanoma: results of an Eastern Cooperative Oncology study (E 1687). Anticancer Drugs 1999; 10: 245-248 [49] Hof H, Hoess A, Oetzel D, Debus J, Herfarth K. Stereotactic singe-dose radiotherapy of lung metastases. Strahlentherapie und Onkologie 2007; 183(12): 673-678 [50] Hofmann H, Geist C. Geburtshilfe und Frauenheilkunde. Walter de Gruyter 1998:267–72 [51] Hofman HS: Chirurgische Therapie von pulmonalen Metastasen. Thoraxchirurgisches Zentrum Regensburg [52] Hofmann HS, Neef H, Krohe K, Andreev P, Silber PE. Prognostic factors and survival after pulmonary resection of metastatic renal cell carcinoma. Eur Urol. 2005 Jul; 48(1): 77-81 [53] Hongwu Wang, Littrup Peter, YunYou Duan, Yanqun Zhang, Huasong Feng, Zhoushan Nie. Thoracic masses treated with percutaneous cryotherapy: Initial experience with more than 200 procedures. Radiology 2005; 235(1): 289-298 [54] Hosten N, Stier A, Weigel C, Kirsch M, Puls R, Nerger U, Jahn D, Stroszczynski C, Heidecke CD, Speck U. Laser-induced thermotherapy (LITT) of lung metastases: Description of a miniaturized applicator, optimization, and initial treatment of patients, ROFOFORTSCHR RONTG 2003; 175(3): 393-400 [55] Inderbitzi R, Rolle A. Chirurgische Palliation im Thoraxbereich bei primären und sekundären Malignomen. Therapeutische Umschau 2001; 58 (7): 435-441 [56] Inoue Y, Miki C, Hiro J, Ojima E, Yamakado K, Takeda K, Kusunoki M. Improved survival using multi-modality therapy in patients with lung metastases from colorectal cancer: a preliminary study. Oncol Re. 2005; 14(6): 1571-1576 [57] Jaklitsch MT, MeryCM, Lukanich JM, Richards WG, Bueno R, Swanson SJ, Mentzer SJ, Davis BD, Allred EN, Sugarbaker DJ. Sequential thoracic metastasectomy prolongs survival by re-establishing local control within the chest. J Thorac Cardiovasc Surg. 2001; 121: 657-67 [58] Jakse R, Vinzenz: Kopf/Hals Malignome. ACO-ASSO-Manual der chirurgischen Krebstherapie der Österreichischen Gesellschaft für Chirurgische Onkologie (im Web: http://www.aco-asso.at/manual/archiv/kopfhals/kap_b.html (Stand 5.8.2009)) [59] Kane JM, Finley JW, Driscoll D, Kraybill WG, Gibbs JF. The treatment and outcome of patients with soft tissue sarcomas and synchronous metastases. Sarcoma. 2002; 6(2): 69-73 [60] Kawamura M, Izumi Y, Tsukada N, Asakura K, Sugiura H, Yashiro H, Nakano K, Nakatsuka S, Kuribayashi S, Kobayashi K. Percutaneous cryoablation of small pulmonary 89 malignat tumors under computed tomographic guidance with local anesthesia for nonsurgical candidates. The Journal of Thoracic and Cardiovasular Surgery 2006; 131(5): 1007-1013 [61] Kick J, Schelzig H, Heinecke A, Förster R. Lungenmetastasenresektion – Chance oder Risiko?, Zentralbl Chir 2005; 130: 534-538 [62] Knappe V, Mols A. Lasertherapie in der Lunge – Biophysikalischer Hintergrund. Der Radiologe 2004; 44(7): 677-683 [63] Knösel, T. Chromosomale Signaturen und Immunprofile in der Tumorprogression kolorektaler Karzinome. Habilitationsschrift an der Medizinischen Gakultät der Charite – Universitätsmedizin Berlin, 2006:10 [64] Koong HN, Pastorino U, Ginsberg RJ. Is there a role for pneumonectomy in pulmonary metastases? Ann Thorac Surg. 1999; 68: 2039-2043 [65] Köveker G, Böhm P, Bokemeyer C, Budach W, Einsele H, Hoffmann W, Laniado M, Loichat-Makowiec J, Maurer F, Müller-Schauenburg W, Preßler H, Sökler M. Weichgewebsund Knochensarkome bei Erwachsenen – Empfehlungen zur Diagnostik, Therapie und Nachsorge, Hrsg: Tumorzentrum der Eberhard-Karls-Universität Tübingen 1998 [66] Kraus D. Chirurgische Therapie bei Lungenmetastasen. Nürnberger Fortbildungskongress 2006. Repetitorium Chirurgie [67] Krebs in Deutschland 2003-2004 Häufigkeiten und Trends. Eine gemeinsame Veröffentlichung des Robert-Koch-Instituts und der Gesellschaft der epidemiologischen Krebsregister in Deutschland e.V. 6. überarbeitete Auflage, 2008 [68] Küfer R. Metastasenchirurgie beim Nierenzellkarzinom. Vortrag auf 5. Onkologisches Kolloquim Nierenzellkarzinom. 2007 [69] Ladanyi, A. Detection of Circulating Tumor Cells in the Peripheral Blood of Solid Tumor Patients. Dissertation an der Semmelweis University Budapest 2007: 135 [70] Landreneau RJ, DeGiacomo T, Mack MJ, Hazelrigg SR, Ferson PF, Keenan RJ, Luketich JD, Yim AP, Coloni GF. Therapeutic video-assisted thorascopic surgical resection of colorectal pulmonary metastases. Eur J Cardiothorc Surg 2000; 18(6): 671-677 [71] Lanza LA, Putnam Jr JB, Benjamin RS, Roth RA. Response to Chemotherapy does not predict survival after resection of sarcomatous pulmonary metastases. Ann Thorac Surg. 1991; 51: 219-224 [72] Lee JM, Gin GY, Goldberg SN, Lee YC, Chung GH, Han YM, Lee SY, Kim CS. Percutaneous radiofrequency ablation for inoperable non-small cell lung cancer and metastases: preliminary report. Radiology 2004; 230: 125-134 90 [73] Lee WS, Yun SH, Chun HK et al: Pulmonary resection for metastases from colorectal cancer: prognostic factors und survival. International Journal of Colorectal Disease Vol.22 (6) 2007: 699-704 [74] Lencioni R, Crocetti L, Cioni R, Suh R, Glenn D, Regge D, Helmberger T, Gillams AR, Frilling A, Ambrogu M, Bartolozzi C, Mussi A. Response to radiofrequency ablation of pulmonary tumors: a prospective, intention-to-treat, multicentre clinical trial. Lancet Oncol. 2008; 9(7): 621-628 [75] Leo F, Cagini L, Rocmans P, Cappello M, Van Gell AN, Maggi G, Goldstraw P, Pastorino U. Lung metastases from melanoma: when is surgical treatment warranted? Bristish Journal of Cancer 2000; 83: 569-572 [76] Lindemayr S, Lehnert T, Korkusuz H, Hammerstingl R, Vogl TJ. Transpulmonary Chemoembolization: A Novel Approach for the Treatment of Unresectable Lung Tumors. Tech Vasc Interventional Rad 2007; 10: 114-119 [77] Lindner M, Strauss T. Chirurgie von Lungenmetastasen, in: Tumoren der Lunge und des Mediastinums, Tumorzentrum München und W. Zuckschwerdt Verlag München 2006, 78-84 [78] [142] Lu MD, Chen JW, Xie XY, Liu L, Huang XQ, Liang LJ, Huang JF. Hepatocellular carcinoma: US-guided percutaneous microwave coagulation therapy. Radiology 2001; 221: 162-172 [79] Mahnken AH, Bruners P, Günther RW. Techniken der interventionellen Tumortherapie. Deutsches Ärzteblatt 2008; 105(38): 646-653 [80] McGahan JP, Browning PD, Brock JM, Tesluk H. Hepatic ablation using radiofrequency electrocautery. Invest Radiol 1990; 25:267-270 [81] Mentzer SJ, Antman KH, Attinger C, Shemin R, Corson JM, Sugarbaker DJ: Selected benefits of thoracotomy and chemotherapy for sarcoma metastatic to the lung. J Surg Oncol 1993 May,53(1)54-9 [82] Mountain CF, McMurtrey MJ, Hermes KE. Surgery for pulmonary metastases: a 20-year experience. Ann Thorac Surg. 1984; 38: 323-330 [83] Liu D, Abolhoda A, Burt ME, Martinin N, Bains MS, Downey RJ, Rusch W, Bosl GJ, Ginsberg RJ. Pulmonary metastasectomy for testicular germ cell tumor:A 28-year experience. Ann Thorac Surg 1998; 66: 1709-1714 [84] Meimarakis M, Winter H, Hoffmann G, Zilbauer A, Rüttinger D, Piltz S, Jauch KW, Hatz R, Löhe F: Langzeitergebnisse und Prognosefaktoren nach Resektion pulmonaler Metastasen beim Nierenzellkarzinom. Deutsche Gesellschaft für Chirurgie. 124. Kongress der 91 Deutschen Gesellschaft für Chirurgie. München, 01.-04.05.2007. Düsseldorf, Köln: German Medical Science; 2007. Doc 07dgch7753 [85] Morris DL, King J, Zhao J, Glenn D, Clarke W, Clingan P. Percutaneous imaging-guided radio frequency ablation (RFA) of metastastic colorectal cancer (CRC) in lung. Proc Am Soc Clin Cncol 2002; 21: (abstr 2216) [86] Müller MR, Salat A, Murabito, Staffen A. Verbesserte Prognose durch chirurgische Entfernung isolierter Lungenmetastasen nach Mammakarzinom. Geburtsh Frauenheilk 1998; 58(11): 609-613 [87] Müller MR, Stangl P, Salat A, Böhm D, Pulaki S, Kandioler D, Gröger A, Klepetko W, Eckersberger E, Wolner E. Chirurgische Behandlung von Lungenmetastasen. European Surgery 1996; 28(2): 86-90 [88] Musial A. Nierenzellkarzinom – Möglichkeiten der lokalen Therapie und Therapieoptionen bei metastasierter Erkrankung. Im Web: www.dkfz.de/tzhdma/texte/tzmahe2000e.doc (Stand: 18.5.2009) [89] Mutsaerts E, Zoetmulder FA, Meijer S, Baas P, Hart Aa, Rutgers EJ. Outcome of thoracoscopic pulmonary metastasectomy evaluated by confirmatory thoracotomy. Ann Thorac Surg 2001; 72: 230-233 [90] Nagakura S, Shirai Y, Yamato Y, Yokoyama N, Suda T, Hatakeyama K. Simultaneous detection of colorectal carcinoma liver and lung metastases does not warrant resection. J Am Coll Surg 2001; 193: 153-160 [91] Neri B, Doni L, Fulignati C, Gemelli MT, Turrini M, Di Cello V, Dominici A, Mottola A, Raugei A, Ponchietti R, Cini G. Gemcitabine plus Epi-doxorubicin as first-line chemotherapy for bladder cancer in advanced or metastatic stage: a phase II. Anticancer Res. 2002 Sep-Oct; 22(5): 2981-2984 [92] Ogata Y, Matono K, Hayashi A. Repeat Pulmonary Resection for Isolated Recurrent Lung Metastases Yields Results Comparable to Those After First Resection in Colorectal Cancer. World J Surg 2005; 29: 363-368 [93] Okuma T, Matsuoka T, Yamamoto A, Oyama Y, Inoue K, Nakamura K, Inoue Y. Factors Contributing to Cavitation after CT-guided Percutaneous Radiofrequency Ablation for Lung Tumors. J Vasc Interv Radiol 2007; 18: 399-404 [94] Okunieff P, Petersen AL, Phillip A, Milano MT, Katz AW, Boros L, Schell MC. Stereotactic Body Radiation Therapy for lung metastases. Acta Oncologica 2006; 45(7): 808817 92 [95] Padda S, Kothary N, Donington J et al.: Complications of Ablative Therapies in Lung Cancer. Clinical Lung Cancer 2008;9(2)122-126 [96] Pass HI, Mew DJ, Kranda KC, Temeck BK, Donington JS, Rosenberg SA. Isolated lung perfusion with tumor necrosis faktor for pulmonary metastases. Ann Thorac Surg.1996; 61: 1609-1617 [97] Pearson AS, Izzo F, Fleming RY, et al.: Intraoperative radiofrequency ablation or cryoablation for hepatic malignancies. Am J Surg 1999; 178: 592-599 [98] Peters N, Wieners G, Pech M, Hengst S, Rühl R, Streitparth F, Lopez Hänninen E, Felix R, Wust P, Ricke J. CT-Guided Interstitial Brachytherapy of Primary and Secondary Lung Malignancies. Strahlentherapie & Onkologie 2008; 184(6):296-301 [99] Pfannschmidt J, Dienemann H, Hoffmann H: Surgical resection of pulmonary metastases from colorectal cancer: a systematic review of published series. Annals of Thoracic Surgery 2007; 84(1):324-338 [100] Pfannschmidt J, Muley T, Hoffmann H, Dienemann H. Prognostic factors and survival after complete resection of pulmonary metastases from colorectal carcinoma: experiences in 167 patients. J Thorac Cardiovasc Surg. 2003 Sep; 126(3): 732-739 [101] Piltz S, Meimarakis G, Wichmann M, Oberneder R, Jauch K.-W, Fürst H. Lungenmetastasenresektion beim Nierenzellkarzinom. Der Urologe 2003; 42(9): 1230-1237 [102] Ratto GB, Civalleri D, Esposito M, Spessa E, Alloisio A, De Cian F, Vannozzi MO. Pleural space perfusion with cisplatin in the multimodality treatment of malignant mesothelioma: a feasibility and pharmakokinetic study. J Thorac Cardiovasc Surg.1999; 177: 759-765 [103] Rau B, Kandioler D, Stamatis G. Lungenmetastasen. In: Gnant M, Schlag PM [Hrsg]: Chirurgische Onkologie: Strategien und Standards für die Praxis. Springer Wien 2008; 133143 [104] Rau B, Roth C, Schnider A, Metzger U. Chirurgie der Lungenmetastasen extrapulmonaler Primärtumore. Schweiz Med Forum 2002; 49: 1166-1170 [105] Ricke J, Wust P, Hengst S, Wieners G, Pech M, Herzog H, Felix R. CT-gesteuerte Brachytherapie von Lungenmalignomen – Technik und erste Ergebnisse. Der Radiologe 2004; 44(7): 684-686 [106] Ricke J, Wust P, Wieners G, Hengst S, Pech M, Lopez Hänninen E, Felix R. CT-guided interstitial single-fraction brachytherapy of lung tumors: phase I results of a novel technique. Chest. 2005; 127(6): 2237-2242 93 [107] Rosenberg C, Puls R, Hegenscheid K, Kühn J, Bollman T, Westerholt A, Weigel C, Hosten N. Laser Ablation of Metastatic Lesions of the Lung: Long-Term Outcome. American Journal of Roentgenology 2009; 192: 785-792 [108] Rosenberg C, Weigel C, Puls R, Hosten N. Klinisches Umfeld, Methodik und Ergebnisse – Perkutane, interventionelle Laserablation von Lungenmetastasen. Klinikarzt 2006; 35(8): 304-209 [109] Rossi S, Buscarini L. Percutaneous ultrasoundguided radiofrequency electrocautery for the treatment of small hepatocellular carcinoma. J Intervent Radiol 1993; 8:97-103 [110] Rossi S, Fornari F, Pathies C, Buscarini L. Thermal lesions induced by 480 KHz localized current field in guinea pig and pig liver. Tumori 1990; 76:54-57 [111] Rothenberg ML. Aktuelle Strategien bei der Behandlung des metastasierten kolorektalen Karzinoms. Onkologie 2000; 23(5): 3-4 [112] Rotolo N, De Monte L, Imperatori A, Dominioni L: Pulmonary resections of single metastases from colorectal cancer. Surgical Oncology, Vol.16: 141-144 [113] Ruf G, Frommhold H, Farthmann EH, Henke M, Engelhardt R, Schäfer HE. Empfehlungen zur standardisierten Diagnostik, Therapie und Nachsorge des Ösophaguskarzinoms, Hrsg: Tumorzentrum Freiburg 2001; 1: 9 [114] Saito Y, Omiya H, Kohno K. Pulmonary metastasectomy for 165 patients with colorectal carcinoma: A prognostic assessment. J Thorac Cardiovasc Surg 2002; 124(5): 1007-1013 [115] Schirren J, Bölükbas S, Bergmann Th, Beqiri S, Trainer St. Die chirurgische Therapie von Lungenmetastasen. Hessisches Ärzteblatt 2006; 5: 319-328 [116] Schmiegel W, Pox C, Reinacher-Schick A, Adler G, Fleig W, Fölsch UR, Frühmorgen, Graeven U, Hohenberger W, Holstege A, Junginger T, Kopp I, Kühlbacher T, Porschen R, Propping P, Riemann JF, Rödel C, Sauer R, Sauerbruch T, Schmitt W, Schmoll HJ, Zeitz M, Selbmann HK. S3-Leitlinie „Kolorektales Karzinom“: Ergebnisse evidenzbasierter Konsensuskonferenzen am 6./7. Februar 2004 und am 8./9. Juni 2007 (für die Themenkomplexe IV, VI und VII). S3-Guideline „Colorectal Cancer“ 2004/2008. Gastroenterol 2008; 46: 37 [117] Schneider P, Foitzik T, Pohlen, Golder W, Buhr HJ. Temporary unilateral microembolization of the lung – a new approach to regional chemotherapy for pulmonary metastases. J Surg Res 2002; 107; 159-166 [118] Schneider P, Kampfer S, Loddenkemper C, Foitzik T, Buhr HJ. Chemoembolization of the lung improves tumor control in a rat model. Clin Cancer Res 2002; 8: 2463-2468 94 [119] Shibata T, Iimuro Y, Yamamoto Y, Maetani Y, Ametani F, Itoh K, Konishi J. Small hepatocellular carcinoma: comparison of radiofrequency ablation and percutaneous microwave coagulation therapy. Radiology 2002; 223: 331-337 [120] Siewert JR (Hrsg). Chirurgie, Springer Verlag: Berlin, New York 2000: 967 [121] Simon CJ, Dupuy DE, DiPetrillo TA, Safran HP, Grieco CA, Ng T. Pulmonary radiofrequency ablation: long-term safety and efficacy in 153 Patients. Radiology 2007; 243: 268-275 [122] Steinke K, Glenn D, King J, Clark W, Zhao J, Clingan P, Morris DL. Percutaneous Imaging-Guided Radiofrequency Ablation in Patients With Colorectal Pulmonary Metastases: 1-Year Follow-Up. Ann Surg Oncol 2004; 11(2): 207-212 [123] Steinke K, Sewell PE, Dupuy D, Lencioni R, Helmberger T, Kee ST, Jacob AL, Glenn DW, King J, Morris DL. Pulmonary radiofrequency ablation – an international study survey. Anticancer Res 2004; 24(1): 339-343 [124] Stier A, Heidecke CD. Die chirurgische Therapie von Lungenmetastasen – Indikationen, Techniken und Ergebnisse. Der Radiologe 2004; 44(7): 715-718 [125] Stroszczynski C, Gaffke G, Gnauck M, Puls R, Hosten N, Speck U, Ricke J, Oettle H, Hohenberger P, Felix R. Aktueller Stand und Entwicklungen der Laserablation in der Tumortherapie. Der Radiologe 2004; 44(4): 320-329 [126] Thanos L, Mylona S, Pomoni M, Athanassiadi K, Theakos N, Zoganas L, Batakis N. Percutaneous radiofrequency thermal ablation of primary and metastatic lung tumors. Eur J Cardiothorac Surg. 2006; 30(5): 797-800 [127] Thomford NR, Woolner LB, Clagett OT. The surgical treatment of metastatic lung tumors in the lung. J Thorac Cardiovasc Surg. 1965; 49: 357-363 [128] Vogl TJ, Fieguth HG, Eichler K, Straub R, Lehnert T, Zangos S, Mack M. Laserinduzierte Thermotherapie von Lungenmetastasen und primären Lungentumoren. Radiologe 2004; 44 (7): 693-699 [129] Vogl TJ, Lehnert T, Zangos S, Eichler K, Hammerstingl R, Korkusuz H, Lindemayr S: Transpulmonary chemoembolization (TPCE) as a treatment for unresectable lung metastases. European Radiology Vol.18(11) November 2008 [130] Vogl TJ, Mack MG, Roggan A. Magnetresonanztomographisch gesteuerte laserinduzierte Thermotherapie von Lebermetastasen. Deutsches Ärzteblatt 2000; 37: 23862391 [131] Vogl TJ, Mack MG, Straub R, Zangos S, Engelmann K, Eichler K. Percutaneous laser ablation of malignant liver tumors. Zentralbl Chir. 2001; 126(8): 571-575 95 [132] Vogl TJ, Straub R, Lehnert T, Eichler K, Lüder-Lühr T, Peters J, Zangos S, Söllner O, Mack M: Percutaneous thermoablation of pulmonary metastases. Experience with the application of laser-induced thermotherapy (LITT) and radiofrequency ablation (RFA), and a literature review]. RoFo: Fortschritte auf dem Gebiete der Röntgenstrahlen und der Nuklearmedizin 176(11):1658-66, 2004 Nov [133] Vogl. TJ, Wetter A, Lindemayr S, Zangos S. Treatment of Unresectable Lung Metastases with Transpulmonary Chemoembolization: Preliminary Experience, Radiology 2005; 234: 917-922 [134] von Hoff DD. Head and Neck Cancer. In Stein JH (Hrsg.): Internal Medicine, Mosby Year Book 1994: 943-947 [135] Warwick R, Page R. Resection of pulmonary metastases from colorectal carcinoma. European Journal of Surgical Oncology 2007; 33: 59-63 [136] Weigel C, Kirsch M, Mensel B, Nerger U, Hosten N. Perkutane laserinduzierte Thermotherapie von Lungenmetastasen: Erfahrungen nach 4-jähriger Anwendung. Radiologe 2004; 44: 700-707 [137] Weigel C, Rosenberg C, Langner S, Fröhlich CP, Hosten N. Laser ablation of lung metastases: results according to diameter and location. European Radiology 2006 Aug; 16(8): 1769-1778 [138] Weigel C, Schuchmann S, Kirsch M, Mensel B, Hosten N. Perkutane Laserablation von Lungenmetastasen - Indikation, technische Durchführung, erste Ergebnisse und Bildbefunde. Radiologe 2004; 44: 491-499 [139] Weigelt B, Peterse JL, van't Veer LJ. Breast cancer metastasis markers and models, Nat Rev Cancer 2005; 5: 591-602 [140] Welcker K, Diemel KD, Halberstadt J, Branscheid D. Einsatz des Nd-YAG Lasers in der Resektion intrapulmonaler Metastasen, Deutsche Gesellschaft für Chirurgie. 122. Kongress der Deutschen Gesellschaft für Chirurgie. München, 05.-08.04.2005. Düsseldorf, Köln: German Medical Science; 2005 [141] Welter S, Jacobs J, Krbek T, Tötsch M, Stamatis G: Pulmonary metastases of breast cancer. When is resection indicated?. Eur J Cardiothorac Surg 2008; 34:1228-1234 [142] Woolley ML, Schulsinger DA, Durand DB, Zeltser IS, Waltzer WC. Effect of freezing parameters (freeze cycle and thaw process) on tissue destruction following renal cryoablation. J Endourol 2002; 16: 519-522 96 [143] Wolf FJ, Grand D, Machan JT, DiPetrillo T, Mayo-Smith W, Dupuy DE. Microwave ablation of Lung Malignancies: Effectiveness, CT Findings, and Safety in 50 Patients. Radiology 2008; 247: 871-879 [144] Wu F, Wang ZB, Chen WZ, Wang W, Gui Y, Zhang M, Zheng G, Zhou Y, Xu G, Li M, Zhang C, Ye H, Feng R. Extracorporeal high intensity focused ultrasound ablation in the treatment of 1038 patients with solid carcinomas in China: an overview. Ultrason Sonochem 2004; 11: 149-154 [145] Wu F, Wang ZB, Zhu H, Chen WZ, Zou JZ, Bai J, Li KQ, Jin CB, Xie FL, Su HB. Extracorporeal high intensity focused ultrasound treatment for patients with breast cancer. Breast Cancer Res Treat 2005; 92: 51-61 [146] Wulf J, Haedinger U, Oppitz U, Thiele W, Müller G, Flentje M. Stereotactic radiotherapy for primary lung cancer and pulmonary metastases: a non-invasive treatment approach in medically inoperable patients. Int J Radiat Oncol Biol Phy. 2004; 60(1):186-196 [147] Yamakado K, Hase S, Matsuoka T, Tanigawa N, Nakatsuka A, Takaki H, Takao M, Inoue Y, Kanazawa S, Inoue Y, Sawada S, Kusunoki M, Takeda K. Radiofrequency Ablation for the Treatment of Unresectable Lung Metastases in Patients with Colorectal Cancer: A Multicenter Study in Japan. JVIR 2007 Mar; 18(3): 393-398 [148] Yan TD, King J, Glenn D, Steinke K, Morris DL. Percutaneous radiofrequency ablation of inoperable pulmonary metastases from colorectal cancer. Journal of Clinical Oncology, 2006 ASCO Annual Meeting Proceedings Part I. 2006; 24(18): 3502 [149] Yasui K, Kanazawa S, Sano Y, Fujiwara T, Kagawa S, Mimura H, Dendo S, Mukai T, Fujiwara H, Iguchi T, Hyodo T, Shimizu N, Tanaka N, Hiraki. Thoracic tumors treated with CT-guided radiofrequency ablation: initial experience. Radiology 2004 Jun; 231(3): 850-857 [150] Yoneda KY, Louis S, Shelton DK. Approach to pulmonary metastases, Curr Opin Pulm Med 2000; 6: 356-363 [151] Zanella A, Marchet A, Mainente P, Nitti D, Lise M. Resection of pulmonary metastases from colorectal carcinoma. Eur J Surg Oncol 1997; 23: 424 – 427 [152] Zimmermann R. et al: Pharynx- und Larynxtumoren, Hrsg: Tumorzentrum der Eberhard-Karls-Universität Tübingen, Dezember 2003 [153] Zusammenfassender Bericht des Untersuchungsausschusses „Ärztliche Behandlung“ des Gemeinsamen Bundesausschusses über die Bewertung der Laserinduzierten Interstitiellen Thermotherapie (LITT) bei malignen Tumoren gemäß § 135 Abs. 1 SGB V vom 04.11.2005 97 7 ABBILDUNGSVERZEICHNIS Abb.1 Prozentualer Anteil ausgewählter Tumorlokalisationen an allen Krebsneuerkrankungen in Deutschland 2004 Abb.2 Prozentualer Anteil ausgewählter Tumorlokalisationen an allen Krebssterbefällen in Deutschland 2004 Abb. 3 Minimalinvasive Behandlungsmöglichkeiten Abb. 4 Aufbau eines gekühlten Applikators und Wirkprinzip der Laserablation Abb. 5 Alterstruktur und Geschlechterverteilung Abb. 6 Prozentuale Verteilung der Primärtumore Abb. 7 Absolute Metastasenhäufigkeit im Patientengut Abb. 8 Anzahl behandelter pulmonaler Metastasen Abb. 9 Prozentuale Verteilung nach Tumorgröße Abb. 10 Applikatorsystem Abb. 11 Platzierung des Applikators Abb. 12 CT-gesteuerte Laserablation einer Lungenmetastase Abb. 13 Technisch komplette Ablation in Bezug zur Größe der Metastasen Abb. 14 Technisch komplette Ablation in Bezug zur Primärtumorentität Abb. 15 Diagnose von Progressen auf Patientenbasis Abb. 16 Lokale Progression nach Primärtumorentität Abb. 17 Lokale Progression und Größe des Tumors Abb. 18 Technischer Erfolg der Gesamtbehandlung und Primärtumorentität Abb. 19 Verteilung der echten und zensierten Fälle (Gesamtüberleben) Abb. 20 Überlebensfunktion des Gesamtpatientenkollektivs Abb. 21 Gesamtüberleben komplett erfolgreiche vs. zytoreduktive Therapie Abb. 22 Gesamtüberleben (CRC) Abb. 23 Gesamtüberleben (CRC) komplett erfolgreiche vs. zytoreduktive Therapie Abb. 24 Gesamtüberleben (RCC) Abb. 25 Gesamtüberleben (RCC) komplett erfolgreiche vs. zytoreduktive Therapie Abb. 26 Gesamtüberleben (Malignes Melanom) Abb. 27 Gesamtüberleben (MM) komplett erfolgreiche vs. zytoreduktive Therapie Abb. 28 Gesamtüberleben (Mamma-Ca.) Abb. 29 Gesamtüberleben (HNO-Tumore) Abb. 30 Gesamtüberleben (Mamma-Ca.) komplett erfolgreiche vs. zytoreduktive Therapie 98 Abb. 31 Gesamtüberleben (HNO) komplett erfolgreiche vs. zytoreduktive Therapie Abb. 32 Progressionsfreies Intervall des Gesamtpatientenkollektivs Abb. 33 Lokalprogressionsfreies Überleben (Gesamtpatientenkollektiv) Abb. 34 Progressionsfreies Überleben bei Auftreten eines lokalen Tumorprogresses Abb. 35 Lokalprogressionsfreies Überleben- Gesamtpatientenkollektiv (zytoreduktiv vs. komplett) Abb. 36 Progressionsfreies Überleben bei Auftreten eines lokalen Tumorprogresses (zytoreduktiv vs. komplett) Abb. 37 Lokalprogressionsfreies Überleben (Größe der Metastasen < 3 cm) Abb. 38 Lokalprogressionsfreies Überleben (Größe der Metastasen 3-5 cm) Abb. 39 Lokalprogressionsfreies Überleben (Größe der Metastasen > 5 cm) Abb. 40 Lokalprogressionsfreies Überleben bezogen auf technischen Erfolg (Größe der Metastasen < 3 cm) Abb. 41 Intrapulmonal-progressionsfreies Überleben (Gesamtpatientenkollektiv) Abb. 42 Progressionsfreies Überleben bei Auftreten eines intrapulmonalen Tumorprogesses Abb. 43 Extrapulmonal-progressionsfreies Überleben (Gesamtpatientenkollektiv) Abb. 44 Progressionsfreies Überleben bei Auftreten eines systemischen Tumorprogresses Abb. 45 Entstehung der Inhomogenität der Temperaturverteilung im Tumorgewebe 99 8 TABELLENVERZEICHNIS Tab. 1 Geschätzte 5-Jahres-Überlebensraten ausgewählter Primärtumore Tab. 2 Prozentuales Auftreten von Metastasen in der Lunge ausgewählter Primärtumore Tab. 3 Überlebensraten nach Resektion der Lungenmetastasen verschiedener Primärtumore Tab. 4 Studien zur Radiofrequenztherapie von Lungenmetastasen Tab. 5 Komplikationsraten der Radiofrequenzablation von Lungenmetastasen Tab. 6 Überlebensraten minimalinvasiver Behandlungsmethoden primärer und sekundärer Lungentumore Tab. 7 Überlebensraten nach stereotaktischer Strahlen- und Brachytherapie von Lungenmetastasen Tab. 8 Komplikationsraten minimalinvasiver Behandlungsmethoden primärer und sekundärer Lungentumore 100 9 ABKÜRZUNGSVERZEICHNIS 3D - Dreidimensional Abb. - Abbildung bzw. - beziehungsweise °C - Grad Celsius ca. - circa Ca. - Carcinom cm - Zentimeter CRC - Kolorektales Karzinom CT - Computertomographie EKG - Elektrokardiogramm et al. - et alii, und andere EU - Europäische Union F - French HCC - Hepatozelluläres Karzinoms HIFU - Hoch intensiver fokussierter Ultraschall HNO - Hals-Nasen-Ohren Hz - Hertz JÜR - Jahres-Überlebensrate kV - Kilovolt KI - Konfidenzintervall LENT-SOMA – Late effects on normal tissues, in subjective, objective, management and analytic categories LITT - Laserinduzierte Thermotherapie m - Meter mA - Milliampere mg - Milligramm ml - Milliliter mm - Millimeter µm - Mikrometer µl - Mikroliter med. - medianes MHz - Megahertz 101 min - Minute MM - Malignes Melanom Mon. - Monate MRT - Magnetresonanztomographie n/ N - Anzahl NaCl - Natriumchlorid Nd:YAG – Neodym dotierte Yttrium-Aluminium-Grant nm - Nanometer NSCLC – Non small cell lung cancer OP - Operation p - Signifikanz PMA - Perkutane Mikrowellenablation PT - Primärtumor PTT - Partielle Thromboplastinzeit RCC - Nierenzellkarzinom RFA - Radiofrequenzablation RIS - Radiologie-Informationssystem S. – Seite SPSS - Statistical Package for the Social Sciences Tab. – Tabelle TPCE - Transpulmonale Chemoembolisation u. - und u.a. - unter anderem ÜLZ - Überlebenszeit USA - United States of America var. - variabel VATS - videoassistierte Thoraxchirurgie vgl. - vergleiche W - Watt WHO - World Health Organization 102 10 EIDESSTATTLICHE ERKLÄRUNG Hiermit erkläre ich, dass ich die vorliegende Dissertation selbstständig verfasst und keine anderen als die angegebenen Hilfsmittel benutzt habe. Die Dissertation ist bisher keiner anderen Fakultät vorgelegt worden. Ich erkläre, dass ich bisher kein Promotionsverfahren erfolglos beendet habe und dass eine Aberkennung eines bereits erworbenen Doktorgrades nicht vorliegt. Berlin, 9. April 2010 Karen Bock 103 11 LEBENSLAUF Name: Karen Bock Geburtstag: 29. März 1980 Geburtsort: Berlin Schulausbildung: 1986 – 1992 Grundschule, 32. Oberschule Berlin-Hohenschönhausen 1992 – 1994 „Konrad-Wolf-Gymnasium“, Berlin-Weißensee 1994 – 1999 „Anne-Frank-Gymnasium“, Berlin-Treptow Hochschulausbildung: 1999 – 2006 Medizinstudium an der Ernst-Moritz-Arndt-Universität Greifswald Praktika: 1994 Intensivstation, 3 Wochen, Krankenhaus Aschersleben 1995 Praxis für Kindermedizin, 2 Wochen, Berlin-Treptow Famulaturen / Praktisches Jahr: 2000/2001 Station für Gastroenterologie, 8 Wochen, Krankenhaus Neukölln, Berlin 2002 Station für Kardiologie, 4 Wochen, Krankenhaus Neukölln, Berlin 2003 Institut für Radiologie, 4 Wochen, Krankenhaus Neukölln, Berlin 2004 Praxis für Obdachlose, 4 Wochen, Berlin-Lichtenberg 2005 – 2006 Praktisches Jahr, je 1 Tertial Innere Medizin, Chirurgie, Radiologie, Universitätsklinikum Greifswald Ärztliche Tätigkeit: seit 2006 Institut für Diagnostische Radiologie und Neuroradiologie, Ernst-Moritz-Arndt-Universität Greifswald (Direktor: Prof. Dr. med. N. Hosten) Mitgliedschaft: Deutsche Röntgengesellschaft European Society of Radiology Karen Bock 104 12 DANKSAGUNG Als erstes möchte ich mich herzlich bei Herrn Prof. Dr. med. Norbert Hosten bedanken, dem Direktor des Instituts für Diagnostische Radiologie und Neuroradiologie, der mir die Möglichkeit gab in Freude für ihn zu arbeiten und meine Dissertation in seiner Abteilung zu erstellen. Ich danke ihm für die Überlassung des Themas. Seine rasche Rückmeldung, fachliche Bewertung meiner Arbeit und sein immerwährendes Interesse sowie seine Geduld waren maßgeblich für die Erstellung und das Gelingen dieser Arbeit. Bedanken möchte ich mich bei Dr. med. Christian Rosenberg für seine Unterstützung und die Hilfe beim Verstehen und Interpretieren der Patientendaten. Auch schulde ich meinen übrigen Kollegen und den medizinisch technischen Assistenten/ -innen unserer Abteilung einen Dank, da sie mir oft den Rücken frei hielten. Für die Hilfe bei der statistischen Auswertung danke ich Dr. rer. nat. Pawel Kolyschkow und Dr. rer. nat. Ralf-Peter Blum für die physikalische Weiterbildung, die sich wann immer möglich Zeit für mich nahmen. Meine Familie, insbesondere meine Eltern Elke und Andreas Bock, und meine Freunde haben einen ganz besonderen Dank verdient, da sie mich sowohl in meiner Studienzeit als auch beim Erstellen dieser Arbeit mit Ermunterung, manchmal Aufmunterung und immer mit voller Tat-/ Kraft unterstützten. Mein letzter und innigster Dank gilt jedoch meiner Hauptstütze in den letzten 3 Jahren, Steven Blum. Ohne ihn, seine Unterstützung, sein Verständnis, die inspirierenden Gespräche und fortwährende Motivation hätte ich niemals die Kraft gehabt, diese Arbeit anzufangen bzw. fertig zustellen. 105