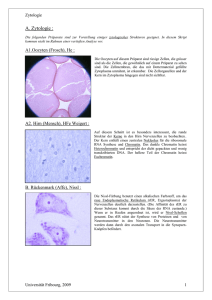
Aus dem Institut für Tierzucht (Mariensee)
Werbung

Aus dem Institut für Tierzucht (Mariensee) der Bundesforschungsanstalt für Landwirtschaft (FAL) Braunschweig Experimentelle Untersuchungen zur Verbesserung der Entwicklungsfähigkeit boviner Oozyten präpuberaler Spender durch In-vitro-Reifung auf Granulosazellmonolayern adulter Tiere INAUGURAL–DISSERTATION zur Erlangung des Grades einer DOKTORIN DER VETERINÄRMEDIZIN (Dr. med. vet.) durch die Tierärztliche Hochschule Hannover Vorgelegt von Simona Ponebšek aus Kranj/Slowenien Hannover 2005 Wissenschaftliche Betreuung: Apl.-Prof. Dr. H. Niemann 1. Gutachter: Apl.-Prof. Dr. H. Niemann 2. Gutachter: Prof. Dr. B. Meinecke Tag der mündlichen Prüfung: 21.11.2005 Meinen Eltern Liljana und Bojan, meiner Schwester Tatjana und Javier Inhaltsverzeichnis 1 EINLEITUNG .................................................................................................1 2 LITERATUR ..................................................................................................4 2.1 Oozytenentwicklung ....................................................................................4 2.1.1 Oogenese ......................................................................................................4 2.1.2 Oozytenreifung ..............................................................................................6 2.2 Follikulogenese..........................................................................................10 2.2.1 Kommunikation zwischen Oozyte und Follikelzellen....................................11 2.2.2 TGF-β Familie..............................................................................................12 2.2.3 Regulation des Follikelwachstums beim Rind..............................................14 2.2.4 Wachstumsdynamik ovarieller Follikel bei Kühen und Kälbern....................16 2.2.5 Funktionen der Follikelzellen nach der Ovulation ........................................18 2.3 Gewinnung unreifer KOK beim Rind durch OPU ....................................19 2.4 Unterschiede in der Entwicklungskapazität von Oozyten aus Kälbern und Kühen....................................................................................23 2.5 Ansätze zur Steigerung der Entwicklungskapazität von präpuberalen bovinen Oozyten ................................................................25 2.6 Kokultur in der In-vitro-Produktion von Embryonen ..............................27 2.7 Expression entwickunglsrelevanter Gene bei bovinen präimplantatorischen Embryonen............................................................28 2.7.1 Growth differentiation factor-9 (GDF-9)........................................................33 2.7.2 Heat shock- Protein 70 (Hsp.70)..................................................................33 2.7.3 Glukosetransporter-3 (Glut-3) ......................................................................35 3 MATERIAL UND METHODEN ....................................................................37 3.1 Kultivierung der Granulosazellen und Fibroblasten...............................37 3.1.1 Medien .........................................................................................................37 3.1.1.1 PBS..............................................................................................................37 3.1.1.2 Zellkulturmedien ..........................................................................................37 3.1.1.3 Einfriermedium.............................................................................................37 3.1.2 Gewinnung und Kultivierung der Granulosazellen .......................................38 i Inhaltsverzeichnis 3.1.3 Aliquotieren und Einfrieren der Granulosazellen..........................................38 3.1.4 Erstellen der Granulosazellmonolayer .........................................................39 3.1.5 Erstellen von Fibroblastenmonolayern.........................................................39 3.2 Transvaginale Ultraschall geleitete Follikelpunktion oder Ovum pick-up (OPU).............................................................................................40 3.2.1 Vorbereitung der Versuchstiere ...................................................................41 3.2.2 Ovum-Pick-Up (OPU) ..................................................................................41 3.3 Klassifizierung der Kumulus-Oozyten-Komplexe...................................42 3.4 In-vitro-Produktion boviner Embryonen ..................................................43 3.4.1 Medien .........................................................................................................43 3.4.1.1 PBS – Phosphate buffered saline ................................................................43 3.4.1.2 TCM air ........................................................................................................43 3.4.1.3 TCM + BSA (Reifungsmedium)....................................................................43 3.4.1.4 Sperm-TALP und Fert-TALP (Fertilisationsmedien) ....................................44 3.4.1.5 SOF-Medium (Kulturmedium) ......................................................................44 3.4.2 Reifung der Oozyten ....................................................................................44 3.4.3 Reifung der Oozyten auf Monolayern ..........................................................44 3.4.4 In-vitro-Befruchtung .....................................................................................45 3.4.5 Aufbereitung der Spermien ..........................................................................45 3.4.6 In-vitro-Kultivierung ......................................................................................45 3.5 Einfrieren ungereifter, gereifter Oozyten und Embryonen für RT-PCR ....46 3.6 Bestimmung der Zellzahlen ......................................................................47 3.7 RT-PCR Analyse ........................................................................................47 3.7.1 Isolierung von mRNA aus Oozyten und Embryonen....................................48 3.7.2 Reverse Transkription (RT)..........................................................................48 3.7.3 Polymerasekettenreaktion (PCR) ................................................................50 3.7.4 Verwendete Primer ......................................................................................51 3.7.5 Analysen der RT-PCR Produkte mit Hilfe der Gelelektrophorese................53 3.8 Versuchsaufbau.........................................................................................53 3.9 Statistische Auswertung ...........................................................................56 4 ERGEBNISSE .............................................................................................57 ii Inhaltsverzeichnis 4.1 OPU mit 7-8 Monate alten Kälbern und laktierenden Kühen..................57 4.2 IVP mit KOK aus 7- 8 Monate alten Kälbern und Kühen.........................63 4.3 Zellzahlen in expandierten Blastozysten .................................................63 4.4 Messenger RNA-Expression bei ungereiften und gereiften Oozyten von Kälbern und Kühen .............................................................65 4.5 Messenger RNA-Expression bei 8-16 Zellern und expandierten Blastozysten von Kälbern und Kühen .....................................................65 5 DISKUSSION ..............................................................................................71 6 ZUSAMMENFASSUNG...............................................................................79 7 SUMMARY ..................................................................................................82 8 LITERATURVERZEICHNIS ........................................................................85 9 ANHANG, ABBILDUNGEN UND TABELLEN..........................................109 9.1 Geräte und Material für OPU...................................................................109 9.2 Geräte und Material für die In-vitro-Produktion von Embryonen ........110 9.3 Geräte und Material für Zellkultur ..........................................................110 9.4 Geräte, Lösungen und Material für RT-PCR ..........................................111 9.5 Zusammensetzung der Medien ..............................................................112 9.5.1 Zellkulturmedium .......................................................................................112 9.5.2 Einfriermedium...........................................................................................113 9.5.3 PBS - Phosphate buffered saline...............................................................113 9.5.4 TCM-air......................................................................................................114 9.5.5 TCM + BSA (Reifungsmedium)..................................................................114 9.5.6 Sperm-TALP und Fert-Talp (Fertilisationsmedien) ....................................115 9.5.7 SOF-Medium (Kulturmedium) ....................................................................116 9.6 Abbildungsverzeichnis............................................................................117 9.7 Tabellenverzeichnis.................................................................................119 DANKSAGUNGEN .................................................................................................121 iii Inhaltsverzeichnis iv Einleitung ___________________________________________________________________________ 1 EINLEITUNG Die Technologie der Ultraschall geleiteten, transvaginalen Follikelpunktion ermöglicht es, ungereifte Oozyten wiederholt, von lebenden, präpuberalen Rindern zu gewinnen. Durch den Einsatz dieser Technologie in der Zucht kann das Generationsintervall verkürzt und das weibliche Keimzellpotential verstärkt genutzt werden. Von genotypisch wertvollen Tieren können schon vor Erreichen der Zuchtreife Nachkommen erhalten und entsprechend früher auf Leistungen und Eigenschaften geprüft werden. Bereits durchgeführte Untersuchungen haben jedoch gezeigt, dass die Entwicklungskompetenz von Oozyten präpuberaler Rinder (präpuberale Oozyten) deutlich geringer ist als die von adulten Tieren (adulte Oozyten). Morphologische Unterschiede zwischen präpuberalen und adulten Oozyten, niedrigere Befruchtungsund Teilungsraten, niedrigere Blastozystenraten und nach Transfer in Empfängertiere deutlich niedrigere Trächtigkeitsraten deuten auf Veränderungen im Stoffwechsel, Zellwachstum, Zellteilung und Empfindlichkeit gegenüber äußeren Einflüssen, im Vergleich zu Oozyten und Embryonen adulter Tiere hin (DE PAZ et al. 2001; TANEJA et al. 2000; MAJERUS et al. 1999; STEEVES et al. 1999; STEEVES u. GARDENER 1999; PRESICCE et al. 1997; DUBY et al. 1996; REVEL et al. 1995). Ursachen für diese niedrigere Entwicklungskompetenz werden vor allem in der mangelhaften zytoplasmatischen Reifung präpuberaler Oozyten vermutet (DAMIANI et al. 1996) Während ihrer Entwicklung sind Säugetieroozyten von Follikelzellen umgeben. Die Follikelzellen sind untereinander und mit der Oozyte durch Zellfortsätze über Gap junctions verbunden (HYTTEL et al. 1997). Zusammen mit der Follikelflüssigkeit bilden sie die Mikroumgebung für das Wachstum und die Reifung der Oozyte. Diese physiologische Bedeutung der Follikelzellen kann zur Unterstützung der Oozytenreifung in vitro genutzt werden, in dem Granulosazellen als Monolayer in das Reifungsverfahren einbezogen werden (Rind: LUTTERBACH et al. 1987, FUKUI u. ONO, 1989; Ziege: TEOTIA et al. 2001). 1 Einleitung ___________________________________________________________________________ Einige der Faktoren, die in der molekularen Regulation zu Erlangung der vollständigen Entwicklungskompetenz von Oozyten beteiligt sind, konnten in den letzten Jahren identifiziert werden. DONG et al. (1996) berichteten bei der Maus über den Growth differentiation Factor-9 (GDF-9), der von der Oozyte synthetisiert wird und auf parakrinem Wege für Differenzierung und Proliferation der Follikelzellen verantwortlich ist. GDF-9 hat auch bedeutenden Einfluss auf die Expansion der Kumuluszellen während der Reifung (ELVIN et al. 1999a). Rinderoozyten synthetisieren GDF-9 vom Primordial- bis zum 8-16 Zellstadium (SENDAI et al. 2001). Die Glukoseversorgung präimplantatorischer Embryonen wird durch Moleküle der Glukosetransporter-Familie gesichert. Bei der Maus wurde die Expression von Glukosetransporter-3 (Glut-3) in expandierten Blastozysten nachgewiesen. Er befindet sich apikal an den Zellen des Trophektoderms und ist für den direkten Transport von Glukose in die Zellen der inneren Zellmasse und das Blastozoel verantwortlich (PANTALEON et al. 1997). Glut-3 mRNA Expression ist bei bovinen Embryonen nachgewiesen worden (AUGUSTIN et al. 2001). Heat shock-Proteine wirken in eukaryontischen Zellen als Schutzproteine, in der sie bei der Faltung von Proteinen eine Rolle spielen. Heat shock-Proteine werden in großen Mengen synthetisiert, wenn die Zellen für kurze Zeit höheren Temperaturen (etwa 42°C) ausgesetzt werden (ALBERTS 1994c). Sie dienen dem Embryo auch als Schutz bei schädlichen Umweltveränderungen, wie Temperaturschwankungen oder suboptimalen Kulturbedingungen. Ihre erhöhte Expression kann ein wichtiger Hinweis für die Empfindlichkeit von Embryonen gegenüber schlechten Umweltbedingungen sein (EALY et al. 1993). Heat shock- Protein 70 (Hsp.70) wird beim Rind in allen präimplantatorischen Stadien exprimiert. In-vivo-expandierte Blastozysten weisen eine geringere Expression von Hsp.70 mRNA auf als Embryonen aus der In-vitro-Produktion (WRENZYCKI et al. 1998). In dieser Arbeit sollte der Frage nachgegangen werden, ob Granulosazellen adulter Tiere in der Lage sind, die Entwicklungskompetenz boviner präpuberaler KumulusOozyten-Komlpexe (KOK) zu steigern, um so eine größere Anzahl an entwicklungsfähigen Blastozysten zu erhalten. Es sollte geklärt werden, ob die 2 Einleitung ___________________________________________________________________________ Reifung auf den beiden Zellkulturen die mRNA-Expression von drei entwicklungsrelevanten Genen beeinflusst, die in der frühen Follikelentwicklung und der frühen Embryonalentwicklung großen Einfluss haben. Dafür sollte der relative Gehalt an Transkripten für GDF-9 bei ungereiften und gereiften Oozyten der verschiedenen Reifungsgruppen, mit Hilfe der RT-PCR untersucht werden. Ferner wurden die Expressionsmuster von Glut-3 und Hsp.70 m-RNA in 8-16 Zellern und expandierten Blastozysten aus Oozyten der verschiedenen Reifungsgruppen untersucht. Diese Gene wurden bisher noch nicht bei präpuberalen bovinen Oozyten oder präimplantatorischen Embryonen untersucht. Kumulus-Oozyten-Komplexe von laktierenden Kühen wurden in die Untersuchungen mit einbezogen, um mögliche Abweichungen bei Kälberoozyten darstellen zu können. 3 Literatur ___________________________________________________________________________ 2 LITERATUR 2.1 Oozytenentwicklung 2.1.1 Oogenese Beim weiblichen Säugetier beginnt die Oogenese bereits in der frühen embryonalen Entwicklung mit der Ausbildung der Primordialkeimzellen im Dottersack des Embryos. Aus dem Dottersack gelangen die Keimzellen später in die Gonadenanlagen ventral der Urniere. Durch mehrere mitotische Teilungen entstehen Oogonien. Im Verlauf mehrerer Monate werden durch Proliferation und mitotische Teilungen eine bestimmte Anzahl Oogonien gebildet. Abbildung 1: Schema der Oogenese (nach SCHNORR und KRESSIN 2001) 4 Literatur ___________________________________________________________________________ Beim Rind beginnt die Oogonienbildung am 75. Tag der Embryonalentwicklung und endet am 160. Tag (ERICKSON 1966a). Die Oogonien nehmen an Größe zu und werden nun Primäroozyte oder Oozyte I genannt. Bei der Geburt hat der weibliche Säuger bereits eine bestimmte Anzahl von Oozyten 1. Ordnung, die für das reproduktive Leben zur Verfügung stehen. Ihre Anzahl wird von nun an nur noch durch Ovulation oder Atresie reduziert. Beim Rind erreichen die Oogonien die erste meiotische Prophase zwischen Tag 75 und 80 nach der Befruchtung (ERICKSON 1966a). Während dieser Phase wird das genetische Material zwischen den homologen Chromatiden durch „Crossing Over“ ausgetauscht, und es entstehen neue genetische Kombinationen (SCHNORR und KRESSIN 2001). Die meiotische Prophase besteht aus mehreren Stadien, wobei die Oozyten im letzten Stadium, dem Diplotän, während der ersten meiotischen Teilung, arretiert werden. Die arretierten Oozyten sind durch einen großen Nukleus oder „Germinal vesicle“ charakterisiert (BAKER und FRANCHI 1967). Bei der Geburt sind bei Kälbern durchschnittlich ca. 130000 Oozyten vorhanden, die in der ersten Prophase arretiert bleiben (ERICKSON 1966b). Bevor die Primäroozyten in der Lage sind, die Meiose wieder aufzunehmen, müssen sie an Größe zunehmen. FAIR et al. (1995) haben festgestellt, dass Oozyten erst bei einem Durchmesser von ~ 100 µm die Meiose wieder aufnehmen können. Ab einem Durchmesser von 110 µm können sie, die Meiose bis zum Erreichen der Metaphase II vollenden. In der In-vitro-Produktion von Rinderembryonen erhöhen sich die Teilungs- und Blastozystenraten signifikant, wenn die Oozyten einen Durchmesser von mehr als 120 µm aufweisen (DE LOOS et al. 1989). Die Wachstumsphase der Oozyten geht mit der Differenzierung der Follikelzellen einher. Zwischen Kumuluszellen und Oozyte werden Gap Junctions ausgebildet, um den Transport von Nährstoffen, aber auch Signalmolekülen, mit geringem Molekulargewicht zu ermöglichen (FAIR et al. 1997; HYTTEL et al. 1997). Während dieser Wachstumsphase bilden sich die Zona pellucida und die kortikalen Granula. Die Entstehung dieser Strukturen ist besonders für die reguläre monosperme Befruchtung von großer Bedeutung, in dem sie helfen, Polyspermie zu verhindern (FAIR et al. 1997). 5 Literatur ___________________________________________________________________________ 2.1.2 Oozytenreifung Die Reifung der Oozyte beginnt mit der Wiederaufnahme der Meiose bis zur Vollendung der Metaphase II. Durch die vollständige Reifung von Zytoplasma und Kern erhält die Säugetieroozyte die Fähigkeit zur Befruchtung und für die frühe Embryonalentwicklung (NIEMANN und MEINECKE 1993). Die Reifung wird in vivo bei geschlechtsreifen Tieren durch den präovulatorischen Gonadotropinimpuls ausgelöst (TSAFRIRI et al. 1976). Um die meiotische Metaphase I erreichen zu können, laufen im Ooplasma mehrere Veränderungen ab. Die Kernmembran wird aufgelöst (Germinal Vesicle Break Down, GVBD) und es folgt die Kondensierung der Chromosomen. Es werden vermehrt Lipide eingelagert, die Mitochondrien verteilen sich gleichmäßig im Zytoplasma und die kortikalen Granula formieren sich am äußeren Rand der Eizelle unterhalb des Oolemms (HYTTEL et al. 1997; KRUIP et al. 1983). Die gepaarten homologen Chromosomen trennen sich und werden zu den entgegen gesetzten Spindelpolen gezogen (Anaphase I). Mit Erreichen der Telophase I teilt sich die Oozyte in zwei haploide Zellen. Die kleinere wird als erster Polkörper abgeschnürt. Die größere, die sekundäre Oozyte verharrt bis zur Befruchtung in der Metaphase II (SCHNORR und KRESSIN 2001). Zum Zeitpunkt der zweiten Arretierung findet in vivo auch die Ovulation statt (HYTTEL et al. 1997). In der Oozyte werden große Mengen RNA synthetisiert. Diese Syntheseleistung nimmt zur Reifung hin immer mehr ab bzw. bis die Oozyte einen Durchmesser von ca. 110 µm erreicht hat (FAIR et al. 1995) und im Stadium der Metaphase II kaum noch nachgewiesen werden kann (MEMILI et al. 1998). Die Oozyte synthetisiert RNA im Wesentlichen für den eigenen Gebrauch, da sie für ihr weiteres Wachstum Proteine benötigt. RNA ist auch für die Reifung und frühe embryonale Entwicklungsprozesse erforderlich (HYTTEL et al. 2001; SIRARD et al. 1989). Die Vorgänge bei der Reifung von Zytoplasma und Kern werden im Wesentlichen von den Zellzyklusregulatoren Maturation Promoting Factor (MPF) und Mitogen Activated Protein Kinase (MAPK) gesteuert (GORDO et al. 2001). MAPK und MPF werden etwa zeitgleich mit dem GVBD aktiviert (WEHREND und MEINECKE 2001). 6 Literatur ___________________________________________________________________________ Abbildung 2: MAPK, MPF, Cyclin B und ihre Rolle bei der Oozytenreifung und Befruchtung beim Säugetier (nach FAN et al. 2004 und ABRIEU et al. 2001) Auch für die Arretierung in der Metaphase II (Second meiotic arrest) spielen diese beiden Faktoren eine entscheidende Rolle. Die Aufrechterhaltung der M II wird beim Rind durch eine wechselnde MPF-Aktivität reguliert (WU et al. 1997), die wiederum durch MAPK aufrecht gehalten wird (GORDO et al. 2001). MAPK wird durch Phosphorylierung aktiviert. Diese Phosphorylierung wird wiederum durch Protein 7 Literatur ___________________________________________________________________________ Kinase C, cAMP (cyclic Adenosine-Mono-Phosphate) und Protein PhosphataseModulatoren reguliert. MPF ist ein Komplex aus den Proteinen p34cdc2 (Cell-devision Cycle 2) und Cyclin B und kann Oozyten, die sich in der G2-Phase des Zellzyklus befinden, in die M- Phase überführen und so die Meiose wieder aufnehmen lassen (NURSE 1990; ALBERTS et al. 1994a; KUBELKA 2000; MEINECKE und KRISCHEK 2003). In bovinen Oozyten reguliert die PI 3-Kinase (Phosphatidylinositol 3-kinase) den Übergang der Oozyte von M I in die M II- Phase (ANAS et al. 2000). Das Protooncogen c-Mos aktiviert die MAPK-Kaskade und ist somit ein Schlüsselmolekül für den Reifungsprozess bei Wirbeltieren (GEBAUER und RICHTER 1997; NEBREDA u. HUNT 1993; POSADA et al. 1993; SAGATA et al.1989). Mos, ein Produkt des cMos, wird von bovinen Oozyten in der Metaphase II synthetisiert (WU et al. 1997). Abbildung 3: Zellzyklus mit seinen Phasen. G1, S, G2 bilden die Interphase und M bildet die Mitosephase (nach NIEMANN und MEINECKE 1993) 8 Literatur ___________________________________________________________________________ Durch Injektion von Mos-mRNA in bovine Oozyten wurden GVBD und die Wiederaufnahme der Meiose beschleunigt, was die Existenz eines Mos/MAPKPfades vermuten lässt (FISSORE et al. 1996). In vitro Versuche haben gezeigt, das eine Inaktivierung der MAPK, durch Injektion von MAPK-Phosphatase (MKP-1) in die Oozyten, zu einem fehlerhaften Aufbau der MII-Spindel führt (GORDO et al. 2001). Aus humaner Follikelflüssigkeit sowie aus Bullenhoden wurde ein Sterol isoliert, das als FF-MAS (Follicular Fluid Meiosis Activating Sterol) bezeichnet wird (BYSKOV et al. 1995). FF-MAS spielt eine entscheidende Rolle bei der Wiederaufnahme der Meiose. GRØNDAHL et al. (1998) haben gezeigt, dass FF-MAS die Reifung muriner Oozyten in vitro induziert. Auch bei humanen Oozyten förderte FF-MAS ihre Reifung (CAVILLA et al. 2001); ebenso bei Oozyten von Patientinnen, die an PCO (Polycystic Ovaries) litten (GRØNDAHL et al. 2000). Durch Zusatz von FFMAS im Reifungsmedium für präpuberale Kälberoozyten konnte der Anteil der in die Metaphase II übergegangenen Oozyten erhöht werden. Die weitere Entwicklungsfähigkeit der präpuberalen Kälberoozyten nach der Befruchtung war aber nicht verbessert (DONNAY et al. 2004). Die G1- und S- Phase werden während der Fetalentwicklung durchlaufen. In der SPhase wird die DNA verdoppelt. Wenn die Meiose wieder aufgenommen wird, befinden sich die Oozyten in der G2 Phase (siehe Abbildung 2). Um die M- Phase zu erreichen und so die Meiose wieder aufzunehmen, muss das p34 Protein aktiviert werden, in dem es sich an Cyclin B anlagert, zu Prä-MPF wird und durch Dephosphorylierung aktiviert wird (MPF). Wenn die Konzentration von MPF sinkt, durchlaufen Oozyten die Ana- und Telophase. Der zweite Anstieg der MPF Konzentration erfolgt zeitgleich mit der Arretierung der Oozyte in der Metaphase II (ANAS et al. 2000). Die meisten Oozyten erreichen diese Entwicklungsstufe nicht, da sie zuvor schon atresieren. Die Oozyten, die zur Ovulation kommen, besitzen einen haploiden Chromosomensatz, haben die Reifung erfolgreich durchlaufen und können nach erfolgreicher Befruchtung die Entwicklung zu einem neuen Individuum fortsetzten. 9 Literatur ___________________________________________________________________________ 2.2 Follikulogenese Im bovinen fetalen Ovar beginnt ab dem 90. Trächtigkeitstag die Follikelbildung mit der Ausbildung von Primordialfollikeln (WANDJI et al. 1992). Bereits am 180. Trächtigkeitstag sind auf fetalen Ovarien wachsende Primär- und Sekundärfollikel zu finden und ab dem 220. Trächtigkeitstag sind auch schon einige tertiäre Follikel erkennbar (WANDJI et al. 1992). Bei der Geburt sind schon alle Primordialfollikel ausgebildet, die in dieser Phase, bis zum Eintreten in die Wachstumsphase, jahrelang verharren können. Die verschiedenen Stadien der Follikelentwicklung unterscheiden sich durch spezifische morphologische Merkmale von einander. Die in der meiotischen Prophase I arretierten Primäroozyten, mit einem Durchmesser von ca. 35 µm, sind von einer Lage aus flachen, undifferenzierten Plattenepithelzellen umgeben (SCHNORR und KRESSIN 2001). Die Granulosazellen verändern nun ihre Form und werden kubisch. Proliferation und Differenzierung der Granulosazellen und das Wachstum der Oozyten im Primordialfollikel führen zur Entstehung der Primärfollikel. Die Oozyten der Primärfollikel sind von einer Schicht kubischer Granulosazellen umgeben (BRAW-TAL und YOSSEFI 1997; FAIR et al. 1997). Durch mitotische Teilungen entsteht ein mehrschichtiges, kubisches Granulosazellepithel, das charakteristisch für die Sekundärfollikel ist. Der Durchmesser des Sekundärfollikels beträgt ca. 55 µm, wobei die Oozyte in dieser Phase nicht größer wird. Die Zellfortsätze der Granulosazellen schieben sich in das Oolemm. Am Ende dieser Zellfortsätze bilden sich Gap Junctions (FAIR et al. 1997), die einen Austausch von Molekülen zwischen Oozyten und Granulosazellen ermöglichen. In tertiären Follikeln bildet sich durch Flüssigkeitsansammlung das Antrum. Die Oozyte ist von vielen Schichten Granulosazellen umgeben, die den Kumulus Oophorus bilden. Diese Follikel haben bereits eine Theca interna und Theca externa an der basalen Lamina, und die Oozyte ist bereits vollständig von der Zona pellucida umgeben (BRAW-TAL und YOSSEFI 1997; FAIR et al. 1997). Wenn der tertiäre Follikel einen Durchmesser von 15-20 mm erreicht hat, wird er als präovulatorischer bzw. Graaf’scher Follikel bezeichnet. Die Oozyte hat dann einen Durchmesser von ca. 120µm, die Kumuluszellen sind expandiert und werden auch 10 Literatur ___________________________________________________________________________ als Kumulus oophorus bezeichnet. Die Expansion der Kumulszellen wird durch die Sekretion der Hyaluronsäure induziert, die wiederum durch den präovulatorischen Gonadotropinimpuls ausgelöst wird (EPPIG 2001). In dieser Phase wird die Meiose wieder aufgenommen und erst in der Metaphase II der zweiten Meiose arretiert (HYTTEL et al. 1986). 2.2.1 Kommunikation zwischen Oozyte und Follikelzellen Die Kommunikation zwischen Oozyten und Follikelzellen erfolgt in beide Richtungen (EL-FOULY et al. 1970; NEKOLA und NALBANDOV 1971). Ein komplexes Zusammenspiel ist für die Entwicklung der Oozyte und der Follikelzellen wichtig und zwar vom Entstehen primordialer Follikel bis zur Ovulation (siehe Abbildung 4). Abbildung 4: Beidseitige Kommunikation von Oozyte und Follikelzelle (modifiziert nach EPPIG 2001) Die Mechanismen, die die Follikelbildung induzieren, sind kaum bekannt. Ein bedeutender Faktor scheint der ooozytenspezifische Factor In The Germline, Alpha (Figlα) zu sein, dessen mRNA bereits bei 13 Tage alten Mäuseembryonen nachgewiesen wurde. Bei der Maus koordiniert Figlα die Expression einiger 11 Literatur ___________________________________________________________________________ Strukturgene für Komponenten der Zona pellucida (LIANG et al. 1997) und scheint auch mit für den Beginn der Follikelbildung verantwortlich zu sein. Figlα Knock-out Mäuse bilden auf ihren Ovarien keine Primordialfollikel und sind steril (SOYAL et al. 2000). Ein anderer, ebenfalls von Oozyten synthetisierter Faktor, der Growth Differentiation Factor-9 (GDF-9) aus der Transforming Growth Factor-Familie (TGF-β) ist bei der Maus mit für die Entwicklung der Follikel vom Primärfollikelstadium an verantwortlich. Er wird von allen Säugetieroozyten, auch von humanen Eizellen synthetisiert (McGRATH et al. 1995; LAITINEN et al. 1998; AALTONEN et al. 1999; BODENSTEINER et al. 1999). 2.2.2 TGF-β Familie Die TGF-β Familie umfasst eine große Anzahl extrazellulärer Faktoren, die beim Säugetier in vielen Geweben und Organen weit reichenden Einfluss ausüben. Die meisten der über 35 Mitglieder regulieren die Fertilität (KNIGHT und GLISTER 2001; CHANG et al. 2002; KNIGHT und GLISTER 2003). GDF-9, vermutlich zusammen mit GDF-9B, auch Bone-Morphogenetic Factor-15 (BMP-15) genannt, steuert im Ovar die Follikelbildung bis hin zur Ovulation und Befruchtung. Mit der Antrumbildung beginnen sich die Granulosazellen in wandständige Granulosazellen und Kumuluszellen zu differenzieren, was im Wesentlichen von der Oozyte gesteuert wird (LI et al. 2000). Die Kumuluszellen sind mit der Oozyte und untereinander durch Gap Junctions verbunden (HYTTEL et al. 1997) so dass Moleküle mit geringem Molekulargewicht wie Ionen, Nährstoffe und Aminosäuren ausgetauscht werden können, die für das Oozytenwachstum- und Entwicklung wichtig sind (SIMON et al. 1997). Größere Moleküle werden mittels Endozytose transportiert. Die wandständigen Granulosazellen, die vermutlich nur über die Follikelflüssigkeit Kontakt zur Oozyte haben, besitzen eine niedrige Proliferationsrate, höhere Stroidsynthesekapazität und höhere Expression von LH- Rezeptoren (RICHARDS et al. 1976). 12 Literatur ___________________________________________________________________________ Die Oozyte beeinflusst Follikelentwicklung und Differenzierung der Follikelzellen durch parakrine Botenstoffe. Drei wichtige Botenstoffe sind GDF-9, BMP15 und BMP-6. Sie werden bei Nagern in Primärfollikeln und bei Wiederkäuern in Primordialfolliken exprimiert (McGRATH et al 1995; JAATINEN et al 1999; BODENSTEINER et al. 1999; ELVIN et al. 1999a; KNIGHT und GLISTER 2003). Rinderoozyten synthetisieren GDF-9 vom Primordialstadium bis nach der Befruchtung und bis hin zur Aktivierung des embryonalen Genoms (SENDAI et al. 2001). GDF-9 knock-out Mäuse sind auf Grund gestörter früher Follikelentwicklung, unfruchtbar (DONG et al. 1996). Die arretierten Follikel besitzen morphologisch abnorme Granulosazellen und keine Thecazellschichten (ELVIN et al. 1999b). Die Oozyten wachsen schneller, sind größer und haben strukturelle Defekte (CARABATSOS et al.1998). Der Knockout der Gene BMP-15 und BMP-6 hatte nur geringe oder keine Auswirkungen (SOLLOWAY et al.1998). Abbildung 5: GDF-9 und seine vielfältige Rolle im Säugetierovar (modifiziert nach ELVIN 1999) Abkürzungen: : hoch reguliert, : herunter reguliert, upA: Urokinase Plasminogen Activator, GDF-9: Growth Differentiation Factor-9, HAS 2: Hyaluransynthase 2, StAR: Steroidogenic Acute Regulator Protein, COX2: Cyclooxigenase 2, LH: luteinisierendes Hormon 13 Literatur ___________________________________________________________________________ Bei der Maus bewirkt GDF-9 im Graaf’schen Follikel durch Induktion von Hyaluransynthase 2 (HAS2) und gleichzeitiger Herunterregulierung des Urokinase Plasminogen Activator (uPA) während der Reifung die Produktion von Hyaluronsäure angereicherter extrazellulärer Matrix (ELVIN et al. 1999a). Der präovulatorische Gonadotropinimpuls bewirkt die Sekretion von Hyaluronsäure in die Zellzwischenräume, die sich vergrößern, bis die Kumuluszellen in klebriger, dickflüssiger Matrix eingebettet sind (CHEN et al. 1993). Über die Expression von Steroidogenic Acute Regulator Protein (StAR) und der Stimulierung von Cyclooxigenase 2 (COX-2) wird die Produktion von Progesteron und Prostaglandin erhöht. Zudem wird über diesen parakrinen Signalweg die Expression von LHRezeptoren mRNA herunter reguliert (ELVIN et al. 2000; EPPIG et al. 1997) (siehe Abbildung 5). In den humanen Granulosa- und Thecazellen inhibiert GDF-9 die cAMP induzierte Steroidhormonproduktion und die Expression von Genen, die für die Steroidhormonproduktion wichtig sind (YAMAMOTO 2002). 2.2.3 Regulation des Follikelwachstums beim Rind Das Follikelwachstum ist ein komplexer Prozess, der sowohl hormonellen aber auch systemischen extraovariellen und lokalen intraovariellen Steuerungen unterworfen ist. Während der verschiedenen Phasen der Follikulogenese sind vor allem die intraovariellen Faktoren von großer Bedeutung. Einige Faktoren, wie GDF-9, BMP-15 und BMP-6 werden von der Oozyte während der gesamten Follikelentwicklung bis über die Ovulation hinaus synthetisiert. Sie fördern die Entwicklung des Follikels über das Primordial- und Primärstadium hinaus und stimulieren Proliferation und Differenzierung der Granulosazellen. TGF-β beeinflusst vom Primärfollikelstadium an die Granulosa- und Thecazellproliferation und ihre Differenzierung und unterdrückt die Produktion von Androgenen in den Thecazellen. Aktivin stimuliert die Granulosazellproliferation in präantralen und frühen antralen Follikeln. FSH-Rezeptoren und die FSH induzierte AromataseAktivität werden gesteigert und fördern die Oozytenreifung. Follistatin verringert die Aktivität von Aktivin und fördert vermutlich die Luteinisierung bzw. Atresie großer 14 Literatur ___________________________________________________________________________ antraler Follikel. Inhibin vermehrt die LH- induzierte Androgenproduktion in großen antralen Follikeln (KNIGHT und GLISTER 2003) (siehe Abbildung 6). Abbildung 6: Abgestimmtes Zusammenwirken von extra- und intraovariellen Faktoren im Follikel (nach Knight und GLISTER 2001) Die hormonelle Regulierung der Follikelentwicklung und das Wachstum der Oozyten werden vor allem durch die Gonadotropine LH (luteinisierendes Hormon) und FSH (Follikel stimulierendes Hormon) bestimmt. LH und FSH sind Glykoproteine und werden im Hypophysenvorderlappen (Adenohypophyse) gebildet. Ihre Freisetzung erfolgt durch die Ausschüttung des Neurohormons GnRH (Gonadotropin Releasing Hormon), das aus dem Hypothalamus stammt (WALTERS und SCHALLENBERGER 1984). 15 Literatur ___________________________________________________________________________ Im dominanten Follikel stimuliert LH die Reifung der Oozyte und Ovulation (DIELEMAN et al. 2002). Im Follikel stimuliert LH die Synthese von Androstendion in den Thecazellen (GINTHER et al. 2001). FSH fördert die Entwicklung vom primären zum präovulatorischen Follikel und stimuliert die Östrogensynthese durch die Aktivität des Enzyms Cytochrome P450 Aromatase in den Granulosazellen (YING 1988). 2.2.4 Wachstumsdynamik ovarieller Follikel bei Kühen und Kälbern Auf Grund einer periodischen Ausschüttung von FSH, beim Rind verläuft das Wachstum der Follikel wellenförmig in zwei bis drei Wachstumswellen pro Zyklus (PIERSON und GINTHER 1988, SAVIO et al. 1988). Die Anzahl der Follikelwellen während des Zyklus wird durch die sich ändernden Konzentrationen von Inhibin A und FSH während ovulatorischer und anovulatorischer Wellen bestimmt (PARKER et al. 2003). Jede Follikelwelle verläuft in drei Phasen: 1.) Rekrutierung, 2.) Selektion und 3.) Dominanz. In der ersten Phase wird aus einem Pool gonadotropinreaktiver ovarieller Follikel eine kleine Kohorte mit Follikeln im Durchmesser von ca. 3mm rekrutiert (GINTHER et al. 1996). Die Follikel dieser Kohorte werden einer Selektion unterworfen, bei der ein dominanter Follikel weiter wächst, während die anderen Follikel der Kohorte atresieren (DRIANCOURT 2001). Dieses wellenartige Follikelwachstum läuft kontinuierlich ab; auch bei präpuberalen und trächtigen Rindern kommt es zur Bildung anovulatorischer Follikelwellen (ROCHE und BOLAND 1991). Die Selektion des dominanten Follikels wird unter anderem über die Granulosa- und Thecazellen gesteuert. In den Granulosazellen der gonadotropinreaktiven Follikel wird vermehrt mRNA für LH- Rezeptoren und Aromatase synthetisiert (BAO et al. 1997) und Theca-interna-Zellen bilden LHRezeptoren aus. Es wurde mRNA für FSH-Rezeptoren in den Granuloszellschichten primärer Follikel festgestellt (BAO und GRAVERICK 1998). Die Zahl der FSHRezeptoren erhöht sich erst in den folgenden Follikelstadien durch Proliferation der Granulosazellen. Wenn nach einer periodischen Ausschüttung von FSH die Follikel eine Größe von ca. 8,5 mm erreichen, wird der dominante Follikel aus der Kohorte 16 Literatur ___________________________________________________________________________ selektiert (GINTHER et al. 1997). Wenn der FSH Spiegel im Blut auf basale Konzentrationen abfällt hat das zur Folge, dass die untergeordneten Follikel nicht mehr genug FSH binden können. Sie stellen ihr Wachstum ein und atresieren (ADAMS et al. 1992). Im zukünftigen dominanten Follikel stimuliert die basale Ausschüttung von LH in den Thecazellen die Synthese von Androgenen, die in den Granulosazellen, stimuliert durch Bildung von basalem FSH, zu Östrogenen aromatisiert werden (siehe Abbildung 7). Abbildung 7: Östrogensynthese in Granulosazellen (nach ENGELHARDT und BREVES 2000) Die hohe Östrogenkonzentration führt zu Bildung von Blutgefäßen in der Theca interna. Der Follikel kann so indirekt mehr FSH an sich binden. Durch die erhöhte Bildung von Östrogenen und Inhibin wird die FSH Konzentration gesenkt und es kann keine neue Rekrutierung mehr stattfinden (DRIANCOURT 2001, EVANS et al. 1997). In der präovulatorischen Phase induziert Östrogen die Bildung von LH– Rezeptoren an den Granulosazellen (BAO et al. 1997, BERGFELT et al. 2000). 17 Literatur ___________________________________________________________________________ Der Follikel kann das präovulatorische LH binden und eine Reihe von Enzymsystemen aktivieren, die für die Luteinisierung der Granulosa- und Thecazellen nötig sind. Bei Kälbern wurden die ersten antralen Follikel schon im Alter von 2 Wochen festgestellt (RAWLINGS et al. 2003). Durch Ultraschalluntersuchungen stellten ADAMS et al. (1994) bei 8 Monate alten, präpuberalen Kälbern ein wellenartiges Follikelwachstum, ähnlich wie bei Kühen, fest. Langzeitbeobachtungen an Kälbern ergaben regelmäßige Follikelwellen nach vorausgehenden FSH-Impulsen. Anzahl und Größe der Follikel waren mit denen von Kühen vergleichbar (EVANS et al. 1994), wobei sich der Durchmesser der Follikel mit dem Alter vergrößerte (RAWLINGS et al. 2003). Bei präpuberalen Kälbern handelt es sich um anovulatorische Follikelwellen, die erst mit Erreichen der Pubertät ovulatorisch werden. DRIANCOURT et al. (2001) haben in Follikeln von Kälbern eine geringere Aromatase Aktivität der Granulosazellen und folglich auch eine geringere Östrogensynthese festgestellt. Die Achse Hypothalamus-Hypophyse-Ovar ist beim juvenilen Kalb bereits in das Follikelwachstum integriert; allerdings kommt es durch fehlende Östradiol- Rezeptoren an den GnRH-Neuronen zu einer negativen Rückkopplung beim Freisetzen von LH (DAY et al. 1987; SHIVERS et al. 1983). Erst die vermehrte Freisetzung von LH führt in den antralen Follikeln zur Östrogensynthese, präovulatorischen LH- Impuls und ersten Ovulation im Alter von 52-56 Wochen (RAWLINGS et al. 2003). Durch die verstärkte GnRH- Synthese und Sekretion wird letztendlich die Hypophysen-Gonadenachse aktiviert, was zum Erreichen der Pubertät und damit zur Geschlechtsreife führt (EBLING 2005). 2.2.5 Funktionen der Follikelzellen nach der Ovulation Nach der Ovulation formen sich die wandständigen Granulosazellen zu großen, die Thecazellen zu kleinen Luteinzellen um. Sie bilden das Drüsengewebe des Corpus luteum und synthetisieren das Steroidhormon Progesteron (NISWENDER und NETT 1994; NISWENDER 2002). Kumulus- Oozyten Komplexe (KOK) werden unmittelbar nach der Ovulation von Infundibulum tubae aufgenommen und durch den Zilienschlag des Eileiterepithels 18 Literatur ___________________________________________________________________________ zum Ort der Befruchtung, der Ampulla tubae weitertransportiert (SCHUMMER und VOLLMERHAUS 1995). Auf diesem Weg wird der Kumulus oophorus durch Reibung an den Zilien des Eileiters und unter Einwirkung von Enzymen, vor allem der Hyaluronidase, von der Oozyte entfernt. Beim Rind geschieht das 3-10 Stunden nach der Ovulation (LORTON und FIRST 1979; HYTTEL 1988). Vermutlich erleichtert der Kumulus oophorus die Weiterleitung des KOK im Infundibulum. Beim Hamster kommt es zur Adhäsion der extrazelluären Kumulusmatrix und der Zilien des Infundibulums (LAM et al. 2000). Für eine erfolgreiche Befruchtung in vivo und in vitro ist der Verbund von Kumuluszellen mit den Oozyten bedeutsam. Beim Hamster sind Oozyten ohne Kumuluszellen, nicht oder nur zu einem geringeren Maße befruchtungsfähig (MOORE und BEDFORD 1978). Die Entfernung der Kumuluszellen vor der In-vitroBefruchtung beim Rind war mit einem geringeren Anteil von Spermienpenetration verbunden (ZHANG et al. 1995, THANGE 2003). Vermutlich erfüllen die Kumuluszellen vielschichtige Aufgaben während der In-vivo- und In-vitro-Befruchtung, in dem sie als Selektionsfilter für die Spermien dienen. Sie bilden eine für die Kapazitation und Penetration der Spermien, günstige Umgebung (THANGE 2002; VAN SOOM et al. 2002). 2.3 Gewinnung unreifer KOK beim Rind durch OPU Die ultraschall geleitete, transvaginale Follikelpunktion oder Ovum-Pick-Up (OPU) wurde ursprünglich im humanmedizinischen Bereich bei Fertilitätspatientinnen eingesetzt, um unreife Eizellen für die In-vitro-Fertilisierung zu gewinnen. Diese minimal invasive In-vivo-Technik wurde modifiziert und erstmals von PIETERSE et al. (1988) bei Kühen eingesetzt. Sie kann auch bei anderen Nutztierarten (Pferden: (BRÜCK et al.1997; Büffel: BONI et al. 1996) und Wildtierarten (Lama: BROGLIATTI et al. 2000; Zebra: MEINTJES et al. 1997) erfolgreich angewendet werden (siehe Tabelle 1). OPU kann beim Rind, bei 2 wöchentlichen Sitzungen über mehrere Monate durchgeführt werden, ohne dass Schäden am Tier entstehen, die eine weitere Zuchtverwendung beeinträchtigen (RICK 1996; BAGE et al. 2003). CHASTANT- 19 Literatur ___________________________________________________________________________ MAILLARD et al. (2003) stellten fest, dass die Punktion selbst keinen größeren Stress als routinemäßige tierärztliche Eingriffe wie rektale Untersuchungen oder das Setzen einer Epiduralanästhesie für die Tiere darstellt. OPU hat auch keine negativen Auswirkungen auf die Milchleistung und den Immunstatus der Tiere. Tabelle 1: Effizienz der ultraschall geleiteten, transvaginalen Follikelpunktion bei einigen Nutz- und Wildtierarten Tierart MW KOK/Tier/Sitzung Teilungsrate Blastozystenrate Autor Pferd (Equus caballus) 2,4 k.A. k.A. BRÜCK et al.1996 Büffel (Bubalus bubalis) k.A. 38% 15% KITIYANANT et al. 1995 Büffel (Bubalus bubalis) 4,5 40,1 15,6% GALLI et al. 2001 Büffel (Bubalus bubalis) 2,7 k.A. 16,7% BONI et al. 1996 Ziege (Capra aegagrus) 4,3** k.A. 16-24% GRAFF et al. 1999 Addax Antilope (Addax nasomaculus) k.A. 83% 0 ASA et al. 1998 Lama (Lama glama) 3,1* 9,0** k.A. k.A. BROGLIATTI et al. 2000 Zebra (Equus burchelli) 6,6 38% 16% MEINTJES et al.1997 MW = Mittelwert, k.A. = keine Angaben, * nicht stimuliert, ** mit FSH stimuliert Histologisch stellten CHASTANT-MAILLARD et al. (2003) blutgefüllte Follikel 4 Tage nach der letzten Punktion fest. 30 Tage nach der letzten Punktion waren kaum noch Veränderungen festzustellen, außer geringfügige Fibrinbildung im Ovargewebe. Technische Einflussfaktoren wie Nadellänge, Nadelanschliff, Vakuum, Häufigkeit der Punktion und Punktionsdauer können die Effizienz beträchtlich beeinflussen (PIETERSE et al. 1988; BOLS et al. 1995; BUNGARTZ und NIEMANN 1994; SIMON et al. 1993). 20 Literatur ___________________________________________________________________________ Abbildung 8: OPU beim Kalb mit Detailansicht der Punktion 21 Literatur ___________________________________________________________________________ Ebenso können tierindividuelle Faktoren wie Alter, Reproduktionsstatus und Rasse der punktierten Tiere die Punktionsergebnisse beeinflussen. Von Färsen konnten mit OPU weniger Oozyten und weniger Blastozysten erhalten werden als von adulten Kühen (KRUIP et al.1993, RICK et al. 1996, KIESSLING 2000). BUNGARTZ et al. (1995) gewannen eine signifikant höhere Anzahl von Oozyten und Blastozysten von Kühen, die sich 6- 20 Wochen nach der Kalbung befanden als von Kühen, die vor mehr als 20 Wochen abgekalbt hatten. Eine OPU Grundausstattung besteht aus einem Ultraschallgerät mit Bildschirm, einem Träger für Ultraschallkopf und Punktionsnadel, einem Spülsystem mit Schläuchen und Auffangröhrchen, einer Vakuumpumpe und einem Wasserbad. Trotz dieses beträchtlichen technischen Aufwands wird OPU häufig in der Praxis in Verbindung mit der In-vitro-Produktion von Embryonen (IVP), als Alternative oder Ergänzung zu MOET eingesetzt (TERBECK-HASENPUSCH et al. 2005; ROSCHLAU et al. 2005). OPU kann vielseitig erfolgreich angewendet werden, um zum Beispiel In-vitroFertilisation (IVF) taugliche KOK von älteren Tieren (KLOSSOK 1997), von Tieren während des ersten Drittels der Trächtigkeit (EICKELMANN 1999), Tieren kurz nach dem Abkalben (KNIEP 2000) oder von so genannten Problemtieren (LOONEY et al. 1994; ROSCHLAU 1997) zu gewinnen. OPU kann auch bei präpuberalen Tieren ab dem Alter von 5-6 Monaten eingesetzt werden, ohne die weitere Entwicklung der Tiere negativ zu beeinflussen. Im Institut für Tierzucht in Mariensee wurde das Punktionsgerät für Kälber modifiziert (RICK et al. 1996; WIEKING 2001; OROPEZA et al. 2004). Um die Anzahl und Qualität der gewonnen KOK, besonders von präpuberalen Tieren zu erhöhen, sollten die Ovarien der Tiere durch Gonadotropingabe stimuliert werden (ARMSTRONG et al. 1994; DUBY et al. 1996; PRESICCE et al. 1997; WIEKING 2001). 22 Literatur ___________________________________________________________________________ 2.4 Unterschiede in der Entwicklungskapazität von Oozyten aus Kälbern und Kühen Das Follikelwachstum beginnt beim Rind bereits während der Fetalentwicklung; die ersten antralen Follikel werden im Alter von 2 Wochen beobachtet (RAWLINGS 2003). Wellenartiges Follikelwachstum tritt bereits bei präpuberalen Rindern auf (PIERSON und GINTHER 1988; SAVIO et al. 1988; ADAMS et al. 1994). Untersuchungen einiger Forschergruppen haben jedoch gezeigt, dass aus Follikeln präpuberaler Rinder gewonnene Oozyten eine schlechtere Entwicklungskompetenz besitzen als Oozyten erwachsener Tiere (DAMIANI et al. 1996; REVEL et al. 1995; PRESICCE et al. 1997). Es wurden niedrigere Teilungs- und Blastozystenraten erzielt (siehe Tabelle 2). Eine mögliche Ursache ist, dass Oozyten präpuberaler Tiere nicht fähig sind, die zytoplasmatische Reifung vollständig zu durchlaufen. SALAMONE et al. (2001) haben die Aktivität von MPF, MAPK und IP3R (Inositol1, 4, 5-Triphosphat Rezeptor) in Oozyten von Kälbern analysiert. Diese war signifikant niedriger als in adulten Oozyten. Elektronenmikroskopische Untersuchungen zeigten bei Oozyten von Kälbern morphologische Unterschiede im Vergleich zu Oozyten von Kühen. Eine verspätete und ungleichmäßige Verteilung der Zellorganellen wie Mitochondrien, Lipidtröpfchen und kortikale Granula deutet auf eine mangelhafte zytoplasmatische Reifung hin (DAMIANI et al. 1996). Die geringere Anzahl an Mitochondrien zeigt einen niedrigeren Energiestoffwechsel bei Kälberoozyten an; in vitro wurde bei Oozyten aus Kälbern eine geringere Verstoffwechslung von Glutamin und Pyruvat in den ersten Stunden nach der Befruchtung festgestellt als bei Oozyten von Kühen (DE PAZ et al. 2001; STEEVES und GARDENER 1999). Die Stoffwechselaktivität erreichte bei Oozyten von 3-4 Monate alten Kälbern erst nach 24 Stunden Reifung das Niveau der Oozyten erwachsener Rinder (STEEVES und GARDNER 1999; GANDOLFI et al. 1998). Bei Embryonen von 5-7 Monate alten Kälbern stellten STEEVES et al. (1999) eine im Vergleich zu Embryonen von Kühen um die Hälfte niedrigere Glukoseaufnahme fest. OROPEZA et al. (2004) vermutete, dass der Insulin-like Growth Factor (IGF-I) die Aufnahme von Glukose in die Zellen von 23 Literatur ___________________________________________________________________________ Embryonen präpuberaler Tiere während der Kompaktierung und der Blastozystenbildung positiv beeinflusst. Es gibt aber auch Anhaltspunkte für eine unvollständige Kernreifung von Kälberooyzten. Im Nukleolus unreifer Kälberoozyten wurden zwei dichte, ovale Strukturen festgestellt, die von Fibrillen umgeben waren. Ungereifte Oozyten von Kühen besitzen dagegen nur eine solche Struktur (DAMIANI et al. 1996), was als ein Zeichen gewertet wird, dass die Oozyte die RNA- und Proteinsynthese abgeschlossen hat (FAIR et al. 1996). KATHIR et al. (1998) fanden nach 20 Stunden in vitro Kultur eine signifikant verzögertes Erreichen der Metaphase II in Kälberooyzten. Tabelle 2: Entwicklungskapazität von Oozyten aus Kälbern und Kühen im Hinblick auf Teilungs- und Blastozystenraten Alter der Kälber Teilungsrate Blastozystenrate 36,7% k.A.* 41-42% 10-11% TANEJA et al. (2000) 3 Monate 85,0% 73% REVEL et al. (1995) 5 Monate 24,0% 0 6 Monate k. A. 5,5% RICK (1996) 6 Monate 58,0% 12,2% KUWER (1998) 7 Monate 49,0% 5,0% PRESICCE et al. (1997) ≥ 7 Monate 33,8% 0 LOONEY et al. (1995) ≤ 7 Monate 63,4% 18,9% LOONEY et al. (1995) 9 Monate 88,0% 11,0% PRESICCE et al. (1997) 11 Monate 88,0% 48,0% PRESICCE et al. (1997) Kühe 73,3% 31,6% LOONEY et al.(1995) Kühe 87% 79,0% REVEL et al. (1995) Kühe k.A. 33,0% DAMIANI et al.(1996) 7,5 Monate v. Geburt, fetal 2-3 Monate Autor CHOHAN (2004) PRESICCE et al. (1997) *k.A.: keine Angaben Nach intraovarieller Applikation von IGF-I bei präpuberalen Kälbern erreichten die mRNA- Expression der Gene eIF1A (Eukaryontic Translation Initiation Factor-1A), 24 Literatur ___________________________________________________________________________ UBF (Upstream Binding Factor) und Glut-1 (Glukosetransporter-1), in präimplantatorischen Embryonen auf ein ähnliches Niveau erhöht wie das bei Embryonen aus erwachsenen Kühen, was auf eine wichtige Rolle von IGF-I bei der Erlangung vollständiger Entwicklungskapazität hindeutet (OROPEZA et al. 2004). Die Reifungskompetenz präpuberaler boviner Oozyten hängt auch mit ihrem Durchmesser zusammen (FAIR 2003). FAIR et al. (1995) stellten fest, dass bovine Oozyten erst von einem Durchmesser ab 110 µm fähig sind, die Meiose fortzusetzen. Oozyten von Kälbern sind kleiner (113,3-119,7 µm) als die von Kühen (117-125 µm) (DUBY et al. 1996, GANDOLFI et al. 1998). Kälberooyzten die weniger als 110 µm Durchmesser aufwiesen, erreichten nicht die Metaphase II, während Oozyten mit einem Durchmesser von 110-119 µm zu 30%, und Oozyten mit mehr als 120 µm Durchmesser zu 55% die Metaphase II erreichten (MAJERUS et al. 1999). Die Follikelflüssigkeit von Kühen beinhaltet mehr Proteine, weist eine höhere AromataseAktivität und einen höheren Gehalt an Östradiol auf, als die von 3 Monate alten Kälbern (DRIANCOURT et al. 2001). Zu ähnlichen Ergebnissen sind auch Untersuchungen bei anderen Nutztierarten gekommen. Bei Oozyten von 6-8 Wochen alten Lämmern wurden Unterschiede im Stoffwechsel zu solchen von erwachsenen Schafen gefunden. Der Metabolismus von Glutamin war bei Lämmern signifikant niedriger. In Glukose- und Pyruvatstoffwechsel wurden jedoch keine Unterschiede festgestellt (O’BRIEN et al. 1996). Von Oozyten präpuberaler Schweine wurden niedrigere Teilungs-und Blastozystenaten erhalten als von erwachsenen Sauen (IKEDA und TAKAHASHI 2003). 2.5 Ansätze zur Steigerung der Entwicklungskapazität von präpuberalen bovinen Oozyten Um Anzahl und Entwicklungskapazität präpuberaler boviner Oozyten zu steigern, wurden in der Vergangenheit verschiedene Untersuchungen durchgeführt. Präpuberale Tiere können hormonell durch eine i.m. Applikation von Gonadotropinen stimuliert werden (KUWER 1997; PRESICCE et al. 1997; FRY et al. 1998). KUWER (1997) erhielt nach intramuskulärer Applikation von hCG (humanes Choriongonadotropin) und FSH vor Anwendung von OPU eine signifikant größere 25 Literatur ___________________________________________________________________________ Anzahl an IVF tauglichen Oozyten als von Kontrolltieren ohne Behandlung. PRESICCE et al. (1997) konnten mit eCG (equines Choriongonadotropin) und FSH Applikationen den Anteil an Morulae und Blastozysten aus Oozyten von 5 Monate alten Kälbern auf ~10% steigern. Bei unstimulierten Tieren wurden keine Morulae und Blastozysten erhalten. Nach Superovulation mit FSH, hCG oder GnRH wurden mehr Follikel bei den mit GnRH stimulierten Tieren gefunden (FRY et al. 1998). Die Anzahl erhaltener Oozyten nach OPU war ähnlich wie bei unstimulierten Kälbern. Die intraovarielle Injektion von Gonadotropinen (WIEKING 2001) oder Wachstumsfaktoren (OROPEZA 2004) ist eine technisch aufwendigere Methode, um Follikelwachstum, Oozytenanzahl und Qualität bei juvenilen Kälbern zu stimulieren. WIEKING (2001) konnte mit 1,25 mg bzw. 2,5 mg intraovariell (i.o.) verabreichtem FSH Anzahl und Qualität Oozyten im Vergleich zu unstimulierten Kälbern steigern. Es konnten auch Kälber nach Transfer von in vitro erzeugten Embryonen aus Kälberoozyten produziert werden. Nach i.o. Injektionen des Wachstumsfaktors IGF-I und 60 mg FSH i.m. erhielt OROPEZA (2004) von Kälbern im Alter zwischen 6-7 Monaten mehr Blastozysten als von Kontrolltieren. Bei den älteren Tieren von 9-11 Monaten waren die Blastozystenraten ähnlich denen bei Kühen. Die Anzahl von Follikeln und Oozyten waren bei allen Altersgruppen ähnlich. PALMA et al. (2001) versuchten durch Zugabe von FSH und Oestradiol-17β in das Reifungsmedium, die Entwicklungskompetenz von Kälberoozyten zu erhöhen. Höhere Konzentrationen Blastozystenraten zur von Folge. Oestradiol-17β Höhere hatten Konzentrationen aber von FSH niedrigere dagegen verbesserten die Entwicklungsfähigkeit der Kälberoozyten. Eine in vivo Kultur in Kanincheneileitern erhöhte die Entwicklungskapazität präpuberaler Ziegenoozyten nicht im Vergleich zur In vitro Kultur mit oder ohne Eileiterzellen (IZQUIERDO et al. 2002). Weder der Zusatz von fetalem Kälberserum noch Follikelflüssigkeit aus Follikeln präpuberaler Kälber oder erwachsenen Kühen im Reifungsmedium erhöhte die Entwicklungsfähigkeit von KOKs aus Kühen und Kälbern. Dagegen waren die Entwicklungsraten der KOKs von Kühen erhöht (KHATIR et al. 1997). 26 Literatur ___________________________________________________________________________ Die bei Oozyten adulter Rinder erfolgreiche Prämaturation durch reversible Meioseinhibitoren wie Butyrolactone-I (BL-I) und Roscovitine (Rosco) hatte bei Oozyten von 6-9 Monate alten Kälbern einen negativen Einfluss auf ihre Entwicklungskompetenz (DONNAY et al. 2004; PAVLOK et al. 2000). Durch Zusatz von FF-MAS in das Reifungsmedium konnte die Kernreifung präpuberaler Kälberoozyten stimuliert werden. Auf die Verbesserung ihrer Entwicklungskompetenz nach der Befruchtung hatte FF-MAS jedoch keinen positiven Effekt, was zeigte, dass die Folgen einer mangelhaften zytoplasmatischen Reifung durch eine erfolgreiche Kernreifung nicht aufgehoben werden konnten. Die Stimulierung der Glutathion-Synthese (GSH) durch den Zusatz von Cystein und Cystamin ins Reifungsmedium (DE MATOS et al. 2000) konnte die zytoplasmatische Reifung und nachfolgende Entwicklungsfähigkeit juveniler Kälberoozyten verbessern (DONNAY et al. 2004). 2.6 Kokultur in der In-vitro-Produktion von Embryonen Um die Effizienz der In-vitro-Produktion von Embryonen zu steigern wurden in der Vergangenheit Eileiterzellen und Follikelzellen in verschiedenen IVP-Schritten mit verwendet. ROMAR et al. (2001) gelang es, durch Kultivierung porziner KOK für 4 Stunden auf porzinen Oviduktepithelzellen und Verkürzung der IVF-Phase auf 6 Stunden, die Polyspermierate zu senken. Durch den Einsatz porziner Granulosazellen in verschiedenen Reifungssystemen konnte die Kernreifung porziner Oozyten aber nicht gesteigert werden. Bovine Granulosazellen allein, aber auch die Zugabe von EGF und FSH, steigerten die Kernreifung der porzinen Oozyten (SOMMER 1991). Epithelzellen aus den Eileitern präpuberaler und erwachsener Ziegen wurden in der Ko-Kultur eingesetzt, um die Entwicklungskompetenz präpuberaler Ziegenoozyten zu steigern (IZQUIERDO et al. 2002). Die Blastozystenraten waren in beiden Versuchsgruppen aber ähnlich. MOGAS et al. (1997) setzten Granulosazellmonolayer aus Follikeln präpuberaler und adulter Ziegen während der Reifung und Embryokultur von Ziegenoozyten bzw. Zygoten ein. Sie stellten eine signifikant höhere Maturations-, Teilungs- und Blastozystenrate bei der Gruppe fest, die auf 27 Literatur ___________________________________________________________________________ Granulosazellmonolayern von FSH behandelten, juvenilen bzw. adulten Ziegen stammten, im Vergleich zu den unbehandelten juvenilen bzw. adulten Tieren. Ähnliche Ergebnisse, im Hinblick auf Befruchtung, Teilung und Blastozystenzahlen, erreichten TEOTIA et al. (2001) nach Reifung von Ziegenoozyten auf Granulosazellmonolayern. Die Granulosazellen stammten aus kleinen (≤ 4mm) oder großen (≥ 4mm) Follikeln. Das Reifungsmedium wurde 18-24 Stunden vor der Reifung auf den Monolayer verbracht. Im Bereich der In-vitro-Produktion beim Rind gibt es nur wenige Untersuchungen, in denen Granulosazellen verwendet wurden, um das Entwicklungspotential von präpuberalen Oozyten zu erhöhen. REVEL et al. (1995) verwendeten bovine Granulosazellmonolayer für die Reifung von Oozyten 3 Monate alter Kälber nach der Schlachtung. Die Blastozysten- und Trächtigkeitsraten (9-11% und 1/23 Übertragungen) waren jedoch deutlich niedriger als bei Kühen (20% Blastozystenraten und 38% Trächtigkeitsrate). Der Einfluss verschiedener Zusätze wie fetal calf serum (FCS), oestrous cow serum (ECS) mit entweder FSH, LH, Oestradiol oder Granulosazellen, in unterschiedlichen Schritten der IVP auf adulte bovine Oozyten wurde von FUKUI und ONO (1989) untersucht. Die höchsten Blastozystenraten wurden nach Kokultur mit Granulosazellen erhalten (FUKUI und ONO 1989). Mit Zusatz von Progesteron im Kulturmedium konnte im Vergleich zu einem Granulosazellmonolayer keine höheren Befruchtungsraten von adulten bovinen Oozyten erzielt werden (THANGE et al. 2001). Die Anzahl polysperm befruchteter Oozyten war jedoch signifikant höher. 2.7 Expression entwickunglsrelevanter Gene bei bovinen präimplantatorischen Embryonen Die Genexpression in eukaryontischen Zellen beginnt mit der Produktion einer RNAKopie eines bestimmten Abschnittes der DNA-Dopplelhelix eines Gens, der Transkription. Bei der anschließenden Translation werden die Basensequenzen der RNA in die Aminosäurensequenzen der Proteine übersetzt. 28 Literatur ___________________________________________________________________________ Die Transkription findet im Zellkern und die Translation im Zytoplasma statt. Sie wird in drei Abschnitte unterteilt. 1. Die Initiation, in der sich die RNA-Polymerase in der Promotorregion an die DNA bindet, in der die funktionelle RNA kodiert ist. Dort befindet sich die so genannte TATA-Box mit vielen T und A Nukleotiden. 2. Die Elongation bei der nur der codogene Strang der DNA kopiert wird. 3. Die Termination mit der die RNA-Synthese endet. Es gibt fünf Arten von RNA, die in der Zelle unterschiedliche Funktionen haben (ALBERTS et al. 1994a; GELDERMANN et al. 2005). 1. Ribosomale RNA (rRNA): Sie befindet sich in den Ribosomen im Nukleolus und wird von der Polymerase I an DNA-Matrizen synthetisiert. 2. Prä-rRNA: Sie befindet sich zusammen mit Proteinen in den Ribosomen im Nukleolus. 3. Heterogene Kern RNA (hnRNA): Sie gilt als Vorläufer der mRNA und befindet sich im Zellkern. 4. Messenger RNA (mRNA): Sie wird von der Polymerase II synthetisiert und trägt die Information für die Proteinsynthese 5. Transfer RNA (tRNA): RNA-Polymerase III synthetisiert die tRNA und ihren Vorläufer, die 5S-rRNA. Bevor die mRNA in Proteine umgeschrieben werden kann, kommt es zu so genannten posttranskriptionellen Modifikationen. Die hnRNA ist das Transkript der RNA-Polymerase II. Sie wird an ihren 5’- und 3’- Enden modifiziert, was als RNAProzessing bezeichnet wird (TAKAGAKI et al. 1988) Am 5’- Ende wird ein methyliertes G- Nukleotid als Kappe (cap) angeheftet. Diese Cap-Struktur gilt als Startstelle für die spätere Translation. Weiterhin wird am 3’- Ende, durch die Poly(A)Polymerase ein so genannter Poly(A)-Schwanz angehängt, der aus 100-200 AdeninNukleotiden besteht. Er schützt die mRNA gegen Abbau im Zytoplasma (FRIEDMAN et al. 1987; GANDOLFI und GANDOLFI 2001). Die Prä-mRNA beinhaltet noch die Introns. Diese unkodierten Sequenzen befinden sich in der kodierten Sequenz, den 29 Literatur ___________________________________________________________________________ Exons. Bevor die endgültige mRNA entstehen kann, werden die Introns während des „Gen-Splicing“ herausgeschnitten und die Enden wieder verknüpft. Die mRNA wird nun aus dem Zellkern in das Zytoplasma geschleust, wo die Basensequenz in die Aminosäurensequenz übersetzt wird (ALBERTS et al. 1994a). RNA-Molküle und Proteine werden während der Wachstumsphase von Oozyten für die frühe embryonale Entwicklung gespeichert. Durch die Regulierung der Poly(A)Schwanzlänge, RNA-Lokalisierung Dephosphorylierung werden RNA und und Proteinphosphorylierung Proteine stillgelegt und bzw. gespeichert (GANDOLFI und GANDOLFI 2001). Untersuchungen an bovinen Oozyten haben gezeigt, dass der Poly(A)-Schwanz bei einigen entwicklungsrelevanten Genen z.B. Connexin 43, GLUT1, Hsp.70, RNA Poly(A), Polymerase, oct-4 und Plakophilin, nach der In-vitro-Reifung kürzer waren als in der Metaphase II (BREVINIGANDOLFI et al. 1999). BREVINI et al. (2002) stellten einen Zusammenhang zwischen niedriger Entwicklungskapazität boviner Oozyten und abweichenden Mustern in der Polyadenylierung und Deadenylierung spezifischer mRNA-Transkripte her. Für die Translation werden mRNA und tRNA an Ribosomen, die aus Proteinen und rRNA bestehen, gebunden. Transfer-RNAs sind kleine RNA-Molküle, die sich in einer Kleeblattformation anordnen. Auf der mittleren Schleife befindet sich das Antikodon, das komplementär zu dem Kodon ist, der die jeweilige Aminosäure kodiert und aus drei Nukleotiden besteht. Weil aber 4 Basen zur Verfügung stehen, könnten 64 Aminosäuren kodiert werden. Es werden aber nur Kodierungen für 20 Aminosäuren gebraucht und darum gibt es für eine Aminosäure mehrere Kodons (CRICK 1966). Die Translation beginnt normalerweise mit dem „AUG“-Triplet nach dem 5’Cap. Während der folgenden Elongation werden andere Aminosäuren an die wachsende Polypeptidkette gebunden. Die Translation endet mit den Sequenzen UAA, UAG oder UGA (ALBERTS et al. 1994). Oozyten speichern schon während der Oogenese Gentranskripte und Proteine für die frühe embryonale Entwicklung (SCHULTZ 1993). Fortschritte in der molekularbiologischen Technik ermöglichen Grundlagenforschung an Oozyten und Embryonen unterschiedlicher Spezies, um kritische Schritte in der Oozyten- und 30 Literatur ___________________________________________________________________________ Embryonenentwicklung auf molekularer Ebene zu verstehen. Mit der Entwicklung der RT-PCR (Reverse Transcriptase Polymerase Chain Reaktion) konnten viele Gene bestimmt und deren Expressionsmuster analysiert werden. Die RT-PCR ermöglicht es, auch kleinste Mengen an genetischem Material zu analysieren, wie sie zum Beispiel in Oozyten oder Embryonen enthalten sind. Die Zelle liest und verwendet den genetischen Code, der im Nukleus vorhanden ist, um für sich notwendige Proteine, über die Umschreibung der DNA Information in der RNA (Transkription) und die Übersetzung der Basensequenzen der RNA in die Aminosäurenfolge der Proteine (Translation), zu synthetisieren (ALBERTS et al. 1994b). Das Wissen über die Fähigkeit der Zelle, diesen genetischen Code zu nutzen und welche Gene wann exprimiert werden, hilft beim Verständnis vieler wichtiger Vorgänge in Zellen, Gewebsstrukturen und im präimplantatorischen Embryo. Die Oozyte synthetisiert und speichert schon während der Oogenese Gentranskripte und Proteine, die sie für die embryonale Entwicklung nach der Befruchtung benötigt (SCHULTZ 1993). In diesem Zustand verharrt sie bis zur Befruchtung (GANDOLFI und GANDOLFI 2001). Nach der Befruchtung werden mit jeder Zellteilung die mütterlichen Transkripte und Proteine weniger und das embryonale Genom übernimmt mehr und mehr die Kontrolle über die Entwicklung des Embryos (TELFORD et al. 1990). VIUFF et al. (1996) stellten schon in bovinen Zygoten und 24 Zellstadien eine geringe Transkriptionsaktivitäten fest. Nach dieser ersten Phase der geringen Transkriptionsaktivitäten kommt es in der zweiten Phase zu einer sehr starken Zunahme der Transkriptionsaktivtät. Diese findet beim Rind im 8-16 Zellstadium statt (KOPECNY et al. 1989; VIUFF et al. 1996; MEMILI et al. 1998, MEMILI und FIRST 2000). Während der frühen Embryonalentwicklung in vitro kann es beim Rind nach dem vierten Zellzyklus zum Entwicklungsstopp kommen. Das entspricht dem Übergang vom 8 zum 16 Zellstadium (CAMOUS et al. 1984; EYESTONE et al. 1991). Zwei Hauptursachen werden für diesen Entwicklungsstopp vermutet. Entweder der Embryo ist nicht fähig, die Transkription entwicklungsrelevanter Gene zu aktivieren oder es liegen negative Umwelteinflüsse vor, wie zum Beispiel suboptimale Kulturbedingungen (BETTS und KING 2001). 31 Literatur ___________________________________________________________________________ Die Proteinsynthese nimmt vom 8-16 Zellstadium bis zum Blastozystenstadium kontinuierlich zu (FREI et al. 1989). Die embryonale mRNA-Expression und somit die Entwicklung boviner präimplantatorischer Embryonen können durch In-vitro-Produktion d.h. Kulturmedien, Manipulation und Umwelteinflüsse wie Atmosphäre oder Temperatur, verändert werden (WRENZYCKI et al. 2005a, b, 2004; NIEMANN und WRENZYCKI 2000). So unterscheiden sich in vitro produzierte bovine Embryonen von in vivo gewonnenen Embryonen in ihren relativen mRNA Transkriptgehalten zum Beispiel durch Up– oder Downregulierung, Abschaltung oder de-novo Induktion von Genen (WRENZYCKI et al. 1999; LAZZARI et al. 2002, WRENZYCKI et al. 2005 a, b). Trotz der Fortschritte in der In-vitro-Produktion boviner Embryonen und beim Kerntransfer kann es zum Auftreten des „Large offspring syndrome“ (LOS) kommen. Die am häufigsten beobachteten Symptome in LOS sind: Hydramnion, Hydrops fetalis, veränderte Plazenta, erhöhte Geburtsgewichte, Totgeburten, vergrößerte Organe, Anomalien des Skelettes. Die Symptome können einzeln oder in unterschiedlichen Kombinationen auftreten (KRUIP und DEN DAAS 1997; WALKER et al.1996; YOUNG et al. 1998). Es wird vermutet, dass epigenetische Veränderungen in der fetalen und embryonalen Genexpression, wie DNAMethylierung oder Histon-Modifikationen, die an die Regulierung der imprinted und nonimprinted Gene beteiligt sind, für das Auftreten von LOS mit verantwortlich sind (WRENZYCKI et al. 2004, 2005 a, b; BIRD und WOLFFE 1999). Unterschiedliche IVP-Protokolle können eine veränderte mRNA-Expression zur Folge haben (WRENZYCKI et al. 2005 a, b). Die Herkunft der Embryonen ist dabei von erheblicher Bedeutung. Embryonen aus präpuberalen Tieren wiesen ebenfalls einen unterschiedlichen Transkriptionsgehalt bei einigen Genen im Vergleich zu solchen von adulten Tieren auf. Dabei handelt es sich um Gene, die insbesondere in Stoffwechsel (Glut-1) und Proteinsynthese (UBF, eIF1A) beteiligt sind (OROPEZA et al. 2004). Im Folgenden sollen Eigenschaften und Funktionen von Genen, die in der vorliegenden Arbeit untersucht wurden, beschrieben werden. 32 Literatur ___________________________________________________________________________ 2.7.1 Growth differentiation factor-9 (GDF-9) Der zur großen Familie der TGF-β Wachstumsfaktoren gehörende GDF-9 wird von Oozyten während der frühen Follikelentwicklungsphase synthetisiert und ist vor allem für Differenzierung und Proliferation der Granulosazellen und Kumulusexpansion verantwortlich (KNIGHT und GLISTER 2001; SENDAI 2001; CHANG et al. 2002; KNIGHT und GLISTER 2003). Die vielseitigen und komplexen Funktionen von GDF-9 wurden bereits in Kapitel 2.2.1- 2.2.3 behandelt. Mit Hilfe von Northern Blot und RT- PCR Analysen haben FITZPATRICK et al. (1998) GDF-9 mRNA bei Mäusen und Ratten in Ovar, Hoden, und Hypothalamus festgestellt. Beim Menschen war GDF-9 im Ovar und im Hoden, im Uterus und in der Hypophyse vorhanden. Über die Funktion von GDF-9 außerhalb der Gonaden ist noch wenig bekannt. In Ovarien zyklischer Ziegen wurde in Follikeln- und im Corpus luteum mRNA für GDF-9, BMP15 und BMP Rezeptoren festgestellt. Die Anwesenheit der BMP- Rezeptoren und Proteinen in allen Entwicklungsstadien der Follikel (außer Primordialfollikel) lässt einen Zusammenhang von GDF-9 auch mit der Luteinisierung der Granulosa- und Thecazellen vermuten (SILVA et al. 2004). In bovinen Oozyten und präimplantatorischen Embryonen wurden GDF-9 Transkripte in Primordialfollikeln (BODENSTEINER et al.1999) bis zum 5-8 Zellstadium des Embryos (PENNETIER et al. 2004) festgestellt. Der relative Transkriptgehalt von GDF-9 war in unreifen bovinen Oozyten am höchsten. Nach der Reifung fiel die Expression von GDF-9 stark ab. Während des LH-Puls gewonnene Oozyten und in vitro gereifte Oozyten wiesen einen höheren Transkriptgehalt als in vivo gereifte Oozyten auf (LONERGAN et al. 2003). HUMBLOT et al. (2005) stellten dagegen eine höhere Expression von GDF-9 12 h nach Prostaglandingabe, d.h. 24 Stunden vor dem erwarteten LH- Puls, fest. Bei Kälberoozyten ist die Expression von GDF-9 noch nicht untersucht worden. 2.7.2 Heat shock- Protein 70 (Hsp.70) Heat shock-Proteine wirken in eukaryontischen Zellen im wesentlichen als Schutzproteine. Sie helfen bei der Faltung von Proteinen im endoplasmatischen 33 Literatur ___________________________________________________________________________ Retikulum. Sie haben eine Affinität zu hydrophoben Aminosäuren, die bei unvollständig gefalteten Proteinen an der Oberfläche liegen. Heat shock-Proteine werden in großen Mengen synthetisiert, wenn die Zellen für kurze Zeit hohen Temperaturen (etwa 42°C) ausgesetzt werden (ALBERTS et al. 1994c) Schädliche Umwelteinflüsse wie zum Beispiel zu hohe Außentemperaturen am ersten Tag der Trächtigkeit (Östrus=Tag 0) können die Entwicklungsfähigkeit von Embryonen beeinträchtigen. Ab Tag 2-7 werden die Embryonen dann widerstandsfähiger (EALY et al. 1993). Die erhöhte Expression von Hsp.70 kann ein wichtiger Hinweis für die Empfindlichkeit von Embryonen gegenüber Veränderungen in ihrer Umgebung sein. Die Anwesenheit von Kumuluszellen während der Reifung erhöhte die Proteinsynthese in den Oozyten (EDWARDS und HANSEN 1996) während ohne Zellen die Synthese von Hsp.70 verringert war und die Embryonen empfindlicher gegenüber Temperaturerhöhungen wurden (EDWARDS und HANSEN 1997) Suboptimale Kulturmedien können den Gehalt an Transkripten für Hsp.70 in Rinderembryonen erhöhen. Von der gereiften Oozyte bis zur Blastozyste weisen in Medium mit Zusatz von PVA (Polyvinyl Alkohol) kultivierte Oozyten und Embryonen einen höheren Transkriptgehalt auf als in Medium mit Zusatz von Serum (ECS) (WRENZYCKI et al. 1999). In TCM 199 (Tissue Culture Medium 199) kultivierte Morulae und Blastozysten zeigten eine signifikant höhere Expression von Hsp.70 als solche in SOF+ (FAF)-BSA (Synthetic Oviduct Fluid+Fattyacid-Free Bovine Serum Albumin) kultivierte Embryonen (WRENZYCKI et al. 2001a). In vivo gewonnene, expandierte Blastozysten wiesen dagegen geringere Expressionen von Hsp.70 mRNA auf als Embryonen aus der In-vitro-Produktion (WRENZYCKI et al. 1998). Hsp.70 erwies sich in verschiedenen Untersuchungen als sensitiver Indikator für suboptimale Kulturbedingungen (WRENZYCKI et al. 1999; WRENZYCKI et al. 2001 a, b; LAZZARI et al. 2002; RIEF et al. 2002; HUMBLOT et al. 2005). Hsp.70 wird beim Rind in Oozyten und allen präimplantatorischen Embryonalstadien exprimiert. Der Gehalt an Hsp.70 Transkripten ist bei Oozyten und präimplantatorischen Embryonen von präpuberalen Kälbern noch nicht untersucht worden. 34 Literatur ___________________________________________________________________________ 2.7.3 Glukosetransporter-3 (Glut-3) Die Energieversorgung von Embryonen vor der Kompaktierung ist hauptsächlich von der ATP-Synthese (Adenosin Triphosphat) abhängig. Das ATP wird zum größten Teil aus der Oxidation von Pyruvat gewonnen (THOMPSON 1996; KHURANA und NIEMANN 2000). Mit fortschreitender Weiterentwicklung und verstärkter Proteinsynthese und Bildung des Blastozoel steigt der Verbrauch an ATP. Der Embryo verwendet nun vermehrt auch Glukose und Aminosäuren zur Energieversorgung (PARTRIGE und LEESE 1996). Vom 8-16 Zellstadium an steigt der Glukoseverbrauch des Embryos stetig an (KHURANA und NIEMANN 2000). Die Familie der Glukosetransporter umfasst zahlreiche Mitglieder (Glut-1-12), deren Sequenzen ähnlich, aber in verschieden Geweben zu finden sind (JOOST et al. 2002). Sie konnten auch in präimplantatorischen Embryonen verschiedener Spezies gefunden werden. Die Glukoseaufnahme gilt als wichtiger Parameter für die Beurteilung der Entwicklungsfähigkeit von Oozyten präpuberaler Kälber und adulter Kühe (GANDOLFI et al. 1998; STEEVES et al. 1999). Bei der Maus wurde Glut-3 in expandierten Blastozysten nachgewiesen (PANTALEON et al. 1997). Dieses Molekül befindet sich apikal an den Zellen und ist für den direkten Transport von Glukose in die Zellen der inneren Zellmasse verantwortlich. Zusammen mit Glut-1, das an den basolateralen Oberflächen der Trophektodermzellen und Zellen des Embryonalknotens (Inner Cell Mass, ICM) lokalisiert ist, sichert Glut-3 die Glukoseversorgung der Blastozyste (PANTALEON und KAYE 1998). Die Glut-3 und Glut-1 mRNA Expression ist bei bovinen Embryonen nachgewiesen worden (WRENZYCKI et al. 1999; AUGUSTIN et al. 2001). Geschlüpfte Blastozysten wiesen einen höheren Transkriptgehalt von Glut-1 als unreife und gereifte Oozyten, Zygoten und Embryonen bis zum 8-16 Zellstadium (WRENZYCKI et al. 1999; WRENZYCKI et al. 1998; AUGUSTIN et al. 2001). Glut-3 wurde in Blastozysten aus in vitro KulturSystemen (SOF-Serum, SOF-BSA) und aus ligierten Schafeileitern stärker exprimiert als bei in vivo gewonnenen Blastozysten (LAZZARI et a. 2002). Transkripte für Glut-1 sind in präpuberalen bovinen Embryonen nachgewiesen worden (OROPEZA et al. 2004). Der mRNA- Gehalt nahm vom 2-4 Zeller bis zum 8-16 Zeller ab. In 35 Literatur ___________________________________________________________________________ expandierten Blastozysten stieg der Transkriptgehalt jedoch wieder an, wobei Embryonen von mit IGF-I und rbST behandelten Tieren höhere Werte zeigten. Glut-3 ist bei präpuberalen bovinen Embryonen noch nicht nachgewiesen worden. 36 Material und Methoden ___________________________________________________________________________ 3 MATERIAL UND METHODEN Die in der vorliegenden Arbeit verwendeten Geräte, Medien und deren Inhaltsstoffe und Materialien werden im Anhang aufgeführt. 3.1 Kultivierung der Granulosazellen und Fibroblasten Die in der vorliegenden Arbeit beschriebenen Zellkulturen wurden zur Vermeidung von Kontamination unter einer sterilen Laborbank mit laminarem Luftstrom angesetzt. 3.1.1 Medien 3.1.1.1 PBS Für die Gewinnung von Granulosazellen aus den Follikeln wurde 9,25 g/l Dulbecco’s phosphate buffered saline (PBS), angereichert mit 50 IU/ml Penicillin G, 50 µg/ml Streptomycinsulfat, 36 µg/ml Na-Pyruvat, 1 mg/ml D-Glukose und 133 µg/ml CaCl2 verwendet, das am Tag der Gewinnung frisch mit Aqua bidest. angesetzt wurde. Am Tag der Gewinnung wurden 1 % FCS hinzugegeben und sterilfiltriert. 3.1.1.2 Zellkulturmedien Die gewonnenen Granulosazellen wurden in Natriumhydrogenkarbonat abgepuffertem Dulbecco’s Modified Eagle’s Medium (DMEM) bei einem pH von 7,17,4 kultiviert. Die Kontrolle der pH Werte erfolgte mit Phenolrot als Indikator. Das Grundmedium wurde mit 10ml/100ml fetalem Kälber Serum (FCS), 1ml/100ml Penicillin/Streptomycin Sulfat Stocklösung, 1ml/100ml Non Essential Amino Acids und 2,5 µg/ml Amphotericin angereichert. Das Medium wurde bei 4°C gelagert und für den Gebrauch auf 37°C im Wasserbad erwärmt. 3.1.1.3 Einfriermedium Das Zellkulturmedium diente auch als Grundmedium, dem als Kryoprotektivum Dimethyl Sulfoxid (DMSO) im Verhältnis 9:1 zugegeben wurde. Die Zusammensetzung der Medien ist in den Tabellen 15-17 dargestellt. 37 Material und Methoden ___________________________________________________________________________ 3.1.2 Gewinnung und Kultivierung der Granulosazellen Für die Gewinnung von Granulosazellen wurden Rinderovarien aus dem Schlachthof in Lübbecke verwendet, die Gelbkörper aufwiesen. Follikel mit einem Durchmesser zwischen 2 und 5 mm wurden punktiert. Die Ovarien wurden gründlich im 30°C warmen PBS gewaschen und vor dem Punktieren mit einem Papiertuch abgetrocknet. Für die Punktion wurde sterilfiltriertes PBS mit 1% Serumzusatz (FCS) verwendet, das bei Raumtemperatur gehalten wurde. Die Follikel wurden mit einer 0,9x40mm Kanüle und einer 1 ml Spritze punktiert. Das Punktat wurde in sterile 50 ml Zentrifugenröhrchen verbracht und für 4 min bei 200 g zentrifugiert. Nach Absaugen des Überstandes wurde das weissliche Zellpellet mit 10 ml PBS resuspendiert und noch einmal zentrifugiert. Die Zellen in der Suspension wurden mit 10 ml Zellkultumedium verdünnt, mittels NeubauerZählkammer die Zellzahl bestimmt und die Zellkonzenration pro Milliliter errechnet. Die Suspension wurde entsprechend verdünnt und mit einer Glaspipette in 75 cm2 Zellkulturflaschen überführt. Die Zellen wurden im Inkubator bei 37°C, 5 %CO2 und gesättigter Luftfeuchtigkeit kultiviert. Nach 24 Stunden wurde das Medium gewechselt, um die auf der Oberfläche schwimmenden, toten Zellen zu entfernen. Das Wachstum der Zellen wurde täglich kontrolliert. Innerhalb von 5 Tagen proliferierten die Zellen zu einem ca. 70-80% konfluenten Monolayer. 3.1.3 Aliquotieren und Einfrieren der Granulosazellen Das Medium wurde abgesaugt, 2x mit PBS gewaschen, anschließend vollständig abgesaugt, auf die Zellen in 2 ml EDTA/Trypsin pipettiert und für 5-10 Minuten auf die Wärmeplatte gestellt. Zwischendurch wurde immer wieder unter dem Mikroskop kontrolliert, ob die Zellen sich schon von der Oberfläche der Kulturflasche gelöst hatten. Die Ablösung der Zellen wurde durch sanftes Klopfen der Flasche auf den Tisch und Schwenken des Trypsins unterstützt. Wenn sich alle Zellen von der Oberfläche gelöst hatten, wurde das Trypsin durch Zusatz von 6-8 ml Zellkulturmedium inaktiviert. Anschließend wurde der Flascheninhalt in ein Zentrifugenröhrchen verbracht, mit PBS bis 10 ml aufgefüllt und bei 200 g für 4 38 Material und Methoden ___________________________________________________________________________ Minuten zentrifugiert. Der Überstand wurde abgesaugt, das Pellet gelöst, bis 10 ml aufgefüllt und zentrifugiert. Nachdem der Überstand abgesaugt worden war, wurde Einfriermedium dazugegeben und die Zellen gut durchpipettiert. Aus einer 75 cm2 Zellkulturflasche erhielt man ca. 15-18 Aliquots à 1 ml. Die 2 Wells einer 4-Well Schale füllen können. Es wurden jeweils 1 ml Granuloszellsuspension in 1ml Kryotubes pipettiert, beschriftet und bei -80°C eingefroren. 3.1.4 Erstellen der Granulosazellmonolayer Die Kryotubes wurden im 38°C warmen Wasserbad aufgetaut. Schon vor dem Auftauen wurden 8 ml Zellkulturmedium in Zentrifugenröhrchen pipettiert. Sobald sich die Zellsuspension verflüssigt hatte, wurde der Inhalt suspendiert, in das Zentrifugenröhrchen verbracht und anschließend 4 Minuten bei 200 g zentrifugiert. Dieser Vorgang wurde wiederholt und nachdem der Überstand abgesaugt worden war, wurden 2 ml Zellkulturmedium hinzugefügt und wiederum gut durchpipettiert. Pro Well wurden 0,5 ml Zellsuspension in die Schale pipettiert. Die beschriftete 4-Well-Schale wurde für 48 h bei 37°C in gesättigter Luftfeuchtigkeit und 5% CO2 in den Inkubator gestellt. Nach 24 Stunden wurde die Kultur unter dem Mikroskop auf Kontamination und konfluentes Wachstum überprüft und das Medium gewechselt (siehe Abbildung 9). Nach weiteren 22- 24 Stunden vor dem Einsetzen der KOK wurde das Zellkulturmedium durch Reifungsmedium ersetzt. Das Zellkulturmedium wurde vorsichtig mit abgeflammter Pasteurpipette abgesaugt. Danach erfolgte die Spülung des Monolayers mit 0,5 ml PBS. Das PBS wurde abgesaugt und durch Reifungsmedium ersetzt. Das Reifungsmedium war vorher mindestens 30 Minuten im Inkubator äquilibriert worden. 3.1.5 Erstellen von Fibroblastenmonolayern Die Fibroblasten wurden freundlicherweise von Dr. Wilfried Kues für diese Versuche zur Verfügung gestellt. Sie waren aus der Ohrbiopsie eines gesunden, fertilen Rindes (Ohrmarke 8146) gewonnen, anschließend in flüssigem Stickstoff gelagert worden und für die Untersuchungen aufgetaut. 39 Material und Methoden ___________________________________________________________________________ Die weitere Aufbereitung, Kultivierung, Vermehrung, Einfrieren und Erstellung der Monolayer erfolgten wie für die Granulosazellen beschrieben. a) b) Abbildung 9: a) Granulosazell- und b) Fibroblastenmonolayer, Vergrößerung 200x 3.2 Transvaginale Ultraschall geleitete Follikelpunktion oder Ovum pick-up (OPU) KOK wurden von 46 weiblichen Kälbern, im Alter zwischen 7-8 Monaten, und 18 laktierenden Kühe (ab 60 Tage post partum, zyklisch) durch transvaginale Ultraschall geleitete Follikelpunktion gewonnen. Die Tiere der Rassen Holstein Friesian (HF) und Deutsches Schwarzbuntes Rind mit unterschiedlich hohen HF-Anteilen, stammten aus der Versuchsherde des Institutes für Tierzucht (FAL) in Mariensee. Es wurden nur Tiere in den Versuchen verwendet, deren Allgemein- und Geschlechtsgesundheit intakt war. Alle Kälber waren zu Beginn und während der gesamten Punktionen präpuberal, d.h. die Ovarien waren ohne Hinweise auf Ovulationen. Während der Versuche wurden die Kälber auf Spaltenböden gehalten. Die Kühe waren in Anbindehaltung aufgestallt. Die Futterration bestand aus Silage, Heu, Kraftfutter, Mineralien und Wasser ad libitum. 40 Material und Methoden ___________________________________________________________________________ 3.2.1 Vorbereitung der Versuchstiere Den Kälbern wurde 48 Stunden vor jeder OPU-Sitzung 60 mg FSH (Folltropin) i.m verabreicht. Den laktierenden Kühen wurde 48 Stunden vor jeder OPU-Sitzung 100 mg FSH i.m. appliziert. 3.2.2 Die Ovum-Pick-Up (OPU) Punktionssitzungen fanden im Biotechnologiezentrum innerhalb der Rinderversuchsanlage des Institutes für Tierzucht in Mariensee statt. Es wurde ein speziell für Kälber entwickelter und in Mariensee hergestellter Sondenträger mit integrierter Führungsschiene für die Punktionsnadel verwendet. Dieses Gerät ist kürzer, besitzt einen geringeren Durchmesser als das für Kühe (WIEKING 2001). Damit können präpuberale Tiere der Rasse HF ab dem Alter von 6-7 Monaten ohne Schaden punktiert werden. Zur Durchführung der Ultraschall geleiteten Follikelpunktion wurden die Kälber in einen Zwangstand geführt und fixiert. Die Kälber wurden mit 0,15-0,25 ml Xylazin sediert (Proxylaz, Atarost, Twistringen) und eine Epiduralanesthesie mit 2 ml Procain Hydrochlorid (Minocain2%) zur Ruhigstellung der Darmmotorik und Schmerzausschaltung gesetzt. Die Kühe bekamen entsprechend mehr Procain Hydrochlorid (4-5 ml) ohne vorherige Sedierung. Mit der linken Hand wurde das Ovar rektal fixiert. Nach trockener Reinigung der Vulva, wurde mit der rechten Hand der Sondenträger mit dem Ultraschallkopf in die Vagina eingeführt. Der Sondenträger wurde zuvor mit einer Einmal-Schutzhülle und etwas Ultraschallgel versehen, in einem Hautdesinfektionsbad geschwenkt und mit Gleitgel versehen. Unter Bildschirmkontrolle wurden die Follikel auf einem Ovar nacheinander auf die Punktionslinie gelegt und punktiert. Nach jeweils 3-4 Punktionen wurden Punktionsnadel und Schlauchsystem mit PBS gespült, um das Punktat in das Sammelröhrchen zu spülen und um ein Verstopfen der Schläuche mit Blut zu verhindern. Die Sammelröhrchen waren mit der Ohrmarkennummer des punktierten Tieres beschriftet und befanden sich während der gesamten Punktionssitzung im Wasserbad bei 38°C. 41 Material und Methoden ___________________________________________________________________________ Nach Beendigung der Punktion wurde das Sammelröhrchen in das IVF Labor gebracht. Das Punktat wurde durch ein Industriesieb mit 50 µm Porengröße gegossen. Dieses wurde erst mit PBS gespült und anschließend wurden die KOKs unter einem Stereomikroskop bei 50 facher Vergrößerung gesucht. Von jedem Tier wurden die Punktate einzeln gesammelt, getrennt gesucht und beurteilt. Erst zur Aufteilung in die verschiedenen Reifungsgruppen wurden die KOKs gepoolt. Es wurde darauf geachtet, das die Punktate maximal 30 Minuten nach beendeter Punktion durchsucht wurden. Der genauere Hergang der Punktion und die technischen Details wurden bereits ausführlich in den Arbeiten von RICK (1996), KUWER (1997) und WIEKING (2001) beschrieben. 3.3 Klassifizierung der Kumulus-Oozyten-Komplexe Nachdem die KOKs aus dem Punktat herausgesucht waren, wurden sie unter einem Stereomikroskop bei 50x Vergrößerung anhand der Morphologie des Zytoplasmas und der Kumuluszellagen in 5 Klassen (I-V) aufgeteilt (LOONEY et al. 1994). Klasse I Oozyten mit homogenem, gleichmäßig granuliertem Zytoplasma und mindestens 3 Lagen Kumuluszellen Klasse II Oozyten mit homogenem, gleichmäßig granuliertem Zytoplasma und weniger als 3 Lagen Kumuluszellen Klasse III Oozyten mit unregelmäßig granuliertem Zytoplasma, dunklen Flecken und einer Lage Kumuluszellen Klasse IV Oozyten ohne Kumuluszellen Klasse V Oozyten mit bereits expandiertem Kumulus 42 Material und Methoden ___________________________________________________________________________ 3.4 In-vitro-Produktion boviner Embryonen 3.4.1 Medien 3.4.1.1 PBS – Phosphate buffered saline Als OPU- Spülmedium wurde 9,25 g/l Dulbecco’s phosphate buffered saline (PBS) mit 50 IU/ml Penicillin G, 50 µg/ml Streptomycinsulfat, 36 µg/ml Pyruvat 1 mg/ml DGlukose und 133 µg/ml CaCl2 verwendet. Es wurde an den Tagen vor dem OPU mit Aqua bidest. angesetzt. Am Tag der Punktionssitzung wurden 10 ml/l (1%) hitzeinaktiviertes New Born Calf Serum (NBCS, Invitrogen) und 2,2 IU/ml Heparin-Na hinzugefügt. 3.4.1.2 TCM air Während des IVP Vorganges, wie Sammeln, Beurteilung und Denudieren der Oozyten und Zygoten wurde als Grundmedium TCM 199 Tissue Culture Medium verwendet. Es wurde in Aqua bidest. (Ampuwa) mit 22 µg/ml Pyruvat, 350 µg/ml NaHCO3, 50 µg/ml Gentamycin und 0,1 % BSA FAF hergestellt. NaHCO3 wurde vor den anderen Komponenten in Ampuwa gelöst, der pH-Wert bei 7,2 eingestellt und vor dem Lösen von BSA sterilfiltriert. 3.4.1.3 TCM + BSA (Reifungsmedium) Als Grundmedium wurde TCM 199 Tissue Culture Medium verwendet. Es wurde in Aqua bidest (Ampuwa) mit 22 µg/ml Pyruvat, 2,2 mg/ml NaHCO3, 50 µg/ml Gentamycin und 0,1 % BSA FAF hergestellt. NaHCO3 wurde vor den anderen Komponenten in Ampuwa gelöst, der pH-Wert bei 7,4 eingestellt und vor Zugabe von BSA sterilfiltriert. Am Tag des Gebrauchs wurden 10 IU/ml equines Choriogonadotropin (eCG) und 5 IU/ml humanes Choriongonadotropin (Suigonan, Intervet, Tönisvorst, Deutschland) zugegeben. 43 Material und Methoden ___________________________________________________________________________ 3.4.1.4 Sperm-TALP und Fert-TALP (Fertilisationsmedien) Für die In-vitro-Befruchtung (IVF) wurden zwei modifizierte Tyrode Medien verwendet. Sperm-Talp diente für das Swim-up und zum „Waschen“ der aufgetauten Spermien. Aus dem Fert-Talp wurden Wasch- und Fertilisationstropfen für die KOKs hergestellt. Die genaue Herstellung der Fertilisationsmedien und die Vorbereitung der Swim-up Methode wurden von OROPEZA (2004) beschrieben. Die Zusammensetzung der Medien ist im Anhang in Tabelle 20 dargestellt. 3.4.1.5 SOF-Medium (Kulturmedium) Die Zygoten wurden in mit 4mg/ml BSA-FAF angereichertem Synthetic-oviduct-fluid Medium (SOF) kultiviert. Die Stocklösungen wurden einmal im Monat hergestellt und bei 4°C aufbewahrt. Das eigentliche Medium wurde einmal pro Woche hergestellt, sterilfiltriert und bei 4 °C in sterilen Zentrifugenröhrchen gelagert. Für die Waschtropfen wurden 80 µl und für die Kulturtropfen je 30 µl SOF-Medium verwendet. Die genauen Zusammensetzungen der Stocklösungen bzw. des Kulturmediums sind im Anhang in den Tabellen 21und 22 dargestellt. 3.4.2 Reifung der Oozyten Die Oozyten wurden im Brutschrank bei 39 °C, 5 %CO2 und gesättigter Luftfeuchtigkeit in vitro gereift. Zur Reifung der Oozyten und als Waschmedium diente TCM-199. Am Tag der Verwendung wurden die Hormone eCG und hCG zugefügt. Die KOKs wurden in 4Well Schalen in 500 µl Reifungsmedium 24 Stunden gereift. 3.4.3 Reifung der Oozyten auf Monolayern Es wurde das gleiche Reifungsmedium verwendet und der gleiche Zeitrahmen befolgt wie für die Reifung ohne Monolayer. KOKs der Klassen I-III wurden aus dem Pool der gewonnenen Oozyten, unter Berücksichtigung von Qualität und Anzahl, gleichmäßig in zwei Gruppen aufgeteilt und in die Wells mit den Granulosazellen bzw. Fibroblastenmonolayern verbracht. 44 Material und Methoden ___________________________________________________________________________ Parallel wurde stets eine Gruppe KOKs im Standardverfahren, d.h. ohne somatische Zellen gereift. Nach der Reifung wurde die Kumulusexpansion beurteilt (sehr stark expandiert, leicht expandiert, nicht expandiert) in allen Versuchgruppenbeurteilt. Für die Reifung wurden in den Hauptversuchen stets nur Zellen einer Charge, d.h. eines Gewinnungstages verwendet. 3.4.4 In-vitro-Befruchtung Die KOKs wurden in Fert-Talp gewaschen und in 100 µl Mikrotropfen aus Fert-Talp verbracht. Diese wurden schon vorher hergestellt und mindestens 30 min äquilibriert. Die Tropfen waren mit Silikonöl überschichtet. Bis zur Zugabe der aufbereiteten Spermien verblieben die KOKs im Inkubator. 3.4.5 Aufbereitung der Spermien Für alle IVF-Versuche wurde Tiefgefriersperma des Bullen „Erwin“ (Charge 2704), das auf IVF-Tauglichkeit getestet war, verwendet. Das Sperma wurde bei 39°C in 25 Sekunden aufgetaut und nach dem leicht modifizierten Swim-Up Verfahren nach PARRISH et al. (1988, 1986) aufbereitet. Die endgültige Spermienkonzentration pro IVF-Drop betrug 1x106/ml Spermien. Der genaue Ablauf der Spermienaufbereitung ist bei OROPEZA (2004) beschrieben. 3.4.6 In-vitro-Kultivierung 18 Stunden nach der Zugabe der Spermien wurden die Zygoten in TCM-air verbracht und dort noch anhaftende Kumuluszellen und Spermien mechanisch, mit Hilfe von Glaskapillaren und Mundpipette, entfernt. Die denudierten Zygoten wurden in 80 µl Waschtropfen aus SOF-Medium 3x gewaschen und anschließend in 30 µl Kulturtropfen verbracht. Die beschrifteten Petrischalen wurden in luftdicht verschließbaren Kulturkammern (Modular Incubation Chamber) unter Begasung mit 5 %O2, 90 %N2 und 5 %CO2 7-8 Tage kultiviert. 45 Material und Methoden ___________________________________________________________________________ b) a) Abbildung 10: Tag 8 Blastozysten von a) Kühen und b) Kälbern (auf Granulosazellen gereift), Vergrößerung 100x 3.5 Einfrieren ungereifter, gereifter Oozyten und Embryonen für RT-PCR Um anhaftende Kumuluszellen von ungereiften Oozyten der Qualitätsklassen I-III zu entfernen, wurde 0,1 % Hyaluronidase verwendet, die bei -20°C in Aliquots gelagert und unmittelbar vor Gebrauch im Inkubator aufgetaut und erwärmt wurde. KOKs für die RT-PCR Analyse, wurden sofort nach der Punktion gesammelt, in einem 2 ml Eppendorf-Reaktionsgefäß mit Hyaluronidase pipettiert und für 10 Minuten weiter inkubiert. Zur Inaktivierung der Hyaluronidase wurden 2 ml TCM-air zupipettiert. Anschließend wurden die restlichen Kumuluszellen durch wiederholtes Pipettieren mit Hilfe einer Glaskapilare und Mundpipette von den Oozyten entfernt. Die denudierten Oozyten wurden 3x in TCM-air gewaschen und anschließend in PBS/0,1 %PVA 3x gewaschen und einzeln in minimalem PBS/PVA Volumen in 600 µl silikonbeschichteten Eppendorf-Reaktionsgefäßen bei -80°C eingefroren und bis zur RT-PCR Analyse gelagert. Ooyzten wurden 22-24 Stunden nach Beginn der Reifung nach dem gleichen Protokoll eingefroren. Es wurden nur Oozyten eingefroren, bei denen unter dem Mikroskop bei 50 x Vergrößerung ein Polkörper deutlich sichtbar war. 72 Stunden nach der In-vitro-Befruchtung wurden in den entsprechenden Gruppen 8-16 Zeller eingefroren, gleichzeitig wurde die Teilungsrate ermittelt. An 46 Material und Methoden ___________________________________________________________________________ Tag 7 und Tag 8 nach der Befruchtung, wurden expandierte Blastozysten eingefroren und die Blastozystenrate bestimmt. 3.6 Bestimmung der Zellzahlen Bei expandierten Blastozysten von den Tagen 7 und 8 wurden die Zellkerne mit dem Fluoreszenzfarbstoff Bisbenzimid (Hoechst 33342) angefärbt und die Zellzahlen ermittelt. Es wurden 1 µl Farbstoff pro 100 µl PBS (mit 1mg/ml PVA) eingesetzt. Nach 10 Minuten Inkubationszeit in einer Dunkelkammer wurden die blau gefärbten Kerne der Blastozysten (siehe Abbildung 11) unter einem Fluoreszenzmikroskop bei 400 facher Vergrößerung gezählt. Abbildung 11: Expandierte Blastozyste an Tag 8 angefärbt mit Bisbenzimid, 400 x Vergrößerung (Fluoreszenzmikroskop) 3.7 RT-PCR Analyse Ungereifte und gereifte Oozyten, 8-16 Zeller und expandierte Blastozysten aus den verschiedenen Versuchs- und Reifungsgruppen wurden der Reverse Transkriptase Polymerase Kettenreaktion (RT-PCR) Analyse zugeführt, um die mRNA Expressionsmuster der Gene für den GDF-9 und das Hsp.70 bei ungereiften und 47 Material und Methoden ___________________________________________________________________________ gereiften Oozyten zu bestimmen. Der mRNA Gehalt für Glut3 und Hsp.70 wurde bei 8-16 Zellern und expandierten Blastozysten bestimmt. 3.7.1 Isolierung von mRNA aus Oozyten und Embryonen Pro Oozyte bzw. Embryo wurden 40 µl Lysis Puffer in ein Eppendorf-Reaktionsgefäß pipettiert und anschließend 1 µl (1 pg) Kaninchen Globin mRNA hinzugefügt. Die Reaktionsgefäße wurden bei Raumtemperatur für 10 Minuten inkubiert, während dessen wurden 5 µl Dynabeads oligo (dt)25 pro Oozyte/Embryo zweimal mit 20 µl Lysispuffer gewaschen. Der Überstand wurde mit Hilfe eines Magnetständers entfernt. Nach dem zweiten Waschgang wurden den Dynabeads 5 µl Lysispuffer pro Oozyte/Embryo hinzugefügt. Nach 10 Minuten wurden den Reaktionsgefäßen mit den Proben jeweils 5 µl Dynabeads zupipettiert. Die Reaktionsgefäße wurden für weitere 5 Minuten bei 25 °C in einem Thermoshaker geschüttelt. Dabei kam es zum Verbund zwischen Dynabeads und polyA-Schwanz der Oozyten/Embryonen mRNA. Mit Hilfe des Magnetständers wurden die Dynabeads zuerst mit 40 µl Waschpuffer A 1x und 3x mit 40 µl Waschpuffer B gewaschen. Zwischen den Waschschritten wurden die Dynabeads kurz durch Schnippen des Reaktionsgefäßes geschüttelt. Nach dem letzten Waschschritt wurden 11 µl steriles Wasser dazupipettiert. Die mRNA wurde im Biometra PCR-Cycler bei 65 °C in 2,5 Minuten von den Dynabeads getrennt. Die Reaktionsgefäße wurden sofort in den eisgekühlten Magnetständer gesteckt. 3.7.2 Reverse Transkription (RT) Das Umschreiben der mRNA in cDNA wurde in einem Biometra PCR Cycler in einem Endvolumen von 20 µl vorgenommen. Um Fehler beim Pipettieren zu reduzieren, wurden die einzelnen Bestandteile in einen Mastermix (MM) pipettiert. Die Medien wurden aufgetaut und bis zur Verwendung in Eis gelegt. In Tabelle 3 ist die Zusammensetzung des RT-Reaktionsgemisches dargestellt. 48 Material und Methoden ___________________________________________________________________________ Tabelle 3: Zusammensetzung des RT-Reaktionsgemisches Komponente 1x MM Endkonzentration 10x PCR Puffer 2 µl 1x MgCl2 (50mM) 2 µl 5mM dNTP’s (10mM) 2 µl 1mM Hexamer Primer (50 µM 1 µl 2,5 µM Rnase Inhibitor (20U/ µl) 1 µl 20 U Reverse Transkriptase (50U/ µl) 1 µl 20 U Die einzelnen Schritte der reversen Transkription waren wie folgt: - 10 Minuten bei 25°C - 60 Minuten bei 42°C (reverse Transkription der mRNA in cDNA) - 5 Minuten bei 99°C (Denaturierung der Enzyme) - Herunterkühlen auf 4°C Endtemperatur Um eine mögliche Kontamination der Proben zu erkennen, wurde eine Negativkontrolle mit Wasser, ohne mRNA, mit einbezogen. Dazu wurde noch eine Globin Kontrolle mit 1 pg Kaninchen mRNA ohne Präparation, d.h. direkt in die RT Reaktion pipettiert, um die Effizienz der mRNA Wiedergewinnung bestimmen zu können. Während der Optimierung der RT-PCR wurden jeweils mit jedem Primer Paar zwei Negativkontrollen durchgeführt, um zu prüfen, ob die Primer auch an mRNA binden, Dafür wurde 1 pg Kaninchen mRNA zugegeben und statt Rnase Inhibitor und Reverser Transkriptase wurden 2 µl steriles Wasser hinzugefügt, Endvolumen von 20 µl zu erhalten. 49 um ein Material und Methoden ___________________________________________________________________________ 3.7.3 Polymerasekettenreaktion (PCR) Noch während die mRNA umgeschrieben wurde, wurden die Mastermixe (MM) für die zu amplifizierenden Gene in ein 1 ml Eppendorf-Reaktionsgefäß pipettiert. Die PCR wurde in einem Endvolumen von 50 µl durchgeführt. Um eine spezifische Amplifizierung zu gewährleisten, erfolgte eine „Hot Start“ PCR bei 72°C bei der 0,2 µl Taq DNA Polymerase dazu pipettiert wurden. Die Zusammensetzung der MM ist in Tabelle 4. dargestellt. Um eine bessere Effizienz zu erreichen, mussten einige Parameter der PCR angepasst werden. Für das Hsp.70 wurden die Embryonenanteile (EA) von 0,2 EA auf 0,4 EA erhöht. Zyklenzahl und Annealingtemperatur wurden von GUTIERREZ und GUERRIORO (1995) übernommen. Die Zyklenzahl wurde für die PCR von Glut-3 von 34 auf 33 reduziert, da die Banden für die Analyse mit dem Computerprogramm zu intensiv waren. Die Parameter für das GDF-9 konnten bis auf die Zyklenzahl aus der Literatur übernommen werden (HUMBLOT et al. 2005). Sie wurde von 36 auf 34 reduziert. Tabelle 4: Zusammensetzung der Mastermixe (MM) Komponente 1x MM Endkonzentration 5 µl 1x MgCl2: (50mM) 1,5 µl 1,5 mM dNTP’s (10mM) 1 µl 0,2 µM 1,3 bzw. 2,5 µl 0,5 bzw.1 µM *Taq-Polymerase: (5U/µl) 0,2 µl 1U *H2O 15 µl - H2O bis 50 µl - 10x PCR Puffer –MgCl2 Primer upper/lower: (20µM) *Taq DNA Polymerase und Wasser wurden für den Hot Start bei 72°C dazu pipettiert 50 Material und Methoden ___________________________________________________________________________ Tabelle 5: PCR- Bedingungen für die Amplifizierung spezifischer Gentranskripte Gentranskript Hsp.70 GDF-9 Glut-3 Globin Denaturation 95°C 2min 95°C 2min 95°C 2min 95°C 2min Hot Start Mix 72°C 2min 72°C 2min 72°C 2min 72°C 2min Denaturation 95°C 15 sec 95°C 15 sec 95°C 15 sec 95°C 15 sec 36 34 33 27 Denaturation 95°C 15 sec 95°C 15 sec 95°C 15 sec 95°C 15 sec Primer Annealing 59°C 15 sec 56°C 15 sec 58°C 15 sec 60°C 15 sec DNA Extension 72°C 15 sec 72°C 15 sec 72°C 15 sec 72°C 15 sec Letzte Extension 72°C 5 min 72°C 5 min 72°C 5 min 72°C 5 min 8°C 8°C 8°C 8°C Zyklenzahl Endtemperatur 3.7.4 Die Verwendete Primer verwendeten Primersequenzen, Annealingtemperaturen, Fragmentgrößen, Embryonenäquivalente und die dazugehörigen Referenzen sind in Tabelle 6 dargestellt. Die Primerpaare von Hsp.70, Glut-3 und Kaninchen Globin waren schon im Labor von vorherigen RT-PCR Analysen vorhanden. Die Sequenzen für das Primerpaar GDF-9 wurde der Literatur (LONERGAN et al. 1995) entnommen. 51 Material und Methoden ___________________________________________________________________________ Tabelle 6: Primerpaare für PCR, Annealingtemperaturen, Zyklenanzahl, Embryonenanteile, Fragmentgröße der PCR Produkte und Referenzen für Hsp.70, Glut-3, GDF-9 und Globin Annealingtemp./ Zyklenzahl EA* Fragmentgröße Referenz Hsp.70 5’AAGGTGCTGGACAAGTGCCAGGAGGTGATT 3’ACTTGGAAGTAAACAGAAACGGGTGAAAAA 59°C 36 0,4 488bp GUTIERREZ und GUERRIORO (1995) U09861 Glut-3 5’CCTTGGAGGGATGGCTTTTTGTTC 3’CGTGGCTGAGGGGAAGAGCAGTCC 58°C 33 0,1 259bp BENNET (1995) L39214 GDF-9 5’TGCTCAGGCTTTTCACAGGT 3’GGACAGTCACGGTTTTACTT 56°C 34 0,1 581bp LONERGAN et al(2003) AF307092 Globin 5’GCAGCCACGGTGGCGAGTAT 3’GTGGGACAGGAGCTTGAAAT 60°C 27 0,05 257bp CHENG et al (1986) X04751 *Embryonenanteile 52 Material und Methoden Primersequenzen 52 Gene Material und Methode ___________________________________________________________________________ 3.7.5 Analysen der RT-PCR Produkte mit Hilfe der Gelelektrophorese Es wurde ein 2% Agarosegel von 10x15cm Größe angefertigt. Dazu wurden 2g Agarose in 100ml 1x TBE-Puffer (90mMTris, 90mM Borsäure, 2mM EDTA) gelöst und in der Mikrowelle aufgekocht. Nachdem es auf ca. 65°C heruntergekühlt worden war, wurden 2 µl Ethidium-Bromid-Lösung dazupipettiert. Das gut durchmischte, flüssige Gel wurde anschließend sofort in einen Gelträger mit den entsprechenden Probekämmchen gegossen. Nach ca. 45 Minuten bei Raumtemperatur erstarrte das Gel. Die Elektrophorese erfolgte in 1x Tris Puffer. Den RT-PCR Produkten wurde 5 µl Loading Puffer zupipettiert. Anschließend wurden 25 µl jeder Probe in die Taschen pipettiert. Die Spannung wurde nach 5 Minuten von anfangs 100 V auf 80 V herunter reguliert und für weitere 30 Minuten laufengelassen. Die Fragmente wurden mit Hilfe eines UV-Transilliuminators sichtbar gemacht und jedes Gel wurde mit einer CCD Kamera aufgenommen. Die Auswertung des Gels erfolgte mit dem IPLab Spectrum Programm. Der relative Gehalt der mRNA wurde durch Teilung der Intensität der Bande des jeweiligen Entwicklungsstadiums durch die Intensität der entsprechenden Globinbande errechnet. 3.8 Versuchsaufbau Ziel der vorliegenden Arbeit war es, durch Reifung auf Granulosazellkultur von adulten Tieren die Entwicklungskapazität von Oozyten präpuberaler Rinder zu verbessern. Die verwendeten Oozyten wurden mit Hilfe der OPU-Technik von Kälbern gewonnen, die bei Punktionsbeginn 7-8 Monate alt waren. Zur Kontrolle wurden Oozyten von laktierenden Kühen (ab 60 Tage post partum, zyklisch) mit OPU gewonnen. Unter Berücksichtigung von Anzahl und Qualität wurden die KOKs zufällig entweder auf die Granulosazellmonolayer adulter Tiere, Fibroblastenmonolayer oder ohne Kokultur mit somatischen Zellen in TCM 199 mit BSA Zusatz gereift. Die der Kälberoozyten wurden mit der Entwicklungskapazität von Oozyten laktierender Kühe verglichen, die ohne Kokultur gereift wurden. Die Kumulusexpansion, Teilungsraten, Blastozystenraten sowie Zellzahlen in expandierten Blastozysten wurden ermittelt. 53 Material und Methode ___________________________________________________________________________ Mit Hilfe der semi- quantitativen RT-PCR Analyse sollten Unterschiede in Oozyten und Embryonen aus den verschiedenen Reifungsgruppen im relativen Gehalt von Transkripten für drei entwicklungsrelevante Gene (GDF-9, Hsp.70 und GLUT-3) festgestellt werden. Die mRNAs von GDF-9 und Hsp.70 sollten bei unreifen Oozyten und in den verschiedenen Reifungssystemen gereiften Oozyten ermittelt werden. Der relative Gehalt von Hsp.70 und GLUT-3 wurde bei Embryonen im 8-16 Zellstadium und im Blastozystenstadium festgestellt, die aus den unterschiedlichen Reifungsgruppen stammten. Für die Ermittlung des relativen Gehalts von mRNA wurden für die verschiedenen Embryonalstadien der Versuchsgruppen zwischen 6 bis 9 Wiederholungen der RTPCR durchgeführt. 54 Material und Methode ___________________________________________________________________________ Präpuberale Kälber (60 mg FSH im) Laktierende Kühe (100mg FSH im) Ungereifte Oozyten Ungereifte Oozyten In-vitro-Maturation Fibroblasten Monolayer Granulosazell Monolayer In-vitro-Maturation Kontrolle ohne Kokultur Kontrolle ohne Kokultur Beurteilung der Kumulusexpansion Gereifte Oozyten Gereifte Oozyten In-vitro-Fertilisation In-vitro-Fertilisation In-vitro-Kultur in SOF Medium In-vitro-Kultur in SOF Medium nach 72 h p.i. 8-16Zeller an Tag 7 und 8 expandierte Blastozysten Relativer Gehalt von mRNA Hsp.70 und GDF-9 bei ungereiften und gereiften Oozyten Hsp.70 und Glut 3 bei 8-16 Zellern und expandierten Blastozysten (Tag 7u.8) Abbildung 12: Schematische Darstellung des Versuchsaufbaus 55 Material und Methode ___________________________________________________________________________ 3.9 Statistische Auswertung Die statistische Auswertung der Daten erfolgte mit SigmaStat 2.0 (Jandel Scientific, San Rafael, CA, USA). Für die Auswertung der Teilungs- und Blastozystenraten, der Zellzahlen sowie auch der Genexpressionsmuster wurde zunächst die Normalverteilung festgestellt, danach wurde eine One-way ANOVA (StudentNewmans-Keuls-Methode) durchgeführt, um paarweise Vergleiche verschiedenen Reifungsgruppen anzustellen. Unterschiede die p≤0,05 waren wurden als signifikant bewertet. 56 zwischen Ergebnisse ___________________________________________________________________________ 4 ERGEBNISSE 4.1 OPU mit 7- 8 Monate alten Kälbern und laktierenden Kühen Für diese Untersuchung wurden 46 weibliche Kälber und 18 laktierende Kühe 2mal pro Woche, insgesamt 6mal hintereinander, im Zeitraum vom 06.10.2003 bis zum 12.05.2005 punktiert. Vor der eigentlichen Follikelpunktion zur Gewinnung von Oozyten wurden die Tiere gynäkologisch untersucht und der dominante Follikel durch Aspiration entfernt. Ein Kalb schied während der laufenden Punktionsreihe durch Krankheit aus. Die erhaltenen Oozyten von diesem Tier wurden nicht in die Untersuchungen mit einbezogen. Die Ergebnisse der OPU-Sitzungen der Kälber und Kühe werden in den Tabellen 7, 8 und 9 dargestellt. Von den 46 Kälbern reagierten 14 Tiere nicht auf die FSH Applikation. Um mögliche saisonale Einflüsse auf die Ergebnisse zu erfassen, wird die Anzahl punktierter Follikel, erhaltene KOK und der Anteil IVF tauglicher Oozyten bei Kälbern und Kühen in den Monaten April bis September im Vergleich zu den Punktionen von Oktober bis Februar in Tabelle 10 und 11 dargestellt. Um einen möglichen Einfluss des Körpergewichts der Kälber zu Beginn der Punktionen zu erfassen, werden die Punktionsergebnisse von Tieren bis 200 kg Körpergewicht und ab 200kg Körpergewicht, in Bezug auf Anzahl der punktierten Follikel pro Tier, die Anzahl der erhaltenen KOK und die Anzahl der IVF-tauglichen KOK in Tabelle 12 gezeigt. 57 Tabelle 7: Übersicht zu den Ergebnissen der OPU Sitzungen und gewonnenen KOK bei Kälbern taugl.KOK/ Tier/ Sitzung [n] 81 5,1 3,4 68,2 72 4,2 3,0 202 69,4 140 5,6 3,8 270 207 77,5 132 5,8 3,6 209,6 222 155 69,8 105 5,1 3,5 7,3 207,2 195 137 69,9 100 4,6 3,3 6 7,4 191,4 190 152 79,2 120 4,2 3,3 08.11.-25.11.04 6 7,4 168,8 228 203 89,8 111 5,6 3,1 25.04.-12.05.05 4 7,5 211,5 318 277 87,1 178 11,5 7,4 46 7,5 197,8 2017 1558 76,5 1039 5,7 3,8 Kälber [n] Alter* [Monate] Gewicht** [kg] Punktierte Follikel/ Sitzung [n] KOK gesamt [n] Wiederfindungsrate [%] taugl.KOK gesamt [n] 1. KV4 06.10-23.10.03 4 7,8 - 157 122 77,7 2. KV5 10.11.-27.11.03 4 7,2 - 151 103 3. KV6 19.04.-06.05.04 6 7,9 209,7 286 4. KV7 10.05.-01.06.04 6 7,6 186,7 5. KV8 17.06.-05.07.04 5 7,5 6. KV9 12.07.-29.07.04 5 7. KV10 04.10.-21.10.04 8. KV11 9. KV12 58 * Durchschnittsalter der Kälbergruppe bei Punktionsbeginn; **durchschnittliches Gewicht der Kälbergruppe bei Punktionsbeginn Ergebnisse KOK/Tier/ Sitzung [n] OPU Datum OPU Gruppe Tabelle 8: Übersicht zu den Ergebnissen der OPU-Sitzungen und gewonnener KOK bei Kühen Wiederfindungsrate [%] taugl.KOK gesamt [n] KOK/ Tier/ Sitzung [n] taugl.KOK/ Tier/ Sitzung [n] 4,7 2,0 229 152 66,4 104 5,1 3,5 5 5,1 2,6 281 199 70,8 140 6,6 4,6 02.11.-20.11.04 5 4,9 2,2 197 128 65,0 103 4,3 3,4 25.04.-12.05.05 3 4,7 2,3 149 105 70,5 86 5,8 5,8 18 4,9 2,3 856 584 68,2 433 5,5 4,3 Alter [Jahre] LK1 05.02.-23.02.04 5 LK2 16.08.-02.09.04 LK3 LK4 4 • Durchschnittsalter der Kuhgruppe bei Punktionsbeginn; **durchschnittliche Anzahl der Laktationen; die Kühe befanden sich nach der 1. bis 5. Laktation Ergebnisse KOK gesamt [n] OPU Datum OPU Gruppe 59 Laktation** Nr. Punktierte Follikel/ Sitzung [n] Kühe [n] Tabelle 9: Vergleichende Darstellung der Anzahl punktierter Follikel, KOK und IVF tauglicher KOK bei Kälbern und Kühen ( ± SD ) 60 Tiere [n] OPU Follikel Sitzungen gesamt [n] KOK gesamt [n] Follikel Tier/Sitzung [ ± SD ] [n] KOK Tier/Sitzung [ ± SD ] IVF taugliche IVF taugl. KOK gesamt KOK Tier/Sitzung [n] [ ± SD ] Kälber 46 54 2017 7,4 ± 2,3 1558 5,7 ± 2,2 1039 3,8 ± 1,4 Kühe 18 24 856 8,0 ± 1,2 584 5,5 ± 0,9 433 4,3 ± 1,1 Ergebnisse Gruppe Tabelle 10: Anzahl punktierter Follikel, erhaltener KOK und IVF tauglicher Oozyten in den Monaten April bis September im Vergleich zu Punktionen von Oktober bis Februar bei Kälbern ( ± SD ) (Saisonale Auswirkung) OPU Gruppe OPU Datum Tiere [n] IVF taugl.KOK Tier/Sitzung [ ± SD ] IVF taugl. KOK Gesamt [n] KOK Tier/Sitzung [ ± SD ] KOK gesamt [n] Follikel gesamt [n] Follikel Tier/Sitzung [ ± SD ] 06.10-23.10.03 4 157 6,6 122 5,1 81 3,4 2. KV5 10.11.-27.11.03 4 151 6,3 103 4,2 72 3,0 7. KV10 04.10.-21.10.04 6 190 5,2 152 4,2 120 3,3 8. KV11 08.11.-25.11.04 6 228 6,3 203 5,6 111 3,1 20 726 6,1±0,6 580 4,8±0,7 384 3,2±0,2 3. KV6 19.04.-06.05.04 6 286 7,9 202 5,6 140 3,8 4. KV7 10.05.-01.06.04 6 270 7,5 207 5,8 132 3,6 5. KV8 17.06.-05.07.04 5 222 7,4 155 5,1 105 3,5 6. KV9 12.07.-29.07.04 5 195 6,5 137 4,6 100 3,3 9. KV12 25.04.-12.05.05 4 318 13,2 277 11,5 178 7,4 26 1291 8,5±2,7 978 6,5±2,8 655 4,3±1,7 Ergebnisse 61 1. KV4 Tabelle 11: Anzahl punktierter Follikel, erhaltener KOK und IVF tauglicher Oozyten in den Monaten April bis September im Vergleich zu Punktionen von Oktober bis Februar bei Kühen ( ± SD ) (Saisonale Auswirkung) KOK Tier/Sitzung [ ± SD ] KOK Gesamt [n] Follikel Tier/Sitzung IVF taugl.KOK Tier/Sitzung 62 OPU Gruppe OPU Datum Tiere [n] LK1 05.02.-23.02.04 5 229 7,6 152 5,1 104 3,5 LK3 02.11.-20.11.04 5 197 6,6 128 4,3 103 3,4 10 426 7,1±0,7 280 4,7±0,6 27 3,5±0,1 [ ± SD ] [ ± SD ] LK2 16.08.-02.09.04 5 281 9,4 199 6,6 140 4,6 LK4 25.04.-12.05.05 3 149 8,2 105 5,8 86 5,8 8 430 8,8±0,9 304 6,2±0,6 226 5,2±0,9 Ergebnisse IVF taugl. KOK gesamt [n] Follikel gesamt [n] Ergebnisse ___________________________________________________________________________ Tabelle 12: Einfluss des Kälbergewichts auf die Punktionsergebnisse Ausgewertete Parameter Kälber bis 200 kg Kälber ab 200 kg [ ± SD ] [ ± SD ] Follikelanzahl/ Tier 44,3±27,4 45,9±17,3 Anzahl erhaltener KOK/Tier 37,3±30,1 32,5±16,4 Anzahl IVF tauglicher 24,8±18,4 21,7±11,5 KOK/Tier 4.2 IVP mit KOK aus 7- 8 Monate alten Kälbern und Kühen Die Ergebnisse der In-vitro-Produktion von bovinen Embryonen sind in Tabelle 13 dargestellt. Eine Tendenz zur stärkeren Kumulusexpansion zeigten die auf Granulosazellen gereiften Oozyten der Kälber, allerdings waren die Unterschiede zu den anderen untersuchten Gruppen nicht signifikat. Die Teilungsraten wurden 72h nach IVF ermittelt. Die auf Granulosazellen gereiften Kälberoozyten (70,0%, 142/214) und die von adulten Tieren (74,3%, 188/252) hatten eine signifikant höhere (p≤0,05) Teilungsrate als die auf Fibroblasten gereiften Kälberoozyten (53,6%, 99/175) und die Gruppe mit Kälberoozyten ohne Kokultur auf somatischen Zellen (55,2%, 137/244). Die Blastozystenraten waren ebenfalls signifikant höher (p≤0,05) bei auf Granulosazellen gereiften Kälberoozyten und adulten Tieren (22,3%, 43/214 und 22,3%, 53/250) als bei auf Fibroblasten gereiften Kälberoozyten (5,5%, 12/175) und der Kälbergruppe ohne Kokultur (11,7%, 31/244). 4.3 Zellzahlen in expandierten Blastozysten Um den Einfluss der verschiedenen Reifungssysteme auf die Zellzahlen zu untersuchen, wurden die Zellkerne expandierter Blastozysten von Tag 7 oder 8 mit dem Fluoreszenzfarbstoff Bisbenzimid (Hoechst 33342) gefärbt. Die Zellzahlen in expandierten Blastozysten der auf Granulosazellen gereiften Kälberoozyten und die der adulten Tiere unterschieden sich signifikant (p≤0,05) zu expandierten 63 Ergebnisse ___________________________________________________________________________ Blastozysten der Kälberoozyten, die auf Fibroblasten und ohne Kokultur gereift wurden. Die Ergebnisse sind in Tabelle 14 dargestellt. Tabelle 13: Teilungs- und Blastozystenraten bei den unterschiedlichen Reifungsgruppen 72h nach IVF bzw. Tag 7 und Tag 8 Gruppen Teilungsrate [ ± SD ] Blastozystenrate [ ± SD ] Kälber Kontrolle 55,2% ± 23,9b (137/244) 11,7% ± 14,0b (31/244) Kälber Granulosazellen 70,0% ± 27,8a (142/214) 22,3%± 21,9a (43/214) Kälber Fibroblasten 53,6% ± 21,2b (99/175) 5, 5% ± 7,1b (12/175) Kühe Kontrolle 74,3% ± 16,8a (188/252) 22,3% ± 21,1a (53/250) (ANOVA one way, Student-Newman-Keuls-Methode; a:b; p≤0,05; ± S.D.) Tabelle 14: Zellzahlen der expandierten Blastozysten (Tag 7 und Tag 8) Reifungsgruppe Zellzahlen [ ± SD ] 95,0 ± 4,6a (n=4) Kälber F Kälber GZ 114,8 ± 7,9b (n=8) 96,2 ± 4,6a (n=5) Kälber K Kühe 118,7 ± 15,5b (n=20) F: Fibroblasten, GZ: Granulosazellen, K: Kontrolle (Reifung ohne somatische Zellen) (ANOVA one way, Student-Newman-Keuls-Methode; a:b; p≤0,05; ± S.D.) 64 Ergebnisse ___________________________________________________________________________ 4.4 Messenger RNA-Expression bei ungereiften und gereiften Oozyten von Kälbern und Kühen Generell war nach Reifung ein signifikanter Abfall in der Expression von GDF-9 mRNA bei Kälberoozyten festzustellen (p≤0,05). Gereifte Oozyten von Kühen zeigten eine signifikant höhere Expression von GDF-9 mRNA als gereifte Oozyten von Kälbern und werden in Abbildung 13 gezeigt. Die Hsp.70 mRNA war nach Reifung, im Vergleich zu allen Reifungsgruppen, ebenfalls signifikant erniedrigt. Der relative Transkriptgehalt der Oozyten verschiedener Reifungsgruppen ist in Abbildung 14 dargestellt. 4.5 Messenger RNA-Expression bei 8-16 Zellern und expandierten Blastozysten von Kälbern und Kühen Bei Embryonen im 8-16 Zellstadium von Kälbern und Kühen waren keine signifikanten Unterschiede in der mRNA-Expression von Hsp.70 festzustellen. Blastozysten von adulten Oozyten hatten einen signifikant höheren relativen Transkriptgehalt als Blastozysten von präpuberalen Oozyten ohne Kokultur. Gegenüber anderen Reifungsgruppen waren keine signifikanten Unterschiede festzustellen (siehe Abbildung 15). Die Umrechnung des relativen Transkriptgehaltes auf die Zellzahl der expandierten Blastozysten bestätigt den signifikanten Unterschied in der Expression von Hsp.70 bei expandierten Blastozysten aus präpuberalen und adulten Oozyten (siehe Abbildung 16). Glut-3 wurde von 8-16 Zellern aller Reifungsgruppen und auch von den Tag 7 und Tag 8 Blastozysten ähnlich hoch exprimiert. Der relative Transkriptgehalt war bei expandierten Blastozysten aus der Granulosazellreifung am höchsten, ohne jedoch statistische Signifikanz zu erreichen (siehe Abbildung 17). 65 Ergebnisse ___________________________________________________________________________ a) GDF-9 b) rel. Transkriptgehalt 5,0 a a 4,0 a 3,0 b b 2,0 b 1,0 Kalb Kuh Kalb F Kalb GZ Kalb K Kuh 0,0 ungereifte Oozyten greifte Oozyten Abbildung 13: a) Repräsentativer gelektrophoretischer Nachweis der semi-quantitativen RT- PCR Analyse der GDF-9 Expression und b) relativer Transkriptgehalt von GDF-9 mRNA in ungereiften und gereiften Oozyten von Kälbern und Kühen Abkürzungen: Kalb: Oozyten von 7-8 Monate alten Kälbern, Kuh: Oozyten von laktierenden Kühen, F: Fibroblasten, GZ: Granulosazellen, K: Kontrolle (ohne Kokultur) (ANOVA one way, Student-Newman-Keuls-Methode; a:b; p≤0,05; ± S.E.M.) 66 Ergebnisse ___________________________________________________________________________ a) Hsp.70 b) 1,4 a a rel. Transkriptgehalt 1,2 1,0 b b 0,8 0,6 b b 0,4 Kalb Kuh Kalb F Kalb GZ Kalb K Kuh 0,2 0,0 ungereifte Oozyten gereifte Oozyten Abbildung 14: a) Repräsentativer gelektrophoretischer Nachweis der semi-quantitativen RT-PCR Analyse der Hsp.70 Expression und b) relativer Transkriptgehalt von Hsp.70 mRNA in ungereiften und gereiften Oozyten von Kälbern Kühen Abkürzungen: Kalb: Oozyten von 7-8 Monate alten Kälbern, Kuh: Oozyten von laktierenden Kühen, F: Fibroblasten, Granulosazellen, K: Kontrolle (ohne Kokultur) (ANOVA one way, Student-Newman-Keuls-Methode; a:b; p≤0,05; ± S.E.M.) 67 GZ: Ergebnisse ___________________________________________________________________________ a) Hsp.70 b) a rel. Transkriptgehalt 2,0 a a 1,5 a ab Kalb GZ ab Kalb K a b 1,0 Kalb F Kuh 0,5 0,0 8-16 Zeller exp.Blastozysten Abbildung 15: a) Repräsentativer gelektrophoretischer Nachweis der semi-quantitativen RT-PCR Analyse der Hsp.70 Expression und b) relativer Transkriptgehalt von Hsp.70 mRNA in 8-16 Zellern und expandierten Blastozysten (Tag 7 und Tag 8) von Kälbern und Kühen Abkürzungen: exp. Blastozysten: expandierte Blastozysten, Kalb: 8-16 Zeller/exp. Blastozysten von 7-8 Monate alten Kälbern, Kuh: 8-16 Zeller/exp. Blastozysten von laktierenden Kühen, F: Fibroblasten, GZ: Granulosazellen, K: Kontrolle (ohne Kokultur) (ANOVA one way, Student-Newman-Keuls-Methode; a:b; p≤0,05; ± S.E.M.) 68 Ergebnisse ___________________________________________________________________________ Hsp.70 rel.Transkriptgeh./ Zelle 1,6 ab a 1,4 ab 1,2 b 1,0 Kalb F 0,8 Kalb GZ 0,6 Kalb K 0,4 Kuh 0,2 0,0 expandierte Blastozyten Abbildung 16: Relativer Transkriptgehalt von Hsp.70 mRNA pro Zelle in expandierten Blastozysten an Tag 7 und Tag 8 Abkürzungen: Kalb: expandierte Blastozysten von 7-8 Monate alten Kälbern, Kuh: expandierte Blastozysten von laktierenden Kühen, F: Fibroblasten, GZ: Granulosazellen, K: Kontrolle (ohne Kokultur) (ANOVA one way, Student-Newman-Keuls-Methode; a:b; p≤0,05; ± S.E.M.) 69 Ergebnisse ___________________________________________________________________________ a) rel. Transkriptgehalt b) Glut3 4,5 4,0 3,5 3,0 2,5 2,0 1,5 1,0 0,5 0,0 a a a a a a a Kalb F Kalb GZ Kalb K a Kuh 8-16 Zeller exp. Blastozysten Abbildung 17: a) Repräsentativer gelektrophoretischer Nachweis der semi-quantitativen RT-RCR Analyse der Glut-3 Expression und b) relativer Transkriptgehalt von Glut-3 mRNA in 8-16 Zellern und expandierten Blastozysten (Tag 7 und Tag 8) von Kälbern und Kühen Abkürzungen: exp. Blastozysten: expandierte Blastozysten, Kalb: 816 Zeller/exp. Blastozysten von 7-8 Monate alte Kälbern, Kuh: 8-16 Zeller/exp. Blastozysten von laktierenden Kühen, F: Fibroblasten, GZ: Granulosazellen, K: Kontrolle (ohne Kokultur)(ANOVA one way, Student-Newman-Keuls-Methode; a:b; p≤0,05; ± S.E.M.) 70 Diskussion 5 Die DISKUSSION Verwendung von Kälbern in Zuchtprogrammen zur Verkürzung des Generationsintervalls erfordert eine verbesserte Entwicklungskapazität präpuberaler Kälberoozyten, insbesondere die Verbesserung der zytoplasmatischen Reifung. In der Vergangenheit wurden bereits mehrere Versuche unternommen, Anzahl und Qualität der erhaltenen Oozyten sowie die der Blastozysten aus in vitro Programmen präpuberaler Kälberoozyten zu erhöhen. Jedoch ist die Entwicklungskompetenz juveniler boviner Oozyten im Vergleich zu der von erwachsenen Tieren immer noch niedriger. Durch i.m. Applikation von FSH, eCG, sowie deren Kombinationen konnten die Anzahl der Follikel und erhaltener KOKs gesteigert werden (PRESICCE et al. 1997; KUWER et al. 1999; GALLI et al. 2001). Durch intraovarielle Injektion von FSH oder IGF-I konnte die Anzahl IVP- tauglicher KOKs und Embryonen von präpuberalen Kälbern deutlich verbessert werden (WIEKING 2001; OROPEZA 2004). Auch durch Modifikationen bewährter Kulturmedien in der In-vitro-Produktion konnten höhere Entwicklungsraten erzielt werden. Durch Zusätze von FSH, Cystein, Cystamin ins Reifungsmedium konnte die Entwicklungsfähigkeit juveniler Kälberoozyten gesteigert werden (PALMA et al. 2001; DONNAY et al. 2004). Kokulturen mit bovinen Granulosazellen erhöhten die Entwicklungskompetenz von Oozyten 3 Monate alter Kälber (REVEL et al. 1995). In der vorliegenden Arbeit sollte durch In-vitro-Reifung juveniler boviner Oozyten auf Granulosazellmonolayern von adulten Tieren die Entwicklungskapazität verbessert werden. Es sollte ferner geklärt werden, ob durch Reifung auf den beiden Monolayern die mRNA-Expression von drei entwicklungsrelevanten Genen beeinflusst wurde, die in der frühen Follikel- und Embryonalentwicklung eine wichtige Rolle spielen und als mögliche Markergene für das Entwicklungspotential dienen könnten. Von 46 punktierten Kälbern im Alter zwischen 7-8 Monaten bei Punktionsbeginn, reagierten 14 Tiere nicht auf die FSH Applikation. FRY et al. (1998) und OROPEZA 71 Diskussion et al. (2004) berichteten ebenfalls, dass ca. 30% der präpuberalen Kälber nicht auf FSH-Applikation ansprachen. Insgesamt wurden bei dieser Untersuchung pro Tier und Punktionssitzung, gleich viele IVP-taugliche KOKs von laktierenden Kühen und Kälbern gewonnen. Auch die Anzahl der punktierten Follikel war ebenfalls ähnlich (siehe Tabelle 9). Dies steht zum Teil im Gegensatz zu den Feststellungen von OROPEZA (2004), der von Kühen mehr IVP-taugliche KOKs gewann als von präpuberalen Kälbern. Um eventuelle jahreszeitliche und damit auch fütterungsbedingte Einflüsse auf die Punktionsergebnisse auszuschließen, wurden die Punktionen über alle Jahreszeiten hinweg vorgenommen. Im Gegensatz zu den Feststellungen von BROUSSARD et al. (1996), die eine signifikante Steigerung in der erhaltenen Oozytenzahlen während der Monate Februar bis März feststellten, war die Anzahl der erhaltenen IVPtauglichen KOK pro Tier und Sitzung in der vorliegenden Arbeit, bei Kühen und Kälbern in den Monaten April bis September leicht erhöht (siehe Tabelle 10 u. 11). Diese Ergebnisse der vorliegenden Arbeit sind statistisch nicht abzusichern, da keine Signifikanzen aufgetreten sind und es sich somit vermutlich um Zufallsbefunde handelt. Auf Grund ihrer vielfältigen physiologischen Funktionen in der Oozytenreifung liegt es nahe, Granulosazellen in die In-vitro-Produktion einzubeziehen. Granulosazellen adulter bzw. mit FSH behandelter juveniler Ziegen wirkten sich positiv auf die Reifung juveniler Ziegenoozyten aus (MOGAS et al. 1997). ). FUKUI und ONO (1989) verwendeten für die Reifung von Ooyzten adulter Tiere verschiedene Protokolle: Fetales Kälberserum (FCS) oder oestrisches Kuhserum (ECS) mit oder ohne Zusatz von Hormonen (FSH, LH und Oestradiol) und mit oder ohne Kokultur auf Granulosazellen. In den Versuchsgruppen nach Kokultur auf Granulosazellen wurden höhere Blastozystenraten erreicht (11,0%, 16,5%, 6,9%, 16,3%) als nach IVP ohne Kokultur (1,3%, 1,7%, 4,3%, 0,9%). Auf Oozyten 3 Monate alter, mit FSH stimulierter Kälber wirkte sich die Reifung auf Granulosazellmonolayern im Vergleich zu Oozyten unbehandelter Kälber ebenfalls positiv aus (REVEL et al. 1995). 72 Diskussion In der vorliegenden Arbeit wurden für die Reifung präpuberaler boviner Oozyten Granulosazellen adulter Tiere verwendet. Um für die gesamte Versuchsreihe möglichst standardisierte Reifungsbedingungen zu erhalten, wurde stets die gleiche Charge Granulosazellen zur Herstellung der Monolayer verwendet. Die Teilungsraten von auf Granulosazellen gereiften Kälberoozyten waren mit 70,0% nahezu identisch mit der Teilungsrate der Oozyten von Kühen (74,3%). REVEL et al. (1995) reiften Oozyten von 3 Monate alten Kälbern auf Granulosazellmonolayern mit 10% FCS im Medium und erhielten ähnliche Ergebnisse. In früheren Untersuchungen in der gleichen Arbeitsgruppe konnte die Teilungsrate von Oozyten präpuberaler Kälber im Alter zwischen 6-7 Monaten durch Applikation von rbST oder IGF-I im Vergleich zu Oozyten von adulten Kühen nicht wesentlich erhöht werden (PALMA et al 1993; LOONEY et al. 1995; PRESICCE et al. 1997; STEEVES et al. 1999; OROPEZA 2004). In den eigenen Untersuchungen erreichten juvenile Oozyten, die auf Fibroblastenmonolayern (53,6%) oder ohne Kokultur (55,2%) gereift wurden, ähnliche Teilungsraten, wie bereits von PRESICCE et al. (1997), TANEJA et al. (2000) und OROPEZA (2004) berichtet wurden (49%, 41%, 37- 42%). Ebenso weicht die durchschnittliche Teilungsraten von Embryonen aus Kühen (74,3%) nicht von vergleichbaren (73,3%, 79%, 76,0% und 72-80%) Untersuchungen ab (LOONEY et al. 1995; REVEL et al. 1995; PRESICCE et al. 1997; OROPEZA 2004). Die in der vorliegenden Arbeit erzielten Blastozystenraten mit Kälberoozyten, die auf Granulosazellen gereift wurden, waren mit 22,3 % gleich hoch wie die mit Oozyten aus laktierenden Kühen. Dagegen erreichten die auf Fibroblastenmonolayern gereiften präpuberalen Kälberoozyten nur eine Blastozystenrate von 5,5%. Bei laktierenden Kühen (25%) und bei Kälbern ähnlichen Alters (28%) nach intraovariellen Injektion von IGF-I erreichten OROPEZA et al. (2004) etwas höhere Blastozystenraten als in den vorliegenden Resultaten ausgewiesen. Präpuberale Oozyten, die ohne Kokultur gereift wurden, ergeben mit 11,7% eine vergleichbar geringe Blastozystenrate wie von OROPEZA et al. (2004) beschrieben. Andere Untersuchungen berichteten von ähnlichen Blastozystenraten (7,1% und 11,7%) mit Oozyten stimulierter (eCG und FSH) Kälber (LOONEY et al. 1995). Nicht stimulierte, 7 Monate alte Kälber erreichten im Vergleich zu stimulierten eine deutlich niedrigere 73 Diskussion Blastozystenrate (1% und 17%) (PRESICCE et al.1997). REVEL et al. (1995) berichtete, dass die Teilungsraten der Embryonen von unstimulierten und stimulierten Kälbern (81% und 73%) und Kühen (85%), die zuvor auf bovinen Granulosazellmonolayern gereift worden waren ähnlich waren. Die Blastozystenraten waren deutlich niedriger (11% und 9%) als von adulten Tieren (21%-27%). Vorhergehende Untersuchungen haben gezeigt, dass Oozyten präpuberaler Kälber eine mangelhafte zytoplasmatische Reifung durchlaufen und darum in ihrer Entwicklungsfähigkeit eingeschränkt sind (DAMIANI et al. 1996; STEEVES und GARDNER 1999; SALAMONE et al. 2001). Es gibt aber auch Anhaltspunkte für eine unzureichende Kernreifung präpuberaler boviner Oozyten (DAMIANI et al. 1996). Untersuchungen von DONNAY et al. (2004) scheinen diese Hypothese zu bestätigen. Durch Zusatz von FF-MAS in das Reifungsmedium konnte ein positiver Effekt auf die Kernreifung bei Oozyten von 6-8 Monate alten Kälbern erreicht werden, in dem der Anteil der Oozyten, die die Metaphase II erreichten, erhöht wurde. Auf die weitere Entwicklungsfähigkeit hatte FF-MAS jedoch keinen Einfluss. Eine Stimulierung der GSH-Synthese durch Zusatz von Cystein und Cystamin ins Reifungsmedium präpuberaler Oozyten verbesserte die zytoplasmatische Reifung und führte zu Blastozystenraten von 38% (DONNAY et al. 2004). In der vorliegenden Arbeit unterscheiden sich die Kernzahlen expandierter Tag 7 und Tag 8 Blastozysten von Kälbern und Kühen innerhalb der Reifungsgruppen signifikant untereinander. Expandierte Blastozysten der auf Granulosazellen gereiften Kälberoozyten besaßen ähnliche Zellzahlen wie expandierte Blastozysten von Kühen und waren im Vergleich zu den anderen Reifungsgruppen signifikant höher (siehe Tabelle 14). Das steht teilweise im Gegensatz zu den Ergebnissen von KHATIR et al. (1998), STEEVES et al. (1999) und OROPEZA (2004), die keine deutlichen Unterschiede in den Zellzahlen expandierter Blastozysten von Kälbern und Kühen feststellen konnten. Mit Hilfe der Transkriptionsgehalte semi-quantitativen dreier RT-PCR verschiedener können Gene in relative Oozyten mRNAbzw. präimplantatorischen Embryonen dargestellt werden. Allerdings können nicht die 74 Diskussion absoluten Gehalte der jeweiligen mRNAs verglichen werden, da die Effizienz von Primern in den Zyklen nicht bekannt ist (HO et al. 1995; McPHERSON und MØLLER 2000). In der vorliegenden Arbeit wurden relative Transkriptgehalte einzelner ungereifter Oozyten, unterschiedlich kultivierter Embryonen im 8-16 Zellstadium sowie expandierten Blastozysten an den Tagen 7 und 8 von präpuberalen Kälbern und laktierenden Kühen, untersucht und miteinander verglichen. In früheren Untersuchungen wurde der höchste Transkriptgehalt von GDF-9 in ungereiften adulten bovinen Oozyten festgestellt. Nach der Reifung kam es zu einem signifikanten Abfall in der Expression von GDF-9 (LONERGAN et al. 2003). Diese Feststellungen stimmen mit den eigenen Resultaten überein. Es wurde ein signifikanter Abfall in der mRNA-Expression von GDF-9 nach der Reifung bei juvenilen und adulten Oozyten beobachtet. Die Transkriptgehalte von GDF-9 bei ungereiften präpuberalen und adulten Oozyten war gleich hoch. Vermutlich laufen physiologische Prozesse wie Differenzierung und Proliferation der Granulosazellen sowie die Follikelentwicklung, an denen GDF-9 beteiligt ist, bei Kälbern auf ähnlich hohem Niveau ab wie bei Kühen. Nach der Reifung wurde eine signifikant höhere Expression von GDF-9 bei adulten Oozyten als bei präpuberalen festgestellt. Allerdings wiesen die auf Granulosazellen gereiften Oozyten einen höheren Transkriptgehalt auf als die ohne Kokultur beziehungsweise auf Fibroblasten gereiften Oozyten, wobei die letzteren den niedrigsten relativen mRNA-Gehalt aufwiesen. Demnach scheinen adulte Granulosazellen einen positiven Einfluss auf die Expression von GDF-9 bei bovinen Oozyten zu haben. Die auf Granulosazellen gereiften Oozyten präpuberaler bzw. erwachsener Rinder zeigten tendenziell eine stärkere Kumulusexpansion als Oozyten der anderen Gruppen. Eine durch GDF-9 verbesserte Expansion der Kumuluszellen, damit eine erfolgreiche Befruchtung und nachfolgend eine bessere Entwicklungsfähigkeit könnten möglicherweise die signifikant höheren Entwicklungsraten in dieser Reifungsgruppe erklären. Interessant ist, dass LONERGAN et al. (2003) bei in vivo gereiften Oozyten den niedrigsten Transkriptgehalt feststellten. Sie erklären diese Beobachtung mit der Vermutung, dass die Mechanismen, die den Übergang vom 75 Diskussion maternalen zum embryonalen Genom regulieren, bei in vitro gereiften Embryonen verändert sind. HUMBLOT et al. (2005) stellten eine Erhöhung der Expression von GDF-9 bereits 12h nach Prostaglandin F2α (PGF2α)-Applikation fest, was vermutlich mit einer Beeinflussung der Granulosazellen kurz vor der Ovulation zusammenhängt. In der vorliegenden Arbeit war die mRNA Expression von Hsp.70 bei ungereiften Oozyten adulter Kühe höher als bei ungereiften Oozyten präpuberaler Rinder. Sie fiel nach der Reifung in allen Reifungsgruppen signifikant ab. Von einem ähnlichen Ergebnis berichteten auch WRENZYCKI et al. (1999) bei Oozyten adulter Rinder. HUMBLOT et al. (2005) berichteten, das die Expression von Hsp.70 bei in vivo gereiften Oozyten adulter Rinder am niedrigsten war. In der vorliegenden Arbeit wiesen Embryonen im 8-16 Zellstadium in den verschiedenen Versuchgruppen keine signifikanten Unterschiede in der Hsp.70 Expression auf (siehe Abbildung 15), während expandierte Blastozysten von Kühen eine signifikant höhere Expression von Hsp.70 zeigten als Blastozysten aus Kälberoozyten, die ohne Kokultur inkubiert wurden. Dieses Ergebnis stützt die Feststellungen von EDWARDS und HANSEN (1996), dass in Anwesenheit von Kumuluszellen während der Reifung die Proteinsynthese der Oozyten erhöhte, während ihre Abwesenheit die Proteinsynthese verringerte und die Embryonen empfindlicher gegenüber Temperaturerhöhungen wurden, weil auch weniger Hsp. 70 synthetisiert wurde (EDWARDS und HANSEN 1997). Heat shock Proteine haben in eukaryontischen Zellen wichtige Funktionen bei der Faltung von Proteinen im endoplasmatischen Retikulum und stabilisieren die Proteine im Falle von schädlichen Einflüssen. Im 8-16 Zellstadium wird das bovine embryonale Genom aktiviert (KOPECNY et al. 1989; VIUFF et al. 1996, MEMILI et al. 1998, MEMILI und FIRST 1999, 2000), und es beginnt eine starke Zunahme der Transkriptionsaktivität. WRENZYCKI et al. (1999) stellten eine Zunahme im relativen Hsp.70 Gehalt bei 8-16 Zellern und expandierten Blastozysten fest, die in Medien mit Serumzusatz kultiviert wurden und einen niedrigen Gehalt in Medien mit PVA- Zusatz. Die Blastozystenraten waren bei Blastozysten mit Serumzusatz signifikant höher. Möglicherweise versuchen die Embryonen mit der erhöhten Hsp.70 mRNA- 76 Diskussion Expression auf ein suboptimales Kulturmedium zu reagieren. In Embryonen nach Kerntransfer änderte sich der Gehalt von Hsp.70 Transkripten in Abhängigkeit vom Kerntransferprotokoll (WRENZYCKI et al. 2001b). Bei in vivo gewonnenen expandierten Blastozysten war der relative Transkriptgehalt an Hsp.70 am niedrigsten (WRENZYCKI et al. 1998; KNIJN et al. 2002), was die These einer Reaktion auf suboptimale Umweltbedingungen stützt. Der Glukoseverbrauch des bovinen Embryos steigt ab dem 8-16 Zellstadium kontinuierlich an (KHURANA und NIEMANN 2000). Geschlüpfte Blastozysten aus Kühen wiesen einen höheren Transkriptgehalt von Glut-1 auf als unreife und gereifte Oozyten, Zygoten und Embryonen bis zum 8-16 Zellstadium adulter Tiere (WRENZYCKI et al. 1998; WRENZYCKI et al. 1999; AUGUSTIN et al. 2001). In der vorliegenden Arbeit wurde ebenfalls ein Anstieg im relativen Transkriptgehalt von Glut-3 vom 8-16 Zellstadium zum Blastozystenstadium festgestellt, aber keine signifikanten Unterschiede zwischen den adulten und präpuberalen 8-16 Zellstadien (siehe Abbildung 17). Die mRNA- Expression von Glut-1 war bei präpuberalen 8-16 Zellstadien niedriger als bei adulten (OROPEZA et al. 2004). STEEVES et al. (1999) stellten keinen Unterschied in der Aufnahme von Glukose zwischen adulten und präpuberalen 8-16 Zellstadien fest. Bei murinen expandierten Blastozysten ist Glut-3 zusammen mit Glut-1 an der Aufnahme von Glukose aus der Umgebung beteiligt. Glut-3 ist apikal an den Zellen des Trophektoderms lokalisiert und ist für den direkten Transport aus dem Medium in die Zellen verantwortlich. Glut-1 ist auch bei bovinen expandierten Blastozysten basolateral lokalisiert und leitet die Glukose in das Blastozoel weiter. (PANTALEON et al. 1997; PANTALEON und KAYE 1998; AUGUSTIN et al. 2001) Die Ergebnisse der vorliegenden Arbeit stützen die These, dass präpuberale und adulte bovine expandierte Blastozysten eine ähnliche Glukoseversorgung besitzen. In der vorliegenden Arbeit wurden weder signifikante Unterschiede in der Expression von Glut-3 zwischen juvenilen und adulten expandierten Blastozysten noch zwischen den verschiedenen Reifungsgruppen festgestellt (siehe Abbildung 17). In der Arbeit von OROPEZA (2004) wurden in expandierten Blastozysten aus Oozyten von Kälbern und Kühen keine signifikanten 77 Unterschiede im relativen Diskussion Transkriptionsgehalt der Gene Glut-1, eIF1A und UBF gefunden. Betrachtet man diese Ergebnisse gemeinsam, so deuten sie darauf hin, dass präpuberale bovine Embryonen wenn sie die Entwicklung bis zum Blastozystenstadium erreicht haben, sie sich im Hinblick auf die relativen Transkriptgehalte der bisher untersuchten Gene nicht von denen adulter Tiere unterscheiden. Die vorliegende Arbeit zeigt einen positiven Einfluss von Granulosazellen adulter Tiere auf die Reifung und auf die embryologische Entwicklung von Oozyten 7-8 Monate alter Kälber. Sie zeigt ferner, dass positive Effekte auch auf mRNA- Ebene zu finden sind. Die erhöhten relativen Transkriptgehalte von GDF-9 und Glut-3 im Zusammenhang mit den signifikant höheren Teilungsraten, Blastozystenraten und Kernzahlen lassen einen direkten positiven Einfluss der adulten Granulosazellen auf die Entwicklungskapazität vermuten. Die erzielten Ergebnisse scheinen die Hypothese zu bestätigen, dass der verminderten Entwicklungskompetenz präpuberaler Kälberooyzten eine mangelhafte zytoplasmatische Reifung zu Grunde liegt, die auch mit eine verringerten Expression von GDF-9 und Glut-3 verbunden ist. Als zweite Arbeit, nach OROPEZA (2004), in der präpuberale bovine Blastozysten auf mRNA- Ebene untersucht wurden, bestätigen die Ergebnisse auch, dass bovine Embryonen aus präpuberalen Oozyten nach dem Umschalten auf das embryonale Genom nur noch wenig Unterschiede im relativen Transkriptgehalt einiger entwicklungsrelevanter Gene zu Embryonen adulter Tiere aufweisen. Allerdings ist dies vor dem Hintergrund der begrenzten Anzahl analysierter Gene zu sehen. Neue Erkenntnisse würden sich möglicher weise durch die Analyse des gesamten Transkriptoms präpuberaler und adulter Oozyten und Embryonen ergeben. Es bedarf noch weiterer Forschung auf diesem Gebiet, um weitere Faktoren und Zusammenhänge zu definieren die an der Steigerung der Entwicklungskapazität präpuberaler Kälberoozyten beteiligt sind. Die relativ einfache Herstellung und Anwendung von Granulosazellmonolayern könnte in der praktischen Anwendung zu besseren Ergebnissen in der Einbindung von Kälbern in Zuchtprogrammen beitragen. 78 Zusammenfassung 6 ZUSAMMENFASSUNG Simona Ponebšek Experimentelle Untersuchungen zur Verbesserung der Entwicklungsfähigkeit boviner Oozyten präpuberaler Spender durch In-vitro-Reifung auf Granulosazellmonolayern adulter Tiere Oozyten präpuberaler Kälber weisen im Vergleich zu Oozyten von Kühen, eine niedrigere Entwicklungskompetenz im Hinblick auf Teilungs- und Blastozystenrate, auf. Ursachen dafür werden vor allem in der mangelhaften zytoplasmatischen Reifung der Kälberoozyten vermutet. Ziel dieser Arbeit war, durch Reifung boviner Oozyten juveniler Spender auf Granulosazellmonolayern von adulten Tieren die Entwicklungskapazität der Oozyten zu verbessern. Im Rahmen dieser Arbeit wurden 46 Kälber im Alter zwischen 7-8 Monaten zweimal wöchentlich in sechs auf einander folgenden Ovum-pick-up (OPU)-Sitzungen punktiert. Basierend auf den Ergebnissen vorausgegangener Untersuchungen wurde den Kälbern 48 Stunden vor jeder OPU-Sitzung 60 mg FSH i.m. appliziert. Oozyten von 18 laktierenden Kühen (100mg FSH, i.m.) dienten als Kontrolle und wurden ohne Kokultur gereift. Für die Gewinnung von Granulosazellen adulter Spender wurden Rinderovarien mit Gelbkörpern aus einem kommerziellen Schlachthof verwendet. Die Zellen wurden gewaschen und in Kulturschalen ausgesät. Nach 5 Tagen wiesen sie ein 70-80% konfluentes Wachstum auf und konnten aliquotiert werden. Die Aliquots wurden bei 80°C eingefroren. Für die gesamte Versuchsreihe wurden Aliquots einer Charge (Granulosazellen eines Gewinnungstages) verwendet. IVF-taugliche Oozyten von Kälbern, der morphologischen Klassifizierung Klasse I-III, wurden 24 Stunden auf Granulosazell- oder Fibroblastenmonolayern in einem Standardmedium (TCM199 substituiert mit BSA, hCG und eCG) gereift und die Kumulusexpansion wurde beurteilt, bevor sie in Fert-Talp (substituiert mit Heparin, 79 Zusammenfassung Hypotaurin, Epinephrin und BSA) in vitro fertilisiert wurden. Dazu wurde Tiefgefriersperma eines Bullen verwendet, dessen IVF-Tauglichkeit nachgewiesen war. Nach 18-20 Stunden wurden die Zygoten mechanisch mit einer Mundpipette von den noch anhaftenden Kumuluszellen befreit und anschließend in SOF mit BSAZusatz für 7-8 Tage kultiviert. Es wurde die Gesamtzahl IVF-tauglicher Oozyten sowie die Teilungs- und Blastozystenraten erfasst, und mit denen adulter Tiere verglichen. Der mögliche Einfluss der verschiedenen Reifungsmethoden auf die mRNAExpression von drei entwicklungsrelevanten Genen, GDF-9, Hsp.70 und Glut-3, wurden mit Hilfe eines semi-quantitativen RT-PCR Assays bei einzelnen ungereiften und gereiften Oozyten (GDF-9 und Hsp.70) sowie frühen Teilungsstadien (8-16 Zellern) und expandierten Blastozysten (Hsp.70 und Glut-3) von Kälbern und Kühen, erfasst. Folgende Ergebnisse wurden erzielt: 1. Bei Kälbern und Kühen wurden ähnliche Punktionsergebnisse im Hinblick auf die Anzahl punktierter Follikel, gewonnener KOKs und IVF- tauglicher KOKs pro Tier erzielt. Jahreszeitliche Unterschiede in den Punktionsergebnissen waren nicht festzustellen. Das Gewicht der Tiere zu Beginn der Punktion hatte keinen Einfluss auf die Punktionsergebnisse. 2. Es wurden signifikant höhere (p≤0,05) Teilungsraten bei den auf Granulosazellen gereiften Kälberoozyten (70,0%) und den Eizellen von adulten Tieren (74,3%) erzielt als bei den auf Fibroblasten gereiften Kälberoozyten (53,6%) und der Gruppe von Kälberoozyten ohne Kokultur (55,2%). 3. Die Blastozystenraten bei den auf Granulosazellen gereiften Kälberoozyten und den von adulten Tieren (22,3% und 22,3%) waren signifikant höher (p≤0,05) als für die auf Fibroblasten (5,5%) und die ohne Kokultur gereiften (11,7%) Kälberoozyten. 4. Die Zellzahlen expandierter Blastozysten der auf Granulosazellen gereiften Kälberoozyten (114,8 ± 7,9) und die von adulten Tieren (118,7 ± 15,5) unterschieden sich signifikant (p≤0,05) von expandierten Blastozysten aus 80 Zusammenfassung Kälberooyzten der Gruppe ohne Kokultur (96,2 ± 4,6) und den aus auf Fibroblasten (95,0 ± 4,6) gereiften Kälberoozyten. 5. Nach der Reifung war ein signifikanter Abfall im relativen Transkriptgehalt von Hsp.70 in allen Reifungsgruppen festzustellen. Expandierte Blastozysten von Kühen wiesen signifikant (p≤ 0,05) höhere relative Transkriptmengen pro Zelle auf als expandierte Blastozysten von Kälbern, die ohne Kokultur inkubiert wurden. 6. GDF-9 zeigte bei allen Versuchsgruppen nach der Eizellreifung einen signifikanten Abfall in der Expression. Gereifte Oozyten von Kühen wiesen eine signifikant höhere (p≤ 0,05) Expression von GDF-9 als greifte Oozyten der Kälber. 7. Frühe Teilungsstadien (8-16 Zeller) und expandierte Blastozysten zeigten in allen untersuchten Gruppen ähnliche relative Transkriptgehalte für Glut-3 mRNA. Die Ergebnisse zeigen, dass die Reifung von Oozyten präpuberaler Kälber auf Granulosazellen adulter Tiere die Entwicklungskompetenz deutlich verbessert. Sie bestätigen aber auch, dass bovine Embryonen präpuberaler Tiere im Vergleich zu Embryonen von adulten Tieren nach dem Umschalten auf das embryonale Genom nur noch wenige Unterschiede im relativen Transkriptgehalt einiger entwicklungsrelevanter Gene aufweisen. In zukünftigen Forschungsarbeiten sind weitere Faktoren zu identifizieren, mit denen die Entwicklungsfähigkeit boviner Oozyten präpuberaler Spender weiter erhöht und charakterisiert werden kann. 81 Summary 7 SUMMARY Simona Ponebšek Improvement of the developmental competence of prepubertal bovine oocytes by invitro maturation on a granulosa cell monolayer from adult animals Oocytes from prepubertal calves show decreased developmental capacity with regard to cleavage and blastocysts rate compared with oocytes from adult animals. It is likely that this is due to incomplete cytoplasmatic maturation. The goal of the present study was to improve the developmental competence of juvenile oocytes by maturing them on granulosa cell (GC) monolayers from adult animals. Therefore numbers of suitable oocytes for IVP, cleavage and blastocysts rates were determined and compared with oocytes from adult animals. For this study 46 Holstein Frisian calves at 7-8 months of age underwent OPU twice per week in six consecutive OPU-sessions. Based on previous experiments the calves received an i.m. injection of 60 mg FSH 48 hours prior to each OPU-session. Oocytes obtained from 18 lactating cows (100 mg FSH-P, i.m.) served as controls and were matured without co-culture. Granulosa cells for the monolayers were isolated from the follicles of bovine ovaries obtained from a commercial abattoir. The cells were washed and sewed in culture dishes. After five days they grew to a 70-80% confluent monolayer and could be aliquoted. The aliquots were frozen at -80°C. For the whole experiment aliquots from one charge were used. IVP suitable calf oocytes of morphological classes I-III were matured for 24 hours on either GC, fibroblasts or without co-culture in a standard medium (TCM199 with BSA supplement and hCG and eCG) before they were fertilised in Fert-Talp with heparin, hypotaurine and epinephrine. Fertilisation was carried out using frozen-thawed semen from one IVF tested bull. After 20-24 hours presumptive zygotes were mechanically denuded using a mouth pipette and cultured in SOF medium supplemented with BSA for 7-8 days. 82 Summary A possible influence of the different maturation methods on the mRNA expression of three developmental important genes, growth differentiation factor-9 (GDF-9), heat shock protein 70 (Hsp.70) and glucose transporter 3 (Glut-3) was investigated by semi quantitative RT-PCR assays . Single immature and mature oocytes (GDF-9 and Hsp.70), 8-16 cell embryos and expanded blastocysts of day 7 and day 8 (Hsp.70 and Glut-3) were investigated. The following results are obtained: 1. Similar results were obtained from calves and cows with regard to numbers of punctured follicles, numbers of obtained COCs and suitable COCs per animal. Seasonal differences were not found. The bodyweight of the calves at the beginning of the session had no influence on the results obtained. 2. The cleavage rate was significantly higher (P≤ 0.05) in oocytes derived from cows and calves matured on GC (74.3% and 70.0%, respectively) than in oocytes derived from the group without co-culture and the fibroblast groups (55.2% and 53.6%, respectively). 3. Blastocyst rates were similar in oocytes derived from cows and calves matured on GC (22.3% and 22.3%, respectively) but significantly higher (P≤ 0.05) than the group without co-culture and the fibroblast groups (11.7% and 5.5%, respectively). 4. Cell numbers of expanded blastocysts derived from calf oocytes matured on GC and from adult cows were significantly higher than in the group matured without co-culture and the fibroblast group (114.8 ± 7.9 and 118.7 ± 15.5 vs. 96.2 ± 4.6 and 95.0 ± 4.6, respectively). 5. After maturation, a significant (P≤ 0.05) decrease in Hsp.70 expression was observed. Expanded blastocysts derived from adult oocytes expressed Hsp.70 significantly more than blastocysts derived from oocytes of the control calves. 6. After maturation, a significant decrease in GDF-9 expression was observed in calf oocytes. Matured cow oocytes showed a significantly higher mRNA abundance of GDF-9 than matured calf oocytes 83 Summary 7. The relative abundance of Glut-3 was similar in 8-16 cell embryos and expanded blastocysts in all groups. The overall mRNA expression patterns for Hsp.70 and Glut-3 in blastocysts from GC matured oocytes were similar to that of cow blastocysts. These results indicate that the maturation of juvenile calf oocytes on granulosa cells from adult animals improves their developmental competence and that bovine embryos from prepubertal oocytes, after they switch to the embryonic genome, do show only a few differences in relative abundance for some developmental important genes. These findings provide clues towards identification of factors critically involved in acquiring full developmental capacity at puberty. 84 Literaturverzeichnis ___________________________________________________________________________ 8 LITERATURVERZEICHNIS AALTONEN, J., M. P. LAITINEN, K. VUOJOLAINEN, R. JAATINEN, N. HORELLIKUITUNEN, L. SEPPÄ, H. LOUHIO, T. TUURI, J. SJÖBERG, R. BÜTZOW, O. HOVATTA, L. DALE u. O. RITVOS (1999): Human growth differentiation factor 9 (GDF-9) and its novel homolog GDF-9B are expressed in oocyte during early folliculogenesis. JCE&M 84, 2744-2750 ABRIEU, A. M. DOREE u. D. FISHER (2001): The interplay between cyclin-B-Cdc2 kinase (MPF) and MAPK during maturation of oocytes. J.Cell Sci. 114, 257-267 ADAMS, G. P., R. L. MATTERI, J. P. KASTELIC, J. C. KO u. O. J. GINTHER (1992): Association between surges of follicle- stimulating hormone and the emergence of follicular waves in heifers. J. Reprod. Fertil. 94, 177-188 ADAMS, G. P., A. C. O. EVANS u. N. C. RAWLINGS (1994): Follicular waves and circulating gonadotrophins in 8-month-old prepubertal heifers. J. Reprod. Fertil. 100, 27-33 ADAMS, G. P. (1999): Comparative patterns of follicle development and selection in ruminants. J. Reprod. Fertil. Suppl. 54, 17-32 ALBERTS, B., D. BRAY, J. LEWIS, M. RALF, K. ROBERTS u. J.D. WATSON (1994a): Der Zell-Teilungszyklus Aus: Molekulare Biologie der Zelle VHC, Verlagsgesellschaft mbH, Weinheim, Deutschland, S. 1019-1076 ALBERTS, B., D. BRAY, J. LEWIS, M. RALF, K. ROBERTS u. J.D. WATSON (1994b): Genetische Grundmechanismen Aus: Molekulare Biologie der Zelle VHC, Verlagsgesellschaft mbH, Weinheim, Deutschland, S. 259-339 ALBERTS, B., D. BRAY, J. LEWIS, M. RALF, K. ROBERTS u. J.D. WATSON (1994c): Molekulare Genetik, Protein-Funktion Aus: Molekulare Biologie der Zelle VHC, Verlagsgesellschaft mbH, Weinheim, Deutschland, S. 247-248 85 Literaturverzeichnis ___________________________________________________________________________ ANAS, M.-K. I., A. SHOJO, M. SHIMADA u. T. TERADA (2000): Effects of wortmannin on the kinetics of GVBD and the activities of the maturationpromoting factor and mitogen-activated protein kinase during bovine oocyte maturation in vitro. Theriogenology 53, 1797-1806 ARMSTRONG, D. T., B. J. IRVINE, C. R EARL, D. MCLEAN u. R. F. SEAMARK (1994): Gonadotropin stimulation regimens for follicular aspiration and in vitro embryo production from calf oocytes. Theriogenology 42, 1227-1236 ASA, C. S., K. L. BAUMAN, E. W. HOUSTON, M. T. FISCHER, R. E. JUNGE, R. L. KRISHER (1998): Transvaginal oocyte retrieval and in vitro maturation, fertilization and embryo culture in addax (Addax nasomaculatus). Theriogenology 49, 261 abstr. AUGUSTIN, R., P. POCAR, A. NAVARETTE-SANTOS, C. WRENZYCKI, F. GANDOLFI, H. NIEMANN u. B. FISCHER (2001): Glucose transporter expression is developmentally regulated in in vitro derived bovine preimplantation embryos. Mol. Reprod. Dev. 60, 370-376 BAGE, R., S. PETYIM, B. LARSSON, T. HALLAP, A. S. BERGQVIST, H. GUSTAFSSON u. H. RODRIGUEZ-MARTINEZ (2003): Oocyte competence in repeat breeder heifers: effects of an optimized ovum pick-up schedule on expression of oestrus, follicular development and fertility. Reprod. Fertil. Dev. 15, 115-123 BAKER, T. G. u. L. L. FRANCHI (1967): The fine structure of chromosomes in bovine primordial oocytes. J. Reprod. Fertil. 14, 511-513 BAO, B., H. A. GARVERICK, G. W. SMITH, M. F. SMITH, B. E. SALFEN u. R. S. YOUNGQUIST (1997): Changes in messenger ribonucleic acid encoding leuteinizing hormone receptor, cytochrome P450-side chain cleavage, and aromatase are associated with recruitment and selection of bovine ovarian follicles. Biol. Reprod.56, 1158-1168 BAO, B. u. H. A. GAVERICK (1998): Expression of steroidogenic enzyme and gonadotropin receptor genes in bovine follicles during ovarian follicular waves: a review. J Am Sci 76, 1903-1921 86 Literaturverzeichnis ___________________________________________________________________________ BENNETT, B. L., C. G. PROSSER u. M. R. GRIGOR (1995): Isolation of cDNAs and tissue specific expression of ovine glucose transporters. Biochem Mol Biol Int 37, 9-16 BERGFELT, D. R., L. J. KULICK, K. KOT u. O.J. GINTHER (2000): Follicular and hormonal response to experimental suppression of FSH during follicle deviation in cattle. Theriogenology 54, 1191-1206 BETTS, D. H. u. W. A. KING (2001): Genetic regulation of embryo death and senescence. Theriogenology 55, 171-191 BIRD, A. P. u. A. P. WOLFFE (1999): Methylation - induced repression: belts, braces and chromatin. Cell 99, 451-454 BODENSTEINER, K. J., C. M. CLAY, C. L. MOELLER u. H. R. SAWYER (1999): Molecular cloning of the ovine growth/differentiation factor-9 gene and expression of growth/differentiation factor-9 in ovine and bovine ovaries. Biol. Reprod. 60, 381-386 BOLS, P. E. J., J. M. M. VANDENHEEDE, A. VAN SOOM u. A. DE KRUIF (1995): Transvaginal ovum pick-up (OPU) in the cow: a new disposable needle guidance system. Theriogenology 49, 983-995 BONI, R., S. ROVIELLO u. L. ZICARELLI (1996): Repeated ovum pick-up in Italian Mediterranean buffalo cows. Theriogenology 46, 899-909 BRAW-TAL, R. u. S. YOSSEFI (1997): Studies in vivo and in vitro on the initiation of follicle growth in the bovine ovary. J. Reprod. Fertil. 109, 165-171 BREVINI, T. A., P. LONERGAN, F. CILLO, C. FRANCISCI, L.A. FAVETTA, T. FAIR u. F. GANDOLFI (2002): Evolution of mRNA polyadenylation between oocyte maturation and first embryonic cleavage in cattle and its relation with developmental competence. Mol. Reprod. Dev. 63, 510-517 BREVINI-GANDOLFI, T. A., L. A. FAVETTA, L. MAURI, A. M. LUCIANO, F. CILLO u. F. GANDOLFI (1999): Changes in poly(A) tail length of maternal transcripts during in vitro maturation of bovine oocytes and their relation with developmental competence. Mol. Reprod. Dev. 52, 427-433 87 Literaturverzeichnis ___________________________________________________________________________ BROGLIATTI, G. M., A. T. PALAZ, H. RODRIGUEZ-MARTINEZ, R. J. MAPLETOFT u. G. P. ADAMS (2000): Transvaginal collection and ultrastructure of llama (Lama glama) oocytes. Theriogenology 54, 1269-1279 BROUSSARD, J. R., A. ROCHA, J. M. LIM, R. M. BLAIR, J. D. ROUSSEL u. W. HANSEL (1996): The effect of environmental temperature and humidity on the quality and developmental competence of bovine oocytes obtained by transvaginal ultrasoundguided aspiration. Theriogenology 45, 351 abstr. BRÜCK, I., B. SYNNESTVEDT u. T. GREVE (1997): Repeated transvaginal oocyte aspiration in unstimulated and FSH-treated mares. Theriogenology 47, 1157-1167 BUNGARTZ, L. u. H. NIEMANN (1994): Assessment of the presence of a dominant follicle and selection of dairy cows suitable for superovulation by a single ultrasound examination. J. Reprod. Fertil. 101, 583-591 BUNGARTZ, L., A. LUCAS-HAHN, D. RATH u. H. NIEMANN (1995): Collection of oocytes from cattle via follicular aspiration aided by ultrasound with or without gonadotropin pretreatment and in different reproductive stages. Theriogenology 43, 667-675 BYSKOV, A. G., C. Y. ANDERSEN, L. NORDHOLM, H. THOGERSEN, G. XIA, O. WASSMANN, J. V. ANDERSEN, E. GUDDAL u. T. ROED (1995): Chemical structure of sterols that activate occyte meiosis. Nature 374 (6522), 559-562 CAMOUS, S., Y. HEYMAN, W. MEZIOU u. Y. MENEZO (1984): Claevage beyond the block stage and survival after transfer of early bovine embryos cultured with trophoblastic vesicles. J. Reprod. Fertil. 72, 479-485 CARABATSOS, M. J., J. ELVIN, M. M. MATZUK u. D. F. ALBERTINI (1998): Characterisation of oocyte and follicle development in growth differentiation factor-9deficient mice. Dev. Biol. 204, 373-384 CAVILLA, J. L., C. R. KENNEDY, M. BATESEN, L. D. KLENTZERIS, A. G. BYSKOV u. G. M. HARTSHORNE (2001): The effects of meiosis activating sterol on in-vitro maturation and fertilisation of human oocytes from stimulated and unstimulated ovaries. Hum. Reprod. 16, 547-555 88 Literaturverzeichnis ___________________________________________________________________________ CHANG, H., C. W. BROWN u. M. M. MATZUK (2002): Genetic analysis of the mammalian transforming growth factor-β super family. Endocrine Reviews 23 (6), 787-823 CHASTANT- MAILLARD, S., H. QUINTON, J. LAUFFENBURGER, N. CORDONNIER-LEFORT, C. RICHARD, J. MARSHAL, P. MORMEDE u. J. P. RENARD (2003): Consequences of transvaginal puncture on well-being in cows. Reprod. 125, 555-563 CHEN, L., P. T. RUSSELL u. W. J. LARSEN (1993): Functional significance of cumulus expansion in the mouse: roles for the preovulatory synthesis of hyaluronic acid within the cumulus mass. Mol. Reprod. Dev. 34, 87-93 CHENG, J. F., L. RAID u. R. C. HARDISON (1986): Isolation and nucleotide sequence of the rabbit globin gene cluster psi zeta-alpha 1psi alpha. Absence of a pair of alpha-globin genes evolving in concert. J. Biol. Chem. 261, 839-848 CHOHAN, K. R. u. A. G. HUNTER (2004): In vitro maturation, fertilisation and early cleavage rates of bovine fetal oocytes. Theriogenology 61, 373-380 CRICK, F. H. C (1966): The genetic code: III Sci. Am. 215, 55-62 DAMIANI, P., R. A. FISSORE, J. B. CIBELLI, C. R. LONG, J. J. BALISE, J. M. ROBL u. R. T. DUBY (1996): Evaluation of developmental competence, nuclear and ooplasmic maturation of calf oocytes. Mol. Reprod. Dev. 45, 521-534 DAY, M. L, K. IMAKAWA, P. L. WOLFE, R. J. KITTOK u. J. E. KINDER (1987): Endocrine mechanisms of puberty in heifers. Role of hypothalamo- pituitary estradiol receptors in the negative feedback of estradiol on luteinizing hormone secretion. Biol. Reprod. 37, 1054-1065 DE LOOS, F., C. VAN VLIET, P. VAN MAURIK u. Th. A. M. KRUIP (1989): Morphology of immature bovine oocytes. Gamete Res. 24, 197-204 89 Literaturverzeichnis ___________________________________________________________________________ DE MATOS, D. G. u. C. C. FURNUS (2000): The importance of having high glutathione (GSH) level after bovine in vitro maturation on embryo development: effect of beta-mercaptoethanol, cysteine and cystine. Theriogenology 60, 943-952 DE PAZ, P., A. J. SANCHEZ, J. DE LA FUENTE, C. A. CHAMORRO, M. ALVAREZ, E. ANEL u. L. ANEL (2001): Ultrastructural and cytochemical comparison between calf and cow oocyte. Theriogenology 55, 1107-1116 DIELEMAN, S. J., P. J. HENDRIKSEN, D. VIUFF, P. D. THOMSEN, P. HYTTEL, H. M. KNJIN, C. WRENZYCKI, T. A. KRUIP, H. NIEMANN, B. M. GADELLA, M. M. BEVERS u. P. L. VOS (2002): Effects of in vivo prematuration and in vivo final maturation on developmental capacity and quality of pre-implantation embryos. Theriogenology 57, 5-20 DONG, J., D. F. ALBERTINI, K. NISHIMORI, T. R. KUMAR, N. LU u. M. M. MATZUK (1996): Growth differentiation factor-9 is required during early ovarian folliculogenesis. Nature 383, 531-535 DONNAY, I., I. FAERGE, C. GRØNDAHL, B. VERHAEGHE, H. SAYOUD, N. PONDERATO, C. GALLI u. G. LAZZARI (2004): Effect of prematuration, meiosis activating sterol and enriched maturation medium on the nuclear maturation and competence to development of calf oocytes. Theriogenology 62, 1093-1107 DRIANCOURT, M. A. (2001): Regulation of ovarian follicular dynamics in farm animals. Implications for manipulation of reproduction. Theriogenology 55, 1211-1239 DRIANCOURT, M. A., K. REYNAUD u. J. SMITZ (2001): Differences in follicular function of 3- month-old calves and mature cows. Reproduction 121, 463-474 DUBY, R. T., P. DAMIANI, C. R. LOONEY, R. A. FISSORE u. J. M. ROBL (1996): Prepubertal calves as oocyte donors: Promises and problems. Theriogenology 45, 121-130 EALY, A. D., M. DROST u. P. J. HANSEN (1993): Developmental changes in embryonic resistance to adverse effects of maternal heat stress in cows. J. Dairy. Sci. 76, 2899-2905 90 Literaturverzeichnis ___________________________________________________________________________ EBLING, F. J. P. (2005): The neuroendocrine timing of puberty. Reproduction 129, 675-683 EDWARDS, J. L. u. P. J. HANSEN (1996): Elevated temperature increases heat shock protein 70 synthesis in bovine two-cell embryos and compromises function of maturing oocytes. Biol. Reprod. 55, 340-346 EDWARDS, J. L. u. P. J. HANSEN (1997): Differential responses of bovine oocytes and preimplantation embryos to heat shock. Mol. Reprod. Dev. 46, 138-145 EICKELMANN, E. (1999): Experimentelle Untersuchungen zur wiederholten ultraschallgeleiteten transvaginalen Follikelpunktion bei trächtigen Rindern und Kühen. Hannover, Tierärztl. Hochschule. Diss. EL-FOULY, M. A., B. COOK, M. NEKOLA u. A. V. NALBANDOV (1970): Role of the ovum in follicular luteinization. Endocrinoloy 87, 288-293 ELVIN, J. A., A. T. CLARK, P. WANG, N. M. WOLFMAN u. M. M. MATZUK (1999a): Paracrine actions of growth differentiation factor-9 in the mammalian ovary. Mol. Endo. 13, (6) 1035- 1048 ELVIN, J. A., C. YANG, P. WANG, K. NISHIMORI u. M. M. MATZUK (1999b): Molecular characterisation of the follicle defects in the growth differentiation factor-9deficient ovary. Mol. Endo. 13, (6) 1018-1033 ELVIN, J. A., C. YAN u. M. M. MATZUK (2000): Growth differentiation factor-9 stimulates progesterone synthesis in granulosa cells via prostaglandin E2/EP2 receptor pathway. Proc. Natl. Acad. Sci. 97, 10288-10293 ENGELHARDT v. W. und G. BREVES (2000): Endokrinologie. Reproduktion beim Säugetier. Aus: Physiologie der Haustiere Enke im Hippokrates Verlag GmbH, Stuttgart 2000, S. 528 EPPIG J. J. (2001) Oocyte control of ovarian follicular development and function in mammals. Reproduction 122, 829-838 91 Literaturverzeichnis ___________________________________________________________________________ EPPIG, J. J., K. WIGGELSWORTH, F. PENDOLA u. Y. HIRAO (1997): Murine oocytes suppress expression of luteinizing hormone receptor messenger ribonucleic acid by granulosa cells. Biol. Reprod. 56, 976-984 ERICKSON, B. H. (1966a) Development and radio- response of the prenatal bovine ovary. J. Anim. Sci.10, 97-105 ERICKSON, B. H. (1966b) Development and senescence of the postnatal bovine ovary. J. Anim. Sci.25, 800-805 EVANS, A. C. O., G. P. ADAMS u. N. C. RAWLINGS (1994): Follicular and hormonal development in prepubertal heifers from 2 to 36 weeks of age. J. Reprod. Fertil. 102, 463-470 EVANS, A. C. O., C. M. KOMAR, S. A. WANDJI u. J. E. FORTUNE (1997): Changes in androgen secretion and luteinizing hormone pulse amplitude are associated with the recruitment and growth of ovarian follicles during the luteal phase of the bovine estrus cycle. Biol. Reprod. 57, 394-401 EYESTONE, W. u. N. L. FIRST (1991): Characterisation of developmental arrest in early bovine embryos cultured in vitro. Theriogenology 35, 613-624 FAIR, T, P. HYTTEL u. T. GREVE (1995): Bovine oocyte diameter in relation to maturational competence and transcriptional activity. Mol. Reprod. Dev. 42, 437-442 FAIR, T, P. HYTTEL, T. GREVE u. M.BOLAND (1996): Nucleus structure and transcriptional activity in relation to oocyte diameter in cattle. Mol. Reprod. Dev. 43, 503-512 FAIR, T, S. C. J. HULSHOF, P. HYTTEL, T. GREVE u. M. BOLAND (1997): Oocyte ultrastructure in bovine primordial to early tertiary follicle. Anat. Embryol. 195, 327-336 FAIR, T (2003) Follicular oocyte growth and aquisiton of developmental competence. Anim. Reprod. Sci. 78, 203-216 92 Literaturverzeichnis ___________________________________________________________________________ FAN, H. Y. u. Q. Y. SUN (2004): Involvement of Mitogen activated promoting kinase cascade during oocyte maturation and fertilisation in mammals. Biol. Reprod. 70, 535-547 FISSORE, R. A., C. L HE u. G.F. VANDE WOUDE (1996): Potential role of mitogen-activated protein kinase during meiosis resumption in bovine oocytes. Biol. Reprod. 55, 1261-1270 FITZPATRICK, S. L., D. M. SIDONI, P. J. SHUGHRUE, M. V. LANE, I. J. MERCHENTHALER u. D. E. FRAIL (1998): Expression of growth differentiation factor-9 messenger ribonucleic acid in ovarian and nonovarian rodent and human tissues. Endo. 139 (5), 2571-2578 FREI, R. E., G. A. SCHULTZ u. R. B. CHURCH (1989): Qualitative and quantitative changes in protein synthesis occur at the 8-16-cell stage of embryogenesis in the cow. J. Reprod. Fertil. 86, 637-641 FRIEDMAN, D. I., M. J. IMPERIALE u. S. L. ADHYA (1987): RNA 3’ end protection in the control of gene expression. Annu.Rev. Genet. 21, 453-488 FRY, R. C., T. L. SIMPSON u. T. J. SQUIRES (1998): Ultrasonically guided transvaginal oocyte recovery from calves treated with or without GnRH. Theriogenology 49, 1077-1082 FUKUI, Y., u. H. ONO (1989): Effects of sera, hormones and granulosa cells added to culture medium for in-vitro maturation, fertilisation, cleavage and development of bovine oocytes. J. Reprod. Fertil. 86, 501-506 GALLI C, G. CROTTI, C. NOTARI, P. TURINI, R. DUCHI u. G. LAZZARI (2001): Embryo production by ovum pick-up from live donors. Theriogenology 55, 1341-1357 GANDOLFI, F., E. MILANESI, P. POCAR, A. M. LUCIANO, T. A. BREVINI, F. ACOCELLA, A. LAURIA u. D. T. ARMSTRONG (1998): Comparative analysis of calf and cow oocytes during in vitro maturation. Mol. Reprod. Dev. 49, 168-175 93 Literaturverzeichnis ___________________________________________________________________________ GANDOLFI; T. A. L., u. F. GANDOLFI (2001): The maternal legacy to the embryo: cytoplasmatic components and their effects on early development. Theriogenology 55, 1255-1276 GEBAUER, G. D. u. J. D. RICHTER (1997): Synthesis and function of Mos: the control switch of vertebrate oocyte meiosis. Bioessays 19 (1), 23-28 GELDERMANN, H. (2005): Struktur und Funktion von Genen. In: Tier-Biotechnologie Eugen Ulmer Verlag, Stuttgart, S. 63-88 GINTHER, O. J., M. C. WILTBANK, P. M. FRICKE, J. R. GIBBONS u. K. KOT (1996): Selection of the dominant follicle in cattle. Biol. Reprod. 55, 1187-1194 GINTHER, O. J., K. KOT, L. J. KULICK, u. M. C. WILTBANK (1997): Emergence and deviation of follicles during the development of follicular waves in cattle. Theriogenology 48, 75-87 GINTHER, O. J., M. A. BEG, D. R. BERGFELT, M. A. BEG, F. X. DONADEU u. K. KOT (2001): Follicle selection in monovular species. Biol. Reprod. 65, 638-647 GORDO, A. C., C. L. HE, S. SMITH u. R. A. FISSORE (2001): Mitogen activated protein kinase plays a significant role in metaphase II arrest, spindle morphology and maintenance of maturation promoting factor activity in bovine oocytes. Mol. Reprod. Dev. 59, 106-114 GRAFF, K. J., M. MEINTJES, V. W. DYER, J. B. PAUL, R. S. DENNISTON, C. ZIOMEK u. R. A. GODKE (1999): Transvaginal ultrasound-guided oocyte retrieval following FSH stimulation of domestic goats. Theriogenology 51, 1099-1119 GRØNDAHL, C., J. L. OTTESEN, M LESSEL, P. FAARUP, A. MURRAY, F. C. GRØNVALD, C. HEGELE- HARTUNG u. I. AHNFELT-RØNNE (1998): Meiosis-activating sterol promotes resumption of meiosis in mouse oocytes cultured in contrast to related oxysterols. Biol. Reprod. 58, 1297-1302 94 Literaturverzeichnis ___________________________________________________________________________ GRØNDAHL, C., T. H. HANSEN u. K. MARKY-NEILSON (2000): Human oocyte maturation in vitro is stimulated by meiosis activating sterol (FF-MAS). Hum. Reprod. 15 (Suppl.5) 3-15 GUTIERREZ, J. A. u. V. Jr. GUERRIORO (1995): Chemical modifications of a recombinant bovine stress- inducible 70 kDa heat-shock protein (Hsp 70) mimics Hsp 70 isoforms from tissues. Biochem J 305, 197-203 HO, Y. K. WIGGELSWORTH u J. J. EPPIG (1995): Preimplantation development of mouse embryos in KSMO: augmentation by amino acids and analysis of gene expression. Mol. Reprod. Dev. 41, 232-238 HUMBLOT, P., P. HOLM, P. LONERGAN, C. WRENZYCKI, A.-S. LEQUARRE, C. GUYADER JOLY, D. HERRMANN, A. LOPEZ, D. RIZOS, H. NIEMANN u. H. CALLESEN (2005): Effect of stage of follicular growth during superovulation on developmental competence of bovine oocytes. Theriogenology 63, 1149-1166 HYTTEL, P., K. P. XU, S. SMITH u. T. GREVE (1986): Ultrasturcutre of in-vitro oocyte maturation in cattle. J. Reprod. Fertil. 78, 615-625 HYTTEL, P., T. GREVE u. H. CALLESEN (1988): Ultrastructure of in-vivo fertilisation in cattle. J. Reprod. Fertil. 82, 1-13 HYTTEL, P. T. FAIR, H. CALLESEN u. T. GREVE (1997): Oocyte growth, capacitation and final maturation in cattle. Theriogenology 47, 23-32 HYTTEL, P., J. LAURINCIK, D. VIUFF, T. FAIR, V. ZAKHARTCHENKO, C. ROSENKRANZ, B. AVERY, D. RATH, H. NIEMANN, P. D. THOMSEN, K: SCHELLANDER, H. CALLESEN, E. WOLF, R. L. OCHS u. T. GREEVE (2001): Activation of ribosomal RNA genes in preimplantation cattle and swine embryos Anim. Reprod. Sci. 60-61, 49-60 IKEDA, K. u. Y. TAKAHASHI (2003): Comparison of maturational and developmental parameters of oocytes recovered form prepubertal and adult pigs. Reprod. Fertil. Dev. 15, 215-221 95 Literaturverzeichnis ___________________________________________________________________________ IZQUIERDO, D., P. VILLAMEDIANA, M. LOPEZ-BEJAR u. M. T. PARAMINO (2002): Effect of in vitro and in vivo culture on embryo development from prepubertal goat IVM-IVF oocytes. Theriogenology 57, 1431-1441 JAATINEN, R., M. P. LAITINEN, K. VUOJOLAINEN , J. AALTONEN, H. LOUHIO, K. HEIKINHEIMO, E. LEHTONEN u. O. RITVOS (1999): Localization of growth differentiation factor- 9 (GDF-9) mRNA and protein in rat ovaries and cDNA cloning of rat GDF-9 and its novel homolog GDF-9B. Mol. Cell Endocrinol. 156 (1-2), 189-193 JOOST, H. G., G. I. BELL, J. D. BEST, M. J. BIRNBAUM, M. J. CHARRON, Y. T. CHEN, H. DOEGE, D. E. JAMES, H. F. LODISH, K. H. MOLEY, J. F. MOLEY, M. MUECKLER, S. ROGERS, A. SCHÜRMANN, S. SEINO u. THORENS (2002): Nomenclature of the GLUT/SLC2A family of sugar/polyol transport facilitators. Am. J. Physiol. Endocrinol. Metab. 282, E974-E976 KHATIR, H., C. CAROLAN, P. LONERGAN u. P. MERMILLOD (1997): Characterization of calf follicular fluid and its ability to support cytoplasmic maturation of cow and calf oocytes. J. Reprod. Fertil. 111, 267-275 KHATIR, H., P. LONERGAN, J. L. TOUZE u. P. MERMILLOD (1998): The characterisation of bovine embryos obtained from prepubertal calf oocytes and their viability after non surgical embryo transfer. Theriogenology 50, 1201-1210. KHURANA, N. K. u. H. NIEMANN (2000): Energy metabolism in preimplantation bovine embryos derived in vitro and in vivo. Biol. Reprod. 62, 847-856 KIESSLING, S. (2000): Ambulante Follikelpunktion beim Rind- eine Feldstudie. München, Univ., Tierärztl. Fak., Diss. KITIYANANT, Y., C. TROCHARUS, M. AREEKIJSEREE, u. K. PAVASUTHIPAISIT (1995): Swamp buffalo oocytes from transvaginal ultrasound-guided aspiration fertilized in vitro with bovine oviductal epithelian cells. Theriogenology 47, 250, abstr. KLOSSOK, G. (1997): Tierspezifische Einflussfaktoren auf das Ergebnis der transvaginalen ultraschalgeleiteten Follikelpunktion bei adulten Tieren. Hannover, Tierärztl. Hochsch.,Diss. 96 Literaturverzeichnis ___________________________________________________________________________ KNIGHT, P. G, C. GLISTER (2001): Potential local regulatory functions of inhibins, actvins and follistatin in the ovary. Reproduction 121, 503-512 KNIGHT, P. G, C. GLISTER (2003): Local roles of TGF-β superfamily members in the control of ovarian follicle development. Anim. Reprod. Sci. 78, 165-183 KNIEP, G. H. M. (2001): Gewinnung entwicklungskompetenter Oozyten durch ultraschallgeleitete Follikelpunktion bei Kühen im postpartalen Zeitraum und Auswirkungen für die weitere Fruchtbarkeit. Hannover, Tierärztl. Hochschule. Diss. KNIJN, H. M., C. WRENZYCKI, P. J. M. HENDRIKSEN, P. L. A. M. VOS, D. HERRMANN, G. C. VAN DER WEIJDEN, H. NIEMANN u. S. J. DIELEMAN (2002): Effects of maturation regimen on the relative abundance of gene transcripts in bovine blastocysts derived in vitro and in vivo. Reprod. 124, 365-375 KOPECNY, V., J. E. FLECHON, S. CAMOUS u. J. FULKA JR. (1989): Nucleologenesis and the onset of transcription in the eight- cell bovine embryo: finestructural autoradiographic study. Mol. Reprod. Dev. 1, 79-90 KRUIP, T. A., D. G. CRAN, T. H. VAN BENEDEN u. S. J. DIELEMAN (1983): Structural changes in bovine oocytes during final maturation in vivo. Gamete Res. 8, 29-47 KRUIP, T. A., R. BONI, M. W. M. ROELOFSEN, Y. A. WURTH u. M. C. PIETERSE (1993): Application of OPU for embryo production and breeding in cattle. Theriogenology 39, 251 KRUIP, A. T., R. BONI, Y. A. WURTH, M. W. M. ROELOFSEN u. M. C. PIETERSE (1994): Potential use of ovum pick-up for embryo production and breeding in cattle. Theriogenology 42, 675- 684 KRUIP, TH. A. M. u. J. H. G. DEN DAAS (1997) In vitro produced and cloned embryos: Effects on pregnancy, parturition and offspring. Theriogenology 47, 43-52 97 Literaturverzeichnis ___________________________________________________________________________ KUBELKA, M. , J. MOTLIK, R. M. SCHULTZ u. A. PAVLOK (2000): Butyrolactone I reversibly inhibits meiotic maturation of bovine oocytes, without influencing chromosome condensation activity. Biol. Reprod. 62, 292-302 KUWER, A. (1997): Gewinnung entwicklungskompetenter Oozyten bei hormonell stimulierten präpuberalen Rindern durch ultraschallgeleitete transvaginale Follikelpunktion. Hannover, Tierärztl. Hochschule. Diss. LAITINEN, M., K. VUOJOLAINEN, R. JAATINEN, I. KETOLA, J. AALTONEN, E. LEHTONEN, M. HEIKINHEIMO u. O. RITVOS (1998): A novel growth differentiation factor- 9 (GDF-9) related factor is co-expressed with GDF-9 in mouse oocytes during folliculogenesis. Mech. Dev. 78 (1-2), 135-140 LAM, X., C. GIESEKE, M. KNOLL u. P. TALBOT (2000): Assay and importance of adhesive interaction between hamster (Mesocricetus auratus) oocyte- cumulus complexes and the oviductal epithelium. Biol. Reprod. 62, 579-588 LAZZARI, G., C. WRENZYCKI, D. HERRMANN, R. DUCHI, T. KRUIP, H. NIEMANN u. C. GALLI (2002): Cellular and molecular deviations in bovine in vitro-produced embryos are related to the large offspring syndrome. Biol. Reprod. 67, 767-775 LI, R., R. J. NORMAN, D. T. ARMSTRONG u. R. B. GILCHRIST (2000): Oocyte-secreted factor(s) determine functional differences between bovine mural granulosa cells and cumulus cells. Biol. Reprod. 63, 839-845 LIANG, L.-F., S. SOYAL u. J. DEAN (1997): Figα, a germ cell specific transcription factor involved in the coordinate expression of the zona pellucida genes. Development 124, 4939-4949 LONERGAN, P., A. GUTIERREZ-ADAN, D. RIZOS, B. PINTADO, J. DE LA FUENTE u. M. P. BOLAND (2003): Relative messenger RNA abundance in bovine oocytes collected in vitro or in vivo before and 20 hr after the preovulatory luteinizing hormone surge. Mol. Reprod. Dev. 66, 297-305 LOONEY, C. R., B. R. LINDSEY, C. L. GONSETH u. D. L. JOHNSON (1994): Commercial aspects of oocyte retrival and in vitro fertilisation (IVF) for embryo production in problem cows. Theriogenology 42, 67-72 98 Literaturverzeichnis ___________________________________________________________________________ LOONEY, C. R., P. DAMIANI, B. R. LINDSEY, C. R. LONG, C. L. GONSETH u. D. L. JOHNSON (1995): Use of prepubertal heifers as oocyte donors for IVF: effect of age and gonadotropin treatment. Theriogenology 43, 268, abstr. LORTON, S. P. u. N. L. FIRST (1979): Hyaluronidase does not disperse the cumulus oophorus surrounding bovine ova. Biol. Reprod. 21, 301-308 LUTTERBACH, A., R. A. KOLL u. G. BREM (1987): In vitro maturation of bovine oocytes in coculture and granulosa cells and their subsequent fertilisation and development. Zuchthygiene 22, 145-150 MAJERUS, V., R. DE ROOVER, D. ETIENNE, S. KAIDI, A. MASSIP, F. DESSY u. I. DONNAY (1999): Embryo production by ovum pick up in unstimulated calves before and after puberty. Theriogenology 52, 1169-1179. McGRATH, S. A., A. F. ESQUELA u. S. J. LEE (1995): Oocyte- specific expression of growth/differentiation factor-9. Mol. Endocrinol. 9 (1) 131-136 McPHERSON, M. J. u. S. G. MØLLER (2000): PCR: The basic from background to bench. The Cromwell Press, Trowbridge, Uk. MEINECKE, B. u. C. KRISCHEK (2003): MAPK/ERK kinase (MEK) signalling is required for resumption of meiosis in cultured cumulus-enclosed pig oocytes. Zygote 11, 7-16 MEINTJES, M., C. BEZUIDENHOUT, P. BARTELS, D. S. VISSER, J. MEINTJES, N. M. LOSKUTOFF, F. L. FOURIE, D. M. BARRY u. R. A.GODKE (1997): In vitro maturation and fertilization of oocytes recovered from free-ranging Burchell’s zebra (Equus burchelli) and Hartmann’s zebra (Equus zebra hartmannae). J. Zoo Wildl. Med. 28, 251-259 MEMILI, E., T. DOMINKO u. N. L. FIRST (1998): Onset of transcription in bovine oocytes and preimplantation embryos. Mol. Reprod. Dev. 51, 36-41 MEMILI, E. u. N. FIRST (1999): Control of gene expression at the onset of bovine embryonic development. Biol. Reprod. 61, 1198-1207 99 Literaturverzeichnis ___________________________________________________________________________ MEMILI, E. u. N. FIRST (2000): Zygotic and embryonic gene expression in cow: a review of timing and mechanisms of early gene expression as compared with other species. Zygote 8, 87-96 MOGAS, T., M. J. PALOMO, M. D. IZQUIERDO u. M. T. PARAMIO (1997): Developmental capacity of in vitro matured and fertilized oocytes from prepubertal and adult goats. Theriogenology 47, 1189-1203 MOORE, H. D. M. u. J. M. BEDFORD (1978): An in vivo analysis of factors influencing the fertilisation of hamster eggs. Biol. Reprod. 19, 879-885 NEBREDA, A. R. u. T. HUNT (1993): The c-mos proto-oncogene protein kinase turns on and maintains the activity of MAP-kinase, but not MPF in cell free extracts of Xenopus oocytes and eggs. Embo. J. 12, 1979-1986 NEKOLA, M. V. u. A. V. NALBANDOV (1971): Morphological changes of rat follicular cells as influenced by oocytes. Biol. Reprod. 4, 154-160 NIEMANN, H. u. B. MEINECKE (1993): In vitro Produktion von Embryonen. In: Embryotransfer und assoziierte Biotechniken bei landwirtschaftlichen Nutztieren. Enke Verlag, Stuttgart, S. 85-101 NIEMANN, H. u. C. WRENZYCKI (2000): Alterations of expression of developmentally important genes in preimplantation bovine embryos by in vitro culture conditions: Implications for subsequent development. Theriogenology 53, 21-34 NISWENDER, G. D. u. T. M. NETT (1994): Coprus luteum and its control in infraprimate species. In: Physiology of Reproduction Vol.1 pp 781-816 Eds. E. Knobil and JD Neill. Raven Press, New York NISWENDER, G. D. (2002): Molecular control of luteal secretion of progesterone. Reproduction 123, 333-339 NURSE, P. (1990): Universal control mechanism regulating onset of M-phase. Nature 344, 503-508 100 Literaturverzeichnis ___________________________________________________________________________ O’BRIEN J. K., D. DWARTE, J. P. RYAN. W. M. MAXWELL u. G. EVANS (1996): Developmental capacity, energy metabolism and ultrastructure of mature oocytes from prepubertal and adult sheep. Reprod. Fertil. Dev. 8, 1029-1037 OROPEZA, A. (2004): Improvement of the developmental capacity of oocytes from prepubertal cattle by intraovarian IGF-I application. Hannover. Tierärztl. Hochschule, Diss. OROPEZA, A., C. WRENZYCKI, D. HERRMANN, K. G. HADELER u. H. NIEMANN (2004): Improvement of the developmental capacity of oocytes from prepubertal cattle by intraovarian insulin-like growth factor-I application. Biol. Reprod. 70, 1634-1643 PALMA, G. A., C. SEGEWALD u. H. KREFFT (1993): In vitro production of cattle embryos from calf oocyte. Theriogenology 39, 278, abstr. PALMA, G. A., D. J. TORTONESE u. F. SINOWATZ (2001): Developmental capacity in vitro of prepubertal oocytes. Anat. Histol. Embryol 30, (5), 295-300 PANTALEON, M., M. B. HARVEY, W. S. PASCOE, D. E. JAMES u. P. L.KAYE (1997): Glucose transporter GLUT3: Ontogeny, targeting, and role in the mouse blastocyst. Proc. Natl. Acad. Sci. U.S.A. 94, 3795-3800 PANTALEON, M. u. P. L. KAYE (1998): Glucose transporters in preimplantation embryos. J. Reprod. Fertil. 3, 77-81 PARKER, K. I., D. M. ROBERTSON, N. P. GROOME u. K. L. MACMILLAN (2003): Plasma concentrations of inhibin A and follicle-stimulating hormone differ between cows with two or three waves of ovarian follicular development in a single estrous cycle. Biol. Reprod. 68, 822-828 PARRISH, J. J., J. SUSKO-PARRISH, M. L. LEIBFRIED-RUTLEDGE, E. S. CRISTER, W. H. EYESTONE u. N. L. FRIST (1986): Bovine in vitro fertilisation with frozen-thawed semen. Theriogenology 25, 591-600 PARRISH, J. J., J. SUSKO-PARRISH, M. A. WINER u. N. L. FRIST (1988): Capatication of bovine sperm by heparin. Biol. Reprod. 38, 1171-1180 101 Literaturverzeichnis ___________________________________________________________________________ PARTRIDGE, R. J., u. H. J. LEESE (1996): Consumption of amino acids by bovine preimplantation embryos. Reprod. Fertil. Dev. 8, 945-950 PAVLOK, A., J. KANKA, J. MOTLIK u. P. VODICKA (2000): Culture of bovine oocytes from small antral follicles in meiosis-inhibition medium with butyrolactone-I: RNA synthesis, nuclear morphology and meiotic competence. Anim. Reprod. Sci. 64, 1-11 PENNETIER, S., S. UZBEKOVA, C. PERREAU, P. PAPILLIER, P. MERMILLOD u. R. DALBIES- TRAN (2004): Spatio-temporal expression of the germ cell marker genes MATER, ZAR 1, GDF-9, BMP15 and VASA in bovine adult tissues, oocytes and preimplantation embryos. Biol. Reprod. 71 (4) 359-366 PIERSON, R. A. u. O.J. GINTHER (1988): Ultrasonic imaging of the ovaries and uterus in cattle. Theriogenology 29, 21-38 PIETERSE, M. C., K. A. KAPPEN, Th. A. M. KRUIP u. M. A. M. TAVERNE (1988): Aspiration of bovine oocytes during transvaginal ultrasound scanning of the ovaries. Theriogenology 35, 857-862 POSADA, J., N. YEW, N. G. AHN, G.F. VANDE WOUDE u. J. A. COOPER (1993): Mos stimulates MAP kinase in Xenopus oocytes and activates a MAP kinase in vitro. Mol. Cell Biol. 13, 2546-2553 PRESICCE, G. A., S. JIANG, M. SIMKIN, L. ZHANG, C. R. LOONEY, R. A. GODKE, u. X. YANG (1997): Age and hormonal dependence of acquisition of oocyte competence for embryogenesis in prepubertal calves. Biol. Reprod. 56, 386-392 RAWLINGS, N. C., A. C. O. EVANS, A. HONARAMOOZ u. P. M. BARTLEWSKI (2003): Antral follicle growth and endocrine changes in prepubertal cattle, sheep and goats. Anim. Reprod. Sci 78, 259-270 REVEL, F., P. MERMILLOD, N. PEYNOT, J. P. RENARD u. Y. HEYMAN (1995): Low developmental capacity of in vitro matured and fertilized oocytes from calves compared with that of cows. J. Reprod. Fertil. 103, 115-120 RICK, G. (1996): Experimentelle Untersuchungen zur Follikelpunktion und Oozytenentwicklung bei Jungrindern. Hannover, Tierärztl. Hochschule, Diss. 102 Literaturverzeichnis ___________________________________________________________________________ RICK, G., K. G. HADELER, E. LEMME, A. HAHN, D. RATH, L. SCHINDLER u. H. NIEMANN (1996): Long-term ultrasound guided ovum pick-up in heifers from 6 to 15 month of age. Theriogenology 45, 356, abstr. RICHARDS, J. S., J. J. IRELAND, M. C. RAO, G. A. BERNATH, A. R. MIDGLEY jr. u. L. E. REICHERT jr. (1976): Ovarian follicular development in the rat: hormone receptor regulation by estradiol, follicle stimulating hormone and luteinizing hormone. Endocrinology 99 (6), 1562-1570 RIEF, S., F. SINOWATZ, M. STOJKOVIC, R. EINSPANIER, E. WOLF u. K. PRELLE (2002): Effects of a novel co-culture system on development, metabolism and gene expression of bovine embryos produced in vitro. Reproduction 124, 543-556 ROCHE, J. F. u. M. P. BOLAND (1991): Turnover of dominant follicles in cattle of different reproductive states. Theriogenology 35, 81-90 ROMAR, R., P. COY, I. CAMPOS, J. GADEA, C. MATAS u. S. RUIZ (2001): Effect of co-culture of porcine sperm and oocytes with porcine oviductal epithelial cells on in vitro fertilisation. Anim. Reprod. Sci. 68, 85-98 ROSCHLAU, K., A. KUWER, U. MICHAELIS, C. KUHNT, D. ROSCHLAU, P. POPPE u. J. REINEKE (2005): Wichtiges Instrument für die Rinderzucht- Embryotransfer wird 30 Jahre alt. Jahrestagung der AET- d 30. Juni/01. Juli 2005 ROSCHLAU, K., P. UNIKI, A. KUWER, R. ROSELIUS, U. MICHAELIS, R. STREHL, U. DEXNE, D. ROSCHLAU u. N. RINK (1997): Routinemäßige In vitro - Produktion nach ovum pick-up bei Problemkühen. Jahrestagung der AET- d, 19./20.06.1997 SAGATA, N., N. WATANABE, G. F. VANDE WOUDE u. Y. IKAWA (1989): The c-mos proto-oncogen product is a cytostatic factor responsible for meiotic arrest in vertebrate eggs. Nature 342, 512-518 SALAMONE, D. F., P. DAMIANI, R. A. FISSORE, J. M. ROBL u. R. T. DUBY (2001): Biochemical and developmental evidence that ooplasmatic maturation of prepubertal bovine oocytes is compromised. Biol. Reprod. 63, 1761-1768 103 Literaturverzeichnis ___________________________________________________________________________ SAVIO, J. D., L. KEENAN, M. P. BOLAND u. J. F. ROCHE (1988): Pattern of growth of dominant follicles during the oestrus cycle of heifers. J. Reprod. Fertil. 83, 663-671 SCHNORR, B. u. M. KRESSIN (2001): Progenese, Vorentwicklung In: Embryologie der Haustiere Enke Verlag, Stuttgart, S. 3-43 SCHULTZ, R. M. (1993): Regulation of zygotic gene activation in the mouse. Bioessays 15, 531-538 SCHUMMER, A. u. B. VOLLMERHAUS (1995): Weibliche Geschlechtsorgane der Wiederkäuer. in: K.-H. HABERMEHL, B. VOLLMERHAUS u. H. WILKENS (Hrsg.): Lehrbuch der Anatomie der Haustiere, 7. Auflage, Blackwell Wissenschaftsverlag. Berlin, S. 406415 SENDAI, Y., T. ITOH, S. YAMASHITA u. H. HOSHI (2001): Molecular cloning of a cDNA encoding a bovine growth differentiation factor-9 (GDF9) and expression of GDF-9 in bovine ovarian oocytes and in virto-produced embryos. Cloning 3, 3-10 SHIVERS, B. D., R. E. HARLAN, J. I. MORRELL u. D. W. PFAFF (1983): Absence of oestradiol concentration in cell nuclei of LHRH- immunoreaktive neurones. Nature 304, 345-347 SILVA, J. R. V., R. VAN DEN HURK, H. T. A. VAN TOL, B. A. J. ROELEN u. J. R. FIGUEIREDO (2004): Expression of growth differentiation factor-9 (GDF-9), bone morphogenic protein 15 (BMP15), and BMP receptors in the ovaries of goats. Mol. Reprod. Dev. 70, 11-19 SIMON, A. M., D. A. GOODENOUGH, E. LI u. D. L. PAUL (1997): Female infertility in mice lacking connexin 37. Nature 385, 535-529 SIMON L., L. BUNGARTZ, D. RATH u. H. NIEMANN (1993): Repeated bovine oocyte collection by means of a permanently rinsed ultrasound guided aspiration unit. Theriogenology 39, 312 104 Literaturverzeichnis ___________________________________________________________________________ SIRARD, M. A., H. M. FLORMAN, M. L. LEIBFRIED-RUTLEDGE, F. L. BARNES, M. L. SIMS u. N. L. FIRST (1989): Timing of nuclear progression and protein synthesis necessary for meiotic maturation of bovine oocytes. Biol. Reprod. 40, 1257-1263 SOLLOWAY, M. J. A. T. DUDLEY E. K. BIKHOFF, K. M. LYONS, B. L. HOGAN u. E. J. ROBERTSON (1998): Mice lacking Bmp6 function. Dev. Genet. 22, 321-339 SOMMER, P. (1991): Experimentelle Untersuchungen zur Modulation der In-vitro-Reifung porziner Kumulus-Oozyten-Komplexe durch Granulosazellen. Hannover, Tierärztl. Hochschule, Diss. SOYAL, S. M., A. AMLEH u. J. DEAN (2000): FIGα, a germ cell-specific transcription factor required for ovarian follicle formation. Development 127, 4645-4654 STEEVES, T. E. u. D. K. GARDNER (1999): Metabolism of glucose, pyruvate, and glutamine during the maturation of oocytes derived from pre-pubertal and adult cows. Mol. Biol. 54, 92-101 STEEVES, T. E., D. K. GARDNER, K. A. ZUELKE, T. S. SQUIRES u. R. C. FRY (1999): In vitro development and nutrient uptake by embryos derived from oocytes of prepubertal and adult cows. Mol. Reprod. 54. 49-56 TANEJA, M., P. E. J. BOLS, A. VAN DE VELDE, J. C. JU, D. SCHREIBER, M. W. TRIPP, H. LEVINE, Y. ECHELARD, J. RIESEN u. X. YANG (2000): Developmental competence of juvenile calf oocytes in vitro and in vivo: Influence of donor animal variation and repeated gonadotropin stimulation. Biol. Reprod. 62, 206-213. TAKAGAKI, Y., L. C. RYNER u. J. L. MANLEY (1988): Separation and characterisation of a poly(A)polymerase and a cleavage/specificity factor required for pre-mRNA polyadenilation. Cell 52, 731-742 TELFORD, N. A., A. J. WATSON u. G. A. SCHULTZ (1990): Transition from maternal to embryonic control in early mammalian development: a comparison of several species. Mol. Reprod. Dev. 26, 90-100 105 Literaturverzeichnis ___________________________________________________________________________ TERBECK-HASENPUSCH, H., B. HARDER, A. KUWER u. W. JUNGE (2005): ‚Reproduktionsleistung’ von Bullenmüttern in der NOG-Stationsprüfung in biotechnologischen Verfahren: Beziehungen, Einflüsse und Erfahrungen. Jahrestagung der AET- d 30. Juni/01. Juli 2005 TEOTIA, A., G.T. SHARMA u. A.C. MAJUMDAR (2001): Fertilisation and development of caprine oocytes matured over granulosa cell monolayers. 1: 0921-4488, 40 (2), 165-177 Abstr. THANGE, S., A. VAN SOOM, M. CORYN, H. LAEVENS u. A. DE KRIUF (2001): Progesterone alone is not sufficient to mimic the beneficial effect of a cumulus monolayer on the penetration rates of cumulus - fee oocytes. Theriogenology 55, 439, abstr. THANGE, S., A. VAN SOOM, H. NAUWYNCK, M. CORYN u. A. DE KRUIF (2002): Functions of the cumulus oophorus during oocyte maturation, ovulation and fertilisation. Mol Reprod. Dev. 61, 414-424 THANGE, S., A. VAN SOOM, J. MEHRZAD, D. MAES, L. DUCHATEAU u. A. DE KRIUF (2003): Cumulus contribution during bovine fertilisation in vitro. Theriogenology 60, 135-149 THOMPSON, J. G., R. J. PARTRIDGE, F. D. HOUGHTON, C. I. COX u. H. J. LEESE (1998): Oxygen uptake and carbohydrate metabolism by in vitro derived bovine embryos. J. Reprod. Fertil. 106, 299-306 TSAFRIRI, A., M. E. LIEBERAN, Y. KOCH, S. BAUMINGER, P. CHOBSIENG, U. ZOR u. H. R. LINDNER (1976): Capacity of immunologically purified FSH to stimulate cyclic AMP accumulation and steroidogenesis in graafian follicles and to induce ovum maturation and ovulation in the rat. Endocrinology 98, 655-661 VAN SOOM, A., S. THANGE, I. DE PAUW, D. MAES u. A. DE KRUIF (2002): Function of the cumulus oophorus before and during mammalian fertilisation. Reprod. Dom. Anim. 37, 144-151 VIUFF, D., B. AVERY, T. GREVE, W. A. KING u. P.HYTTEL (1996): Transcriptional activity in in vitro produced bovine two- and four-cell embryo. Mol. Reprod. Dev. 43, 171-179 106 Literaturverzeichnis ___________________________________________________________________________ WALKER, S. K., K. M. HARTWICH u. R. F. SEAMARK (1996): The production of unusually large offspring following embryo manipulation: Concepts and challenges. Theriogenology 45, 111-120 WALTERS, D. L. u. E. SCHALLENBERGER (1984): Pulsatile secretion of gonadotropins, ovarian steroids and ovarian oxytocin during the luteal phase of the oestrus cycle of the cow. J. Reprod. Fertil. 71, 503-512 WANDJI, S. A., M. A. FORTIER u. M. A. SIRARD (1992): Differential response to gonadotropin and prostaglandin E2 in ovarian tissue during prenatal and postnatal development in cattle. Biol. Reprod. 46, 1034-1041 WEHREND, A. u. B. MEINECKE (2001): Kinetics of meiotic progression, M-phase promoting factor (MPF) and mitogenactivated protein kinase (MAP kinase) activities during in vitro maturation of porcine and bovine oocytes: species specific differences in the length of meiotic stages. Anim. Reprod. Sci. 66, 175-184 WIEKING, M. (2001): Experimentelle Untersuchungen zur Verbesserung der Effizienz der Ultraschallgeleiteten, transvaginalen Follikelpunktion bei präpuberalen Rindern durch intraovarielle Verabreichung von Gonadotropinen. Hannover, Tierärztl. Hochsch., Diss. WRENZYCKI, C., D. HERRMANN, J. W. CARNWATH u. H. NIEMANN (1998): Expression of RNA from developmentally important genes in preimplantation bovine embryos produced in TCM supplemented with BSA. J. Reprod. Fertil. 112, 387-398 WRENZYCKI, C., D. HERRMANN, J. W. CARNWATH u. H. NIEMANN (1999): Alterations in the relative abundance of gene transcripts in preimplantation bovine embryos cultured in medium supplemented with either serum or PVA. Mol. Reprod. Dev. 53, 8-18 WRENZYCKI, C., D. HERRMANN, L. KESKINTEPE, A. MARTINS JR., S. SIRISATHIEN, B. BRACKETT u. H. NIEMANN (2001a): Effects of culture system and protein supplementation on mRNA expression in preimplantation bovine embryos. Human Reprod. 16, 893-901 107 Literaturverzeichnis ___________________________________________________________________________ WRENZYCKI, C., D. WELLS, D. HERRMANN, A. MILLER, J. OLIVER, R. TREVIT u. H. NIEMANN (2001b): Nuclear transfer protocol affects RNA expression patterns in cloned bovine blastocysts. Biol. Reprod. 65, 309-317 WRENZYCKI, C., D. HERRMANN, A. LUCAS-HAHN, E. LEMME, K. KORSAWE u. H. NIEMANN (2004): Gene expression patterns in in vitro-produced and somatic nuclear transfer - derived preimplantation bovine embryo: relationship to the large offspring syndrome? Anim. Reprod. Sci 82-83, 539-603 WRENZYCKI, C., D. HERRMANN, A. LUCAS-HAHN, C. GEBERT, K. KORSAWE, E. LEMME, J. W. CARNWATH u. H. NIEMANN (2005a): Epigenetic reprogramming throughout preimplantation development and consequences for assisted reproductive technologies. Birth Defects Research 75, 1-9 WRENZYCKI, C., D. HERRMANN, A. LUCAS-HAHN, K. KORSAWE, E. LEMME, J. u. H. NIEMANN (2005b): Messenger RNA expression patterns in bovine embryos derived from in vitro procedures and their implications for development. Reprod. Fertil. Dev. 17, 23-35 WU, B., G. IGNOTZ, W. B. CURRIE u. X. YANG (1997): Expression of Mos-proto-oncoprotein in bovine oocytes during maturation in vitro. Biol. Reprod. 56, 260-265 YAMAMOTO, N., L. K. CHRISTENSON, J. M. McALLISTER, u. J. E. STRAUSS III (2002): Growth differentiation factor-9 inhibits 3’ 5’- adenosine – monophosphate - stimulated steroidogenesis in human granulosa and theca cells. J. Clin. Endocrinol. Metab. 87 ,(6), 2849- 2856 YING, J. Y. (1988) Inhibins, activins and follistatins: gonadal proteins modulating the secretion of folliclestimulating hormone. Endocr. Rev. 9, 267-293 YOUNG L. E., K. D. SINCLAIR u. I. WILMUT (1998): Large offspring syndrome in cattle and sheep. Rev.Reprod. 3, 155-163 ZHANG, L., S. JIANG, P. J. WOZNIAK, X. YANG u. R. A. GODKE (1995): Cumulus cell function during bovine oocyte maturation, fertilisation, and embryo development in vitro. Mol. Reprod. Dev. 40, 338-344 108 Anhang 9 ANHANG, ABBILDUNGEN UND TABELLEN 9.1 Geräte und Material für OPU Einmal-Schutzhülle Mapa GmbH, Zeven Epiduralanestesie 2-5 ml Prokain Hydrochlorid (Minocain 2%) Atarost, Twistringen FSH Folltropin, Bioniche, Canada Gerätedesinfektion Korosolex plus, 973899, Bode Chemie Gleitgel Bovi-Vet Gel, Kruuse, Marslev, Dänemark Hautdesinfektion Baktonium, Bode Chemie, Hamburg Kanüle für Punktion 20G23/4 (0,9x70, Terumo Europe, N.V.-3001 Leuven, Belgien) Mikropipette 20µl, Brand, Wertheim Sieb Industriesieb 50 µm, Jürgens, Hannover Sondenträger mit Punktionführung Eigenbau, Feinmechanik, Mariesee (FAL) Stereomikroskop Nikon, Düsseldorf Sedierung 0,2-0,3 ml Rompun Ultraschallbildschirm Picker Model CS9000, Picker, München Ultaschallkopf 6,5MHz, Picker Model: EUP-F-331, Picker, München Vakuumpumpe IVF Ultra Quiet, COOK Veterinary Products, Mönchengladbach Zentrifugenröhrchen 50 ml Greiner, Nürtingen 109 Anhang 9.2 Geräte und Material für die In-vitro-Produktion von Embryonen Co2-Inkubatoren Hera Cell, Heraeus, Hanau Modular Incubation Chamber Billups-Rothenberg, INC, CA, USA Phasenkontrastmikroskop Olympus, Hamburg Petrischalen 35/10mm, 60/10mm, GmbH, Nürtingen Sterilfilter 0,22 µm Fliter, Nr.10462200, Schleicher&Schuell, Dassel, Deutschland Silikonöl Serva, Heidelberg Zählkammer Neubauer Zentrifuge Megafuge 1,0 R, Heraeus Hanau Zentrifugenröhrchen 14ml Greiner, Nürtingen 9.3 94/16mm Greiner Geräte und Material für Zellkultur Laborbank mit laminarem Luftstrom 2 KR Biowizard 130, Kojar,Tampere, Finnland 75cm Kulturflaschlasche Tissue Culture Flask, 9296, Fa.TPP/Schweiz Kryoröhrchen PP-Röhrchen streril, 1ml, 12,5/42MM, Greiner Bio-one GmbH, Frickenhausen Pipetten 0,5-10,0 µl/10,0-100 µl/100-1000µl, Eppendorf Wärmeschrank Hera Cell, Typ BB16, Fa Heraus Instruments, Hanau 4-Well Dish 176740, Nunclon Surface, Dänemark Zentrifuge Megafuge 1,0R, Heraeus, Hanau 110 Anhang 9.4 Geräte, Lösungen und Material für RT-PCR Agarose SeaKem®LE Agorose, No. AG4487, Cambrex, Biscience, Rockland, USA CCD Kamera Quantix Photometrics, München Dynabeads mRNA Direct Kit Dynal, Oslo, Norwegen Gelelektrophoresekammer Eigenbau, Mariensee (FAL) IPLab Gel Software Programm Signal Analytics Corporation Vienna, USA IPLab Spectrum Software Progr. Signal Analytics Corporation Vienna, USA Stromquelle f. Elektrophorese PP2-79, Daela ApS, Uldum, Dänemark Elektrophorese TBE- Puffer, Tris-Acetat-EDTA Tris: 4855.2, Carl Roth GmbH, Karlsruhe Borsäure: 6943.1, Carl Roth GmbH EDTA: 8043.2, Carl Roth GmbH PCR-Cycler PTC-200, MJ Research, Watertown, USA Pipettenspitzen Safeseal-Tips Thermoschüttler Thermomixer 5436, Eppendorf, Hamburg Tischzentrifuge Typ 5415, Eppendorf, Hamburg Transilluminator Chromato-Vue TM-20, UVP, USA 10x RT Puffer Y02028, Invitrogen, Karlsruhe 50mM MgCl2 Y02016, Invitrogen, Karlruhe dNTPs Amersham, Biosciences Europe GmbH, Freiburg Random Hexamers N808-0127, GeneAmp® RNA PCR Kit components, Applied Bisosystems, USA RNAse- Inhibitor N808-0119, GeneAmp® RNA PCR Kit components, Applied Bisosystems, USA Reverse Transcriptase N808-0018, GeneAmp® RNA PCR Kit components, Applied Bisosystems, USA Taq DNA Polymerase 10342-010, Invitrogen, Karlsruhe 111 Anhang 9.5 Zusammensetzung der Medien 9.5.1 Zellkulturmedium Tabelle 15: Zellkulturmedium Komponente Menge (ml) DMEM-Stock 1l Endkonzentration Hersteller 10x DMEM-Stock Dulbecco’s Modified Eagle’s Medium 100 D-2554, Sigma Autoklaviertes H2O 839 NaHCO3 50 4,5mM 31437, Riedel 100x L-Glutamin 10 2mM G-5763,Sigma 0,1mM M-7522, Sigma 2,5µg/ml A-2942, Sigma 100U/ml 50µg/ml PEN-NA,Sigma S-6501,Sigma 0,1M ßMercapthoethanol Amphotericin B preparation Zellkulturmedium 100ml Penicillin/ Streptomycin Sulfat Non essential amino acids MEM 1 M-7145, Sigma Fetal Calf Serum (FCS) 10 10270-106, GIBCOTM, FA. Invitrogen DMEM-Stock bis 100ml auffüllen 112 Anhang 9.5.2 Einfriermedium Tabelle 16 Einfriermedium Komponente Menge DMEM-Stock 80ml Dimethyl Sulphoxid, DMSO 10% D-2650, Sigma FCS 10% 10270-106, GIBCOTM, Invitrogen 9.5.3 Hersteller PBS - Phosphate buffered saline Tabelle 17: PBS- Phosphate buffered saline Komponente Einheit Menge g/l 9,25 Penicilin G IU/ml 50 Sigma Streptomycin Sulfat µg/ml 50 35500 Serva, Heidelberg Pyruvat µg/ml 36 P-3662, Sigma D-Glukose mg/ml 1 Carl-Roth GmbH, Karlsruhe CaCl2 2H2O µg/ml 133 Merck, Darmstadt ml/l 10 Invitrogen IU/ml 2,2 24590 Serva Dulbeco’s phosphate buffered saline hitzeinaktiviertes NBCS Heparin 113 Katalog Nr. D-5773, Sigma-Aldrich Chemie GmbH, Taufkirchen Anhang 9.5.4 TCM-air Tabelle 18: TCM-air Komponente Einheit Menge TCM 199 mg/ml 15,1 Pyruvat µg/ml 22 P-3662, Sigma NaCO3 µg/ml 350 31437, Sodium Hydrogen Karbonat, Riedel-de Haen AG, Seelze Gentamycin µg/ml 50 G-3632, Sigma % 0,1 A-7030,Sigma BSA-fatty acid free FAF Ampuwa® 9.5.5 Katalog Nr. M-2520, mit L-Glutamin und 25mM Hepes, Sigma Fresenius AG, Bad Homburg TCM + BSA (Reifungsmedium) Tabelle 19: TCM + BSA (Reifungsmedium) Komponente Einheit Menge Katalog Nr. TCM 199 mg/ml 15,1 M-2520, mit L-Glutamin und 25mM Hepes, Sigma Na-Pyruvat µg/ml 22 P-3662, Sigma NaCO3 mg/ml 2,2 31437, Sodium Hydrogen Karbonat, Riedel-de Haen AG, Seelze Gentamycin µg/ml 50 G-3632, Sigma BSA-fatty acid free FAF % 0,1 A-7030,Sigma Ampuwa® Fresenius AG, Bad Homburg Equine chorionic Gonadotropin (eCG) IU/ml 10 Suigonan, Intervet, Tönisvorst Human chorionic gonadotropin (hCG) IU/ml 5 Suigonan, Intervet, Tönisvorst 114 Anhang 9.5.6 Sperm-TALP und Fert-Talp (Fertilisationsmedien) Tabelle 20: Sperm-TALP und Fert-TALP (Fertilisationsmedien) Komponente Einheit SpermTalp Fert-Talp Hersteller NaCl mM 100 114 S-5886, Sigma KCl mM 3,1 3,1 P-5405, Sigma NaCO3 mM 25 25 Merck NaH2PO4xH2O mM 0,3 0,3 S-4019, Sigma CaCl2x2H2O mM 2 2 Merck MgCl2 mM 0,4 0,5 Merck HEPES mM 10 - H-6147, Sigma Na-Laktat mM 21,6 10 L-4263, Sigma Na-Pyruvat mM 1,0 0,2 P-3662, Sigma Penicillamin mM -- 20 P-4875, Sigma Phenolrot mg/ml 0,01 0,01 7241, Merck Gentamycin mg/ml 50 50 G-3632, Sigma Heparin IU/ml -- 0,1 24590, Serva Hypotaurin µM -- 10 H-1384, Sigma Epinephrin µM -- 1 E-4250, Sigma mg/ml 6 6 A-9647, Sigma BSA 115 Anhang 9.5.7 SOF-Medium (Kulturmedium) Tabelle 21: SOF-Stockmedien Komponente g/mol mM Katalog Nr. Sigma 1,08M NaCl 58,44 108 S-5886 0,072M KCl 74,55 7,2 P-5405 0,012M KH2PO4 136,1 1,2 P-5655 MgSO4 120,4 1,5 M-3643 SOF-Stock A (100x) Sigma Wasser (ml) *0,042m Na-Laktat (ml) W-1503 112,1 4,2 L-4263 0,25M NaHCO3 84,01 25 S-4019 Phenolrot (g) 376,4 1mg/100ml P-5530 *als letztes Reagent hinzufügen SOF-Stock B (10x) Sigma Wasser (ml) W-1503 SOF-Stock C (100x) 0,073M Na-Pyruvat (g) 110,0 0,73 Sigma Wasser (ml) P-3662 W-1503 SOF-Stock D (100x) 0,178M CaCl2xH2O (g) 147,0 1,78 Sigma Wasser (ml) C-7902 W-1503 Lagerung bei 4°C und nach Sterilfiltrieren 4 Wochen haltbar 116 Anhang Tabelle 22: SOFaa Kulturmedium SOFaa Kultur Medium Komponente g/mol mM 50 ml Katalog Nr. Sigma Myo-Inositol 180,2 2,77 0,025g I-7508 Tri-Na-Zitrat 294,1 0,34 0,005g S-4641 50µg/ml 0,0025g G-3632 0,2 50µl G-6392 Gentamycin Glutamin Stock A 5,0ml Stock B 5,0ml Stock C 0,5ml Stock D 0,5ml BME 50x 30µg/ml 1,5ml B-6766 MEM 100x 10µg/ml 0,5ml M-7145 BSA-FAF wird am Ende hinzugefügt (4mg/ml) 9.6 Abbildungsverzeichnis Abbildung 1: Schema der Oogenese (nach SCHNORR und KRESSIN 2001)........4 Abbildung 2: MAPK, MPF, Cyclin B und ihre Rolle bei der Oozytenreifung und Befruchtung beim Säugetier (nach FAN et al. 2004 und ABRIEU et al. 2001) ...........................................................................7 Abbildung 3: Zellzyklus mit seinen Phasen. G1, S, G2 bilden die Interphase und M bildet die Mitosephase (nach NIEMANN und MEINECKE 1993) ..................................................................................................8 Abbildung 4: Beidseitige Kommunikation von Oozyte und Follikelzelle (modifiziert nach EPPIG 2001).........................................................11 Abbildung 5: GDF-9 und seine vielfältige Rolle im Säugetierovar (modifiziert nach ELVIN 1999)............................................................................13 117 Anhang Abbildung 6: Abgestimmtes Zusammenwirken von extra- und intraovariellen Faktoren im Follikel (nach Knight und GLISTER 2001)....................15 Abbildung 7: Östrogensynthese in Granulosazellen (nach ENGELHARDT und BREVES 2000)..........................................................................17 Abbildung 8: OPU beim Kalb mit Detailansicht der Punktion ................................21 Abbildung 9: a) Granulosazell- und b) Fibroblastenmonolayer, Vergrößerung 200x .................................................................................................40 Abbildung 11: Expandierte Blastozyste an Tag 8 angefärbt mit Bisbenzimid, 400 x Vergrößerung (Fluoreszenzmikroskop) ..................................47 Abbildung 12: Schematische Darstellung des Versuchsaufbaus ............................55 Abbildung 13: a) Repräsentativer gelektrophoretischer Nachweis der semiquantitativen RT-PCR Analyse der GDF-9 Expression und b) relativer Transkriptgehalt von GDF-9 mRNA in ungereiften und gereiften Oozyten von Kälbern und Kühen ...........................66 Abbildung 14: a) Repräsentativer gelektrophoretischer Nachweis der semiquantitativen RT-PCR Analyse der Hsp.70 Expression und b) relativer Transkriptgehalt von Hsp.70 mRNA in ungereiften und gereiften Oozyten von Kälbern und Kühen........................................67 Abbildung 15: a) Repräsentativer gelektrophoretischer Nachweis der semiquantitativen RT-PCR Analyse der Hsp.70 Expression und b) relativer Transkriptgehalt von Hsp.70 mRNA in 8-16 Zellern und expandierten Blastozysten (Tag 7und Tag 8) von Kälbern und Kühen...............................................................................................68 Abbildung 16: Relativer Transkriptgehalt von Hsp.70 mRNA pro Zelle in expandierten Blastozysten an Tag 7 und Tag 8 ...............................69 118 Anhang Abbildung 17: a) Repräsentativer gelektrophoretischer Nachweis der semiquantitativen RT-PCR Analyse der Glut-3 Expression und b) relativer Transkriptgehalt von Glut-3 mRNA in 8-16 Zellern und expandierten Blastozysten (Tag 7 und Tag 8) von Kälbern und Kühen ...............................................................................................70 9.7 Tabellenverzeichnis Tabelle 1: Effizienz der ultraschall geleiteten, transvaginalen Follikelpunktion bei einigen Nutz- und Wildtierarten.........................20 Tabelle 2: Entwicklungskapazität von Oozyten aus Kälbern und Kühen im Hinblick auf Teilungs- und Blastozystenraten...................................24 Tabelle 3: Zusammensetzung des RT-Reaktionsgemisches ............................49 Tabelle 4: Zusammensetzung der Mastermixe (MM)........................................50 Tabelle 5: PCR- Bedingungen für die Amplifizierung spezifischer Gentranskripte..................................................................................51 Tabelle 6: Primerpaare für PCR, Annealingtemperaturen, Zyklenanzahl, Embryonenanteile, Fragmentgröße der PCR Produkte und Referenzen für Hsp.70, Glut-3, GDF-9 und Globin ..........................52 Tabelle 7: Übersicht zu den Ergebnissen der OPU Sitzungen und gewonnenen Kumulus-Oozyten-Komplexen bei Kälbern .................58 Tabelle 8: Übersicht zu den Ergebnissen der OPU-Sitzungen und gewonnener Kumulus-Oozyten-Komplexen bei Kühen ....................59 Tabelle 9: Vergleichende Darstellung der Anzahl punktierter Follikel, KOK und IVF tauglicher KOK bei Kälbern und Kühen ( ± SD ) ..............60 Tabelle 10: Anzahl punktierter Follikel, erhaltener KOK und IVF tauglicher Oozyten in den Monaten April bis September im Vergleich zu Punktionen von Oktober bis Februar bei Kälbern ( ± SD ).............61 119 Anhang Tabelle 11: Anzahl punktierter Follikel, erhaltener KOK und IVF tauglicher Oozyten in den Monaten April bis September im Vergleich zu Punktionen von Oktober bis Februar bei Kühen ( ± SD )...............62 Tabelle 12: Einfluss des Kälbergewichts auf die Punktionsergebnisse...............63 Tabelle 13: Teilungs- und Blastozystenraten bei den unterschiedlichen Reifungsgruppen 72h nach IVF bzw. Tag 7 und Tag 8 ....................64 Tabelle 14: Zellzahlen der expandierten Blastozysten (Tag 7 und Tag 8) ..........64 Tabelle 15: Zellkulturmedium ............................................................................112 Tabelle 16 Einfriermedium ..............................................................................113 Tabelle 17: PBS- Phosphate buffered saline ....................................................113 Tabelle 18: TCM-air ..........................................................................................114 Tabelle 19: TCM + BSA (Reifungsmedium) ......................................................114 Tabelle 20: Sperm-TALP und Fert-TALP (Fertilisationsmedien).......................115 Tabelle 21: SOF-Stockmedien ..........................................................................116 Tabelle 22: SOFaa Kulturmedium.....................................................................117 120 DANKSAGUNGEN Mein Dank gilt Herrn Prof. Dr. Heiner Niemann für die Überlassung des Themas. Herzlichen Dank für die wissenschaftliche Betreuung und die Unterstützung bei der Durchführung und Fertigstellung und die schnelle Korrektur dieser Arbeit. Dem Leiter des Instituts für Tierzucht FAL in Mariensee Herrn Prof. Dr. sc.agr. Dr. habil. Dr. h.c. Franz Ellendorff, danke ich für die Bereitstellung des Arbeitsplatzes. Veterinarski fakulteti v Ljubljani se iskreno zahvaljujem za finančno pomoč pri mojemu izobraževanju v Marienseeju. Professor Marjan Kosec, predstojnik Klinike za reprodukcijo in konje Veterinarske fakultete v Ljubljani, prisrčna hvala za vašo pomoč in podporo. Frau PD Dr. Christine Wrenzycki herzlichen Dank für die große Hilfsbereitschaft bei der Durchführung, vor allem des molekularbiologischen Teils dieser Arbeit und bei der statistischen Auswertung. An Doris Herrmann und Monika Nowak-Imialek einen großen Dank für die Hilfe, die vielen guten Ratschläge im Labor und die Geduld. Ich danke besonders Karin Korsawe für die Einarbeitung in die IVP Technik. Für die Hilfe bei der Einarbeitung in OPU und die vielen guten Ratschläge möchte ich mich bei Klaus-Gerd Hadeler ganz herzlich bedanken. Un especial agradecimiento a mi amigo Dr. Armando Oropeza, quien con su conocimientos y experiencia me ayudó mucho en este trabajo. Für die Hilfe beim Punktieren, der Versorgung der Tiere während der Versuche und für die stets entspannte Arbeitsatmosphäre möchte ich mich bei Hans-Georg Sander, Rolf Poppenga, und besonders Grit Möller ganz, ganz herzlich bedanken. Gunnar Scharnhorst und seinen Mitarbeitern in Mecklenhorst einen großen Dank für die Versorgung der Kälber. An die fast zahllosen aber nicht namenlosen Helfer beim Punktieren, Suchen und Fertigstellen der Medien geht mein herzlicher Dank: Corinna Backhaus, Manon Elfers, Viktor Funk, Katharina Höffmann, Stefanie Holler, Karin Korsawe, Kerstin Meyer, Monika Nowak-Imialek, Armando Oropeza, Lothar Schindler und Anna-Lisa Queißer. Vielen Dank an Dr. Wilfried Kues für das zur Verfügung stellen der Fibroblasten und die vielen gute Ratschläge für das Arbeiten im Zellkulturlabor. An Björn Petersen vielen lieben Dank für die Einarbeitung im Zellkulturlabor, die vielen Tipps Rund um Word (vor allem für das „x quer“) und die lustige Zeit als Tischnachbar. 121 Für die kompetente Hilfe beim Herstellen der Medien im Zellkulturlabor möchte ich mich bei Wiebke Mysegades bedanken. Ein herzlicher Dank an Frau Dr. Andrea Lucas-Hahn und Erika Lemme für die vielen guten Ratschläge, für das Gewinnen der Granulosazellen und für IVP. Vielen Dank an Frau Dr. Christine Ehling für das Bestellen der Arzneimittel. Bei Dieter Bunke möchte ich mich für das Einscannen der Zeichnungen bedanken. Ein herzlicher Dank an Hans-Hermann Döpke für das Bestellen von Labormaterial und beim Korrigieren dieser Arbeit. Vielen Dank an Ph.D. Joe Carnwath für die Korrektur der Summary. Diese Arbeit würde ohne Christine Weidemann „anders“ aussehen! Herzlichen Dank für die Hilfe beim Formatieren! Für den Kaffee und die Gesellschaft in den frühen Morgenstunden vielen Dank an Gabi Reinsch. Allen Mitarbeitern der Arbeitsgruppe Biotechnologie, herzlichen Dank für die freundliche Aufnahme, tatkräftige Unterstützung und gute Zusammenarbeit. Für die vielen kleinen Tipps und fürs Mitfiebern in der Schlussphase ein lieber Dank an Monika und Katharina. Für die schöne gemeinsame Zeit als „Hohenhorst-Truppe“ möchte ich mich bei Claudia Gebert, Marianna und Armando Oropeza, Javier Zaraza, Monika und Marek Imialek und Primoz Klinc bedanken. Ganz besonders herzlich möchte ich mich bei Franček und Uschi Klobasa für all die Fürsorge und Unterstützung bedanken. Javier, gracias para tu confianza, apoyo y amor sin fronteras. Tati, Du ahnst nicht wie oft Du genau im richtigen Moment angerufen hast! Danke für alles! Liebe Eltern, an euch geht mein tiefster Dank für eure Unterstützung, euer Vertrauen und euer Verständnis. 122