Häufige Augenerkrankungen im Alter
Werbung

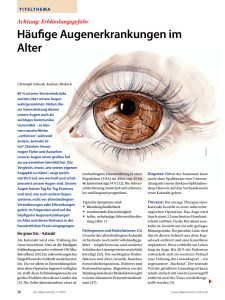
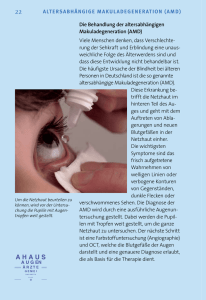
FORTBILDUNG Häufige Augenerkrankungen im Alter Wie man sie erkennt und welche Massnahmen zur Verfügung stehen Unsere Augen leisten Tag für Tag Enormes und sind, wie auch andere Organsysteme, nicht vor altersbedingten Veränderungen oder Erkrankungen gefeit. Im Folgenden wird auf die häufigsten Augenerkrankungen im Alter und deren Relevanz in der hausärztlichen Praxis eingegangen. CHRISTOPH SCHWAB UND ANDREAS WEDRICH 80 Prozent unserer Sinneseindrücke werden über unsere Augen wahrgenommen. Neben dieser Sinnesleistung dienen unsere Augen auch als wichtiges Kommunikationsmittel – so können manche Blicke «verführen», während andere «beinahe töten». Darüber hinaus tragen Farbe und Aussehen unserer Augen einen grossen Teil zur persönlichen Identität bei. Der Vergleich, etwas «wie seinen eigenen Augapfel zu hüten», zeigt sprichwörtlich auf, wie wertvoll und schützenswert unsere Augen sind. Der graue Star – Katarakt Als Katarakt wird eine Trübung der Linse bezeichnet. Dies ist die häufigste Erblindungsursache weltweit (30 Mio. Betroffene) (1). Ein mikrochirurgischer Eingriff kann die Sehkraft wiederherstellen. Da vor allem in Entwicklungsländern diese Operation begrenzt verfügbar ist, stellt diese Erblindungs- Merksätze ❖ Aufgrund des geringen Blutungsrisikos braucht eine etwaig bestehende Antikoagulation bei der präoperativen Kataraktuntersuchung nicht abgesetzt zu werden. ❖ Rauchen ist der wichtigste beeinflussbare Risikofaktor bei der Makuladegeneration. ❖ Ab dem 40. Lebensjahr sollten selbst beschwerdefreie Personen einem Glaukomscreening unterzogen werden. Die alleinige Augendruckmessung kann ein Glaukom jedoch weder ausschliessen noch kann sie den Verlauf beurteilen. ❖ Bei Tropffrequenzen von über 6-mal täglich sollte man ein konservierungsmittelfreies Tränenersatzpräparat verordnen. ursache ein grosses Problem eben dieser Länder dar (2). Die Inzidenz einer altersbedingten Linsentrübung in einer Population (USA) im Alter von 43 bis 86 Jahren beträgt innert 10 Jahren 54 Prozent (3). Die Sehverschlechterung entwickelt sich schmerzlos und langsam progredient. Typische Symptome sind: ❖ Blendempfindlichkeit ❖ zunehmende Kurzsichtigkeit ❖ trübe, nebelartige Sehverschlechterung (Abbildung 1). Pathogenese und Risikofaktoren: Die Ursache der altersbedingten Katarakte ist bis heute noch nicht vollständig geklärt – möglicherweise sind oxidative Schäden der Linsenproteine ursächlich beteiligt (4). Die wichtigsten Risikofaktoren sind Alter, Genetik, Rauchen, Sonnenlichtexposition, Diabetes und Kortisontherapien. Abgesehen von der Meidung änderbarer Risikofaktoren gibt es keine bekannten Präventivmassnahmen (5). Diagnose: Neben der Anamnese kann auch ohne Spaltlampe eine Untersuchung mit einem direkten Ophthalmoskop Hinweis auf das Vorhandensein einer Katarakt geben. Therapie: Die einzige Therapie einer Katarakt besteht in einer mikrochirurgischen Operation. Das Auge wird durch einen 2,5 mm breiten Hornhautschnitt eröffnet. Da die Hornhaut avaskulär ist, besteht nur ein sehr geringes Blutungsrisiko. Die getrübte Linse wird durch diesen Schnitt aus dem Kapselsack entfernt, und es wird eine Kunstlinse implantiert. Diese verbleibt ein Leben lang im Auge. Bei 20 Prozent der Patienten entwickelt sich im weiteren Verlauf eine Trübung der Linsenkapsel – ein sogenannter «Nachstar». Der zentrale Teil der getrübten Linsenkapsel kann relativ einfach mit einem Lasereingriff entfernt und der Visus wiederhergestellt werden (6). Altersbedingte Makuladegeneration Die altersbedingte Makuladegeneration (AMD) ist die häufigste Erblindungsursache bei über 50-Jährigen in den industrialisierten Ländern (7). Man versteht darunter eine chronisch degenerative Erkrankung der zentralen Netzhaut. Unterschieden wird eine trockene von einer feuchten Form. Bei der trockenen AMD atrophiert die zentrale Netzhaut langsam progredient (über Monate bis Jahre). Als Folge des Verlusts zentraler Fotorezeptoren nehmen die Patienten einen dunklen Fleck in der Mitte des Gesichtsfeldes wahr (Zentralskotom). Objekte werden erst wahrgenommen, wenn die Patienten daran «vorbeischauen», anstatt direkt daraufzublicken (Abbildung 2). ARS MEDICI 17 ■ 2014 851 FORTBILDUNG Abbildung 1: Katarakt: links normaler, rechts veränderter Seheindruck Abbildung 2: Trockene AMD: links normaler, rechts veränderter Seheindruck Abbildung 3: Feuchte AMD: Amslernetz, links normaler, rechts veränderter Seheindruck Bei der feuchten AMD kommt es zum Einwachsen neuer Gefässe (Neovaskularisation). Diese Gefässe sind jedoch von minderer Qualität: Flüssigkeit und Blut treten aus – es kommt relativ rasch zu einer Verwerfung der Netzhaut. Typischerweise nehmen Patienten dadurch gerade Linien als verzogen wahr (Metamorphopsien; Abbildung 3). Unbehandelt ist eine irreversible Schädigung der Netzhaut durch eine Narbenbildung die Folge (8). Die genaue Pathogenese der AMD ist noch nicht vollständig geklärt. In Diskussion sind eine Änderung der Stoffwechsellage, Zellapoptose durch Entzündungen oder Alterungsprozesse beziehungsweise genetische Alterationen (9–11). Bei der feuchten Form ist zumindest die molekulare Pathogenese bekannt: Ein Überschuss an Gefässwachstumsfaktoren (v.a. Vascular Endothelial Growth Factor, VEGF) führt zu einer Neovaskularisation. Neben Alter und genetischen Faktoren ist das Rauchen als wichtigster änderbarer Risikofaktor identifiziert worden (12). Diagnose: Meist ist die Anamnese bereits hinweisend. Die endgültige Diagnose kann durch eine genaue Fundusuntersuchung, gegebenenfalls in Verbindung mit einer Angiografie und einer Schichtaufnahme der Netzhaut (optische Kohärenztomografie, OCT), gestellt werden (8). Therapie der feuchten AMD: Eine intravitreale (= in den hinteren Augenabschnitt) Injektion von Anti-VEGF dichtet die 852 ARS MEDICI 17 ■ 2014 Neovaskularisationen ab. Da die Makuladegeneration eine chronische Erkrankung ist, sind häufig lebenslang Injektionen notwendig (13). Therapie der trockenen AMD: In der Age-Related Eye Disease Study (AREDS) untersuchte man die Wirkung antioxidativer Vitamine und Zink (500 mg Vitamin C, 400 IE Vitamin E, 15 mg Betacarotin, 80 mg Zink und 2 mg Kupfer) auf den Verlauf einer AMD. Bei Patienten mit einer fortgeschrittenen trockenen AMD konnte das Risiko, eine feuchte Form zu entwickeln, durch Einnahme dieser Substanzen reduziert werden (14, 15). Aufgrund der statistischen Auswertung sind diese Ergebnisse jedoch nicht unumstritten. Cave: Raucher und ehemalige Raucher müssen bedenken, dass Betacarotin ihr Risiko, ein Lungenkarzinom zu entwickeln, vermutlich erhöht (16). Allgemeinmassnahmen: Einige Patienten mit fortgeschrittener AMD profitieren von vergrössernden Sehhilfen (7, 8). Das sogenannte Amslernetz kann auch dazu dienen, Patienten eine Selbstkontrolle zu ermöglichen. Es besteht aus einem Netz mit einem mittig gelegenen Fixierpunkt. Werden bei Blick auf dieses Netz neue oder vermehrte Verwerfungen der Linien wahrgenommen, ist dies ein Hinweis auf eine Krankheitsprogression (Abbildung 2) – eine augenärztliche Vorstellung sollte baldig erfolgen (17). Der grüne Star – Glaukom Der Begriff Glaukom bezeichnet eine Gruppe von Erkrankungen, welchen ein progredienter Verlust retinaler Nervenfasern gemeinsam ist – am häufigsten ist das sogenannte primäre Offenwinkelglaukom (POWG). Im Erkrankungsverlauf entwickeln sich charakteristische Gesichtsfeldausfälle, welche bis zur Erblindung führen können (18). Es ist die zweithäufigste Erblindungsursache weltweit. 2010 waren 44,7 Mio. Menschen am POWG erkrankt, laut Schätzungen soll diese Zahl bis im Jahr 2020 auf 58,6 Mio. Menschen ansteigen (19). Die Prävalenz ist stark altersabhängig. Im Alter unter 55 Jahren beträgt diese 1 Prozent und steigt von 2 Prozent bei unter 65-Jährigen auf 4 Prozent bei unter 80-Jährigen an (20). Patienten mit einem Glaukom bemerken Symptome erst in fortgeschrittenen Stadien. Das Gehirn ergänzt in frühen Stadien fehlende Gesichtsfeldanteile. Im Gegensatz zum akuten Glaukomanfall bestehen keine Schmerzen. Pathogenese und Risikofaktoren: Die Pathogenese des Nervenfaserverlustes ist noch nicht vollständig geklärt. Vermutet wird eine Störung der Mikrozirkulation am Sehnervenkopf (13). Bekannte Risikofaktoren sind erhöhter Augendruck, ein niedriger Blutdruck, genetische Faktoren, ein RaynaudSyndrom, hohe Kurzsichtigkeit und ein hohes Lebensalter (18, 21). Diagnose: Da die Patienten Symptome dieser Erkrankung erst sehr spät bemerken, wird ein Glaukomscreening ab dem 40. Lebensjahr empfohlen. Weitere Untersuchungen sollten in einem Intervall von 1 bis 3 Jahren (abhängig von Risikofaktoren) stattfinden (22). Obwohl der Augendruck einen wichtigen Risikofaktor für das Glaukom darstellt, kann eine alleinige Augendruckmessung ein Glaukom weder ausschliessen noch den Verlauf beurteilen. Würde man nur den Augendruck messen, könnte man 50 Prozent aller Glaukome nicht diagnostizieren (23). FORTBILDUNG Um die Diagnose zu stellen beziehungsweise den Verlauf zu beurteilen, sind neben einer Augendruckmessung eine Funduskopie und gegebenenfalls eine Gesichtsfelduntersuchung notwendig. Weitere Risikofaktoren sind nächtliche Hypotonien und ein Schlafapnoesyndrom (8, 21, 24). Therapie: Die Therapie eines Glaukoms besteht in der Augendrucksenkung. Die Therapieoptionen umfassen eine medikamentöse Drucksenkung, eine Laserbehandlung im Kammerwinkel oder einen mikrochirurgischen Eingriff. Auch eine Optimierung der Blutdruckmedikation (abendliche Einnahme könnte zu nächtlichen Hypotonien führen) oder die Behandlung eines Schlafapnoesyndroms wirken sich bei einigen Patienten positiv auf den Krankheitsverlauf aus. Ziel der Therapie ist es, den Fortschritt dieser Erkrankung zu verhindern, denn ein glaukomatöser Schaden ist irreversibel (8, 21). Der weitere Krankheitsverlauf wird folgendermassen kontrolliert (22): ❖ 3-monatliche Augendruckmessungen mit Fundusuntersuchung, ❖ halbjährliche Gesichtsfelduntersuchungen und ❖ jährliche apparative Vermessung der Papille. Das trockene Auge – Conjunctivitis sicca Eine der häufigsten Augenbeschwerden sind trockene Augen: Bis zu 30 Prozent der über 50-Jährigen (25, 26) leiden unter dadurch bedingten Beschwerden. Patienten klagen häufig über Brennen, Kratzen, Fremdkörpergefühl, Tränen oder Rötung der Augen (27). Oftmals werden auch Sehbeschwerden angegeben, welche sich in ihrer Ausprägung durch wiederholten Lidschluss ändern. Pathogenese: Trockene Augen haben eine multifaktorielle Ätiologie. Risikofaktoren sind vor allem Alter, weibliches Geschlecht und hormonelle Umstellungsphasen. Beim trockenen Auge kommt es zu einer ungenügenden Tränenbenetzung des Auges. Ursächlich reicht entweder die Produktion der Tränenflüssigkeit nicht aus, oder aber eine veränderte Tränenfilmzusammensetzung führt zu einer vermehrten Evaporation beziehungsweise Tränenfilminstabilität. Ist Letzteres der Fall, kann die Tränenflüssigkeit nicht mehr am Auge gehalten werden – paradoxerweise hat der Patient trockene Augen, obwohl er über Tränen der Augen klagt. Therapie: Zur Behandlung des trockenen Auges steht mittlerweile eine breite Palette an Tränenersatzmitteln zur Verfügung. Eine Therapie könnte beispielsweise mit 3-mal täglich einem Tropfen begonnen werden. Bemerkt der Patient in den folgenden Tagen keine Besserung, kann die Tropffrequenz auf bis zu stündlich gesteigert werden (25, 28). Bei Tropffrequenzen von über 6-mal pro Tag ist wegen der dosisabhängigen zytotoxischen Wirkung von Konservierungsmitteln auf eine konservierungsmittelfreie Rezeptur zurückzugreifen (29). Differenzialdiagnosen: Vor Therapiebeginn sollten Erkrankungen wie Lidfehlstellungen, okuläre Infektionen oder Fremdkörper ausgeschlossen werden. Stellt sich trotz Therapie keine ausreichende Besserung ein, empfiehlt sich die Weiterleitung an den Augenarzt zum Ausschluss anderer Ursachen. ❖ 854 ARS MEDICI 17 ■ 2014 Korrespondenzadressen: Dr. med. Univ. Christoph Schwab Univ.-Prof. Dr. med. univ. Andreas Wedrich Universitäts-Augenklinik Graz Auenbruggerplatz 4 A-8036 Graz E-Mail: [email protected] [email protected] Interessenkonflikte: keine deklariert Diese Arbeit erschien zuerst in «Der Allgemeinarzt» 11/2014. Die Übernahme erfolgt mit freundlicher Genehmigung von Verlag und Autoren. Literatur: 1. Thylefors B et al.: Global data on blindness. Bull World Health Organ 1995; 73: 115. 2. Asbell PA et al.: Age-related cataract. Lancet 2005; 365: 599. 3. Klein BE et al.: Incidence of age-related cataract over a 10-year interval: the Beaver Dam Eye Study. Ophthalmology 2002; 109 (11): 2052–2057. 4. Vinson JA: Oxidative stress in cataracts. Pathophysiology 2006; 13(3): 151–162. 5. West SK, Valmadrid CT: Epidemiology of risk factors for age-related cataract. Surv Ophthalmol 1995; 39(4): 323–334. 6. Cheng JW et al.: Efficacy of different intraocular lens materials and optic edge designs in preventing posterior capsular opacification: a meta-analysis. Am J Ophthalmol 2007; 143(3): 428–436. 7. Jager RD et al.: Age-related macular degeneration. N Engl J Med 2008; 358(24): 2606–2617. 8. Kanski JJ: Klinische Ophthalmologie. Elsevier, Urban & Fischer, 2005. 9. Friedman E et al.: Ocular blood flow velocity in age-related macular degeneration. Ophthalmology 1995; 102(4): 640–646. 10. Yang Z et al.: Toll-like receptor 3 and geographic atrophy in age-related macular degeneration. N Engl J Med 2008; 359(14): 1456–1463. 11. Zarbin MA: Age-related macular degeneration: review of pathogenesis. Eur J Ophthalmol 1998; 199–206. 12. Hyman L, Neborsky R: Risk factors for age-related macular degeneration: an update. Curr Opin Ophthalmol 2002; 13(3): 171–175. 13. Ferrara N et al.: Development of ranibizumab, an anti-vascular endothelial growth factor antigen binding fragment, as therapy for neovascular age-related macular degeneration. Retina 2006; 26(8): 859–870. 14. AREDS Report No. 11. Arch Ophthalmol 2003; 121(11): 1621–1624. 15. Tan JS et al.: Dietary antioxidants and the long-term incidence of age-related macular degeneration: the Blue Mountains Eye Study. Ophthalmology 2008; 115(2): 334–341. 16. AREDS Report No. 8. Arch Ophthalmol 2001; 119(10): 1417–1436. 17. Amsler M: Die Untersuchung des qualitativen Sehens mit dem quadratischen Netz. Anweisung zum Gebrauch der Test-Tafeln. Theodore Hamblin LTD, London 1958. 18. Weinreb RN, Khaw PT: Primary open-angle glaucoma. Lancet 2004; 363: 1711–1720. 19. Kingman S: Glaucoma is second leading cause of blindness globally. Bull World Health Organ 2004; 82(11): 887–888. 20. Friedman DS et al.: Eye Diseases Prevalence Research Group. Prevalence of openangle glaucoma among adults in the United States. Arch Ophthalmol 2004; 122(4): 532–538. 21. Kwon YH et al.: Primary open-angle glaucoma. N Engl J Med 2009; 360 (11): 1113–1124. 22. AAO PPP Glaucoma Panel, Hoskins Center for Quality Eye Care: Primary Open-Angle Glaucoma Suspect PPP 2010. http://one.aao.org/preferred-practice-pattern/primaryopenangle-glaucoma-suspect-ppp-october-20. 23. Leske MC: The epidemiology of open-angle glaucoma: a review. Am J Epidemiol 1983; 118(2): 166–191. 24. Omoti AE et al.: Current concepts in the diagnosis of primary open angle glaucoma. West Afr J Med 2009; 28(3): 141–147. 25. Moss SE et al.: Prevalence of and risk factors for dry eye syndrome. Arch Ophthalmol 2000; 118: 1264. 26. Santaella RM, Fraunfelder FW: Ocular adverse effects associated with systemic medications: recognition and management. Drugs 2007; 67: 75. 27. Gilbard JP: The diagnosis and management of dry eyes. Otolaryngol Clin North Am 2005; 38: 871. 28. Drugs for some common eye disorders. Treat Guidel Med Lett 2010; 8: 1. 29. Management and therapy of dry eye disease: report of the Management and Therapy Subcommittee of the International Dry Eye WorkShop 2007; 5: 163.