Schilddrüse, Kalziumhomöostase
Werbung
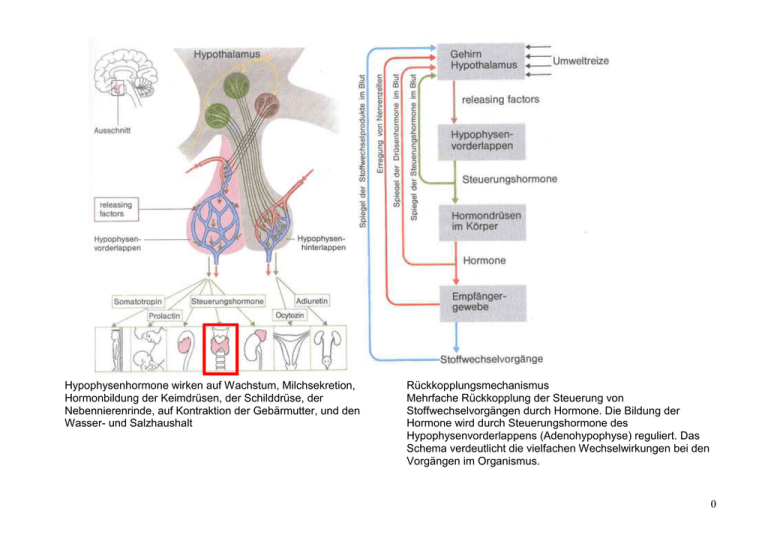
Hypophysenhormone wirken auf Wachstum, Milchsekretion, Hormonbildung der Keimdrüsen, der Schilddrüse, der Nebennierenrinde, auf Kontraktion der Gebärmutter, und den Wasser- und Salzhaushalt Rückkopplungsmechanismus Mehrfache Rückkopplung der Steuerung von Stoffwechselvorgängen durch Hormone. Die Bildung der Hormone wird durch Steuerungshormone des Hypophysenvorderlappens (Adenohypophyse) reguliert. Das Schema verdeutlicht die vielfachen Wechselwirkungen bei den Vorgängen im Organismus. 0 A. Schilddrüse (glandula thyroidea) Hypothalamisches Freisetzungs-Hormon: TRH (=Thyreotropin-RH =Thyreoliberin) stimuliert die Abgabe von TSH (Tripeptid) Hypophysäres Hormon: TSH=Thyreoide-astimulierendes Hormon=Thyreotropin (Glycoprotein) Aufgabe der Schilddrüse: normale Entwicklung des ZNS, metabolische Homöostase Hormone der Schilddrüse - Iodstoffwechsel: Thyroxin T4, Triiodthyronin T3 Calciumstoffwechsel: Calcitonin, Parathormon Follikel (50-500µm): Bildung der Schilddrüsenhormone T3 und T4, Speicherung in Kolloid der Follikel T4(Thyroxin), T3(Triiodthyronin): wichtig für Wachstum, Reifung und Stoffwechsel C-Zellen=parafollikuläre Zellen: Bildung von Calcitonin (Kontrolle der Plasmacalciumkonzentration siehe unten) Struktureller Feinbau der Schilddrüse Nebenschilddrüse (glandula parathyreoidea) Produktion von Parathormon (Kontrolle der Plasmacalciumkonzentration siehe unten) 1 A.1. Synthese und Wirkungsweise der Schilddrüsenhormone T3, T4 ClO4- 2 A.2. Schilddrüsenerkrankungen A.2.1. Euthyreote Struma (Iodmangelstruma) Mitteleuropa 30% der Bevölkerung Bei vermindertem Iodidspiegel und sinkender T3/T4-Konzentration im Blut verminderte negative RückkopplungTSHgesteigerte Aktivität der Schilddrüse und Zellvermehrung bessere Verwertung des Iod aber - - - Iodmangelstruma mit Euthyreose (kann operationsbedürftige Größe erreichen) Während Schwangerschaft bleibende Schäden beim Kind (Kretinismus) Bildung autonomer Adenome Prophylaxe: Zufuhr von Iodsalzen, Ernährung (Seefisch, Meerestiere) (tägl. Iodbedarf: Erwachsene/Kinder 200/50-100 µg/Tag) Therapie: Iodsalze T3, T4: Ruhigstellung der Schilddrüse Kombinationtherapie 30% Reduktion, keine Normalisierung der Schilddrüsengröße Thyreoidektomie 3 A.2.2. Hyperthyreose Überfunktion der Schilddrüse Steigerung von schilddrüsenhormonabhängigen biologischen Prozessen Anzeichen einer Überfunktion: Allgemeine Unruhe, Herzklopfen, Gewichtsverlust, Schlaflosigkeit, starkes Schwitzen, Haarausfall, Gesteigerte Stuhlfrequenz, Tremor, Muskelschwäche Immunhyperthyreose Basedow-Krankheit (Morbus Basedow) Autoimmunerkrankung: IgG Antikörper mit TSH artiger Wirkung TSH-Rezeptor-Antikörper (TRAK) stimulieren Schilddrüse abnormalT3, T4 steigen Hypophyse setzt kein TSH mehr frei Schildrüsenautonomie (Autonomes Adenom) Gewebsareale mit autonomer Hormonproduktion, die nicht mehr der Kontrolle hypophysären Regelkreises unterliegenunkontrollierte HormonproduktionHyperthyreose A.2.3. Hypothyreose Unterfunktion der Schilddrüse biologische Prozesse verlangsamt (geringer Fett- und Eiweißstoffwechsel) unzureichende Versorgung der Körperzellen mit Schilddrüsenhormonen Anzeichen einer Unterfunktion: Antriebsarmut, Konzentrationschwäche, Kälteempfindlichkeit, Brüchige Fingernägel, Sprödes Haar, Verstopfung, Rheumatische Gliederschmerzen, Schwerhörigkeit, Potenz- Libidoverlust (Kretinismus) Neugeborenenhypothyreose (angeboren): Fehlanlage der Schilddrüse, Neugeborene 1:4000TSH-Screening am 5. Lebenstag Postnatal erworbene Hypothyreose: Zerstörung von Schilddrüsengewebe z.B. Folge von Thyreoditis, Strahlentherapie, Medikamenten 4 A.3. Therapie A.3.1. Iod-Ionen Iodid (z.B. Jodetten®, Strumex®) Orale Zufuhr, schnelle, vollständige Resorption im Dünndarm, Ausscheidung im Harn Anwendung: -in Iodmangelgebieten Prophylaxe Iodmangelstruma -Vorsicht: Dosis > 5mg/Tag Kropfbildung, Wachstumshemmung bei Kindern -bei Hyperthyreose in hohen Dosen T3, T4 -Freisetzung Nebenwirkungen: Reizwirkungen an Haut und Schleimhaut (Iodismus, Iodschnupfen) A.3.2. Schilddrüsenhormone T3, T4 T4, L-Thyroxin, Levothyroxin, im Körper entsteht Wirkform T3 T3Triiodthyronin T3 aktiviert T3- Rezeptor (Transkriptionsfaktor) Regulation der Genexpression Anwendung: - Hypothyreose Dosis je nach Grad der Schilddrüsenrestfunktion (T4) - in akuten Fällen T3, zeigt schnelleren Wirkungseintritt - Euthyreote Struma, TSH Suppressionstherapie Nebenwirkungen: bei zu hoher exogener Zufuhr Symptome der Hyperthyreose 5 A.3.3. Hemmung der Hormonbildung in der Schilddrüse Jodid und Lithium- Ionen Wirkung: vorübergehende Hemmung der T3, T4 –Freisetzung Anwendung: - Iodid vor OP in hohen Dosen - Lithium bei Iodinduzierter Hyperthyreose, Psychosen, Manien Radioakties Iod (131I) Speicherung in Schilddrüse zerstört Schilddrüsengewebe durch ßStrahlung, T1/2 = 8 Tage, Alternative zur Röntgenbestrahlung Anwendung: bei inoperablen Tumoren z.B. bei älteren Menschen Nebenwirkung: wie bei Röntgenbestrahlung, Zerstörung von gesundem Gewebe Jodinationshemmer: Perchlorat (ClO4-) Wirkung: kompetetive Inhibition der Iodid-Aufnahme in die Schilddrüse Anwendung: nur bei Versagen anderer Mittel Nebenwirkung: Magen-, Darmstörungen, Anämien 6 Jodisationshemmer: Schwefelhaltige Thyreostatika Propylthiouracil, Methimazol, Carbimazol Wirkung: - Thioharnstoffhaltige Ringstruktur - konkurrieren mit Iod um thyreoidale Peroxidase (reversibel) - Propylthiouracil hemmt zusätzlich Umwandlung von T4 zu T3 Anwendung: - Hyperthyreose 131 - vor und nach Behandlung mit J Nebenwirkung: dosisabhängig, Übelkeit, Geruchsstörungen, Leukopenie, Allergie (ß-Blocker) mildern Symptome der Hyperthyreose Anwendung: Ergänzung zur thyreostatischen Therapie 7 B. Calcium -2% des Körpergewichts -99% des Calcium in Knochengewebe als Hydroxylapatit deponiert, 1% gelöst -extrazelluläres Calcium (mM): ca. 50% ionisiertes Calcium, 50% proteingebunden wichtig für Blutgerinnung, Knochenbildung, Nerven- und Muskelerregbarkeit -intrazelluläres Calcium (µM): Anstieg von Calcium in der Zelle bewirkt u.a. Muskelzellkontraktion, Exozytose von Neurotransmittern und Hormonen Ca2+- und Phosphatstoffwechsel werden durch Parathormon (PTH, Parathyrin), Vitamin D Hormon (Calcitriol) und Calcitonin geregelt, sie wirken v.a. im Darm, Knochen und in der Niere Weitgehend unabhängig von Hypothalamus/Hypophysenachse Präparate: Calciumsalze z.B. Calciumgluconat Enterale Resorption 20% der verabreichten Dosis i.v. Injektion (10%) langsam, sonst Beeinträchtigung Herzfunktion; nach hohen Dosen Gefahr der Hypercalciämie Anwendung: bei Hypokalzämie, Osteoporose, Vit-D Mangel, Schwangerschaft, Laktation 8 B.1. Wirkstoffe zur Erhaltung der CalciumHomöostase B.1.1. Calcitonin Erniedrigung der Calciumkonzentration im Blut Peptidhormon mit 32 AS, gebildet in C-Zellen der Schilddrüse -Ausschüttung bei Ca++ (Hypercalciämie) - Osteoklastentätigkeit Ca++Mobilisierung aus Knochen Anwendung: Hypercalciämie, Osteoporose (Nasenspray) Nebenwirkungen: Erbrechen, gastrointestinale Beschwerden, Flush B.1.2. Parathormon (Parathyrin, PTH) Erhöhung der Calcium-Konzentration im Blut - Peptidhormon mit 84 AS, gebildet in Nebenschilddrüse - Ausschüttung bei Ca++ (Ca++-Sensoren) - Osteoklastentätigkeit Ca++Mobilisierung aus Knochen - Rückresorption aus Nierentubuli - Anregung der Bildung von Vitamin-D-Hormon in der Niere durch Aktivierung der 1-Hydroxylase Calcium-Konzentration Phosphat-Konzentration im Blut 9 B.1.3. Vitamin-D-Hormon (Calcitriol, 1,25Dihydroxycholecalciferol) Erhöhung der Calcium-Konzentration im Blut Lipophiles, steroidähnliches Hormon, entsteht aus Vitamin D3 (Cholecalciferol) Letzter Syntheseschritt in Niere: 1-Hydroxylase - Ca++ und Parathormon stimulieren Synthese - Aktivierung von Vit D-Rezeptor (Transkriptionsfaktor) Regulation der Genexpression - Resorption von Ca++ aus Darm - Rückresorption von Ca++ aus Niere - Osteoklastenakt. Ca++Mobilisierung Anwendung: Hypocalciämie, Vit. DMangelkrankheiten (z.B. Rachitis) Calcitriol oder Vorstufen B.2. 10 B.2. Therapie B.2.1. Hypercalciämie Hemmung der Osteoklastentätigkeit Calcitonin: Wirkung kann im Laufe einiger Tage abnehmen Biphosphonate (Etidronsäure, Alendronsäure): evtl. Minderung der Abbaubarkeit der Hydroxylapatit-Kristalle Anwendung: auch bei Osteoporose und Knochenmetastasen Akute „Entfernung“ freier Calciumionen - Komplexierung (z.B. EDTA, Citrat) - Diurese (z.B. Furosemid) - Dialyse B.2.2. Hypocalciämie - Substitution von Calcium (z.B. Calciumgluconat, Diät?) - Vitamin-D Derivate 11 Osteoporose generalisierte Erkrankung des Knochens, Aktivität Osteoklasten > Osteoblasten, Abnahme der Knochenmasse, Verschlechterung der Mikroarchitektur des Knochens, erhöhtes Frakturrisiko Ursachen: Menopause (85% aller Osteoporosen sind in postmenopausal), senile Osteoporose, endokrine Erkrankung (Morbus Cushing, Hyperthyreose, Hyperparathyreodismus) Prophylaxe: Risikofaktoren senken, körperliche Aktivität ausreichende Zufuhr Calcium: 1g/Tag Hormonbehandlung: Estrogen-Behandlung (Ethinylestradiol) Knochenabbau, Frakturneigung + Gestagene (verhindern Endometriumkarzinom !) 10 Jahre hormonellen Zyklus aufrechterhalten bei Abruch Hormongabe aber: dann rascher Knochenabbau! besser bis ins hohe Senium! Therapie der manifesten Osteoporose: Ziel: Erhöhen der Knochenmasse, verhindern von Wirbelfraktionen wichtigste pharmakologische Maßnahme: Vitamin D und Calcium: <50 Jahre 400 IU Vit D/1000mg Ca >50 Jahre 800 IU Vit D/1200mg Ca Alle folgenden nicht überzeugend wirksam: Fluorid: anstelle von OH-Gruppe in Apatit eingebaut, Zunahme an Knochenmasse, aber: Frakturhäufigkeit hoch, „spröde“ Knochen Biphosphonate Prävention 5mg /d Alendronsäure oder 5mg Risedronsäure Behandlung 10 mg/d Alendronsäure oder 5 mg RisedronsäureRaloxifen: Selektiver Östrogen Rezeptor Modulator (SERM) Calcitonin (Nasenspray): wirkt analgetisch bei Knochenschmerzen, erhöht Knochenmasse, Abnahme Frakturhäufigkeit Parathormon: in Kombination mit Sexualhormonen gute Ergebnisse Ganzkörperknochendichte, Zunahme um 8% Am besten Alendronat, Risedronat und Raloxifen neben Vit D und Calcium Wichtig: physikalische und orthopädische Verfahren 12 Take Home Message Schilddrüsenhormone T3, T4, Bildung, Transkriptionsfaktoren, Regelkreislauf Euthyreose, Hyper-, Hypothyreose Angriffspunkte für Pharmaka Iodid, Schilddrüsenhormone, Thyreostatika Calciumhomöostase Calciumstoffwechsel Abfall der Calciumkonzentration Anstieg der Calciumkonzentration Freisetzung von PTH aus Parathyroid Umwandlung von Calciferol in Calcitriol Verringerte Sekretion von Ca aus Niere Erhöhte Ca-Absorbtion in Dünndarm Calcitonin Mobilisation von Ca aus Knochen Hormone: PTH, Vitamin D Hormon, Calcitonin, Wirkung Hyper-, Hypocalciämie Angriffspunkte für Pharmaka Senken des Serumcalciums (Osteoklasten-Hemmstoffe, Calcium-Komplexbildner) Erhöhen der Calciumausscheidung (0,9% NaCl- Lösung, Furosemid) 13 Schilddrüsenhormone und Calciumhomöostase A. Schilddrüse (glandula thyroidea) A.1. Synthese und Wirkungsweise der Schilddrüsenhormone T3, T4 A.2. Schilddrüsenerkrankungen A.2.1. Euthyreote Struma (Iodmangelstruma) A.2.2. Hyperthyreose A.2.3. Hypothyreose A.3. Therapie A.3.1. Iod-Ionen A.3.2. Schilddrüsenhormone T3, T4 A.3.3. Hemmung der Hormonbildung in der Schilddrüse B. Calcium B.1. Wirkstoffe zur Erhaltung der Calcium-Homöostase B.1.1. Calcitonin B.1.2. Parathormon (Parathyrin, PTH) B.1.3. Vitamin-D-Hormon (Calcitriol, 1,25Dihydroxycholecalciferol) B.2. Therapie B.2.1. Hypercalciämie B.2.2. Hypocalciämie 14