Kap5+6_Kokristalle
Werbung

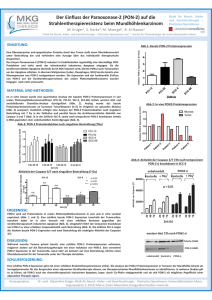
Phenazin und meso-1,2-Diphenyl-1,2-ethandiol 5 17 Kokristalle aus Phenazin und substituierten meso-1,2Ethandiolen 5.1 Phenazin und meso-1,2-Diphenyl-1,2-ethandiol[36] Phenazin (5,10-Diazaanthracen) wurde in die Versuche der Kokristallisation einbezogen, da es ein aromatisches, heterocyclisches "Bisimin" ist, in dem die Anordnung des "Bisimin-Strukturelements" synperiplanar fixiert ist. Auch ist der N,N-Abstand mit 281.7 pm deutlich kürzer, als der der substituierten N,N´-Bis(benzyliden)ethyendiamine und der 1,4-Diaza-1,3-butadiene, die im Bereich von 350-371 pm und 347–351 pm liegen. Es stellte sich somit die Frage, ob auch mit Phenazin das beschriebene treppenartige, polymere Aufbauprinzip mit meso-1,2-Diphenyl-1,2-ethandiol verwirklicht werden kann.[17-20] Die Darstellung des 1 : 1-Kokristalls erfolgt durch Lösen von äquimolaren Stoffmengen des Diols und des Phenazins in Essigsäureethylester und anschließendem Verdampfen des Lösungsmittels unter Lichtausschluß. Der Kokristall kann auch durch Zusammenschmelzen oder starkes Verreiben dargestellt werden. Nachgewiesen wurde dies nicht nur durch die beim Kokristall auftretende Änderung des Schmelzpunktes, sondern auch durch die Verschiebung der Banden der OH-Valenzschwingung im IR-Spektrum. Die bei der ersten Kristallisation an Tageslicht erhaltenen Kokristalle waren unerwarteterweise violett gefärbt, denn Phenazin ist gelb und meso-1,2Diphenyl-1,2-ethandiol ist farblos. Mit Hilfe der ESR-Spektroskopie wurde Paramagnetismus durchgeführte festgestellt. Kristallisation Die führte daraufhin zu unter gelben, Lichtausschluß transparenten, diamagnetischen Kristallen, deren Schmelzpunkt mit 121 °C niedriger als der der Edukte ist. 18 Kapitel 5.1 Die Röntgenstrukturanalyse bestätigte die Bildung des Kokristalls (Abb. 5.1.1). Seine Raumgruppe ist P 1 , d.h. das Kristallgitter ist zentrosymmetrisch. Abb. 5.1.1: Ausschnitt aus der Struktur des Kokristalls aus Phenazin und meso-1,2Diphenyl-1,2-ethandiol. Die treppenartigen Ketten aus Phenazin und meso-1,2-Diphenyl-1,2-ethandiol werden durch H-Brücken (Abb. 5.1.1/5.1.2) mit einem ON-Abstand von 285.0 pm verknüpft ( = 167.2°). Attraktive Csp2-H-Kontakte werden durch die in einem Winkel von 63.4° zu den Phenazinmolekülen stehenden Phenylgruppen der Diole ermöglicht. Innerhalb der Ketten wird ein Csp2-H-Kontakt zwischen einem Wasserstoffatom des Phenazins und einem Phenylring des Diols ausgebildet, der Csp2-H-Abstand zum Zentrum beträgt 280.3 pm ( = 136.4°; Abb. 5.1.1). Die Ketten selbst sind übereinander gestapelt (Abb. 5.1.2). Es wird keine reine edge-to-face-Stapelung zwischen den Phenylringen des Diols und dem aromatischen System des Phenazins, sondern eher eine Csp2-HC=CWechselwirkung ausgebildet. So ist der Abstand des Wasserstoffatoms des Phenazin und meso-1,2-Diphenyl-1,2-ethandiol 19 Diols zum Mittelpunkt eines darunter- und darüberliegenden C=C-Fragmentes der Phenazinmoleküle 280.1 pm lang ( = 153.8°), wohingegen der Abstand dieses Wasserstoffatoms zum Zentrum des entsprechenden Phenylrings mit 293.6 pm länger ist ( = 126.6°). Abb. 5.1.2: Anordnung der Ketten im Kokristall aus Phenazin und meso-1,2-Diphenyl1,2-ethandiol und die zwischen ihnen auftretenden Wechselwirkungen. Die Phenazinmoleküle sind innerhalb der Stapel gegeneinander parallel entlang der kurzen Molekülachse verschoben, d.h. sie bilden eine offset faceto-face-Stapelung aus, so daß nur eine geringe Überlappung der -Systeme benachbarter Heteroaromaten vorhanden ist (Abb. 5.1.2). Der Abstand der Pyrazin-Centroide beträgt 566 pm und der Ebenenabstand der Phenazinmoleküle ist 309 pm. Diese bevorzugte Anordnung von -Systemen vermindert die repulsiven Wechselwirkungen der -Elektronen und ermöglicht andererseits attraktive Wechselwirkungen zwischen dem positiv polarisierten -Gerüst und den Elektronen.[37] 20 Kapitel 5.1 Zum Vergleich zeigt die Abbildung 5.1.3 die Kristallstruktur des Phenazins, das im Fischgrätenmuster kristallisiert.[38] Die benachbarten Phenazinmoleküle sind entlang ihrer Längsachse um etwa einen Phenylring gegeneinander verschoben, so daß auch hier die sogenannte offset face-to-face-Stapelung verwirklicht wird. Der Abstand der Pyrazin-Centroide innerhalb eines Stapels beträgt 508 pm, während der Abstand der Ebenen mit 349 pm etwa der Summe der van-der-Waals-Radien der Kohlenstoffatome entspricht. Abb. 5.1.3: Ausschnitt aus der Kristallstruktur des -Phenazins. Durch die Beteiligung der Stickstoffatome des zentralen Pyrazinrings an der HBrücke im Kokristall wird die Länge der C-N-Bindungen nicht verändert. Eine geringfügige Aufweitung erfährt nur der entsprechende Winkel der Imineinheit des Phenazins (Tabelle 5.1.1). Tabelle 5.1.1: Vergleich der Bindungslängen [pm] und Winkel [°] des Kokristalls aus Phenazin und meso-1,2-Diphenyl-1,2-ethandiol Einzelkomponenten. mit den Literaturwerten der Phenazin und meso-1,2-Diphenyl-1,2-ethandiol Kokristall Einzelkomponenten C-O 142.3 142.9[39] C=N–C 134.1/134.2 134.2(1), 134.1(1) 21 bzw. 133.9(2), 134.2(2)[38] C=N–C 117.5° 116.72(7)° bzw. 116.79(10)° Mit der Bildung des Kokristalls treten Änderungen in den IR-Teilspektren auf. So liegt die Bande der OH-Valenzschwingung im Kokristall bei 3256 cm-1 . Bei 3378 cm-1 ist eine schmale Schulter zu erkennen (Abb. 5.1.4). Im Spektrum des Diols ist bei 3371 und 3321 cm-1 eine Doppelbande zu sehen. Sie wird durch die beiden auftretenden H-Brücken im Festkörper des meso-Diols hervorgerufen.[39] Das reine meso-Diol bildet unendliche über H-Brücken verknüpfte Ketten, die über eine weitere H-Brücke mit der Nachbarkette verbunden sind. Im Kokristall aus Phenazin und meso-1,2-Diphenyl-1,2-ethandiol wird nur ein Typ von H-Brücken ausgebildet, so daß nur eine OH-Valenzschwingung beobachtet wird. Eine geringfügige Verschiebung zu kleineren Wellenzahlen erfährt die Bande der Csp3-HValenzschwingung des Diols, sie ist um 17 cm-1 auf 2872 cm-1 erniedrigt. Trans. 80 100 Trans. 80 60 60 40 40 20 20 1600 3500 3000 1400 1200 1000 800 [cm -1] 2500 [cm -1] Abb. 5.1.4: IR-Spektren: — Kokristall, — meso-1,2-Diphenyl-1,2-ethandiol, — Phenazin. 22 Kapitel 5.1 Im Fingerprint-Bereich sind weitere Veränderungen erkennbar, die bis auf wenige Ausnahmen schwierig zu interpretieren sind (Abb. 5.1.4). Die Doppelbande bei 1032 und 1022 cm-1 wird den C-O-Valenzschwingungen des reinen Diols zugeschrieben. Im Kokristall tritt nur eine C-O- Valenzschwinungsbande bei 1051 cm-1 auf. Diese Beobachtung kann entsprechend der Bande der OH-Valenzschwingung erklärt werden. Aus den Veränderungen im IR-Teilspektrum des meso-Diols kann geschlossen werden, daß die O-H-Bindung im Kokristall geschwächt, die C-O-Bindung hingegen gestärkt ist. Ein identisches IR-Spektrum wird durch Zusammenschmelzen oder intensives Vermahlen äquimolarer Mengen der Komponenten erhalten. Der Kokristall ist photoaktiv und zeigt eine Farbänderung von gelb über grün nach violett. Die in einer Kaliumbromid-MatrixA (A s. exp. Teil) vermahlene Probe wurde mit einer Hg/Xe-Hochdrucklampe (1 kW, UG5-Filter) durch ein zusätzliches GG395-Kantenfilter bestrahlt. Bei 3378 cm-1 zeichnet sich eine scharfe Bande ab, und die OH-Absorption wird schwächer und strukturierter (Abb. 5.1.5). 100 Trans. 100 Trans. 80 80 60 60 40 40 20 1800 20 3500 3000 2500 [cm -1] 1600 1400 1200 1000 [cm -1] Abb. 5.1.5: IR-Spektren des Kokristalls aus Phenazin und meso-1,2-Diphenyl-1,2ethandiol: — unbestrahlt und — 8 s bestrahlt (GG395). Phenazin und meso-1,2-Diphenyl-1,2-ethandiol 23 Die scharfe Bande bei 3378 cm-1 wird aufgrund ihrer Lage und Form einer NH-Valenzschwingung zugeordnet. In der Literatur liegt die NH-Bande der Chloridverbindung des 5,10-Dihydrophenazinradikalkations bei 3400 cm-1 (breit).[40] Eigene Messungen zeigen im IR-Spektrum des 5,10- Dihydrophenazins eine scharfe NH-Bande bei 3383 cm-1. In der Literatur wird die Lage der scharfen NH-Bande des 5,10-Dihydrophenazins mit 3400 cm-1 angegeben.[40] Die entstehende Strukturierung der OH-Absorption deutet auf veränderte Verhältnisse in den OHN-Brücken hin. Im Bereich der Doppelbindungsvalenzschwingungen und der NH- Deformationsschwingungen treten im IR-Spektrum Änderungen auf, die nicht eindeutig interpretierbar sind. Im Fingerprint-Bereich, in dem auch die C-Ound N-C-Valenzschwingungsbanden liegen, wird das Spektrum stark verändert. Die beiden durch die Bestrahlung neu entstandenen Banden bei 1279 und 1300 cm-1 sind auch in den Spektren des 5,10-Dihydrophenazins und der Chloridverbindung des 5,10-Dihydrophenazinradikalkations als intensive Banden vertreten.[40] Die Bande bei 1300 cm-1 wird vom C-N-C-Fragment verursacht.[41] Das ionische monoprotonierte Phenazin hat an dieser Stelle keine Banden.[42] Desweiteren entstehen neue Banden bei 1036 und 1021 cm 1, während die Intensität der Bande bei 1059 cm -1 deutlich abnimmt. Die Veränderungen bei 1059-1021 cm-1 deuten auf veränderte Verhältnisse in den C-O-Bindungen im Diol des bestrahlten Kokristalls hin. Das 48stündige Erhitzen der Probe in einer Kaliumbromid-Matrix bei 60 °C führte zum Spektrum des reinen meso-Diols, da das Phenazin aus der Oberfläche der pulverigen Probe sublimierte. Daraufhin wurde die Messung an einer kristallinen Probe wiederholt. Auch hier verändert sich das Spektrum durch die Bestrahlung entsprechend (Abb. 5.1.5). Das Erhitzen der Probe führt weitgehend wieder zum Ausgangsspektrum. Im 1H-NMR-Lösungsspektrum der drei Minuten durch ein GG395-Kantenfilter bestrahlten werden. Kokristalle können keine Zersetzungsprodukte beobachtet 24 Kapitel 5.1 Das UV/VisA-Spektrum des reinen Phenazins, das in diffuser Reflexion in einer Kaliumbromid-Matrix aufgenommen wurde, besitzt Absorptionsmaxima bei 253 und 369 nm mit einer Schulter bei 398 nm. Das Spektrum des Kokristalls ist keine reine Überlagerung der Einzelspektren, seine Maxima liegen bei 251, 375, 398 und 404 nm (Abb. 5.1.6). In Analogie zu den UV/Vis-Spektren des Phenazins in protischen Lösungsmitteln, in denen der verbotene n*-Übergang zu kürzeren und der erlaubte *-Übergang zu längeren Wellenlängen verschoben ist[43], wird das Auftreten der langwelligen Bande bei 404 nm im Spektrum des Kokristalls mit der fixierten protischen Umgebung des Phenazins in Verbindung gebracht. Das UV/Vis-Spektrum des Phenazins im Methanol (c = 10-4 M) hat bei 400 nm eine Schulter.[42] Dieser Vergleich ist zulässig, da das UV/Vis-Spektrum eines isolierten Moleküls in Lösung und des entsprechenden Moleküls im Festkörper sich sehr ähneln, solange alle Moleküle einer Molekülsorte in der Elementarzelle äquivalent sind.[44] Unter dieser Voraussetzung sind die Bandenmaxima in den Festkörperspektren im Lösungsspektren lediglich etwas langwellig verschoben. Abs. 1.0 0.8 0.6 0.4 0.2 0.0 200 300 400 500 [nm] Vergleich zu den Phenazin und meso-1,2-Diphenyl-1,2-ethandiol 25 Abb. 5.1.6: UV/VisA-Spektren: — Kokristall, — Phenazin und — meso-1,2-Diphenyl-1,2ethandiol. Durch die Bestrahlung der gemahlenen Probe in einer Kaliumbromid-MatrixA nimmt die Extinktion der Maxima bei 375 und 404 nm ab und aus der zu kürzeren Wellenlängen verschobenen Schulter bildet sich ein Absorptionsmaximum neues bei 320 nm (Abb. 5.1.7.a). a) 0.8 Abs. b) 0.6 Abs. 0.5 0.6 0.4 0.4 0.3 0.2 0.2 0.1 0.0 0.0 300 400 500 600 700 800 [nm] 500 600 700 800 [nm] Abb. 5.1.7: UV/Vis-Spektren des Kokristalls aus Phenazin und meso-1,2-Diphenyl-1,2ethandiol: a) 33%-GitterA: — unbestrahlt; — 1 s und — 7 s bestrahlt; b) Kristalle: — unbestrahlt; — 3 s bestrahlt (WG360) und — 20 h bei 94 °C erhitzt. Im Bereich von 420-800 nm nimmt die Absorption stark zu. Nach 1 s Bestrahlung sind die langwelligen Absorptionen noch strukturiert. Hier treten Banden bei 448, 522, 557 und 608 nm auf. Mit fortschreitender Bestrahlung wird daraus eine breite Bande mit einem Maximum bei 560 nm, die sich über einen Bereich von 420 bis über 800 nm erstreckt. Oberhalb von ca. 650 nm 26 Kapitel 5.1 nimmt die Absorption kontinuierlich ab, bis 1000 nm ist kein weiteres Maximum sichtbar. Die bestrahlte Probe ist violett gefärbt. In der Abbildung 5.1.7.b sind die Vis-Spektren der unbestrahlten, der bestrahlten und der erhitzten Kristalle zu sehen. Das Vis-Spektrum der erhitzten Kristalle entspricht dem der unbestrahlten. Die Bestrahlung durch ein GG435-Kantenfilter, das ab 405 nm eine geringe Durchlässigkeit besitzt, führt zu keiner Farbänderung. Aufgrund des eingestrahlten Wellenlängenbereiches, das GG395-Kantenfilter ist für Licht der Wellenlängen größer 340 nm durchlässig, lag die Vermutung nahe, daß durch die Bestrahlung die Phenazinmoleküle angeregt werden und eventuell weiterreagieren. Mögliche Photoprodukte können die verschieden protonierten Phenazinmoleküle sowie die verschiedenen radikalischen Phenazinverbindungen sein (Tabelle 5.1.3). Die mono- und die diprotonierte Form des Phenazins weisen nur Banden unterhalb 500 nm auf, so daß sie nicht für die Veränderungen im Vis-Bereich des Spektrums verantwortlich sein können.[42] Tabelle 5.1.3: UV/Vis-Spektren von radikalischen Phenazinverbindungen (P). Phenazin und meso-1,2-Diphenyl-1,2-ethandiol . P+ . P. PH2 + [a]Es 27 Lösungsmittel/Konzentrationen [nm] H2O[45] 420, 490, 580 bis 600a PE-Film, 77 K[46] 478, 586a,b t-BuCl-90%; CCl4-10%, 77 K[47] 432, 481, 556, 575a PE-Film, 77 K[46] 509, 547, 554, 602a MTHF Matrix, 77 K[47] 460, 515, 550, 590, 600a HCl/MeOH (c = 212-5 M)[33] <208, 250-277, 384, 434c H2SO4/H2O (c = 10-4 M)[35] 383, 430, 443a,c C2 F3H2OH (c = 10-4 M)[48] 300, 384, 430b, 455, 584d, 670d, 700d, 772d ist nur der Vis-Bereich abgegeben, [b]Schulter, [c]Der Bereich über 500 nm wurde bei diesen Konzentrationen nicht angegeben, [d]Wenig intensiv. Die besten Übereinstimmungen mit dem Vis-Bereich des Spektrums des bestrahlten Kokristalls (Abb. 5.1.7.b) ergibt eine Kombination der Spektren aus Phenazinradikalkation, Phenazinradikalanion und dem diprotonierten Phenazinradikalanion. Während das Phenazinradikalanion eine rote Färbung besitzt, zeigt die diprotonierte Form eine grüne Farbe. Das Phenazinradikalkation ist violett gefärbt. Beim Vergleich der genauen Bandenlage des UV/Vis-Spektrums des bestrahlten Kokristalls mit den Literaturdaten ist allerdings zu bedenken, daß diese Verbindungen alle in Lösung oder bei tiefen Temperaturen in einer Matrix vermessen wurden. Die unbestrahlten gelben Kristalle sind diamagnetisch. Durch Bestrahlung werden sie paramagnetisch. Das ESR-Spektrum zeigt, wie für pulverige Festkörperproben häufig typisch, keine Feinaufspaltung, so daß keine Kopplungen mit den Stickstoff- und den Wasserstoffatomen beobachtet werden können (Abb. 5.1.8). Es ist allerdings eine von der Bestrahlungsdauer abhängige Bildung von zwei verschiedenen Radikalen an der unterschiedlichen Intensitätszunahme der beiden Signale zu erkennen (Abb. 5.1.8). Der gemessene g-Wert ist 2.0036 und liegt damit im Bereich der 28 Kapitel 5.1 in der Literatur beschriebenen g-Werte für Phenazinradikale. Der g-Wert für das Phenazinradikalanion in Acetonitril beträgt g = 2.00336. Der des diprotonierten Phenazinradikalanions ist mit g = 2.00285 angegeben.[49] 3320 3340 3360 3380 3400 H[G] Abb. 5.1.8: ESR-Spektren des Kokristalls aus Phenazin und meso-1,2-Diphenyl-1,2ethandiol: — unbestrahlt, — 1 s (33%-Gitter), — 7 s und — 507 s bestrahlt. Das Phenazinradikalanion ist thermodynamisch relativ stabil, so beträgt z.B. seine Halbwertszeit in Acetonitril 3-4 Minuten bei 22 °C. Thermisch ist der Paramagnetismus reversibel. Wird ein 120 s durch ein GG395Kantenfilter bestrahlter Kristall 21.5 Stunden bei 90 °C erhitzt, so wird er wieder diamagnetisch. Die genau benötigte Zeit zum Erreichen des Ausgangszustandes beim Erhitzen auf 90 °C wurde nicht bestimmt. Nach 1.5 Stunden hatte das ESR-Signal nur wenig an Intensität eingebüßt. Wichtig ist in diesem Zusammenhang nur, daß der Paramagnetismus thermisch reversibel ist. Die intensive dreiminütige Bestrahlung von reinem Phenazin bei Raumtemperatur führte zu keinem ESR-Signal. Unter Einbeziehung aller Ergebnisse wird folgender Mechanismus für die Photochromie vorgeschlagen. Aufgrund der Orientierung zweier Phenazin und meso-1,2-Diphenyl-1,2-ethandiol 29 Phenazinmoleküle im Kristallgitter zueinander, der parallelen Orientierung und des relativen Abstands, wird angenommen, daß sich bei der photochemischen Anregung eines Moleküls ein Excimer bildet. Ein wichtiger Parameter für die Excimerbildung ist der Abstand beider Moleküle voneinander.[50] Sowohl berechnet als auch experimentell wurde er meist im Bereich von 300 bis 360 pm gefunden. Der Bindungszustand dieses Excimers kann mit den folgenden Anregungs- und Ladungsresonanzstrukturen wiedergegeben werden. P*P PP* P-P+ P+PVon Fall zu Fall können entweder die polaren oder die unpolaren Zustände das größere Gewicht besitzen. Hat das Excimer die Möglichkeit, sich in ein stabiles Photoprodukt beobachtet. Würde umzuwandeln, nur das dann angeregte wird keine Phenazin Fluoreszenz (P*) von den Hydroxygruppen des Diols protoniert, dann würde als Photoprodukt das monoprotonierte diamagnetische Phenazin erhalten werden (PH+). Die Basizität von Stickstoff im ersten Singulett-Zustand kann fünf- bis sechsmal stärker sein als im Grundzustand.[51] Eine erneute Anregung zu einem Exciplex mit einem weiteren Phenazinmolekül könnte zum Elektronentransfer ((PH+)*P (PH.*)(P.+)) und einer weiteren Protonierung des angeregten Zustandes führen ((PH .+)(P.+). Anders sieht es im Falle der ein- bis zweifachen 2 Protonierung des ladungsgetrennten Excimers aus, hier würden sich als Produkte PH. bzw. PH2.+ und P.+ bilden (Abb. 5.1.9/5.1.10). Eine andere Erklärungsmöglichkeit wäre die direkte Bildung zweier unabhängiger Radikale, von denen das Radikalanion dann protoniert wird. . N N N H N . N . N h/ET .+ PT N T N N .+ T N H N N .+ 30 Kapitel 5.1 Abb. 5.1.9: Darstellung des möglichen Mechanismus für den photochromen Effekt in den Phenazinstapeln des Kokristalls aus Phenazin und meso-1,2-Diphenyl-1,2ethandiol. Die unterschiedlichen Strichstärken sollen das gestapelte Vorliegen der Phenazinmoleküle hervorheben. Die durch den Elektronentransfer gebildeten primären Radikalkationen und –anionen sollten thermodynamisch relativ stabil sein, da sie Radikale vom sogenannten Wurster- bzw. Weitz-Typ darstellen. Das diprotonierte Phenazinradikalanion, das ebenfalls für seine Stabilität bekannt ist, kann aus dem Radikalanion durch zweifache Protonierung gebildet werden (Abb. 5.1.9/5.1.10). Der postulierte Mechanismus steht im Einklang mit den beobachteten Veränderungen im IR-Spektrum des bestrahlten Kokristalls. Bei allen genannten Phenazinradikalen sollten sich die Verhältnisse in den betroffenen H-Brücken ändern. Zum Einen wird eine NH-Valenzschwingung beobachtet, die mit der Bildung des protonierten Phenazinradikalanions erklärt werden kann. Zweitens wird die OH-Bande strukturierter, was auf die Bildung des Phenazinradikalkations zurückgeführt werden könnte. Denn das Phenazinradikalkation sollte eine geringfügig weniger starke H-Brücke als die neutralen Phenazinmoleküle ausbilden. OH OH OH O OH O H H . N . O H N .+ N. H N. T N .+ H .+ N. N H OH O H O N O PT H OH O OH O OH Phenazin und meso-1,2-Diphenyl-1,2-ethandiol Abb. 5.1.10: Darstellung des möglichen Mechanismus 31 der Protonierung des Radikalanions innerhalb der Ketten des Kokristalls aus Phenazin und meso-1,2Diphenyl-1,2-ethandiol. 5.2 Phenazin und alkylsubstituierte 1,2-Ethandiole Um eine Beteiligung des -Systems des meso-1,2-Diphenyl-1,2-ethandiols an der beobachteten Photochromie dieses Kokristalls auszuschließen, wurden Versuche unternommen, Kokristalle aus Phenazin und alkysubstituieten 1,2Ethandiolen zu erhalten und deren Eigenschaften zu untersuchen. 5.2.1 Phenazin und 1,2-Ethandiol Die ersten Untersuchungen an dem System Phenazin und 1,2-Ethandiol wurden schon in der Diplomarbeit[20] durchgeführt. Die bei der Kristallisation aus wasserfreiem 1,2-Ethandiol erhaltenen gelben Fasern mit einer Zusammensetzung von 56 : 44 von Diol zu Phenazin hatten keine für eine Röntgenstrukturuntersuchung geeignete Qualität. Da es auch mit Hilfe der Kapillartechnik bisher nicht gelang, geeignete Kristalle zu ziehen, wurde von den Fasern ein Pulverdiffraktogramm aufgenommen. Hierbei konnten keine Veränderung der Elementarzellen gegenüber denen der einzelnen Komponenten festgestellt werden. Alle weiteren Versuche aus diversen Lösungsmitteln (Diethylether, THF, Aceton, Essigsäureethylester, 1,2-Ethandiol) bei Temperaturen von Raumtemperatur bis –35 °C Kokristalle zu gewinnen, waren erfolglos. Die Fasern besitzen keinen definierten Schmelzpunkt. Die OH- 32 Kapitel 5.2 Valenzschwingung bei 3389 cm-1 im IR-Spektrum der unbestrahlten Probe liegt im Bereich der sehr breiten OH-Bande des reinen Diols, doch sie ist bedeutend schärfer. Die C-O-Valenzschwingungen des Diols in den Fasern werden den Banden bei 1086 und 1042 cm-1 zugeordnet. Die gleichen IR-Spektren könnten auch durch Verreiben oder Zusammenschmelzen äquimolarer Stoffmengen der beiden Komponenten erhalten werden. Beim Verreiben wird eine hellgelbe Paste erhalten. Die Probe zeigte bei Bestrahlung dasselbe Verhalten wie die Kokristalle des Phenazins mit meso-1,2-Diphenyl-1,2ethandiol. Sie verfärbt sich violett und bei 1300 cm-1 entsteht im IR-Spektrum eine neue Bande, die beim Kokristall aus Phenazin und meso-1,2-Diphenyl-1,2-ethandiol einer 5,10-Dihydrophenazinverbindung zugeordnet wurde. Die OH-Valenzschwingung nimmt sehr stark ab, wobei Banden mit sehr geringer Intensität bei 3380 und 3250 cm -1 zurückbleiben. Wird der Preßling zwei Stunden bei 60 °C getempert, verändert sich die Durchlässigkeit so stark, daß das Spektrum nicht mehr ausgewertet werden konnte. Das in diffuser Reflexion an Fasern aufgenommene UV/Vis-Spektrum zeigt im Vis-Bereich keinerlei Veränderungen, es entspricht dem der Phenazinkristalle, (Abb. 5.2.1.1.a) und auch im UV-Bereich unterscheiden sich die Spektren nur geringfügig. Die Phenazinkristalle zeigen Maxima bei 375 und 443 nm mit einer Schulter bei 424 nm, während der Kokristall zwei Schultern bei 359 und 437 nm erkennen läßt. a) Abs. b) Abs. 0.8 0.6 0.6 0.4 0.4 0.2 0.2 0.0 0.0 400 500 600 [nm] 400 500 600 700 800 [nm] Phenazin und alkylsubstituierte 1,2-Ethandiole 33 Abb. 5.2.1.1: UV/Vis-Spektren: a) — Fasern aus Phenazin und 1,2-Ethandiol, — Phenazin (Kristalle); b) Fasern aus Phenazin und 1,2-Ethandiol, 33%-Gitter: – 0 s; — 90 s und – 29 min bestrahlt. Die Abbildung 5.2.1.1.b zeigt die nach längerer Bestrahlung der Fasern hervorgerufenen Veränderungen des UV/Vis-Spektrums. Im Vis-Bereich bildet sich eine breit auslaufende Schulter bei 520 nm, die bis knapp über 800 nm reicht. Eine über einen längeren Zeitraum dem Tageslicht, jedoch nicht der direkten Sonneneinstrahlung, ausgesetzte, verriebene Probe hat sich violett gefärbt. Sie zeigt im Vis-Bereich Schultern bei 365, 421 und 436 nm. Ab etwa 460 nm erstreckt sich eine fast gerade Bande bis weit über 800 nm, nur bei 578 nm weist sie ein schwaches Maximum auf. Die Reversibilität der Farbveränderung konnte bei Erhitzen auf 60 °C nicht festgestellt werden, da sich die Probe zersetzt. Die bestrahlten Fasern aus Phenazin und 1,2-Ethandiol sind paramagnetisch, der g-Wert beträgt 2.0031. Das abgebildete feinaufgespaltene Siebenlinienhauptspektrum konnte mehrfach reproduziert werden (Abb.: 5.2.1.2.a). a) 3340 3360 3380 N + N OHOH H2 C CH2 H[G] b) 3340 H N . 3360 .+ 3380 N + N H N H[G] .+ 34 Kapitel 5.2 Abb. 5.2.1.2: a) Experimentelles ESR-Spektrum der bestrahlten Fasern aus Phenazin und 1,2-Ethandiol; b) Simuliertes ESR-Spektrum für ein diprotoniertes Phenazinradikalanion und ein Phenazinradikalkation.[52] Die Ursache des Paramagnetismus nach Bestrahlung könnte, ähnlich wie im Kokristall aus Phenazin und meso-1,2-Diphenyl-1,2-ethandiol, ein lichtinduzierter Elektronentransfer zwischen den Phenazinmolekülen sein. Nachforschungen in der Literatur ergaben, daß ein dem aufgenommenen verwandtes Spektrum für das diprotonierte Phenazinradikalanion erhalten wird. Bei der Simulation dieses Spektrums sind die beiden äußeren Signalgruppen im Verhältnis zu den mittleren fünf allerdings zu intensiv. Da das ESR-Spektrum des Phenazinradikalkations, welches ebenfalls beim angenommenen Elektronentransfer gebildet wird, unbekannt ist, wurde die Vereinfachung vorgenommen, daß sich die Kopplung der Wasserstoffatome mit dem ungepaarten Elektron nicht verändert, wenn die Stickstoffatome nicht protoniert sind und Phenazin als Kation vorliegt (Abb. 5.2.1.2.b). Zur Simulation des Spektrums des Phenazinradikalkations wurden also die beiden Kopplungskonstanten der Protonen an den Stickstoffatomen weggelassen. Die 1 : 1-Überlagerung der simulierten ESR-Spektren (Abb. 5.2.1.2.b) des Phenazinradikalkations und des diprotonierten Phenazinradikalanions gibt das experimentell erhaltene Spektrum gut wieder (Abb. 5.2.1.2.a).[52] Die Beteiligung von 10-Hydrophenazin-5(10H)-yl an der Photochromie kann ausgeschlossen werden, da das ESR-Spektrum ein anderes Aufspaltungsmuster zeigt.[53] Obwohl die Ergebnisse der Untersuchungen an den Fasern aus Phenazin und 1,2-Ethandiol weitaus weniger aussagekräftig sind, als die des Kokristalls aus Phenazin und meso-1,2-Diphenyl-1,2-ethandiol, wird angenommen, daß die gleichen Reaktionen unter Bestrahlung ablaufen. Phenazin und alkylsubstituierte 1,2-Ethandiole 35 5.2.2 Phenazin und meso-2,3-Butandiol Zur Darstellung des Kokristalls aus meso-2,3-Butandiol wurden jeweils äquimolare Mischungen der beiden Komponenten bei verschiedenen Temperaturen in Raumtemperatur Essigsäureethylester abgekühlt. gelöst Anschließend und konnte langsam das auf Lösungsmittel verdampfen. In allen Fällen konnte nur Phenazin isoliert werden. Das Mischen und Zusammenschmelzen äquimolarer Mengen beider Substanzen führt zu einem IR-Spektrum mit einer schmaleren OH-Bande als der im Spektrum des Diols. Das Maximum der OH-Bande der Verreibung liegt bei 3357 cm-1, während das Maximum der sehr breiten Bande des meso-2,3-Butandiol bei 3379 cm-1 liegt. Wird ein Preßling der Schmelze bestrahlt, so verändert sich das IR-Spektrum, indem bei 1300 cm-1 eine Bande intensiver wird. Optisch war die Probe nach der Bestrahlung nur punktuell gefärbt und zeigte ein schwaches ESR-Signal, das etwa 60-70 G breit ist und einen g-Wert von 2.0033 hat. Die Auswertung des Pulverdiffraktogramms der zusammengeschmolzenen Probe ergab, wie auch schon bei den Fasern aus 1,2-Ethandiol und Phenazin, daß sich die Elementarzellen gegenüber denen der Einzelkomponenten nicht verändert haben. Auch der Versuch, einen Kokristall mit Hilfe der Kapillartechnik zu ziehen, gelang nicht. Die über Wochen dem Tageslicht ausgesetzte Probe wurde entsprechend der Probe aus Phenazin und 1,2-Ethandiol violett. Das Vis-Spektrum der violetten Probe hat ein Absorptionsmaximum bei 578 nm mit Schultern bei 377 und 434 nm. Aufgrund des niedrigen Schmelzpunktes des Butandiols konnte die Reversibilität der Farbveränderung nicht getestet werden. Die Ergebnisse der Untersuchungen der zusammengeschmolzenen Probe deuten darauf hin, daß unter Bestrahlung vergleichbare Reaktionen, wie im Kokristall aus Phenazin und meso-1,2-Diphenyl-1,2-ethandiol ablaufen. 36 Kapitel 5.2 6 Versuche zur Kokristallisation von Phenazin mit weiteren Diolen Neben den in Kapitel 5.2 beschriebenen alkylsubstituierten Diolen wurden auch Pinakol Gründen in beschriebenen und meso-Dicyclohexyl-1,2-ethandiol die Kristallisationsversuche meso-1,2-Ethandiole aus einbezogen. enthalten anders beschriebenen Alle weiteren substituierte aromatische Systeme als das meso-1,2-Diphenyl-1,2-ethandiol. Von Ihnen konnten keine Kokristalle erhalten werden. Desweiteren sollte das deuterierte meso-1,2-Diphenyl-1,2-ethandiol in den Kokristall mit Phenazin eingebaut werden, da eine deutliche Separierung der OD- von der ND-Bande im IRSpektrum des bestrahlten Kokristalls erhofft wurde. 6.1 Phenazin und Pinakol Es wurden Versuche unternommen, aus 95proz. wäßrigem Pinakol als Lösungsmittel Kokristalle mit Phenazin zu erhalten. Die Kristallisationen dauerten zum Teil einige Wochen. Alle Fraktionen bestanden aus reinem Phenazin. Das IR-Spektrum einer zusammengeschmolzenen oder verriebenen äquimolaren Probe ist eine reine Überlagerung der Spektren der Einzelkomponenten. Der 2 min mit 33% der Strahlungsintensität einer Hg/XeHochdrucklampe (1 kW, UG5-Filter) bestrahlte Preßling liefert ein nicht mehr auswertbares IR-Spektrum. Gleichfalls wird die Probe unter Bestrahlung nicht paramagnetisch und behält ihre Farbe bei. Versuche der Kokristallisation von Phenazin mit weiteren Diolen 37 6.2 Phenazin und meso-1,2-Dicyclohexyl-1,2-ethandiol Mehrere Versuche, meso-1,2-Dicyclohexyl-1,2-ethandiol mit Phenazin zu kokristallisieren, führten nicht zum gewünschten Erfolg. Das meso-1,2Dicyclohexyl-1,2-ethandiol ist in gängigen Lösungsmitteln ungewöhnlich schlecht löslich. So konnten aus Aceton bei einem Verhältnis von 1 : 1 der Komponenten oder mit Phenazin im Überschuß aus Ethanol, Essigsäureethylester oder wasserfreiem THF keine Kokristalle gewonnen werden. Auch das Zusammenschmelzen oder Verreiben der Monomere konnte keine Komplexbildung bewirken. Von meso-1,2-Dicyclohexy-1,2-ethandiol konnten kleine Nadeln erhalten werden, anhand derer die Kristallstruktur des Diols aufgeklärt werden konnte. Die Raumgruppe, in der meso-1,2-Dicyclohexyl-1,2-ethandiol kristallisiert, ist Pbcn. Jedes Diol ist mit vier weiteren Diolen über H-Brücken verbunden, wobei das Wasserstoffatom der Hydroxygruppen stark fehlgeordnet ist (Abb. 6.2.1). Abb. 6.2.1: Molekülstruktur des fehlgeordneten meso-1,2-Dicyclohexyl-1,2-ethandiols. Das Diol ist zwar wie das meso-1,2-Diphenyl-1,2-ethandiol langgestreckt, doch können die Csp2-H-Wechselwirkungen, die im Falle des Kokristalls aus meso1,2-Diphenyl-1,2-ethandiol und Phenazin wirken, nicht ausgebildet werden (Abb. 5.1.1). Die Bildung eines Kokristalls mit Phenazin könnte zusätzlich durch die sterisch anspruchsvollen, unpolaren Cyclohexylringe unterbunden werden. Die Diole haben sich im Kristallgitter so angeordnet, daß jede Hydroxygruppe zwei H-Brücken, je eine als Donor und eine als Akzeptor, ausbilden kann. Zwischen vier meso-1,2-Dicyclohexyl-1,2-diolen bilden sich 38 Kapitel 6 quadratische Anordnungen aus, deren Ecken von den Sauerstoffatomen gebildet werden (Abb. 6.2.2). Abb. 6.2.2: Anordnung von vier meso-1,2-Dicyclohexyl-1,2-ethandiolen. Die OO-Abstände liegen bei 280.3, 285.7 und zweimal bei je 274.5 pm ( = 143.2°/147.1°/168.4°/ 176.6°). Über die zweite Hydroxygruppe jedes Diols erfolgt die zweidimensionale Vernetzung mit zwei weiteren Diolen. So bilden sich Schichten, die außen lipophil und in der Mitte über starke H-Brücken verknüpft sind. 6.3 Phenazin und meso-(O,O)-Dideutero-1,2-diphenyl-1,2- ethandiol Der photochrome Kokristall kann durch Zusammenschmelzen, Verreiben oder Kristallisation aus Essigsäureethylester erhalten werden. Phenazin und das deuterierte Diol wurden in äquimolarer Zusammensetzung bei Raumtemperatur in wasserfreiem Essigsäureethylester unter Argon gelöst und bei 4 °C kristallisiert. Da der Deuterierungsgrad des Diols von ursprünglich 99.7 % auf 87.0 % in den Kokristallen sank, scheint ein H/D-Austausch mit dem Lösungsmittel stattgefunden zu haben. Um dies auszuschließen, könnte der Versuche der Kokristallisation von Phenazin mit weiteren Diolen 39 Kokristall durch Verreiben beider Komponenten gewonnen werden. Die Kristallstruktur undeuterierten ist von Fall untergeordneter bekannt ist. Bedeutung, Aufgrund der da sie fehlenden für den deutlichen Separierung der OD- und ND-Valenzschwingungen im IR-Spektrum, die NDBande liegt als Schulter unter der OD-Bande, wurden weitere Versuche zur Synthese dieses Kokristalls unterlassen. 6.4 Phenazin und meso-1,2-Bis-(4-dimethylaminophenyl)-1,2- ethandiol Äquimolare Mischungen in Ethanol und Essigsäureethylester wurden bei 40 °C und 60 °C hergestellt und langsam auf Raumtemperatur abgekühlt. Es wurden jedoch keine Kokristalle erhalten, und auch die intensive Verreibung beider Komponenten führte im IR-Spektrum zu keiner Verschiebung von charakteristischen Valenzschwingungen. Obwohl sich die Dimethylaminogruppen in der Kristallpackung versetzt anordnen könnten, scheinen sie die Kokristallbildung zu behindern. 6.5 Phenazin und 1,4-Bis-(hydroxymethyl)-benzol Es wurden äquimolare Mischungen in Ethanol bzw. Essigsäureethylester bei Raumtemperatur, bei 40 °C und 60 °C gelöst und langsam abgekühlt, ohne daß Kokristalle isolierte werden konnten. Auch die intensive Verreibung und das Zusammenschmelzen führte zu keiner Verschiebung charakteristischer Valenzschwingungen im IR-Spektrum. 40 Kapitel 6 6.6 Phenazin und meso-1,2-Di(4-pyridyl)-1,2-ethandiol Aus äquimolaren Mischungen in wäßrigem 80proz. Ethanol und Methanol konnten keine Kokristalle isoliert werden, da das Diol aufgrund seiner schlechten Löslichkeit immer zuerst ausfiel. Nur in DMSO ist das Diol besser löslich, woraus es allerdings nicht mehr auskristallisiert. Desweiteren wurde versucht, einen Kokristall durch Zusammenschmelzen der beiden Komponenten unter Argon und unter Vakuum herzustellen. Die Mischungen unter Argon färbten sich grüngrau. Das Zusammenschmelzen unter Vakuum wurde abgebrochen, da Phenazin aus der Mischung sublimierte. Die IRSpektren dieser Proben sind eine Überlagerung der Einzelspektren. Auch durch intensives Verreiben konnte kein anderes Ergebnis erzielt werden. Nach einigen Versuchen gelang es, das als farbloses Pulver vorliegende meso-1,2-Di(4-pyridyl)-1,2-ethandiol aus wäßrigem 80proz. Methanol so zu kristallisieren, daß Kristalle ausreichender Größe und Qualität für eine Röntgenstrukturuntersuchung erhalten werden konnten. Die in Abbildung 6.6.1.a/b gezeigten Ausschnitte aus der Struktur des Diols, das die Raumgruppe Pbca besitzt, machen deutlich, warum das Diol so schlecht löslich ist. An jedem Molekül wirken vier starke O-HN-Brücken, so daß ein zweidimensionales Netzwerk ausgebildet wird. Der NO-Abstand ist 280.1 pm ( = 159.7°). Es werden keine Csp2-H- bzw. Csp2-HO-Wechselwirkungen beobachtet. a) b) Versuche der Kokristallisation von Phenazin mit weiteren Diolen 41 Abb. 6.6.1: a) Ausschnitt aus der Kristallstruktur des meso-1,2-Di(4-pyridyl)-1,2ethandiols entlang der a-Achse; b) Seitliche Ansicht von Ausschnitt a. Phenazin könnte im gewünschten Kokristall dem Diol jedoch nur zwei dieser H-Brücken und die schwächeren Csp2-HN-Brücken und Csp2-H-Wechselwirkungen anbieten. Denkbar wäre z.B. die Bildung eines Kokristalls mit 2,7Dihydroxyphenazin, wenn eine vergleichbare Kristallstrukur, wie bei Phenazin und meso-1,2-Diphenyl-1,2-ethandiol verwirklicht würde (Abb. 5.1.1/2). Die Hydroxygruppen der Phenazinmoleküle könnten an den Stickstoffatomen der Pyridylgruppen in den seitlich benachbarten Ketten angreifen. 6.7 Phenazin und meso-Weinsäuredimethylester Die beiden Komponenten wurden bei verschiedenen Temperaturen in Essigsäureethylester, Chloroform und in wasserfreiem Methanol gelöst. In allen Fällen kristallisierten die Komponenten nebeneinander aus. Die durch Verreiben oder Zusammenschmelzen erhaltenen hellgelben Proben zeigten in den IR-Spektren keine neuen oder verschobenen Absorptionsbanden. Die beiden möglichen intramolekularen H-Brücken im Weinsäureester könnten die Kokristallisation verhindern. Das IR-Spektrum des Esters zeigt allerdings nicht die für diesen Fall zu erwartende Valenzschwingungsbande. starke Erniedrigung der C=O-