Pankreasinzidentalome
Werbung

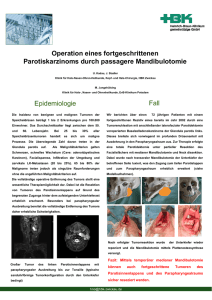
Leitthema Chirurg 2007 · 78:713–720 DOI 10.1007/s00104-007-1373-x Online publiziert: 14. Juli 2007 © Springer Medizin Verlag 2007 U. Hopt · T. Keck Abteilung für Allgemein- und Viszeralchirurgie, Chirurgische Universitätsklinik, Freiburg Pankreasinzidentalome Bewertung und Therapie Inzidentalome sind Tumoren, die keine klinischen Symptome hervorrufen und daher zufällig bei Schnittbilduntersuchungen, die aus anderen Gründen veranlasst wurden, diagnostiziert werden. Grund für solche CT-/ MRT-Untersuchungen können Erkrankungen anderer Organe, wie z. B. eine Nephrolithiasis sein, ferner ein spezielles Tumorscreening bei Patienten mit genetisch erhöhtem Tumorrisiko oder ein allgemeines Tumorscreening im Rahmen von Voruntersuchungen [47]. Inzidentalome im weiteren Sinne sind auch die Pankreastumoren, die aufgrund eines subjektiv nicht bemerkbaren Anstiegs der Gallengangs- und Pankreasenzyme bei der nachfolgenden Schnittbilddiagnostik entdeckt werden. Bei Nachweis eines Inzidentaloms im Pankreas ergibt sich als erstes die Frage nach der Dignität des Tumors. Zu unter­ scheiden ist hier zwischen sicher benigne, prämaligne und maligne. Bei der Thera­ pieentscheidung muss zum einen bedacht werden, wie sicher mit den heutigen di­ agnostischen Möglichkeiten eine Unter­ scheidung zwischen benigne auf der ei­ nen Seite und prämaligne und maligne auf der anderen Seite möglich ist und wel­ che Konsequenzen eine verzögerte opera­ tive Therapie nach sich zieht. Auf der an­ deren Seite müssen das perioperative Ri­ siko einer Tumorresektion und die mög­ lichen postoperativen Folgezustände be­ rücksichtigt werden. Von Bedeutung sind dabei die Art der Operation, die geplante chirurgische Radikalität und natürlich auch die spezifischen Risikofaktoren des betreffenden Patienten. Bei inzidentell im Pankreas gefun­ denen Tumoren hat die Unterscheidung zwischen soliden und zystischen Tumo­ ren eine besondere Bedeutung. Die Dif­ ferenzialdiagnose, das Malignitätsrisi­ ko und auch das therapeutische Prozede­ re unterscheiden sich bei diesen Tumor­ enentitäten nämlich grundlegend. Solide Pankreasinzidentalome Duktales Adenokarzinom Das duktale Adenokarzinom ist der bei weitem häufigste Pankreastumor. Bei über 80% der Patienten wird dieser Tu­ mor zu spät diagnostiziert und ist dann nicht mehr kurativ resezierbar. Insofern ist die zufällige Diagnose eines frühen Sta­ diums eines Pankreaskarzinoms für den betreffenden Patienten hinsichtlich sei­ ner Langzeitprognose von zentraler Be­ deutung. Die 5-Jahres-Überlebensrate nach Resektion eines Pankreaskopfkar­ zinoms liegt in den meisten Zentren nur zwischen 20% und 30%. Kleinere Tumo­ ren haben bei fehlender Lymphknoten­ metastasierung (N0) eine deutlich besse­ re Prognose [9, 47]. EEine wirklich hohe Chance auf Kuration besteht lediglich bei Tumoren mit einer Größe von ≤1 cm. Solche Tumoren weisen praktisch nie ei­ ne Lymphknotenmetastasierung, eine Ge­ fäßinfiltration, eine perineurale Infiltrati­ on oder Lebermetastasen auf. Bei Resek­ tion dieser Tumoren sind die Chancen auf eine definitive Heilung ausgezeichnet [6]. Aufgrund der retroperitonealen La­ ge des Pankreas verursachen derart klei­ ne Tumoren keine klinischen Symptome. Unspezifische Symptome, wie z. B. Ober­ bauchbeschwerden werden in den meisten Fällen nicht durch den Tumor, sondern durch andere Erkrankungen, wie z. B. ei­ ne chronische Gastritis hervorgerufen. Bei einem Drittel der Patienten findet sich ei­ ne leichte Erhöhung der Leber-/Gallen­ gangs- oder Pankreasenzyme. Aufgrund der extremen Aggressivität des Pankreas­ karzinoms führt bei Nachweis eines klei­ nen, inzidentell entdeckten Pankreaskar­ zinoms eine sich über Monate erstrecken­ de Diagnostik bzw. eine zuwartende Hal­ tung mit der Konsequenz einer Größen­ zunahme des Tumors von 1 cm auf 2 cm Durchmesser zu einer katastrophalen Verschlechterung der Langzeitprognose des Patienten. Neuroendokrine Pankreastumoren ohne klinische Symptomatik Neuroendokrine Tumoren sind charak­ terisiert durch den immunhistologischen Nachweis von charakteristischen Diffe­ renzierungsmarkern wie neuronenspezi­ fische Enolase, Chromogranin A und Syn­ aptophysin. Häufig sezernieren sie große Mengen an Hormonen, die dann zu klas­ sischen klinischen Symptomen führen. Typische Beispiele sind das Insulinom, das Gastrinom und das Vipom. Etwa ein Viertel der neuroendokrinen Tumoren im Pankreas sind aber klinisch stumm, da sie entweder nicht oder nur in geringen Men­ gen Hormone sezernieren oder die sezer­ nierten Hormone keine klinischen Symp­ tome hervorrufen, wie z. B. das „pancre­ atic polypeptide“ [40]. Die Inzidenz der neuroendokrinen Tumoren im Pankreas ist gering. In Pankreaszentren weisen al­ Der Chirurg 8 · 2007 | 713 Leitthema Abb. 1 9 Tpyische Inzidentalome im Pankreas: a Lipom, b Hibernom, c solider pseudopapillärer Tumor, d intraduktale papilläre muzinöse Neoplasie lerdings bis zu 10% der Patienten, die we­ gen eines Tumors einer Pankreasresektion unterzogen werden, einen neuroendokri­ nen Tumor auf. Bei fehlender oder klinisch nicht rele­ vanter Hormonsekretion können die Tu­ moren relativ groß werden, bis sie dann zufällig entdeckt werden. Im Gegensatz zum Insulinom, welches nur selten, d. h. in weniger als 10% der Fälle maligne entartet, weisen die anderen neuroendokrinen Tu­ moren ein hohes Malignitätspotenzial von 60–70% auf. Dies gilt auch für die nicht aktiven neuroendokrinen Tumoren [25]. Das Malignitätsrisiko steigt zwar mit der Tumorgröße. Es gibt aber auch Berichte über eine maligne Entartung von neu­ roendokrinen Tumoren mit einer Größe von 1–3 cm [37]. Hormonell inaktive Tu­ moren werden häufig erst sehr spät dia­ gnostiziert, dennoch ist die Langzeitpro­ gnose nach kurativer Resektion wesent­ lich besser als beim duktalen Pankreas­ karzinom [28]. Die 5­Jahres­Überlebens­ rate liegt bei über 50%. Inzidentalome bei Patienten mit speziellen Erbkrankheiten Für die Bewertung eines soliden Inziden­ taloms im Pankreas ist die Unterschei­ dung, ob es sich um eine sporadische Tu­ 714 | Der Chirurg 8 · 2007 morentstehung handelt oder ob bei dem Patienten eine genetische Systemerkran­ kung vorliegt, von spezieller Bedeutung. Es gibt eine Reihe von erblichen Syndro­ men, die mit einem deutlich erhöhten Ri­ siko für die Entwicklung eines Pankreas­ karzinoms verbunden sind, wie z. B. die hereditäre Pankreatitis, das Peutz­Jegers­ Syndrom oder das HNPCC („heredita­ ry non­polyposis colorectal carcinoma“) [24]. Daneben gibt es auch Familien mit einem massiv erhöhten Pankreaskarzi­ nomrisiko, bei denen der genetische De­ fekt noch nicht abgeklärt ist [43]. Falls bei solchen Patienten im Rahmen von Vor­ sorgeuntersuchungen ein Inzidentalom im Pankreas entdeckt wird, hat dies natür­ lich eine spezielle klinische Tragweite. Auch neuroendokrine Pankreastumo­ ren können im Rahmen von Erbkrank­ heiten auftreten. Zu nennen sind hier das MEN­1­Syndrom, die von Hippel­Lin­ dau­Erkrankung, die Neurofibromatose und die tuberöse Sklerose [36]. Das MEN­ 1­Syndrom ist eine autosomal­dominante Erkrankung mit hoher Penetranz. Charak­ teristisch ist das Auftreten eines Hyperpa­ rathyreoidismus, von Hypophysenadeno­ men sowie von neuroendokrinen Tumo­ ren im Pankreas. Ein größerer Teil dieser neuroendokrinen Tumoren im Pankreas ist nicht funktionell aktiv und entspricht damit den Charakteristika eines Inziden­ taloms. Bei MEN­1­Patienten treten typi­ scherweise die neuroendokrinen Tumo­ ren im Pankreas nicht isoliert, sondern multiple auf [12]. Wichtig ist, dass die Pro­ gnose von Patienten mit MEN­1­Syndrom letztendlich von den sich im Pankreas ent­ wickelnden Tumoren bestimmt wird. Seltene Pankreastumoren Seltene Pankreastumoren sind zwar diffe­ renzialdiagnostisch von Bedeutung, auf­ grund ihrer Inzidenz spielen sie jedoch nur eine untergeordnete Rolle. In den meisten Fällen erfolgt die definitive Di­ agnose erst bei histologischer Untersu­ chung des Operationspräparates. Das primäre Pankreaslymphom ist ex­ trem selten. Weniger als 2% aller extrano­ dalen malignen Lymphome und etwa 0,5% aller Pankreastumoren sind primä­ re Pankreaslymphome. Die prä­ bzw. ggf. postoperative histologische Sicherung eines Lymphoms ist wichtig, da die The­ rapie der Wahl nicht die chirurgische Re­ sektion, sondern eine Kombination von Chemotherapie und Bestrahlung oder die Stammzelltransplantation darstellt [33]. In seltenen Fällen liegt einem bild­ morphologisch nachgewiesenen Pank­ reastumor auch ein Lipom oder ein Hi­ Zusammenfassung · Abstract bernom zugrunde [20]. Diese Tumoren sind grundsätzlich benigne. Typischer­ weise werden sie inzidentell entdeckt (. Abb. 1 a,b). Differenzialdiagnostisch muss ein primäres Pankreassarkom abge­ grenzt werden. Solide pseudopapilläre Tumoren kom­ men vor allem bei jungen Frauen vor [19]. Sie sind in 10–15% der Fälle maligne. Et­ wa ein Drittel wird bei fehlenden Symp­ tomen inzidentell entdeckt (. Abb. 1 c). Mehr als 90% der Patientinnen können durch eine vollständige chirurgische Ent­ fernung geheilt werden. Wenn die Tumo­ ren groß werden, können sie zentral ein­ schmelzen. Solid papilläre Tumoren spie­ len daher auch bei der Differenzialdiag­ nose von großen zystischen Pankreastu­ moren eine Rolle. Im Rahmen der Nachsorge nach Re­ sektion von extrapankreatischen Tumoren können inzidentelle Läsionen im Pankre­ as entdeckt werden. Bei der Autopsie von Patienten mit primärem Nierenzellkarzi­ nom wurden in 1–3% der Fälle Metasta­ sen im Pankreas gefunden. Metachrone Pankreasmetastasen können auch viele Jahre nach Resektion eines Nierenzellkar­ zinoms noch auftreten [16]. Sie sind häu­ fig zunächst symptomlos. Falls es sich um isolierte Metastasen handelt, ist die Indi­ kation zur Resektion durchaus gegeben. Pseudotumoren Ursache eines Inzidentaloms im Pankre­ as können auch Pseudotumoren sein [2]. Am häufigsten handelt es sich um ent­ zündliche Pseudotumoren, die im Verlauf einer chronischen Pankreatitis, einer Au­ toimmunpankreatitis oder einer Paradu­ odenalpankreatitis auftreten können. Die Patienten weisen chronische oder rezidi­ vierende Beschwerden im Oberbauch auf. Im Rahmen der rezidivierenden Untersu­ chungen der Patienten fällt dann gelegent­ lich plötzlich eine fokale Läsion auf, oh­ ne dass sich die bereits seit längerem be­ stehende klinische Symptomatik geändert hätte. Solche Läsionen können deswegen im weiteren Sinne ebenfalls als Inzidenta­ lome bezeichnet werden. Es gibt Hinweise darauf, dass die chro­ nische Pankreatitis einen Risikofaktor für die Entstehung eines Pankreaskarzinoms darstellt. Die zentrale Problematik besteht darin, dass bei Patienten mit chronischer Pankreatitis ein de novo entstandenes duktales Pankreaskarzinom von einem fo­ kalen entzündlichen Pseudotumor weder klinisch noch bildmorphologisch mit an­ nehmbarer Sicherheit unterschieden wer­ den kann (s. unten) [42]. Die Differen­ zialdiagnose ist deswegen so schwierig, da das Pankreaskarzinom typischerwei­ se eine starke desmoplastische Bindege­ websreaktion und eine ausgeprägte peri­ tumoröse Entzündung aufweist. Bei der Autoimmunpankreatitis kann das Vor­ liegen von anderen Autoimmunerkran­ kungen, die Mitbeteiligung der Gallen­ gänge außerhalb des Pankreas und ein hoher IgG4-Spiegel auf die Diagnose hin­ weisen. Beweisend ist ein rasches Anspre­ chen auf eine Kortikoidtherapie [3]. Die Paraduodenalpankreatitis ist charakteri­ siert durch die Ausbildung eines Pseudo­ tumors in unmittelbarer Nachbarschaft zur Duodenalwand, meist im Bereich der Minorpapille. >Pseudotumoren treten im Verlauf einer chronischen Pankreatitis auf Weitere Ursachen für einen Pseudotu­ mor, der in der Bildgebung als Inzidenta­ lom imponieren kann, sind das Pseudo­ lymphom, die heterotope akzessorische Milz und Granulome im Rahmen einer Sarkoidose. Differenzialdiagnose Der Nachweis eines Inzidentaloms im Pankreas erfolgt normalerweise mittels Schnittbildgebung, d. h. mittels CT, MRT oder perkutanem Ultraschall. Die enor­ men technologischen Fortschritte vor allem im Bereich des CT und des MRT haben in den letzten Jahren dazu geführt, dass immer kleinere Tumoren entdeckt werden [30]. Die Artdiagnose ist aber wei­ terhin problematisch. Klassischerweise ist ein duktales Adenokarzinom hypovasku­ larisiert und zeigt deswegen ein verrin­ gertes Enhancement, während neuroen­ dokrine Tumoren typischerweise hyper­ vaskularisiert sind und ein vermehrtes Kontrastmittelenhancement aufweisen. Trotzdem ist eine Differenzialdiagnose zwischen diesen beiden Tumorentitäten Chirurg 2007 · 78:713–720 DOI 10.1007/s00104-007-1373-x © Springer Medizin Verlag 2007 U. Hopt · T. Keck Pankreasinzidentalome. Bewertung und Therapie Zusammenfassung Aufgrund der Fortschritte in der Schnittbildtechnologie werden Inzidentalome im Pankreas zunehmend häufiger diagnostiziert. Wichtig ist die Unterscheidung nach soliden und zystischen Tumoren. Eine definitive Artdiagnose ist häufig weder bei soliden noch bei zystischen Tumoren präoperativ möglich. Die Operationsindikation richtet sich nach dem Risiko einer malignen Entartung. Dementsprechend ist die Operationsindikation bei soliden Inzidentalomen in Abhängigkeit vom Zustand des Patienten und unabhängig von der Größe des Tumors fast immer gegeben. Bei zystischen Inzidentalomen sollten benigne Veränderungen soweit als möglich ausgeschlossen werden. Ansonsten besteht eine Operationsindikation bei einer Größe von >2 cm. Bei Vorliegen einer intraduktalen papillären muzinösen Neoplasie mit entsprechenden Risikofaktoren wird eine Operationsindikation bei einer Größe von ≥1 cm empfohlen. Schlüsselwörter Inzidentalom · Solider Pankreastumor · Zystischer Pankreastumor · Differenzialdiagnose · Operationsindikation Pancreatic incidentalomas. Correct assessment and therapy Abstract Due to recent advances in CT/MRI technology, incidentalomas of the pancreas are detected with increasing frequency. Pancreatic incidentalomas should be differentiated into solid and cystic tumors. In both subgroups definitive classification of the tumor is often not possible. Operative therapy is recommended in premalignant or malignant pathologies. Thus solid incidentalomas should be resected independently of their size, if the patient is without serious comorbidities. In case of cystic incidentalomas, benign cystic lesions should be excluded as far as possible. Otherwise they should be resected if their size is ≥2 cm. In case of IPMN with specific risk factors, resection is recommended when the tumor size exceeds 1 cm. Keywords Cystic pancreatic tumor · Differential diagnosis · Incidentaloma · Indication for operation · Solid pancreatic tumor Der Chirurg 8 · 2007 | 715 Leitthema häufig nicht mit ausreichender Sicher­ heit möglich. Noch wesentlich problema­ tischer ist der Versuch bildmorphologisch ein Pankreaskarzinom von einem ent­ zündlichen Pseudotumor, z. B. bei chro­ nischer Pankreatitis zu unterscheiden. Le­ diglich Lipome lassen sich im CT/MRT mit ausreichender Sicherheit diagnosti­ zieren [13]. >Die Artdiagnose ist problematisch Der endoskopische Ultraschall (EUS) ist hervorragend geeignet, das Pankreas dar­ zustellen. Es wird immer wieder betont, dass der EUS in geübter Hand dem CT/ MRT überlegen ist [27]. Zu bedenken ist allerdings, dass der EUS extrem unter­ sucherabhängig ist. Dies wird durch die Tatsache unterstrichen, dass bei Beurtei­ lung desselben Befundes durch drei ver­ schiedene, sehr erfahrene Untersucher die Überstimmung der EUS-Befunde nur sehr mäßig ist [4]. Die mittels EUS durch­ geführte Feinnadelbiopsie ist sicher we­ sentlich aussagekräftiger als die früher propagierte Bürstenzytologie. Die Spe­ zifität hinsichtlich des Nachweises eines Malignoms ist sehr hoch, die Sensitivität aber weiter­hin unzureichend. Dies gilt vor allem bei gleichzeitigem Vorliegen von chronisch entzündlichen Veränderungen wie z. B. bei der chronischen Pankreati­ tis [45]. Selbst bei Befunden, bei denen von der Biopsie her ein maligner Tumor sicher ausgeschlossen wird, liegt die Ra­ te an falsch-negativen Befunden weiter­ hin bei 10–25%. Ein negativer Befund der Feinnadelbiopsie kann demnach nicht zum Ausschluss einer Operationsindika­ tion führen. Sinn eines PET oder PET-CT bei Vor­ liegen eines Inzidentaloms ist der Nach­ weis oder Ausschluss einer malignen Ent­ artung des Tumors. Leider ist die Sensi­ tivität des PET bzw. PET-CT bei kleinen Tumoren immer noch unzureichend. Es gibt ferner falsch-positive und falsch-ne­ gative PET-Befunde. Der negativ prädik­ tive Wert des PET-CT für maligne Pank­ reastumoren liegt lediglich bei 64% [15]. Prämaligne Tumoren sind ohnehin PETnegativ. Ob bei Vorliegen eines kleinen Pankreastumors ein negativer PET-Be­ fund einen Einfluss auf das Ausmaß und 716 | Der Chirurg 8 · 2007 die Radikalität der Operation hat, ist um­ stritten. Die Somatostatin-Rezeptor-Szinti­ graphie ist hochspezifisch und hat einen positiv prädiktiven Wert von annähernd 100%. Leider ist die Rate an falsch-nega­ tiven Befunden gerade bei hormoninak­ tiven Tumoren sehr hoch. Die Sensitivität liegt bei unter 70% [26]. Die Somatosta­ tin-Rezeptor-Szintigraphie ist ferner aus­ schließlich zum Nachweis eines neuro­ endokrinen Tumors, nicht aber zur Dif­ ferenzialdiagnose zwischen benigne und maligne geeignet. Der Einsatz von Tumormarkern zur Differenzialdiagnose zwischen benignen und malignen soliden Inzidentalomen ist wenig sinnvoll. Der Überlappungsbereich für beide Entitäten ist sehr groß [29]. Je nach Cutt-off-Level steigt die Spezifi­ tät bei gleichzeitiger Reduktion der Sen­ sitivität und vice versa. Bei kleinen, in­ zidentell diagnostizierten Tumoren sind auch im Falle einer malignen Entartung die Tumormarker im Blut verständlicher­ weise nicht oder nur mäßig erhöht. Der Versuch im Pankreassaft genetische Ver­ änderungen wie zum Beispiel K-ras-Mu­ tationen etc. nachzuweisen, ist zur Bestä­ tigung oder zum Ausschluss einer malig­ nen Läsion im Pankreas im Moment noch nicht Erfolg versprechend [21]. ESämtliche uns derzeit zur Verfügung stehenden Untersuchungsverfahren sind demnach nicht in der Lage, mit ausreichender Sicherheit benigne von prämalignen bzw. malignen Tumoren im Pankreas zu unterscheiden. Beim sicheren Nachweis eines soliden In­ zidentaloms im Pankreas mittels Schnitt­ bilddiagnostik sind deswegen weitere dia­ gnostische Verfahren nicht angezeigt. Falls im CT/MRT nur der Verdacht auf ein soli­ des Inzidentalom besteht, ist eine zusätz­ liche EUS-Untersuchung indiziert. Operationsindikation und Radikalität der Operation Da die überwiegende Mehrzahl der so­ liden Tumoren im Pankreas prämaligne oder maligne ist, besteht bei inzidentellem Nachweis eines solchen Tumors im Pank­ reas immer eine Operationsindikation. Lediglich bei MEN-1-Patienten mit hor­ moninaktiven neuroendokrinen Tumo­ ren <1 cm kann unter Umständen zuge­ wartet werden. Auch bei Verdacht auf ein primäres Pankreaslymphom ergibt sich ein anderes Vorgehen. Bei solchen Pati­ enten sollte eine Diagnosesicherung mit­ tel Biopsie oder laparoskopischer Lymph­ knotenentnahme versucht werden, da die Therapie dieses Tumors primär mittels Chemotherapie bzw. Strahlentherapie er­ folgt. Bei hochgradigem Verdacht auf ei­ ne Immunpankreatitis ist unter Umstän­ den zunächst ein kurzfristiger Therapie­ versuch mit Steroiden angezeigt. >Die Operation sollte onkologisch radikal erfolgen Wegen des hohen Malignitätsrisikos sollte die Operation in der Regel onkologisch ra­ dikal erfolgen [22]. Bei neuroendokrinen Tumoren wird gelegentlich vorgeschlagen, diese nur zu enukleieren bzw. organerhal­ tend durch Pankreasteilresektion zu re­ sezieren [10]. Dabei ist allerdings zu be­ denken, dass die Fistelrate nach Enuklea­ tion deutlich höher ist als nach einer Re­ sektion. Die Frage, ob ein Tumor malig­ ne ist, lässt sich häufig im Schnellschnitt nicht klären. Es ist weiterhin zweifelhaft, ob z. B. der partielle Erhalt des Pankreas­ kopfes oder der Duodenalpassage lang­ fristig eine wesentliche Verbesserung der Lebensqualität im Vergleich zur klas­ sischen Pankreaskopfresektion mit sich bringt. Bei linksseitig gelegenen, inziden­ tell entdeckten neuroendokrinen Tumo­ ren sind aber durchaus Verfahren mit ein­ geschränkter Radikalität wie eine milzer­ haltende Pankreaslinksresektion oder ei­ ne zentrale Pankreasresektion zu disku­ tieren. Ähnlich ist die Situation bei MEN1-Patienten mit multiplen neuroendokri­ nen Tumoren [5]. Hier wird eine Pankre­ aslinksresektion und die Enukleation der dann noch verbleibenden Tumoren aus dem Pankreaskopf empfohlen, um diese Patienten nicht einer totalen Pankreatek­ tomie mit sekundärem insulinpflichtigem Diabetes zuführen zu müssen. Zystische Pankreasinzidentalome Zystische Veränderungen im Pankreas werden mit der modernen Bildgebung immer häufiger entdeckt. In der Mehr­ zahl der Fälle handelt es sich um Pank­ reaspseudozysten. Die Patienten haben dann in der Regel eine typische Anam­ nese hinsichtlich einer akuten bzw. chro­ nischen Pankreatitis. Bei 10–20% handelt es sich aber um zystische Tumoren [34]. Diese verursachen, solange sie klein sind, keine klinischen Symptome und werden deshalb in der Regel inzidentell entdeckt. Wie bei den soliden Inzidentalomen gibt es auch bei den zystischen Pankreastu­ moren ganz unterschiedliche Tumorenti­ täten, die entweder als grundsätzlich be­ nigne, als prämaligne oder als definitiv maligne eingestuft werden müssen. Seröses Zystadenom Der Tumor besteht in der Regel aus vie­ len kleinen Zysten und weist deswegen in der Bildgebung eine bienenwabenartige Struktur auf. Es gibt aber auch eine ma­ krozystische Variante. Fast 80% der se­ rösen Zystadenome finden sich bei älteren Frauen. Die Tumoren sind immer gutar­ tig, können aber wachsen. Bei einer Größe von unter 2 cm ist die Wachstumstendenz offensichtlich sehr gering. Bei einer Grö­ ße von ≥4 cm scheint die Wachstumsge­ schwindigkeit deutlich erhöht [44]. Symp­ tomatisch werden seröse Zystadenome le­ diglich aufgrund ihrer Größe. Muzinöses Zystadenom Das muzinöse Zystadenom (MCN) ist ein makrozystischer Tumor bestehend aus einer oder mehreren Zysten. Charak­ teristisch sind die Mucinproduktion des Zystenepithels sowie ein „ovarähnliches“ Stroma. Die Läsion kommt fast nur bei Frauen um die Menopause vor und ist fast immer im Pankreaskorpus oder im Pank­ reasschwanz lokalisiert [34]. Eine Verbin­ dung zum Pankreasgang besteht nicht. Muzinöse Zystadenome sind potenziell maligne. Bei kurativer Resektion ist das Rezidivrisiko sehr gering. Etwa 15–20% der MCN sind definitiv maligne. Sie wer­ den dann als muzinöses Zystadenokarzi­ nom bezeichnet. Intraduktale papilläre muzinöse Neoplasie Unter den mucinproduzierenden Pank­ reastumoren ist zwischenzeitlich die in­ traduktale papilläre muzinöse Neoplasie (IPMN) als eigenständiges Krankheits­ bild definiert (. Abb. 1 d). Unterschie­ den wird die „Main-Duct“-IPMN und die „Branch-Duct“-IPMN [34]. Charak­ teristisch für die „Main Duct“-IPMN ist ein auf über 1 cm erweiterter Pankreas­ hauptgang, der mit hochviskösem Mucin angefüllt ist. Beweisend für das Vorliegen einer IPMN ist bei der endoskopisch re­ trograden Cholangiopankreatikographie (ERCP) der Nachweis von zähflüssigem Mucin, welches sich aus der stark promi­ nenten Papille ergießt. Betroffen von der „Main-Duct“-IPMN sind meistens Män­ ner in der 6. und 7. Lebensdekade. Bei der „Branch-Duct“-IPMN be­ schränkt sich der mucinproduzierende Tumor auf einen oder mehrere Seitenäste des Pankreashauptganges. Diese sind zys­ tisch aufgeweitet. Häufig davon betroffen ist der Processus uncinatus. In seltenen Fällen gibt es auch multifokale Befunde. >Die IPMN ist ein potenziell maligner Tumor Die IPMN ist ein potenziell maligner Tu­ mor. Die Dignität wird histologisch ein­ geteilt in benigne, borderline und maligne (nichtinvasiv/invasiv). Die „Main-Duct“IPMN hat mit 70% ein deutlich höheres Malignitätsrisiko als die isolierte „BranchDuct“-IPMN mit 25%. Das Vorhanden­ sein von klinischen Symptomen, eine Tu­ morgröße von über 3 cm, der Nachweis von knotigen Veränderungen in der Wand („mural nodules“) und eine Aufweitung des Pankreashauptganges auf über 6 mm stellen Risikofaktoren für das Vorliegen einer malignen Entartung dar [41]. Ande­ rerseits weisen bis zu 20% der Patienten mit einer weitgehend oder völlig asympto­ matischen IPMN im histologischen Prä­ parat ein Carcinoma in situ oder ein in­ vasives Karzinom auf [35]. Bei Operation im prämalignen Stadium ist eine defini­ tive Heilung erreichbar. Postoperative Re­ zidive sind allerdings auch bei negativem Schnittrand nicht ungewöhnlich und wei­ sen auf ein multifokales Geschehen oder eine globale Störung des Pankreasgang­ epithels hin. Bei Vorliegen eines infiltra­ tiv wachsenden Karzinoms ist die Progno­ se mit einer 5-Jahres-Überlebensrate von 40% nur wenig besser als beim duktalen Pankreaskarzinom. Seltene zystische Tumoren Bei raschem Größenwachstum oder ge­ störter Gefäßversorgung können auch bei primär soliden Tumoren durch eine zen­ trale Nekrose zystische Bereiche entstehen [31]. Beschrieben ist dies für neuroendo­ krine Tumoren, das duktale Adenokarzi­ nom und den solid-pseudopapillären Tu­ mor. Typisch ist die Kombination von zys­ tischen und soliden Tumoranteilen. Eine Abgrenzung von den typischen zystischen Tumoren ist bildmorphologisch in der Re­ gel nur sehr eingeschränkt möglich. Kongenitale Pankreaszysten Grundsätzlich abgegrenzt werden müs­ sen von den zystischen Pankreastumoren die kongenitalen Pankreaszysten. Sie fin­ den sich gehäuft bei Patienten mit einer von Hippel-Lindau-Erkrankung, bei Pati­ enten mit polyzystischen Nieren- und Le­ bererkrankungen oder auch bei Vorliegen einer zystischen Fibrose. Da es sich nicht um zystische Tumoren handelt, sind diese Zysten immer benigne und haben in der Regel keine klinische Relevanz. Differenzialdiagnose Nach Ausschluss von kongenitalen Zys­ ten in Folge von Erbkrankheiten (s. oben) muss zunächst unterschieden werden zwischen Pankreaspseudozysten und zys­ tischem Pankreastumor. Entscheidend ist die Anamnese hinsichtlich einer akuten oder einer chronischen Pankreatitis. Oft finden sich dann die typischen bildmor­ phologischen Zeichen einer chronischen Pankreatitis wie Parenchymverkalkungen und Gangveränderungen. Typischerwei­ se ist die gesamte Drüse bildmorpholo­ gisch verändert. Abzugrenzen davon sind aber die Patienten, bei denen die Ätiolo­ gie der Pankreatitis ungeklärt ist. Das­ selbe gilt für CT-Befunde, bei denen die Verkalkungen ausschließlich in der Zys­ tenwand nachweisbar sind und bei de­ Der Chirurg 8 · 2007 | 717 Leitthema nen das gesamte übrige Pankreasparen­ chym sich völlig normal darstellt. Bei die­ sen Patienten ist die Wahrscheinlichkeit, dass der zystische Befund nicht eine Pseu­ dozyste, sondern einen zystischen Tumor darstellt, sehr hoch. Bei der Zystenpunk­ tion ergibt sich bei der Pankreaspseudo­ zyste typischerweise ein hoher Amylase­ wert und ein niedriger bis nicht nachweis­ barer CEA-Wert. EBei einem signifikanten Anteil der zystischen Befunde kann aber letztendlich nicht mit ausreichender Sicherheit präoperativ zwischen Pankreaspseudozyste und zystischem Tumor unterschieden werden [23]. Klarheit darüber ergibt sich dann erst durch die histologische Untersuchung der Zystenwand im Rahmen einer ausgedehn­ ten Biopsie oder nach Resektion des Ge­ samtbefundes. Dementsprechend wurden in einzelnen operativen Serien bis zu 50% der resezierten zystischen Pankreastumo­ ren primär als Pseudozyste fehldiagnosti­ ziert [34]. Die Unterscheidung zwischen gene­ rell benignen zystischen Tumoren wie dem serösen Zystadenom und poten­ ziell malignen/definitiv maligne entar­ teten zystischen Tumoren wie dem muzi­ nösen Zystadenom, dem muzinösen Zyst­ adenokarzinom und der IPMN ist häufig bildmorphologisch nicht mit letzter Si­ cherheit möglich [32]. Es gibt zwar häu­ fig typische Befunde wie das bienenwa­ benartige Bild beim serösen Zystadenom oder den stark dilatierten Pankreashaupt­ gang bei der „Main-Duct“-IPMN, die ei­ ne weitgehend sichere Diagnose ermögli­ chen. Andererseits gibt es aber sehr häu­ fig überlappende und nicht eindeutige Be­ funde. Hinsichtlich der Differenzialdiag­ nose kann dann die Berücksichtigung der typischen Alters- und Geschlechtsvertei­ lung sowie der typischen Lokalisation der verschiedenen zystischen Pankreastumo­ ren hilfreich sein [34]. Ein weiteres, wich­ tiges Unterscheidungsmerkmal zwischen der IPMN und der MCN ist die Tatsache, dass die IPMN im Gegensatz zur MCN immer eine Verbindung zum Pankreas­ gangsystem hat. Obwohl immer wieder enthusiastische Bericht über die Möglichkeiten des EUS 718 | Der Chirurg 8 · 2007 publiziert werden, gibt es auch bei diesem Verfahren einen großen Graubereich bei der Differenzialdiagnose von zystischen Pankreastumoren [7]. Die zytologische Diagnostik der Zystenflüssigkeit nach EUS-geführter Feinnadelbiopsie ist nur selten hilfreich. Hinsichtlich der Diagnose eines mucinproduzierenden Tumors liegt die Genauigkeit bei nur 54%. Eine bessere diagnostische Aussagekraft hat die Unter­ suchung der Zystenflüssigkeit auf Amy­ lase und CEA [46]. Hohe Amylasewer­ te weisen auf eine Verbindung der zysti­ schen Läsion zum Pankreasgangsystem hin. Typisch ist dies bei der Pankreaspseu­ dozyste und bei der IPMN. Hohe CEAWerte sind charakteristisch für mucinpro­ duzierende Tumoren wie die IPMN und die MCN, niedrige CEA-Werte typisch für Pseudozysten und das seröse Zystade­ nom. Bei niedrigem CEA-Wert kann al­ lerdings ein mucinproduzierender Tumor nicht mit letzter Sicherheit ausgeschlossen werden. In der Literatur werden zur Di­ agnose eines mucinproduzierenden Tu­ mors unterschiedliche, mehr oder weni­ ger willkürlich festgelegte Cutt-off-Werte der CEA-Konzentration in der Zystenflüs­ sigkeit empfohlen. Am häufigsten wird ein Cutt-off-Wert von 192 ng/ml genannt [8]. Je höher der Cutt-off-Wert festgelegt wird, desto mehr steigt verständlicherwei­ se die Spezifität, allerdings mit dann sin­ kender Sensitivität. Wirklich hilfreich bei der Therapieentscheidung sind letztend­ lich nur sehr hohe oder kaum nachweis­ bare CEA-Werte. >Die IPMN hat im Gegensatz zur MCN immer eine Verbindung zum Pankreasgangsystem Die Aussagekraft eines PET ist bei zysti­ schen Pankreastumoren noch wenig un­ tersucht. Bei positivem Befund besteht ei­ ne hohe Wahrscheinlichkeit auf eine be­ reits vorhandene maligne Entartung [38]. Die Rate an falsch-negativen Befunden ist bisher aber noch nicht bekannt. Prämalig­ ne Befunde, die ebenfalls eine Operations­ indikation darstellen, werden durch das PET nicht erfasst. Der zusätzliche Nutzen einer PET-Untersuchung bei zystischen Inzidentalomen hinsichtlich der OP-In­ dikation ist demnach fragwürdig. Operationsindikation und Radikalität der Operation Pankreaszysten/zystische Tumoren mit einem Durchmesser unter 2 cm, die kei­ ne Symptome verursachen, keine Septen, keine knotigen soliden Veränderungen in der Wand und kein Kontrastmittelenhan­ cement in der Schnittbildgebung aufwei­ sen, haben ein extrem geringes Risiko der malignen Entartung. Sie können ohne Ri­ siko beobachtet und kontrolliert werden [14]. Das schließt aber nicht aus, dass es sich um prämaligne Befunde handelt, die im weiteren Verlauf operationspflich­ tig werden [11]. Bei Vorliegen von Symp­ tomen und Risikofaktoren in der Schnitt­ bildgebung (s. oben) können allerdings auch solch kleine Befunde bereits eine Operationsindikation darstellen. Seröse Zystadenome sind immer be­ nigne und stellen per se keine Operati­ onsindikation dar. Da sie ab einer Größe von 4 cm aber eine erhöhte Wachstums­ tendenz aufweisen und damit zunehmend mechanische Probleme verursachen kön­ nen, kann bei Patienten mit längerer Le­ benserwartung und geringem Operati­ onsrisiko eine Resektion erwogen wer­ den [44]. >Mucinproduzierende Tumoren können generell als prämaligne angesehen werden Mucinproduzierende Tumoren können generell als prämaligne angesehen wer­ den. In Abhängigkeit vom Allgemeinzu­ stand und den Begleiterkrankungen des Patienten besteht demnach eine grund­ sätzliche Operationsindikation. Von Be­ deutung für die Operationsindikation und Operationstaktik sind die Größe des Befundes, die Frage, ob Symptome beste­ hen und das Vorliegen von malignitäts­ verdächtigen Befunden in der Schnittbild­ gebung. Bereits das Vorliegen von Symp­ tomen erhöht die Wahrscheinlichkeit ei­ ner malignen Entartung bei zystischen Pankreastumoren von 23% auf 66% [39]. Bei der IPMN gibt es aktuelle Leit­ linien einer Konsensuskonferenz [41]. Demnach stellt eine „Main-Duct“-IPMN eine grundsätzliche Operationsindikation dar. Bei der „Branch-Duct“-IPMN mit ei­ ner Größe unter 1 cm kann zunächst zu­ gewartet werden. Bei einer Größe von 1– 3 cm kann bei fehlenden Risikofaktoren, d. h. fehlender klinischer Symptomatik, Pankreasgang <6 mm, keine knotigen Befunde in der Wand („mural nodules“) ebenfalls zugewartet werden. Bei Tumo­ ren mit einer Größe von über 3 cm bzw. bei einer Größe von 1–3 cm und Vorlie­ gen der erwähnten Risikofaktoren sollte die Resektion erfolgen. Falls beim serösen Zystadenom die Operationsindikation gestellt wird, kann die Operation eingeschränkt radikal erfol­ gen. Falls technisch möglich genügt eine Enukleation. Eingeschränkt radikale Ver­ fahren wie eine zentrale Pankreasresekti­ on, eine milzerhaltende Pankreaslinksre­ sektion oder eine duodenumerhaltende Pankreaskopfresektion sind möglich. Zu bedenken ist allerdings, dass insbesonde­ re bei lokaler Enukleation die Häufigkeit von postoperativen Pankreasfisteln deut­ lich erhöht ist. Prämaligne Tumoren, d. h. alle mucin­ produzierenden zystischen Tumoren und zystische Tumoren unklarer Dignität soll­ ten radikal reseziert werden [18]. Je nach Lokalisation ist die onkologische Pankre­ askopfresektion bzw. Pankreaslinksresek­ tion indiziert. Der Nutzen einer Lymph­ adenektomie ist umstritten, da maligne entartete zystische Pankreastumoren im Gegensatz zum duktalen Pankreaskarzi­ nom sehr selten lymphogen metastasie­ ren. Bei kleinen, exzentrisch gelegenen muzinösen Zystadenomen wird gelegent­ lich auch die Enukleation empfohlen [39]. Vorteil ist das geringere Ausmaß der Ope­ ration, der Erhalt von gesundem Pankre­ asparenchym und die Möglichkeit, den Eingriff laparoskopisch durchführen zu können. Eine solche Entscheidung muss immer abhängig gemacht werden vom in­ dividuellen Risiko einer bereits vorhande­ nen malignen Entartung (s. oben). Zu be­ denken ist ferner, dass mit allen derzeit zur Verfügung stehenden Untersuchungsver­ fahren eine maligne Entartung nicht mit ausreichender Sicherheit ausgeschlossen werden kann, dass die definitive Festle­ gung, ob eine maligne Entartung vorliegt, auch im Schnellschnitt häufig nicht mög­ lich ist und dass damit immer das Risiko besteht, einen malignen Tumor intraope­ rativ eröffnet bzw. onkologisch nicht aus­ reichend reseziert zu haben. Ob ein prä­ operativ negativer PET-Befund dieses Ri­ siko deutlich reduziert, ist noch unklar. Während die Indikation zur Opera­ tion bei der IPMN seit kurzem gut defi­ niert ist, steht das Ausmaß der Resektion weiterhin zur Debatte [35, 41]. Von vielen wird vor allem bei der „Main-Duct“-IP­ MN die klassische onkologische Pankre­ askopf- bzw. Pankreaslinksresektion un­ ter Berücksichtigung des Schnellschnitt­ ergebnisses empfohlen. Bei der „BranchDuct“-IPMN werden dagegen häufig ein­ geschränkte Resektionsverfahren ange­ wandt. Andererseits wird bei multifoka­ len Befunden z. T. auch die Indikation zur totalen Pankreatektomie gesehen. Klare Entscheidungskriterien für den Einzelfall müssen erst erarbeitet werden. Fazit für die Praxis Inzidentalome im Pankreas werden zunehmend häufiger diagnostiziert. Bei soliden Inzidentalomen ist wegen des hohen Malignitätsrisikos die Operationsindikation sehr weit zu stellen. Das gilt auch für Tumoren mit einem Durchmesser von ≤1 cm. Von Bedeutung ist dabei die katastrophale Prognose von größeren duktalen Pankreaskarzinomen. Bei zystischen, inzidentell entdeckten Pankreasprozessen sollten zunächst so weit als möglich kongenitale Zysten und Pseudozysten ausgeschlossen werden. Bei Verdacht auf einen zystischen Pankreastumor kann bei einer Tumorgröße von ≤2 cm zugewartet werden. Zu bedenken ist allerdings, dass bei 50% dieser kleinen Tumoren ein prämaligner Zustand vorliegt und dass sie bei Wachstumstendenz unbedingt reseziert werden müssen [11]. Eine zuverlässige Überwachung der Patienten ist deswegen absolut notwendig. Dementsprechend kann auch bei jüngeren Patienten ohne spezielles Risiko und dringendem Verdacht auf einen mucinproduzierenden Tumor durchaus auch die Operationsindikation bei Tumoren ≤2 cm gestellt werden. Gleiches gilt auch für Patienten mit „Main-Duct“-IPMN und bei Patienten mit „Branch-Duct“-IPMN und entsprechenden Risikofaktoren. Da bei Patienten mit einem Inzidentalom im Falle einer Operation häufig prämaligne oder gar vollständig benigne Tu- Leitthema moren entfernt werden, muss das Operationsrisiko so gering wie möglich gehalten werden. Das gilt speziell für die postoperative Mortalität nach Pankreaskopfresektion. Diese liegt in Pankreaszentren heutzutage bei deutlich unter 5% [1, 9]. Zu bedenken ist, dass formale Pankreasresektionen bei kleinen Tumoren nicht einfacher, sondern wegen des in der Regel völlig unveränderten und sehr weichen Pankreasparenchyms eher schwierig sind [17, 47]. Inzidentalome im Pankreas sind relativ selten. Ihre Differenzialdiagnose ist schwierig. Patienten mit derartigen Befunden sollten deswegen in Zentren mit entsprechender Erfahrung behandelt werden. Nur dort kann eine nach unserem derzeitigen Wissen sinnvolle Entscheidung hinsichtlich Zuwartens bzw. Operation getroffen werden. Korrespondenzadresse Prof. Dr. Dr. h.c. U. Hopt Abteilung für Allgemein- und Viszeralchirurgie, Chirurgische Universitätsklinik, Hugstetter Straße 55, 79106 Freiburg [email protected] Interessenkonflikt. Der korrespondierende Autor gibt an, dass kein Interessenkonflikt besteht. Literatur 1. Adam U, Makowiec F, Riediger H et al. (2004) Risk factors for complications after pancreatic head resection. Am J Surg 187: 201–208 2. Adsay NV, Basturk O, Klimstra DS, Klöppel G (2004) Pancreatic pseudotumors: non-neoplastic solid lesions of the pancreas that clinically mimic pancreas cancer. Sem Diagnost Pathol 21: 260–267 3. Adsay NV, Basturk O, Thirabanjasak D (2005) Diagnostic features and differential diagnosis of autoimmune pancreatitis. Sem Diagn Pathol 22: 309– 317 4. Ahmad NA, Kochman ML, Brensinger C et al. (2003) Interobserver agreement among endosonographers for the diagnosis of neoplastic versus non-neoplastic pancreatic cystic lesions. Gastrointest Endosc 58: 59–64 5. Akerström G, Hessman O, Skogseid B (2002) Timing and extent of surgery in symptomatic and asymptomatic neuroendocrine tumors of the pancreas in MEN 1. Langenbeck’s Arch Surg 386: 558– 569 6. Ariyama J, Suyama M, Satoh K, Sai J (1998) Imaging of small pancreatic ductal adenocarcinoma. Pancreas 16: 396–401 7. Bounds BC, Brugge WR (2001) EUS Diagnosis of cystic lesions of the pancreas. Int J Gastrointest Cancer 30: 27–31 8. Brugge WR, Lewandrowski K, Lee-Lewandrowski E et al. (2004) Diagnosis of pancreatic cystic neoplasms: a report of the cooperative pancreatic cyst study. Gastroenterology 126: 1330–1336 720 | Der Chirurg 8 · 2007 9. Cameron JL, Riall TS, Coleman JA, Belcher KA (2006) One thousand consecutive pancreaticoduodenectomies. Ann Surg 244: 10–15 10. Dralle H, Krohn SL, Karges W et al. (2004) Surgery of resectable nonfunctioning neuroendocrine pancreatic tumors. World J Surg 28: 1248–1260 11. Fernandez-del Castillo C, Targaroma J, Thayer SP et al. (2003) Incidental pancreatic cysts. Clinicopathologic characteristics and comparison with symptomatic patients. Arch Surg 138: 427–434 12. Grama D, Skogseid B, Wilander E et al. (1992) Pancreatic tumors in multiple endocrine neoplasia type 1: clinical presentation and surgical treatment. World J Surg 16: 611–619 13. Gritzmann N, Macheiner P, Hollerweger A, Hübner E (2004) CT in the differentiation of pancreatic neoplasms – progress report. Dig Dis 22: 6–17 14. Handrich SJ, Hough DM, Fletcher JG, Sarr MG (2005) The natural history of the incidentally discovered small simple pancratic cysts: long-term follow-up and clinical implications. AJR 184: 20–23 15. Heinrich S, Goerres GW, Schäfer M et al. (2005) Positron emission tomography / computed tomography influences on the management of resectable pancreatic cancer and its cost-effectiveness. Ann Surg 242: 235–243 16. Hirota T, Tomida T, Iwasa M et al. (1996) Solitary pancreatic metastasis occurring eight years after nephrectomy for renal cell carcinoma. Int J Pancreatol 19: 145–153 17. Hopt UT, Makowiec F, Adam U (2004) Nahtinsuffizienzen im biliopankreatischen Bereich. Chirurg 75: 1079–1087 18. Horvath KD, Chabot JA (1999) An aggressive resectional approach to cystic neoplasms of the pancreas. Am J Surg 178: 269–274 19. Kang CM, Kim KS, Choi JS et al. (2006) Solid pseudopapillary tumor of the pancreas suggesting malignant potential. Pancreas 32: 276–280 20. Katz DS, Nardi PM, Hines J et al. (1998) Lipomas of the pancreas. AJR 170: 1485–1487 21. Kimura W, Zhao B, Futukawa N et al. (1999) Significance of K-ras codon 12 point mutation in pancreatic juice in the diagnosis of carcinoma of the pancreas. Hepato-Gastroenterol 46: 532–539 22. Lairmore T, Chen VY, DeBenedetti MK et al. (2000) Duodenopancreatic resections in patients with multiple endocrine neoplasia type 1. Ann Surg 231: 909–918 23. Le Borgne J, de Calan L, Partensky C, and the French Surgical Association (1999) Cystadenomas and cystadenocarcinomas of the pancreas. A multiinstitutional restrospective study of 398 Cases. Ann Surg 230: 152–161 24. Lowenfels AB, Maisonneuve EP, Dimagno YE et al. and International Hereditary Pancreatitis Study Group (1997) Hereditary pancreatitis and the risk of pancreatic cancer. J Natl Cancer Inst 89: 442– 446 25. Matthews BD, Heniford BT, Reardon PR et al. (2000) Surgical experience with nonfunctioning neuroendocrine tumors of the pancreas. Am Surg 66: 1116–1122 26. Meko JB, Doherty GM, Siegel BA, Norton JA (1996) Evaluation of somatostatin-receptor scintigraphy for detecting neuroendocrine tumors. Surgery 120: 975–984 27. Mertz HR, Sechopoulos P, Delbeke D, Leach SD (2000) EUS, PET, and CT scanning for evaluation of pancreatic adenocarcinoma. Gastrointest Endosc 52: 367–371 28. Mulkeen AL, Yoo PS, Cha C (2006) Less common neoplasms of the pancreas. World J Gastroenterol 12: 3180–3185 29. Nazli O, Bozdag AD, Tansug T et al. (2000) The diagnostic importance of CEA and CA 19–9 for the early diagnosis of pancreatic carcinoma. HepatoGastroenterol 47: 1750–1752 30. Nichols MT, Russ PD, Chen YK (2006) Pancreatic Imaging. Current and emerging technologies. Pancreas 33: 211–220 31. Park MS, Kim KW, Lim JS et al. (2005) Unusual cystic neoplasms in the pancreas. Radiologic-pathologic correlation. J Comput Assist Tomogr 29: 610– 616 32. Procacci C, Biasiutti C, Carbognin G et al. (1999) Characterization of cystic tumors of the pancreas: CT accuracy. J Comput Assist Tomogr 23: 906–912 33. Saif MW (2006) Primary pancreatic lymphomas. J Pancreas 7: 262–273 34. Sakorafas GH, Sarr MG (2005) Cystic neoplasms of the pancreas; what a clinician should know. Cancer Treatm Rev 31: 507–535 35. Sakorafas GH, Sarr MG, Velde CJH van de, Peros G (2005) Intraductal papillary mucinous neoplasms of the pancreas: a surgical perspective. Surg Oncol 14: 155–178 36. Simon P, Spilcke-Liss E, Wallaschofski H (2006) Endocrine tumors of the pancreas. Endocrinol Metab Clin N Am 35: 431–447 37. Solorzano CC, Lee JE, Pisters PWT et al. (2001) Nonfunctioning islet cell carcinoma of the pancreas: survival results in a contemporary series of 163 patients. Surgery 130: 1078–1085 38. Sperti C, Pasquali C, Giandomenico D et al. (2005) F-18 Fluorodeoxyglucose positron emission tomography in differentiating malignant from benign pancreatic cysts: a prospective study. J Gastrointest Surg 9: 22–29 39. Spinelli KS, Fromwiller TE, Daniel RA et al. (2004) Cystic pancreatic neoplasms. Observe or operate. Ann Surg 239: 651–659 40. Stephen AE, Hodin RA (2006) Neuroendocrine tumors of the pancreas, excluding gastrinoma. Surg Oncol N Am 15: 497–510 41. Tanaka M, Chari S, Adsay V et al. (2006) International consensus guidelines for management of intraductal papillary mucinous neoplasms and mucinous cystic neoplasms of the pancreas. Pancreatology 6: 17–32 42. Taylor B (2003) Carcinoma of the head of the pancreas versus chronic pancreatitis: diagnostic dilemma with significant consequences. World J Surg 27: 1249–1257 43. Tersmette AC, Petersen GM, Offerhaus GJA et al. (2001) Increased risk of incident pancreatic cancer among first-degree relatives of patients with familial pancreatic cancer. Clin Cancer Res 7: 738–744 44. Tseng JF, Warshaw AL, Sahani DV et al. (2005) Serous cystadenoma of the pancreas. Ann Surg 242: 413–421 45. Varadarujulu S, Tamhane A, Eloubeidi MA (2005) Yield of EUS-guided FNA of pancreatic masses in the presence or the absence of chronic pancreatitis. Gastrointest Endosc 62: 728–736 46. Waaij LA van der, van Dullemen HM, Porte RJ (2005) Cyst fluid analysis in the differential diagnosis of pancreatic cystic lesions: a pooled analyisis. Gastrointest Endosc 62: 383–389 47. Winter JM, Cameron JL, Lillemoe KD et al. (2006) Periampullary and pancreatic incidentaloma. A single institution’s experience with an increasingly common diagnosis. Ann Surg 243: 673–683