ZD6474 blockiert zwei Signalwege der Tumorprogression
Werbung

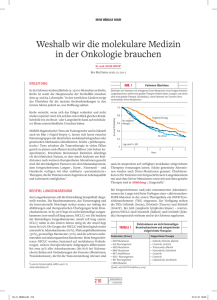
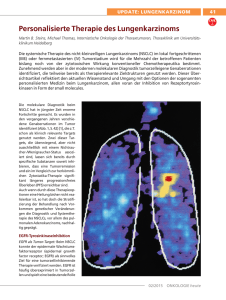
PharmaForum ZD6474 blockiert zwei Signalwege der Tumorprogression Die Einführung neuer platinhaltiger Regime und effektiver Zweitlinientherapien hat sich für Patienten mit fortgeschrittenem nichtkleinzelligen Bronchialkarzinom (NSCLC) in einer moderaten Überlebensverlängerung ausgezahlt. Damit ist aber heute die Effektivität der Chemotherapie ausgereizt. Eine weitere Verbesserung der Langzeitergebnisse erwarten Experten erst durch innovative Therapiekonzepte mit molekularem Wirkmechanismus. Im Fokus: VEGFR und EGFR Präklinische und klinische Studien haben jüngst klar gemacht, dass das NSCLC mit zwei therapeutisch interessanten Zielstrukturen aufwarten kann: Einmal ist dieser Tumor häufig durch eine Überexpression des EGFR (epidermal growth factor receptor) charakterisiert, die mit erhöhter Proliferation, Metastasierung, Apoptose-Inhibition und daher schlechter Prognose einhergeht. Der zweite viel versprechende Ansatzpunkt ist VEGFR (vascular endothelial growth factor receptor), der die Tumorangiogenese stimuliert und eine Schlüsselrolle bei der Regulation der vaskulären Permeabilität spielt. Eine hohe Dichte von Mikrogefäßen im Tumorgewebe hat sich beim NSCLC als Prädiktor einer raschen Progression und Metastasierung herausgestellt. Die kombinierte Hemmung von VEGFRund EGFR-Signalweg erscheint daher als potenter Weg zur Suppression des Tumorwachstums. Bestätigt wird dieser Ansatz durch Ergebnisse mit der Kombination des VEGF-Antikörpers Bevacizumab und dem EGFR-Blocker Erlotinib. Tyrosinkinase. In den randomisierten Phase-II-Studien IDEAL I und II führte die oral verfügbare Substanz bei teilweise intensiv vorbehandelten NSCLCPatienten (Stadium III/IV) zu Remissionsraten zwischen 12 und 18%. Bei weiteren 30–36% wurde eine Tumorstabilisierung erreicht. Bemerkenswert ist außerdem die rasch eintretende symptomatische Besserung bei etwa 40% der Patienten. Die anschließenden Phase-III-Studien INTACT I und II, in denen Gefitinib in Kombination mit Standard-Chemotherapien geprüft wurden, verliefen allerdings negativ: Die zusätzliche Gabe des EGFRBlockers zur Chemotherapie führte nicht zu einer Überlebensverlängerung. Positive Erfahrungen zu Gefitinib hat man dagegen im Extended Access Program (EAP) bei mittlerweile über 100 000 Patienten sammeln können. Auch die Arbeitsgruppe um Dr. Wilfried Eberhardt, Essen hat im Rahmen des EAP rund 250 Patienten behandelt. Dabei handelt es sich um prognostisch sehr ungünstige Patienten, die den EGFR-Blocker zum Teil als Sechstlinientherapie erhielten. Trotz der intensiven Vortherapie sprechen einzelne Patienten bereits seit mehr als 3 Jahren auf Gefitinib an, und dies bei Erfahrungen mit der EGFR-Blockade Bereits erheblich mehr Erfahrungen hat man mit Substanzen gesammelt, die nur den EGFR hemmen. Hierzu gehört Gefitinib, ein selektiver Inhibitor der EGFR- Abb. 1. Wirkmechanismus von ZD6474. 1. Anti-VEGFR: an der Endothelzelle: ZD6474 ◆ inhibiert Angiogenese durch • Verminderung der Endothelzellen-Proliferation und -Migration ◆ vermindert vaskuläre Permeabilität © 2005 S. Karger GmbH, Freiburg Fax + 49 761 4 52 07 14 E-mail [email protected] www.karger.com Accessible online at: www.karger.com/onk 2. Anti-EGFR: an der Tumorzelle: ZD6474 ◆ inhibiert Zellproliferation ◆ vermindert Invasion ◆ fördert Apoptose ◆ inhibiert Metastasenbildung Downloaded by: 88.99.70.242 - 11/3/2017 4:41:34 AM Molekulare Therapieansätze beim NSCLC guter Lebensqualität. «Ein gewisser Teil der Patienten scheint demnach einen Langzeit-Benefit von der Substanz zu haben, wie es auch insgesamt im EAP beobachtet wurde», so Eberhardt. Die 1-Jahres-Überlebensrate beträgt rund 30% und ist damit vergleichbar mit der bei Zweitlinien-Chemotherapie. Prädiktiv für ein Ansprechen auf Gefitinib sind Vorliegen eines Adenokarzinoms, weibliches Geschlecht und Nieraucher-Status. Außerdem wurden im vergangenen Jahr Mutationen im EGFR als prädiktiver Marker für eine Response identifiziert. Allerdings ging die für die Zulassung der Substanz erforderliche plazebokontrollierte ISEL-Studie negativ aus: Im Gesamtkollektiv wurde durch Gefitinib lediglich eine tendenzielle Überlebensverlängerung versus Plazebo erreicht. Nur in Subgruppenanalysen bei Nierauchern (8,9 vs. 6,1 Monate) und Asiaten (9,5 vs. 5,5 Monate) war der Überlebensunterschied versus Plazebo signfikant. Signifikante Vorteile für den EGFR-Blocker wurden auch bei Zeit bis zum Therapieversagen (3,0 vs. 2,6 Monate) und Responserate (8 vs. 1,3%) beobachtet. Als mögliche Gründe für den unerwarteten Ausgang der Studie führte Eberhardt eine ungünstige Patientenselektion und ein zu kurzes Follow-up von nur 7 Monaten an. Eine Auswertung nach Regionen zeigte zudem, dass Patienten in den stark vertretenen osteuropäischen Zentren keinen Überlebensvorteil durch den EGFR-Blocker hatten. Interessante Daten könnte seiner Meinung nach jedoch eine Studie zur Second-line-Therapie liefern, in der Gefitinib mit dem Standard Docetaxel verglichen wird – die INTEREST-Studie. PharmaForum Kombinierte EGFR/VEGFR-Hemmung Phase-II-Studien beim NSCLC weiter zu prüfen», informierte Eberhardt. In ZD6474 (ZACTIMA) konnten beide Wirkprinzipien in einem Molekül vereint werden. «Das oral applizierbare ZD6474 zeigt eine bifunktionelle Wirksamkeit», konstatierte Eberhardt. Schon die Blockade der EGFR-Tyrosinkinase in Tumorzellen durch ZD6474 hat multiple Effekte, da Zellproliferation, Invasion, Metastasierung und VEGF-Produktion verringert werden. Zudem wirkt die Substanz auch direkt gegen VEGFR: Sie verhindert die Bindung von ATP an die Tyrosinkinase des VEGF-Rezeptors 2 (VEGFR 2) und unterbindet so die Proliferation und Migration von Endothelzellen der Tumorgefäße. Auch verbessert sie die vaskuläre Integrität (Abb. 1). Die pleiotropen Effekte von ZD6474 auf EGFR- und VEGFRSignaltransmission, Proliferation und Apoptose konnten in Tumor- und Endothelzellmodellen bestätigt werden. In Invivo-Modellen zeigte die Substanz mit der Inhibition der tumorinduzierten Angiogenese und einer Reduktion der Gefäßdichte im Tumor die erhoffte Aktivität. Auch die Nagelprobe, den klinischen Einsatz beim Patienten, hat ZD6474 bereits bestanden. Zunächst wurde der Wirkstoff in zwei Phase-I-Studien bei 77 bzw. 18 austherapierten Patienten mit unterschiedlichen Tumoren in fortgeschrittenen Stadien evaluiert. Hier erwies sich ZD6474 in Tagesdosen bis maximal 300 mg als gut verträglich. Häufigste Nebenwirkungen sind Diarrhöen, Hautausschläge, Hypertonie und asymptomatische QTc-Verlängerungen. Bei 4 von 9 NSCLC-Patienten wurden objektive Remissionen nach den RECIST-Kriterien induziert. «Die Ergebnisse waren der Auslöser, die Substanz in randomisierten Kombinierte Hemmung effektiver als alleinige EGFR-Blockade In der ersten doppelblinden Multizenterstudie wurde ZD6474 (300 mg) als Monotherapie mit dem EGFR-Inhibitor Gefitinib (Iressa®; 250 mg) verglichen. Insgesamt wurden rund 160 vorbehandelte Patienten mit fortgeschrittenen NSCLC (Stadium IIIB/IV) aufgenommen und bis zur Progression behandelt (Phase A), danach auf die jeweils andere Substanz umgestellt (Phase B). In der jetzt abgeschlossenen Phase A zeigte sich ein signifikanter Vorteil für ZD6474 beim primärem Endpunkt (p = 0,011): Das progressionsfreie Überleben wurde im Vergleich zu Gefitinib um 56% verlängert. Auch beim Gesamt-Überleben gab es einen tendenziellen Vorteil zugunsten von ZD6474. In der zweiten Multizenterstudie wurde die Kombination von ZD6474 mit Docetaxel, einem derzeitigen Standard in der Second-line-Therapie des NSCLC, erprobt. Rekrutiert wurden 127 vorbehandelte Patienten (Stadium III/IV) und zunächst offen zur Sicherheitsüberprüfung mit dem Taxan (75 mg/m2 alle 3 Wochen) plus ZD6474 in Dosierungen von 100 oder 300 mg täglich behandelt. Der zweite randomisierte Studienteil beinhaltet außerdem einen dritten Arm mit Docetaxel/Plazebo. Auch diese Studie erbrachte ein positives Ergebnis für ZD6474: In beiden Kombinationsarmen konnte das progressionsfreie Überleben im Vergleich zur Docetaxel-Monotherapie erheblich verlängert werden: So betrug das progressionsfreie Intervall bei alleiniger Doce- taxel-Therapie nur 12 Wochen, bei zusätzlicher Gabe von ZD6474 dagegen rund 18 Wochen (Abb. 2). In einer ebenfalls noch laufenden Doppelblindstudie wird ZD6474 (200 mg bzw. 300 mg) mit Carboplatin/Paclitaxel, einem Standard in der First-line-Therapie des NSCLC, untersucht. Auch hier wurde zunächst offen die Sicherheit der Dreifachkombination überprüft. Zurzeit wird im randomisierten Studienteil in 3 Armen die ZD6474-Monotherapie mit der alleinigen Chemotherapie mit Carboplatin/Paclitaxel und der Dreierkombination verglichen. Der Stellenwert von ZD6474 in der Second- und First-line-Therapie des NSCLC soll nun in großen randomisierten Studien geklärt werden. Nach Eberhardts Meinung könnte die Substanz zukünftig in der Monotherapie und in Kombination mit konventioneller Chemotherapie eine interessante neue Option darstellen. Referenzen Heymach JV: Br J Cancer 2005:92(suppl I):S14–S20. Fukuoka M, et al.: J Clin Oncol 2003:21:2237–2246 Kris MG, et al.: JAMA 2003:290:2149–2158. Giaccone G: J Clin Oncol 2004:22:777–784. Herbst RS: J Clin Oncol 2004:22:785–794. Quelle Satellitensymposium anlässlich der Gemeinsamen Jahrestagung der Deutschen, Österreichischen und Schweizerischen Gesellschaften für Hämatologie und Onkologie, Hannover, 4. Oktober 2005. Bericht: Dr. Katharina Arnheim, Berlin Impressum Molekulare Therapieansätze beim NSCLC ZD6474 blockiert zwei Signalwege der Tumorprogression PharmaForum in Onkologie 28 l 12 l 05 © 2005 by S. Karger Verlag für Medizin und Naturwissenschaften GmbH Plazebo + Docetaxel ZD6474 100 mg + Docetaxel Hazard Ratio = 0,64 (95% CI = 0,38–1,05) p = 0,074 (vs. Plazebo + Docetaxel) 0,75 ZD6474 300 mg + Docetaxel Hazard Ratio = 0,83 (95% CI = 0,50–1,36) p = 0,461 (vs. Plazebo + Docetaxel) 0,50 0,25 0 0 50 100 150 200 250 300 350 400 Progressionsfreies Überleben, Tage © 2005 S. Karger GmbH, Freiburg Fax + 49 761 4 52 07 14 E-mail [email protected] www.karger.com Accessible online at: www.karger.com/onk Lörracher Straße 16a D-79115 Freiburg Tel. +49 761 45 20 70 E-mail [email protected] Mit freundlicher Unterstützung der AstraZeneca GmbH. Der Verlag und die Herausgeber der Zeitschrift übernehmen keine Verantwortung für diese Rubrik. Die Wiedergabe von Gebrauchsnamen, Handelsnamen, Warenbezeichnungen usw. in dieser Zeitschrift berechtigt auch ohne besondere Kennzeichnung nicht zur Annahme, dass solche Namen im Sinne der Warenzeichen- und Markenschutz-Gesetzgebung als frei zu betrachten wären und daher von jedermann benutzt werden dürfen. Downloaded by: 88.99.70.242 - 11/3/2017 4:41:34 AM Abb. 2. Signifikante Verlängerung des progressionsfreien Überlebens durch Kombination von ZD6474 und Docetaxel. Wahrscheinlichkeit des progressionsfreien Überlebens 1,00