1 - GIBZ - Physik für Polymechaniker
Werbung

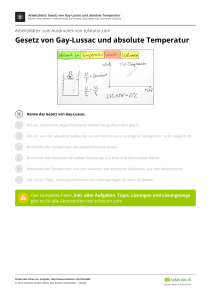
GIBZ Gewerblich-industrielles Bildungszentrum ZUG Physik KON3/PME3/AU3 9.1 Ausdehnung von Gasen, Boyle, Gay-Lussac Druck und Temperatur Wie dies bei Feststoffen und Flüssigkeiten der Fall ist, dehnen auch Gase sich bei Erwärmung aus. Dies wird im folgenden Versuch deutlich: Die Versuchsanordnung besteht aus einem Wasserbad mit Tauchsieder, einen Thermometer und einem verschlossenen, mit Luft gefüllten Glaskolben. Eine Leitung führt vom Glaskolben in einen umgekehrten, mit Wasser gefüllten Masszylinder. Bei Erwärmung des Wasserbades mittels des Tauchsieders, steigt auch die Lufttemperatur im Kolben an. Die Luft dehnt sich aus und presst das Wasser aus dem Masszylinder. Es besteht also einen Zusammenhang zwischen Temperatur und Volumen eines Gases. Der französische Wissenschaftler Joseph Gay-Lussac stellte fest, dass das Quotient von Volumen (V) und Temperatur (T) eines Gases bei gleichbleibender Temperatur und Gasmenge konstant ist. Gesetz von Gay-Lussac: V --- = konstant, oder T ACHTUNG: 9.1 Ausdehnung von Gasen, Boyle, Gay-Lussac V1 ---T1 V2 = ---T2 T = absolute Temperatur in K Seite 120 GIBZ Gewerblich-industrielles Bildungszentrum ZUG KON3/PME3/AU3 Physik Volumen und Druck Wenn ein Gas komprimiert wird, d.h. wenn das Gasvolumen verringert wird, stossen die Gasmoleküle häufiger an einander und an die Wand. Dabei steigt der Druck an. Die Physiker Robert Boyle und Edme Mariotte stellten fest, dass dieser Druckanstieg nicht linear sondern exponentiell erfolgt. Aufgrund dieser Beobachtung entstand das Gesetz von Boyle-Mariotte : p * V = konstant oder p1 * V1 = p2 * V2 Allgemeines Gasgesetz Fügt man die Beobachtung von Gay-Lussac und Boyle-Mariotte zusammen, entsteht das allgemeine Gasgesetz: p*V ------ = konstant T oder p1 * V1 p2 * V2 -------- = --------T1 T2 ACHTUNG: T = absolute Temperatur in K 9.1 Ausdehnung von Gasen, Boyle, Gay-Lussac Seite 121 GIBZ Gewerblich-industrielles Bildungszentrum ZUG KON3/PME3/AU3 Physik Gasmenge und Druck Mittels einer Fahrradpumpe wird Luft in einen Reifen gepumpt. Wenn sich anfänglich keine Luft im Reifen befindet, wird dieser sich zuerst auffüllen. Sobald er gefüllt ist, kann sein Volumen nicht mehr zunehmen und steigt der Druck an. Der Gasdruck ist offensichtlich auch abhängig von der Gasmenge. Der italienische Physiker und Chemiker Amedeo Avogadro stellte fest, dass 1 Mol eines idealen Gases bei gleicher Temperatur und Druck 6,022 * 1023 Teilchen (Moleküle) enthalten (Avogadro-Konstante). Molare Massen einiger Gase: Wasserstoff Sauerstoff Stickstoff Methan Kohlenstoffdioxid H2 O2 N2 CH4 CO2 2g 32 g 28 g 16 g 44 g Nach dieser Feststellung kam er zum Schluss, dass diese Gasmenge (1 Mol = 6,022 * 1023 Moleküle) bei 0°C und 1013 hPa Druck immer ein Volumen von 22,4 L hat. Molares Volumen: 22,4 dm3 Zum Beispiel: 62 g Sauerstoff (2 Mol) haben bei 0°C (273 K) und 1013 hPa ein Volumen von 2 * 22,4 dm3 = 44,8 dm3 Umrechnungen: 1 Pa = 1 N/m2 = 0.00001 bar 1 bar = 10 N/cm2 = 1 daN/cm2 = 105 Pa 1 mbar = 100 Pa = 1 hPa 9.1 Ausdehnung von Gasen, Boyle, Gay-Lussac Seite 122 GIBZ Gewerblich-industrielles Bildungszentrum ZUG KON3/PME3/AU3 Physik Uebungsaufgaben: 1. Das Manometer einer mit Sauerstoff gefüllten Stahlflasche zeigt einen Überdruck von 150 bar an. Die Flasche hat einen Rauminhalt von 50 Liter. Wie viel Liter Sauerstoff können bei 1013 hPa entnommen werden? 2. Die Luft in einem Zimmer von 16 m2 Fläche und 2.5 m Deckenhöhe wird von 5°C auf 22°C erwärmt. Wie viel Luft muss entweichen, damit der Druck im Zimmer konstant bleibt? 3. In einer Stahlflasche befinden sich 40 Liter Sauerstoff bei einer Temperatur von 20 °C und einem Druck von 150 bar. Wie groß ist das Volumen des Sauerstoffs bei Normbedingungen? Wie groß ist die Masse des Sauerstoffs? 4. Ein Wagenreifen wird auf ein Volumen von 30 dm3 und einen Druck von 3.5 bar mit Luft aufgepumpt. Durch das Zusammenpressen der Luft steigt ihre Temperatur auf 38°C. Auf welchen Druck verringert sich die Luft im Reifen, wenn sie sich nach einigen Minuten auf 20°C abgekühlt hat (Näherung: Volumen bleibt konstant!). 5. Ein Taucher lässt eine Luftblase mit einem Volumen von 10 cm3 aus einer Tiefe von 8 m aufsteigen. Welches Volumen hat diese Luftblase an der Wasseroberfläche? 6. Es wurden 2.4 m3 Gas verbraucht, das unter einem Überdruck von 600 Pa stand. Der Atmosphärendruck war 1032 hPa und die Raumtemperatur 24°C. Wie groß ist das Volumen diese Gases unter Normbedingungen? 7. Der Brennwert von Stadtgas beträgt im Normzustand 17500 kJ/m3. Welche Wärmemenge wird frei, wenn 1m3 Gas bei einer Außentemperatur von 22°C und einem Atmosphärendruck von 1030 hPa verbrannt werden? 8. Für einen Versuch werden V = 480 cm3 Wasserstoff bei T = 39°C abgemessen. Der Atmosphärendruck beträgt 1035 hPa. Mit einer Waage wird die Masse des Gases zu m = 0.0386 g bestimmt. Wie groß ist die Dichte von Wasserstoff unter Normbedingungen? 9.1 Ausdehnung von Gasen, Boyle, Gay-Lussac Seite 123