Stoffverteilungsplan - Hinnerk Haidjer Schule, Förderschule Lernen
Werbung

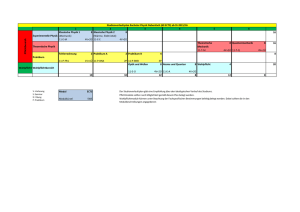
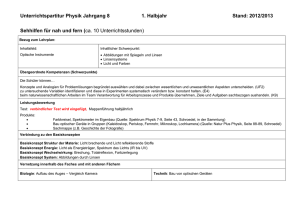
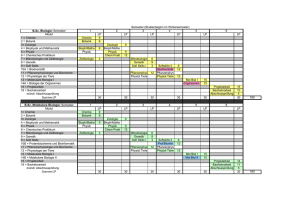
Hinnerk-Haidjer-Schule Stoffverteilungsplan Physik-Chemie 1.3.2007 Stoffverteilungsplan im Fach Physik Für die Klassen 5-9 der Hinnerk-Haidjer-Schule Vorbemerkung: Dem Physikunterricht liegt an wichtigen Stellen (Elektrizität, Wärmelehre) ein Spiralcurriculum zugrunde. Aufbauend auf grundlegende Erkenntnisse insbesondere der Lerninhalte der Klassen 5 und 6 findet der Unterricht der oberen Jahrgänge statt. Aufgrund der schwierigen Unterrichtssituation bez. der Stunden/Fachlehrerrecourcen sowie der sehr unterschiedlichen Leistungsstärken der Klassen wird es immer wieder nötig sein, Grundlagen zu wiederholen. So kann und soll es möglich sein, die Unterrichtsinhalte den Möglichkeiten der Klasse anzupassen, auch wenn es der Stoff der vorangegangenen Jahrgänge sein sollte. Im Anhang sind Ergänzungen zum Stoffverteilungsplan für die einzelnen Klassen als weitere Erläuterungen zum Unterrichtsinhalt verfügbar. Klasse Themengebiete 5 Wärme und Kälte 5 Magnete 5 Wasser 6 Aggregatzustände des Wassers 6 Der elektrische Strom Inhalte/ Vorschläge für mögliche Unterthemen Literaturhinweise Wir fühlen Wärme, Messen von Temperaturen, verschiedene Thermometer, Wärmeausdehnung bei Flüssigkeiten, Siedepunkt, Schmelzpunkt Magnete ziehen nicht alles an, Magnete ziehen sich an und stoßen sich ab, Die Erde als „Magnet“ Trinkwasser-Brauchwasser, Gewässerverschmutzung, vom Schmutzwasser zum Trinkwasser „Stark in Biologie, Physik, Chemie Bd 1“, Schroedel, Seite 108-114 Ergänzend: „Natur begreifen Physik/Chemie Bd 1“, Seite 6-12 Stoffe in drei Aggregatzuständen, Stoffe verändern ihren Aggregatzustand, Der Wasserkreislauf, Eis Stromkreis, verschiedene Schalter, Schaltpläne, Leiter und Isolatoren, Leitfähigkeit verschiedener Stoffe, Die Glühlampe, Gefahren „Stark in Biologie, Physik, Chemie Bd 1“, Schroedel, Seite 148-159 Ergänzend: „Natur begreifen Physik/Chemie Bd 1“, Seite 6474 „Stark in Biologie, Physik, Chemie Bd 1“, Schroedel, Seite 176-186 Ergänzend: „Natur begreifen Physik/Chemie Bd 1“, Seite 116126 „Stark in Biologie, Physik, Chemie Bd 1“, Schroedel, Seite 124-130 Ergänzend: „Natur begreifen Physik/Chemie Bd 1“, Seite 3036 „Stark in Biologie, Physik, Chemie Bd 1“, Schroedel, Seite 132-147 Ergänzend: „Natur begreifen Physik/Chemie Bd 1“, Seite 3862 6 Wasser- und Luftdruck 7 Wärme und Kälte, (Vertiefung) 7 Schall 7 7 8 8 8 9 9 9 Wasserdruck, Auftrieb, Schiff aus Metall, Wasser in verbundenen Gefäßen, Luft ist ein Körper, Luft drückt auf die Erde Wärmeleitung, Wärmemitführung, Wärmestrahlung Wie ensteht Schall, laut-leisehoch-tief, Schallausbreitung, Transportmittel für Schall, Schallschutz Licht und Sehen Woher kommt das Licht, immer geradeaus, Lichtumlenkung, verschieden Spiegel, Optische Geräte Verbrennung - eine Bedingungen für die chemische Reaktion Verbrennung, Zusammensetzung der Luft Der elektrische Strom Elektronen als Träger des Stromes, Stromstärke, Spannung, Schaltungen, Messgeräte Säuren und Laugen Nachweis von Säuren und Laugen, Der Abfluss ist verstopft, Gefahren, Seifenlauge Kräfte Kräfte können Körper verformen, Geschwindigkeit, Reibung, Kräfte ändern die Bewegungsrichtung, Kräfte kann man messen Elekromagnetismus Der elektrische Strom hat magnetische Kraft, SpulenMagnete zum abschalten, Elektromagnete in vielen Geräten, Klingel, Magnet als Schalter Nährstoffe Kohlenhydrate, Zucker und Stärke, Fette, Fett ist oft versteckt, Eiweiß ist unersetzlich Einfache Maschinen Einseitiger- und zweiseitiger Hebel, Hebel im Alltag, Gewichtskraft, der Flaschenzug „Stark in Biologie, Physik, Chemie Bd 1“, Schroedel, Seite 160-174 Ergänzend: „Natur begreifen Physik/Chemie Bd 1“, Seite 88114 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 144-146 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 2228 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 136-141 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 4860 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 200-217 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 3046 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 232-235 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 130134 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 176-182 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 8894 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 248-259 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 144154 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 218-224 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 6270 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 184-185 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 100110 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 260-267 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 156164 „Stark in Biologie, Physik, Chemie Bd 2“, Schroedel, Seite 226-230 Ergänzend: „Natur begreifen Physik/Chemie Bd 2“, Seite 7278 Anhang Ergänzungen zum Stoffplan Physik Klasse 5 Luft und Wasser Luft braucht Platz Papiertuch unter Wasser, Senkkastenprinzip, Wasser verdrängt Luft Blumentöpfe, ( 2 übereinander) Tauchheber Tropfpipetten Luft verdrängt Wasser Atemluft mit Strohhalm pneumatisch auffangen, Feuerzeuggas pneumatisch sammeln, Wasser in verbundenen Gefäßen Schlauchwaage, Anwendungsbeispiele zeichnerisch: Teekanne, Schleuse, Geruchsverschluss Kapillarität Tinte in Kapillarröhrchen und Kreide, (Ring von brauner Tinte in Wasser), Anwendung: Schutz von Grundmauern, Pflanzenernährung Aufschwemmung und Lösung Mehl und Salz in Wasser rühren, Mehl abfiltern, Filter mit Lupe betrachten; Salzwasser eindampfen; (Video: Mit Wasser zaubern,2) Zusammengepresste Luft Luftpumpe, Patronen schießen, Luftströme zeichnen Thermometer und Temperaturmessung Entstehung von Wärme Bilder in Tabelle ( Feuer, Strom, Reibung) zeichnen oder kleben Funktion eines Thermometers Kennenlernen verschiedener Thermometer, Video: Messen aber Wie, Maßeinheiten m, l, g, °C, Modellversuch zur Flüssigkeitsausdehnung mit Tinte; Teile des Thermometers zeichnen und benennen, Definition O°C durch Wasser (Messen von Schnee); Messübungen Messen von Wasser mit Schülerthermometern und Zuordnen der passenden Begriffe ( kalt, lau, Tiefe und hohe Temperaturen warm, heiß); Fieber messen Eis und Schnee messen Zeichnung einer Temperatursäule von –20°C bis 6000°C Einfacher Stromkreis Pole an Batterie und Lämpchen Lämpchen an Batterie anschließen, Kontaktstellen finden und zeichnen; Stromkreis mit Klingeldraht; Stromkreis Stromkreis mit Experimentierkabeln und Lampenfassung aufbauen und zeichnen; Gefahrloser Umgang AP zu besonderen Gefahrensituationen, Körperschluss vermeiden Verbraucher und Quelle Stromverbraucher und Quellen in Tabelle zeichnerisch einordnen; verschiedene Stromquellen und ihre Gefährlichkeit und Voltzahl (AP); Transformator Funktion und Umgang, Stromkreis aufbauen und zeichnen; Stromkreis mit Trafo und Schalter aufbauen, verschiedene Unterbrechungen ausprobieren; Strom leistet Arbeit in Form von Wärme, Licht und Bewegung, Video: Um uns herum elektrischer Strom Teil 1, Tabelle erstellen; Kurzschluss Kurzschluss als Stromweg ohne Verbraucher; Hitzeentwicklung; Sicherung; Lamettakokeln; Elektrische Leitfähigkeit Leiter und Nichtleiter Aufbau eines Stromkreises mit Prüfstrecke; freies Experiment; systematische Untersuchung von Materialien auf ihre Leitfähigkeit (Schraube, Nagel, Glasrohr, Holzstäbchen, Heftstreifen, Porzellanunterteller, Silberschmuck, Kupferblech, Alufolie, Kohlestäbchen, Papier, Plastiklineal, doppelt gespitzter Bleistift,...), Eintragung in Tabelle, Ergebnissatz finden; Die leitenden Teile an den Schülergeräten herausfinden und zeichnen; Leiter und Isolatoren einfärben; Leitfähigkeit von Flüssigkeiten Erde,Salzwasser,Kupferelektroden, Mensch ein Leiter; Badewannenund Drachenunfälle (m-Amperemeter) Stromkreis an Taschenlampe Zerlegen; Zeichnung; Fahrradbeleuchtung Lampe mit Klingeldraht an Dynamo; Pole des Dynamo einzeichnen; Stromkreis von Dynamo über Kabel und Rahmen (Modell); Schaltzeichen Schaltzeichen für Batterie, Kabel, Lampe, Schalter; Stromkreise nach Schaltskizzen aufbauen; Weiteres Explosionen Brennendes Reagenzglas (Schutzbrille!) Backpulverbombe ( Überraschungsei oder Filmdose mit phosphathaltigem Natriumcarbonat und warmem Wasser oder Sprudel) draußen! Ergänzungen zum Stoffplan Physik Klasse 6 Aggregatzustände Schmelzen Eiswürfel oder Schnee: Schmelzpunkt messen; Kerzenwachs: Erstarrungstemperatur im Teelicht messen; Tropfbilder mit durchgefärbten Kerzen (Herz, Anfangsbuchstabe) Blei schmelzen; Verdunsten Benzintropfen verschwinden vom Uhrglas (Zeichnung im Teilchenmodell mit Nase); Wasser verdunstet auf Straßen, Tafel, Wäsche und Haaren; Wasservernebler Verdampfen Zustandsänderungen im Kreislauf Wasser über Gasbrenner kochen, Kochpunkt messen, Dampf am Deckel kondensieren lassen; Tochterflamme der Kerze ableiten und entzünden; Zeichnung; Video: 1 Wasser-3 Gesichter Destillation von Tintenwasser mit Liebigkühler Wasserkreislauf in der Natur Magnetismus Nur Eisen, (Kobalt und Nickel) wird angezogen Testen verschiedener Gegenstände mit Magnet: Alufolie, Plastik, Büroklammern, Heftstreifen, Kork, Holz, Streichholzschachteln, Papier, Kupferdraht, Nägel, Schmuck,etc. Anwendungen Seifenhalter, Magnetschloss, Magnettafel zeichnen;(Buch S.67) Magnetkraft überwindet Erdanziehungskraft Schwebende Büroklammer (Nähgarn, Tesa) Magnetkraft durchdringt Stoffe -Wasser (Korken mit Heftzwecke); -Pappe (Streichholzschachtel mit Büroklammer) -Holz (Büroklammerspiel auf Sperrholzplatten) -Plastik (Hefter,Lineale, Klassenraumwände) -Metalle (Sortieren von Löffeln und Pfennigen nach Eisenkern oder Massivkupfer bzw. Silber) Pole des Magneten Wo ist der Magnet am stärksten? Nagelkopf unter Magnetmitte; Büroklammer am Faden über Magnetmitte aufhängen Anziehen und Abstoßen Probe mit 2 Magneten auf Tisch; Magnete im Plastikreagenzglas Magnetspiele (Hunde, Auto) Magnetisierung Nagel durch Überstreichen magnetisieren; verwenden; Entmagnetisieren durch Klopfen, Hinwerfen oder Erwärmen; Modellzeichnung mit grün-roten Teilchen Eisendrähte mit Brechkerben magnetisieren, zerbrechen und Einzelmagnete beweisen; Kompass Zur Kompassnadel eine Windrose zeichnen; Ergänzungen zum Stoffplan Physik Klasse 7 Optik Lochkamera Strahlendes Licht farbige Schatten Blende auf! (Video) Bau aus Pappröhren und Pergamentpapier erfordert Geduld; starke Lichtquelle und nicht zu kleines Loch notwendig Die Abbildungseigenschaften sind nur bei sehr großen und kontrastreichen Objekten auszumachen (oben-unten). Lichtquellen Lichtausbreitung Schattenwurf Schatten im rechten Licht Geblendet (Video) Sonne, Lampe als echte Lichtquellen (Selbstleuchter) Fremdleuchter durch diffuse Reflexion, mit weißem Papier bei starker Lichtquelle Schatten mit Lampe und Stab Kernschatten, Halbschatten Schattenlänge je nach Einfallswinkel und Entfernung zwischen Stab und Schirm Ziel verfehlt! Licht im Kanal (Video) Abbildungseigenschaften Aufbau eines Diaapparates Dias L, blau/gelb, freie Motive rechts/links-Vertauschung und oben/unten Vertauschung Lichtreflexion Der Schein trügt In den Spiegel geblickt (Video) Das Spiegelbild ist seitenverkehrt (vorne-hinten). Spiegelschrift. Spiegelsymmetrische Zeichnungen vervollständigen, mit Spiegel vorher ausprobieren. Doppel- und Mehrfachspiegelungen - um die Ecke gucken, Kaleidoskop Sammel- und Streulinsen Augen auf! Ein scharfes Bild (Video) Bau des Auges, Korrektur durch Brillen Im Sommer mit dem Brennglas auf dem Hof den Brennpunkt finden (schwarzes Papier). Lupe und Mikroskop benutzen. Achtung Aufnahme! Kleines Bild - ganz groß (Video) Wärmeausdehnung Feststoffausdehnung Eisenkugelversuch; Anwendungsbeispiele: Eisenbahnschienen, Überlandkabel, Estrich, Alufenster, Brücken,Betonstraßen, Aufschrumpfen von Gasrohren, Auspuffrohren, etc.; Video: Brücken mit Lücken; Flüssigkeitsausdehnung Thermometermodell mit Tinte; Anwendungsbeispiele: Kühlwasser, Benzintank, Getränkeflaschen, Einwecken; Gasausdehnung Bläschen zählen beim Erlenmeyer mit Glasrohr unter Wasser; tanzender Groschen; Luftballon auf Erlenmeyer mit Wassertropfen; Implosionsbüchse; Anwendungsbeispiele:Tischtennisbälle, Spraydosen, Bimetall Zeichnung von Metallstreifen mit unterschiedlicher Wärmeausdehnung Versuch: Bimetallstreifen in Feuerzeugflamme; Video: Kann Metall denken; Feuermelder mit Bimetallschalter; Bügeleisen-Automatikschalter nach gleichem Versuchsaufbau nur Kontaktstift unten; Ergänzungen zum Stoffplan Chemie Klasse 7 Verbrennung Die 3 Bedingungen für Feuer: Luft, Hitze, Brennstoff; Löschen als Entzug Anzünden einer Kerze; Feststellen der 3 Bedingungen; Löschen mit Glas und Kerzentöter; (evtl. Tochterflamme) Weitere Beispiele für Luftentzug: Wasser, Schaum, Sand, Löschdecke, sich rollen; Versuch: Papierfeuer auf Unterlagen mit nassen Lappen löschen; äOfenversuchä: Kerze im offenen Glasrohr und Luftzufuhr lenken: (oben oder unten, beides, nichts) Lehrerdemo: Benzinflamme in Porzellanschale erst mit Wasser, dann mit Sand löschen; Zusammensetzung der Luft Kerze im abgeschlossenen Luftraum im Wasserbecken; Anteile der Luft benennen und einzeichnen; Gasbrenner Sicherer Umgang mit dem Brenner Gasanzünder betätigen; Sicherheitsregeln mit Nummern aufschreiben (Gas nicht ausströmen lassen, Standsicherheit prüfen, Kopf zurück, nicht kippeln, nicht pusten, Gasschlauch nicht knicken) (bei Verstoß dreimaliges Abschreiben); Simulieren von Gefährdungen; Zeichnung des Brenners; Benennung der Funktionsteile; Anschließen und Entzünden durch jeden Schüler nacheinander; Einzelübungen: Ein- und Ausschalten, Flammengröße regulieren, Luftregler nutzen; Haar verbrennen; Acrylgarn in Flammennähe schmelzen (Vorsicht mit Synthetics!); Bedeutung der Luftzufuhr Rauschende und leuchtende Flamme einstellen; Luftzufuhr bei geöffneter Luftschraube im Teilchenmodell zeichnen; Welche Flamme ist heißer? Nagel zum Glühen bringen; Eigenschaften von Stoffen Stoffbegriff Brennstoff, Baustoff, Werkstoff, Kunststoff, Nährstoff, Süßstoff, Eigenschaften: Farbe, Glanz, Oberfläche, Magnetismus, Tabelle erarbeiten; Materialstäbe zur Wärmeleitung vergleichen (auch mit Magnet); gleich aussehende Münzen; elektrische Leitfähigkeit, Wdhg. der Leitfähigkeitsprüfung beliebiger Materialien; Löslichkeit in Wasser z.B. Mehl und Zucker Schmelzverhalten Blei schmelzen; Glas schmelzen; Schmelztemperatur von Wasser und Paraffin; Chemische Reaktion Stoff- und Eigenschaftsänderung: Ammoniumdichromat (NH4Cr2O7) (Demo-) Vulkanversuch; Vergleich vorher ---- nachher: Farbe, Wasserlöslichkeit, Volumen oder Gewicht, Giftigkeit; Eisensulfid Darstellung aus Eisen- und Schwefelpulver; Stinkbombe mit HCl nach draußen; s.o. Kupfersulfid Energieumsatz bei Reaktionen Tabelle Stoffänderung/Energieform (Wärme, Licht, Bewegung) der obigen 3 Versuche und: Mg + HCl (verd.) ------ Wärme, Salmiak + Wasser -----Kälte; Mg + O2 ------Wärme, Licht Ergänzungen zum Stoffplan Physik Klasse 8 Elektrizitätslehre Schaltskizzen Wdhg. der Schaltsymbole; Aufbau versch. Stromkreise nach Skizze; Reihen- und Parallelschaltung Aufbau einer Reihen- und einer Parallelschaltung mit 2 Lampen; Was, wenn eine Lampe ausfällt? Welche brennen heller? Anwendungen; beide Schaltungen mit vielen Lampen in 2 Gruppen; (Weihnachtsbaumlichterkette) Erprobung eines Schalters in Reihen- und Parallelschaltung (Kurzschluss zeitlich begrenzen!) Spannungsaddition durch Reihenschaltung von Batterien Strom erzeugt Wärme Konstantandraht im Kurzschluss als Schmelzdraht (Strohhalme) Sicherungshäuschen; Zerlegung und Zeichnung der Schmelzsicherung; Leitfähigkeit testen; Lammettakokeln; Eisenwolle im Kurzschluss; Gerät mit Heizwendeln zerlegen und zeichnen; erwünschte und gefährliche Wärmewirkung; Umschalter Blinkschaltung (Fußgängerampel); Wechselschaltung (Treppenhaus); Elektromagnetismus Nagel-E-Magnet Nagel mit Klingeldraht umwickeln; mit Gleichstrom (Batterie) verwenden; (nicht abschaltbar,da Stahl magnetisch bleibt) Magnetspule und Eisenkern Büroklammerkette durch leere Spule; Kraftverstärkung durch geblätterten Eisenkern; Anwendung der Abschaltbarkeit beim Schrottheber; Wärmeausbreitung Wärmeleitung bei festen Körpern Buch II, S.22 ff; Versuch in Dreiergruppe: Eisen-, Kupferstab und Glasrohr gleicher Länge zum gleichen Zeitpunkt in rauschende Brennerflamme mit 4 Fingern am hinteren Ende halten (Unterlage zum Ablegen der heißen Stäbe); Einfache Maschinen Kraftmesser, Federwaage Spiralfedern am Stativ: Dehnung je nach Gewicht; Anwendung bei Federwaagen; Zeichnungen; Umlenkung der Kraft durch Stange oder feste Rolle Richtungsänderung bei gleicher Kraft (Federwaage) mit fester Rolle am Stativ erproben; Zeichnung der Anwendungen beim Brunnen oder am Futterspeicher Halbierung der Kraft durch lose Rolle Versuch mit fester und loser Rolle und Federwaage; Brunnen für Frauen; Balkenwaage Zeichnung und Benennung der Einzelteile; Aufbau und Tarierung Gewichtssatz erproben; Wiegen kleiner Gegenstände Hebelgesetz Bedeutung von Last- und Kraftarm an der Mathe-Waage Hebelwerkzeuge Beispiele nennen (Brechstange, Nussknacker, Zange, Flaschenöffner, Schubkarre, Schere) und zeichnen; Zange und Nussknacker ausprobieren; Ergänzungen zum Stoffplan Chemie Klasse 8 Säuren Lebensgefährliche Säuren Schwefelsäure konz. auf Baumwollstoff, Zucker, Holz, Papier, rohes Ei; Verdünnt als Akkusäure; Umgang mit Schutzbrille; Gefährdung der Schleimhäute; äBills Vergiftungsgeschichteä Gefahrensymbol erläutern und zeichnen; Genießbare Säuren Ascorbinsäure (Vitamin C) kosten; saurer Geschmack -- Säure; Skorbut als Mangelerscheinung; Vorstellen von Essig, Zitronensäure, Kohlensäure, Sorbinsäure; Konzentration und Gefahr am Beispiel Essigsäure und HCl Tabelle: genießbar - schädlich - tödlich; Essig 5%, Essig-Essenz 25%, Eisessig 98%, Magensäure 0,3%, verdünnte Salzsäure 7%, rauchende Salzsäure 39%; Säuren lösen Kalk Kalkstücke in HCl verd. auflösen; Anwendung zum Absäuern nach Verfugung von Mauern; Entkalkung von Heißwassergeräten; Absäuern von verkalkten RGs; Säuren lösen Metall und fördern Rosten Mg-Band in HCl verd. lösen; verrostete Scharniere zeigen; Warnung vor Garagenaufbewahrung; Indikatoren Indikator=Anzeiger zeigt nicht die Gefahr; Lackmustinktur auf Essig, Wasser, Zitronensäure, Sprudel, HCl verd., Apfel, Zitrone, Kartoffel, etc.; dito mit Indikatorpapier Bodentest Calcitest zur ungefähren PH-Wert-Bestimmung einer Bodenprobe; Auswertung Oxidation Verbrennung als chemische Reaktion; Begriffe Oxygenium und Oxidation; Kerze im abgeschlossenen Luftraum; Luftzusammensetzung; Spanprobe mit Kaliumpermanganat; Metalloxidation Kupferbrief; Eisenwolle, Magnesiumband; Metallpulver, Wunderkerze; Fe-Wolle in reinem Sauerstoff, Vacu-Blitzlicht; Rost-Versuch; Reaktionsgleichungen ohne Berücksichtigung der Molmassenverhältnisse Fe + O --> Fe/O Mg + O --> Mg/O Nichtmetalloxide: Kohlenoxid Me + O --> Me/O Eigenschaften von Kohlendioxid (aus Sprudelwasser): Gewicht (Umgießversuch), feuerlöschend (Natron im RG erhitzen u. Gas in Glas mit Teelicht leiten); (Grottenhund); säurebildend (feuchtes I-Papier oder in Lackmuswasser leiten); trübt Kalkwasser; Atemluft einblasen; Verbrennung von Holzkohle in O2 aus KMnO4 , Nachweis des CO2 mit Kalkwasser; Schwefeloxid Verbrennung von Schwefelpulver in reinem Sauerstoff aus KMnO4 unter dem Abzug; SO2-Gas färbt Lackmuswasser rot; Umweltschäden durch sauren Regen; Ergänzungen zum Stoffplan Physik Klasse 9 Spannung und Stromstärke Schaltskizzen Schaltsymbole wiederholen; Stromkreise nach Schaltplänen aufbauen und auf Funktionsfähigkeit prüfen; Kurzschluss finden; Spannung Voltzahl, Voltmeter Voltangabe als Maß für die Gefahr; Messungen an Batterie, Trafo, Dynamo, Fahrrad auf dem Hof; im Stromkreis parallel zum Verbraucher; Stromstärke Ampere Amperemeter Maß für die Geschwindigkeit des Stroms (Ladung pro Zeit); Messgeräte sind empfindlich!!! -deshalb immer in Reihe schalten (Verbraucher als Hindernis davor) Messung mit 1, 2 und 3 Lampen (6V 0,4A) ---> 0,4A 0,3A 0,2A; Zusammenhang von Volt und Ampere Versuch mit 1 Lampe (6V 0,4A) und Amperemeter in Reihe und Voltmeter parallel; Messwerttabelle: Je mehr Volt (Kraft), desto mehr Ampere (Tempo). Elektrische Leistung: Watt V . A = W Messungen mit Lämpchen verschiedener Amperezahl bei gleicher Spannung (6V am Trafo) mit Voltmeter und Amperemeter, Messwerte multiplizieren nach Formel und mit Wattangabe auf Lampensockel vergleichen; Elektrische Arbeit kWh Film FT 217 Leistungsfähige El. Beispielrechnungen W . h : 1000; kWh . Eur ; Stromzähler; Widerstand Materialabhängigkeit Film FT 216 E. passt sich an A-messung bei 6V mit Drähten 1,5m 0,2mm í Eisen, Konstantan,Kupfer; Vergleich der Leuchtkraft; Regelwiderstand; Dimmerprinzip mit langem Konstantandraht; Eisenwolle im Stromkreis; Ergänzungen zum Stoffplan Chemie Klasse 9 Kunststoffe Herkunft und Verwendung Gewinnung aus Erdöl, Kunststoffbuch S.35-39; Verwendungsbeispiele aus der Umgebung; Eigenschaften wie leicht, billig, unzerbrechlich, hitzeempfindlich; Joghurtbecher löchern; Kunststoffnamen; Syntheticgarn; Namensanfang mit Poly-; Materialproben vergleichen; Kunststoffbuch S.14-19; Polyacrylgarn über Brennerflamme; Fäden ziehen mit Polypropylen: Zottbecher, Linoleumschweißdraht; Thermoplaste, Duroplaste Kunststoffbuch S.27 Verformte Thermoplaste aus dem Haushalt: Lego, Zahnbürste, Butterdose, etc.; Duroplaste: Aschenbecher, Lampenfassung; Strohhalmfiguren kokeln Verarbeitung von Kunststoffen Zeichnung zu Spritzguss, Kalandrieren und Verspinnen; Film Kunststoffe II, Ihre Verarbeitung:(3200542) Kunststoffbuch S.58-67; Styropor schneiden; Linoleum schweißen, Wasserwaage mit Schlauchstück herstellen; PE-Stücke zusammenschweißen; Haare an Sektkorken (Schweißdraht) Vor- und Nachteile für die Umwelt Säurenachweis mit Indikatorpapier bei PVC-Verbrennung unter dem Abzug; Müll-Problem; Hygienische und sichere Verpackungen, leichtere Autos, etc. Buch Schroedel 2 S.182 ff Baustoffe Kalkmörtel Buch Schroedel 2 S.152 ff; Löschen von Branntkalk mit wenig Wasser und Messen der Temperatur; Mörtel aus Löschkalk und Sand in Streichholzschachteln; Versetzen einer Mörtelprobe mit CO2 aus Sprudel; Kalkkreislauf; Lösen von Kalkstein in verdünnter Salzsäure --> Saurer Regen Zement und Beton Zementmörtel aus Zementpulver, Sand und Wasser herstellen; Gegenstände in Quarkschalen einbetonieren; braucht zum Abhärten nur Wasser; Anwendungsbeispiele auch von Beton und Stahlbeton; Anrühren und Verarbeitung von Gips für Gipsförmchen; Formelvergleich Calciumcarbonat und Calciumsulfat (vorne Ca- hinten O) Gips Energieträger Chemische Energie durch Verbrennung Wdhg. des Oxidationsbegriffes; Spanprobe; Video Feuerwerk; Mg-Band, etc.; Kohle Verschiedene Sorten und ihre Heizwerte (Buch S.175); Verbrennung in reinem Sauerstoff und Nachweis des CO2 mit Kalkwasser; Treibhausklima; Erdöl, Erdgas Vorkommen, Verarbeitung und Verwendung (Buch S.170 ff); Benzin verbrennen und löschen mit Wasser und mit Sand (Demo); Benzinexplosion im Papprohr, (Viertaktmotor); Feuerzeuggas im RG auffangen und anzünden, Hinweis aus explosive Mischungen; Umweltbelastung Nachweis von CO2 bei der Verbrennung von Erdöl, Benzin (Wattebausch in RG tränken), Gas (Feuerzeug), Kerzenwachs und Holz,(Abgase mit umgedrehtem Trichter in RG auffangen, verschließen und mit Kalkwasser versetzten)--> bei jeder Verbrennung von fossilen Brennstoffen und ihren Produkten entsteht CO2, teilweise auch andere gasförmige Oxide, wie Stickoxide und Schwefeloxid. Energiesparen Beispiele für Umweltentlastungen sammeln (Wo wir sparen können:) Wasserstoff als Energiequelle Mg in verd. HCl, Knallgas entzünden (Schutzbrille) Lebensmittelchemie Kohlenstoffgehalt Verkohlung von Reis, Kartoffel, Brot, Mehl, Spaghetti im RG Stärkenachweis Stärkenachweis mit Jodtinktur bei Kartoffeln, Reis, Mehl, Brot; Spaghetti in Jodlösung tauchen; Stärke ist das, was stark macht Traubenzucker Glukoteststreifen in Traubenzuckerwasser Fette Fettfleckprobe (Speckstück zwischen Papier) Fettfeuer löschen (sparsam!! feuchte Tücher) (Rauchentwicklung!!) Eiweiß Gerinnungsprobe von Eiklar in kochendem Wasser, HCl