Periodensystem
Werbung

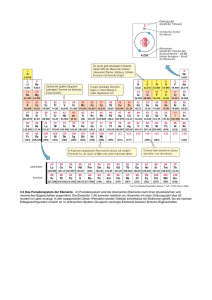
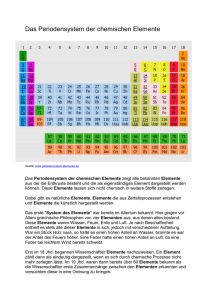
1 Periodensystem Grundlagen Sämtliche uns umgebende Materie besteht aus Atomen. Jedes Atom besteht aus einem Atomkern und einer Elektronenhülle. Jeder Atomkern enthält positiv geladene Protonen (mindestens eines, höchstens etwas mehr als 100), die Anzahl der Protonen wird als „Kernladungszahl“ bezeichnet und dient als „Ordnungszahl“ (OZ) für die betreffende Atomsorte. Jeder Atomkern ist von einer Elektronenhülle umgeben. Wenn diese Hülle genau so viele (negativ geladene) Elektronen enthält, wie im zugehörigen Kern Protonen vorhanden sind, befindet sich das Atom im „elektrisch neutralen“ Zustand, da die einander entgegen gesetzten elektrischen Ladungen von Proton und Elektron gleich groß sind. Das „Periodensystem“ bezieht sich nur auf Atome in diesem elektrisch neutralen Zustand. Elektronen können sich im Atom nur auf solchen Bahnen befinden, die bestimmte Abstände vom Atomkern haben; für solche zu einem Abstand gehörigen Bahnen wird auch der Begriff „Schale“ benutzt. Jede dieser Schalen bietet nur für eine ganz bestimmte Anzahl Elektronen Platz: In die innerste Schale passen nur zwei Elektronen, also gibt es auch nur zwei Chemische Elemente, die nur diese innerste Elektronenschale haben, das sind die mit den ersten beiden 2 Ordnungszahlen: 1 (Wasserstoff) und 2 (Helium). Sie bilden deshalb in der Darstellung des Periodensystems die oberste Reihe. Die Anordnung der Atome im Periodensystem ist somit vollständig durch die Elektronenkonfiguration erklärbar. Jeder Atomkern - bis auf das Wasserstoff-Isotop 1H - enthält elektrisch ungeladene Neutronen, die aber für den Aufbau des Periodensystems keine Rolle spielen. Sie werden in der „Isotopentabelle“ (und Details zu jedem Nuklid in der „Liste der Isotope“) dargestellt. Da die Elektronen an der Gesamtmasse nur einen verschwindend kleinen Anteil haben, ist nur die Masse der Protonen und Neutronen zusammen maßgeblich für die Atommasse; letztere (früher „Atomgewicht“ genannt) ist in Periodensystemen oft mit angegeben, spielt aber für dessen Aufbau ebenfalls keine Rolle. Zusätzliche Informationen im PSE Die Elemente, die Verbindungen und die Gemische sind die drei Stoffklassen der Chemie. Im Periodensystem kann man feststellen, dass einige Eigenschaften der Elemente sich in bestimmten Positionen und Bereichen im Periodensystem und im Periodensystem finden bzw. darstellen lassen: Masse – nimmt von oben nach unten und von links nach rechts zu (Ausnahmen: Ar vor K, Te vor I, Co vor Ni, Th vor Pa) Atomradius – nimmt von oben nach unten zu, von links nach rechts ab (bei Hauptgruppenelementen) Elektronegativität – nimmt von oben nach unten ab, von links nach rechts zu (Ausnahme: Edelgase) Ionisierungsenergie – nimmt von oben nach unten ab, von links nach rechts zu Metallcharakter – nimmt von oben nach unten zu, von links nach rechts ab Basizität der Oxide – nimmt von oben nach unten zu, von links nach rechts ab Schrägbeziehungen: Ähnlichkeiten zwischen: Lithium – Magnesium, Beryllium – Aluminium, Bor – Silicium Grimmscher Hydridverschiebungssatz Lanthanoidenkontraktion Lösung – homogene Mischung verschiedener Stoffe (kann im weitesten Sinne aus Gasen, Flüssigkeiten oder festen Bestandteilen zusammengesetzt und selbst gasförmig, flüssig oder fest sein) Metalle glänzen. Sie leiten Strom und Wärme. Das Kupfer ist hellrot, sehr dehnbar und hart. Es ist ein guter Leiter für Warme und Elektrizität. Silber ist ein weißes Metall. Es ist dehnbar und weich. Sein Schmelzpunkt liegt bei 961 Grad Celsius. Gold ist weicher als Blei. Ähnlich den Elementen haben auch die Verbindungen bestimmte Eigenschaften. 3 Geschichte Die Datierung der Entdeckung solcher chemischer Elemente, die bereits seit der Frühzeit oder Antike bekannt sind, ist nur ungenau und kann je nach Literaturquelle um mehrere Jahrhunderte schwanken. Sicherere Datierungen sind erst ab dem 18. Jahrhundert möglich. Bis dahin waren erst 15 Elemente als solche bekannt und beschrieben (Metalle wie Eisen, Kupfer, Blei, Bismut, Arsen, Zink, Zinn, Antimon, Platin, Silber, Quecksilber und Gold oder Nichtmetalle wie Kohlenstoff, Schwefel und Phosphor). Die meisten Elemente wurden im 19. Jahrhundert entdeckt und wissenschaftlich beschrieben. Zu Beginn des 20. Jahrhunderts waren nur noch zehn der natürlichen Elemente unbekannt. Seither wurden vor allem schwer zugängliche, oftmals radioaktive Elemente dargestellt. Viele dieser Elemente kommen nicht in der Natur vor und sind das Produkt von künstlichen Kernverschmelzungsprozessen. Erst im Dezember 1994 wurden die beiden künstlichen Elemente Darmstadtium (Eka-Platin) und Roentgenium (Eka-Gold) hergestellt. Anfang des 19. Jahrhunderts stellte Johann Wolfgang Döbereiner erstmals einen Zusammenhang zwischen der Atommasse und den chemischen Eigenschaften einzelner Elemente fest. 1863 stellte Newlands eine nach Atommassen geordnete Tabelle der Elemente in Achtergruppen (Gesetz der Oktaven) auf. Das Periodensystem selbst wurde 1869 nahezu gleichzeitig und unabhängig voneinander von Dmitri Mendelejew (1834–1907) und Lothar Meyer (1830–1895) aufgestellt. Dabei ordneten sie ebenfalls die chemischen Elemente nach steigenden Atommassen, wobei sie Elemente mit ähnlichen Eigenschaften (Anzahl der Valenzelektronen) untereinander anordneten. Im 20. Jahrhundert wurde der Aufbau der Atome entdeckt, die Periodizität wurde durch den Aufbau der Elektronenhülle erklärt. Quellen: Wiktionary: Periodensystem – Bedeutungserklärungen, Wortherkunft, Synonyme, Übersetzungen Wikibooks: Anorganische Chemie für Schüler/ Hauptgruppen des PSE – Lern- und Lehrmaterialien Periodensystem der Elemente (Universität Ulm) 4 Beantworten Sie folgende Fragen! a) b) c) d) e) f) g) Woraus bestehen Atome? Was sind Elemente? Wonach sind die Elemente geordnet? Wieviele Hauptgruppen gibt es im PSE? Und wieviele Nebengruppen gibt es? Wer sind Mendelejew und Meyer? Wann wurde der Aufbau der Atome entdeckt? Definieren Sie folgende Begriffe und beschreiben Sie ihre Eigenschaften: das chemische Element das Atom die Verbindung die chemische Reaktion das Gemisch die Atommasse die Lösung Bilden Sie weitere Beispiele nach dem Muster! a) b) c) d) e) f) g) h) i) j) erklären – die Erklärung lösen – rechnen – wohnen – verändern – entdecken prüfen vorstellen – forschen – untersuchen – Nennen Sie Substantive mit gleicher Endung! Lehrer/in Schriftsteller/in ______________________, ________________________,_____________________, ______________________, ________________________, _____________________ 5 Die Eigenschaften sind durch Adjektive, Substantive oder Verben auszudrücken. Verwenden Sie folgendes Muster! Die meisten Metalle lassen sich dehnen. Sie sind dehnbar. Sie besitzen eine gute Dehnbarkeit. leiten Leiter leitfähig brennen Brennbarkeit brennbar trennen Trennbarkeit trennbar glänzen Glanz glänzend Ergänzen Sie die Tabelle. Deutsch Blei Symbol Pb Kroatisch olovo željezo Ag Gold He sumpor Sauerstoff Cu Wasserstoff C dušik Aluminium W kositar