Atombau & Periodensystem: Lehrbuchauszug
Werbung

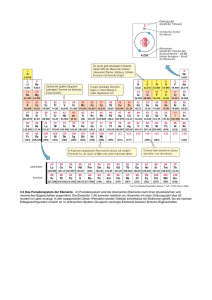
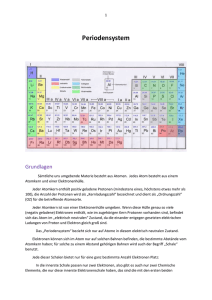
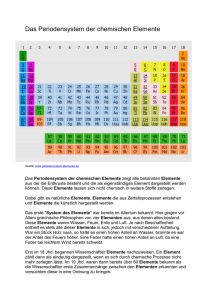
9.2 Atombau und gekürztes Periodensystem Atomaufbau/ Kern-Hülle Modell Bausteine der Atome Elementarteilchen Neutron Proton Elektron Ort Ladung Kern neutral Kern +1 Hülle -1 Kernbausteine=Nukleonen Atome bestehen aus einem winzigen positiv geladenen Kern, in dem die Masse konzentriert ist, und einer riesigen, fast massefreien Atomhülle aus Elektronen. Nach außen hin ist das Atom elektrisch neutral. Die Elektronen haben unterschiedliche Energieniveaus („Schalen“). 9.2 Atombau und gekürztes Periodensystem Isotope Definition Isotope: Atome eines Elements, die sich in ihrer Neutronenzahl und somit in ihrer Masse unterscheiden. Die Masseangaben im Periodensystem stellen einen Durchschnittswert der Isotopmassen des Elements dar. Die Häufigkeit der Isotope wird mit verrechnet. 9.2 Atombau und gekürztes Periodensystem Edelgaskonfiguration Edelgaskonfiguration: Die Elektronenkonfiguration der Edelgase wird als Edelgaskonfiguration bezeichnet. Sie ist besonders stabil. Beim Helium wird sie als Elektronenduett, bei allen weiteren Edelgasen als Elektronenoktett, bezeichnet. Chemische Reaktionen laufen meist so ab, dass die Reaktionspartner am Ender der chemischen Reaktion Edelgaskonfiguration besitzen. 9.2 Atombau und gekürztes Periodensystem Ordnung der Elemente im Periodensystem