Quantenphysik der Atomhülle
Werbung

Quantenphysik der Atomhülle
Sommeruniversität 2009
NW1, Raum N3380
25. & 26.06.2009
Ausgangslage, Voraussetzungen
Schülerinnen und Schüler sind vertraut mit
Mechanik
Größen: s, t, v, a, m, p, Wkin, Wpot
Schwingungen, Wellen, Kreisbewegungen
Stehende Welle
Elektromagnetismus
Ladung Q, Strom I, Spannung U
1
Q Q
Felder E und B
F
1 2 2
4 0
r
Coulomb
r
r
r
r
F
Q
(
v
B) I (A B)
Lorentzkraft
L
Induktion
c f, W h f
Elektromagnetische Welle
Ausgangslage, Voraussetzungen
Schülerinnen und Schüler sind vertraut mit
Licht als elektromagnetischer Welle
Farbe, Wellenlänge, Frequenz, h·f in eV
Huygenssches Prinzip, Interferenz,
Polarisation
Spektrum
Quantenmechanik
Richtung der Behandlung:
Licht und Elektronen sind Mikroobjekte
Beugung und Interferenz
Doppelspalt und Mach-Zehnder-Interferometer
Elektronenbeugung
de Broglie-Wellenläge und Impuls
Unschärfe/ Unbestimmtheitsrelation
Atommodell
Franck-Hertz-Experiment
Spektren
Potentialtopfmodell
Kernbaustein
Mikroobjekte
Kernbaustein
Quantenphysik
der Atomhülle
Unbestimmtheitsrelation
Impuls-Ort-Unbestimmtheit
Formulierung: Ort und Impuls von
Quantenobjekten lassen sich gleichzeitig nicht
beliebig genau bestimmen. Für die mittleren
Unbestimmtheiten gilt:
h
x px
4
Energie-Zeit-Unbestimmtheit
Die Formulierung lautet:
E t
h
4
Konsequenz: Lokalisierungsenergie
Wkin
h2
8 m L2
auch
Beispiele finden sich auch in
den veröffentlichten Aufgaben
und Musteraufgaben für das
Bremer Zentralabitur Physik
F. Kranzinger, Impulse Physik Quantenphysik, Klett 2002
Material zu Quantenmechanik
Im Netz:
Uni Bremen: Materialien des IDN - Physik
milq: Münchner Internetprojekt zur
Lehrerfortbildung in Quantenmechanik
BaWü: Quantenphysik in elementaren
Portionen
educeth.ch: Kann man Atome sehen?
Uni Bonn: Physik 2000; Dialoge
Franck-Hertz-Experiment
James Franck (1882 -1962),
jüdischer Physiker,
Göttingen, Chikago
Gustav Hertz (1887 - 1975),
jüdischer Physiker,
Arbeit in der Sowjetunion,
Karriere in der DDR
Zur Anzeige wird der QuickTime™
Dekompressor „“
benötigt.
Zur Anzeige wird der QuickTime™
Dekompress or „“
benötigt.
Quellen: http://nobelprize.org/nobel_prizes/physics/laureates/1925/hertz-bio.html, http://upload.wikimedia.org/wikipedia/commons/6/6c/James_Franck.jpg
Franck-Hertz-Experiment
1912/1914: Konzeption des
Elektronenstoßexperiments,
„Dozent und Postdoc“
Beide nahmen in der deutschen
Armee im Weltkrieg am
„Gaskrieg“ teil
Für 1925: Physik-Nobelpreis
Ab 1933 bzw. 1935 war Arbeit
an der Universität unmöglich,
Emigration bzw. Rückzug
Zur Anzeige wird der QuickTime™
Dekompressor „“
benötigt.
Zur Anzeige wird der QuickTime™
Dekompress or „“
benötigt.
Quellen: http://nobelprize.org/nobel_prizes/physics/laureates/1925/hertz-bio.html, http://upload.wikimedia.org/wikipedia/commons/6/6c/James_Franck.jpg
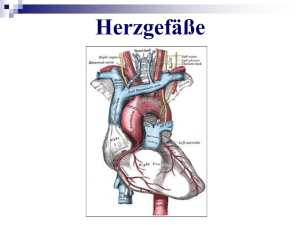
Franck-Hertz: Aufbau
Gasgefüllter Kolben mit Glühkathode,
Gitter und Anode, Hg-Dampf von 10mbar
Regelbare Beschleunigungsspannung Ub
und kleine Gegenspannung Ug
Strom an der Anode wird gemessen
Franck-Hertz: Durchführung
Bei Gegenspannung von Ug = 1 V werden
sehr geringe Ströme (nA) gemessen, die
stark davon abhängen, welche
Beschleunigungsspannung Ub anliegt
Franck-Hertz-Experiment mit Neon
Strom in willkürlichen Einheiten
2
1,8
1,6
1,4
1,2
1
0,8
0,6
0,4
0,2
0
0
10
20
30
40
Spannung / V
50
60
70
Franck-Hertz: Bauformen
Die Hg-Röhre benötigt Heizung
Die Ne-Röhre benötigt höhere Spannungen
Zur Anzeige wird der QuickTime™
Dekompressor „“
benötigt.
http://www.physik.tu-muenchen.de/studium/betrieb/praktika/anfaenger/bilder/FHV-01.jpg
Franck-Hertz: Erklärung
Der parabelförmige Beginn der
Kennlinie verläuft wie bei einer Diode
in Durchlassrichtung
Ab ca. Ub = 5 V nimmt der Strom kräftig ab, dieses
Verhalten wiederholt sich regelmäßig
Die Abstände der relativen Maxima sind jeweils gleich
und vom Füllgas abhängig
Für Hg: ∆U = 4,9 V, für Ne: ∆U = 19 V
Die Elektronen verlassen die Kathode und werden im
(homogenen) elektrischen Feld von Ub beschleunigt.
Dabei gewinnen sie auf dem Weg kinetische Energie. So
können sie die Gegenspannung Ug überwinden und zum
gemessenen Strom beitragen
Franck-Hertz: Erklärung 2
Die Elektronen stoßen mit den
Gasmolekülen, zunächst elastisch
Bei elastischen Stößen verlieren sie keine Energie, da
die Hg-Atome viel schwerer sind
Steigt die kinetische Energie der Elektronen auf mehr als
Wkin = 4,9 eV, kommt es zu unelastischen Stößen
Die Elektronen sind anschließend zu langsam um die
Gegenspannung Ug zu überwinden und können nicht
mehr zum Anodenstrom beitragen: Die Stromkurve sinkt
Bei Beschleunigungsspannungen von Ub = 10 V,
15 V, ... kann dies zweimal, dreimal, ... passieren
Erst bei höheren Spannungen findet Ionisation statt
Franck-Hertz: Erklärung 3
Die unelastischen Stöße werden so
gedeutet, dass die Hg-Atome die
Energieportionen von ∆W = 4,9 eV
aufnehmen können
Dass dies plausibel ist, zeigt ein Blick in die Röhre: In
Form von sichtbaren Licht wird die aufgenommene
Energie wieder abgegeben
Bei der Ne-Röhre kann man - je nach
Beschleunigungsspannung Ub - mehrere leuchtende
Schichten identifizieren
Spannung Ub ist ca, 20 V, 40 V, 60 V
Franck-Hertz: Deutung
Die freien Atome sind in der Lage auch ohne
Ionisation Energieportionen aufzunehmen
Diese sind für die jeweiligen Elemente
spezifisch, z.B.
für Quecksilber Hg: ∆W = 4,9 eV
für Neon Ne: ∆W = 19 eV
Atome, die Energieportionen aufgenommen
haben, bezeichnet man als „angeregt“
Sonst sind sie „im Grundzustand“
Franck-Hertz: Didaktik
Etliche Erklärungsmuster in Schulbüchern und
Webseiten.
Animationen und interaktive Web-Experimente
Häufig Thema von Abiturprüfungen
EPA Physik
Grundkursaufgabe 2007
Musteraufgabe LK Franck-Hertz
Anlass für historische Betrachtungen, bei LeifiPhysik finden sich Teile der Originalarbeit.
Spektren: Information über das Atom
Linienspektren von leuchtenden Gasen wie Hg,
H2, He, O2
Spektren ausmessen!!!
Balmer (1885) findet eine Formel für die vier
sichtbaren Linien
1
R(
1
22
1
n
7 1
);
n
3,
4,...;
R
1,
097
10
m
2
Wasserstoff: Auch Spektrallinien im Infrarot- und
im Ultraviolettbereich
Angeregte Atome geben Energie in Portionen ab
Spektrum des Wasserstoffs
Zur Anzeige wird der QuickTime™
Dekompressor „“
benötigt.
Quelle: wikipedia
Historische Atommodelle?
Sicher physikalisch interessant
z.B. das Schokokeksmodell
oder Rutherford übers Netz
(http://rutherford.gymnasium.isernhagen.de/ger/index.htm)
aber ...
Bohrs Modell ist so suggestiv, dass man
ganz drauf verzichten sollte
Zur Anzei g e wir d der Qui ckTime™
D ekompr essor „ “
benötig t.
Schrödingergleichung
Der Zustand von physikalischen Systemen
wird durch (r,t) beschrieben.
Zu physikalischen Größen gibt es einen
Operator,
h
px
zum Impuls:
i x
zur Energie:
h
i t
E
Schrödingergleichung
Gesucht ist eine mathematische Beschreibung von
Mikroobjekten für alle Orte r und alle Zeiten t.
Die zeitunabhängige Schrödingergleichung mit der
komplexwertigen Funktion (r)
und dem Potential V(r) lautet:
h2
2m
(r) V (r) (r) E (r)
Exakte Lösungen sind nur in Spezialfällen
bekannt, wenn das Potential besonders einfach ist.
Z.B. habe es die Größe V0 in einem „Kasten“ der
Breite L in der einzigen Dimension x. Dann ist das
Elektron auf diesen Raum beschränkt, 0 ≤ x ≤ L.
Lösung der Schrödingergleichung
Außerhalb des Kastens verschwindet die
Wellenfunktion, ebenso an den beiden Grenzen
x = 0 und x = L
Innerhalb des Kastens sind Funktionen gesucht,
die - bis auf Faktoren - gleich der 2. Ableitung sind.
Ansatz ist, wie bei stehenden Wellen (x) A sin(B x)
h
B V E
Dann folgt
2m
n
B
Andrerseits ist
L
h
E
n V
und damit
2m L
2
0
2
n
2
2
0
2
Lösungen im Potentialtopf
Quelle: milq
Nur in einfachen Fällen ergeben sich reellwertige
Lösungen, daher kommt der komplexen Größe keine
anschauliche Bedeutung zu.
2
Aber das Quadrat von hat eine anschauliche
(x)
Interpretation: Die Wahrscheinlichkeitsdichte
drückt aus, mit welcher Wahrscheinlichkeit wir das Objekt,
das durch
beschrieben wird,
am Ort x
treffen
1-dim. Potentialtopf - Bedeutung
Damit haben wir ein Atommodell, das zwar sehr
stark vereinfacht, aber „physikalisch richtig“ stabile
Zustände für das Elektron bei unterschiedlichen
Energien liefert.
E (n) n 2
Wir haben die Existenz von „Stufen“ gefunden,
aber die Abstände stimmen noch nicht.
Es gibt tatsächlich„1-dimensionale“ Strukturen wie KWSt
mit alternierenden Doppelbindungen, für die dies Modell
realistische Beschreibungen liefern kann (Bei milq: Benzol).
Von der Beschreibung eines Atoms sind wir noch
ein Stück entfernt.
1-dimensionaler Potentialtopf, n = 2
Verschiedene
Methoden, dies
Ergebnis darzustellen:
Verteilung
Simulation
Dichte
(Metzler Physik)
Dreidimensionaler Potentialtopf
Quelle: milq
milq:
Dreidimensionaler Potentialtopf
Danach gibt es nun drei
voneinander
unabhängige
„Quantenzahlen“, die die
Energie eines
Zustandes festlegen.
Jede Kombination ist
möglich, die Übergänge
lassen sich in einem
Termschema
übersichtlich darstellen.
Zur Anzeige wird der QuickTime™
Dekompressor „“
benötigt.
Quelle: milq
Dreidimensionaler Potentialtopf
(x, y, z)
2
Die räumliche Verteilung der Wahrscheinlichkeitsdichte
wird als Orbital bezeichnet. Bemerkenswert sind Knotenflächen, wo
Nullstellen von (x, y, z) vorliegen. (Impulse Physik)
2
Realistisches Potential
Das Kastenpotential ist nur eine grobe
Annäherung an das reale CoulombPotential mit der Proportionalität zu 1/r
Durch geeignete
Wahl von V0 und
R kann das
Modell zeigen:
En
1
n2
Quelle: milq
Weitere Quantenzahlen
Hauptquantenzahl n
n {1, 2, 3,...}
Nebenquantenzahl l
l {0,1, 2,..,n 1}
Magnetische QZahl m
Zur Anzeige wird der QuickTime™
Dekompressor „“
benötigt.
m {l, l 1,.., 1, 0,1,..,l }
Spinquantenzahl s
1 1
s { , }
2 2
Bedeutsam bei höheren
Energien oder
Mehrelektronensystemen
http://www.tf.uni-kiel.de/matwis/amat/mw1_ge/kap_2/illustr/terme3.gif
Hydrogenlab
Das Projekt www.hydrogenlab.de widmet sich der
Frage: Wie kann ich mir ein Wasserstoffatom
vorstellen?
Präsentiert werden graphische Darstellungen der
Lösungen der Schrödingergleichung.
„Man sieht den Bildern viele Eigenschaften des
Atoms unmittelbar an: seinen Platzbedarf, seinen
Drehimpuls und seinen Magnetismus...
Am Ende hat man das Gefühl, dass man doch
wüsste, wie das Atom aussieht.“
Hydrogenlab
Auf der Startseite werden 4 Menüs angeboten:
Zum Start bietet sich die Multimediapräsentation an.
Bearbeiten Sie das Kapitel Einleitung mit den Unterkapiteln
Hauptseite (3 Folien) und Darstellungsverfahren (9 Folien)
Charakterisieren Sie die drei Darstellungsverfahren
1.
2.
3.
Arbeiten Sie die Galerie durch. Als Überblick gibt es auf der
Startseite 6 Fenster mit Einzelbildern und Animationen.
Problem: Was unterscheidet den Übergang
(2,1,0) --> (1,0,0) vom Übergang (2.0.0) --> (1,0,0)?
Hydrogenlab
Auf der Startseite werden 4 Menüs angeboten:
Programme liefert vier Java-Applets:
1. Density
2D Darstellung der Elektronendichteverteilung des Wasserstoffatoms bis n=16
2. Orbital
3D Darstellung der Orbitale des Wasserstoffatoms
3. Animation
Elektronendichteverteilung bei Übergängen im Wasserstoffatom bis n=16
4. Animation3D
Orbitale bei Übergängen im Wasserstoffatom bis n=9
Die Berechnungen können zum Teil sehr
lange dauern!
Hydrogenlab
Auf der Startseite werden 4 Menüs angeboten:
Materialien verweist auf
1. die CD
2. download-bare Dateien zur Illustration der
atomaren Zustände
3. downloadbare Dateien zur Illustration der
atomaren Übergänge
4. Poster
Hydrogenlab
Auf der Startseite werden 4 Menüs angeboten:
Elektronium verweist auf Material für SuS eines
Kurses Atomphysik für die Sek. I
1. Eine 9-stündige Unterrichtseinheit
2. Didaktische Hinweise dazu
3. Fortsetzung in der Sek. II (Hier werden die
Themen vertieft, die in der Galerie nur angedeutet
werden konnten.)
Das Elektroniumkonzept ist ein Bestandteil des Karlsruher
Physikkurses KPK und außerhalb von Ba-Wü wenig
bekannt. Äquivalent dazu kann man mit dem Modell
der Aufenthaltswahrscheinlichkeit arbeiten.
Hydrogenlab
Aufträge:
Start und Galerie durcharbeiten (Lageplan)
Einige Zustände und einen (einfachen)
Übergang erläutern können
Den Sek. I - Kurs überfliegen (mit
Aufenthaltswahrscheinlichkeit statt Elektronium)
In der Gruppe die 6. Stunde (Wie entsteht Licht?)
auf Machbarkeit abklopfen
Anders Vorgehen ist selbstverständlich möglich
(Wir haben ja Ferien :-)