1.1 AUFBAU DER ATOME
Werbung

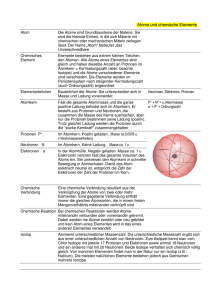
1 ATOME – TEILCHEN DES UNIVERSUMS Nebel aus frei beweglichen Teilchen Gruppe Entwicklung von Galaxien, Planeten etc. 1 2 3 6 7 8 9 10 11 12 13 14 15 16 17 18 2 H 3 Ausdehnung des Weltalls 4 Li 2 Lithium 11 3 weitere Ausdehnung Au des Weltalls Urknall Natrium Magnesium 20 Entwicklung des Universums 24 25 26 27 9 8 C Kohlenstoff N Stickstoff 28 29 10 O F Sauerstoff Fluor 17 16 Ne Neon 18 Si P S Cl Ar Aluminium Silicium Phosphor Schwefel Chlor Argon 31 30 15 14 Al 32 33 34 35 36 Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Scandium Titan Vanadium Chrom Mangan Eisen Cobalt Nickel Kupfer Zink Gallium Germanium Arsen Selen Brom Krypton 38 Rb 39 Sr Strontium 56 40 Y Yttrium 57 - 71 41 Zr 42 Nb Zirconium 72 Niob 73 43 Mo Molybdän 74 44 Tc Technetium 75 Ru Ruthenium 76 45 46 Rh Rhodium 77 47 Pd 49 48 Ag Palladium 78 Silber 79 Cd Cadmium 50 In 51 Sn Indium 81 80 Zinn 52 Sb 53 54 Te Antimon 83 82 I Tellur 84 Iod 85 Xe Xenon 86 Cs Ba Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn Caesium Barium Hafnium Tantal Wolfram Rhenium Osmium Iridium Platin Gold Quecksilber Thallium Blei Bismut Polonium Astat Radon 87 heute 23 B Bor 13 Halbmetalle Calcium Rubidium 7 22 7 6 Metalle Nichtmetalle radioaktive Elemente K 55 Erde 21 Kohlenstoff 5 Fe O Hg feste Elemente gasförmige Elemente C Elementname Helium Kalium 37 6 6 Elementsymbol flüssige Elemente Mg 4 5 Ordnungszahl Be Beryllium 12 Na 19 He Periodensystem der Elemente Wasserstoff 4,6 Milliarden Jahre vor heute 5 1 1 13,7 Milliarden Jahre vor heute 4 Periode 88 89 - 103 104 105 106 107 108 109 Fr Ra Rf Db Sg Bh Hs Mt Francium Radium Rutherfordium Dubnium Seaborgium Bohrium Hassium Meitnerium 57 58 La 57 – 71 Lanthan 89 89 – 103 59 Ce Cer 90 60 Pr Praseodym 91 61 Nd Neodym 92 Pm Promethium 93 62 Sm Samarium 94 63 Eu Europium 95 110 111 Ds Rg Darmstadtium Röntgenium 64 65 Gd Gadolinium 96 Tb Terbium 97 113 112 114 115 116 117 118 Cn Uut Fl Uup Lv Uus Uuo Copernicium Ununtertium Flerovium Ununpentium Livermorium Ununseptium Ununoctium 66 67 69 70 71 Dy Dysprosium 98 68 Ho Holmium 99 Er Erbium 100 Tm Thulium 101 Yb Ytterbium 102 Lu Lutetium 103 Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Actinium Thorium Protactinium Uran Neptunium Plutonium Americium Curium Berkelium Californium Einsteinium Fermium Mendelevium Nobelium Lawrencium Der menschliche Körper besteht aus über einer Pentillion Atomen. Das ist eine 1 mit 27 Nullen. Aber was sind Atome? Was unterscheidet sie voneinander? Aus welchen Atomen bestehen wir? Wie kann man einen Mangel an bestimmten Atomen im Körper messen? Und woher kommt das, woraus unser Körper besteht? Atomkern mit Protonen und Neutronen 1.1 AUFBAU DER ATOME Die Teilchen eines Atoms Die gesamte Materie im Universum ist aus Atomen zusammengesetzt. Aus dem Griechischen übersetzt bedeutet Atom das „Unteilbare“. Das entspricht nicht mehr unserer heutigen Erklärung von Atomen. Heute weiß man, dass Atome aus noch kleineren Teilchen, den Protonen, Neutronen und Elektronen, aufgebaut sind. Heute definiert man Atome so: Atome sind kleine Teilchen der Materie, die aus Protonen, Neutronen und Elektronen bestehen. Der größte Unterschied zwischen diesen Teilchen ist die Ladung. Protonen sind positiv geladen, Neutronen sind neutral und Elektronen sind negativ geladen. Da sich diese drei Teilchenarten an ganz bestimmten Orten aufhalten, unterteilt man ein Atom in zwei Bereiche: Teilchenart Ladung Abkürzung Ort Protonen positiv p+ Atomkern Neutronen neutral n Atomkern Elektronen negativ e— Atomhülle Abb. 1 Protonen, Neutronen und Elektronen im Vergleich 8 Atomhülle Elektron Abb. 2 Skizze eines Atoms Den inneren Teil nennt man Atomkern und den äußeren Atomhülle. Protonen und Neutronen halten sich nur im Atomkern auf. Elektronen befinden sich nur in der Atomhülle. Protonen und Neutronen sind etwa 2 000-mal schwerer als Elektronen. Daher hat der Atomkern fast die ganze Atommasse. Die Atomhülle hat fast keine Masse. Sie nimmt aber fast den ganzen Atomdurchmesser ein. Wäre ein Atomkern so groß wie ein Kirschkern, hätte die Atomhülle einen Durchmesser von ca. 1 Kilometer. Wenn nichts anderes angeführt ist, geht man immer von neutralen Atomen aus. In einem neutralen Atom sind gleich viele positive Protonen wie negative Elektronen vorhanden. ATOME – TEILCHEN DES UNIVERSUMS Beschreibung der Atome Das wichtigste Merkmal von Atomen ist ihre Anzahl an Protonen. Man nennt diese Zahl auch Protonenzahl. Sie allein bestimmt, um welches Element es sich handelt. Ein Element ist ein Stoff, dessen Atome alle die gleiche Anzahl an Protonen haben. Heute kennen wir 118 verschiedene Elemente. Die Atome des größten Elements enthalten also 118 Protonen im Kern. So wie das Wort Atom hatte in der Antike auch das FEUER Wort Element eine andere warm und trocken Bedeutung. Vor mehr als 2 000 Jahren gingen grieERDE LUFT chische Philosophen davon kalt warm und und aus, dass die ganze Welt aus trocken feucht den vier Elementen Erde, Feuer, Wasser und Luft aufWA S S E R kalt gebaut ist. Dass dem nicht und feucht Abb. 3 Die vier Elemente in der so ist, weiß die Wissenschaft seit ca. 200 Jahren. Antike Protonen- lateinische zahl Bezeichnung Symbol deutsche Bezeichnung 1 Hydrogenium H Wasserstoff 2 Helium He Helium 6 Carboneum C Kohlenstoff 7 Nitrogenium N Stickstoff 8 Oxigenium O Sauerstoff 16 Sulfuricum S Schwefel 26 Ferrum Fe Eisen Abb. 4 Wichtige Elemente und ihre Symbole Ein zweiter Buchstabe kommt nur dann vor, wenn der erste Buchstabe des Namens schon als chemisches Symbol vergeben wurde (z. B. H steht für Hydrogenium, He steht für Helium). Dieser zweite Buchstabe wird immer klein geschrieben. 1) Nenne die Bestandteile eines Atoms. Erkläre, wodurch sie sich unterscheiden. Chemische Elementnamen und ihre Symbole Jedes chemische Element hat einen eigenen Namen. Da diese Namen oft lateinisch und sehr lange sind, verwendet man Abkürzungen. Man nennt sie chemische Symbole. Meistens wird nur der erste Buchstabe des Elementnamens als Abkürzung verwendet. Auf den Punkt gebracht! 2) Skizziere ein Atom und beschrifte deine Skizze. 3) Nenne die lateinischen Bezeichnungen und die chemischen Symbole für Wasserstoff, Kohlenstoff, Stickstoff und Sauerstoff. 4) Nenne das wichtigste Merkmal eines Elements. 5) Definiere den Begriff chemisches Element. Summary Atome sind kleine Teilchen, die aus Protonen, Neutronen und Elektronen aufgebaut sind. Atoms are small particles built from protons, neutrons and electrons. Ein Atom teilt man in einen Atomkern und eine Atomhülle ein. An atom is divided into a nucleus and an electron shell. Im Atomkern sind positiv geladene Protonen und neutrale Neutronen. The nucleus contains positively charged protons and uncharged neutrons. In der Atomhülle befinden sich negativ geladene Elektronen. The shell contains negatively charged electrons. Die Elemente unterscheiden sich durch ihre Protonenzahl. Ein Element besteht aus Atomen mit gleicher Protonenzahl. Atom types differ in the number of protons. If a substance contains just one kind of atom, it is called a chemical element. Jedes der 118 chemischen Elemente wird durch ein bestimmtes chemisches Symbol gekennzeichnet. Each of the 118 chemical elements are identified by a chemical symbol. 9