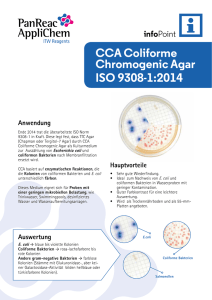
BD Brilliant Green Agar
Werbung

GEBRAUCHSANWEISUNG – GEBRAUCHSFERTIGE PLATTENMEDIEN PA-212097.07 Rev.: Oct 2013 BD Brilliant Green Agar VERWENDUNGSZWECK BD Brilliant Green Agar (Brillantgrün-Agar) ist ein hochselektives Medium zur Isolierung von Salmonellen, mit Ausnahme von S. typhi, aus Fäzes und anderen klinischen Proben. GRUNDLAGEN UND ERLÄUTERUNG DES VERFAHRENS Mikrobiologische Methode. Die Verwendung von Brillantgrün-Agar zur Isolierung von Salmonellen wurde erstmals von Kristensen et al. beschrieben. 1 Später wurde das Medium von Kauffmann modifiziert.2 Das Medium ermöglicht nachweislich die Inokulation starker Inokulate in der klinischen und nichtklinischen Anwendung. Es ist im Arzneimittelbuch der USA (United States Pharmacopeia, USP) bei den mikrobiologischen Verfahren für die Abwesenheit angegebener Mikroorganismen in Nahrungsergänzungsmitteln (Microbiological procedures for absence of specified microorganisms—nutritional and dietary supplements) aufgeführt und wird für die Untersuchung von Milchprodukten verwendet. Außerdem wird es in klinischen Mikrobiologie-Handbüchern erwähnt.3-8 Hefeextrakt und zwei Peptone liefern die Nährstoffe in BD Brilliant Green Agar; Lactose und Saccharose bilden gemeinsam mit Phenolrot ein Differenzierungssystem zum Ausschluss von Lactose- und/oder Saccharosefermentern (z.B. E. coli), da Salmonellen keine Säure aus diesen Zuckern produzieren. Brillantgrün ist der selektive Stoff zur Hemmung des Wachstums der begleitenden Flora. REAGENZIEN Zusammensetzung* pro Liter destilliertem Wasser BD Brilliant Green Agar Hefeextrakt 3,0 g Bacto Proteose-Pepton 10,0 Lactose 10,0 Saccharose 10,0 Natriumchlorid 5,0 Phenolrot 0,08 Agar 20,0 Brillantgrün 12,5 mg pH 6,9 ± 0,2 *Nach Bedarf abgestimmt und/oder ergänzt auf die geforderten Testkriterien. VORSICHTSMASSNAHMEN . Nur für den professionellen Gebrauch. Agarplatten bei Anzeichen von mikrobieller Kontamination, Verfärbung, Austrocknung, Rissen oder sonstigen Anzeichen von Produktverfall nicht verwenden. Hinweise zur aseptischen Arbeitsweise, Biogefährdung und Entsorgung des Produkts sind der ALLGEMEINEN GEBRAUCHSANLEITUNG zu entnehmen. AUFBEWAHRUNG UND HALTBARKEIT Nach Erhalt Platten bis unmittelbar vor dem Gebrauch im Dunkeln bei 2 – 8 °C in der Originalverpackung lagern. Einfrieren und Überhitzen vermeiden. Die Platten können bis zum Verfallsdatum (s. Kennzeichnung auf der Verpackung) inokuliert und entsprechend den empfohlenen Inkubationszeiten inkubiert werden. Platten aus bereits geöffneten Stapeln mit jeweils 10 Platten können bei Lagerung in einem sauberen Bereich bei 2 – 8 °C bis zu einer Woche verwendet werden. PA-212097.07 -1- QUALITÄTSSICHERUNG DURCH DEN ANWENDER Repräsentative Proben mit den nachfolgend aufgeführten Stämmen inokulieren (detaillierte Informationen siehe ALLGEMEINE GEBRAUCHSANLEITUNG). Platten bei 35 – 37 °C 18 – 48 Stunden lang aerob inkubieren. Stämme Escherichia coli ATCC 25922 Enterococcus faecalis ATCC 29212 Salmonella Abony DSM 4224 Salmonella Typhimurium ATCC 14028 Nicht inokuliert Wachstum Kein bis mittleres Wachstum; gelbe bis grün-gelbe Kolonien, gelbe Höfe Kein bis geringes Wachstum; gelbliche Kolonien mit oder ohne gelbe Höfe 10 bis 100 Kolonien; weißliche Kolonien, rote Höfe Gutes bis sehr gutes Wachstum; weißliche Kolonien, rote Höfe Bräunlich bis Olivgrün VERFAHREN Mitgeliefertes Arbeitsmaterial BD Brilliant Green Agar (90 mm Stacker-Platten). Mikrobiologisch kontrolliert. Nicht mitgeliefertes Arbeitsmaterial Zusätzliche Kulturmedien, Reagenzien und Laborgeräte nach Bedarf. Probenarten Stuhl- oder Rektalabstriche von Patienten mit Verdacht auf Infektion mit Salmonella-Spezies außer S. typhi (siehe auch LEISTUNGSMERKMALE UND VERFAHRENSBESCHRÄNKUNGEN). Das Medium wird auch für tierische oder Nahrungsmittelmaterialien verwendet. Testverfahren Probe direkt ausstreichen oder das Medium mit einer geringen Menge Wachstums aus einem flüssigen Anreicherungsmedium (z.B. Tetrathionat-Bouillon) inokulieren. Ein oder zwei weniger selektive Medien sollten ebenfalls inokuliert werden, insbesondere wenn das Material eine niedrige Population aufweist. Probe zur Verdünnung ausstreichen und Platten bei 35 – 37 °C 42 – 48 Stunden lang aerob inkubieren. Platten nach 18 – 24 sowie nach 42 – 48 Stunden ablesen. Ergebnisse Typischerweise weisen die Organismen auf BD Brilliant Green Agar folgendes Erscheinungsbild auf: Organismus Ergebnisse Salmonella (außer S. Typhi und Weiße bis rote Kolonien, umgeben von roten Zonen S. Paratyphi) S. Typhi und S. Paratyphi Kein Wachstum bis Spuren von Wachstum Shigella spp. Kein Wachstum bis Spuren von Wachstum Escherichia coli, Klebsiella und Gelbe bis grünliche Kolonien, umgeben von gelb-grünen Zon Enterobacter Pseudomonas Kein Wachstum bis Spuren von Wachstum grampositive Bakterien Kein Wachstum bis Spuren von Wachstum LEISTUNGSMERKMALE UND VERFAHRENSBESCHRÄNKUNGEN BD Brilliant Green Agar ist ein hoch selektives Medium zur Isolierung von Salmonellen und ermöglicht die Isolierung dieser Organismen selbst aus stark kontaminierten Materialien, einschließlich Fäzes.4-8 PA-212097.07 -2- Weniger selektive Medien zur Isolierung von Salmonellen sowie eine MacConkey II-Agar-Platte sollten mit der Probe bzw. dem Material inokuliert werden. Proteus kann pathogenen Darmbakterien ähneln, da weiße bis rote Kolonien mit roten umgebenden Zonen produziert werden. Obwohl das Wachstum bestimmter Stämme möglich ist, eignet sich BD Brilliant Green Agar nicht für die Isolierung von Salmonella typhi und S. paratyphi. Obwohl bestimmte diagnostische Tests direkt auf diesem Medium durchgeführt werden können, sind für eine vollständige Identifizierung biochemische und serologische Tests unter Verwendung von Reinkulturen erforderlich. LITERATUR 1. Kristensen, M., V. Lester, and A Jurgens. 1925. On the use of trypsinized casein, brom thymol blue, brom cresol purple, phenol red and brilliant green for bacteriological nutrient media. Brit. J. Exp. Pathol. 6: 291. 2. Kauffmann, F. 1935. Weitere Erfahrungen mit den kombinierten Anreicherungsverfahren für Salmonellabacillen. Z. Hyg. Infektionskr. 117: 26. 3. The United States Pharmacopeial Convention. The United States Pharmacopeia-National formulary, current edition. U.S. Pharmacopeial Convention, Inc., Rockville, Md. 4. Flowers, R.S., W. Andrews, C.W. Donelly, and E. Koenig. 1993. Pathogens in milk and milk products, p. 103-212. In: R.T. Marshall (ed.). Standard methods for the examination of dairy 5. products, 16th ed. American Public Health Association, Washington DC, USA. 6. Osborn, W.W., and J.L. Stokes. 1955. The determination of Salmonellae in foods. Food and Drug Laboratories, Ottawa, Canada. 7. MacFaddin, J. 1985. Media for the isolation-cultivation- identification-maintenance of medical bacteria. Williams and Wilkins, Baltimore, USA. 8. Bopp, C. A., F. W. Brenner, P. I. Fields, J. G. Wells, and N. A. Stockbrine. 2003. Escherichia, Shigella, and Salmonella. In: Murray, P. R., E. J. Baron, J.H. Jorgensen, M. A. Pfaller, and R. H. Yolken (ed.). Manual of clinical microbiology, 8th ed. American Society for Microbiology, Washington, D.C. LIEFERBARE PRODUKTE BD Brilliant Green Agar Best.-Nr. 212097 Gebrauchsfertige Plattenmedien, 20 Platten WEITERE INFORMATIONEN Weitere Informationen erhalten Sie bei Ihrer örtlichen BD-Vertretung. Becton Dickinson GmbH Tullastrasse 8 – 12 D-69126 Heidelberg/Germany Phone: +49-62 21-30 50 Fax: +49-62 21-30 52 16 [email protected] http://www.bd.com http://www.bd.com/europe/regulatory/ ATCC is a trademark of the American Type Culture Collection BD, BD Logo and all other trademarks are the property of Becton, Dickinson and Company. © 2013 BD PA-212097.07 -3-