Das Lungenkarzinom - Krebsregister Bern
Werbung

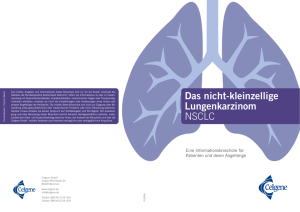
Das Lungenkarzinom Marco Weber Krebsregister Kanton Bern Das Lungenkarzinom 0. Gliederung 1. Einführung 1.1 Epidemiologie, Risikofaktoren, Anatomie der Lunge Topographie, Morphologie (Histologische Einteilung) 2. Klassifikation TNM, VALG-Klassifikation 3. Diagnostik Symptome, Diagnostik 4. Therapie Operative Therapie, Radiotherapie, Chemotherapie, Targettherapie, Immuntherapie, nahe Zukunft Das Lungenkarzinom 1. Einführung 1.1 Epidemiologie • Welt (Jahr 2012) − − − − • Inzidenz: 1.8 Millionen Fälle (♂: 1.2 Mio. ♀: 583 Tsd.) Entspricht 12.9 % aller Krebserkrankungen Mortalität: 1.59 Millionen (♂: 1.099 Mio. ♀: 491 Tsd.) höchste Mortalität mit 19.4 % aller Krebserkrankungen Schweiz (Durchschnittswerte 2008-2012) − − − − Inzidenz: 3972 Fälle (♂: 2463 ♀: 1509) Entspricht ca. 10,3 % aller Krebserkrankungen Mortalität: 3089 (♂: 2010 ♀: 1079) Höchste Mortalität mit 19.1 % aller Krebserkrankungen Das Lungenkarzinom 1. Einführung 1.1 Epidemiologie Männer Welt (2012) Frauen Das Lungenkarzinom 1. Einführung 1.1 Epidemiologie Inzidenz der 5 häufigsten Krebsarten nach Geschlecht* Schweiz Krebsarten mit höchster Mortalität nach Geschlecht* *Schweiz, Durchschnittswerte 2008-2012, Schätzungen Das Lungenkarzinom 1. Einführung 1.1 Epidemiologie Das Lungenkarzinom 1. Einführung 1.2 Risikofaktoren In erster Linie schädigende Substanzen, die mit der Atemluft in die Lunge gelangen: • Rauchen (für 90 % der Lungenkarzinome verantwortlich) Risiko für Lungenkrebs bei 25 Zigaretten/Tag 24 mal höher als bei Nichtrauchern Entscheidend sind Ausmass und Dauer des Konsums • Passivrauchen ca. 1.6 % aller Bronchialkarzinome sind darauf zurückzuführen Bis zu 5-fach erhöhtes relatives Risiko je nach Dauer der Exposition • Berufliche Exposition mit Schadstoffen (umstritten!) z. B. Asbest, Arsen, Chrom, Nickel, aromatische Wasserstoffe Das Lungenkarzinom 1. Einführung 1.2 Risikofaktoren Raucherquote ausgewählter Länder (2012) Das Lungenkarzinom 1. Einführung 1.2 Risikofaktoren • Schadstoffbelastung in der Atemluft Bis zu 1.5-fach höheres Lungenkrebsrisiko, z. B. durch Dieselruss macht ca. 11 % der Lungenkrebsfälle in Europa aus • Infektionen chronische und/oder langwierige Infektionskrankheiten der Lunge z. B. Tuberkulose, COPD • Genetische Disposition häufige Ursache für Entstehung von Lungenkrebs bei Nierauchern 2-3fach erhöhtes Risiko • Ernährung Doppelt so hohes Risiko bei geringem Konsum von Früchten und Gemüse Das Lungenkarzinom 1. Einführung 1.3 Aufbau der Lunge Das Lungenkarzinom 1. Einführung 1.3 Aufbau der Lunge Das Lungenkarzinom 1. Einführung 1.3 Aufbau der Lunge Das Lungenkarzinom 1. Einführung 1.4 Topographie (ICD-10/ICD-O) R ICD10/ ICD-O Beschreibung C34.0 Hauptbronchus (incl. Carina, Lungenhilus) C34.1 Oberlappen C34.2 Mittellappen C34.3 Unterlappen C34.8 Bronchus und Lunge, mehrere Teilbereiche überlappend C34.9 Bronchus und Lunge, n. n. b. D02 Carcinoma in situ, Bronchus und Lunge (nur ICD-10) Das Lungenkarzinom 1. Einführung 1.5 Morphologie (Histologische Einteilung) • Lungenkarzinome: alle malignen epithelialen Tumoren des Lungenparenchyms einschliesslich der neuroendokrinen Karzinome • 8046/3 Nichtkleinzellige Lungenkarzinome (NSCLC) − 8070/3 Plattenepithelkarzinome (H*: 30-40 %, TVZ**: 300 Tage) − 8140/3 Adenokarzinome (H: 45 %, TVZ: 180 Tage) − 8012/3 Grosszellige Karzinome (H: 10 %) • 8041/3 Kleinzellige Lungenkarzinome (SCLC) (H: 20 %, TVZ: 10-50 Tage) − Zählen zu den neuroendokrinen Tumoren − Charakterisiert durch schnelles Wachstum und frühe Metastasierung • Karzinoide (H: <5 %) − Typische (8240/3) und atypische (8249/3) Karzinoide * Häufigkeit aller LC ** Tumorverdopplungszeit Das Lungenkarzinom 2. Klassifikation 2.1 TNM - Primärtumor Tx Tis T1 T1a T1b T2 T2a T2b positive Zytologie aus Sputum oder Bronchiallavage, Primärtumor nicht beurteilbar Carcinoma in situ (kein invasives Wachstum) Tumorgrösse max. 3 cm Feinere Unterteilung: Tumorgrösse max. 2 cm oder kleiner Tumorgrösse mehr als 2 cm, aber max. 3 cm Tumor grösser als 3 cm, aber kleiner als 7 cm und mit mind. einer der folgenden Eigenschaften: − Infiltration des Hauptbronchus ≥ 2 cm distal der Karina − Infiltration von viszeraler Pleura (Lungenfell) − Assoziierte Atelektase (fehlende/unvollständige Belüftung der Lunge) oder obstruktive Entzündung bis zum Hilus, aber nicht der ganzen Lunge Kann noch feiner unterteilt werden: Tumorgrösse mehr als 3 cm, aber kleiner als 5 cm Tumorgrösse mehr als 5 cm, aber kleiner als 7 cm Das Lungenkarzinom 2. Klassifikation 2.1 TNM - Primärtumor T3 T4 Tumor grösser als 7 cm oder Tumor mit einer der folgenden Eigenschaften Infiltration von Brustwand, Zwerchfell, Perikard, parietale Pleura (Rippenfell), mediastinale Pleura, N. phrenicus oder Infiltration des Hauptbronchus < 2 cm distal der Karina (ohne Befall der Karina) oder Atelektase der ganzen Lunge oder separate(r) Tumorknoten im gleichen Lappen wie der Primärtumor Tumor jeder Grösse Infiltration von Mediastinum, Herz, großen Gefäßen, Trachea, Ösophagus, N. recurrens, Wirbelkörper, Karina Tumorknoten im gleichen Lungenflügel wie der Primärtumor, aber nicht im selben Lappen Das Lungenkarzinom 2. Klassifikation 2.2 TNM – regionäre Lymphknoten Regionäre Lymphknoten • Zu den regionären Lymphknoten gehören die hilären, peribonchialen, intrapulmonalen, mediastinalen sowie die supraklavikulären und Skalenus-Lymphknoten • Lymphknotenmetastasen in anderen Regionen gelten als Fernmetastasen (M1b) • Die Seitenlokalisation kann das N-Stadium beeinflussen, wenn die Lymphknoten kontralateral (die dem Primärtumor gegenüberliegende Seite) befallen sind N0 N1 N2 N3 kein Lk-Befall Lk: ipsilateral hilär u/o peribronchial u/o intrapulmonal Lk: ipsilateral mediastinal u/o subkarinal Lk: kontralateral mediastinal u/o hilär, u/o ipsi-/kontralaterale Skalenus- und supraklavikuläre LK Das Lungenkarzinom 2. Klassifikation 2.2 TNM – regionäre Lymphknoten N0 kein Lk-Befall Das N1 Lungenkarzinom Lk: ipsilateral hilär u/o peribronchial u/o intrapulmonal N2Klassifikation Lk: ipsilateral mediastinal u/o subkarinal 2. N3 Lk: kontralateral mediastinal u/o kontralateral hilär, 2.2 T u/o M ipsi-/kontralaterale – regionäre Lymphknoten Skalenus- und supraklavikuläre LK N R Beispiele: N1 10-hilär ipsilateral T N2 2R/4R - mediastinal ipsilateral 7 - subkarinal N3 1 - supraklavikulär 10- hilär kontralateral Das Lungenkarzinom 2. Klassifikation 2.1 TNM - Fernmetastasen Fernmetastasen • bevorzugtes Befallsmuster: Lymphknoten, Lunge, Leber, Knochen, ZNS und Nebennieren • Fernmetastasen am häufigsten beim kleinzelligen Bronchialkarzinom • Beim NSCLC am häufigsten beim Subtyp Adenokarzinom M1a maligner Pleura- o. Perikarderguss* Pleurakarzinose, kontralaterale Tumorherde M1b Andere Fernmetastasen * mikroskopische Sicherung erforderlich Das Lungenkarzinom 2. Klassifikation 2.2 Stadiengruppierung Stadium (AJCC) TNM 5-J-ÜLR NSCLC 5-J-ÜLR SCLC IA T1a/b N0 M0 73 % IB T2a N0 M0 58 % IIA T1 a/b N1 M0 T2a N1 M0 T2b N0 M0 T2b N1 M0 T3 N0 M0 T1a/b N2 M0 T2a/b N2 M0 T3 N1/2 M0 T4 N0/1 M0 jedes T N3 M0 T4 N2 M0 jedes T jedes N M1 46 % IIB IIIA IIIB IV 20 % 15 % 36 % 24 % 8% 9% 13 % 1% Das Lungenkarzinom 2. Klassifikation 2.3 Klassifikation SCLC • auch für das SCLC wird die Verwendung der TNM empfohlen • Allerdings wird häufig immer noch die modifizierte VALGKlassifkation verwendet • Hauptgrund liegt in der im Gegensatz zum NSCLC seltenen OPIndikation VALG entspricht TNM Entspricht AJCC Very limited Disease (VLD) T1-2 N0-1 M0 IA, IB, IIA, partiell IIB (T2bN1M0) Limited Disease (LD) T3-4 und/oder N2-3 M0 Partiell IIB (T3N0M0) IIIA, IIIB Exensive Disease (ED) T1-4 N0-3 M1 IV Das Lungenkarzinom 3. Diagnostik 3.1 Symptome ca. 90 % der Patienten mit Lungenkarzinom weisen initial Krankheitssymptome auf Aufteilung der Symptome − 1/3 direkt durch Primärtumor verursacht (z. B. Husten) − 1/3 infolge der Tumorerkrankung wie z. B. Gewichtsverlust − 1/3 sind metastasenbedingte Symptome Verzögerungen in der Diagnosestellung von mehreren Wochen bis mehreren Monaten sind häufig Diese Verzögerungen entstehen einerseits durch die relativ späte Vorstellung beim Hausarzt, andererseits durch die verzögerte Überweisung an einen Lungenspezialisten Das Lungenkarzinom 3. Diagnostik 3.1 Symptome Symptom/klinische Zeichen mit abnehmender Häufigkeit: Das Lungenkarzinom 3. Diagnostik 3.2 Diagnostik Basisdiagnostik Anamnese, klinische Untersuchung Laboruntersuchungen Röntgen Thorax (p.a. und seitlich) Spiral-CT Thorax (incl. Oberbauchregion und incl. Nebennieren) Bronchoskopie Sonografie (Ultraschall) Abdomen Erweiterte Diagnostik PET-CT sowie MRT/CT des ZNS (ausser Stadium IA) zur Ausbreitungsdiagnostik bei kurativer Intention Bei potentiell operablen Tumoren Prüfung der Herz-Lungenfunktionalität z. B. mittels Lungenfunktion, Spiroergometrie usw. Das Lungenkarzinom 3. Diagnostik 3.2 Diagnostik Mikroskopische Diagnosesicherung Eine mikroskopische Sicherung ist zwingend notwendig! Wichtig ist vor allem die Unterscheidung zwischen kleinzelligem und nicht kleinzelligem Karzinom (unterschiedliche Therapie!) Bronchoskopie mit Biopsie/Zytologie bei bildgebendem Verdacht bei zentral gelegenen Tumoren > 2 cm Transthorakale Biopsie US/CT/MRT-gesteuert, wenn bronchoskopisch nicht erreichbar (z. B. kleiner Herd in der Peripherie) Bei schwer erreichbaren Tumorherden histologische Sicherung mittels Thorakoskopie oder Medistinoskopie Das Lungenkarzinom 3. Diagnostik 3.2 Diagnostik Bei Verdacht auf mediastinalen Lymphknotenbefall endobronchialer Ultraschall (EBUS) zur Inspektion der LK-Stationen und ggf. transbronchiale Feinnadelaspiration (TBNA) von verdächtigen Lymphknoten Pleurapunktion zum zytologischen Malignitätsnachweis bei Pleuraerguss (wenn Nachweis von Tumorzellen = M1a) Bei negativer Zytologie und fehlender Organmetastasierung ggf. Thorakoskopie mit Gewebeentnahme zum Nachweis einer Pleurakarzinose (M1a) Das Lungenkarzinom 4. Therapie 4.1 Stadienadaptierte Therapie NSCLC Stadium (AJCC) IA Stadienadaptierte Therapie NSCLC (Vereinfacht) - Operative Therapie IB - Operative Therapie + (ggf. adjuvante Chemotherapie) IIA - Operative Therapie + adjuvante Chemotherapie IIB - Operative Therapie + adjuvante Chemotherapie IIIA - Operative Therapie + adjuvante Chemotherapie - Induktionschemotherapie + Resektion + Radiotherapie - Simultane Radio-/Chemotherapie IIIB - Simultane Radio-/Chemotherapie - Sequentielle Radio-/Chemotherapie IV - Palliative Systemtherapie (Chemotherapie, Targettherapie) Das Lungenkarzinom 4. Therapie 4.1 Stadienadaptierte Therapie SCLC Stadium (AJCC) Stadienadaptierte Therapie SCLC (Vereinfacht) Very Limited Disease St. IA, IB, IIA, partiell IIB (T2bN1M0) - Operative Therapie + adjuvante Chemotherapie + ggf. adjuvante Radiotherapie - Prophylaktische Ganzhirnbestrahlung empfohlen Limited Disease St. partiell IIB (T3N0M0) IIIA, IIIB - Chemotherapie - Simultane Radio-/Chemotherapie - Prophylaktische Ganzhirnbestrahlung empfohlen Extensive Disease Stadium IV - Chemotherapie - Bei sehr guter Remission der Metastasen ggf. Radiotherapie des Primärtumors - Prophylaktische Ganzhirnbestrahlung Das Lungenkarzinom 4. Therapie 4.2 Operative Therapie • OP in kurativer Absicht ist das Verfahren der Wahl in den Stadien I, II sowie cT3 cN1 M0 beim nicht kleinzelligem Lungenkarzinom • Beim kleinzelligen Bronchialkarzinom OP nur bei cT1-2, cN0-1, M0 bzw. Very limited disease • Voraussetzung ist eine adäquate kardio-pulmonale Reserve sowie anatomische Operabilität • Bei R1/R2-Resektion sollte eine Nachresektion mit dem Ziel R0 erfolgen, ist das nicht möglich wird eine Strahlentherapie empfohlen Das Lungenkarzinom 4. Therapie 4.2 Operative Therapie Operation des Primärtumors Limitierte Resektion Indikation: kleinere peripher lokalisierte Tumoren (< 2 cm) Segmentresektion: Entfernung eines Lungensegmentes Atypische Resektion (Keilresektion): Entfernung des Tumors Nur in Ausnahmefällen (z. B. Kontraindikation gegen Lobektomie) im Stadium I empfohlen Wirken sich positiv auf die postoperative Lungenfunktion aus, allerdings erhöhtes Rezidivrisiko Lobektomie Indikation: Tumorwachstum überschreitet nicht die Lungenlappengrenze Entfernung eines Lungenlappens Das Lungenkarzinom 4. Therapie 4.2 Operative Therapie Bilobektomie Indikation: rechter Lungenflügel, lappenüberschreitendes Wachstum Betrifft nur den rechten Lungenflügel, da dieser 3 Lappen hat Man unterscheidet die obere Bilobektomie (Ober- und Mittellappen) und die untere Bilobektomie (Mittel- und Unterlappen) Pneumektomie In seltenen Fällen ist die Entfernung eines Lungenflügels erforderlich (z.B. bei zentral gelegenem Tumor, mehreren Primärtumoren) Manschettenresektion alternativ zur Pneumektomie hier bei wird nur der befallene Lungenlappen sowie die Bronchus- oder Trachealmanschette entfernt Vorteile: höherer Erhalt von Lungenparenchym, somit auch bei lungenfunktionell leicht eingeschränkten Pat. möglich Das Lungenkarzinom 4. Therapie 4.2 Operative Therapie Operation der regionären Lymphknoten Systematische Lymphknotendissektion Komplette Entfernung der regionären Lymphknoten in den Lymphknotenstationen Ist als Standard empfohlen Systematisches Lymphknotensampling Entfernung einzelner Lymphknoten aus den Lymphknotenstationen Punktuelles Lymphknotensampling Entfernung einzelner auffälliger Lymphknoten Das Lungenkarzinom 4. Therapie 4.3 Chemotherapie - NSCLC Chemotherapie bei nicht kleinzelligem Karzinom Präoperative (neoadjuvante) Chemotherapie bei Pancoast-Tumoren (Tumor der Lungenspitze mit Invasion der Umgebung, T3 oder T4) Standard mit simultaner Radiotherapie bei operablen Lungenkarzinomen im Stadium IIIA in Betracht zu ziehen Postoperative (adjuvante Chemotherapie) Ab Stadium II, bei pN0 individuelle Entscheidung, ab pN1 Standard Palliative Chemotherapie Im Stadium IV Das Lungenkarzinom 4. Therapie 4.3 Chemotherapie - NSCLC Protokolle/Zytostatika Standard sind platinhaltige Kombinationsprotokolle mit 2 Zytotastika 1. Adjuvante Chemotherapie Standardprotokoll: Cisplatin und Vinorelbin Cisplatin ist stark nephro- und ototoxisch, im Vorfeld sind Nierenfunktion und Hörvermögen zu prüfen Alternativ kann Cisplatin durch Carboplatin ersetzt werden Im adjuvanten Einsatz werden insgesamt 4 Zyklen im Abstand von 28 Tagen durchgeführt Zytostatikum Dosis Tage im Zyklus Cisplatin 80 mg/m² oder 50 mg/m² Tag 1 Tag 1, 8 Vinorelbin 25-30 mg/m² Tag 1, 8, 15, 22 Das Lungenkarzinom 4. Therapie 4.3 Chemotherapie - NSCLC 2. Palliative Chemotherapie Im palliativem Setting sind 4-6 Zyklen üblich (1st line Therapie) Standardprotokoll (Beispiele): − Plattenepithelkarzinom: Cisplatin (Carboplatin)/Vinorelbin − Nicht-Plattenepithelkarzinom: Immunchemotherapie (Bevacizumab z. B. mit Carboplatin/Paclitaxel), Cisplatin/Pemetrexed Nach Abschluss der 1st line Therapie erfolgt bei entsprechender Remission Therapiepause oder Erhaltungstherapie Bei Tumorprogress 2nd line-Therapie mit anderem Chemoprotokoll oder Targettherapie Das Lungenkarzinom 4. Therapie 4.3 Chemotherapie - SCLC Chemotherapie beim kleinzelligen Bronchialkarzinom Präoperative (neoadjuvante) Chemotherapie • Diskutabel im operablen Stadium VLD Postoperative (adjuvante Chemotherapie) • Nach operativer Therapie Standard Palliative Chemotherapie • Wenn keine OP erfolgt Das Lungenkarzinom 4. Therapie 4.3 Chemotherapie - SCLC Protokolle/Zytostatika Adjuvante Chemotherapie Standardprotokoll ist Cisplatin (Carboplatin) und Etoposid über 4 Zyklen 2. Palliative Chemotherapie Standardprotokoll in der 1st line Therapie ist Cisplatin (Carboplatin) und Etoposid mit 4 - 6 Zyklen im Abstand von 21 Tagen SCLC sprechen oft nur zeitweise auf die Chemotherapie an und sind rasch progredient Bei Tumorprogress 2nd line-Therapie z. B. mit Topotecan Zytostatikum Dosis Tage im Zyklus Cisplatin 80 mg/m² Tag 1 Etoposid 120 mg/m² Tag 1 - 3 Das Lungenkarzinom 4. Therapie 4.4. Radiotherapie - NSCLC Radiotherapie beim nichtkleinzelligen Lungenkarzinom Postoperative (Adjuvante) Radiotherapie Nach R1/R2-Resektion Bei Kontraindikation gegen Chemotherapie Mediastinale Bestrahlung nach neoadjuvanter Chemotherapie Radiotherapie unabhängig von OP Bei kleinen peripheren Tumoren als Alternative zur OP (Radiochirurgie) Bei Kontraindikation gegen Chemotherapie Bei Fernmetastasen (z. B. symptomatische Knochenmetastasen) Bestrahlung bei akuter Symptomatik (z. B. massive Hämoptysen, obere Einflussstauung) Das Lungenkarzinom 4. Therapie 4.4 Radiotherapie - SCLC Radiotherapie beim kleinzelligen Lungenkarzinom Postoperative (adjuvante) Radiotherapie Nach erfolgter OP bei pN1 diskutabel, bei pN2 empfohlen Radiotherapie unabhängig von OP Bei Kontraindikation gegen Chemotherapie Bei Fernmetastasen (z. B. symptomatische Knochenmetastasen) Bestrahlung bei akuter Symptomatik (z. B. massive Hämoptysen, obere Einflussstauung) Das Lungenkarzinom 4. Therapie 4.4 Radiotherapie - SCLC Prophylaktische Ganzhirnbestrahlung Beim SCLC treten signifikant häufig Hirnmetastasen auf (Risiko bei Langzeitüberleben > 2 Jahre 50-80%) empfohlen in allen Stadien (im Stadium ED nur bei ausreichender Remission nach Chemotherapie) Senkung des Metastasierungsrisikos auf ca. 5 % Das Lungenkarzinom 4. Therapie 4.5 Radiochemotherapie - NSCLC Kombinierte Radiochemotherapie beim NSCLC Bei technischer/funktioneller Inoperabilität in jedem Stadium als definitive Therapie (Primärtherapie) Im Stadium IIIA als Alternative zur OP Im Stadium IIIB als Standardtherapie Neoadjuvant bei Pancoasttumoren Procedere Therapie erfolgt simultan oder sequentiell Chemotherapie erfolgt in geringerer Dosierung (ggü, alleiniger Chemo) Häufig Schemata wie Cisplatin/Vinorelbin, Carboplatin/Paclitaxel, jedoch kein Standard festgelegt Das Lungenkarzinom 4. Therapie 4.5 Radiochemotherapie - SCLC Kombinierte Radiochemotherapie beim SCLC Standardtherapie in nicht operablen Stadien bei fehlender Fernmetastasierung Procedere Therapie erfolgt simultan oder sequentiell Chemotherapie erfolgt in geringerer Dosierung (ggü. alleiniger Chemo) Protokoll: Cisplatin/Etoposid Das Lungenkarzinom 4. Therapie 4.6 Targettherapie (nur NSCLC) EGF-Hemmer: Erlotinib, Geftinib, Afatinib (2. Generation) EGF Rezeptor-Tyrosinkinase, Wachstumsfaktor fördert bei aktivierender Mutation das Tumorwachstum Therapie Blockieren den EGF-Rezeptor molekularpathologische Analyse (Adenokarzinom) auf EGFR-Mutation erforderlich Diese liegt bei ca. 10 % der Adenokarzinome vor Alternative Option zur Chemotherapie im fortgeschrittenem Stadium in der Erstlinientherapie beim Nicht-Plattenepithelkarzinom Das Lungenkarzinom 4. Therapie 4.6 Targettherapie (nur NSCLC) Geringeres Nebenwirkungsprofil im Vergleich mit Chemotherapie Höhere Ansprechraten, bessere Symptomkontrolle, längeres progressionsfreies Überleben (PFS) gegenüber Chemotherapie Afatinib/Erlotinib ist mittlerweile auch beim Plattenepithelkarzinom zugelassen (diese weisen keine EGFR-Mutation auf) und in der zweiten Therapielinie (2nd line) eine gute Option (Afatinib besser als Erlotinib) Orale Einnahme (Kapsel) Nach ca. 9-13 Monaten Therapie kommt es zu einer Resistenz des Tumors, d. h. die Medikamente wirken nicht mehr EGFR-Hemmer der 3. Generation befinden sich aktuell in Studien und könnten nach einer Resistenzbildung eingesetzt werden Das Lungenkarzinom 4. Therapie 4.6 Targettherapie (nur NSCLC) ALK-Hemmer und ROS-1-Hemmer: Crizotinib, Ceritinib ALK Rezeptor-Tyrosinkinase mit weitgehend unbekannter Funktion fördert das Tumorwachstum, wenn eine dauerhafte Aktivierung durch Fusion mit einem anderen Gen, z. B. EML4 stattfindet Translokation liegt bei ca. 3-4 % der Adenokarzinome vor ROS-1 Rezeptor-Tyrosinkinase, welche für Zellwachstum und Zelldifferenzierung mitverantwortlich ist Wird wie bei ALK durch Fusion mit anderem Gen daueraktiviert Nachweis in ca. 1-2 % aller Adenokarzinome Das Lungenkarzinom 4. Therapie 4.6 Targettherapie (nur NSCLC) Therapie Blockiert den ALK- und ROS-Rezeptor Vor Therapieeinsatz FISH-Analyse auf EML4-ALK-Translokation und ROS-1-Translokation erforderlich Option in der Erst- /Zweitlinie im fortgeschrittenem Stadium beim NichtPEC mit besserer Ansprechrate und längerem PFS gegenüber Chemo Orale Einnahme (Kapsel) Auch unter Crizotinib nach 11 (1st line) bzw. 8 (2nd line) Monaten Resistenzbildung seit Mai 2015 steht Ceritinib (nur bei ALK+) als Zweitpräparat nach der Resistenzentwicklung zur Verfügung Das Lungenkarzinom 4. Therapie 4.6 Targettherapie/Immuntherapie (nur NSCLC) VEGF-Hemmer: Bevacizumab (monokonaler Antikörper) Nintendanib (Tyrosinkinaseinhibitor) VEGF Vom Tumor exprimierter Gefässwachstumsfaktor, der Ausbildung/Wachstum von Blutgefässen (Angiogenese) stimuliert Therapie binden an VEGF, somit wird die Aus-/Neubildung von den Tumor versorgenden Blutgefässen unterbunden Bevacizumab (intravenös): Einsatz beim Nicht-Plattenepithelkarzinom in Kombination mit Chemotherapie (z. B. Paclitaxel/Carboplatin) in der Erstlinientherapie Nintedanib (oral): Nicht-PEC in Kombination mit Zytostatikum Docetaxel Keine molekularpathologische Analyse erforderlich Das Lungenkarzinom 4. Therapie 4.6 Targettherapie/Immuntherapie (nur NSCLC) PD-L1-Hemmer: Nivolumab (Monoklonaler Antikörper) PD-L1 («Programmed death-ligand») Protein, welches eine wichtige Rolle bei der Immunsuppression spielt Wird natürlicherweise z. B. in der Schwangerschaft überexprimiert Wird von einigen malignen Tumoren exprimiert und scheint der Hauptmechanismus zur Vermeidung einer Entdeckung durch unser Immunsystem zu sein PD-L1 bindet an die Rezeptoren von Immunzellen (z. B. T-Zellen), dadurch wird die Immunantwort unterdrückt Das Lungenkarzinom 4. Therapie 4.6 Immuntherapie (nur NSCLC) Therapie Bindet an PD-L1-Rezeptor auf Immunzellen Dadurch kann das vom Tumor exprimierte PD-L1 nicht mehr an den Rezeptor binden, der Tumor kann vom Immunsystem erkannt und bekämpft werden Zulassungsstudie Nivolumab gegen Docetaxel musste wegen der deutlichen Überlegenheit beim Gesamtüberleben von Nivolumab vorzeitig abgebrochen werden und erhielt eine beschleunigte Zulassung Einsatz beim NSCLC (inkl. Plattenepithelkarzinom) in der Zweitlinientherapie Keine molekularpathologische Analyse erforderlich Orale Einnahme Das Lungenkarzinom 4. Therapie 4.7 Erhaltungstherapie (nur NSCLC) Zeigt der Tumor nach Abschluss der palliativen Erstlinientherapie ein gutes Ansprechen (Remission) und eine gute Verträglichkeit kann zur Hinauszögerung eines Rezidivs eine Erhaltungstherapie erfolgen Man unterscheidet «Continuous Maintenance» Verwendung eines in der Erstlinientherapie eingesetzten Medikamente Pemetrexed nach Chemotherapie Cisplatin/Pemetrexed Bevacizumab nach Immunchemotherapie mit Bevacizumab «Switch Maintenance» Einsatz einer neuen Substanz nach Chemotherapie Genaugenommen «frühe» Zweitlinientherapie Zugelassen ist hierfür Erlotinib Das Lungenkarzinom 4. Therapie 4.8 Zukünftige Entwicklung - NSCLC Nichtkleinzelliges Bronchialkarzinom Weitere Marker (z. B. KRAS, BRAF-V600E, MET, RET) könnten in der Diagnostik zum Standard werden, aktuell laufen einige Therapiestudien bei entsprechend mutierten Lungenkarzinomen Bei PD-L1 mutierten NSCLC sind einige weitere monoklonale Antikörper in der klinischen Erprobung 2 weitere monoklonale Antikörper zur EGFR- bzw. VEGF-Hemmung befinden sich in klinischen Studien Gehört die Therapiezukunft beim NSCLC der Immuntherapie? Das Lungenkarzinom 4. Therapie 4.8 Zukünftige Entwicklung - SCLC Kleinzelliges Bronchialkarzinom Hier sind eher wenige Fortschritte zu erwarten Neue Chemotherapie: PM01183 in Kombination mit Doxorubicin Nedaplatin: Nachfolger von Cisplatin mit geringerem Toxizitätsprofil Studien mit monoklonalen Antikörpern (z. B. Pembrolizumab, Nivolumab) laufen 2 grosse Arbeitsgruppen untersuchen mögliche neue genetische Marker, z. B. TP53 Quellen 1. Einführung 1.1 Epidemiologie (weltweit, europaweit, Min/Max, Schweiz) Daten Welt: Daten/Grafiken Welt : http://globocan.iarc.fr/Pages/fact_sheets_population.aspx Daten Schweiz: Krebsliga Schweiz (2008-2012, Stand 10/15) von www.krebsliga.ch/de/uber_krebs/zahlen_zu_krebs2/ (28.01.15) Grafik Europa: 3. Lung Cancer in the EU Infographic 9.21.15 GERMAN for Switzerland.pdf von www.thenextlungcanceract.bmsconnect.ch (28.01.16) 1.2 Risikofaktoren http://www.krebsgesellschaft.de/onko-internetportal/basis-informationenkrebs/krebsarten/definition/ursachen-und-risikofaktoren.html (28.01.16) Grafik Raucherquote: datewrapper, Daten: OECD via statista 1.3 Aufbau der Lunge Grafik Lunge: lung medical vector eps10 illustration © bilderzwerg - Fotolia.com Grafik Lungenbläschen: www.lungeninformationsdienst.de/praevention/grundlagen-atmung/aufbau-lunge/index.html (29.02.16) Grafik Brusthöhle/Pleura): https://commons.wikimedia.org/wiki/File:2313_The_Lung_Pleurea.jpg#/media/File:2313_The_Lung_Pleurea.jpg 1.4 Topographie (ICD-10/ICD-O) ICD-10-GM-2016 ICD-O—Topographie Grafik: Kodierhilfe Krebsregister CCC Freiburg von www.uniklinikfreiburg.de/fileadmin/mediapool/09_zentren/cccf/pdf/cccf_kkr_kodierhilfe_lungenkrebs.pdf (02.03.16) 1.5 histologische Einteilung https://eliph.klinikum.uni-heidelberg.de/texte_s/651/bronchialkarzinom (28.01.16) Quellen 2. Klassifikation 2.1 TNM, AJCC www.onkologie2016.de/solidetumoren/atemwege/lunge_klassifikation.htm (29.01.16) Grafiken Lymphknoten: http://www.ajronline.org/doi/pdfplus/10.2214/AJR.11.7446 (10.03.16) http://www.radiologyassistant.nl/en/p4646f1278c26f/mediastinum-lymph-node-map.html (11.03.16) 2.2 Klassifikation SCLC https://www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-kleinzellig-sclc/@@view/html/index.html#ID0ENVAE (02.03.16) 3. Diagnostik 3.1 Symptome S3-Leitlinie Lungenkarzinom (www.awmf.org/uploads/tx_szleitlinien/020007l_S3_Praevention_Diagnostik_Therapie_Nachsorge_Lungenkarzinoms_2010-abgelaufen.pdf 01.02.16) 3.2 Diagnostik S3-Leitlinie Lungenkarzinom (www.awmf.org/uploads/tx_szleitlinien/020007l_S3_Praevention_Diagnostik_Therapie_Nachsorge_Lungenkarzinoms_2010-abgelaufen.pdf 01.02.16) https://www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@view/html/index.html (02.03.16) https://www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-kleinzellig-sclc/@@view/html/index.html (02.03.16) Quellen 4. Therapie 4.1 Stadienabhängige Therapie (Überblick) www.onkologie2016.de/solidetumoren/atemwege/nsclc_therapie.htm (02.02.16) www.onkologie2016.de/solidetumoren/atemwege/sclc_therapie_stadien.htm (02.02.16) 4.2 Operative Therapie S3-Leitlinie Lungenkarzinom (www.awmf.org/uploads/tx_szleitlinien/020007l_S3_Praevention_Diagnostik_Therapie_Nachsorge_Lungenkarzinoms_2010-abgelaufen.pdf 01.02.16) www.onkologie2016.de/solidetumoren/atemwege/nsclc_therapie.htm (02.02.16) Chirurgie für Pflegeberufe, 2.. Auflage, Georg-Thieme Verlag, 2013 „Die operative Therapie beim Lungenkarzinom“ von www.rosenfluh.ch/media/onkologie/2006/02/Die-operative-Therapie-beimBronchialkarzinom.pdf (04.02.16) www.bronchialkarzinom-aktuell.de/index.php?id=135 (04.02.16) www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc (04.02.16) 4.3 Chemotherapie (Adjuvant, palliativ) www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc (04.02.16) www.onkologie2016.de/solidetumoren/atemwege/nsclc_therapie.htm (02.02.16) http://www.onkologie2016.de/solidetumoren/atemwege/sclc_therapie.htm (02.02.16) 4.4. Radiotherapie NSCLC/SCLC www.onkologie2016.de/solidetumoren/atemwege/nsclc_therapie.htm (02.02.16) www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc (04.02.16) S3-Leitlinie Lungenkarzinom (www.awmf.org/uploads/tx_szleitlinien/020007l_S3_Praevention_Diagnostik_Therapie_Nachsorge_Lungenkarzinoms_2010-abgelaufen.pdf 01.02.16) 4.5 Radiochemotherapie NSCLC/SCLC www.onkologie2016.de/solidetumoren/atemwege/nsclc_therapie.htm (02.02.16) www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc (04.02.16) S3-Leitlinie Lungenkarzinom (www.awmf.org/uploads/tx_szleitlinien/020007l_S3_Praevention_Diagnostik_Therapie_Nachsorge_Lungenkarzinoms_2010-abgelaufen.pdf 01.02.16) Quellen 4.6 Targettherapie www.lungenkrebs-testen.de (05.02.16) https://de.wikipedia.org/wiki/Crizotinib )05.02.16) www.onkologie2016.de/solidetumoren/atemwege/nsclc_therapie.htm (02.02.16) www.rosenfluh.ch/media/onkologie/2015/04/Aktuelle-Therapiekonzepte-beim-fortgeschrittenen-NSCLC.pdf (05.02.16) https://en.wikipedia.org/wiki/PD-L1_Inhibitor (02.03.16) https://en.wikipedia.org/wiki/ROS1 (02.03.16) State of the Art und Trends in der Molekulardiagnostik, 05/2013 von www.medicalforum.ch (01.03.16) https://www.rosenfluh.ch/media/onkologie/2015/04/Die-molekulare-Diagnostik-des-Lungenkarzinoms.pdf (02.03.16) State-of-the-Art-Gespräch 2015 – Lungenkarzinom, Video von www.krebsgesellschaft.de/onko-internetportal/basis-informationenkrebs/krebsarten/lungenkrebs.html#expertendiskussion (01.03.16) Expertenrunde Lungenkarzinom- ASCO Annual Meeting 2015, , Video von www.krebsgesellschaft.de/onko-internetportal/basisinformationen-krebs/krebsarten/lungenkrebs.html#expertendiskussion (01.03.16) 4.7 Erhaltungstherapie http://www.trillium.de/zeitschriften/trillium-krebsmedizin/2014/heft-12014/systemische-therapie-des-nsclc-ohne-nachgewiesenetreibermutation/html-version.html (02.03.16) 4.8 Zukünftige Entwicklung State-of-the-Art-Gespräch 2015 – Lungenkarzinom, Video von www.krebsgesellschaft.de/onko-internetportal/basis-informationenkrebs/krebsarten/lungenkrebs.html#expertendiskussion (01.03.16) Expertenrunde Lungenkarzinom- ASCO Annual Meeting 2015, , Video von www.krebsgesellschaft.de/onko-internetportal/basisinformationen-krebs/krebsarten/lungenkrebs.html#expertendiskussion (01.03.16)