Wie Axone ihren Weg finden
Werbung

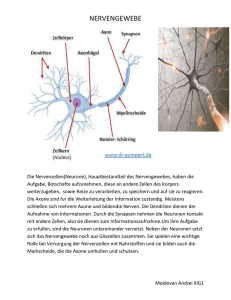
Powered by Seiten-Adresse: https://www.gesundheitsindustriebw.de/de/fachbeitrag/aktuell/wie-axone-ihren-weg-finden/ Wie Axone ihren Weg finden Der visuelle Teil der Welt hat eine räumliche Struktur, die sich im Gehirn widerspiegelt. Eine neuronale Karte im visuellen Zentrum bildet die räumlichen Verhältnisse zwischen verschiedenen Punkten im visuellen Feld ab. Wie kommt es dazu, dass sich Nervenzellverbindungen während der Entwicklung korrekt anordnen und ein neuronales Pendant der Umwelt aufbauen? Die Arbeitsgruppe von Prof. Dr. Martin Bastmeyer vom Zoologischen Institut am KIT (Karlsruhe Institute of Technology) untersucht, wie ein komplexes Netz aus molekularen Landmarken die auswachsenden Zellfortsätze der Netzhaut zum richtigen Punkt auf der Karte im visuellen Zentrum leitet. Ihr Modellorganismus ist das Hühnchen. In Zellkulturen und Computermodellen simulieren sie diese Vorgänge im Gehirngewebe. Dass wir überhaupt etwas wahrnehmen können, verdanken wir einer komplexen Architektur von verschalteten Nervenzellen in unserem Gehirn. Dieser Architektur liegt eine überraschende Ordnung zugrunde. Die visuelle Umgebung etwa wird topographisch abgebildet. Das bedeutet, dass Lichtreize, die zwei benachbarte Sinneszellen in der Retina stimulieren, räumlich korrekt ins Gehirn weiter vermittelt werden: Die Information kommt in nebeneinander liegenden Bereichen im Sehzentrum des Gehirns an. Wissenschaftler bezeichnen diese Abbildung der Information von den Zellen in der Retina ins Gehirn auch als eine neuronale „Karte“. Wie aber kommt diese Karte zustande? Woher wissen die Nervenzellen im sich entwickelnden Auge, wo ihre Zielgebiete im Gehirn liegen? „Eine allgemein anerkannte Hypothese ist, dass es sowohl auf der Oberfläche der wachsenden Nervenzellfortsätze als auch auf derjenigen der Zellen im Zielgebiet komplexe Verteilungen von Molekülen gibt, die wie Schlüssel und Schloss zusammen passen“, sagt Prof. Dr. Martin Bastmeyer vom Zoologischen Institut I des KIT. „Die Interaktionen zwischen diesen Molekülen bestimmen, wohin die Axone aus der Retina wachsen.“ Wachstum und Abstoßung Die experimentellen Grundlagen für diese Hypothese wurden in den 90er Jahren gelegt. Bastmeyer war damals Mitarbeiter am Max-Planck-Institut für Entwicklungsbiologie in Tübingen. Hier hat Prof. Dr. Friedrich Bonhoeffer wegweisende Untersuchungen zur Lenkung retinaler Nervenfortsätze durchgeführt; in seinem Labor wurden unter anderem die Ephrine als axonale Lenkungsmoleküle entdeckt. Ephrine sind Moleküle, die auf der Oberfläche von Nervenzellen angeordnet sind. Sie können an spezielle Rezeptoren binden, die auf anderen 1 Wird Ephrin (blau) in einer gradierten Verteilung auf eine Oberfläche gedruckt, wachsen Axone aus der Retina in diesen Gradienten ein und stoppen an einer definierten Stelle. © Dr. Martin Bastmeyer Neuronen (zum Beispiel an der Spitze von Axonen) zu finden sind. Findet ein Schlüssel ins Schloss, dann treten im Inneren eines wachsenden Axons molekulare Vorgänge in Kraft, die entweder sein Wachstum anregen oder eher bremsen. Eine stark vereinfachte Vorstellung des Vorgangs könnte also so aussehen: Ein Axon aus der Retina mit einer hohen Konzentration von Ephrin-Rezeptoren auf seiner Oberfläche wächst ins Gehirn ein und findet das Zielgebiet. Hier sind hemmende Ephrine in einer gradierten Verteilung auf Nervenzellen angeordnet. Weil das Axon so viele Rezeptoren hat und damit sehr sensibel ist, wird es von Zellen abgestoßen, die eine hohe Konzentration von Ephrinen tragen. Zu Zellen mit einer geringen Konzentration an abstoßenden Ephrinen hingegen wird es Kontakte ausbilden. Dieses Modell ist stark vereinfacht. In den Neuronen im Gehirn gibt es nicht nur einen Ephrintyp sondern mehrere verschiedene. Außerdem besitzen die Axone und die Zielzellen sowohl Ephrine als auch Ephrin-Rezeptoren auf ihrer Oberfläche. Und schließlich können Ephrine auch selbst als Rezeptoren fungieren, was die Komplexität nochmals steigert. Aber das Modell verdeutlicht auch eine wichtige Grundidee: „Wir nehmen an, dass für die Zielfindung von Axonen gradierte Verteilungen von Ephrinen und ihren Rezeptoren notwendig sind“, sagt Bastmeyer. Die Konzentrationen der Moleküle variieren räumlich sehr stark, sowohl in der Retina als auch im visuellen Zentrum des Gehirns. Diese räumlichen Variationen in den zwei Gebieten müssen auf irgendeine Weise korrespondieren. Während der Entwicklung findet eine Verrechnung der verschiedenen Gradienten statt, sodass schließlich die richtigen Zellen zueinander finden. Wie diese Verrechnung funktioniert, untersucht die Arbeitsgruppe Bastmeyer mithilfe von zwei sich ergänzenden Ansätzen. 2 Molekulare Muster in vitro und in silico Im einfachen Streifenassay vermeiden Axone aus der Retina hohe Konzentrationen an Ephrin (rot). © Prof. Dr. Martin Bastmeyer „In Gewebekulturen zerlegen wir das komplexe System in überschaubare Teilsysteme“, erklärt Bastmeyer. Die Karlsruher Forscher schaffen in ihren Petrischalen mithilfe verschiedener Techniken eine molekulare Umgebung, in der genau definierte und stark vereinfachte Verteilungen von Ephrinen angeordnet sind (zum Beispiel Streifenmuster aus Ephrinen oder lineare Gradienten aus Ephrinen und Ephrinrezeptoren). In diese Umgebung setzen sie wachsende Nervenzellen aus der Retina des Hühnchens aus und verfolgen ihr Wachstumsverhalten. Parallel dazu entwickeln sie Computermodelle, die die Vorgänge in der Zellkulturschale nachstellen. Das Modell-Axon statten sie mit verschiedenen Kombinationen aus Ephrinen und Rezeptoren aus. Sie konfrontieren es mit einem Muster aus Ephrinen in einer simulierten Umgebung. Experimente in echten Zellkulturen und im Computer ergänzen und befruchten sich gegenseitig. Denn Erkenntnisse aus simulierten Tests können zu theoretischen Vorhersagen über das Verhalten von echten Nervenzellen führen. Diese Vorhersagen können in vitro überprüft werden. Umgekehrt können Erkenntnisse in der Zellkultur dazu dienen, die Parameter im Computermodell anzupassen. Neben der Frage nach der korrekten Zielfindung von Axonen aus der Retina untersuchen Bastmeyer und sein Team auch die axonale Zielfindung im olfaktorischen System des Zebrafischs. Außerdem interessieren sie sich für Themengebiete wie die Neurogenetik der Maus oder die neuronale Entwicklung des Zebrafisches. „Wir sind hier in Karlsruhe in einer sehr fruchtbaren interdisziplinären Umgebung angesiedelt“, sagt der Biologe. Die Forscher sind zum Beispiel im Exzellenzcluster „Zentrum für funktionelle Nanostrukturen (CFN)“ mit Polymerchemikern, Physikern und anderen Biologen organisiert. Von dem Know-how und den Erfahrungen ihrer Kollegen profitieren sie etwa bei der Entwicklung von dreidimensionalen Wachstumsstrukturen für die Zellkultur. Und ihr eigenes Know-how stellen sie wiederum der Gemeinschaft zur Verfügung. „Gute Forschung funktioniert oft besser in der Zusammenarbeit mit anderen Disziplinen“, sagt Bastmeyer. 3 Fachbeitrag 29.11.2010 mn BioRegion Freiburg © BIOPRO Baden-Württemberg GmbH Weitere Informationen Prof. Dr. Martin Bastmeyer Karlsruher Institut für Technologie (KIT) Zoologisches Institut Abteilung für Zell- und Neurobiologie Haid-und-Neu-Straße 9 (MRI) D-76131 Karlsruhe Tel.: +49 (0) 721/ 608-30 85 (direct) +49 (0) 721/ 608-22 18 (Secretary) +49 (0) 721/ 608-48 48 (Fax) E-Mail: bastmeyer(at)kit.edu KIT, Zoologisches Institut 4