Aktuell - BIOspektrum
Werbung
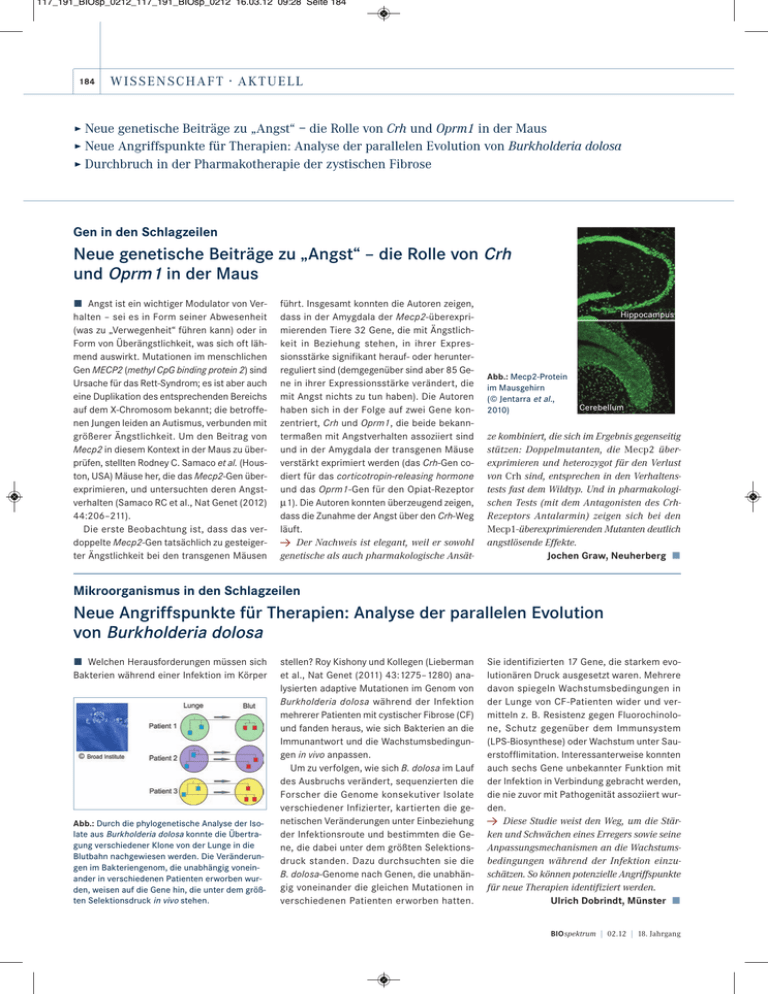
117_191_BIOsp_0212_117_191_BIOsp_0212 16.03.12 09:28 Seite 184 184 W I S S E N SCH AFT · AKTU E LL ÿ Neue genetische Beiträge zu „Angst“ – die Rolle von Crh und Oprm1 in der Maus ÿ Neue Angriffspunkte für Therapien: Analyse der parallelen Evolution von Burkholderia dolosa ÿ Durchbruch in der Pharmakotherapie der zystischen Fibrose Gen in den Schlagzeilen Neue genetische Beiträge zu „Angst“ – die Rolle von Crh und Oprm1 in der Maus ó Angst ist ein wichtiger Modulator von Verhalten – sei es in Form seiner Abwesenheit (was zu „Verwegenheit“ führen kann) oder in Form von Überängstlichkeit, was sich oft lähmend auswirkt. Mutationen im menschlichen Gen MECP2 (methyl CpG binding protein 2) sind Ursache für das Rett-Syndrom; es ist aber auch eine Duplikation des entsprechenden Bereichs auf dem X-Chromosom bekannt; die betroffenen Jungen leiden an Autismus, verbunden mit größerer Ängstlichkeit. Um den Beitrag von Mecp2 in diesem Kontext in der Maus zu überprüfen, stellten Rodney C. Samaco et al. (Houston, USA) Mäuse her, die das Mecp2-Gen überexprimieren, und untersuchten deren Angstverhalten (Samaco RC et al., Nat Genet (2012) 44:206–211). Die erste Beobachtung ist, dass das verdoppelte Mecp2-Gen tatsächlich zu gesteigerter Ängstlichkeit bei den transgenen Mäusen führt. Insgesamt konnten die Autoren zeigen, dass in der Amygdala der Mecp2-überexprimierenden Tiere 32 Gene, die mit Ängstlichkeit in Beziehung stehen, in ihrer Expressionsstärke signifikant herauf- oder herunterreguliert sind (demgegenüber sind aber 85 Gene in ihrer Expressionsstärke verändert, die mit Angst nichts zu tun haben). Die Autoren haben sich in der Folge auf zwei Gene konzentriert, Crh und Oprm1, die beide bekanntermaßen mit Angstverhalten assoziiert sind und in der Amygdala der transgenen Mäuse verstärkt exprimiert werden (das Crh-Gen codiert für das corticotropin-releasing hormone und das Oprm1-Gen für den Opiat-Rezeptor μ1). Die Autoren konnten überzeugend zeigen, dass die Zunahme der Angst über den Crh-Weg läuft. Y Der Nachweis ist elegant, weil er sowohl genetische als auch pharmakologische Ansät- Hippocampus Abb.: Mecp2-Protein im Mausgehirn (© Jentarra et al., 2010) Cerebellum ze kombiniert, die sich im Ergebnis gegenseitig stützen: Doppelmutanten, die Mecp2 über exprimieren und heterozygot für den Verlust von Crh sind, entsprechen in den Verhaltenstests fast dem Wildtyp. Und in pharmakologischen Tests (mit dem Antagonisten des CrhRezeptors Antalarmin) zeigen sich bei den Mecp1-überexprimierenden Mutanten deutlich angstlösende Effekte. Jochen Graw, Neuherberg ó Mikroorganismus in den Schlagzeilen Neue Angriffspunkte für Therapien: Analyse der parallelen Evolution von Burkholderia dolosa ó Welchen Herausforderungen müssen sich Bakterien während einer Infektion im Körper Abb.: Durch die phylogenetische Analyse der Isolate aus Burkholderia dolosa konnte die Übertragung verschiedener Klone von der Lunge in die Blutbahn nachgewiesen werden. Die Veränderungen im Bakteriengenom, die unabhängig voneinander in verschiedenen Patienten erworben wurden, weisen auf die Gene hin, die unter dem größten Selektionsdruck in vivo stehen. stellen? Roy Kishony und Kollegen (Lieberman et al., Nat Genet (2011) 43:1275–1280) analysierten adaptive Mutationen im Genom von Burkholderia dolosa während der Infektion mehrerer Patienten mit cystischer Fibrose (CF) und fanden heraus, wie sich Bakterien an die Immunantwort und die Wachstumsbedingungen in vivo anpassen. Um zu verfolgen, wie sich B. dolosa im Lauf des Ausbruchs verändert, sequenzierten die Forscher die Genome konsekutiver Isolate verschiedener Infizierter, kartierten die genetischen Veränderungen unter Einbeziehung der Infektionsroute und bestimmten die Gene, die dabei unter dem größten Selektionsdruck standen. Dazu durchsuchten sie die B. dolosa-Genome nach Genen, die unabhängig voneinander die gleichen Mutationen in verschiedenen Patienten erworben hatten. Sie identifizierten 17 Gene, die starkem evolutionären Druck ausgesetzt waren. Mehrere davon spiegeln Wachstumsbedingungen in der Lunge von CF-Patienten wider und vermitteln z. B. Resistenz gegen Fluorochinolone, Schutz gegenüber dem Immunsystem (LPS-Biosynthese) oder Wachstum unter Sauerstofflimitation. Interessanterweise konnten auch sechs Gene unbekannter Funktion mit der Infektion in Verbindung gebracht werden, die nie zuvor mit Pathogenität assoziiert wurden. Y Diese Studie weist den Weg, um die Stärken und Schwächen eines Erregers sowie seine Anpassungsmechanismen an die Wachstumsbedingungen während der Infektion einzuschätzen. So können potenzielle Angriffspunkte für neue Therapien identifiziert werden. Ulrich Dobrindt, Münster ó BIOspektrum | 02.12 | 18. Jahrgang 117_191_BIOsp_0212_117_191_BIOsp_0212 16.03.12 09:28 Seite 185 185 Arzneimittel in den Schlagzeilen Durchbruch in der Pharmakotherapie der zystischen Fibrose Cystic Fibrosis Foundation in den USA. Y Die Therapie mit Ivacaftor (Handelsname Kalydeco®) hat ihren Preis: In den USA kostet die Behandlung eines Patienten 294.000 Dollar pro Jahr. Diese Behandlung muss lebenslang durchgeführt werden. Das mag sehr hoch erscheinen, aber man muss die jahrzehntelange Grund- Abb.: Pathophysiologie und Pharmakologie des CFTR bei zystischer Fibrose (Mukoviszidose) ó Die zystische Fibrose (CF) ist eine genetische Erkrankung, bei der ein Chloridkanal, der cystic fibrosis conductance regulator (CFTR), defekt ist. Eine Vielzahl von Mutationen führt zum CFTRDefekt. Am häufigsten ist die F508-Deletionsmutante, bei der der Transport des CFTR vom endoplasmatischen Retikulum (ER) an die Plasmamembran gestört ist. In anderen Fällen liegen Punktmutationen vor. Bei der sehr seltenen G551D-Mutante ist die Chloridleitfähigkeit des CFTR gestört. Als Folge der CFTR-Mutationen wird das Sekret in den Atemwegen zähflüssig, was dann wiederum zu bakteriellen Superinfektionen führt, vor allem mit Pseudomonas aeruginosa. Durch verbesserte antibiotische Therapie, Sekretverflüssigung und Physiotherapie wurde die Lebenserwartung von CF-Patienten deutlich erhöht, aber eine spezifische Therapie auf der CFTR-Ebene war bislang nicht möglich. Van Goor et al. (Proc Natl Acad Sci USA (2009) 106:18825– 18830) entwickelten eine neue Arzneistoffklasse, die CFTR-Potentiatoren, die die Chloridleitfähigkeit der G551D-CFTR-Mutante in vitro erhöhen. Ramsey et al. (N BIOspektrum | 02.12 | 18. Jahrgang Engl J Med (2011) 365:1663–1672) zeigten, dass der CFTR-Potentiator VX-770 (Ivacaftor) bei Patienten mit G551D-Mutation auch klinisch wirksam ist. Um die viel häufigeren Transportdefekte zu korrigieren, wurde die Klasse der CFTRKorrektoren entwickelt. Sie ermöglichen bei der F508-Deletionsmutante den Transport vom endoplasmatischen Retikulum an die Plasmamembran (Van Goor et al., Proc Natl Acad Sci USA (2011) 108:18843–18848). Die Ergebnisse von klinischen Studien mit CFTR-Korrektoren liegen noch nicht vor. Diese Untersuchungen zur CFPharmakotherapie sind ein sehr gutes Beispiel dafür, wie translationale interdisziplinäre Forschung zu Durchbrüchen in der Pharmakotherapie führen kann. Es hat ungefähr 25 Jahre von der Identifikation des CFTR-Gens bis zur Etablierung einer klinisch wirksamen Pharmakotherapie gedauert. Dieser Durchbruch wurde nur durch nachhaltige und nicht an kurzfristigen Erfolgen (deliverables, bench marks, high publication numbers, impact factors, citations) orientierte Forschungsförderung ermöglicht. Eine Schlüsselrolle spielte dabei das Engagement der lagenforschung, die gewonnenen Lebensjahre, die verbesserte Lebensqualität und verringerten Therapiekosten durch verminderte CF-Komplikationen in Betracht ziehen. Da CF die häufigste Stoffwechselerkrankung in Deutschland ist (ca. 8.000 Erkrankte), wird es sicher bald gesundheitspolitische Diskussionen geben. Roland Seifert, Hannover ó