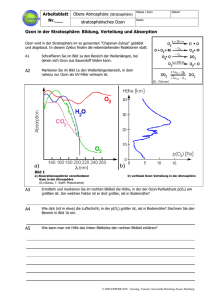
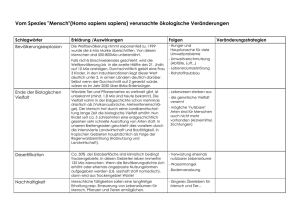
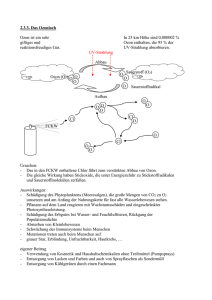
nRT nb V V an p = − + ) )( (
Werbung

_________________________ Abweichungen vom idealen Gasverhalten: van der Waals __________________________________ Der holländische Wissenschaftler J. van der Waals hat in diesem Zusammenhang eine sehr wertvolle Gleichung zur Beschreibung realer Gase vorgeschlagen. Für diese Korrektur hat er 2 Konstanten a und b eingeführt. Idealverhalten: Realverhalten: pV = nRT n2a ( p + 2 )(V − nb) = nRT V Die Konstanten a und b sind für viele Gase tabellarisch verfügbar. Korrektur der Anziehungskräfte Volumenkorrektur 171 _________________________ Die Verflüssigung von Gasen __________________________________ Bei niedrigen Temperaturen kann die Bewegung der Gasmoleküle so stark verlangsamt werden, dass die einzelnen Moleküle oder Atome die gegenseitigen Anziehungskräfte nicht mehr überwinden können ⇒ das Gas wird flüssig. Beim Joule-Thomson Effekt wird ein komprimiertes Gas durch Expansion abgekühlt. Großtechnisch wird dieses Phänomen in einem zyklischen Prozess für die Verflüssigung von Gasen eingesetzt ⇒ Linde-Verfahren 172 _________________________ Volumenarbeit eines Gases __________________________________ Eine in der Chemie besonders wichtige Arbeit ist die Expansions-/Kompressionsarbeit eines Gases. Expansion p= F A w = F∗∆h = p∗A∗∆h A∗∆h = ∆V w: Arbeit ∆h: zurückgelegter Weg ∆V: Volumenvergrösserung w = -p∗∆V Minuszeichen per Konvention: bei Expansion wird Arbeit vom System an Umgebung abgegeben (-) und bei Kompression muss Arbeit an dem System geleistet werden (+). 173 _________________________ Einige charakteristische Phänomene der Erdatmosphäre __________________________________ Höhe/T Höhe/p Das menschliche Leben spielt sich in der Troposphäre ab. Die Temperatur-Extreme zwischen den einzelnen Regionen werden mit der Endung –pause bezeichnet. Diese Grenzen sind wichtig, weil sich Gase (Verunreinigungen) nur sehr langsam über diese Grenzen mischen. Im Gegensatz zur Temperatur variiert der Druck in einer regulären Art und Weise (von 101 kPa auf Meeresniveau auf 3.1∗10-4 kPa in 100 km Höhe). In der Troposphäre und Stratosphäre befinden sich 99.9% der Masse der Atmosphäre (mit 75% in der Troposphäre). 174 _________________________ Funktion der Ozonschicht __________________________________ Hochenergetische (<240 nm) UV-Strahlung (unter der Pflanzen- und Tierwelt nicht überleben könnten) der Sonne wird von dem in der Atmosphäre vorhandenen N2 und O2 zu unserem Schutz absorbiert. Für die Absorption längerwelliger (240-310 nm) Strahlung wird aber Ozon gebraucht. Ozon bildet sich überwiegend in der Stratosphäre in Höhen von 10 – 50 km entsprechend der Reaktion O + O2 ⇒ O3 (Ozon) Dieses Ozon zerfällt als Folge der Absorption solarer Strahlung < 1140 nm wieder und hält diese Strahlung dadurch von der Erdoberfläche ab. Die Ozon-Schicht hat daher für uns eine lebenswichtige Schutzfunktion. 200nm 600nm 1000nm 175 _________________________ Abbau der Ozon-Schicht __________________________________ In 1995 wurde an F. S. Rowland, M. Molina und P. Crutzen der Nobelpreis für Studien zum Abbau der Ozon-Schicht verliehen. Rowland und Molina haben gezeigt, dass Chlorfluorkohlenwasserstoffe, insbesondere CFCl3 und CF2Cl2, die als Treibgase in Sprays und in Kühlschränken und Klimaanlagen eingesetzt werden, wenn sie in die Atmosphäre gelangen, den Ozonabbau hervorrufen. Da diese Verbindungen chemisch nicht sehr reaktiv sind (ein Hauptgrund für ihre Einsatzgebiete) und sich nicht in Wasser lösen, gelangen sie aber in die Stratosphäre und werden dort durch hochenergetische Strahlung zersetzt: CF2Cl2(g) Strahlung CF2Cl(g) + Cl(g) Dieses atomare Chlor bewirkt letztendlich die Rückspaltung von Ozon: 2O3(g) Cl(g) Cl(g) 3O2(g) und führt auf diesem Wege zum Abbau der Ozon-Schicht. Damit steht Ozon nicht mehr für die (für uns lebenswichtige) Absorption solarer Strahlung zur Verfügung. Antarktis, 2004 176 _________________________ NOx und Smog __________________________________ Smog ist ein urbanes Phänomen, wenn die Wetterbedingungen dazu führen, dass große Luftmassen stagnieren. NOx aus Kraftfahrzeugen und Kraftwerken kann im Sonnenlicht zersetzt werden: NO2(g) SonnenSonneneinstrahlung NO(g) + O(g) und dann zur Bildung von Ozon führen: O(g) + O2(g) ⇒ O3(g) Obwohl Ozon in der Stratosphäre als UV-Schild erwünscht ist, ist seine Bildung in der Troposphäre unerwünscht. Smog ist besonders gefährlich für ältere Menschen, Asthmatiker und Sportler in Aktion. Ozon ist also in 10-50 km Höhe erwünscht, aber in Höhen < 10 km unerwünscht. 177 _________________________ H2O, CO2, das Klima und der Treibhauseffekt __________________________________ Wie wir gesehen haben, ist die Atmosphäre wichtig um hochenergetische Strahlung von der Erdoberfläche abzuhalten. Sie hat aber auch eine wichtige Funktion in der Erhaltung einer gleich bleibenden und gemäßigten Temperatur auf der Erdoberfläche. Die wichtigste Rolle spielen dabei H2O und CO2. Genauso wie die Sonne Energie abstrahlt, strahlt auch die Erde (allerdings weniger energetische) Infrarot-Strahlung ab. Die in der Atmosphäre enthaltenen H2O und CO2 Moleküle absorbieren aber einen Großteil dieser Strahlung und tragen damit zu einer einheitlichen Temperatur auf der Erdoberfläche bei. Dieser Einfluss wird “Treibhauseffekt“ genannt. Wie die untenstehende Abbildung zeigt, ist es aber im Laufe der Jahre zu einer starken Anreicherung von CO2 in der Atmosphäre gekommen und Wissenschaftler nehmen an, dass diese Veränderungen zu einem Temperaturanstieg von 0.3 - 0.6°C im Laufe des letzten Jahrhunderts geführt haben. 100 ppm (part per million) = 0.01% 178 _________________________ Flüssigkeiten – einige wichtige Eigenschaften __________________________________ Viskosität: Diese Eigenschaft ist eine Folge der intermolekularen Wechselwirkungen zwischen den Flüssigkeitsmolekülen. Der Widerstand, den eine Flüssigkeit dem Fliessen entgegenbringt, wird Viskosität genannt. Die Messung erfolgt durch Zeitnahme wie lange eine Flüssigkeit benötigt, um durch eine Kapillare zu fließen oder wie lange eine Stahlkugel braucht, um unter dem Einfluss der Schwerkraft durch die Flüssigkeit zu sinken. Viskosität η = kgm-1s-1 Einheit: 1 Poise (P) = 10-1 kgm-1s-1 179 _________________________ Flüssigkeiten – einige wichtige Eigenschaften __________________________________ Die Viskosität einer Flüssigkeit nimmt mit steigender molarer Masse zu und mit steigender Temperatur ab. Die Abnahme mit steigender Temperatur beruht auf der Abschwächung der intermolekularen Wechselwirkungen in der Flüssigkeit ⇒ Beispiel: Motorenöl im Winter ! Die Viskosität eines Gases nimmt dagegen mit steigender Temperatur zu. Die steigende Temperatur führt zu höheren Geschwindigkeiten der Moleküle und damit zu einer stärkeren Wechselwirkung zwischen benachbarten Gasschichten. 180