Aus thoraxchirurgischer Sicht stehen 3 Tumorarten im Vordergrund:
Werbung

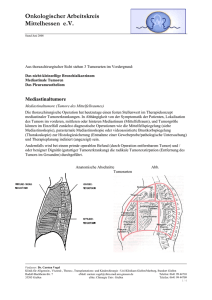
Onkologischer Arbeitskreis Mittelhessen e.V. Stand Juni 2008 Aus thoraxchirurgischer Sicht stehen 3 Tumorarten im Vordergrund: Das nicht-kleinzellige Bronchialkarzinom Mediastinale Tumoren Das Pleuramesotheliom Bronchialkarzinom Bronchialkarzinom (sog. Lungenkrebs) Das Bronchialkarzinom ist mit einer Inzidenz (Häufigkeit) von ca. 38.100 Neuerkrankungen pro Jahr der am häufigsten zum Tode führenden maligne (bösartiger) Tumor weltweit. Die Neuerkrankungsrate ist beim Mann ca. 60-70 Erkrankungen auf 100.000 Männer. Position 1 der tumorbedingten Todesfälle. Dagegen nur 7-9 Neuerkrankungen auf 100.000 Frauen. Bei der Frau der dritthäufigster Tumor (8%), hinter Malignomen der Brust und des Dickdarm (Kolon), Tendenz steigend. Männer : Frauen wie 5:1. Der Altersgipfel liegt in der 6. Lebensdekade. Es besteht kein Zweifel daran, dass das Rauchen der bedeutendste Einzelrisikofaktor für das Bronchialkarzinom ist. Unter den beruflichen Noxen (Giften) ist das Asbest anerkannt. Es werden grundsätzlich zwei Tumorzellarten unterschieden. Die größte Gruppe stellt mit 75-80% der Patienten das nicht-kleinzellige Bronchialkarzinom (NSCLC) dar. Bei ca. 20-25% der Patienten wird ein prognostisch ungünstigeres kleinzelliges Bronchialkarzinom (SCLC) diagnostiziert. Die spätere Metastasierungstendenz, die niedrigere Zellteilungsrate und die langsamere Wachstumsgeschwindigkeit unterscheidet das nicht–kleinzellige vom kleinzelligen Bronchialkarzinom. Abb.1: Großes Bronchialkarzinom im ThoraxCT Abb.2: Operationspräparat mit demselben Bronchialkarzinom (rechter Lungenoberlappen) Verfasser: Dr. Carsten Vogel Klinik für Allgemein‐, Viszeral‐, Thorax‐, Transplantations‐ und Kinderchirurgie ‐ Uni‐Klinikum Gießen/Marburg, Standort Gießen Rudolf‐Buchheim‐Str. 7 eMail: [email protected]‐giessen.de Telefon: 0641 99 44710 35385 Gießen eSite: Chirurgie Univ. Gießen Telefax: 0641 99 44709 1 / 8 Onkologischer Arbeitskreis Mittelhessen e.V. Stand Juni 2008 Nach der Verdachtsdiagnose eines Bronchialkarzinoms (meist in der Röntgen-Aufnahme der Lunge) durch den behandelnden Arzt (Hausarzt, Internist, Lungenfacharzt) wird durch weitere Bildgebung und mögl. Gewebeentnahme die lokale Tumorausdehnung sowie der Ausschluss/Nachweis einer Fernmetastasierung (Tumorstreuung) bestimmt. Folgende Untersuchungen sind zur Einstufung des Ausmaß der Tumorerkrankung (Staging) und Therapieentscheidung (Operation u./o. Chemotherapie) in der Zusammenschau notwendig: Computertomographie des Brustkorbes (Thorax-CT; siehe Abb. 1), Oberbauch-Sonografie (Ultraschall Untersuchung) Oberbauch–CT Lungenfunktion Bronchoskopie (Bronchienspiegelung) Ergänzend könne zusätzlich notwendig sein: • • • • Spezielle Computertomographie mit nuklearem. Marker (PET-CT) Skelettszintigraphie (spezielle Knochenstoffwechsel- Untersuchung) Computertomographie des Kopfes (CCT) Herzecho, Untersuchung der Herzfunktion in Ruhe (ggf. auch mit Belastung) Abb. 3: Bronchialkarzinom im rechten Lungenoberlappen, Befund bei der Bronchoskopie Verfasser: Dr. Carsten Vogel Klinik für Allgemein‐, Viszeral‐, Thorax‐, Transplantations‐ und Kinderchirurgie ‐ Uni‐Klinikum Gießen/Marburg, Standort Gießen Rudolf‐Buchheim‐Str. 7 eMail: [email protected]‐giessen.de Telefon: 0641 99 44710 35385 Gießen eSite: Chirurgie Univ. Gießen Telefax: 0641 99 44709 2 / 8 Onkologischer Arbeitskreis Mittelhessen e.V. Stand Juni 2008 Als operative Untersuchungsverfahren können darüberhinaus noch folgende Maßnahmen vor der endgültigen Therapiefestlegung erforderlich sein: - Mediastinoskopie (Mittelfellspiegelung) - Thorakoskopie, (Brustkorbspiegelung) - Gewebeentnahme von auffälligen Hals-Lymphknoten (Tochtergeschwülste ?) Abb: Mediastinoskopie, schematisch Anhand der Untersuchungsbefunde aus Bildgebung und Gewebeuntersuchung wird das Tumorstadium (nach UICC: Stadium I-IV) und die daraus abzuleitende individuelle Therapie des Patienten festgelegt. Voraussetzung für eine optimale Behandlung und eine möglichst günstige Prognose der Erkrankung ist das frühzeitige Erkennen und ein frühes Erkrankungsstadium. Für die Prognose des Patienten ist die Art des Lungentumors (Entität), die Tumorausbreitung und die Möglichkeit der kompletten chirurgischen Resektion die drei wichtigsten Faktoren. Ganz entscheidend ist bei den o.g. Untersuchungen hierbei, ob der Tumor: lokal auf die Lunge begrenzt ist lokal fortgeschritten und in die Nachbarorganstrukturen eingewachsen ist oder mediastinale Lymphknoten (Lymphknoten des Mittelfellraumes) gestreut hat oder bereits jenseits der Lunge gestreut ist (metastasiert ist) Verfasser: Dr. Carsten Vogel Klinik für Allgemein‐, Viszeral‐, Thorax‐, Transplantations‐ und Kinderchirurgie ‐ Uni‐Klinikum Gießen/Marburg, Standort Gießen Rudolf‐Buchheim‐Str. 7 eMail: [email protected]‐giessen.de Telefon: 0641 99 44710 35385 Gießen eSite: Chirurgie Univ. Gießen Telefax: 0641 99 44709 3 / 8 Onkologischer Arbeitskreis Mittelhessen e.V. Stand Juni 2008 Am Ende der Diagnostik sind im Sinne der individuell bestmöglichen und sinnvollen Behandlung grundsätzlich zwei verschiedene Therapieziele möglich. kurative Therapieansatz (mit dem Ziel einer definitiven Heilung) oder palliative Therapieansatz (Verlängerung der Lebenszeit, Abmilderung der Tumorsymptome und Besserung der Lebensqualität). Allerdings liegt bei Diagnosestellung des Bronchialkarzinoms in ca. 30% der Fälle ein lokal fortgeschrittener Tumor vor (mit mediastinalen Lymphknotenmetastasen oder Tumorinfiltration in benachbarte Gefäß- oder Organstrukturen wie z.B. Brustwand, Herzbeutel, Zwerchfell, obere Hohlvene oder Aorta; Tumor-Stadium IIIb in der Klassifikation nach UICC) und bei weiteren 40% ein bereits fern-metastasierter Tumor (Metastasen / Tochterabsiedlungen in anderen Organen oder Lymphknoten außerhalb des Thorax Brustkorb); Stadium IV in der Klassifikation nach UICC. Beim Stadium IV ist eine Heilung nicht möglich. Therapiekonzept – Operationsplanung: Ein lokal begrenztes oder im Frühstadium nachgewiesenes Bronchialkarzinom (Stadium I+II und IIIa (wenn T3 N1+N2)) sollte durch eine thoraxchirurgische Operation behandelt werden. Hier besteht ein kurativer Behandlungsansatz. Dabei wird der tumorerkrankte Lungenabschnitt und zusätzlich immer die gesamten Lymphknoten im Bereich der erkrankten Thoraxseite entfernt. Im Falle eines lokal fortgeschrittenen Bronchialkarzinoms (Stadium III), sowie bei intraoperativem Nachweis befallener Lymphknoten ist neben der Operation zusätzlich eine Chemotherapie und/oder Strahlentherapie erforderlich. Im Stadium IIIb (keine Fernmetastase) wird fallbezogen eine Chemotherapie (Induktionsbehandlung) vor der Operation empfohlen. Ist eine Operation auf Grund einer Fernmetastasierung (Stadium IV), weiterer Erkrankungen bzw. wegen erheblich reduzierter Lungenfunktion dem Patienten nicht zuzumuten, wird durch den Onkologen eine Zweifach-Chemotherapie (ggf. in Kombination mit platinhaltigen Substanzen) durchgeführt. Wichtig ist, dass in einer gemeinsamen ärztlichen Konferenz unter Beteiligung eines Thoraxchirurgen, Pneumologen (Lungenfacharzt), internistischen Onkologen (Tumorspezialist) und Strahlentherapeuten wird das jeweilige Therapiekonzept für jeden Patienten individuell besprochen und festgesetzt. Grundsätzlich sind 5 Behandlungsstrategien möglich: • • • • • alleinige Operation präoperative Strahlentherapie + Operation (z.B. bei sog. Pancoast-Tumor, siehe unten) präoperative Chemotherapie + Operation (Induktionsbehandlung, neoadjuvant) Operation + postoperative Chemo-/Strahlentherapie alleinige Chemo-- u./o. Strahlentherapie Verfasser: Dr. Carsten Vogel Klinik für Allgemein‐, Viszeral‐, Thorax‐, Transplantations‐ und Kinderchirurgie ‐ Uni‐Klinikum Gießen/Marburg, Standort Gießen Rudolf‐Buchheim‐Str. 7 eMail: [email protected]‐giessen.de Telefon: 0641 99 44710 35385 Gießen eSite: Chirurgie Univ. Gießen Telefax: 0641 99 44709 4 / 8 Onkologischer Arbeitskreis Mittelhessen e.V. Stand Juni 2008 Abb. 4: Verkleinerung eines Bronchialkarzinoms durch präoperative (neoadjuvante) Chemotherapie (Thorax-CT im Verlauf, links vor der Chemotherapie, rechts nach der Chemotherapie) Vor der Operation werden die Patienten intensiv krankengymnastisch (insbes. in der Atemtherapie) geschult, damit das Risiko der Operation möglichst gering gehalten werden kann. Ein Beenden des Rauchens vor der Operation muss unbedingt angestrebt werden. Standard-Operationsverfahren sind: Lobektomie (Entfernung eines Lungenlappen, s. Abb. 2) Pneumektomie (Entfernung eines Lungenflügels) Diese sind die klassischen Resektionsverfahren. Dehnt sich der Tumor oder die entzündliche Infiltration (Begleitreaktion) bis zur Pleura (Rippenfellhaut) aus, muss dieser Lungeabschnitt über diesen Bereichen außerhalb der Rippenhaut (extrapleural) ausgelöst werden. Man spricht hier noch nicht von einer erweiterten Resektion. Weitere Operationsverfahren sind: Keil- und Segmentresektionen sind in der Regel zur Entfernung von Tochtergeschwülsten (Metastasen) indiziert. Erweiterte Resektionsverfahren, wie z.B. die intraperikardiale Gefäßversorgung, Vorhofteilresektion, Resektion der Brustwand, des Zwerchfells oder von Ösophaguswandanteilen en-bloc mit Entfernung des Primärtumors können notwendig sein, um eine komplette Entfernung im Gesunden zu erzielen. Grundsätzlich muss immer mit ausreichendem Abstand zum Tumor, in Korrespondenz zur Tumorausbreitung oder dem Lymphknotenbefall, gegebenenfalls in Abhängigkeit von der Schnellschnittuntersuchung (Resektionslinie am Bronchus, Pleura, Gefäß), operiert werden. Parenchym sparende Resektionsverfahren (Manschettenlobektomie), Plastische Eingriffe an der Trachea, Bronchien und Gefäßen ermöglichen bei entsprechenden Tumorstadien ein gewebesparendes und funktionserhaltendes Operieren. Diese gilt nicht nur für die sogenannten Manschettenresektionen, sondern für alle Eingriffe Verfasser: Dr. Carsten Vogel Klinik für Allgemein‐, Viszeral‐, Thorax‐, Transplantations‐ und Kinderchirurgie ‐ Uni‐Klinikum Gießen/Marburg, Standort Gießen Rudolf‐Buchheim‐Str. 7 eMail: [email protected]‐giessen.de Telefon: 0641 99 44710 35385 Gießen eSite: Chirurgie Univ. Gießen Telefax: 0641 99 44709 5 / 8 Onkologischer Arbeitskreis Mittelhessen e.V. Stand Juni 2008 einschließlich der Bifurkationsresektion (Aufteilung der Hauptluftröhre in den rechten+ linken Hauptbronchus) und End-zu-End-Anastomose des gegenseitigen Hauptbronchus mit der Trachea (Hauptluftröhre) Endoskopische Verfahren (minimal-invasiv, Schlüssellochtechnik) sind bei Resektionen von Bronchialkarzinomen Gegenstand der Forschung und sind zurzeit kein anerkannter Standard. Sog. Lungen-Rundherde d.h. Lungenherde unklaren Verhaltens (benigne/maligne) können oft zunächst endoskopisch entnommen werden. Bei Malignität folgt dann aber immer mindestens die o.g. Lappenentfernung über einen herkömmlichen Rippenrandschnitt. Bei den sog. Pancoast-Tumoren in der oberen Thoraxapertur (Bronchialkarzinom, ausgehend vom Oberlappen mit Anwachsen an die Rippen der oberen Thoraxöffnung) handelt es sich je nach Lymphknotenbefall im Mediastinum (Mittelfell) um einen lokal fortgeschrittenen, aber potentiell resektablen Tumor (TNM: T3 oder T4, Stadium IIIa oder IIIb). Hier ist eine Vorbestrahlung mit 50-60 Gray und ggf. eine Chemotherapie vor Operation erforderlich. Die Resektion (gegebenenfalls mit Rippenresektion kombiniert) muss 12-14 Tage nach Beendigung der Bestrahlung erfolgen. Prognose: Die Überlebenschance nach vollständiger (kurativer) Resektion eines Bronchialkarzinoms ist vom Tumor Stadium abhängig und korreliert vor allem mit dem Vorhandensein und Ausdehnung des Lymphknotenbefalles. Im Frühstadium I (nach UICC) werden 5-Jahres-Überlebensraten bis zu 80- 90% erreicht. Die durchschnittlichen 5-Jahres-Überlebensraten nach Resektion für die Tumorstadien II und IIIA (nach UICC) liegen bei 40 % bzw. 20-25%. Auch bei lokal fortgeschrittenen Tumoren können günstige Ergebnisse erzielt werden. Bei Brustwand- und Zwerchfellbefall oder Tumorausdehnung bis zur Aufteilung der Luftröhre (Bifurkation) werden Überlebensraten von 23-42% mitgeteilt. Voraussetzung für eine optimale Erholung nach Operation (Rekonvaleszenz) und eine möglichst günstige Prognose ist, dass die Diagnose und Indikation (Entscheidung) zur Operation frühzeitig gestellt wird, das Karzinom radikal im Gesunden entfernt wird (sog. R0-Resektion) und der Eingriff ggf. organsparend ausgeführt werden kann. Nachbehandlung: Bei R1- und R2- Resektion (mikroskopisch / makroskopisch nicht radikaler Tumorentfernung) erfolgt eine lokale Strahlentherapie, wenn eine Nachresektion nicht möglich ist. Bei intraoperativem Nachweis eines Befalls der mediastinalen Lymphknoten (Mittelfell, N2-Situation) schließt sich eine Strahlen- bzw. Chemotherapie an. Der postoperative Verlauf und Rehabilitation In der Regel ist mit einem Aufenthalt nach Operation von 10-12 Tagen zu rechnen. Nach der Operation steht die frühe Mobilisation, eine konsequente Atemgymnastik (Atem-Coach) und Sekretolyse durch Inhalationen im Vordergrund. Jeder Patient benötigt zur Entlüftung der operierten Thoraxseite eine Sog-Drainage mit Sekretauffangbehälter. Bei unkomplizierten Verlauf kann diese am 1. bzw. 2. postoperativen Tag entfernt werden. Eine rückenmarksnahe Schmerzmittelpumpe (Peridual-Katheter) in den ersten 3-5 postoperativen Tagen plus Verfasser: Dr. Carsten Vogel Klinik für Allgemein‐, Viszeral‐, Thorax‐, Transplantations‐ und Kinderchirurgie ‐ Uni‐Klinikum Gießen/Marburg, Standort Gießen Rudolf‐Buchheim‐Str. 7 eMail: [email protected]‐giessen.de Telefon: 0641 99 44710 35385 Gießen eSite: Chirurgie Univ. Gießen Telefax: 0641 99 44709 6 / 8 Onkologischer Arbeitskreis Mittelhessen e.V. Stand Juni 2008 analgetische Standard-Medikation ermöglicht eine Mobilisation und schmerzfreies Training trotz Thoraxdrainage bereits am 1. postoperativen Tag. Eine eventuelle Nachbehandlung wird mit den beteiligten Ärzten besprochen. Nach einer Thorakotomie ist normalerweise eine leichte körperliche Arbeit ab der 4.-6. und eine schwere körperliche Arbeit ab der 12. postoperativen Woche vertretbar. Eine Keilresektion, Segmentresektion oder Lobektomie führt bei präoperativ normaler Lungenfunktion kaum zu einer merkbaren Beeinträchtigung der Atmung. Die Patienten können meistens wieder ihre berufliche Tätigkeit nach Abklingen der Thorakotomiebeschwerden ausüben. Nach Entfernung einer ganzen Lungenseite (Pneumektomie) oder bei einer ausgeprägten postoperativen Reduktion der Lungenfunktion muss im Einzelfall zur Arbeitsunfähigkeit Stellung genommen werden. Die endgültige Konsolidierung (Ausheilung) der Pneumektomiehöhle mit kompensatorischer Vergrößerung des gegenseitigen Lungenflügels ist erst nach 12-18 Monaten vollzogen. In dieser Zeit geschieht auch die kreislaufmäßige Umstellung auf die neue kardiopulmonale (Herz-Kreislauf-) Situation. In den ersten 6 Monaten ist der Patient nur gering belastbar. Nach dieser Zeit kann körperlich wenig belastende Arbeit verrichtet werden. Eine körperlich schwere Arbeit ist nach der Pneumektomie meistens nicht mehr zumutbar. Der Sozialdienst unserer Klinik organisiert auf Wunsch den weiteren Rehabilitationsverlauf mit Anschlussheilbehandlung (AHB) bzw. die Bereitstellung einer ambulanten Hilfe zu Hause in den ersten 2 Wochen nach Entlassung. Eine AHB wird in aller Regel für 3 Wochen bewilligt, muss aber spätestens 2 Wochen nach Entlassung begonnen werden. Verfasser: Dr. Carsten Vogel Klinik für Allgemein‐, Viszeral‐, Thorax‐, Transplantations‐ und Kinderchirurgie ‐ Uni‐Klinikum Gießen/Marburg, Standort Gießen Rudolf‐Buchheim‐Str. 7 eMail: [email protected]‐giessen.de Telefon: 0641 99 44710 35385 Gießen eSite: Chirurgie Univ. Gießen Telefax: 0641 99 44709 7 / 8 Onkologischer Arbeitskreis Mittelhessen e.V. Stand Juni 2008 Verfasser: Dr. Carsten Vogel Klinik für Allgemein‐, Viszeral‐, Thorax‐, Transplantations‐ und Kinderchirurgie ‐ Uni‐Klinikum Gießen/Marburg, Standort Gießen Rudolf‐Buchheim‐Str. 7 eMail: [email protected]‐giessen.de Telefon: 0641 99 44710 35385 Gießen eSite: Chirurgie Univ. Gießen Telefax: 0641 99 44709 8 / 8