Titel: Salzgehalt des Wassers Themen: Erforschung des Salzgehalts
Werbung
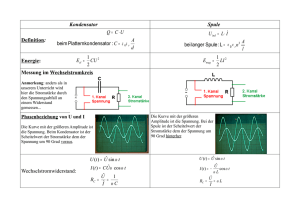
Lithuanian Team Plan Titel: Salzgehalt des Wassers Themen: Erforschung des Salzgehalts im Wasser Zeit: 90 Minuten (2 Unterrichtsstunden) Differenzierung: Richtlinien, IKT Unterstützung etc.: Talentierte Schülerinnen und Schüler werden aufgefordert, die Gleichung der Stromstärke in Abhängigkeit von dem Konzentrationsgrad (von dem Graphen) aufzuschreiben und die physikalische Bedeutung des linearen Richtungskoeffizienten zu definieren. Schülerinnen und Schülern, die die Arbeit rasch erledigen, werden Erweiterungsaufgaben zur Verfügung gestellt. Alter: 14 – 15 Schülerinnen und Schülern werden ein durchgängiger Arbeitsablauf und eine Liste mit dem nötigen Zubehör für diese Aktivität vorgelegt. Da die Ergebnisse dieser Arbeit unter den Schülerinnen und Schülern zuvor noch nicht bekannt sind, ergibt sich die Möglichkeit zu Diskussionen in Gruppen. Analyse der Ergebnisse und Diskussion sind nur wirkungsvoll, wenn die Arbeit in Paaren oder Gruppen von 3-5 Personen durchgeführt wird. Der experimentelle Teil der Unterrichtsstunde kann mit anderen zur Verfügung stehenden Vorrichtungen durchgeführt werden, etwa mit dem computergestützten Lehrsystem Nova5000 (Abbildung 2) oder mit Xplorer GLX, unter Verwendung eines elektrischen Leitfähigkeitssensors. Dann muss nicht die Stromstärke des Elektrolyts gemessen werden, sondern seine Leitfähigkeit (mS). Lithuanian Team Pla n Benötigtes Zubehör für diese Aktivität: Trockenes Salz, Destilliertes Wasser, Waagen, Spannungsquelle (Batterie), 4,5 V, Milliampere Meter, Drähte, Ein Deckel mit 2 Metallelektroden, 100 ml Messzylinder, Ein Glass, Eine Schüssel für Abwasser, Ein Stab, Ein Spatel, Papierhandtücher. Benötigte Kenntnisse: Vorstellungen von Atomen, Ionen, Elektrolyten, der Konzentration einer Lösung, elektrischem Strom. Brüche, Verhältnisse, Prozentrechnung. Lernergebnisse für diese Aktivität: Alle Werden die Haupteigenschaften von Elektrolyten kennen Werden dazu fähig sein, die Prozesse, die in wässrigen Lösungen stattfinden, zu erklären. Werden imstande sein, die Gerätschaften für die Arbeit laut Anleitung vorzubereiten. Werden es schaffen, wässrige Lösungen mit unterschiedlichen Konzentrationen herzustellen. Die meisten Werden den Graphen der Stromstärke in wässrigen Lösungen in Abhängigkeit von der Konzentration aufgelösten Salzes zeichnen können. Werden imstande sein, aus dem Graphen Veränderungen der Stromstärke festzustellen, z. B. Neigungswinkel der Tangente Einige Werden dazu fähig sein, die Gleichung der Stromstärke in Abhängigkeit von der Konzentration niederzuschreiben. Werden imstande sein, die elektrische Leitfähigkeit von Elektrolyten zu bewerten. Gesundheit und Sicherheit: Vorsicht bei der Verwendung der Gerätschaften für das Experiment und der Materialien. 2 Lithuanian Team Pla n Stundenablauf Anfangsaktivität Schülerinnen und Schüler betreten den Klassenraum und räumen ihre Jacken und Taschen weg. Schülerinnen und Schüler werden aufgefordert, sich an den Mathematikunterricht zu erinnern: Brüche, (Verhältnisse), Prozentrechnung und lineare Gleichungen. Dann findet eine Diskussion über die Auswirkungen von Salzgehalt auf Flusswasser, Boden, Pflanzen, und private und gewerbliche Wasseranlagen statt. Schülerinnen und Schüler werden aufgefordert, die Haupteigenschaften von Elektrolyten und den Prozessen, die in ihnen ablaufen, zu erklären. Für die Fähigsten und Talentiertesten kann eine Diskussion über den Einfluss des Salzgehalts von Wasser und Boden auf den Menschen und seine Umgebung durchgeführt werden. Hauptaktivität Schülerinnen und Schüler beginnen mit ihrer Arbeit an dem Arbeitsblatt Erforschung des Salzgehalts im Wasser. Eine praktische Erklärung ist gegeben. Ziel: Die Untersuchung der Abhängigkeit von Stromstärke in Salzlösungen von der Salzkonzentration. Um den Graphen der Stromstärke in der Salzlösung in Abhängigkeit von der Salzkonzentration I = f(c %) zu zeichnen, ist es notwendig, einige wässrige Lösungen mit verschieden hoher Konzentration herzustellen (2 %, 4 %, 6 %, 8 %, 10 %) und die Stromstärke in jeder davon zu messen. Prozentuelle Konzentration [%] c% Figure 1. Electrical scheme md 100 %; wobei m md – Salzmenge, g; m – die ganze Lösungsmasse, g. Um die Stromstärke in der Lösung zu messen, schließe den elektrischen Stromkreis (Abbildung 1). Führe die Messungen und Berechnungen durch. Trage die Ergebnisse in die Tabelle ein. Insgesamt soll immer m 100 g sein, aber unterschiedliche Anteile von Wasser und Salz aufweisen. m md + mv. Die Stromstärke jeder Lösung soll in genau derselben Menge an Lösung gemessen werden (in unserem Fall 100 ml Lösung), damit die Elektroden auf gleiche Weise in der Lösung untergetaucht sind. Erweiterung Talentiertere Schülerinnen und Schüler können zu diesem Zeitpunkt aufgefordert werden, Probleme mit dem Ablauf des Experiments zu betrachten oder Verbesserungen vorzuschlagen. Arbeitsblatt-Aktivität 3 Lithuanian Team Pla n Die Schülerinnen und Schüler sollen die Arbeitsblätter einzeln ausfüllen. Sie sollen die Ergebnisse festhalten, die Daten in die Tabelle eintragen, entscheiden, welche Art von Graph am geeignetsten ist, dann den Graphen zeichnen, von dem Graphen die Veränderungen der Stromstärke berechnen. Nach Veränderung der Konzentration um 1% (in dem Graphen entspricht die Neigung einer Tangente der Stromstärke) definiere mit Hilfe des Graphen die Stromstärke einer 5% bzw. 7%igen NaCl Lösung. Fähigere Schülerinnen und Schüler können aufgefordert werden, die lineare Gleichung aufzuschreiben und den linearen Richtungskoeffizienten zu erklären. Erweiterungsaktivität Schülerinnen und Schüler, die die Arbeit rasch erledigen, können die zur Verfügung gestellten Erweiterungsaufgaben bearbeiten. (Bestimmung der Konzentration einer Salzlösung). Plenum Schülerinnen und Schüler werden über das durchgeführte Verfahren befragt; sie werden aufgefordert, sich Gründe für eigenartige Ergebnisse zu überlegen. Sie werden aufgefordert, Schlussfolgerungen über Stromstärke in Beziehung zu NaCl-Konzentration, über Lösungsleitfähigkeit und den mathematischen Abhängigkeitstyp von NaCl-Konzentration zu machen. Mit den talentierteren Schülerinnen und Schülern wird diskutiert, ob der Prozess immer linear ist und warum Abweichungen von der Linearität möglich sind, wenn die Konzentration der Lösung höher ist. Anmerkung Der experimentelle Teil der Unterrichtsstunde kann mit anderen zur Verfügung stehenden Gerätschaften durchgeführt werden, zum Beispiel mit dem computergestützten Lehrsystem Nova5000 (Abbildung 2) oder Xplorer GLX, unter Verwendung eines elektrischen Leitfähigkeitssensors. Dann muss die Leitfähigkeit (ms) gemessen werden und nicht die Stromstärke. 4 Lithuanian Team Pla n Abbildung 2: Gerätschaften und Materialien des Experiments mit Nova5000 5 Lithuanian Team Worksheet Untersuchung des Salzgehalts von Wasser Substanzen, die sich in Wasser oder in einem anderen polaren Lösungsmittel in positiv geladene Ionen auflösen – Kationen und negativ geladene Ionen – Anionen. Elektrolyte sind Substanzen, die, wenn aufgelöst oder flüssig, elektrischen Strom leiten. Diese Eigenschaften sind charakteristisch für Säure, Hydroxide und für beinahe alle Salzlösungen. Es ist bekannt, dass Salz (NaCl) sich in Wasser auflöst, Moleküle spalten sich in positive (Na+) und negative (cl) Ionen, das heißt elektrolytische Dissoziation findet statt. NaCl (k) → Na+ (aq) + Cl-(aq). Wenn es kein äußeres elektrisches Feld gibt, bewegen sich die Moleküle und Ionen der Lösung chaotisch. Wenn ein elektrisches Feld auftritt, kommt es zu einer unmittelbaren Bewegung der Ionen: positive Ionen bewegen sich in Richtung einer negativen Elektrode und negative Ionen – zu einer positiven hin. Diese zwei entgegengesetzten Ionenflüsse bilden nämlich den elektrischen Strom in den Elektrolyten und die Stromstärke hängt von der Konzentration der Lösung ab Leitfähigkeit ist die Eigenschaft eines Materials elektrischen Strom zu leiten. Die Leitfähigkeit einer Lösung ist bestimmt durch die Gegenwart von aufgelösten anorganischen Salzen, wie etwa Chlorid, Nitrat-, Sulfat- und Phosphat-Anionen (negativ geladenen Ionen) oder NaCl-, Magnesium-, Calcium-, Eisen- und Aluminium-Kationen (positiv geladenen Ionen). Wässrige Lösungen von organischen Verbindungen, wie Öl, Phenol, Alkohol und Zucker leiten den elektrischen Strom nur sehr schwach, weshalb ihre elektrische Leitfähigkeit sehr gering ist. Da die Leitfähigkeit von der Konzentration der Lösung abhängt, sind Messungen zur Leitfähigkeit ein guter Konzentrations-Indikator für die Menge an aufgelösten Festkörpern in der wässrigen Lösung. Leitfähigkeit hängt auch von der Temperatur ab: die Leitfähigkeit einer warmen Lösung ist höher. In einer natürlichen Umgebung kann die Menge an Salz sowohl im Boden als auch im Wasser relativ hoch sein. Zum Beispiel weist das Wasser von Flüssen sehr verschiedene Salzgehalte aufgrund von verschiedener Arten von Boden, geologische Strukturen und salzhaltiges Untergrundwasserströmungen auf. Probleme treten dann auf, wenn die Balance des Salzgehalts in der natürlichen Umgebung sich verändert. Salzgehalt ist eine große Bedrohung für die Oberfläche und Wasserressourcen im Untergrund. Je nach Salzmenge im Boden verändert sich das Wachstum von Pflanzen. Ein hoher Salzgehalt von Flüssen kann die Verwendung des Wassers im Bewässerungssystem, der Landwirtschaft und der Trinkwasserversorgung einschränken. Salinität kann auch die Flora von frischem Wasser, Flora, Fauna und die Küstenvegetation beeinflussen. In Städten vermindert der Salzgehalt von Wasser die Nutzungszeit von Gerätschaften im Haushalt und in der Industrie, und bedingt eine vermehrte Verwendung von Reinigungsmitteln und größere Ausgaben für Wartungen. In wässrigen Lösungen werden für die Leitfähigkeitsmessungen für gewöhnlich Mikrosiemens pro Zentimeter (µS/cm) und Millisiemens pro Zentimeter (mS/cm) verwendet. Lithuanian Team Workshee t Fragen Antworten 1. Was ist elektrische Leitfähigkeit? 2. Was bestimmt die Leitfähigkeit der Lösung? . 3. Wie wird die elektrische Leitfähigkeit der Lösung gemessen? 4. Nach dem Verdampfen von Salzwasser, werden 3% an Salz gewonnen. Wie viel Salz bekommt man, nachdem man 36 kg Salzwasser verdampfen hat lassen? 5. Schreibe die linearen gegebenen Graphen auf. Gleichungen der 7 Lithuanian Team Answer sheet Untersuchung des Salzgehalts von Wasser Antwortblatt Trage die Ergebnisse in die Tabelle ein. Seq. No Salzmenge Wassermenge md, g mv, g Prozentuelle Konzentration c% Stromstärke I, mA 1 2 3 4 5 6 Zeichne mit Hilfe der Daten aus der Tabelle den Graphen der elektrischen Stromstärke in der Salzlösung in Abhängigkeit von der Konzentration I = f(c%). 8 Lithuanian Team Answer sheet Berechne mit Hilfe des Graphen Veränderungen der elektrischen Stromstärke nach der Veränderung der Konzentration um ein Prozent. ∆I/∆c = ............................ mA/%. Berechne mit Hilfe des Graphen was die Stromstärke einer 5%igen NaCl-Lösung ist: I (5 %) = ........................ mA, Berechne mit Hilfe des Graphen was die Stromstärke einer 7%igen NaCl-Lösung ist: I (7 %) = ........................ mA, Im Graphen gibt der Neigungswinkel einer geradlinigen Tangente die Veränderung in der Leitfähigkeit an. Zusatz: Schreibe unter Verwendung des Graphen die Gleichung der Stromstärke in Abhängigkeit von dem Konzentrationsgrad an. .......................................................... Definiere die physikalische Bedeutung des linearen Richtungskoeffizienten. .......................................................... Schlussfolgerungen: Ziehe eine Schlussfolgerung über die Abhängigkeit von Stromstärke von der NaClKonzentration: ................................................................................................................................................ ................................................................................................................................................. Ziehe eine Schlussfolgerung über die Stromstärke einer Lösung und den mathematischen Abhängigkeitstyp von NaCl-Konzentration. .............................................................................................................................................. .............................................................................................................................................. 9 Lithuanian Team Extension Messung der Konzentration einer Salzlösung Wenn man Gurken für den Winter einlegt, ist es notwendig, eine Salzlösung vorzubereiten. Tom und seine Mutter bereiten 1.5 kg einer Salzlösung vor, sie schüttet 3 Löffel Salz in das Wasser. Ein Löffel Salz misst 20 g. Welche Konzentration hat die Salzlösung, die Tom und seine Mutter herstellen? Tom versucht seiner Mutter zu helfen und hat eine größere Menge an Salzlösung zubereitet, aber während der Herstellung hat er vergessen, wie viele Löffel er verwendet hat. Im Unterricht nimmt er 100 g der bereitgestellten Lösung und misst eine Stromstärke von Ix = 150 mA. Bestimme unter Verwendung des Graphen, der die elektrische Stromstärke in der Salzlösung in Abhängigkeit von der Konzentration zeigt (wurde während des Unterrichts gezeichnet), ob Tom eine passende Lösung gemacht hat. 10