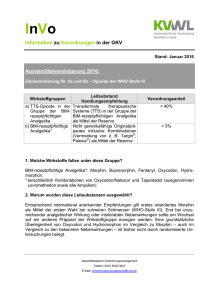
Wechselwirkungen in der Schmerztherapie mit Opioiden
Werbung

forum schmerz 2011 bulletin 13.−14. Mai, Baden-Baden 27.−28. Mai, Nürnberg 22.−23. Juli, Freising ARZNEIMITTELINTERAKTIONEN Liebe Kolleginnen und Kollegen, die Therapie chronischer Schmerzen stellt uns in der täglichen Praxis immer wieder vor neue Herausforder­ ungen. Denn Schmerz ist ein komplexer Bewusst­ seinsinhalt, an dessen Entstehung und Verarbeitung die verschiedensten Gehirnareale beteiligt sind. Des­ halb sind zur Schmerztherapie interdisziplinäre und mechanismenorientierte Ansätze erforderlich. Ein häufiges Problem, mit dem wir immer wieder konfrontiert werden, sind Nebenwirkungen, die bei der Gabe von hochpotenten Analgetika auftreten und die Compliance gefährden. Wir stehen hier im­ mer wieder vor der Herausforderung, die richtige Balance zwischen ausreichender Wirksamkeit und akzeptablen Nebenwirkungen zu finden. Neben ei­ ner bestmöglichen medikamentösen Therapie sollten Schmerzpatienten im Rahmen eines multimodalen Therapiekonzeptes auch nichtmedikamentöse Thera­ piemaßnahmen erhalten. Aktuelle Umfragen bei chronischen Schmerzpatien­ ten zeigen, dass die Kontrolle von Schmerzen immer noch oft unzureichend ist. Es ist deshalb an der Zeit, umzudenken und die neuen Erkenntnisse aus der Forschung in die praktische Schmerztherapie zu in­ tegrieren. Doch wie setzen wir die aktuellen Erkennt­ nisse aus der Schmerzforschung in unsere klinische Praxis um? Welche Therapiemöglichkeiten gibt es für Schmerzen mit einer neuropathischen Komponente? Für diese und viele andere Fragen ist der kollegiale Austausch enorm wichtig. Hierfür boten uns die von der Firma Grünenthal organisierten Symposien „Fo­ rum Schmerz 2011“ in Baden-Baden, Nürnberg und Freising reichlich Gelegenheit. Wir bedanken uns da­ her bei allen Kolleginnen und Kollegen für die aktive Teilnahme an den Diskussionen und für den gemein­ samen Erfahrungsaustausch. Diese Broschüre fasst alle wichtigen Inhalte der drei Veranstaltungen nochmals zusammen. Wir wünschen Ihnen eine anregende Lektüre und viel Erfolg für Ihre tägliche Arbeit in der Praxis. Mit kollegialen Grüßen Dr. med. U. Köster, Stuttgart Prof. Dr. med. C. Maihöfner, Erlangen Wechselwirkungen in der Schmerztherapie mit Opioiden Wechselwirkungen seien in der Schmerztherapie aufgrund der engen therapeutischen Breite vieler Substanzen und dem hohen Anteil an älteren Patienten mit multiplen Begleiterkrankung­ en eine häufige Herausforderung für den Behandler, erläuterte Prof. Dr. med. Walter E. Haefeli von der Abteilung Klinische Pharmakologie und Pharmakoepidemiologie in Heidelberg. Um Wechselwirkungen zu vermeiden, sei es deshalb wichtig, die Stoffwechselwege der Opioide genau zu kennen und die Arzneimitteldosierungen in der Verordnungspraxis der Schmerzthe­ rapie dementsprechend gegebenenfalls anzupassen. Besonders abhängig ist die Sicherheit und Wirksamkeit vieler Schmerzmittel dabei von einer Komedikation, die zu ihrer Akkumu­ lation oder ihrer beschleunigten Elimination führen kann. Insbesondere Analgetika, die über Cytochrom-P450-Stoffwechselwege in der Leber metabolisiert werden, weisen im Allgemei­ nen ein größeres Interaktionspotenzial auf als Substanzen, die über die Uridin-5-DiphosphoGlucuronosyl-Transferase (UGT) zu ihren Glucuroniden abgebaut werden. rapie besonders zu beachten und gegebenenfalls die Dosierung von Analgetika anzupassen. Hierzu sei jedoch eine genaue Kenntnis der wichtigsten Prinzipien von pharmakokinetischen und pharmakodynamischen Arzneimittelinteraktionen von großer Bedeutung. Baden-Baden Prof. Dr. med. Walter E. Haefeli Arzneimittelwechselwirkungen sind eine häufige Ursache für unerwünschte Arzneimittelwirkungen (UAWs). So sind circa fünf Prozent aller Krankenhauseinweisungen auf eine UAW zurückzuführen.1 Dies war auch Gegenstand des Vortrages von Prof. Dr. med. Walter E. Haefeli von der Abteilung ­Klinische Pharmakologie und Pharmakoepidemiologie an der Universitätsklinik Heidelberg. Er erläuterte, dass gerade in der Schmerztherapie, bei der häufig Substanzen mit einer engen therapeutischen Breite eingesetzt werden, die Behandler sehr oft mit Arzneimittelinteraktionen konfrontiert sind. Vor allem die Polypharmazie ist laut Haefeli mit einem erhöhten Risiko für das Auftreten einer UAW assoziiert. Da es sich bei Schmerzpatienten in vielen Fällen um ältere ­Patienten mit multiplen Begleiterkrankungen handle, sei es wichtig, Arzneimittelwechselwirkungen in der Schmerzthe- Arzneimittelinteraktionen – pharmako­ kinetische Arzneimittelinteraktionen sind häufig, Konzentrationsänderung beeinflusst die Wirkung Die Wirkung eines Arzneimittels ist von verschiedenen Prozessen abhängig und weist eine hohe interindividuelle Variabilität auf. Neben der korrekten Einnahme (Verabreichungsprozess) und der Freisetzung aus der Galenik (pharmazeutischer Prozess) tragen insbesondere die Verteilung zum Wirkungsort und die Elimination aus dem Körper (pharmakokinetischer Prozess) sowie die Wirkungen am Wirkort (pharmakodynamischer Prozess) zum therapeutischen Resultat (therapeutischer Prozess) bei.2 Für eine UAW sind häufig pharmakokinetische Wechselwirkungen, bei denen es zu Änderungen der Konzentrations-Zeit-Profile der gleichzeitig verabreichten Arzneimittel kommt, verantwortlich. In Folge davon wird die Wirkung einer Substanz beeinflusst. Davon unterschieden 1 ARZNEIMITTELINTERAKTIONEN werden pharmakodynamische Arzneimittelinteraktionen, bei denen es zu Wirkungsänderungen der verabreichten Substanz kommt, ohne dass deren Konzentration verändert wurde. Opioid-Clearance ist oft abhängig von Cytochrom-P450-Stoffwechselwegen Pharmakokinetische Arzneimittelinteraktionen können die Ausscheidung (Clearance) einer Substanz aus dem Organismus beeinträchtigen. Somit beeinflussen sie den Dosisbedarf eines Arzneimittels. Die Elimination eines Arzneimittels und seiner Abbauprodukte aus dem Organismus erfolgt in den meisten Fällen über die Nieren (renale Clearance) und/oder metabolisch in der Leber (hepatische Clearance) anhand einer Phase1-Reaktion über die Cytochrom-P450-(CYP-) Isoenzyme und mittels einer Phase-2-Konjugation zum Beispiel über die Uridin-5-DiphosphoGlucuronosyl-Transferase (UGT) (Abb.1). Viele Arzneimittel werden in der Leber über die CYP1-, CYP2- und CYP3-Familien metabolisiert. Von besonderer Bedeutung für Arzneimittelinteraktionen ist dabei die CYP3A-Familie, da fast die Hälfte aller Arzneimittel über dieses Enzym abgebaut wird (Abb. 2). Daneben werden circa 20 Prozent der Arzneimittel über die CYP2C-Familie verstoffwechselt, wozu beispielsweise das Phenprocoumon (Marcumar®) gehört. Wichtig sind zudem die Enzyme der CYP2D-Familie. Sie bauen circa 25 Prozent der Arzneimittel ab, während Enzyme der CYP1A-Familie mit nur fünf Prozent eine geringe Rolle spielen.3 In seinem Vortrag wies Haefeli darauf hin, dass man sich für die Schmerztherapie mit Opioiden insbesondere zwei CYP-Isoformen merken solle: Das CYP3A4 sowie das CYP2D6. Beide seien an der Metabolisierung von Opioiden beteiligt. Man solle zudem daran denken, dass bei den drei Isoformen CYP2C9, CYP2C19 sowie CYP2D6 bei circa fünf bis zehn Prozent der Bevölkerung genetische Varianten vorkämen, die eine stark verminderte Enzymaktivität aufwiesen. Als Folge davon würden Medikamente, die an diese drei Isoformen bänden, nur sehr langsam metabolisiert. Bei der Arzneimitteltherapie von Patienten mit diesen CYP-Varianten, sogenannten langsamen Metabolisierern, sei zu berücksichtigen, dass bei allen Medikamenten aufgrund einer erhöhten Arzneimittelkonzentration bereits in der Standarddosierung mit einem geringerem Dosisbedarf und oft auch mit vermehrten Nebenwirkungen gerechnet werden müsse, so Haefeli. Einfluss einer Komedikation auf die CYPStoffwechselwege Die Aktivität der CYP-Enzyme kann durch bestimmte Arzneimittel sowohl erhöht (Enzyminduktion) als auch vermindert (Enzyminhibition) werden. Die CYP-Induktion erfolgt dabei über eine Aktivierung nukleärer Rezeptoren im Zellkern der Leberzelle, die zu einer vermehrten Transkription und damit zur verstärkten Enzymsynthese führt.4 Dieser Prozess dauert in der Regel mehrere Tage, sodass ein maximaler induktiver Effekt erst ein bis zwei Wochen nach der Verabreichung eines induzierenden Arzneimittels zu erwarten ist. Die Folge einer CYP-Induktion ist ein beschleunigter Abbau von Arzneimitteln im Organismus und damit ein erhöhter Dosisbedarf. Laut Haefeli kann die Clearance dabei sogar um das bis zu 20-Fache erhöht werden. Das bedeute, dass auch bis zu 20-fach höher dosiert werden müsse. Für die Schmerztherapie mit Opioiden heißt dies, wie Haefeli erläuterte, dass bei einer gleichzeitigen Phase I (Red/Ox) Phase II (Konjugation) CYP UGT Trsp Bioverfügbarkeit F 50% aller metabolisierten Arzneimittel Gabe eines CYP-Induktors ohne eine Dosiserhöhung des Opioids Entzugssymptome auftreten können. Wichtige CYP3A4-Induktoren seien das Tuberkulostatikum Rifampicin, die Antiepileptika Carbamazepin, Phenytoin und Phenobarbital, das Virustatikum Efavirenz, der Endothelin-Rezeptor­ antagonist Bosentan sowie Johanniskraut. Da es sich bei Letzterem um ein frei verkäufliches pflanzliches Präparat handelt, werde es häufig bei der Anamnese nicht erfasst. Die Inhaltsstoffe von Johanniskraut lassen sich aber laut Haefeli bei circa fünf Prozent aller Patienten im Blut nachweisen. Bei der CYP-Inhibition wird das Enzym durch den Hemmstoff entweder reversibel oder irreversibel gehemmt, woraus ein verminderter Abbau eines Arzneimittels resultiert. Die reversible Hemmung ist dadurch gekennzeichnet, dass das Substrat durch den CYP-Inhibitor kompetitiv von der Bindungsstelle verdrängt wird. Der Effekt der Inhibition ist konzentrationsabhängig und setzt rasch ein. Bei der irreversiblen Hemmung kommt es hingegen zu einer kovalenten Bindung an das Enzym oder zur Zerstörung der CYP-Enzyme. Der inhibitorische Effekt erreicht dann erst verzögert nach einigen Tagen sein Maximum. Die Enzymaktivität ist bei einer irreversiblen Hemmung erst nach einer Neubildung der CYP-Enzyme – in der Regel nach zwölf Tagen – wiederhergestellt.4 Haefeli betonte, dass diese zeitlichen Verzögerungen bei Dosisanpassungen unbedingt zu berücksichtigen seien. CYP-Inhibition – Einfluss auf Opioide, die als Prodrug vorliegen Die Effekte einer CYP-Inhibition auf Opioide hängen von deren pharmakokinetischen Eigenschaften ab. So liegen einige Opioide wie das Tramadol 5% Opioide CYP3A4 CYP1A2 13% 20% UGT CYP2C9 Phase III (gerichteter Transport) CYP: Cytochrom-P450-Isoenzyme UGT: Uridin-5-Diphospho-Glucuronosyl-Transferase Trsp: aktiver Transport Abb. 1: Die meisten Arzneimittel werden vor der Ausscheidung über die Niere in der Leber durch eine Phase-1-Reaktion über die CYP-Enzyme und/oder eine Phase-2-Konjugation über die UGTs metabolisiert und anschließend entweder biliär oder renal eliminiert. Einige Stoffe werden auch direkt über die Nieren ausgeschieden. 20% CYP2C19 Trsp, Filtration Trsp 2 30% 25% CYP2E1 7% CYP2D6 2% Opioide (in-)aktive Metaboliten Abb. 2: Wichtigste CYP-Isoformen des Arzneistoffwechsels. Für die Schmerztherapie mit Opioiden sind insbesondere CYP3A4 und CYP2D6 von Bedeutung. Modifiziert nach Shimada T et al., J Pharmacol Exp Ther 1994. ARZNEIMITTELINTERAKTIONEN oder das Codein als sogenanntes Prodrug vor, was bedeutet, dass sie ihre pharmakologische Wirkung erst nach einer Metabolisierung über das CYP2D6 zum jeweiligen aktiven Metaboliten entfalten. Wird nun Tramadol gemeinsam mit einem Inhibitor des CYP2D6, wie zum Beispiel mit dem Antidepressivum Paroxetin, verabreicht, dann können weniger aktive Tramadolmetaboliten ((+)-O-Desmethyl-tramadol, ein µ-Agonist) gebildet werden und das Prodrug akkumuliert. Die Folge davon ist eine Wirkungsminderung oder -verlust des Tramadols.5 Eine vergleichbare Situation liegt bei Patienten mit einer genetischen Variante des CYP2D6, den langsamen Metabolisierern, vor.6 Dadurch, dass weniger oder langsamer aktive Metabolite gebildet werden können, kommt es bei einer Standarddosierung zu einer beschränkten Response auf Tramadol. Auch das Codein wird über das CYP2D6 in seinen aktiven Metaboliten, das Morphin, umgewandelt. Ungefähr neun Prozent der Bevölkerung sind langsame Metabolisierer im CYP2D6. Bei diesen Patienten ist die Halbwertszeit von Codein um das circa Zehnfache erhöht.7 Sowohl bei langsamen Metabolisierern, als auch bei Patienten, die als Komedikation einen CYP2D6-Inhibitor erhalten, kann mit Codein keine ausreichende Analgesie erreicht werden. Um Wirkungsverluste zu vermeiden, müsse man folglich beim Einsatz von Opioiden in der Schmerztherapie die Inhibitoren von CYP2D6 kennen, erklärte Haefeli. Dazu gehörten zum Beispiel die selektiven Serotonin-Wiederaufnahmehemmer Paroxetin und Fluoxetin (Tab. 1). Wichtig sei jedoch auch zu wissen, dass es ­sich bei pharmakokinetischen Wechselwirkungen nicht um einen Klasseneffekt handelt. Somit habe man, so Haefeli, oft die Möglichkeit, auf eine andere Substanz derselben Klasse, wie zum Beispiel auf Citalopram, auszuweichen. „Eine Kenntnis der wichtigsten CYP-Isoenzyme ist für die Abklärung von Wechselwirkungen in der Schmerztherapie und insbesondere für den Einsatz von Opioiden sehr hilfreich.“ Prof. Dr. Walter E. Haefeli CYP-Inhibition – Einfluss auf Opioide, die als aktive Muttersubstanz vorliegen Die Opioide Fentanyl, Methadon und Oxycodon liegen im Gegensatz zu Tramadol und Codein bereits als aktive Muttersubstanz vor. Sie werden über das CYP3A4 in ihre vorwiegend inaktiven Metaboliten abgebaut. Erhält ein Patient unter einer Therapie mit diesen Opioiden als Komedikation einen CYP3A4-Inhibitor, wie zum Beispiel den HIV-Protease-Inhibitor Ritonavir, kommt es in Folge des verminderten Abbaus zu einer Akkumulation des aktiven Wirkstoffes und damit zu einer Wirkungsverstärkung mit der Gefahr einer Überdosierung.8 Weitere wichtige CYP3A4-Inhi- CYP2D6 CYP3A4 Amiodaron Bupropion Chlorpheniramin Cimetidin Clomipramin Doxepin Duloxetin Fluoxetin Haloperidol Methadon Paroxetin Ritonavir Amiodaron Cimetidin Clarithromycin Diltiazem Erythromycin Fluconazol Grapefruitsaft Indinavir Itraconazol Ketoconazol Nelfinavir Ritonavir Verapamil Voriconazol Tab. 1: Klinisch relevante Inhibitoren der beiden für den Opioidmetabolismus wichtigen CYP-Enzyme CYP2D6 und CYP3A4. Modifiziert nach Hafner V et al., Internist 2010. bitoren sind Azol-Fungistatika (z. B. Itraconazol) und Cimetidin sowie Makrolide, wie Erythromycin und Clarithromycin (Tab. 1).9 Letztere binden sich als irreversible Hemmstoffe kovalent an CYP3A4, sodass mit einer erneuten Enzymaktivität von CYP3A4 erst nach der Neubildung des Enzyms (nach ­vielen Tagen) gerechnet werden kann. Haefeli betonte, dass es im Zusammenhang mit der durch eine CYP-Inhibition auftretenden Wirkungsverstärkung von Opioiden wichtig sei, zwischen Dosis und Konzentration zu unterscheiden. So könne beispielsweise durch eine Komedikation mit Ritonavir die Exposition gegenüber Fentanyl um bis zu 170 Prozent ansteigen, was einer 2,7-fachen Steigerung der ursprünglichen Dosis entspricht.10 Auch bei einer topischen Applikation von Opioiden, wie zum Beispiel bei Verabreichung von Fentanyl über ein Pflaster, führe eine Komedikation mit CYP3A4-Inhibitoren zur Akkumulation von Fentanyl und damit zu einer Wirkungsverstärkung.10 Interessanterweise scheine die topische Applikation von ­Buprenorphin nicht davon betroffen zu sein.11 „Eine bestimmte Dosis muss deshalb nicht immer zur selben Wirkstoff-Konzentration im Menschen führen; vielmehr können besondere Rahmenbedingungen wie Komedikation und Zustand der Eliminationsorgane die Exposition ganz massiv verändern.“ Prof. Dr. Walter E. Haefeli Opioide und Niereninsuffizienz – Akkumula­ tion von aktiven und toxischen Metaboliten Bevor eine Substanz über die Niere ausgeschieden werden kann, wird sie oft über die Enzyme der Phase-2-Konjugation in der Leber wasserlöslich gemacht. Dies erfolgt zum Großteil durch eine Glucuronidierung über die UGTs. Arzneimittelinteraktionen an den UGTs sind laut Haefeli im Gegensatz zu den CYP-Enzymen sehr selten (Abb. 3). Eine hemmende Wirkung auf die UGTs haben, wie Haefeli erläuterte, zum Beispiel das Urikosurikum Probenecid und das NSAID Naproxen. Eine der wenigen Substanzen, die nach Umwandlung durch die UGTs in der Phase-2Konjugation weiterhin als aktiver Metabolit in Form von Morphin-6-Glucuronid vorliege, ist laut Haefeli Morphin. Da dieser Metabolit fast ausschließlich über die Niere eliminiert werde, könne im Falle einer Niereninsuffizienz das pharmakologisch aktive Morphin-6-Glucuronid akkumulieren. Da bei circa 14 Prozent der internistischen Patienten eine Niereninsuffizienz vorliege, sollte man, forderte Haefeli, insbesondere bei älteren Patienten bei akuter Einschränkung der Nierenfunktion Morphin vorsichtig dosieren. Eine Niereninsuffizienz könne, so Haefeli, auch bei der Bildung von toxischen Metaboliten problematisch werden. Dies sei zum Beispiel beim Pethidin der Fall, das in der Leber zu Normeperidin abgebaut werde. Denn Normeperidin wirkt neurotoxisch und kann bei Akkumulation im Organismus Epilepsien auslösen.12 Pethidin eigne sich deshalb nicht für eine Langzeittherapie und sollte bei einer Niereninsuffizienz nicht verabreicht werden. Tapentadol – geringes Interaktionspotenzial durch Metabolisierung über UGTs Das zentral wirksame Analgetikum Tapentadol vereint in einem Molekül zwei unterschiedliche Wirkmechanismen − den µ-Opioidrezeptor-Ago­ nismus (MOR) sowie die Noradrenalin-Wiederauf­ nahmehemmung (NRI).13 Im Gegensatz zu vielen anderen Opioiden spielt der Metabolismus über das Cytochrom-P450-System (CYP2D6, CYP3A4, CYP2C9, CYP2C19) nur eine untergeordnete Rolle.14 Der Abbau erfolgt hingegen hauptsächlich über die UGTs, über die es in seine inaktiven Metaboliten metabolisiert wird. Die Ausscheidung erfolgt nahezu ausschließlich über die Nieren.15 Da die Metaboliten inaktiv seien, sei wahrscheinlich auch eine Niereninsuffizienz ­unproblematisch, vermutete Haefeli. Eine Hemmung der UGTs durch die beiden UGT-Hemmer Probenecid und Naproxen führten zu einem Anstieg der Wirksubstanz (AUC) um 57 beziehungsweise 17 Prozent.16,17 Laut Haefeli wird dies in der Regel als nicht klinisch relevant angesehen. Tapentadol selbst habe, betonte Haefeli, in vitro nur einen leichten hemmenden Effekt auf CYP2D6 gehabt und an den anderen CYP-Enzymen ­weder ein hemmendes noch induzierendes Potenzial aufgewiesen.16 Die gleichzeitige Verabreichung des CYP2C19-Inhibitors Omeprazol ebenso wie eine begleitende Paracetamol- und Aspiringabe hatten laut Haefeli keinen Einfluss auf die Pharmakokinetik von Tapentadol.17 3 ARZNEIMITTELINTERAKTIONEN viele Interaktionen kaum Interaktionen Phase-1-Enzyme vor allem CYP2D6 und CYP3A4 Phase-2-Enzyme Aktive Metaboliten (mit aktivem Beitrag zur Wirkung) Inaktive Metaboliten (ohne Beitrag zur Wirkung) Codein Morphin M-3-Glucuronid Dihydrocodein Dihydromorphin Nordihydrocodein Tilidin Nortilidin Bisnortilidin (Tramadol) O-Desmethyl-Tramadol Prodrug (metabolische Aktivierung erforderlich) Aktives Prinzip (eigentliche Wirksubstanz) M-6-G Buprenorphin Norbuprenorphin Buprenorphin Norfentanyl Fentanyl inaktive Glucuronide Hydromorphon Hydrocodon Hydromorphon UGT Morphin inaktive Glucuronide Morphin-3-Glucuronid M-6-Glucuronid Methadon ? Oxycodon (Oxymorphon) Noroxycodon Pethidin Normeperidin Glucuronide Piritramid ? inaktive Glucuronide Tapentadol Abb. 3: Insbesondere die Opioide, die in der Phase-1-Reaktion über die CYP-Enzyme abgebaut werden, weisen ein erhöhtes Interaktionspotenzial auf. Modifiziert nach Haefeli WE 2011. „Nach den bisherigen Daten zu Tapentadol sind Probleme mit Wechselwirkungen nicht zu erwarten.“ Prof. Dr. Walter E. Haefeli Pharmakodynamische Interaktionen in der Schmerztherapie Bei pharmakodynamischen Interaktionen führt die Anwesenheit zweier Substanzen am gleichen Wirkort zu Wirkungsänderungen, ohne dass deren Konzentration verändert wird. In der 14 Tage Pause Opioide 14 Tage Pause 5 HWZ Pause 14 Tage Pause Tranylcypromin 5 HWZ Pause 14 Tage Pause 7 Tage Pause 14 Tage Pause überlappend einbzw. ausschleichend 1 Tag Pause 5 HWZ Pause HWZ: SSRI: SSNRI: TZA: teraktion, vor der auch in den Fachinformationen gewarnt wird, ist das Auftreten von Kreislauf-, Atem- und ZNS-Störungen im Rahmen eines Serotoninsyndroms bei der Kombination von MAOHemmern und Pethidin. Obwohl diese Interaktion zwar nur für Pethidin eindeutig nachgewiesen wurde, ist die Kombination eines Monoaminoxidase-(MAO-)Hemmers mit einem Opioid kontraindiziert. Es wird deshalb allgemein empfohlen, einen MAO-Hemmer mindestens zwei Wochen vor einer Opioidtherapie abzusetzen (Abb. 4). 14 Tage Pause TZA MAO-B-Hemmer (Selegilin, Rasagilin) Schmerztherapie spielt dies beispielsweise eine Rolle, wenn zu einem vollen Opioidagonisten, wie zum Beispiel Morphin, Fentanyl, Oxycodon oder Pethidin, zusätzlich ein partieller Opioidagonist, wie zum Beispiel Nalbuphin oder Buprenorphin, verabreicht wird.18,19 Dies könne, so Haefeli, zu einer Abschwächung der starken analgetischen Wirkung des vollen Agonisten durch den partiellen Agonisten führen. In Einzelfällen kann es dadurch zu ungenügender Analgesie kommen.20,21 Eine weitere wichtige pharmakodynamische In- 1 Tag Pause 5 HWZ Pause Halbwertszeit Selektiver Serotonin-Wiederaufnahmehemmer Selektiver Serotonin-Noradrenalin-Wiederaufnahmehemmer Trizyklische Antidepressiva SSNRI (Venlafaxin) 7 Tage Pause überlappend einbzw. ausschleichend 14 Tage Pause MAO-A-Hemmer (Moclobemid) SSRI 2 Tage Pause 5 HWZ Pause überlappend ein- bzw. ausschleichend Abb. 4: Empfehlungen zum Ein- und Ausschleichen von MAO-Hemmern bei Trizyklika sowie Opioidtherapie. Modifiziert nach Bienentreu A et al., Ther Umschau 2008 und Haefeli WE 2011. 4 THERAPIE CHRONISCHER SCHMERZEN Mechanismenorientierte Schmerztherapie bei Nichttumorpatienten Die Behandlung chronischer Schmerzen stellt eine große Herausforderung dar. Die Erfahrun­ gen der letzten Jahre zeigen, dass eine erfolgreiche Therapie von chronischen Schmerzen sich an den zugrundeliegenden Schmerzmechanismen orientieren sollte. Tiefere Einblicke in die Mechanismen der Schmerzentstehung und -chronifizierung geben die neuen Erkennt­ nisse aus der (bildgebenden) Schmerzforschung. Neben kortikalen Reorganisationsphäno­ menen, Aktivitätszunahmen in definierten Gehirnarealen und Veränderungen der Neuro­chemie scheint insbesondere auch eine fehlende endogene Schmerzhemmung für die Schmerzchro­ nifizierung von Bedeutung zu sein. Analgetika können über verschiedene Wirkmechanismen in die pathophysiologischen Vorgänge bei der Schmerzchronifizierung eingreifen. Mit Tapen­ tadol steht ein zentral wirksames Analgetikum zur Verfügung, das zwei Wirkmechanismen in einem Molekül vereint: Es bindet nicht nur an µ-Opioidrezeptoren, sondern hemmt auch gleichzeitig die neuronale Wiederaufnahme des Noradrenalins. Damit verstärkt es die Wir­ kung der endogenen Schmerzhemmung. Mindestens 19 Prozent der erwachsenen Bevölkerung in Europa leiden an chronischen nichttumorbedingten Schmerzzuständen.23 Dies de- Therapie chronischer Schmerzen – Bedeu­ tung der körpereigenen Schmerzhemmung monstrierte der Pain-in-Europe-Survey, bei dem die Daten von über 46.000 Teilnehmern aus 15 europäischen Ländern und Israel erhoben wurden. Damit gehören chronische Schmerzen zu den häufigsten Erkrankungen. Dr. med. Stefan Schramm vom Schmerztherapie Zentrum in Mannheim wies in seinem Vortrag darauf hin, dass jedoch trotz der Häufigkeit von chronischen Schmerzzuständen in der klinischen Praxis die Qualität der Schmerzreduktion zu wünschen übrig lasse. Er bezog sich hierbei auf den Pain-in-Europe-Survey in dem 64 Prozent der Studienteilnehmer angaben, dass der Schmerz unter der verordneten Schmerzmedikation nach eigenen Aussagen nur unzulänglich kontrolliert wäre. Eine der Ursachen für eine unzureichende Schmerzkontrolle sind Nebenwirkungen, die eine Dosisreduktion des Analgetikums erforderlich machen oder gar zum Therapieabbruch führen. Laut eines systematischen Reviews brechen chronische Schmerzpatienten unter einer Therapie mit WHO-III-Opioiden eine Behandlung häufiger wegen Nebenwirkungen ab als wegen ungenügender Wirksamkeit.24 Eine unzureichende Schmerzlinderung kann aber auch die Folge einer unzulänglichen Wirkung des verwendeten Schmerzmittels auf die vorherrschende Schmerzart sein. Experten fordern deshalb seit längerem eine mechanismenorientierte Schmerztherapie, die sich an den zugrundeliegenden pathophysiologischen Vorgängen orientiert. Auch die WHO arbeitet im Moment an neuen Leitlinien für die Therapie chronischer gutartiger Schmerzen, die eine individuellere und spezifisch auf den Patienten und seine Schmerzsymptomatik zugeschnittene Therapie ermöglichen soll.25 Für eine mechanismenorientierte Schmerztherapie sind genaue Kenntnisse über die Entstehung nozizeptiver und neuropathischer Schmerzen sowie über die an der Schmerzweiterleitung und ‑modulation beteiligten Schmerzbahnen erforderlich. Durch die aufsteigenden (aszendierenden) Nervenbahnen wird das vom Nozizeptor gesendete Schmerzsignal über das Rückenmark in das Gehirn weitergeleitet. Im zerebralen Kortex und in verschiedenen anderen Kerngebieten wird der Schmerz wahrgenommen und emotional bewertet. Eine wichtige Bedeutung für die Schmerzverarbeitung hat zudem die körpereigene Schmerzhemmung über absteigende (deszendierende) Schmerzbahnen, die zu einer vermehrten Freisetzung der beiden Neurotransmitter Noradrenalin (inhibitorisch) und Serotonin (inhibitorisch und exzitatorisch) im Rückenmark führen. Wie Schramm ausführte, gibt es inzwischen auch Hinweise darauf, dass ein Ausfall der körpereigenen Schmerzhemmung eine wichtige Rolle bei der Entstehung von chronischen Schmerzerkrankungen, wie beispielsweise der Fibromyalgie, spielt. In den nächsten Jahren sei es deshalb möglich, dass therapeutische Ansätze, die in die körpereigene Schmerzhemmung über deszendierende Schmerzbahnen eingreifen, weiter an Bedeutung gewinnen. „Eine spezifische Schmerztherapie kann ich als Schmerztherapeut nur beginnen, wenn ich die spezifischen Schmerzmechanismen kenne.“ Dr. med. Stefan Schramm Pain Router® – Hilfe bei der Schmerzdiffe­ renzierung und Therapieauswahl In der klinischen Praxis kann der Pain Router® dem Arzt bei der Auswahl einer geeigneten mechanis- Baden-Baden Dr. med. Ulrich Köster Nürnberg Dr. med. Stefan Schramm Nürnberg und Freising Prof. Dr. med. Christian Maihöfner Freising Prof. Dr. med. Marcus Schiltenwolf menorientierten Schmerztherapie eine gute Orientierung bieten.26 Mithilfe eines übersichtlichen Schemas können der Schmerzcharakter und die Symptome des Patienten eingeordnet werden. Danach kann der Arzt eine medikamentöse Therapie auswählen, die sich an den zugrundeliegenden Mechanismen orientiert. Leidet der Patient beispielsweise im Rahmen einer Arthrose oder eines myofaszialen Schmerzsyndroms an einem belastungsabhängigen lokalen Druckschmerz ohne Anzeichen einer Entzündung, dann handelt es sich in der Regel um einen rein nozizeptiven Schmerz. Dieser sollte mit Nichtopioiden (NSAR, Paracetamol), Muskelrelaxanzien oder – bei starken Schmerzzuständen – mit Opioiden therapiert werden. Bei einer diabetischen Polyneuropathie hingegen klagt der Patient über brennende und einschießende Schmerzen – insbesondere auch in Ruhe. Bei diesen rein neuropathischen Schmer- 5 THERAPIE CHRONISCHER SCHMERZEN zen kommt es durch die periphere Nervenläsion zur Neubildung von Rezeptoren und Ionenkanälen, die zu einer Veränderung des Ruhepotenzials und damit zu einer vermehrten Spontanaktivität der Nervenzellen führt. Zur Therapie des neuropathischen Schmerzes kommen deshalb membranstabilisierende Substanzen, wie Antikonvulsiva (Natrium- und Kalzium-Kanalblocker) oder Antidepressiva, zum Einsatz. Von Bedeutung sind hier auch Wirkstoffe, die über eine noradrenerge und serotonerge Wiederaufnahmehemmung in die endogene Schmerzhemmung eingreifen. Hierzu gehören bestimmte Antidepressiva wie die selektiven Serotonin- und Noradrenalin-Wiederaufnahmehemmer (SSNRI) oder das zentral wirksame Analgetikum Tapentadol. „Über 70 Prozent der Ärzte verordnen bei neuropathischen Schmerzen ein NSAR.“ Dr. med. Stefan Schramm Tapentadol vereint zwei Wirkmechanismen in einer Substanz Tapentadol vereint zwei Wirkmechanismen – µ-Rezeptor-Agonismus (MOR) und Noradrenalin-Wiederaufnahmehemmung (NRI) in einem Molekül. Beide Mechanismen beteiligen sich auf synergistische Weise am analgetischen Effekt von Tapentadol.27 Aufgrund dieser einzigartigen Pharmakologie wurde Tapentadol von einem internationalen pharmakologischen Advisory Board als erster Vertreter der Substanzklasse „MOR-NRI“ zugeordnet.28,29 Der MOR-Agonismus hemmt spinal über die Stimulation der prä- und postsynaptischen Opioidrezeptoren die Schmerzleitung an den aufsteigenden Bahnen und moduliert den Schmerz supraspinal. Über die NRI wird hingegen in den absteigenden schmerzhemmenden Bahnen die Konzentration von Noradrenalin im synaptischen Spalt erhöht und damit die körpereigene Schmerzhemmung verstärkt (Abb. 1). Studien demonstrierten, dass die relative Beteiligung der beiden Wirkmechanismen dabei von der zugrundeliegenden Schmerzart abhängt. Während im nozizeptiven Schmerzmodell die schmerzhemmende Wirkung verstärkt über den MOR-Agonismus vermittelt wird, hat die NRI im neuropathischen Schmerzmodell eine bedeutendere Rolle bei der Schmerzhemmung als die µ-Rezeptorwirkung.30 Trotz dieser Gewichtung sind immer beide Mechanismen gleichzeitig wirksam und an der Schmerzinhibition beteiligt. Tapentadol weist somit ein breites Wirkspektrum auf und eignet sich deshalb sowohl für die Therapie von nozizeptiven und neuropathischen Schmerzen als auch von gemischten Schmerzen (Mixed Pain). Da die Affinität zum µ-Rezeptor im Vergleich zu Morphin um das 50-Fache geringer ist, kommt es, basierend auf den Erfahrungen des Entwicklungsprogramms, unter Tapentadol zudem zu deutlich weniger opioidtypischen Nebenwirkungen wie beispielsweise Übelkeit und Obstipation, als unter Oxycodon – bei allerdings vergleichbarer Wirksamkeit beider Wirkstoffe.31 Ein weiterer Vorteil im Hinblick auf Neben- und Wechselwirkungen ist die günstige Pharmakokinetik von Tapentadol. Seine absolute Bioverfügbarkeit wird durch eine gleichzeitige Nahrungsaufnahme nur unbedeutend beeinflusst. Tapentadol kann deshalb unabhängig von den Mahlzeiten eingenommen werden. Da es eine niedrige Bindungsaffinität für Plasmaproteine aufweist und weitgehend über CYP-unabhängige Stoffwechselwege abgebaut wird, ist das Interaktionspotenzial gering. Weil beim Abbau von Tapentadol keine aktiven Metabolite gebildet werden, ist zudem das Risiko für eine Kumulation sehr gering.32,33,29 Steuerung der Schmerzweiterleitung über Schmerzbahnen Deszendierende Schmerzbahnen Aszendierende Schmerzbahnen Schmerzweiterleitung zum Gehirn → Hemmung der Schmerzweiterleitung über µ-OpioidRezeptoraktivierung endogene Hemmung der Schmerzweiterleitung (deszendierende Regulation) MOR Tapentadol = µ-Opioid-Rezeptor-Agonist → über Aktivierung des α2-Rezeptors durch Noradrenalinfreisetzung NRI Tapentadol = NoradrenalinWiederaufnahmehemmer Abb. 1: Tapentadol vereinigt zwei Wirkmechanismen in einem Molekül. Es beeinflusst somit über den MOR ­sowohl die Schmerzweiterleitung an den aszendierenden Schmerzbahnen als auch über den NRI die endo­ gene Hemmung der Schmerzweiterleitung über die deszendierenden Bahnen. Modifiziert nach Tzschentke TM et al., Drugs Fut 2006 und Tzschentke TM et al., JPET 2007. 6 Tapentadol – Schmerzreduktion bei nozi­ zeptiven und neuropathischen Schmerzen Die Wirksamkeit von Tapentadol-Retardtabletten wurde in klinischen Studien bei unterschiedlichen chronischen Schmerzzuständen untersucht.31,34,35,36 Bei nozizeptiven Schmerzen zeigte Tapentadol bei Patienten mit starken chronischen Schmerzen aufgrund einer Gonarthrose eine wirksame und gleich starke Schmerzlinderung wie Oxycodon.34 Im Vergleich zu Placebo änderten sich die durchschnittlichen Schmerzintensitätswerte für Tapentadol retard signifikant (p < 0,001). Für Patienten mit chronischen, rein nozizeptiven Schmerzen kann deshalb Tapentadol eine wirksame Therapieoption sein (siehe Kasuistik 1). Die Wirksamkeit von Tapentadol konnte auch bei rein neuropathischen Schmerzen demonstriert werden. In einer Studie zur diabetischen Polyneuropathie führte Tapentadol retard während der dreiwöchigen offenen Titrationsphase zu einer deutlichen Schmerzreduktion (Abnahme der mittleren Schmerzintensität (SE) von NSR 7,3 auf 3,5). In der doppelblinden Erhaltungsphase stieg die durchschnittliche Schmerzintensität in der Placebogruppe wieder an (mittlere Änderung der SE 1,3), wohingegen die Schmerzintensität in der Tapentadol-retard-Gruppe auf einem stabilen Niveau blieb (mittlere Änderung der SE -0,1).35 Die Wirksamkeit von Tapentadol zeigte sich auch in Verbesserungen der gesundheitsbezogenen Lebensqualität. Die Therapie mit Tapentadol führte zu numerischen Verbesserungen aller SF-36Scores.38 Tapentadol – Analgetische Wirkung auch auf gemischte Schmerzsyndrome Daneben wurde die analgetische Wirksamkeit von Tapentadol retard bei gemischten Schmerzsyndromen mit nozizeptivem und neuropathischem Anteil untersucht. In einer klinischen Studie bei Patienten mit chronischen Rückenschmerzen verbesserten sich unter Tapentadol retard (100–250 mg zweimal täglich) sowie Oxycodon CR während der gesamten Titrations- und Erhaltungsphase (15 Wochen) die durchschnittlichen Schmerzintensitätswerte signifikant im Vergleich zu Placebo.36 Tapentadol retard war im Vergleich zu Oxycodon CR besser verträglich, insbesondere hinsichtlich opioidtypischer gastrointestinaler Nebenwirkungen. Die bessere Verträglichkeit von Tapentadol retard im Vergleich zu Oxycodon CR zeigte sich auch an einer deutlich reduzierten Rate an Studienabbrüchen aufgrund behandlungsassoziierter unerwünschter Nebenwirkungen (TEAEs).36 Mit retardiertem Tapentadol steht somit eine Behandlungsoption in Form einer Monotherapie zur Verfügung, die sowohl die nozizeptive als auch die neuropathische Komponen- THERAPIE CHRONISCHER SCHMERZEN i Tapentadol – Fakten für die Praxis • Seit 15. September 2010 als Palexia® retard in Deutschland erhältlich • Untersteht der Betäubungsmittelverschreibungsverordnung • Formulierung: retardierte Filmtabletten • Wirkstärken: 50, 100, 150, 200, 250 mg • Dosierung: zweimal täglich bis 500 mg/Tag • Indikation: starke chronische Schmerzen, die eine Therapie mit Opioiden erfordern Empfehlungen für den Therapiestart: •O pioidnaive und opioiderfahrene Patienten mit Morphinäquivalent von < 80 mg: Startdosis von 50 mg zweimal täglich (circa alle zwölf Stunden) •O pioiderfahrene Patienten mit Morphinäquivalent von ≥ 80 mg: Startdosis von 100 mg zweimal täglich (circa alle zwölf Stunden) •T herapieüberprüfung und Steigerung der Dosis (falls notwendig): circa alle drei Tage •A ls Bedarfsmedikation sind schnell freisetzende Analgetika, auch ­Kombinationen mit anderen Opioiden möglich •E ine adjuvante Therapie mit Antiemetika und Laxanzien ist in der Regel nicht erforderlich te von chronischen Schmerzen behandelt (siehe Kasuistik 2). „Gerade auch bei nicht auf Dauer opioidpflichtigen Schmerzzuständen ist Tapentadol gut geeignet, da es in der Regel beim Absetzen keine Probleme bereitet“ Dr. med. Ulrich Köster Auf das Problem einer Chronifizierung beim neuropathischen Schmerz ging Prof. Dr. med. Christian Maihöfner von der Neurologischen Universitätsklinik in Erlangen in seinem Vortrag ein. Er berichtete, dass das Risiko hier aufgrund der durch die Nervenläsion induzierten morphologischen Veränderungen an den Neuronen höher zu sein scheint als beim nozizeptiven Schmerz. Die anhaltende Aktivität der geschädigten Ner- venfasern führe im ZNS zu dauerhaften neuroplastischen Veränderungen – ein sogenanntes Schmerzgedächtnis bilde sich aus. Ein wesentlicher Teil der Chronifizierungsmechanismen beim chronischen Schmerz findet laut Maihöfner im Gehirn statt. Neue spektakuläre Einblicke in die Schmerzverarbeitung und in die Entstehung des Schmerzgedächtnisses seien in den letzten Jahren durch moderne, nichtinvasive bildgebende Methoden, wie die Magnetenzephalografie (MEG), das funktionelle MRT (fMRT) sowie die Positronenemissionstomografie (PET), ermöglicht worden. Maihöfner betonte, dass es nicht wie früher angenommen nur „ein Schmerzzentrum“ gebe, sondern dass durch Schmerzreize ein komplexes Netzwerk an Hirnarealen aktiviert werde – zum Beispiel das laterale Schmerzsystem. Es besteht laut Maihöfner aus dem primären (S1) und dem sekundären somatosensorischen Kortex (S2).39 Beide Areale verarbeiteten vorwiegend die sensorisch-diskriminativen Subkomponenten der Schmerzempfindung. Das mediale Schmerzsystem sei an der affektiv-motivationalen Verarbeitung des Schmerzes beteiligt und setze sich aus dem anterioren Cingulum (ACC) und dem präfrontalen Kortex (PFC) (Abb. 5a) zusammen. Eine Zwischenstellung bei der Schmerzverarbeitung nehme, so Maihöfner, die Inselrinde (Insula) ein. Da Aktivierungen der Insel mit sympathischen Antworten einhergehen, werde vermutet, dass die Insel ein wichtiger Bestandteil bei der autonomen Subdimension der menschlichen Schmerzerfahrung sei. „Schmerz ist ein komplexer Bewusstseinsinhalt, das Gefühl „Schmerz“ entsteht erst im Gehirn.“ Prof. Dr. med. Christian Maihöfner Kortikale Reorganisationsphänomene bei neuropathischen Schmerzen Bei chronischen neuropathischen Schmerzen kann laut Maihöfner die Schmerzverarbeitung in den beteiligten Gehirnarealen deutlich verändert sein (Abb. 5b). Hierzu gehörten beispielsweise Reorganisationen der somatotopischen Karten in den sensorischen und motorischen Arealen der Hirnrinde. Diese Phänomene beobachte man insbesondere bei Phantomschmerzen und komplexen regionalen Schmerzsyndromen (CRPS). So zeigten CRPS-Patienten eine erhebliche Abweichung der Körperrepräsentationen im sensorischen Kortex. Maihöfner und seine Arbeitsgruppe konnten zeigen, dass bei Patienten mit CRPS die kortikale Ausdehnung der Handrepräsentation kontralateral zur CRPS-Seite schrumpft und sich zudem das Handareal in Richtung Lippe 1 Kasuistik 74-jährige Patientin mit schwerer Gonarthrose Dr. med. Stefan Schramm, Schmerztherapie Zentrum Mannheim Anamnese: Die 74-jährige Patientin stellte sich – bei schwerster Gonarthrose und Deformitäten in beiden Knien – aufgrund von starken chronischen Schmerzen im Schmerzzentrum vor. Wegen einer begleitenden Kardiomyopathie war eine kausale Therapie mit einer Knie-TEP nicht möglich. Diagnose: Bei der Untersuchung zeigte sich eine rein bewegungsabhängige Schmerzsituation ohne Hinweis auf eine neuropathische Schmerzkomponente. Trotz einer analgetischen Therapie mit Fentanylpflastern (200 µg/h, Wechsel alle drei Tage) konnte bei der Patientin keine ausreichende Schmerzreduktion erzielt werden. Die subjektive Schmerzwahrnehmung auf der visuellen Analogskala (VAS) wurde mit 7 von 10 angegeben. Die Funktionskapazität war relevant eingeschränkt. Zudem klagte die Patientin über opioidbedingte Nebenwirkungen mit Obstipation und Schwindel. Therapie: Die Patientin wurde äquianalgetisch auf Tapentadol retard umgestellt. Unter der aktuellen Therapie mit retardiertem Tapentadol in einer Dosierung von 500 mg/Tag weist die Patientin nur noch eine mäßig eingeschränkte Funktionskapazität bei guter Verträglichkeit auf. Die subjektive Schmerzwahrnehmung auf der VAS wird mit 3 von 10 angegeben. Fazit: • Mit Tapentadol konnte bei der Patientin mit rein nozizeptiven chronischen Schmerzen eine gute Schmerzkontrolle bei guter Verträglichkeit erzielt werden. • In der Regel ist bei älteren Patienten über 65 Jahre der bisherigen Studienlage zufolge keine Dosisanpassung notwendig.37 • Im Hinblick auf die bestehende Kardiomyopathie sollte die kardiovaskuläre Verträglichkeit einer Schmerzmedikation berücksichtigt werden. Tapentadol führte in therapeutischen Dosierungen in den klinischen Studien nicht zu Veränderungen der EKG-Parameter – insbesondere zu keiner Verlängerung des QT-Intervalls.37 7 THERAPIE CHRONISCHER SCHMERZEN 2 Kasuistik 76-jährige Patientin mit chronischer Lumboischialgie nach Band­ scheibenoperation Dr. med. Ulrich Köster, Klinik für Anästhesiologie, Spezielle Schmerztherapie, Marienhospital Stuttgart Anamnese: Bei der 76-jährigen berenteten Patientin wurde im Dezember 2010 aufgrund einer chronischen Lumbalgie und eines sensomotorischen L5Syndroms links bei Spinalkanalstenose L4 bis S1, multisegmentaler Facettengelenkshypertrophie lumbal und Bandscheibenprotrusionen (L4/5 neuroforaminal beiderseits sowie L5/S1 neuroforaminal links) eine mikrochirurgische Entfernung des Bandscheibenvorfalls bei L5/S1 durchgeführt. Daraufhin kam es zu einer nahezu vollständigen Rückbildung der Radikulopathie L5 links. Nach sechs Wochen traten erneut Beschwerden auf, worauf die Patientin im März 2011 stationär zur konservativen, multimodalen Schmerztherapie aufgenommen wurde. Diagnose: Bei der Aufnahmeuntersuchung zeigten sich bis auf einen brennenden Streifen links, der vom Gesäß bis ans Sprunggelenk reichte, keine neurologischen Defizite. Es lag jedoch eine schmerzhafte Bewegungseinschränkung des linken Beines vor. Die subjektive Schmerzwahrnehmung auf der visuellen Analogskala (VAS) wurde mit 9 von 10 angegeben. Das LasègueZeichen war beiderseits negativ, der Zehen- und Hackengang nur unter Schmerzen demonstrierbar. Medikation bei Aufnahme: • Tolperison 50 mg 1-0-1 • Novaminsulfon 20 Tropfen bei Bedarf • Prednisolon 20 mg 1-0-0 • Omeprazol 20 mg 1-0-0 • Bisoprolol 10 mg ½-0-0 verschoben hatte. Sowohl bei CRPS als auch bei Phantomschmerzen konnte er eine positive Korrelation zwischen dem Ausmaß der kortikalen a b 8 Im Rahmen der durchgeführten Untersuchungen wurde die Schmerzdiagnose eines L5-Syndroms links mit vorwiegend neuropathischem Schmerzcharakter (pain detect 20) bei einer subjektiven Schmerzstärke auf der VAS (0–10) in Ruhe von 5 sowie 9 unter Belastung gestellt. Im MRT stellte sich eine multisegmentale lumbale Spinalkanalstenose (L4 bis S1 mit absoluter spinaler Enge), eine Protrusion von Bandscheibenmaterial L4/5 beiderseits intraforaminal und L5 links neuroforaminal sowie eine Hypertrophie der Facettengelenke dar. Daneben zeigte sich eine fortgeschrittene lipomatöse Umwandlung der autochthonen Rückenmuskulatur. Therapie: Die Patientin führte eine 18-tägige stationäre multimodale Schmerztherapie durch. An den Wurzeln L5 und S1 links wurde zudem eine periradikuläre Therapie durchgeführt. Medikation bei Entlassung: • Gabapentin 300 mg 1-1-1 • Tapentadol retard 100 mg 1-0-1 • Concor 5 mg 1-0-0 • Novastatin 40 mg 0-0-1 Die subjektive Schmerzstärke bei der Entlassung wurde mit 2 von 10 (VAS) angegeben. Fazit: Die Patientin zeigte ein gemischtes Schmerzsyndrom mit nozizeptiver und überwiegend neuropathischer Komponente, das unter Medikation mit einem Muskelrelaxans, einem NSAR und einem Glukokortikoid nur unzureichend kontrolliert war. Mit der die multimodale Therapie begleitenden Umstellung auf Gabapentin und Tapentadol retard, bei der auch die neuropathische Komponente des Schmerzsyndroms berücksichtigt wurde, konnte eine gute Schmerzreduktion erzielt werden. Veränderungen und der Schmerzstärke feststellen.40,41,42 Kortikale Reorganisationsphänomene seien mittlerweile auch bei anderen Erkrankungen, wie chronischen Rückenschmerzen sowie bei Nervenläsionen, nachgewiesen worden, so Maihöfner. In der Zwischenzeit sei bekannt, dass kortikale Reorganisationsphänomene durch multimodale Therapieprogramme, die eine suffiziente Schmerztherapie sowie neurorehabilitative Therapieverfahren umfassen, wieder verbessert werden können.41,43 Zu den neurorehabilitativen Therapieverfahren gehöre die sogenannte Spiegeltherapie, bei der durch das Spiegelbild der gesunden Extremität und einem sensomotorischen Training die krankheitsbedingten kortikalen Ver- Abb. 5: a) Hirnaktivierung bei experimentellen Schmerz­­reizen: li. laterales Schmerzsystem mit S1 (primärer somatosensorischer Kortex) und S2 (sekundärer somatosensorischer Kortex), re. mediales Schmerzsystem mit ACC (anteriorer cingulärer Kortex) und PFC (präfrontaler Kortex). b) Hirnaktivierung bei neuropathischen Schmerzen. Die Inzidenz der Aktivierungen entspricht den Größendarstellungen der jeweiligen Kortexareale. Modifiziert nach Maihöfner C et al., Schmerz 2010. änderungen und somit die Schmerzentstehung im Gehirn positiv beeinflusst werden sollen (siehe Kasuistik 3). Durch Studien seien die positiven Effekte der Spiegeltherapie bei Phantomschmerzen und CRPS mit einer deutlichen Schmerzreduktion und einer verbesserten Kontrolle der erkrankten Extremität oder des Phantomglieds bereits demonstriert worden, berichtete Maihöfner44,45 Aktivierung von emotionalen Gehirnarealen und fehlende Schmerzhemmung Neben kortikalen Reorganisationsphänomenen in den somatotopischen Hirnrindenkarten beobachte man, so Maihöfner, bei chronischen Schmerzsyndromen zudem eine vermehrte Aktivierung von emotionalen Gehirnarealen wie dem dorsolateralen präfrontalen Kortex (PFC). Diese Aktivierung werde von multiplen Faktoren, wie einem zugrundeliegenden pathologischen Schmerzzustand, Erwartungshaltungen, Aufmerksamkeit, Affekt und Stimmung beeinflusst und somit auch als „individuelle Schmerzsignatur“ bezeichnet. Mehrere tierexperimentelle Studien haben, wie Maihöfner berichtete, gezeigt, dass bei chroni- THERAPIE CHRONISCHER SCHMERZEN 3 Kasuistik 34-jähriger Patient mit CRPS I Stadium 3 nach Mittelhand­ trümmerbruch (MHK 2) rechts Prof. Dr. med. Marcus Schiltenwolf, Universitätsklinikum Heidelberg, Stiftung Orthopädische Universitätsklinik, Heidelberg Anamnese: Der 34-jährige Patient, von Beruf Stukkateur im Bauhauptgewerbe, klemmte sich im Oktober 2008 die rechte Hand in der Autotür ein, nachdem die Tochter die Tür unerwartet zugeschlagen hatte. Dabei erlitt er einen Trümmerbruch des zweiten Mittelhandköpfchens. Die Fraktur wurde operativ mit einer Osteosynthese versorgt. Nach der Metallentfernung im Januar 2009 konnte der Patient wieder in das Berufsleben eingegliedert werden. Im April 2009 fiel während der Arbeit eine Gerüstbauklappe auf die operierte rechte Hand. Im Mai wurde der Patient aufgrund zunehmender Beschwerden stationär aufgenommen. Im Rahmen der dort durchgeführten Untersuchungen wurde ein CRPS I Stadium 3 der rechten Hand sowie eine Anpassungsstörung diagnostiziert und eine medikamentöse Schmerztherapie begonnen. Im November 2009 erhielt der Patient zudem eine ambulante Psychotherapie, die im Januar 2010 aufgrund der weiter bestehenden Schmerzsymptomatik mit einer tagesstationären Schmerztherapie ergänzt wurde. Parallel dazu erfolgten erste Rentengutachten (handchirurgisch, neurologisch, psychiatrisch), die eine Minderung der Erwerbsfähigkeit von 40 Prozent sowie eine Empfehlung zum Einhändertraining aussprachen. Ab Mai 2010 erfolgte eine medizinische und berufliche Rehabilitation bei der ein Einhändertraining sowie eine berufliche Umschulungsmaßnahme zur Qualitätsfachkraft durchgeführt wurden. Nach einem Wegeunfall auf dem Weg zur Schulung, bei der es zu keinen neuen strukturellen Schäden an der Hand kam, brach der Patient die Umschulung ab. Bei weiter fortbestehender Schmerzsymptomatik und deutlicher Funktionseinschränkung der rechten Hand sowie zunehmender Stresssymptomatik mit Panikattacken stellte sich der Patient in der Ambulanz und Tagesklinik für Schmerztherapie in Heidelberg vor. Diagnose: Bei der körperlichen Untersuchung war die Spontanmotorik des rechten Armes kaum mehr vorhanden, nach Aufforderung war ein schwacher Grobgriff und Faustschluss möglich. Der Zeigefinger wurde gestreckt gehalten und war mehr als 2° C kühler. Die funktionellen Einschränkungen der Hand waren teilweise überwindbar. Daneben lagen eine Hyperhidrose und eine mechanische Allodynie vor. Die subjektive Schmerzwahrnehmung auf der visuellen Analogskala (VAS) wurde mit 5–8 von 10 angege- schen Schmerzen zudem eine verminderte Aktivität des endogenen Schmerzhemmungssystems eine Rolle spiele. Man vermute, dass auch beim Menschen eine fehlende Schmerzhemmung für die Schmerzchronifizierung relevant sei. Daneben scheinen auch veränderte Opiatrezeptorbindungsprofile für die Chronifizierung von neuropathischen Schmerzen eine Rolle zu spielen. Nach Maihöfner gebe es Hinweise darauf, dass Fibromyalgiepatienten eine verminderte Anzahl von Opioidrezeptoren im Gehirn aufweisen.46 i ben. Der HADS (Hospitality Anxiety and Depression Scale) Angst lag bei 21 Punkten (Grenzwert 11 Punkte), der HADS Depression bei 14 Punkten (Grenzwert 11 Punkte). Der Wert der freien Rückenfunktion nach dem Funktionsfragebogen Hannover (FfbH-R) lag bei 35 Prozent. Auffällig war ein deutlich angespannter Gesichtsausdruck mit Anzeichen für Ärger und Wut über die Situation. Die psychosomatische Untersuchung ergab gehemmte Aggressionstendenzen gegenüber dem strengen Vater und der Tochter, die der Patient für den Unfall verantwortlich machte. Nach der Befunderhebung wurden die folgenden Diagnosen gestellt: • CRPS, Stadium 3 • Somatoforme Schmerzstörung • Panikstörung mit Panikattacken • Anpassungsstörung Therapie: Zur Refunktionalisierung des rechten Armes wurden eine Spiegeltherapie und eine Ergotherapie veranlasst. Daneben erhielt der Patient eine normale Physiotherapie und ein Belastungstraining. Zur Therapie der psychosomatischen Komponente wurde bei dem Patienten eine begleitende Psychotherapie (vier psychotherapeutische Einzelgespräche pro Woche und drei Gruppengespräche) durchgeführt. Zweieinhalb Wochen nach Therapiebeginn fühlte sich der Patient bereits deutlich besser und war mit dem Therapieergebnis zufrieden. Mit der rechten Hand konnte er wieder einen Händedruck ausführen, der rechte Arm wurde teilweise wieder in die Psychomotorik integriert. Obwohl durch die Therapie noch eine weitere Verbesserung der rechten Hand zu erwarten gewesen wäre, wollte der Patient die Therapie beenden, um sein Anrecht auf eine Umschulung und die Unfallrente nicht einzubüßen. Fazit: • Der Patient wies neben der Bewegungsstörung im Rahmen eines CRPS psychische komorbide Störungen auf. Aufgrund der Häufigkeit von komorbiden psychischen Störungen sollte die Therapie des CRPS immer ganzheitlich orientiert sein – auch Psychotherapie und nichtmedikamentöse Maßnahmen sind ein Bestandteil davon. • Die Persönlichkeit und das Umfeld sowie der sekundäre Krankheitsgewinn sollten immer bedacht und therapeutisch integriert werden. • Mit der Spiegeltherapie als einem ergotherapeutischen Verfahren, das in den Pathomechanismus der kortikalen Reorganisation eingreift, konnte bei dem Patienten eine deutliche Verbesserung der Psychomotorik sowie eine Schmerzreduktion erreicht werden. Spiegeltherapie Bei der Spiegeltherapie soll der Patient anstatt der erkrankten beziehungs­weise amputierten Extremität das Spiegelbild der gesunden Extremität ­wahrnehmen. Dazu steht vor dem Patienten in der Sagittalebene ein Spiegel, hinter dem sich die erkrankte oder nach einer Amputation nicht mehr vorhandene Extremität des Patienten befindet. Der Patient blickt in den Spiegel und sieht somit zwei gesunde Extremitäten. Unter ergotherapeutischer Anleitung führt er ein sensomotorisches Training (zum Beispiel Übungen mit dem Ball, Knetrolle, Nagelbrett) zunächst vor dem Spiegel, nach einiger Zeit dann ohne den Spiegel durch. Indikationsgebiete der Spiegeltherapie Deafferenzierungsschmerzen bei: • Amputationen • CRPS (M. Sudeck) • Plexusläsionen • Hirninfarkt 9 SCHMERZTHERAPIE BEI TUMORPATIENTEN Differenzierte Schmerztherapie bei Tumorpatienten Tumorschmerzen gehören zu den häufigsten und für den Patienten belastendsten Sympto­ men einer Tumorerkrankung. Eine bestmögliche, individuell auf den Patienten ausgerichtete Schmerztherapie ist deshalb die Grundvoraussetzung für den Erhalt der Lebensqualität von Tumorpatienten. Die Behandlung eines Mixed Pain erweist sich häufig als schwierig und er­ fordert eine frühzeitige Kombinationstherapie aus einem Opioid und einem Koanalgetikum, wie zum Beispiel einem Antidepressivum oder einem Antikonvulsivum. Die Anforderungen an eine gute Schmerztherapie umfassen neben einer effektiven Schmerzlinderung auch eine akzeptable Verträglichkeit. Eine mögliche Therapieoption bei Mixed Pain könne, wie PD Dr. med. Christoph Wiese von der interdisziplinären Schmerzambulanz des Universitätsklini­ kums in Regensburg in seinem Vortrag erläuterte, aufgrund seines dualen Wirkmechanismus auch Tapentadol sein. teilten beispielsweise 75 Prozent der Patienten ihre aktuelle Schmerzmedikation im Hinblick auf die Therapie von Durchbruchschmerzen als nur unzureichend.48 Aufgrund der vielen Facet- Nürnberg Prof. Dr. med. Hubert Bardenheuer Freising PD Dr. med. Christoph Wiese Die Zahl von Patienten und Patientinnen, die meist für längere Zeit wegen einer Tumorerkrankung behandelt werden, ist seit 1990 erheblich angestiegen. So erhöhte sich die Prävalenz in den letzten 20 Jahren bei den Frauen um circa 35 Prozent, bei den Männern sogar um 80 Prozent.47 Da rund ein Drittel aller Betroffenen bereits bei der Erstdiagnose Schmerzen aufweist, steigt auch der Bedarf einer geeigneten Schmerztherapie für Tumorpatienten. Das primäre Ziel der Tumorschmerztherapie sei, die Lebenszufriedenheit des Patienten zu verbessern, betonte Wiese. Eine analgetische Therapie sollte dabei möglichst frühzeitig unter Nutzung von medikamentösen und nichtpharmakologischen Therapieoptionen, wie zum Beispiel Physiotherapie, Psychotherapie und transkutane Nervenstimulation (TENS), begonnen werden. Häufig auch neuropathische Komponente beim Tumorschmerz vorhanden Trotz der Möglichkeiten der modernen Schmerztherapie muss vor allem die Behandlung von Tumorschmerzen verbessert werden. So beur- 10 ten, die der Tumorschmerz in puncto Ursachen und Schmerzart aufweisen kann, erscheint dies nicht verwunderlich. Nach pathophysiologischen Gesichtspunkten unterscheidet man beim Tumorschmerz zwischen nozizeptiv-somatischen (45 Prozent), nozizeptiv-viszeralen (30 Prozent) und neuropathischen (zehn Prozent) Schmerzen. Wiese berichtete in seinem Vortrag, dass beim Tumorschmerz häufig gleichzeitig sowohl ein nozizeptiver als auch ein neuropathischer Schmerztyp existiere – man spreche dann vom sogenannten „Mixed Pain“.49 Die Behandlung einer Mischung aus nozizeptiven und neuropathischen Schmerzen sei – ähnlich wie beim chronischen Nichttumorschmerz – in der klinischen Praxis häufig schwierig. Der Mixed Pain erfordere eine spezifisch auf beide Schmerzanteile wirkende analgetische Therapie. Um eine differenzierte Schmerztherapie beim Tumorschmerz zu ermöglichen, sei es allerdings erforderlich, zunächst eine ausführliche Schmerzdiagnostik durchzuführen, betonte Wiese. „Die Diagnose „Mixed Pain“ sollte nach einer korrekten Schmerzdiagnostik bei Vorliegen von nozizeptiven und neuropathischen Schmerzanteilen gestellt werden – häufig wird der Begriff jedoch in der Praxis als Verlegenheitsdiagnose bei schwierig einzuordnender klinischer Symptomatik verwendet.“ PD Dr. med. Christoph Wiese Tumorschmerztherapie – schrittweise therapieren Tumorschmerzen mit rein nozizeptiven Anteilen werden, wie Prof. Dr. med. Hubert Bardenheuer von der Klinik für Anästhesiologie der Universität Heidelberg erläuterte, klassisch nach dem WHO- Stufenschema behandelt. Man beginne dabei mit der Stufe I, also mit den bekannten Nicht­ opioid-Analgetika, die NSARs sowie Paracetamol und Metamizol umfassen. Bei unzureichender Schmerzreduktion kombiniere man diese in der Stufe II mit niederpotenten Opioiden. Führe dies noch nicht zur akzeptablen Schmerzlinderung beim Patienten, könne man die niederpotenten Opioide durch hochpotente Opioide ersetzen (Stufe III). In der modernen Schmerztherapie verzichte man jedoch inzwischen mehr und mehr auf den Einsatz von niedrigpotenten Opioiden und wende stattdessen die heutzutage auch in sehr niedriger Dosierung verfügbaren hochpotenten Opioide an, so Bardenheuer. Da niedrig dosierte hochpotente Opioide häufig verträglicher sind als hochdosierte niedrigpotente Opoide, habe dies vor allem im Hinblick auf die Nebenwirkungen gewisse Vorteile. In Stufe IV des WHO-Stufenschemas kämen dann in der palliativen Situation Schmerzpumpen zum Einsatz. Eine Begleitmedikation mit Antiemetika und Laxanzien sei bei einer Therapie mit Opioiden indiziert. Eine Therapie mit Koanalgetika werde abhängig von der speziellen Situation des Patienten eingesetzt. Hierzu zählen laut Bardenheuer beispielsweise Antidepressiva und Antikonvulsiva, die bei neuropathischen Schmerzen eingesetzt werden. Bardenheuer betonte, dass der Patient allerdings vor dem Einsatz von Antidepressiva und Antikonvulsiva vom behandelnden Arzt gut über die neben der eigentlichen Indikation vorhandene analgetische Wirkung dieser Substanzen informiert werden müsse, um die Compliance und das Vertrauensverhältnis zum Arzt nicht zu gefährden. Anwendung von Opioiden in der ­Tumorschmerztherapie Der Basisschmerz sollte laut Bardenheuer immer mit Retard-Opioiden behandelt werden. Viel zu häufig wende man jedoch in der klinischen Praxis in der Basistherapie Tropfen, also rasch wirksame Opioide, zur Dauertherapie an. Das könne langfristig zu einer psychischen Abhängigkeitsproblematik führen, mahnte Bardenheuer. Die Dosisfindung sollte immer titrierend erfolgen, wobei die Startdosis von der Tumorerkrankung abhängt und je nach Vorgeschichte individuell gewählt werden sollte. Die Dosierung richte sich nach der Schmerzintensität, die anhand der visuellen Analogskala erfasst werden könne. Für Durchbruchschmerzen stünden rasch wirksame Opioide mit einem Wirkeintritt nach drei bis fünf Minuten zur Verfügung, die oral, nasal, rektal, SCHMERZTHERAPIE BEI TUMORPATIENTEN subkutan oder intravenös gegeben werden können. Bei Therapieende müssten Opioide immer ausgeschlichen werden, um einer Entzugssymptomatik mit schwerwiegenden klinischen Folgen insbesondere bei älteren Patienten vorzubeugen. Die Applikation der Opioide erfolge entsprechend der Pharmakokinetik. Bei stabilem Tumorschmerz böten sich Pflaster an, um die Anwendung beim Patienten zu erleichtern. Christoph Wiese merkte in seinem Vortrag an, dass zum Erhalt der individuellen Lebensqualität bei Tumorpatienten – insbesondere in der Palliativsituation – neben einer ausreichenden Wirksamkeit der Schmerztherapie auch auf eine akzeptable Verträglichkeit zu achten sei. Denn immerhin treten laut Wiese bei bis zu 80 Prozent der Patienten bei Therapiebeginn mit Opioiden Nebenwirkungen auf. 71 Prozent der Patienten litten unter einer Opioidtherapie an Obstipation.50 Wiese betonte, dass es deshalb wichtig sei, dass man die Patienten vor Therapiebeginn über diese Nebenwirkungen informiere und darauf hinweise, dass sich diese jedoch in den meisten Fällen im Verlauf der Therapie reduzieren. Therapieoptionen bei neuropathischer Schmerzkomponente Neuropathische Schmerzen entstehen durch eine direkte Schädigung des Nervensystems. Ursachen dafür sind eine Kompression oder Infiltration durch Tumorgewebe oder behandlungsassoziierte Schädigungen durch Chemotherapeutika oder eine Strahlentherapie. Neuropathische Schmerzen werden als brennend, elektrisierend und einschießend beschrieben. Häufig kommt es zudem zu sensorischen positiven Symptomen, wie Hyperalgesie, Allodynie und Dysästhesie, sowie zu sensorischen negativen Symptomen, wie Anästhesie oder Hypalgesie.51 Bardenheuer zufolge treten neuropathische Schmerzen meist spontan auf. Sie seien für den Patienten außerordentlich belastend. Da der neuropathische Schmerz häufig nicht morphinsensibel sei, spielten die Koanalgetika hier eine besonders wichtige Rolle. Als Standardmedikation setze man insbesondere bei lanzierenden Schmerzen Antiepileptika ein. Bei brennenden Schmerzen seien hingegen Antidepressiva vom Typ der Serotonin- und Noradrenalin-Wiederaufnahmehemmer indiziert. Tapentadol zur Schmerztherapie bei Mixed Pain Wenn, wie beim Mixed Pain, nozizeptiver und neuropathischer Schmerz nicht voneinander zu trennen seien, sei es angebracht, eine Behandlungsstrategie zu wählen, die beide Schmerzkomponenten berücksichtigt, erklärte Wiese. Hier stehe mit Tapentadol eine interessante Therapieoption zur Verfügung. Durch die Synergie von zwei Wirkmechanismen, dem µ-Opioidrezeptor- Agonismus (MOR) und der Noradrenalin-Wiederaufnahmehemmung (NRI), in einem Molekül, könne eine breite analgetische Wirksamkeit bei allen Schmerztypen – auch bei neuropathischen Schmerzen – erreicht werden. Ein weiterer Vorteil von Tapentadol sei, dass opioidspezifische Nebenwirkungen aufgrund des µ-sparing-Effektes seltener, weniger ausgeprägt und auch von kürzerer Dauer seien. So seien im Vergleich zu Oxycodon CR unter Tapentadol retard signifikant weniger gastrointestinale Nebenwirkungen wie Übelkeit, Erbrechen und Obstipation aufgetreten (Abb. 6).31 Wiese berichtete, dass deshalb nach den bisherigen Erfahrungen weder Antiemetika noch Laxanzien erforderlich seien. Die Dosierung bei der Ein- beziehungsweise Umstellung auf Tapentadol retard richte sich nach der vorhergegangenen Therapie. Bei Tumorschmerzen sollte zudem eine Bedarfsmedikation zur Verfügung stehen, die ein Fünftel bis ein Sechstel der Morphinäquivalenzdosis entspreche. Patienten, die eine Therapie mit Koanalgetika erhalten, sollten diese während der Umstellung zunächst beibehalten. Nach einer stabilen Dosisfindung könne dann versucht werden, die Dosis der Koanalgetika zu reduzieren. Meist könne man die Antidepressiva im weiteren Verlauf dann vollständig absetzen. Antikonvulsiva können aufgrund des unterschiedlichen Wirkmechanismus jedoch weiterhin hilfreich sein. „Vom Therapieprinzip ist Tapentadol ein interessanter Ansatz zur erfolgreichen Therapie von Mixed Pain.“ Prof. Dr. med. Hubert Bardenheuer Schwerste Schmerzzustände – Schmerz­ therapie mittels Medikamentenpumpe Bei schwersten Schmerzzuständen könne entsprechend der Stufe IV des WHO-Stufenschemas eine invasive Schmerztherapie mit einer Medikamentenpumpe sowohl stationär als auch ambulant eingesetzt werden, erläuterte Bardenheuer. Hierdurch ermögliche man eine kontinuierliche Gabe oder vom Patienten individuell abrufbare Einzelgaben. Eine Schmerzpumpe sei beispielsweise bei Schluckstörungen, Tumoren im HNOBereich, in der Finalphase einer Tumorerkrankung sowie bei trotz höchsten Opioidgaben nicht beherrschbaren Schmerzen indiziert. Zur Gabe über eine Schmerzpumpe eigne sich, so Bardenheuer, zum Beispiel Morphinsulfat in einer Konzentration von 10 mg/ml oder Hydromorphon. Für schwere neuropathische Schmerzen sei insbesondere Levomethadon indiziert. Falls dies nicht ausreiche, könne Levomethadon mit S-Ketamin kombiniert werden. Als weitere invasive Verfahren könne man zudem lokale Infiltrationen, periphere Nervenblockaden, Plexus- und Sympathikusblockaden sowie die Spinal- und Periduralanästhesie anwenden, die jedoch in der Palliativsituation nur eine untergeordnete Rolle spielen. Eine invasive Schmerztherapie sei, so Bardenheuer, bei Vorhandensein eines gut ausgebildeten interdisziplinären Teams aus Ärzten, Apothekern und Pflegekräften auch ambulant sehr gut möglich. Abb. 6: Unter Tapentadol retard traten im Vergleich zu Oxycodon CR weniger opioidtypische Nebenwirkungen auf. Modifiziert nach Lange B et al., Adv Ther 2010. Ausgewählte TEAEs ≥ 5 % der Patienten während der Behandlung 7,4 Übelkeit* 2,9 Erbrechen* 20,7 8,2 21 6,9 Obstipation* 16,9 3,5 Somnolenz 11,6 6,3 Schwindel 1,6 Pruritus 4 0 Placebo (n = 993) *p < 0,001, TAP vs. OXY 33 16,8 17,2 5,2 2,2 Mundtrockenheit 36,2 21 13,4 6,8 10 20 Relative Häufigkeit (%) Tapentadol PR (n = 980) 30 40 Oxycodon CR (n = 1001) TEAE = treatment emergent adverse event 11 PSYCHOLOGISCHE SCHMERZTHERAPIE Placebo- oder Kontextfaktoren bei der Behandlung von Schmerzen „The powerful placebo“ – mit dieser Publikation des Anästhesisten Henry K. Beecher begann die Wissenschaft, sich erstmals mit Placeboeffekten auseinanderzusetzen. Während der Be­ griff „Placebo“ früher häufig als Synonym für Einbildung oder Wirkungslosigkeit verwendet wurde, weisen die neuen Erkenntnisse aus der Hirnforschung darauf hin, dass der Place­ boeffekt physiologische Vorgänge im Gehirn auslöst, welche die Wirkungen einer Therapie imitieren und verstärken oder abschwächen können. Die Placebowirkung stellt dabei keine feste Größe dar, sondern wird von emotionalen, rituellen und situativen Kontextfaktoren be­ einflusst. Mit der Einbeziehung dieser Faktoren in das ärztliche Handeln können die Wirkun­ gen einer Schmerztherapie optimiert werden. telle Subordination sowie die nonverbale Kommunikation. Placeboeffekte induzieren physiologische Mechanismen im Gehirn Freising Dr. med. Andreas Kopf Die Gabe von Scheinpräparaten im Rahmen von Schmerztherapien kann die schmerzlindernde Wirkung erheblich verbessern (Placebo) oder verschlechtern (Nocebo). Im engeren Sinne werden nur positive Wirkungseffekte durch ein Arzneimittel ohne Wirkstoff als Placeboeffekt bezeichnet. Es ist aber nicht das Scheinpräparat selbst, das den Placeboeffekt erzeugt, sondern es sind vielfältige unspezifische „Kontextfaktoren“. Die Kenntnis und die Verwendung solcher Kontextfaktoren kann nach Aussage von Dr. Andreas Kopf von der Klinik für Anästhesiologie und operative Intensivmedizin an der Charité in Berlin helfen, die Therapieergebnisse zu optimieren. Placebos werden gemäß einer Erhebung aus Hannover häufig zur Schmerztherapie eingesetzt. 74 Prozent der 225 befragten Ärzte und Pfleger­ Innen gaben hierbei an, schon einmal Placebos eingesetzt zu haben. Bei 62 Prozent der Anwender führte die Placebogabe sogar zum Therapieerfolg.52 Auch eine Metaanalyse bestätigte den häufigen Einsatz von Placebos in der ärztlichen Praxis – zwölf bis 93 Prozent der Ärzte gaben an, Placebos verwendet zu haben, dies jedoch nicht in den Akten vermerkt zu haben. Wie der Metaanalyse weiter zu entnehmen ist, werden häufig auch nicht indikationsspezifische Substanzen, sogenannte „Impure Placebos“, therapeutisch eingesetzt.53 Man geht heute davon aus, dass für den Placeboeffekt nicht nur die Gabe der Tablette oder der Spritze, sondern auch weitere Veränderungen im Umfeld des Patienten verantwortlich sind. Hierzu zählen beispielsweise die „soziale Erwünschtheit“ beziehungsweise die experimen- 12 Die Hirnforschung hat laut Kopf in den letzten Jahren interessante Erkenntnisse zu den Mechanismen des Placeboeffektes erbracht. Bei der Placeboanalgesie handele es sich zum einen um eine klassische Konditionierung, bei der im prä­ frontalen Kortex endogene Opiate ausgeschüttet würden, die zu einer Schmerzhemmung führten. Daneben könne eine positive Erwartungshaltung über das limbische System die Wirkung eines Medikaments verstärken. Wichtig sei auch die Suggestibilität, die über das Oxytocinsystem vermittelt werde und Patienten für eine Placebowirkung sensibilisieren könne. Analog zum Placeboeffekt könnten überdies über den Hippocampus auch Noceboreaktionen getriggert werden. Dies würde zeigen, dass Placebo- und Noceboeffekte nachweislich physiologische Mechanismen im Gehirn induzieren. Placeboeffekte verändern sich abhängig vom Studiendesign In Studien wird Kopf zufolge gewöhnlich angenommen, dass die Placeboreaktion in der Verumund der Placebogruppe immer konstant ist. Man gehe davon aus, dass die eigentliche Wirkung einer Substanz nach Abzug der Placebowirkung ermittelt werden könne, erklärte Kopf. Er warnte, dass Placeboeffekte jedoch nicht immer konstant seien. Vielmehr seien sie durch viele unspezifische Kontextfaktoren beeinflussbar. Man spreche dann von der sogenannten Placebofalle, bei der die Verumwirkung durch viele unspezifische Kontextfaktoren maskiert und somit die eigentliche Wirkung über- oder unterschätzt werde. Wie Kopf erläuterte, sind bereits kleinere Veränderungen des Studiendesigns in der Lage, die Wirkung von Kontextfaktoren zu beeinflussen. So habe eine Studie bewiesen, dass bei einer höheren Wahrscheinlichkeit, das Studienmedikament zu erhalten, auch die Differenz zwischen Verum- und Placeboeffekt größer wurde.54 Wie groß der Einfluss von Kontextfaktoren auf die Wirkung einer Analgetikagabe sein könne, habe eine Studie aus Italien demonstriert, bei der Patienten postoperativ das Analgetikum einmal offen, das heißt über eine aktive Gabe durch den Pfleger, sowie einmal verdeckt, das heißt ohne Ankündigung über einen Perfusor, erhielten. Bei den Patienten, die das Analgetikum offen bekommen hätten, sei eine Schmerzlinderung früher erreicht worden als bei den Patienten der verdeckten Gruppe.55 Das Medikament sei folglich, so Kopf, initial praktisch unwirksam, wenn der Patient nicht wisse, dass er es bekomme. Kontextfaktoren können die Wirkung einer Schmerztherapie beeinflussen Wie positive Patientenerwartungen die Wirkung einer therapeutischen Maßnahme beeinflussen können, zeigte eine Post-hoc-Analyse von vier Akupunkturstudien. Patienten, die eine hohe Erwartung an die Akupunkturbehandlung hatten, sprachen auch besser auf die Therapie an.56 Von großer Bedeutung für das Ansprechen eines­ Medikaments sei aber auch der Arzt-PatientenKontakt, bemerkte Kopf. Einen Einfluss auf die Wirkung von Analgetika habe zum Beispiel, das Geschlecht des Behandlers. So habe eine Studie demonstrieren können, dass männliche Probanden ihre Schmerztoleranz mehr als verdoppeln würden, wenn der Therapeut weiblich sei. Auch das Aussehen des Arztes könne die Schmerztoleranz beeinflussen. Schmerzen würden beispielsweise besser toleriert, wenn der Behandler ein „professionelles Aussehen“ habe.57 Daneben spiele auch die verbale Kommunikation mit dem Patienten eine Rolle. Dies demonstrierte eine Studie an Patienten, die eine Akupunkturbehandlung erhielten. Bei jenen Patienten, mit denen nicht gesprochen wurde, waren die therapeutischen Effekte nur geringgradig höher als bei den Patienten, die gar keine Therapie erhielten. Bei Patienten, mit denen sich der Arzt ausführlich unterhalten hatte, erbrachte die Behandlung die besten Resultate.58 Ähnliche Effekte lassen sich offensichtlich auch über die nonverbale Kommunikation erzielen. Denn wie eine Studie herausfand, können Behandler, die über ihre Körpersprache dem Patienten vermitteln, dass eine Therapie wahrscheinlich unwirksam ist, die Wirkung einer Therapie negativ beeinflussen.59 PSYCHOLOGISCHE SCHMERZTHERAPIE „Der Placeboeffekt ist keine konstante Größe, sondern etwas, das vom Arzt gut beeinflusst werden kann.“ Dr. med. Andreas Kopf Psychosoziale Kontextfaktoren verändern das Schmerzempfinden Auch der soziale Kontext wie zum Beispiel der Einfluss von Angehörigen oder Arbeitskollegen beeinflusst den Behandlungserfolg. Einen ungewöhnlichen situativen Kontextfaktor demonstrierte eine Studie, in der das Zählen von Geldscheinen zu einer stärkeren Schmerzreduktion als das Zählen von einfachen Papierscheinen führte.60 Daneben scheinen auch andere situative Kontextfaktoren die Therapie zu beeinflussen. Wie Kopf aufzeigte, sind zum Beispiel durch helle Räumlichkeiten sowie durch Ausblicke auf Grünflächen bessere Erfolge einer Schmerztherapie erzielt worden. Interessanterweise scheinen auch Bilder in den Behandlungsräumen die Therapie zu beeinflussen. In einer Studie an postoperativen Patienten wiesen die Patienten, die Naturbilder in den Räumen hatten, weniger Schmerzen auf als Patienten in Räumen mit abstrakten Gemälden oder ganz ohne Bebilderung.61 Stark beeinflusst wird das Schmerzempfinden zudem durch emotionale Kontextfaktoren. Dies zeigte eine Studie an 15 verliebten jungen Männern, deren Schmerzempfinden beim Anblick eines Fotos der Partnerin deutlich reduziert wurde.62 Auch ein ritueller Kontext kann eventuell das Behandlungsergebnis beeinflussen. So können laut Kopf bereits die um einen operativen Eingriff ablaufenden Klinik­ rituale, wie beispielsweise die Aufnahme in eine fremde Umgebung, die „Chefarztvisite“ oder die OP-Kleidung von Patient und Ärzten, die Wirksamkeit einer Behandlung deutlich verbessern.63 Aus ethnologischer Sicht könne somit eine Oper­ation sozusagen als schamanistisches ­Ritual angesehen werden, erläuterte Kopf. Nutzung der Kontextfaktoren für eine opti­ mierte Schmerztherapie Zwar können Placebos in der Schmerztherapie eine Analgetikagabe nicht ersetzen, jedoch sollten Kopf zufolge Kontextfaktoren in der Schmerztherapie auch aktiv genutzt werden. Hierzu zähle beispielsweise, dass der Behandelnde offen mit dem Patienten über eine Analgetikagabe spre- che und die Gründe für die Therapiewahl in einer für den Patienten verständlichen Sprache darlege. Auch die therapeutische Umgebung müsse optimiert werden. Hierzu zählten zum Beispiel das Aussehen des Behandlers sowie ausreichende Lichtverhältnisse im Raum. Auch das Fragen nach den Erwartungen des Patienten spiele eine wichtige Rolle. Hierdurch könne eine für den Patienten und seine Umgebung akzeptable Behandlungsoption mit den therapeutisch indizierten Maßnahmen kombiniert werden und dadurch gerade bei chronischen Schmerzpatienten der Behandlungserfolg deutlich verbessert werden, so Kopf. Als Behandler sollte man zudem selbst von der Therapie überzeugt sein, denn eine skeptische Einstellung gegenüber der therapeutischen Maßnahme werde immer auch nonverbal auf den Patienten übertragen. Es gehe darum, die „ärztliche Kunst“ wiederzuentdecken und nicht anzunehmen, dass eine Leitlinienbefolgung allein ein optimales Behandlungsergebnis sichere. „Die Person des Arztes als beratender Begleiter sollte wieder mehr in den Vordergrund gestellt werden.“ Dr. med. Andreas Kopf INTEGRATIVE SCHMERZTHERAPIE Psychosoziale und spirituelle Bedürfnisse von Patienten mit chronischen Schmerzen Die Ursachen für chronische Schmerzen sind vielfältig. Eine erfolgreiche Schmerztherapie sollte deshalb multimodal erfolgen. Neben den medikamentösen Maßnahmen kommt den psychologischen Therapieansätzen, den Entspannungstherapien sowie den Lebensstil- und Verhaltensänderungen eine bedeutende Rolle zu. Auch die psychosozialen und spirituellen Bedürfnisse von Patienten sollten hierbei berücksichtigt werden, da sie für die Krankheitsbe­ wältigung bedeutsam sind. Baden- Baden und Nürnberg Prof. Dr. med. Arndt Büssing Das Ziel eines multimodalen Therapieansatzes bestehe darin, auch die affektiven Begleiterscheinungen zu berücksichtigen und die Entwicklung der „Schmerzkrankheit“ mit ihren psychosozialen Folgen zu vermeiden, berichtete Prof. Dr. med. Arndt Büssing vom Zentrum für Integrative Me- dizin an der Universität Witten/Herdecke in seinem Vortrag. Neben der Verbesserung der lebensbezogenen Funktionen („Physis“) solle auch die emotionale und psychische Seite des Menschen einbezogen werden – und eben zudem auch die Chance bestehen, möglicherweise vorhandene spirituelle Ressourcen des Patienten einzubeziehen. Die gängigen Methoden der modernen Medizin umfasse heute eine Vielzahl an therapeutischen Ansätzen, mit denen mit guten Erfolgen Körper und Psyche des Menschen behandelt werden könnten. Therapieansätze zur Aktivierung von spirituellen Ressourcen, wie zum Beispiel Achtsamkeit, Meditation, Kreativität und Kunst, würden jedoch häufig zu wenig berücksichtigt. Der Grund hierfür ist, dass die unterschiedlichen Spiritualitäten der Patienten im klinischen Kontext meistens ausgeblendet werden, da sie nicht zum eigentlichen medizinischen Behandlungsauftrag gehören. Oft lägen hier auch Missverständnisse vor („irrelevanter Hokuspokus“) – obwohl diese Büssing zufolge bei der aktiven Krankheitsbewältigung eine wichtige Rolle spielen können. Der Begriff Spiritualität sei ein multidimensionales Konstrukt und bezeichne eine nach Sinn und Bedeutung suchende Lebenseinstellung, die mit einem Gefühl der Verbundenheit mit den anderen, der Natur und/oder dem „Göttlichen“ etc. einhergehe. Daraus resultiere in vielen Fällen ein günstigeres Gesundheitsverhalten. Häufig biete erst eine schwere Erkrankung Menschen den Zugang zur Reflektion über Sinn und Bedeutung des eigenen Lebens. Spiritualität und Religiosität – positive ­Beeinflussung des Lebensstils Spiritualität hat wahrscheinlich einen positiven Einfluss auf die Gesundheit. So zeigte eine Metaanalyse, dass ein Engagement im Rahmen einer 13 INTEGRATIVE SCHMERZTHERAPIE institutionalisierten Spiritualität mit einer geringeren Sterblichkeit einhergehe, während dies für intrinsische Aspekte der Spiritualität scheinbar nicht zutrifft.64 Dieser Effekt sei jedoch nur bei Gesunden und nicht bei Kranken sichtbar gewesen, betonte Büssing. Eine weitere Metaanalyse weist darauf hin, dass Spiritualität/Religiosität aufgrund eines gesünderen Lebensstils das Risiko für lebensstilassoziierte Tumoren verringern könne.65 Es komme also auf das Verhalten im Alltagsleben an, betonte Büssing. Bei Schmerzpatienten beeinflusst ihre religiöse Haltung zwar nicht die Schmerzempfindung, sie ist aber in vielen Fällen mit einer positiveren Einstellung gegenüber der Schmerzerkrankung assoziiert.66 Auf den Verlauf von Erkrankungen haben die verschiedenen Formen der Spiritualität wahrscheinlich keinen direkten Einfluss (sie sind wohl ein Wirkfaktor in einer Reihe verschiedener biopsychosozialer Einflüsse) – wohl aber auf den Umgang mit der Erkrankung. Bessere Krankheitsbewältigung durch Spiritualität Bei Schmerzpatienten sei das Interesse für Spiritualität, im Gegensatz zu Patienten mit Tumor­ erkrankungen, eher niedrig bis moderat ausgeprägt, berichtete Büssing. Schmerzpatienten, die einen Rückhalt in ihrer Spiritualität fänden, würden ihre Erkrankung jedoch häufig deutlich positiver bewerten und könnten trotz Schmerzsymptomatik eher Freude und Glück empfinden.67,68 Unser Gesundheitssystem unterstütze die spirituellen Bedürfnisse von Patienten im Gegensatz zu den primären Bedürfnissen jedoch nur selten, obwohl Patienten, wie die Ergebnisse einer Studie ergeben hätten, eher mit ihrem Arzt als mit ihrem Pfarrer oder Seelsorger über diese Bedürfnisse sprechen würden.67 Spirituelle Bedürfnisse umfassen Büssing zufolge sowohl psychosoziale als auch emotionale, existenzielle und religiöse Faktoren, wobei der Wunsch nach innerem Frieden sowie nach aktiver Weitergabe (von Lebenserfahrungen und sogar Trost) die größte Relevanz für die Patienten haben. Das zeigt auch eine Untersuchung an chronischen Schmerzpatienten. Sie demonstriere, dass ein negativer Zusammenhang zwischen der Lebenszufriedenheit und dem Bedürfnis nach innerem Frieden existiere, während religiöse Bedürfnisse eher mit der Schmerzsymptomatik assoziiert sind. Da psychosoziale und spirituelle Bedürfnisse für eine Vielzahl von Patienten eine wichtige Rolle bei der Krankheitsbewältigung spielten, sollten sie von Ärzten wahrgenommen und wertgeschätzt werden, forderte Büssing. Methoden, wie diese Bedürfnisse vom Gesundheitssystem unterstützt werden können, müssten jedoch noch erarbeitet werden. Mind-Body-Medizin – mit Yoga und Meditation Schmerzen lindern Auch mithilfe bestimmter Verfahren aus dem Bereich der Mind-Body-Medizin sei es möglich, Erkrankungen durch eine Förderung der Bewälti- gungs- und Gesundheitsressourcen, der Selbstkompetenz und der Entspannung positiv zu beeinflussen. Zu den Methoden der Mind-BodyMedizin gehörten unter anderem Entspannungstechniken, Mediation, Yoga, Qigong, autogenes Training, Spiritualität und andere. Eine aktuelle Metaanalyse der Arbeitsgruppe von Büssing zum Einfluss von Yoga, das sowohl Auswirkungen auf die Körperfunktion als auch auf Psyche und ­Spiritualität des Patienten haben kann, auf Schmerz und Schmerz-assoziierte Beeinträchtigungen belegte moderate Effektstärken bei geringen Nebenwirkungsprofilen. Die größten Effekte hätten sich, so Büssing, jedoch bei Gesunden gezeigt. Bei chronischen Schmerzpatienten seien die Behandlungseffekte moderater ausgefallen. Interessanterweise hätte gerade eine kürzere Dauer der Yoga-Intervention günstigere Effekte als eine längere Übungsdauer. Yoga beeinflusse überdies positiv Depressivität, Ängstlichkeit sowie Schlafstörungen und Fatigue. Auch mit bestimmten Formen der Meditation lasse sich laut Büssing die Schmerzsymptomatik, die Stimmungslage, Coping-Fähigkeiten sowie die Lebensqualität von chronischen Schmerzpatienten positiv beeinflussen – wenn es dem Patienten gelänge, sich auf diese Verfahren einzulassen. „Interventionen der Mind-Body-Medizin haben den Vorteil, dass sie vom Patienten selbstständig durchgeführt werden können und relativ kostengünstig sind.“ Prof. Dr. med. Arndt Büssing SCHMERZTHERAPIE IM ALTER Schmerz und Muskel bei geriatrischen Patienten Wer Schmerzen hat, bewegt sich weniger. Weniger Bewegung führt zum Abbau von Muskula­ tur. Dieser Teufelskreis aus Schmerz, Immobilität und Muskelabbau, in dem sich häufig ältere Patienten befinden, führt in den meisten Fällen zum Verlust der funktionellen Selbstständig­ keit. Um eine frühzeitige Pflegebedürftigkeit zu verhindern, sollten deshalb bei geriatrischen Patienten neben einer Schmerztherapie gezielte Bewegungsprogramme zum Erhalt der Mus­ kelmasse durchgeführt werden. Baden-Baden Dr. med. Martin Runge Ein wichtiger Aspekt in der geriatrischen Medizin 14 sei es, die vorzeitige Pflegebedürftigkeit zu verhindern, erläuterte Dr. med. Martin Runge, Ärztlicher Leiter der Aerpah-Klinik in Esslingen. Eine wichtige Aufgabe sei es, den altersassoziierten Muskelabbau zu verhindern, denn dieser sei häufig der Beginn einer Kaskade, die von der Altersgebrechlichkeit (engl. Frailty) über die Pflegebedürftigkeit bis hin zum Tod reiche. Die Bewegung könne hier entscheidend zum Erhalt der neuromuskulären Funktionen beitragen. Denn Muskulatur und Knochen hätten auch im hohen Alter noch die Fähigkeit, sich durch Trainingsreize wieder zu regenerieren, fügte Runge an. Da Schmerzen häufig zur Immobilität führen, sei beim älteren Patienten eine effektive Schmerzlinderung von Bedeutung. Hier sei zu beachten, dass der Schmerz im Alter durch Multimorbidität, Multimedikation, Depression und Demenz sowie durch altersspezifische Veränderungen modifiziert werde. Schmerz werde im Alter zwar weiterhin empfunden, jedoch müsse berücksichtigt werden, dass Schmerzen durch Störungen der Kognition und Kommunikation häufig nicht kommuniziert werden, so Runge. Aufgrund des demografischen Wandels – 55 Prozent der jetzt lebenden Frauen werden wenigstens 85 Jahre alt – müsse auch das Gesundheitssystem in Zukunft vermehrt die speziellen Therapiebedürfnisse geriatrischer Menschen berücksichtigen, betonte Runge.69 SCHMERZTHERAPIE IM ALTER Frauen sind häufiger von Schmerz und Immobilität betroffen als Männer Frauen leben zwar länger als Männer, sind jedoch häufiger immobil und pflegebedürftig. Runge verwies hierbei auf die Berliner Altersstudie. Sie zeige, dass 42,6 Prozent der Frauen ab 85 Jahren nicht mehr in der Lage sind, selbstständig eine Treppe hochzusteigen. Die Folge dieser auch mit dem Begriff gerontologisches Paradox bezeichneten Beobachtung sei, dass insbesondere Frauen im Alter ein Muskelaufbautraining betreiben sollten. Frauen seien auch häufiger von Schmerzen betroffen als Männer, bemerkte Runge. So hätten in einer Erhebung aus Bremen 78 Prozent der älteren Frauen berichtet, dass sie stark oder mittelmäßig von Schmerzen betroffen seien. Bei den Männern hingegen seien dies nur 62 Prozent gewesen. Eine verminderte Mobilität ist laut Runge mit einer erhöhten Rate an Stürzen, Frakturen, Krankenhauseinweisungen und Pflegeheimeinweisungen sowie mit einer erhöhten Mortalität assoziiert. Dies hätten verschiedene Studien demonstriert, in denen schlechte Ergebnisse bei lokomotorischen Testverfahren, wie zum Beispiel der Handkraft, ein hochsignifikanter Prädiktor für eine erhöhte Mortalität ­gewesen sei. „Frauen sind zwar langlebiger, haben aber durchschnittlich eine schlechtere Lokomotion im Alter als Männer.“ Dr. med. Martin Runge Hüftfrakturen sind häufig durch altersbe­ dingte Stürze bedingt Der Begriff der Sarkopenie sei zwar allgemein akzeptiert, habe aber in der klinischen Praxis noch nicht zu einer einheitlichen Operationalisierung gefunden, berichtete Runge. Mithilfe von bildgebenden Verfahren, wie der DXA-Methode oder der peripheren quantitativen Computertomographie, lasse sich zwar die Muskelmasse quantitativ bestimmen, inwieweit damit jedoch eine Korrelation zur Lokomotion getroffen werden könne, sei fraglich. Funktionelle einfache Tests, wie die Bestimmung der Handkraft, der Gehgeschwindigkeit und der Fähigkeit schnell aus dem Sitzen ohne Einsatz der Arme aufzustehen, sind laut Runge besser geeignet, um eine Sarkopenie zu diagnostizieren und Therapieverläufe zu dokumentieren. Denn nach den Ergebnissen von Längsschnittuntersuchungen weisen Handkraft, Gehgeschwindigkeit und die Leistungen beim Aufstehen aus dem Sitzen eine erstaunliche hohe Korrelation mit der Mortalität und dem Eintritt der Pflegebedürftigkeit im hohen Alter auf. Für die Prävention von altersbedingten Stürzen sei deshalb das Erfassen von muskulären Einschränkungen von enormer Bedeutung. So werden 90 Prozent aller proximalen Femurfrakturen, wie Runge anführte, durch einen Sturz verursacht. In vielen Studien könne zwar ein Zusammenhang zwischen dem Vorliegen einer Osteoporose und Frakturen demonstriert werden, jedoch hätten diese Studien nie die Stürze in die Analyse einbezogen. Tatsächlich wiesen nur weniger als die Hälfte der Patienten mit einer Hüftfraktur einen DXA-T-Score von weniger als -2,5 auf.70 Da eine Hüftfraktur häufig den Beginn einer Pflegebedürftigkeit einleite, komme der Prävention von altersbedingten Stürzen und Frakturen eine entscheidende Rolle zu. „Die Hüftfraktur ist ein Paradigma für das Versagen des neuro-muskulo-skelettalen ­Systems im Alter.“ Dr. med. Martin Runge i Assessment des Sturzrisikos bei Verdacht auf ein Frailty-Syndrom Vor dem Eintritt einer Pflegebedürftigkeit weist der ältere Patient häufig Anzeichen einer altersbedingten Gebrechlichkeit auf, die als FrailtySyndrom bezeichnet werden. Dazu gehörten Gewichtsverlust, Erschöpfung, Kraftverlust, eine verminderte körperliche Aktivität sowie ein Verlust der Gehgeschwindigkeit.71 Laut einer aktuellen Longitudinalstudie an 35.000 Teilnehmern eignet sich zur Diagnostik der Frailty vor allem die frei gewählte Gehgeschwindigkeit.72 Desweiteren eignen sich zur Erfassung einer altersbedingten Gebrechlichkeit Runge zufolge der Aufstehtest und das Balancemanöver sowie der Tandemstand. Ein älterer Mensch, der nicht in der Lage ist, mindestens zehn Sekunden in der Tandemposition zu stehen, ist, wie Runge erklärte, erhöht sturzund frakturgefährdet. Ein lokomotorischer Sturz ohne Bewusstseinsveränderung im Alltag sei immer ein Hinweis für einen Rückgang der neuromuskulären Kompetenz. Spätestens dann sollte ein Assessment des Sturzrisikos erfolgen (siehe Kasten). Für den Erhalt der Lokomotion sei eine sorgfältige medikamentöse Schmerztherapie eine unerlässliche Basis, so Runge. Daneben kämen vor allem nichtmedikamentöse Maßnahmen, wie physikalische Therapien und insbesondere Bewegungsprogramme zur Verbesserung von Kraft, Koordination und Beweglichkeit, zum Einsatz. Sturzrisikoassessment bei älteren Patienten 1. Aufstehtest zur Evaluierung der Hüftmuskulatur 2. Tandemstand/-gang zur Evaluierung der Balance zur Seite 3. Visus 4. Medikation: Es besteht ein erhöhtes Sturzrisiko bei einer Multimedikation mit mehr als vier Substanzen. Patienten unter Neuroleptika, Benzodiazepinen, Antidepressiva, Antikonvulsiva oder Opiaten sind besonders gefährdet 5. Kognition/Demenz 6. Kreatinin-Clearance < 65 ml/min Als Screeningverfahren sollten eine Sturzanamnese, eine klinische Ganganalyse sowie als Mobilitätstest ein Up-and-Go-Test (Beurteilung von Beweglichkeit und Gleichgewicht beim Aufstehen und beim Gehen) durchgeführt werden. 15 Literatur 1)Kongkaew C et al. Ann Pharmacother 2000;42(7): 1017−25 2) Haefeli WE. Therap Umschau 2006;63:363−365 3) Shimada T et al. J Pharmacol Exp Ther 1994;270(1): 414−423 4) Hafner V et al. Drug interactions Internist 2010; 51(3):359−369 5) Laugesen S et al. Clin Pharmacol Ther 2005;77(4): 312−323 6) Poulsen L et al. Clin Pharmacol Ther 1996;60(6): 636−644 7) Desmeules J et al. Eur J Clin Pharmacol 1991;41(1): 23−26 8) Nieminen TH et al. Eur J Clin Pharmacol 2010; 66(10):977−985 9) Kharasch ED et al. Anesthesiology 2004;101(3): 729−737 10) Olkkola KT et al. Anesthesiology 1999;91(3):681−685 11) Fachinformation Norspan, Stand März 2009 12) Szeto HH et al. Ann Intern Med 1977;86(6):738−741 13) Fachinformation Palexia retard, Stand August 2010 14) Kneip C et al. Drug Metab Lett 2008;2(1):67−75 15) Terlinden R et al. Eur J Drug Metab Pharmacokinet 2007;32(3):163−169 16) Kneip C et al. Drug Metab Lett 2008;2(1):67−75 17) Smit JW et al. Pharmacotherapy 2010;30(1):25−34 18) Smith J, Guly H. BMJ 2004;328(7453):1426 19) Fachinformation Nalpain, Stand April 2009 20) Harrington CJ et al. Am Surg 2010,76(4):397−399 21) Schuh KJ et al. Psychopharmacology (Berl) 1999; 145(2):162−174 22) Sara Bienentreu et al. Therap Umsch 2008;65:613 23) Breivik H et al. Eur J Pain 2006;10(4):287−333 24) Kalso E et al. Pain 2004;112(3):372−380 25) Scoping Document for WHO Treatment Guideline on Non-malignant Pain in Adults Adopted in WHO Steering Group on Pain Guidelines, 14 October 2008; http://www.who.int/medicines/areas/quality_ safety/Scoping_WHOGuide_non-malignant_pain_ adults.pdf 26) Sittl R, Pain Router. http://www.pain-router.com/ 27) Schröder W et al. J Pharmacol Exp Ther 2011; 337(1):312−320 28) Kress HG. Eur J Pain 2010;14(8):781−783 29) Tzschentke TM et al. Drugs Today (Barc) 2009; 45(7):483−496 30) Schröder W et al. Eur J Pain 2010;14(8):814−821 31) Lange B et al. Adv Ther 2010;27(6):381–399 32) Terlinden R et al. Eur J Drug Metab Pharmacokinet 2007;32(3):163−169 33) Kneip C et al. Drug Metab Lett 2008;2(1):67–75 34) Afilalo M et al. Clin Drug Investig 2010;30(8):489−505 35) Schwartz S et al. Curr Med Res Opin 2011;27(1): 151−162 36) Buynak R et al. Expert Opin Pharmacother 2010 11(11):1787−1804 37) Fachinformation Palexia retard, Stand August 2010 38) Palexia retard (Tapentadol). Produktmonografie, S.39 39) Maihöfner C et al. Schmerz 2010;24(2):137−145 40) Maihöfner C et al. Brain 2007;130:2671−2687 41) Maihöfner C et al. Neurology 2004;63(4):693−701 42) Maihöfner C et al. Neurology 2003;61(12):1707−1715 43) Pleger B et al. Ann Neurol 2005;57(3):425−429 44) Moseley GL. Pain 2005;114(1-2):54−61 45) Moseley GL, Wiech K. Pain 2009;144(3):314–319 46) Harris RE et al. J Neurosci 2007;27(37):10000− 10006 47) Robert Koch-Institut (Hrsg.) (2010) Verbreitung von Krebserkrankungen in Deutschland. Entwicklung der Prävalenzen zwischen 1990 und 2010. Beiträge zur Gesundheitsberichterstattung des Bundes. RKI, Berlin 48) Zeppetella G et al. J Pain Symptom Manage 2000;20(2):87−92 49) Webster LR. Am J Manag Care 2008;14 (5 Suppl 1):116−122 50) Kalso E et al. Pain 2004;112(3):372−380 51) Baron R, Tölle TR. Curr Opin Support Palliat Care 2008;2(1):1−8 52) Bernateck M et al. Schmerz 2009;23(1):47−53 53) Fässler M et al. BMC Med 2010;8:15 54) Papakostas GI, Fava M. Eur Neuropsychopharmacol 2009;19(1):34−40 55) Colloca L et al. Lancet Neurol 2004;3(11):679−684 56) Linde K et al. Pain 2007;128(3):264−271 57) Kállai I et al. Pain 2004;112(1−2):142−147 58) Kaptchuk TJ et al. BMJ 2008;336(7651):999−1003 59) Kelley JM et al. Psychosom Med 2009;71(7):789−797 60) Zhou X et al. Psychol Sci 2009;20(6):700−706 61) Ulrich RS et al. Psychophysiology 30 (S1):7 62) Younger J et al. PLoS One.2010;5(10):e13309 63) Green SA. Clin Orthop Relat Res 2006;450:249−254 64) Chida Y et al. Psychother Psychosom 2009;78(2): 81−90 65) Hoff A et al. Eur J Cancer 2008;44(17):2573−2579 66) Dezutter J et al. J Behav Med 2011 2011;34(6): 542−549 67) Büssing A et al. Pain Med 2009;10(2):327−339 68) Dezutter J et al. Pain Med 2010 11(5):765−773 69) Sterbetafel 2006/2007, Baden-Württemberg 70) Wainwright SA et al. J Clin Endocrinol Metab 2005; 90(5):2787−2793 71) Fried LP et al. J Gerontol A Biol Sci Med Sci 2001;56(3):M146−156 72) Studenski S et al. JAMA 2011;305(1):50−58 Palexia retard 50 mg/100 mg/150 mg/200 mg/250 mg Retardtabletten; Verschreibungspflichtig/Betäubungsmittel; Wirkstoff: ­Tapentadol (als Hydrochlorid). Zusammensetzung: Arzneilich wirksamer Bestandteil: Tapentadol (als Hydrochlorid). Sonstige Bestandteile: Tablettenkern: Hypromellose, Mikrokristalline Cellulose, Hochdisperses Siliciumdioxid, Magnesiumstearat. Tablettenüberzug: Hypromellose, Lactose-Monohydrat, Talkum, Macrogol 6000, Polypropylenglycol, Titandioxid (E 171), Eisen(III)-hydroxid-oxid x H2O (E 172) [nur in Palexia retard 100 mg, 150 mg, 200 mg, 250 mg], Eisen(III)-oxid (E 172) [nur in Palexia retard 150 mg, 200 mg, 250 mg], Eisen(II,III)-oxid (E 172) [nur in Palexia retard 250 mg]. Anwendungsgebiete: Behandlung von starken, chronischen Schmerzen bei Erwachsenen, die nur mit Opioid-Schmerzmitteln ausreichend behandelt werden können. Gegenanzeigen: Überempfindlichkeit gegen Tapentadol oder einen der sonstigen Bestandteile von Palexia retard; Asthma oder eine bedrohlich langsame oder flache Atmung (Atemdepression, Hyperkapnie); Darmlähmung; akute Vergiftung durch Alkohol, Schlaftabletten, Schmerzmittel oder andere Psychopharmaka (Arzneimittel mit Wirkung auf Stimmungslage und Gefühlsleben). Nebenwirkungen: Sehr häufig: Übelkeit, Verstopfung, Schwindel, Schläfrigkeit, Kopfschmerz. Häufig: verminderter Appetit, Ängstlichkeit, depressive Verstimmung, Schlafstörungen, Nervosität, Ruhelosigkeit, Aufmerksamkeitsstörung, Zittern, Muskelzucken, Erröten, Kurzatmigkeit, Erbrechen, Durchfall, Verdauungsstörungen, Juckreiz, verstärktes Schwitzen, Hautausschlag, Schwächegefühl, Müdigkeit, Empfinden von Schwankungen der Körpertemperatur, trockene Schleimhäute, Flüssigkeitsansammlung im Gewebe (Ödem). Gelegentlich: allergische Reaktionen, Gewichtsverlust, Desorientiertheit, Verwirrtheit, Erregbarkeit (Agitiertheit), Wahrnehmungsstörungen, ungewöhnliche Träume, euphorische Stimmung, Bewusstseinsstörungen, Beeinträchtigung des Erinnerungsvermögens, mentale Beeinträchtigung, Ohnmacht, Sedierung, Gleichgewichtsstörungen, Sprachstörungen, Taubheitsgefühl, abnorme Hautempfindungen (z. B. Kribbeln, Prickeln), Sehstörungen, beschleunigter Herzschlag, verlangsamter Herzschlag, erniedrigter Blutdruck, Bauchbeschwerden, Nesselsucht, verzögertes Wasserlassen, häufiges Wasserlassen, funktionelle Sexualstörung, Arzneimittelentzugssyndrom, Störungen des Allgemeinbefindens, Reizbarkeit. Selten: Arzneimittelabhängigkeit, abnormes Denken, epileptischer Anfall, sich einer Ohnmacht nahe fühlen, abnorme Koordination, bedrohlich langsame oder flache Atmung (Atemdepression), gestörte Magenentleerung, Trunkenheitsgefühl, Gefühl der Entspannung. Allgemein ist die Wahrscheinlichkeit des Auftretens von Selbstmordgedanken und entsprechendem Verhalten bei Patienten erhöht, die unter chronischen Schmerzen leiden. Zusätzlich können Arzneimittel zur Behandlung von Depressionen (die eine Wirkung auf die Botenstoffe im Gehirn haben) dieses Risiko besonders zu Beginn einer Behandlung erhöhen. Obwohl Tapentadol auch Botenstoffe im Gehirn beeinflusst, geben die Daten zur Anwendung von Tapentadol beim Menschen keinen Anhalt für das Vorliegen eines solchen erhöhten Risiko. Warnhinweis: Palexia retard enthält Lactose. Packungsbeilage beachten. Stand der Information: 08/2010. Grünenthal GmbH, 52099 Aachen, Deutschland 16 impressum Impressum Grünenthal GmbH 52099 Aachen Redaktion Dr. med. Ute Stefani Haaga medizinwelten-services GbR Nöllenstr. 11, 70195 Stuttgart Angaben zu Dosierungen, Applikationsform und Indikationsgebieten können von der Zulassung abweichen. Jegliche Haftung hinsichtlich der Angaben zu Dosierung, Applikationsform und/oder Indikationen ist ausgeschlossen. Maßgeblich sind in jedem Fall die Angaben der jeweiligen Fachinformation in der aktuellsten Fassung.