Formelsammlung als PDF herunterladen
Werbung

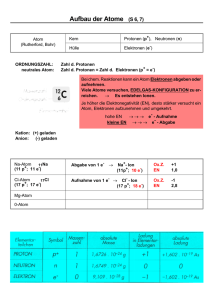
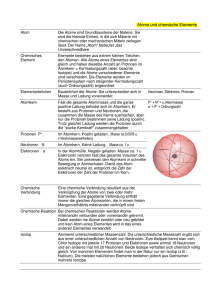
maths2mind® Seite 17 von 56 Grundlagen der Physik Kapitel: Atom- und Kernphysik 798 Aufbau des Atoms 799 800 Atomphysik Kernphysik 801 Abmessungen im Atom Van der Waals Kräfte 802 Bildung von Molekülen 803 Aufbau des Atomkerns 804 Nukleonenzahl oder Massenzahl A 805 Massendefekt 806 Kernbindungs energie 807 Kernspaltungs energie 808 Kernfusions energie 809 Protonenzahl Z oder Ordnungszahl Z 810 Massenzahl Isotop 811 Aufbau der Atomhülle 812 Ion Jedes Atom besteht aus einem Atomkern und einer Atomhülle. Die Nuklide (p, n) des Kerns bestehen aus je 3 elementaren und stabilen u und d Quarks, das Elektron der Hülle ist ebenfalls elementar und stabil. Außerhalb des Atoms gibt es nur noch ein 4-tes elementares und stabiles Teilchen, das Elektron-Neutrino. Die Atomphysik beschreibt das Verhalten der Elektronen in der Atomhülle Die Kernphysik beschreibt das Verhalten der Kernteilchen. Ein Atom ist solange elektrisch Neutral, solange es aus gleich vielen Protonen im Kern wie Elektronen Durchmesser von Quarks … unklar aber < 10-18 m in der Hülle besteht. Die elektrische Kraft bindet die negativ geladenen Elektronen an den positiv Durchmesser des Atomkerns … 10-15 m geladenen Atomkern. Die Eigenschaften der Durchmesser der Atomhülle … 10-10 m Atomhülle bestimmen die chemischen Eigenschaften eines Elements. Kommen sich 2 Atome sehr nahe und dominiert die Abstoßung zwischen den beiden (negativ geladenen) Atomhüllen, dann können sich die Atomhüllen nicht durchdringen Die Van der und es bleibt ein Mindestabstand zwischen den Atomen. Waals Kräfte sorgen für Kommen sich 2 Atome sehr nahe und dominiert die Anziehung zwischen Kern1 und die Bindung Hülle 2 bzw zwischen Kern 2 und Hülle 1 so entsteht ein Molekül. von Atomen zu Molekülen Die van der Waals Kräfte sind sehr schwache elektrische Kräfte und nehmen mit der 6ten Potenz des Abstands ab. Jeder Atomkern besteht aus Protonen p und Neutronen n, die man zusammen als Baryonen p m0 1836 me Q 1,6 10 19 C bezeichnet. Baryonen haben eine innere Struktur (3 n m0 1839 me Q0 Quarks) und sind daher - im Unterschied zu den Elektronen der Hülle - keine Elementarteilchen. Unter der Nukleonenzahl A, auch Massenzahl A genannt, versteht man die A Z N Summe der Protonen Z und der Neutronen N im Atomkern. Die Masse eines Atomkerns ist um den Massendefekt m geringer als die Summe der Masse seiner Protonen und Neutronen, da zu deren Bindung m Z mp N mn mKern im Kern eine Bindungsenergie erforderlich ist. Die entsprechende Wechselwirkung ist die starke Wechselwirkung, die eine Reichweite von ca. 3.10-15 m hat.. Die Kernbindungsenergie ist jene Energie die frei EB m c2 Z mp N mn mKern c2 wird, wenn sich Z freie Protonen und N freie Neutronen zu einem Kern verbinden. Die bei der Kernspaltung eines schweren Atomkerns in mehrere leichte Atomkerne 235 1 89 144 1 92 U 0 n 36 Kr 56 Ba 3 0 n 210 MeV freigesetzte Energie entspricht der Differenz der Bindungsenergien der beteiligten Kerne. 2 H 3H 4 He 3,5 MeV n 14,1MeV Wenn 2 leichte Atomkerne zu einem schwereren 1 Deuteriumkern und 1 Tritiumkern verschmelzen Atomkern unter extremen Druck und unter extremer Temperatur (im Inneren der Sonne, im zu 1 Heliumkern und 1 freien Neutron unter Fusionsreaktor) verschmelzen wird die Energie frei. Freisetzung von 3,5+14,1 MeV Energie Ein Element hat immer eine fixe Anzahl an Protonen, kann aber A unterschiedlich viele Neutronen haben. Die eindeutige Ordnungszahl = Z Element Element A Anzahl der Protonen kennzeichnet ein Element. Ein und dasselbe Element (gleiche Ordnungszahl) kann aber unterschiedliche Massenzahlen haben, wenn es nämlich mit einer unterschiedlichen Anzahl an Neutronen vorkommt. Dann spricht man vom Isotop eines Elements. Die Atomhülle besteht aus den bereits „fundamentalen“ also unteilbaren Elektronen e. Im e m0 1me 9,1110 31kg Q 1,6 10 19 C elektrisch neutralen Atom ist die Anzahl der Protonen gleich der Anzahl der Elektronen Atome haben in neutralen Zustand gleich viele Protonen im Kern wie Elektronen in der Hülle. Atome mit mehr Elektronen als Protonen (Elektronenüberschuss) sind elektrisch negativ geladen (Anionen). Atome mit weniger Elektronen als Protonen sind elektrisch positiv geladen (Kationen). Antimaterie Stand vom: 04.06.2016 Die jeweils aktuellste Version findet sich auf: maths2mind.com Für dieses Werk nehmen wir u.a. §40f und §6 UrhG in Anspruch. Es darf unentgeltlich weitergegeben, jedoch nicht verändert werden. maths2mind® Seite 18 von 56 Grundlagen der Physik Kapitel: Atom- und Kernphysik 813 Radionuklide 814 Alphastrahlung 815 Betastrahlung 816 Gammastrahlung 817 Radioaktives Zerfallsgesetz 818 Radioaktive Halbwertszeit Radionuklide sind Atome mit einen instabilen Kern, die sich in einen anderen Kern umwandeln und dabei Energie in Form von Alpha oder Beta oder Gammastrahlung abgeben. Die positiv geladene Alphastrahlung ist ionisierend und besteht aus Heliumkernen, also aus 2 Protonen p und 2 Neutronen n. Aus dem Mutterkern entsteht ein neues A A 2 4 Z Mutterkern Z2Tochterkern 2 He Element. Alphastrahlen können sehr einfach abgeschirmt werden (Blatt Papier) und haben nur ein sehr kleines Durchdringungsvermögen. Beim Betazerfall (ein W- Boson vermittelt die schwache Wechselwirkung und in der Folge zerfällt ein überschüssiges Neutron in eine Proton und ein A A Elektron) verlassen ein Elektron und ein Antineutrino Z Mutterkern Z1Tochterkern e e oder ein Positron und ein Elektron Neutrino den Kern. A A Z Mutterkern Z1Tochterkern e e Aus dem Mutterkern entsteht ein neues Element. Betastrahlen können einfach abgeschirmt werden (5mm Alublech) und haben nur ein kleines Durchdringungsvermögen. Gammastrahlung ist keine Teilchenstrahlung sondern eine elektromagnetische Strahlung aus Photonen die meist nach einem Alphaoder Betazerfall, aus dem nach dem Zerfall entstandenen angeregten Tochterkern ausgesendet wird, um den Kern in einen niedrigen Grundzustand zu bringen . Gammastrahlen können durch Bleiplatten abgeschirmt werden und haben eine Reichweite von einigen Metern. N0 ist die Anzahl der radioaktiven Isotope am Anfang N N0 et N ist die Anzahl der radioaktiven Isotope, die nach der Zeit t noch nicht zerfallen sind. 2 Die Halbwertszeit gibt an, nach welcher Zeitdauer genau die Hälfte der T50% ln ursprünglichen radioaktiven Isotope zerfallen ist. Stand vom: 04.06.2016 Die jeweils aktuellste Version findet sich auf: maths2mind.com Für dieses Werk nehmen wir u.a. §40f und §6 UrhG in Anspruch. Es darf unentgeltlich weitergegeben, jedoch nicht verändert werden. maths2mind® Seite 19 von 56 Grundlagen der Physik Kapitel: Atom- und Kernphysik 715 Atomare Masseneinheit u 819 Mol 820 Avogadro Konstante NA 12 C u 1,66 10 27 kg 12 u dient also dazu um anzugeben um das Wievielfache die Masse eines Atoms schwerer ist als ein zwölftel der Masse von C-12. Ein Mol enthält immer 6,022.1023 Teilchen. Ein Mol ist jene Stoffmenge, die gleichviele Teilchen (Atome, Moleküle, Ionen) enthält wie 12 g des Mol 6,022 1023 Teilchen Kohlenstoff Isotops C-12 N Die Avogadro Konstante NA gibt die Anzahl der Teilchen N pro 23 1 NA 6,022 10 Stoffmenge n an. n mol M 821 Die atomare Masseneinheit u ist definiert als 1/12 der Massen des Kohlenstoff Isotops C-12. Molare Masse M 1 m N A mM n g 1u NA mol Die molare Masse M ist der Quotient aus der Masse m eines Stoffs und der Stoffmenge n dieses Stoffs. Achtung, bei der molaren Masse handelt es sich nicht um eine „Masse“ sondern um eine Stoffkonstante mit der Dimension g/mol! Die Zahlenwert der Masse mM von 1 Mol (=6,022.1023 Stück) von einem Stoff in Gramm, ist gleich dem Zahlenwert der Atommasse der Atome (Molekülmasse der Moleküle) des selben Stoffs in der atomaren Masseneinheiten u Stand vom: 04.06.2016 Die jeweils aktuellste Version findet sich auf: maths2mind.com Für dieses Werk nehmen wir u.a. §40f und §6 UrhG in Anspruch. Es darf unentgeltlich weitergegeben, jedoch nicht verändert werden.